文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【江西版】
可能用到的相对原子质量:H—1、C—12、O—16、Fe—56
一、单项选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
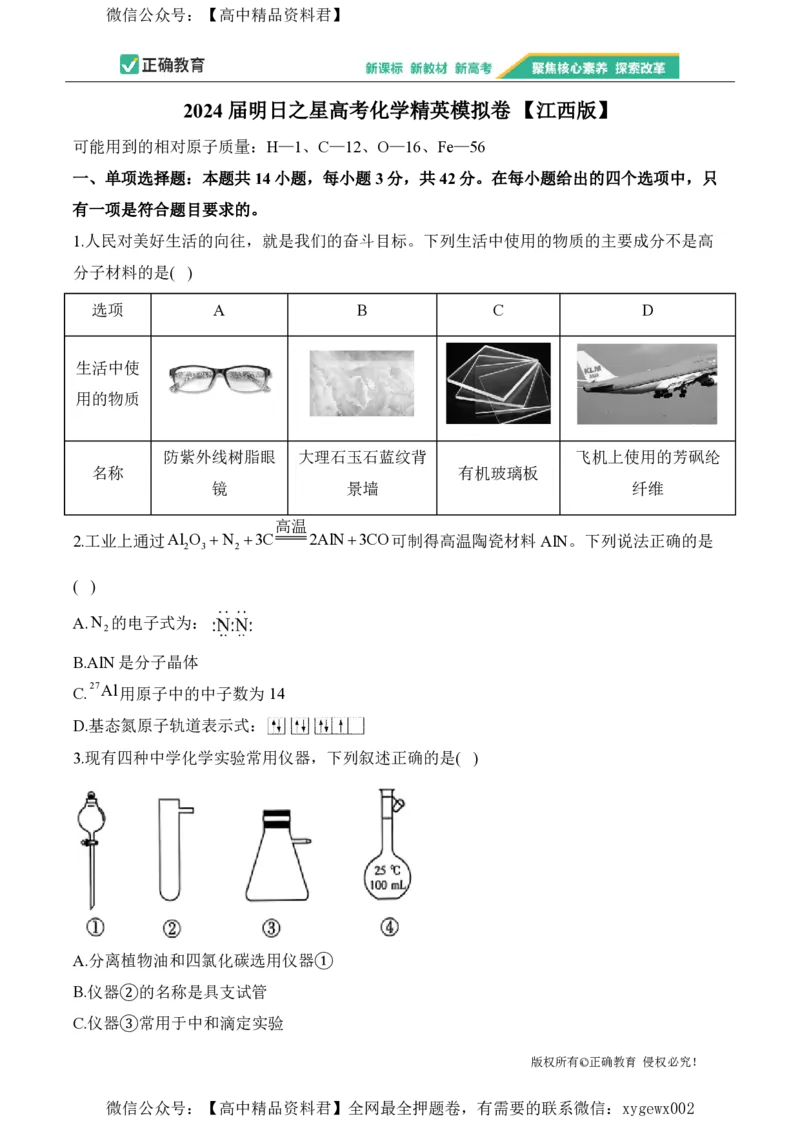
1.人民对美好生活的向往,就是我们的奋斗目标。下列生活中使用的物质的主要成分不是高
分子材料的是( )
选项 A B C D
生活中使
用的物质
防紫外线树脂眼 大理石玉石蓝纹背 飞机上使用的芳砜纶
名称 有机玻璃板
镜 景墙 纤维
高温
2.工业上通过Al O N 3C 2AlN3CO可制得高温陶瓷材料AlN。下列说法正确的是
2 3 2
( )
A.N 的电子式为:
2
B.AlN是分子晶体
C.
27Al用原子中的中子数为14
D.基态氮原子轨道表示式:
3.现有四种中学化学实验常用仪器,下列叙述正确的是( )
A.分离植物油和四氯化碳选用仪器①
B.仪器②的名称是具支试管
C.仪器③常用于中和滴定实验
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
D.可以加热的仪器有②③④
4.乙醛发生银镜反应的原理为
CH CHO2AgNH OHCH COONH 3NH 2AgH O,已知N 表示阿伏加德
3 3 2 3 4 3 2 A
罗常数的值。下列叙述正确的是( )
A.标准状况下,22gCH CHO含有的 键数目为2.5N
3 A
B.常温下,1LpH=9的氨水溶液中由水电离产生的OH数目为109N
A
C.理论上,当有标准状况下2.24LNH 生成时,转移电子的数目为 0.3N
3 A
D.500mL0.2molL1AgNH OH溶液中Ag的数目为0.1N
3 2 A
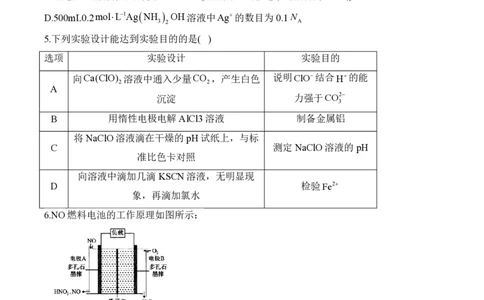
5.下列实验设计能达到实验目的的是( )
选项 实验设计 实验目的
向Ca(ClO) 溶液中通入少量CO ,产生白色 说明ClO结合H的能
2 2
A
沉淀 力强于CO2
3
B 用惰性电极电解 AlCl3溶液 制备金属铝
将NaClO溶液滴在干燥的pH试纸上,与标
C 测定NaClO溶液的pH
准比色卡对照
向溶液中滴加几滴KSCN溶液,无明显现
D 检验Fe2
象,再滴加氯水
6.NO燃料电池的工作原理如图所示:
下列说法错误的是( )
A.电极电势:电极A<电极 B
B.电极 A的电极反应式:NO3e 4OH NO 2H O
3 2
C.若有 3molH经过质子交换膜移向右侧溶液时,电极B理论上消耗16.8LO (标准状况
2
下)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
D.多孔石墨电极可以加快气体的吸附速率
7.短周期元素X、Y、Z、W的原子序数依次增大。X的某一核素中没有中子,Y原子最外层
电子数是内层电子数的3倍,Z元素基态原子M层上只有一个电子,W与Y同主族。下列说
法正确的是( )
A.X与Y可形成原子个数比分别为1:1和2:1的两种离子化合物
B.W元素是短周期中电负性最大的元素
C.Z元素基态原子的电子排布式为1s22s22p63p1
D.由X、Y、Z、W四种元素可形成水溶液呈酸性的一种化合物
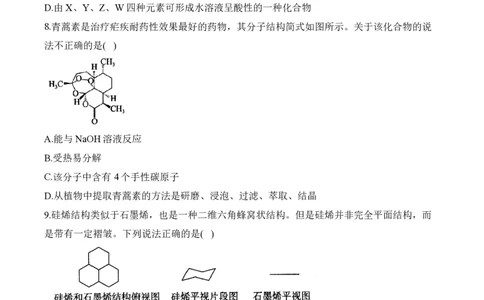
8.青蒿素是治疗疟疾耐药性效果最好的药物,其分子结构简式如图所示。关于该化合物的说
法不正确的是( )
A.能与NaOH溶液反应
B.受热易分解
C.该分子中含有4个手性碳原子
D.从植物中提取青蒿素的方法是研磨、浸泡、过滤、萃取、结晶
9.硅烯结构类似于石墨烯,也是一种二维六角蜂窝状结构。但是硅烯并非完全平面结构,而
是带有一定褶皱。下列说法正确的是( )
A.硅烯分子中的Si原子、石墨烯分子中的C原子均采取sp2杂化
B.Si—Si键强于 C—C键
C.硅烯分子中的原子均满足8电子稳定结构
D.导电性:硅烯<石墨烯
10.分子之间可通过空间结构和作用力协同产生某种选择性,从而实现分子识别。下图是一种
分子梭,在分子A上有两个不同的识别位点。下列说法错误的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.在酸性情况下,A分子中位点2结合H带正电荷,与环状分子B作用力增强
B.通过加入酸或碱,均能实现分子梭在不同状态之间的切换
C.若该分子梭与分子B的识别仅对应两种状态,则其具有设计成分子计算机的可能
D.分子A含有醚键和氨基,属于芳香化合物
11.已知:
CuH
2
O
4
2蓝色4Cl
CuCl
4
2黄色4H
2
O。试管a中溶液做参照,
对试管b中溶液依次进行如下操作:①微热,溶液变为黄色②将其置于冷水中,溶液变为蓝
色③滴加氨水至过量,蓝色沉淀增多,后又逐渐消失变为深蓝色溶液。下列说法正确的是
( )
A.由步骤①可推知该反应的H 0
B.由步骤②可说明降低温度,该反应平衡正向移动
C.步骤③深蓝色溶液中n CuH O 2 1mmol
2 4
D.试管b中生成的CuOH 、CuNH 2 中均含配位键
2 3 4
12.室温下,某实验兴趣小组用10.0mL0.1000molL1Na CO 溶液标定某盐酸浓度,用甲基橙
2 3
作指示剂,滴定曲线如图丁所示。下列说法正确的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.滴定中Na CO 溶液应该盛放在乙仪器中
2 3
B.读数时,应双手一上一下持滴定管
C.Na CO 标准溶液吸收了空气中的CO ,会使测得的盐酸浓度偏大
2 3 2
D.滴定终点pH在b区域
13.铁和碳形成的一种晶体的晶胞结构如图所示。N 为阿伏加德罗常数的值,晶胞边长为
A
acm,下列说法中错误的是( )
A.该晶体的化学式为FeC
B.Fe原子位于C原子围成的正四面体空隙中
C.Fe原子周围有12个紧邻的Fe原子
272
D.该晶体密度为
gcm3
N a3
A
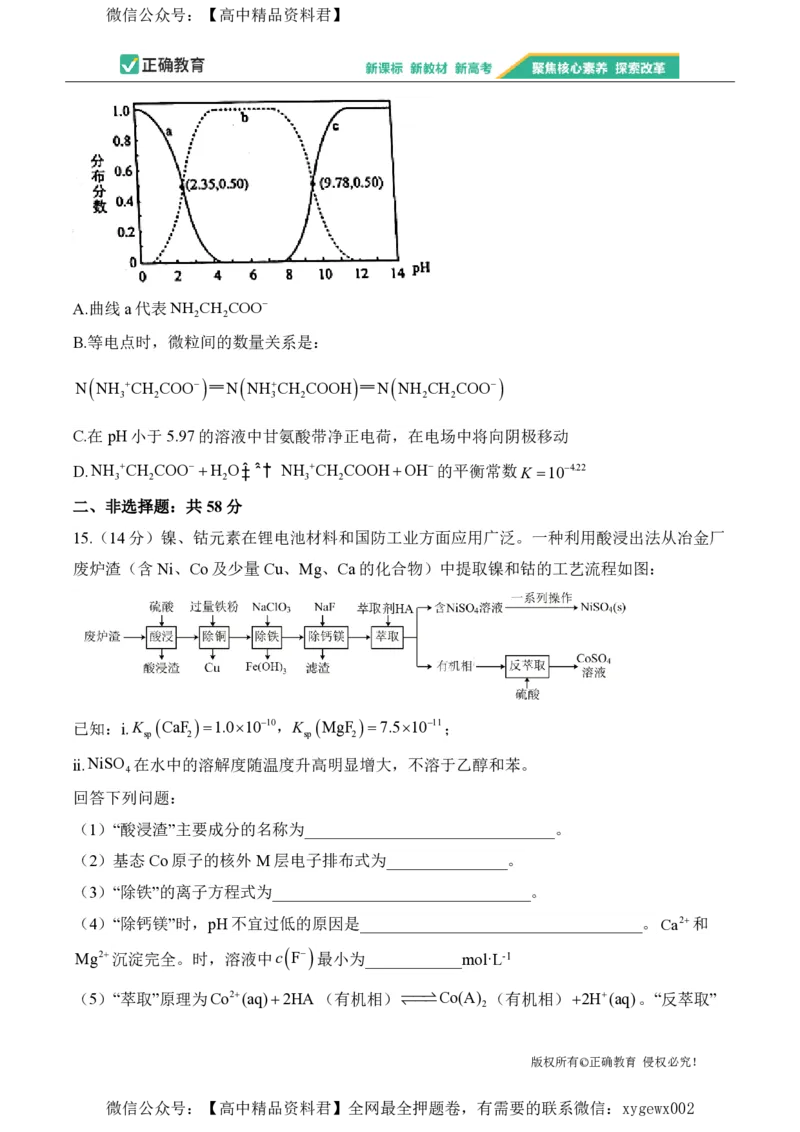
14.甘氨酸H NCH COOH是人体必需氨基酸之一,在晶体和水溶液中主要以偶极离子
2 2
NH CH COO 的形式存在,它是两性电解质有两个可解离基团。在水溶液中,甘氨酸的带
3 2
电状况与溶液的pH有关。当调节溶液的pH使甘氨酸所带正负电荷正好相等时,甘氨酸所带
的净电荷为零,在电场中不发生移动现象,此时溶液的pH即为甘氨酸的等电点,已知甘氨
酸的等电点为5.97。在25℃时,NH CH COO、NHCH COOH和NH CH COO的分布分
2 2 3 2 3 2
c
A2
数[如
A2
]与溶液pH关系如图下列说法正确的是( )
cH Ac HA c A2
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.曲线a代表NH CH COO
2 2
B.等电点时,微粒间的数量关系是:
N NH CH COO N NHCH COOH N NH CH COO
3 2 3 2 2 2
C.在pH小于5.97的溶液中甘氨酸带净正电荷,在电场中将向阴极移动
D.NH CH COO H O‡ˆ ˆˆ†ˆ NH CH COOHOH的平衡常数K 104.22
3 2 2 3 2
二、非选择题:共 58 分
15.(14分)镍、钴元素在锂电池材料和国防工业方面应用广泛。一种利用酸浸出法从冶金厂
废炉渣(含Ni、Co及少量Cu、Mg、Ca的化合物)中提取镍和钴的工艺流程如图:
已知:ⅰ.K CaF 1.01010,K MgF 7.51011;
sp 2 sp 2
ⅱ.NiSO 在水中的溶解度随温度升高明显增大,不溶于乙醇和苯。
4
回答下列问题:
(1)“酸浸渣”主要成分的名称为_______________________________。
(2)基态Co原子的核外M层电子排布式为_______________。
(3)“除铁”的离子方程式为________________________________。
(4)“除钙镁”时,pH不宜过低的原因是___________________________________。Ca2和
Mg2沉淀完全。时,溶液中c
F
最小为____________mol·L-1
(5)“萃取”原理为Co2(aq)2HA(有机相)Co(A) (有机相)2H(aq)。“反萃取”
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
时为促进Co2的转移,应选择的实验条件或采取的实验操作有①_____________;②多次萃
取。
(6)获得NiSO (s)的“一系列操作”中洗涤产品可选用_________(填字母标号)试剂。
4
a.冷水
b.乙醇
c.苯
16.(15分)聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①C H C H g21/2O g 8CO g5H OgH 4386.9kJmol1
6 5 2 5 2 2 2 1
②C H CHCH g10O g 8CO g4H OgH 4263.1kJmol1
6 5 2 2 2 2 2
③H g1/2O g H OgH 241.8kJmol1
2 2 2 3
计算反应④C
6
H
5
C
2
H
5
g
C
6
H
5
CHCH
2
gH
2
g 的H
4
_______kJmol1;
(2)在某温度、100kPa下,向反应器中充入1mol气态乙苯发生反应④,其平衡转化率为
50%,欲将平衡转化率提高至 75%,需要向反应器中充入_______mol水蒸气作为稀释气(计
算时忽略副反应);
(3)在913K、100kPa下,以水蒸气作稀释气。Fe O 作催化剂,乙苯除脱氢生成苯乙烯外,
2 3
还会发生如下两个副反应:
⑤C H C H g C H gCH CH g
6 5 2 5 6 6 2 2
⑥C H C H gH g C H CH gCH g
6 5 2 5 2 6 5 3 4
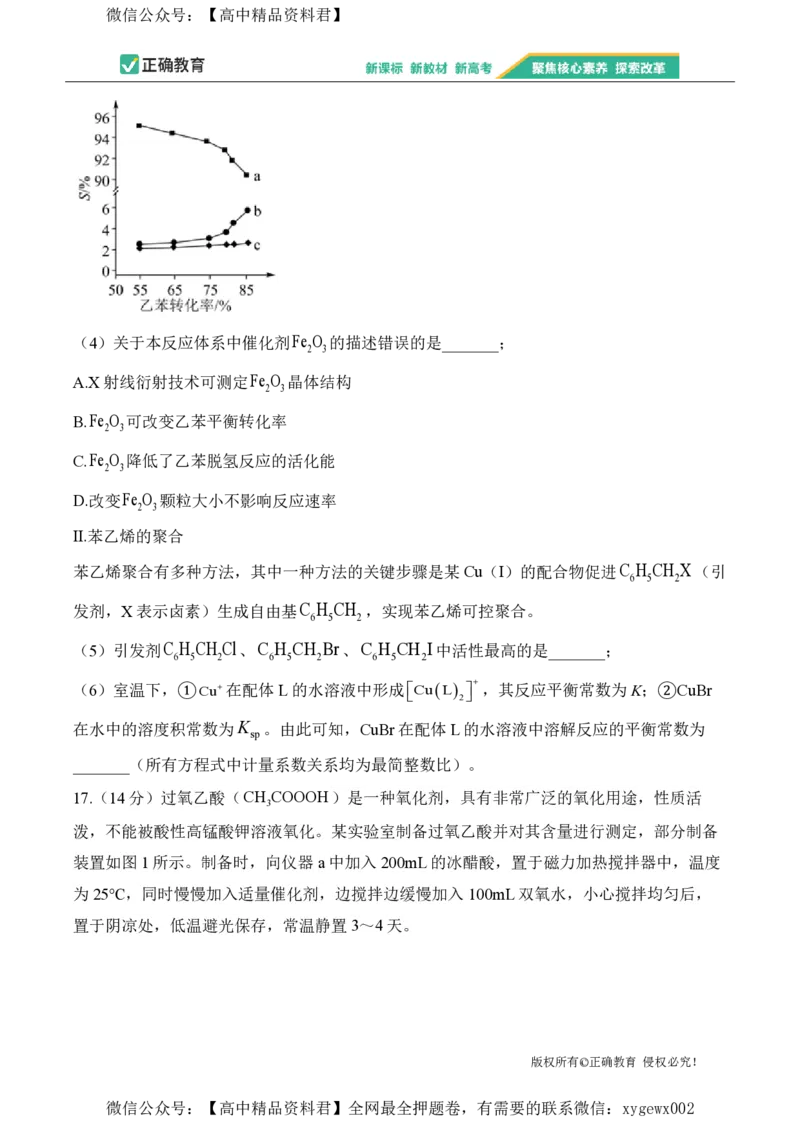
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S
转化为目的产物所消耗乙苯的量
(S 100%)随乙苯转化率的变化曲线如图所示,其中曲
已转化的乙苯总量
线b代表的产物是_______,理由是_______;
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(4)关于本反应体系中催化剂Fe O 的描述错误的是_______;
2 3
A.X射线衍射技术可测定Fe O 晶体结构
2 3
B.Fe O 可改变乙苯平衡转化率
2 3
C.Fe O 降低了乙苯脱氢反应的活化能
2 3
D.改变Fe O 颗粒大小不影响反应速率
2 3
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某Cu(Ⅰ)的配合物促进C H CH X(引
6 5 2
发剂,X表示卤素)生成自由基C H CH ,实现苯乙烯可控聚合。
6 5 2
(5)引发剂C H CH Cl、C H CH Br、C H CH I中活性最高的是_______;
6 5 2 6 5 2 6 5 2
(6)室温下,①Cu在配体L的水溶液中形成CuL ,其反应平衡常数为K;②CuBr
2
在水中的溶度积常数为K 。由此可知,CuBr在配体L的水溶液中溶解反应的平衡常数为
sp
_______(所有方程式中计量系数关系均为最简整数比)。
17.(14分)过氧乙酸(CH COOOH)是一种氧化剂,具有非常广泛的氧化用途,性质活
3
泼,不能被酸性高锰酸钾溶液氧化。某实验室制备过氧乙酸并对其含量进行测定,部分制备
装置如图1所示。制备时,向仪器a中加入200mL的冰醋酸,置于磁力加热搅拌器中,温度
为25℃,同时慢慢加入适量催化剂,边搅拌边缓慢加入100mL双氧水,小心搅拌均匀后,
置于阴凉处,低温避光保存,常温静置3~4天。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
已知:2KI2H SO CH COOOH 2KHSO I CH COOHH O;
2 4 3 4 2 3 2
I 2Na S O 2NaINa S O 。
2 2 2 3 2 4 6
回答下列问题:
(1)图1中仪器a的名称为_______,制备时的化学方程式为_______。
(2)含量测定:i.取1.00mL过氧乙酸试样,配制 100mL溶液,备用;ii.向100mL碘量瓶
(如图2所示)中加入5mLH SO 、3滴10%MnSO 溶液,取稀释好的5.00mL过氧乙酸试
2 4 4
样,用0.01molL1KMnO 溶液滴定至溶液呈粉红色;ⅲ.随即加入10%KI溶液10mL和掩蔽
4
剂(排除其他物质对滴定的干扰),摇匀并用0.05molL1Na S O 标准溶液滴定至淡黄色,
2 2 3
加入3滴0.5%淀粉溶液,继续用Na S O 标准溶液滴定至蓝色消失,Na S O 标准溶液的用
2 2 3 2 2 3
量为 V mL。
①步骤 i中,用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、_______。
②步骤ⅱ的目的是_______,加入MnSO 的作用是_______;用KMnO 溶液滴定时,反应的离
4 4
子方程式为_______。
③原溶液中过氧乙酸的含量为_______gmL1。
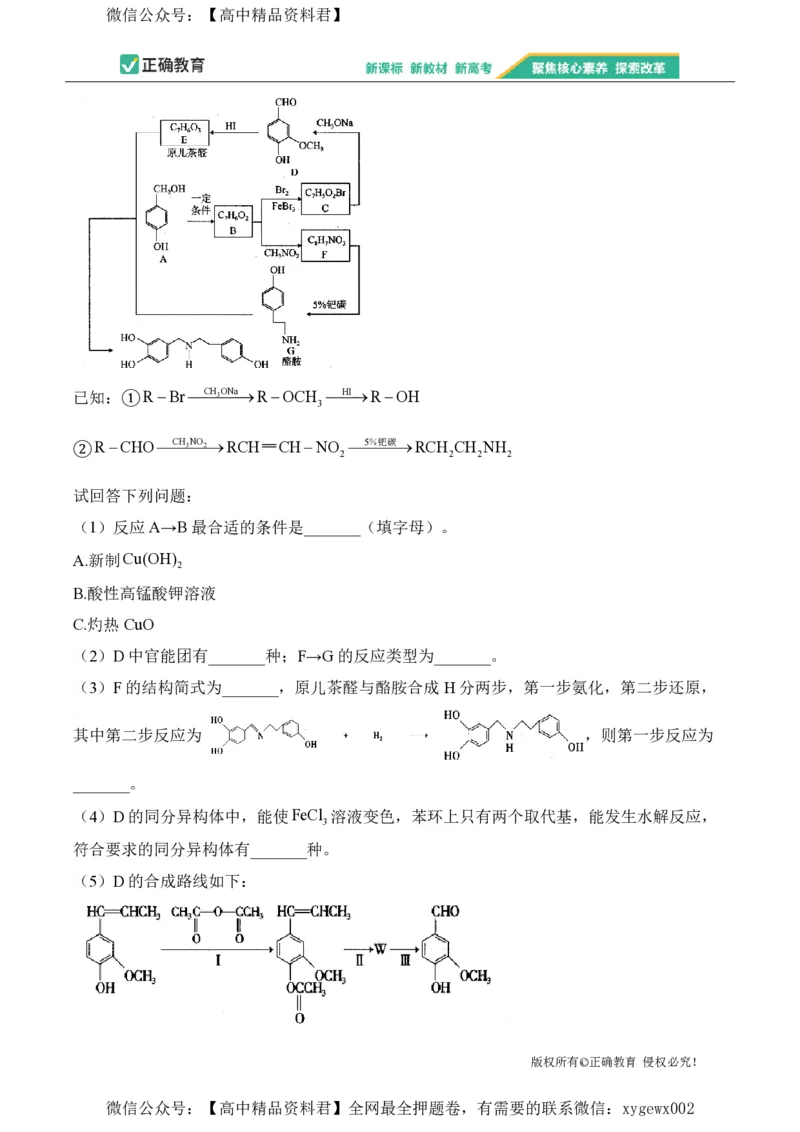
18.(15分)有机化合物H是合成石蒜碱的医药中间体,可由酪胺和原儿茶醛合成。H的一种
常见的合成路线如图所示:
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
已知:①RBrCH
3
ONaROCH HIROH
3
②RCHOCH 3 NO 2RCH CHNO 5%钯碳RCH CH NH
2 2 2 2
试回答下列问题:
(1)反应A→B最合适的条件是_______(填字母)。
A.新制Cu(OH)
2
B.酸性高锰酸钾溶液
C.灼热 CuO
(2)D中官能团有_______种;F→G的反应类型为_______。
(3)F的结构简式为_______,原儿茶醛与酪胺合成 H分两步,第一步氨化,第二步还原,
其中第二步反应为 ,则第一步反应为
_______。
(4)D的同分异构体中,能使FeCl 溶液变色,苯环上只有两个取代基,能发生水解反应,
3
符合要求的同分异构体有_______种。
(5)D的合成路线如下:
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
①步骤Ⅲ中,W在稀硫酸中水解生成 D的化学方程式为_______。
②步骤Ⅰ、Ⅲ的目的是_______。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:B
解析:A.树脂类材料属于有机高分子,故A不符合题意;
B.大理石玉石的主要成分是无机盐,不属于高分子,故B符合题意;
C.有机玻璃属于有机高分子,故C不符合题意;
D.芳砜纶纤维属于有机高分子,故D不符合题意;
答案选B。
2.答案:C
解析:A.N原子最外层有5个电子,2个N原子形成 3对共用电子对,使物质分子中每个原
子都达到最外层8个电子的稳定结构,故N 的电子式为: ,A错误;
2
B.AlN是高温陶瓷材料,物质的熔沸点很高,说明 AlN的存在状态是原子晶体,而不是熔沸
点比较低的分子晶体,B错误;
C.Al是13号元素,原子核内质子数是13,27Al中的中子数为:27-13=14,C正确;
D.原子核外电子总是尽可能成单排列,而且自旋方向相同,这样排布使原子的能量最低,故
基态氮原子轨道表示式是: ,D错误;
故合理选项是C。
3.答案:B
解析:植物油和四氯化碳互溶,用仪器①无法进行分离,A项错误;中和滴定实验使用的锥
形瓶不带支管,避免液体从支管口溅出,C项错误;仪器④为容量瓶,不能加热,D项错
误。
4.答案:B
解析:A项,标准状况下,22gCH CHO含有的 键数目为3N ,A项错误;B项,常温
3 A
下,1LpH=9的氨水溶液中由水电离产生的OH数目等于溶液中的H数目,应为109N ,B
A
项正确;C项,理论上,当有标准状况下2.24LNH 生成时,转移电子的数目为0.067N ,C
3 A
项错误;D项,AgNH 难电离,因此溶液中的Ag极少,D项错误。
3 2
5.答案:D
解析:向Ca(ClO) 溶液中通入少量CO ,产生CaCO 沉淀,不能说明ClO结合H的能力强
2 2 3
于CO2,A不符合题意;在水溶液中,氧化性:H Al3,用惰性电极电解AlCl 溶液不能
3 3
得到铝单质,应电解熔融状态的氧化铝来制备金属铝,B不符合题意;NaClO溶液具有漂白
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
性,不能用pH试纸测定其pH,C不符合题意;向溶液中滴加几滴KSCN溶液,无明显现
象,说明溶液中无Fe3,再滴加氯水,若溶液变红,说明溶液中含Fe2,D符合题意。
6.答案:B
解析:根据题给NO燃料电池的工作原理图可知,电极A上NO失去电子发生氧化反应,则
电极A为负极,电极B上O 得到电子发生还原反应,则电极 B为正极。原电池中,正极的
2
电极电势高于负极,即电极电势:电极A<电极B,A说法正确;电解质溶液为酸性溶液,所
以电极A的电极反应式为NO3e 2H O NO 4H,B说法错误;有3molH经过质子
2 3
交换膜移向右侧溶液时,说明反应中转移了3mol电子,根据电极B的电极反应式
O 4e 4H 2H O可知,每转移3mol电子时,消耗0.75molO ,即在标准状况下消耗
2 2 2
氧气的体积为0.75mol22.4Lmol1 16.8L,C说法正确;多孔石墨的表面积较大,可以加快
气体的吸附速率,D说法正确。
7.答案:D
解析:短周期元素X、Y、Z、W的原子序数依次增大。X的某一核素中没有中子,可推出X
元素为氢元素;Y原子最外层电子数是内层电子数的 3倍,可推出Y元素为氧元素;Z元素
基态原子M层上只有一个电子,可推出Z元素为钠元素;四种元素均为短周期元素且W与
Y同主族,所以W元素为硫元素。H和O可形成原子个数比分别为1:1和2:1的共价化合
物H O 和H O,A错误;同周期主族元素从左到右,电负性逐渐增大,同主族元素从上到
2 2 2
下,电负性逐渐减小,故短周期元素中电负性最大的元素为F,B错误;钠元素基态原子的
电子排布式为1s22s22p63s1,C错误;X、Y、Z、W四种元素可形成NaHSO ,该物质的水溶
4
液呈酸性,D正确。
8.答案:C
解析:该化合物分子中含有酯基,可与NaOH溶液发生水解反应,A说法正确;该化合物分
子中含有过氧键,根据H O 受热分解会断开过氧键可推测青蒿素的热稳定性较差,B说法正
2 2
确;由该化合物的结构简式可知,其分子中含有7个手性碳原子,C说法错误;从植物中提
取有机化合物的一般方法是用有机溶剂浸泡已研磨过的固体原料,过滤获得提取液,再进行
萃取得到浓溶液,最后冷却结晶,D说法正确。
9.答案:D
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
解析:由题干中“硅烯并非完全平面结构”可知,硅烯分子中的 Si原子不采取sp2杂化形成平
面结构,而石墨烯分子中的C原子均采取sp2杂化,A错误;Si原子的半径大于C原子,因
此Si—Si键弱于C—C键,B错误;由题给俯视图可知,每个 Si原子形成3个单键,所以硅
烯分子中的Si原子无法满足8电子稳定结构,C错误;Si元素位于元素周期表中金属元素与
非金属元素的分界线处,Si是一种半导体材料,而石墨是导体,故导电性:硅烯<石墨烯,D
正确。
10.答案:D
解析:由题可知,在酸性条件下,A分子中位点2的烷胺基结合H而带正电荷,与环状分子
B的作用力增强,A正确;在碱性条件下,环状分子 B与带有正电荷的位点1的相互作用较
强,结合A选项分析可知,通过加入酸或碱,均可实现分子梭在两个不同状态之间的切换,
B正确;该分子梭与分子A的识别仅对应两种状态,与目前的二进制计算机相似,C正确;
分子A没有醚键,D错误。
11.答案:A
解析:A.由步骤①可推知,升温,平衡正向移动,则该反应的H >0,故A正确;B.由步骤
②可说明降低温度,该反应平衡逆向移动,故 B错误;C.步骤③深蓝色溶液中
n CuNH 2 1mmol,故C错误;D.试管b中生成的CuNH 2 中含配位键,
3 4 3 4
Cu(OH) 中无配位键,故D错误;故选:A。
2
12.答案:D
解析:由图丁可知实验是用盐酸滴定Na CO 溶液,Na CO 溶液应该盛放在丙仪器中,A项
2 3 2 3
错误;读数时,应单手持滴定管上端无刻度处,并保持其自然垂直,B项错误;当到达滴定
终点时,甲基橙由黄色变为橙色,滴定终点的溶液呈酸性,滴定终点pH在b区域,D项正
确;由于钠元素质量守恒,所以碳酸钠溶液是否吸收空气中的CO 对测定结果没有影响,C
2
项错误。
13.答案:B
解析:A.根据分析可知晶体的化学式为FeC,A正确;
B.Fe原子位于C原子围成的正八面体空隙中,B错误;
C.单看 Fe原子可以发现,Fe原子为面心立方堆积,所以1个Fe原子周围有12个紧邻的Fe
原子,C正确;
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
468 272
D.晶胞的质量为 g,晶胞的体积为a3,所以晶体密度为
gcm3
,D正确;故选
N N a3
A A
B。
14.答案:C
解析:甘氨酸中含有氨基和羟基,氨基显碱性,羧基显酸性,在酸性条件下,存在的形式
为,随着pH增大,逐步转化成NHCH COO,最终转化成NH CH COO,从而确定曲线a
3 2 2 2
代表NHCH COOH,曲线b代表为NHCH COO,曲线c代表NH CH COO,据此分析;
3 2 3 2 2 2
A.根据上述分析,曲线a代表NHCH COOH,故A错误;B.等电点是甘氨酸所带正负电荷
3 2
正好相等,因此NHCH COOH的物质的量等于NH CH COO,甘氨酸等电点为5.97,根据
3 2 2 2
图像可知,N NHCH COO N NHCH COOH N NH CH COO ,故B错误;C.根
3 2 3 2 2 2 2
据B选项分析以及图像可知,当pH小于5.97时,n NHCH COOH n NH CH COO ,
3 2 2 2
甘氨酸带净正电荷,在电场作用下,向阴极移动,故C正确;D.取坐标235,050.此时
K 1014
c NHCH COOH c NHCH COO ,因此有K c OH w 1011.65 ,故D
3 2 3 2 c H 102.35
错误;答案为C。
15.答案:(1)硫酸钙(1分)
(2)3s23p63d7(1分);Co的质量较大的同位素在自然界中丰度较高(2分)
(3)ClO 6Fe2 15H O Cl 6Fe(OH) 12H(2分)
3 2 3
(4)c
H
过高,c
F
减小,不利于钙镁沉淀完全(2分);102.5或3.16103(1分)
(5)酸性条件(2分)
(6)ab(2分)
解析:(1)酸浸时用硫酸,产生的硫酸钙微溶,故“酸浸渣”主要成分的名称为硫酸钙;
(2)Co是27号元素,基态Co原子的核外电子排布式为[Ar]3d74s2或
1s22s22p63s23p63d74s2,故其M层电子排布式为3s23p63d7;
Co的质量较大的同位素在自然界中丰度较高,故虽然Co的核电荷数比Ni小1,但Co的相
对原子质量比Ni的略大;
(3)“除铁”时加入的氯酸钠将亚铁离子氧化,反应生成氢氧化铁,反应的离子方程式为
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
ClO 6Fe2 15H O Cl 6Fe(OH) 12H;
3 2 3
(4)“除钙镁”时,随着pH的降低,溶液中的H增加,H F HF的平衡正向移动,
溶液中c
F
减小,为使CaF 和MgF 的溶解平衡逆向移动,NaF用量更多;已知离子浓度
2 2
105mol/L时,认为该离子沉淀完全,且K CaF 1.01010,K MgF 7.51011,钙
sp 2 sp 2
离子沉淀完全时镁离子已沉淀完全,
1.01010
c F 102.5(mol/L)3.16103(mol/L),所以为使Ca2和Mg2沉淀完全,溶
1105
液中c
F
最小为102.5或3.16103;答案为c
H
过高,c
F
减小,不利于钙镁沉淀完
全;102.5或3.16103;
(5)“反萃取”时为促进Co2的转移,应选择的实验条件或采取的实验操作有①酸性条件;
②多次萃取;
(6)获得NiSO (s)的“一系列操作”中洗涤产品使其溶解度降低而晶体析出,故可选用冷
4
水或乙醇,答案选ab。
16.答案:(1)+118(1分)
(2)5(2分)
(3)苯(2分);反应④为主反应,反应⑤⑥为副反应,苯乙烯的选择性最大(2分);在
恒温恒压下,随乙苯转化率的增大,反应⑤正向移动,反应⑥不移动,则曲线b代表产物苯
(2分)
(4)BD(2分)
(5)C H CH Cl(2分)
6 5 2
(6)KK (2分)
sp
解析:(1)根据盖斯定律,由①-②-③,可得④
C H C H (g)‡ˆ ˆˆ†ˆ C H CH CH (g)H (g) ΔH
6 5 2 5 6 5 2 2 4
4386.9 kJmol1 4263.1 kJmol1 241.8 kJmol1 118 kJmol1。
(2)乙苯的平衡转化率为50%时,由题中信息可得:
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
C H C H (g)‡ˆ ˆˆ†ˆ C H CH CH (g)H (g)
6 5 2 5 6 5 2 2
起始量 1mol 0 0
转化量 0.5mol 0.5mol 0.5mol
平衡量 0.5mol 0.5mol 0.5mol
100 100 100
平衡分压 kPa kPa kPa
3 3 3
p(苯乙烯)pH
100
则压强平衡常数K 2 kPa 。设充入xmol水蒸气时乙苯平衡转化率提
p p(乙苯) 3
高到75%,则:
C H C H (g)‡ˆ ˆˆ†ˆ C H CH CH (g)H (g)
6 5 2 5 6 5 2 2
起始量 1mol 0 0
转化量 0.75mol 0.75mol 0.75mol
平衡量 0.25mol 0.25mol 0.25mol
25 75 75
平衡分压 kPa kPa kPa
1.75x 1.75x 1.75x
p(苯乙烯) pH 225 100
温度不变,平衡常数不变,则压强平衡常数K 2 kPa kPa ,
p p(乙苯) 1.75x 3
解得x5。
(3)反应④为主反应,反应⑤⑥为副反应,苯乙烯的选择性最大;在恒温恒压下,随乙苯
转化率的增大,反应⑤正向移动,反应⑥不移动,则曲线 b代表产物苯。
(4)X射线衍射技术可以测定晶体结构,A项正确;
Fe O 是催化剂,催化剂不能使平衡发生移动,不能改变乙苯平衡转化率,B项错误;
2 3
Fe O 作催化剂,可以降低乙苯脱氢反应的活化能,C项正确;
2 3
改变Fe O 颗粒大小即改变催化剂的表面积,可以改变反应速率,D项错误。
2 3
(5)电负性:ClBr I,C-Cl键的极性更大,更易断裂,故C H CH Cl更易生成自由基
6 5 2
C H CH ,活性最强。
6 5 2
(6)已知Cu(aq)2L‡ˆ ˆˆ†ˆ Cu(L) K 、CuBr(s)‡ˆ ˆˆ†ˆ Cu(aq)Br(aq) K ,两反应相
2 sp
加可得:CuBr(s)2L‡ˆ ˆˆ†ˆ Cu(L) Br(aq),则其平衡常数为KK 。
2 sp
17.答案:(1)三口烧瓶(或三颈烧瓶)(2分);
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
催化剂
CH COOHH O CH COOOHH O(2分)
3 2 2 3 2
(2)①100mL容量(2分);瓶②排除双氧水的干扰,防止其与 KI发生反应MnSO 作为催
4
化剂,可加速H O 的分解(3分);2MnO 5H O 6H 2Mn2 5O 8H O(2
2 2 4 2 2 2 2
分);③0.038V (3分)
解析:(1)仪器a的名称为三口烧瓶或三颈烧瓶。冰醋酸被双氧水氧化为过氧乙酸,故制备
催化剂
时的化学方程式为CH COOHH O CH COOOHH O。
3 2 2 3 2
(2)①配制过氧乙酸试样时,需要在容量瓶里定容,用到的玻璃仪器除烧杯、量筒、玻璃
棒和胶头滴管外,还有100mL容量瓶。②因双氧水具有氧化性,可以与KI发生反应,故在
用碘量法测定过氧乙酸的含量之前,应排除其干扰。提前加入MnSO 作为催化剂,可加速
4
H O 的分解。KMnO 溶液也用于除去过氧化氢,则用KMnO 溶液滴定时,反应的离子方程
2 2 4 4
式为2MnO 5H O 6H 2Mn2 5O 8H O。③由已知中的化学方程式可知碘量法
4 2 2 2 2
测定的原理,计算过程为先根据消耗Na S O 标准溶液的量计算出生成的I 的量,再根据生
2 2 3 2
成的I 的量计算出被还原的过氧乙酸的量(即滴定试样中的过氧乙酸含量),有关系式:
2
CH COOOH~ 2Na S O
3 2 2 3
0.025V103mol 0.05V103mol
mCH COOOH0.025V103mol76gmol1 1.9103Vg,滴定过氧乙酸试样的体积为
3
5 1.9103Vg
1mL 0.05mL,故原溶液中过氧乙酸的含量为 0.038VgmL1。
100 0.05mL
18.答案:(1)C(1分)
(2)3(2分);还原反应(2分)
(3) (3分)
(4)9(2分)
(5)① CH COOH(3分);②保护酚羟基,使其不被氧化(2
3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
分)
解析:(1)A→B的反应为醇氧化为醛的反应,选用新制Cu(OH) 还需酸化,选用酸性高锰
2
酸钾溶液将醇氧化为羧酸,所以最好选用灼热的CuO。
(2)根据D的结构简式可知,其分子中所含官能团为醛基、酚羟基和醚键,共 3种;F→G
的反应即为已知信息②中的第二步反应,属于还原反应。
(3)由综合推断可知,F的结构简式为 、E的结构简式为 ,根据原儿茶醛与
酪胺合成H的第二步反应,可知第一步反应的化学方程式为
。
(4)D的分子式为C H O ,D的同分异构体能使FeCl 溶液变色,说明分子中含有酚羟基;
8 8 3 3
能发生水解反应,说明分子中含有酯基,苯环上只有两个取代基,当两个取代基分别为一个
酚羟基和一个COOCH 时,有邻、间、对3种结构,当两个取代基分别为一个酚羟基和一
3
个OOCCH 时,有邻、间、对3种结构,当两个取代基分别为一个酚羟基和一个
3
CH OOCH时,有邻、间、对3种结构,故符合条件的同分异构体共有9种。
2
(5)①步骤Ⅰ是酚羟基与醋酸酐的取代反应,步骤Ⅱ是引入—CHO,步骤Ⅲ是酯基水解重新
转化为酚羟基,则步骤Ⅲ中,W在稀硫酸中水解生成D的好像方程式为
CH COOH。②由于在氧化碳碳双键引入醛基时酚羟基也易被氧
3
化,所以步骤Ⅰ、Ⅲ的目的是保护酚羟基,使其不被氧化。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002