文档内容
姓名 准考证号
下列有关化学实验操作及作用的说法正确的是
秘密 启用前 3.
★ 容量瓶、分液漏斗和酸式滴定管使用前均需要检查是否漏水
A.
可以用 试纸检测 、 和氯水等溶液的
B. pH NaOH NH4NO3 pH
化 学
酸碱中和滴定时,酸式滴定管、碱式滴定管和锥形瓶均需要润洗
C.
实验室用 制取 以及用 、( )制取 时均需要用到棉花,其作
D. KMnO4 O2 NH4Cl Ca OH 2 NH3
用相同
注意事项: 下列有关元素及其化合物的叙述正确的是
4.
答题前,考生务必将自己的姓名、准考证号填写在本试题相应的位置。 浓 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
1. A. H2SO4
全部答案在答题卡上完成,答在本试题上无效。 加热 固体与浓 混合物可制备 ,说明 比 酸性强
2. B. NaI H3PO4 HI H3PO4 HI
回答选择题时,选出每小题答案后,用 铅笔把答题卡上对应题目的答案标号 石灰乳 盐酸 蒸发结晶
盐卤(含 )溶液 ( ) 溶液 无水
3. 2B
C. MgCl2 Mg OH 2 MgCl2 MgCl2
涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案用
既能和 溶液反应,又能和氢氟酸反应,但 不属于两性氧化物
黑色笔迹签字笔写在答题卡上。
D.SiO2 NaOH SiO2
0.5mm “点击化学”在药物开发和生物医用材料领域有着重要的作用。下图所示是“点击化
5.
考试结束后,将本试题和答题卡一并交回。
4. 学”研究中的一种常用分子的结构简式。关于该化合物说法正确的是
可能用到的相对原子质量:
H1 O16 Fe56 Zr91 Sb122 该物质的分子式为
A. C19H14NO3
该分子中 原子有两种杂化类型
B. C
N
该物质在一定条件下能发生加成反应、取代反应、氧化反应、
一、选择题:本题共 小题,每小题 分,共 分。在每小题给出的四个选项中,只有一
C. OH
14 3 42 O
还原反应
项是符合题目要求的。 O
相同物质的量的该物质分别和 、 充分反应,消耗 、 的物质的量相同
化学工业的迅速发展为满足人民群众日益增长的美好愿望做出了突出贡献。下列说 D. Na NaOH Na NaOH
1.
我国四大发明之一的黑火药爆炸反应为 == 。设
法不合理的是 6. S + 2KNO3 + 3C K2S + N2↑+ 3CO2↑
N 为阿伏加德罗常数的值,下列说法错误的是
规范使用食品防腐剂可以减缓食物变质速率,保持食品营养价值 A
A. 该反应中氧化产物和还原产物的物质的量之比为 ∶
A. 3 2
利用 合成高级脂肪酸,实现了无机小分子向有机高分子的转变
B. CO2 该反应中若有 完全反应,则被 氧化的 的数目为 N
B. 2molKNO3 KNO3 C 3 A
电解海水制氢工艺中的关键材料多孔聚四氟乙烯化学性质稳定且耐腐蚀
基态原子的第一电离能从大到小的顺序为
C.
C. N>O>C>K
我国科学家首次在月壤中发现的“嫦娥石”[ ( )]属于无机盐 溶液中c( ) c( ) c( ) c( )
D. Ca8YFe PO4 7 D.K2S OH - = H + + HS - +2 H2S
下列化学用语表示正确的是 下列实验及现象、结论都正确的是
2. 7.
基态 原子价电子排布式: 2 选项 实验及现象 结论
A. Zn 4s
化 将磁性氧化铁溶于足量浓盐酸中,滴入酸性 溶液,紫色褪去 磁性氧化铁中有二价铁
四氯化碳的电子式: •
•C••l•
•
A
用 计测量醋酸、盐酸的 ,结果盐酸的
K
小
Mn
于
O4
醋酸 是弱电解质
B. Cl •C• Cl B pH pH pH CH3COOH
Cl 在 溶液中滴加 滴 溶液,溶液变红褐色;再滴加 3+ 既发生了水解反应,
5mLFeCl3 2 Na2SO3 Fe
基态 原子电子占据的最高能层符号为 C [ ( )]溶液,产生蓝色沉淀 又发生了还原反应
C. K 4s K3 Fe CN 6
的晶体结构中含有离子键、非极性共价键、键和 键 在火焰上灼烧搅拌过某无色溶液的玻璃棒,火焰出现黄色 无色溶液中含 元素
D Na
D.CaC2 σ π
化学试题 第 页(共 页) 化学试题 第 页(共 页)
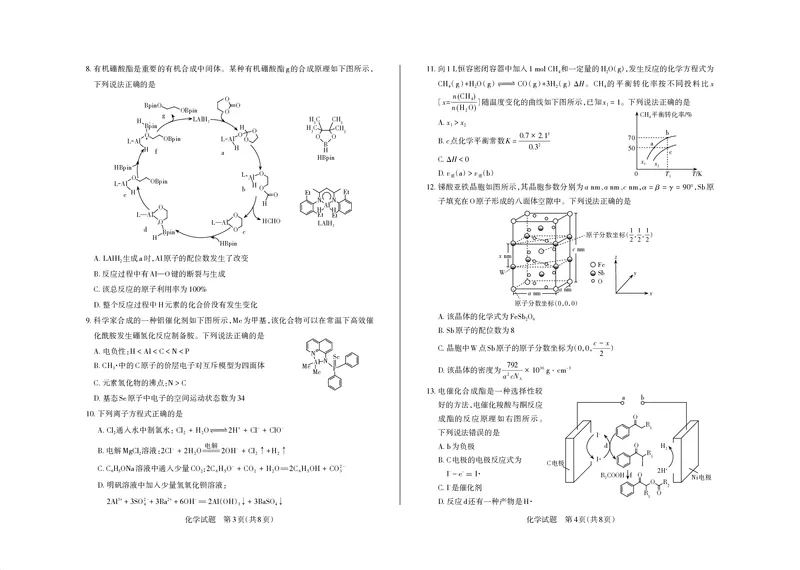
1 8 2 8有机硼酸酯是重要的有机合成中间体。某种有机硼酸酯 的合成原理如下图所示, 向 恒容密闭容器中加入 和一定量的 (),发生反应的化学方程式为
8. g 11. 1L 1molCH4 H2O g
下列说法正确的是 ( ) ( ) ( ) ( ) H。 的平衡转化率按不同投料比x
CH4 g +H2O g CO g +3H2 g Δ CH4
n
O
[x (CH4)]随温度变化的曲线如下图所示,已知x 。下列说法正确的是
BpinO O
=n 1=1
OBpin O (H2O) 平衡转化率
H Bpin g LAlH2 H H H C 3 C C C H H 3 A. x 1> x 2 CH4 /%
L Al O OBpin L Al O O O 3 O B O 3 B. c点化学平衡常数K = 0.7 × 2 2 .1 3 70 a b
H f a H H H 0.3 50 c
HBpin C.Δ <0 x x
1 2
HBpin v () v () T T
O L Al O D. 逆 a > 逆 b 0 1 /K
L Al OBpin b H O 12. 锑酸亚铁晶胞如图所示,其晶胞参数分别为a nm 、a nm 、c nm ,α = β = γ = 90° , Sb 原
e H O Et Et 子填充在 原子形成的八面体空隙中。下列说法正确的是
O H N AAll N O
— H H
L Al O Et Et
—
+O L Al HCHO LAlH2
d B-pin O c 原子分数坐标(1,1,1)
H 2 2 2
HBpin c
生成 时, 原子的配位数发生了改变 x nm z
nm
A.LAlH2 a Al
Fe
反应过程中有 — 键的断裂与生成 y
B. Al O W Sb
O
该总反应的原子利用率为 a
C. 100% a nm x
nm
整个反应过程中 元素的化合价没有发生变化 原子分数坐标( ,,)
D. H 0 0 0
该晶体的化学式为
科学家合成的一种铝催化剂如下图所示, 为甲基,该化合物可以在常温下高效催 A. FeSb2O6
9. Me
原子的配位数为
化酰胺发生硼氢化反应制备胺。下列说法正确的是 B.Sb 8
c x
晶胞中 点 原子的原子分数坐标为( ,, - )
电负性:
C. W Sb 0 0
A. HC
电催化合成酯是一种选择性较
基态 原子中电子的空间运动状态数为 13.
D. Se 34 好的方法,电催化羧酸与酮反应 a b
下列离子方程式正确的是
10. 成酯的反应原理如右图所示。
O
通入水中制氯水:
+ - - 下列说法错误的是
R
1
A.Cl2 Cl2 + H2O 2H + Cl + ClO -
I
电解 为负极
电解 溶液: - ======== - A.b d O H2
B. MgCl2 2Cl + 2H2O 2OH + Cl2↑+H2↑ 电极的电极反应式为 · R 1
溶液中通入少量 : - == 2- B.C C 电极 I I
C.C6H5ONa CO2 2C6H5O + CO2 + H2O 2C6H5OH + CO3 I - -e - = I · R2COOH f O 2H + Ni 电极
明矾溶液中加入少量氢氧化钡溶液:
是催化剂 O R
D. - 2
C.I
== ( ) 反应 还有一种产物是 · R 1 O
3+ 2- 2+ -
2Al +3SO4 +3Ba +6OH 2Al OH 3↓+3BaSO4↓ D. d H
化学试题 第 页(共 页) 化学试题 第 页(共 页)
3 8 4 8常温下,向一定浓度二元弱酸 溶液中加入 (),保持溶液体积和温度不变, ()“碱溶造液”中产生了[ ( )] 离子,该离子中含有的化学键类型
-
14. H2A KOH s 5 Ga OH 4
c 有 (填序号)。
测得 与 [ 为c( )、c(
2-
)、(A 2- )]变化如图所示。下列说法正确的是 ▲
pH -lgX X H2A A c - 极性共价键 非极性共价键 配位键 氢键 离子键
(HA ) a. b. c. d. e.
曲线 代表 与 ( )变化关系 ()“电解”生成镓的过程中阴极的电极反应式为 。
A. Q pH -lgc A 2- 6 ▲
-lgX ( 分)
B. 常温下, H2A 的K a1=10 -4.3 4.00 16. 14
Q a 是日常生活和工农业生产中应用广泛的物质。氢醌法制备 的原理及装置
点溶液中: 3.00 H2O2 H2O2
C.a
2.00 如下: H2 Ni
c( K + ) - c( OH - ) = c( HA - ) + 2 c ( H2A ) 1.00 M b N (一)反应原理:
O OH
0 2.8 4.3 6.0 pH
点溶液中:c( - ) c( 2- ) ()氢醌法制备 总反应 乙基蒽醌 乙基蒽醇
D.b HA = A 1 H2O2
二、非选择题:本题共 小题,共 分。 的化学方程式为 。
4 58 ▲ O OH
(二)反应装置:
( 分)
15. 14
金属镓在电子工业、生物医学等多个领域有广泛应用。利用锌粉置换渣(主要成分
H2O2 O2
Ⅱ Ⅲ
为 、 和少量的 、 、 、 等)制备镓的工艺流程如图所示: 盐酸
Ga2S3 Ga2O3 ZnS FeO Fe2O3 SiO2 b d f g e h m n Ⅳ
高压 、 Ⅰ c 乙基蒽醌
H2SO4 O2 NaOH P204 YW100 H2SO4 NaOH NaOH a 浓 溶液
硫 /Ni 氧
置 锌 换 粉 渣 富氧浸出 中和除杂 协同萃取 反萃取 中和沉镓 碱溶造液 电解 镓 Zn 酸 湿控磁力搅拌器 碱石灰 气 源
A B D F G
浸渣 滤渣 无机相 有机相 滤液 E
已知: 、 等杂质易使催化剂中毒。回答下列问题:
已知: 溶液中相关离子开始沉淀和沉淀完全(c
-5 -1
)时的 : H2O HX
Ⅰ. ≤ 1.0 × 10 mol·L pH
()装置的连接顺序为 ,接 (填接口序
2 a→ ▲ → ▲ → ▲ → ▲ →n g b
物质
Fe 3+ Fe 2+ Zn 2+ Ga 3+ 号,每个装置只能使用一次)。
开始沉淀的
pH 1.9 6.9 6.2 3.2 ()检查装置气密性并加入药品,所有活塞处于关闭状态。开始制备时,打开活
沉淀完全时的 — 3
pH 3.2 8.4 8.0 塞 ,控温 。一段时间后,仅保持活塞 打开,抽出残留气体。随后关闭活塞
▲ 60℃ Ⅱ
、 协同萃取体系对金属离子的优先萃取顺序为:
3+ 3+ 2+ 2+ ,再打开活塞 继续反应一段时间。关闭活塞,过滤三颈烧瓶中混合物,加水萃
Ⅱ.P204 YW100 Fe >Ga >Fe >Zn
Ⅱ ▲
回答下列问题: 取,分液,减压蒸馏,得产品。
()元素 在元素周期表中的位置是 。 ()一段时间后,抽出残留气体的原因是 。
1 Ga ▲ 4 ▲
()装置 的作用是 。
()“富氧浸出”中溶液出现淡黄色浑浊,写出 发生反应的离子方程式为 。 5 E ▲
2 Ga2S3 ▲
()取 产品,加蒸馏水定容至 摇匀,取 于锥形瓶中,用
-1
()滤渣的主要成分是 (写化学式)。 6 2.50g 500mL 50.00mL 0.0500mol·L
3 ▲
酸性 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 、 、
()用 代 表 , 代 表 ,“ 协 同 萃 取”过 程 中 发 生 反 应 :
KMnO4 32.02mL 31.98mL
4 H2A2 P204 RH YW100 。假设其他杂质不干扰结果。
35.05mL
3+
+
,“协同萃取”的作用是 ,“反萃取”加
滴定终点的现象是 ;
Ga + H2A2 + 2RH Ga(HA2)R2 + 3H ▲
① ▲
入稀硫酸的目的是 (用化学方程式表示)。 产品中 质量分数为 。
▲ ② H2O2 ▲
化学试题 第 页(共 页) 化学试题 第 页(共 页)
5 8 6 8( 分)
17. 15
二氧化碳的捕集、利用与储存被国际公认为是实现减排降碳的关键技术手段。用
制备 有利于实现“双碳”目标。该反应分两步进行
CO2 C2H4
() () () () H Ⅰ.CO2 g +H2 g CO g +H2O g Δ 1
() () () () H -1
Ⅱ.2CO g +4H2 g C2H4 g +2H2O g Δ 2=-1308kJ·mol
()反应 的 S 。
1 Ⅱ Δ ▲ 0
()已知部分共价键的键能如下表所示:
2
化学键 == - == - -
C O C≡O H H C C C H O H
键能( )
-1
kJ·mol 803 1071 436 611 414 464
则 H 。
-1
Δ 1= ▲ kJ·mol
()若反应 在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的
3 Ⅱ
是 (填序号)。
▲
容器中混合气体的密度保持不变 容器内混合气体的压强保持不变
A. B.
反应速率 v ( ) v ( ) 同时断裂 — 键和 — 键
C. 2 正 CO = 逆 H2 D. 1molO H 2molH H
()向某 刚性容器中,加入 、 在不同催化剂( 、)下发生上述
4 1 L 1 molCO2 3molH2 M N
反应。相同时间内测得 的转化率和 的选择性(含碳生成物中 的物质的量
CO2 C2H4 C2H4
分数)随温度的变化如图所示。
N
12 80
10 M 70
8 60 N
6
转化率 50
4 M CO2选择性
C2H4 40
温度
500 600 700 800 /K
率化转
%/
2OC
性择选
%/
4H2C
( 分)
18. 15
溴夫定( )是治疗水痘 带状疱疹病毒的药物,其合成路线如下:
H -
H
O O O N
HN ( HCHO ) n HN CH 2 OH MnO2 HN CHO CH ( 2 COOH ) 2/
O N O N DMSO O N N
H H H
A B C
O O
OTMS
HN COOH NBS/CH3COOK HN Br TMCS Br
N
DMF HMDS
O N O N
TMSO N
H H
D E F
O O
Br Br
( ) HN HN
K C21H21O5Cl
O N CH3ONa O N
CH2Cl2
O CH3OH O
OOC CH OH
3
CH COO OH
3
H
G
回答下列问题:
() 中的官能团名称为 。
1 B ▲
()( )的结构简式为 。
2 HCHO n ▲
() 的反应类型为 。
3 G→H ▲
() ( )的名称为 。
4 CH2 COOH 2 ▲
( ,)
700 8 ( , ) () N 中存在大 键,可以表示为 。(苯中大 键表示为 6 )
700 60 5 π ▲ π Π6
() 的结构简式为 。
6 K ▲
()符合下列条件的D的同分异构体有 种。
7 ▲
根据图像,合成乙烯的最佳催化剂为 ;
① ▲ 有苯环 有2个硝基
① ②
~ 之间,乙烯的选择性随温度变化的原因是 ;
②500 800K ▲ ()下列为 ( )的合成路线:
在 催化剂、 条件下反应,反应后混合气体中 的体积分数为 (保 8 CH2 COOH 2
③ M 700K C2H4 ▲
催化剂 +
留至 )。 ¾¾¾¾¾¾¾®M¾¾¾ N ¾ a ¾ C ¾ N ¾® ¾¾¾H¾¾/¾H¾2¾O¾® 化
0.01% CH3COOH N HOOCCH2COOH
Cl2 NaOH
()二氧化锆是制备催化剂 和 的一种原材料,其晶胞如下图
5 M N 的结构简式为 , 生成 的化学方程式为 。
M ▲ M N ▲
所示,其晶胞参数为a 。
nm
原子填充在 原子形成的 空隙中;
①Zr O ▲
个 原子间的最短距离为 。 晶胞
②2 Zr ▲ nm
ZrO2
化学试题 第 页(共 页) 化学试题 第 页(共 页)
7 8 8 8