文档内容
{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}:
{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKAR{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}2025 届高三三模 化学 参考答案详解
1 2 3 4 5 6 7 8 9 10 11 12 13 14
B C A C B A C D D A B D C D
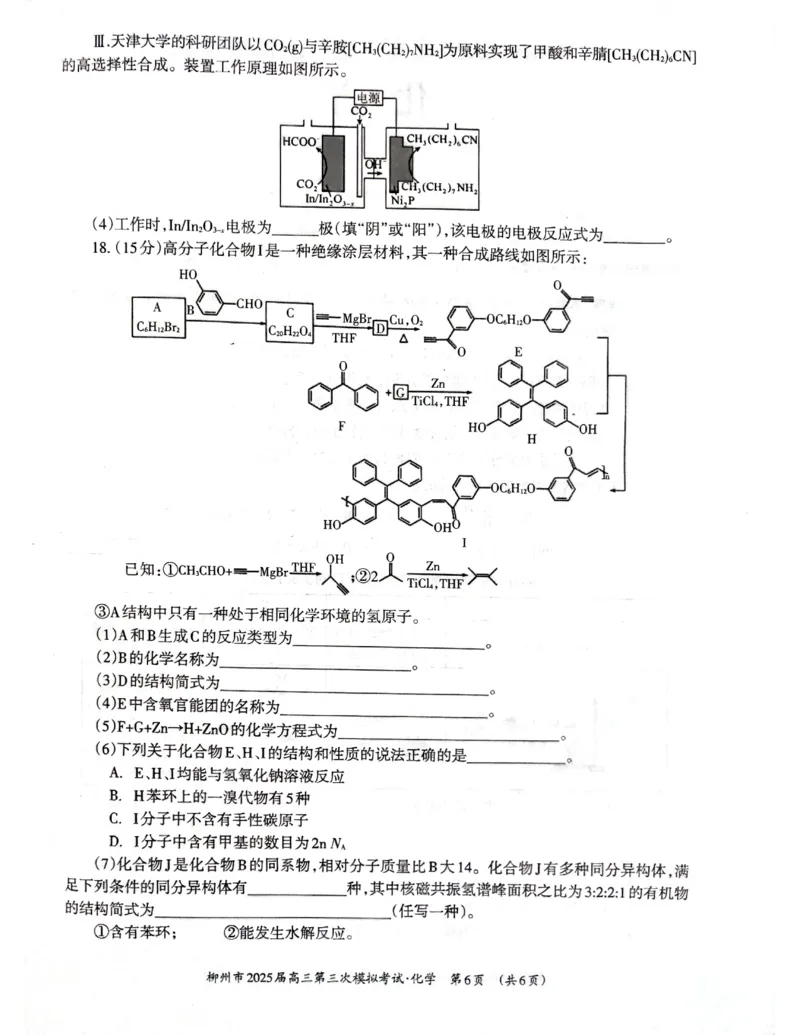
15.(1)将废钯催化剂粉碎(合理即可)。
(2)作还原剂,将PdO还原为Pd单质。
(3)70℃,3∶1。
(4)阴离子。
(5)Fe3+、Cu2+。
(6) N H H O+2PdNH Cl =2Pd+N +4NH Cl+H O
2 4 2 3 2 2 2 4 2
(7)15
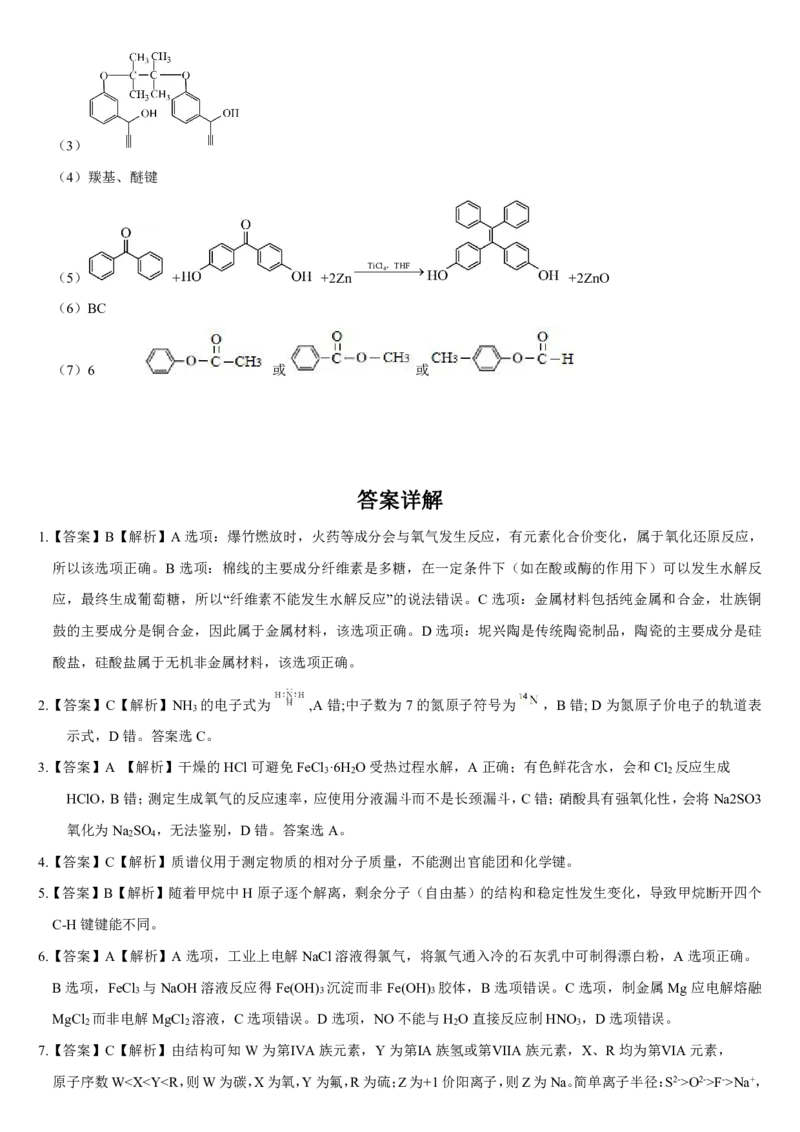
16.(1)(球形)冷凝管,2MnO -+16H++10Cl-==2Mn2++5Cl +8H O;
4 2 2
(2)fgdebc(或debc);
(3)水浴加热; ;
(4)滴入最后半滴标准液,溶液由无色变为红色,且半分钟不褪色;
偏小。
17.(1)-135 ,K 2K 。
1 2
(2)BD
(3) ①>
②随着温度升高,催化剂的活性下降(或者随着温度的升高,以副反应为主)。
③
0.045 0.24
( p)( p)4
3.865 3.865
0.85 2.67
( p)2( p)6
3.865 3.865 MPa-3
(4)CO +2e-+H O=HCOO-+OH-。
2 2
18.(1)取代反应
(2)邻羟基苯甲醛(2-羟基苯甲醛)
{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}(3)
(4)羰基、醚键
(5) + +2Zn
TiCl4,THF
+2ZnO
(6)BC
(7)6 或 或
答案详解
1.【答案】B【解析】A选项:爆竹燃放时,火药等成分会与氧气发生反应,有元素化合价变化,属于氧化还原反应,
所以该选项正确。B选项:棉线的主要成分纤维素是多糖,在一定条件下(如在酸或酶的作用下)可以发生水解反
应,最终生成葡萄糖,所以“纤维素不能发生水解反应”的说法错误。C选项:金属材料包括纯金属和合金,壮族铜
鼓的主要成分是铜合金,因此属于金属材料,该选项正确。D选项:坭兴陶是传统陶瓷制品,陶瓷的主要成分是硅
酸盐,硅酸盐属于无机非金属材料,该选项正确。
2.【答案】C【解析】NH 的电子式为 ,A错;中子数为7的氮原子符号为 ,B错;D为氮原子价电子的轨道表
3
示式,D错。答案选C。
3.【答案】A 【解析】干燥的HCl可避免FeCl ·6H O受热过程水解,A正确;有色鲜花含水,会和Cl 反应生成
3 2 2
HClO,B错;测定生成氧气的反应速率,应使用分液漏斗而不是长颈漏斗,C错;硝酸具有强氧化性,会将Na2SO3
氧化为Na SO ,无法鉴别,D错。答案选A。
2 4
4.【答案】C【解析】质谱仪用于测定物质的相对分子质量,不能测出官能团和化学键。
5.【答案】B【解析】随着甲烷中H原子逐个解离,剩余分子(自由基)的结构和稳定性发生变化,导致甲烷断开四个
C-H键键能不同。
6.【答案】A【解析】A选项,工业上电解NaCl溶液得氯气,将氯气通入冷的石灰乳中可制得漂白粉,A选项正确。
B选项,FeCl 与NaOH溶液反应得Fe(OH) 沉淀而非Fe(OH) 胶体,B选项错误。C选项,制金属Mg应电解熔融
3 3 3
MgCl 而非电解MgCl 溶液,C选项错误。D选项,NO不能与H O直接反应制HNO ,D选项错误。
2 2 2 3
7.【答案】C【解析】由结构可知W为第ⅣA族元素,Y为第ⅠA族氢或第ⅥⅠA族元素,X、R均为第ⅥA元素,
原子序数WO2->F->Na+,
{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}A错;简单气态氢化物稳定性:H O>H S>CH ,B错;第一电离能位于钠和硫之间的元素有镁、铝、硅3种。
2 2 4
8.【答案】D 【解析】0.1mol⋅ L-1CuSO 溶液通入H S气体会生成不溶于稀酸的黑色沉淀CuS,不能说明酸性
4 2
H S>H SO ,A错;SO CO 在水中的溶解度不同,不能通过测定饱和溶液的pH来判断酸性强弱,B错;浓盐酸也
2 2 4 2、 2
会使KMnO 褪色,C错;答案选D。
4
9. 【答案】D【解析】由图中“充电”、“放电”和导电介质中带电粒子的迁移方向可知:左图为电解池原理,a为阳极、
b为阴极;右图为原电池原理,c为正极、d为负极。A.c正极的电势比d负极的电势高,故A错误;B.负极为锂
Li,故导电介质不能为水溶液,故B错误;C.a为阳极,失电子发生氧化反应,电极式为
LiMn O -xe-=Li Mn O +Li+,故C错误;D.外电路通过0.2mol电子时,由负极Li-e-=Li+知活性炭电极应
2 4 (1-x) 2 4
减少1.4g,故D正确。
10.【答案】A【解析】A选项,由已知反应机理可知,带正电的Br+最终以Br原子的形式取代苯环上氢原子的位置。
若将Br 换成ICl,由于I的电负性小于Cl,ICl中I带部分正电荷,Cl带部分负电荷,所以最终生成碘苯而非氯
2
苯,A 选项错误。B 选项,根据反应机理中第一步信息,再结合原子守恒和电荷守恒可推出反应Ⅰ为
Br +FeBr →Br++FeBr -,B选项正确。C选项,有机物分子中不饱和碳原子与其他原子或原子团直接结合生成新的
2 3 4
化合物的反应为加成反应,C选项正确。D选项,反应Ⅲ,苯环中与溴原子相连的碳原子由饱和碳原子变为不饱
和碳原子,成键方式发生了改变,D选项正确。
11.【答案】B【解析】晶体中与B最近且等距的Fe2+是4个,答案选B。
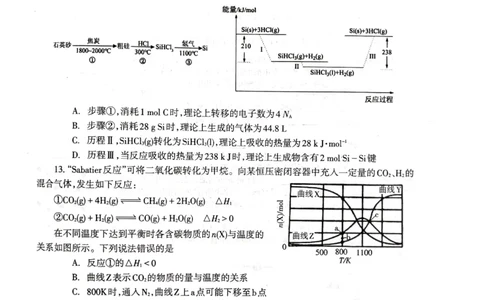
12.【答案】D【解析】A选项,步骤①,C与SiO 反应生成CO,所以1molC参加反应,转移的电子数为2N ,A选
2 A
项错误。B选项,步骤②,未注明标准状况下,所以H 体积无法计算,B选项错误。C选项,由能量变化图可知,
2
历程Ⅱ中SiHCl (g)转化为SiHCl (l)是从高能量转化到低能量,是放热过程,理论上放出的热量为28kJ/mol,而不
3 3
是吸收热量,所以C选项错误。D选项,历程Ⅲ,当反应吸收的热量为238kJ时,根据热化学方程式可知生成1molSi。
硅晶体中每个Si原子与周围4个Si原子形成Si-Si键,所以1molSi中含有2molSi-Si键,选项D正确。
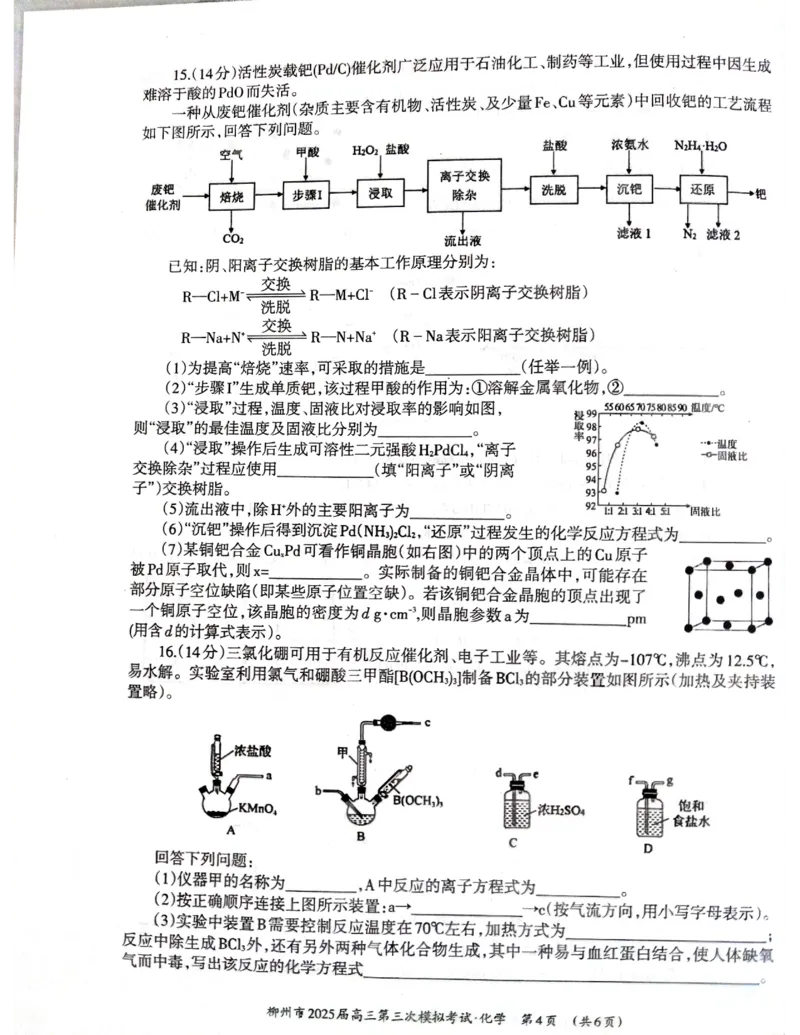
13.【答案】C【解析】恒压条件下,体系中两个反应为竞争反应,反应②为△H >0,温度升高平衡正向移动,CO物
2
质的量增大,曲线Y为CO;根据曲线X和曲线Z的变化趋势,推测反应①△H <0,温度升高平衡逆向移动,
1
CH 的物质的量减小,曲线X为CH ,曲线Z为CO ,1100K之前,以反应①为主,1100K之后,以反应②为主。
4 4 2
故A、B正确。C.恒压条件下通入N ,则容积扩大,反应①逆向移动,CO 的物质的量增大,而压强改变对反应
2 2
②没有影响,故CO 的物质的量增大,应由a点上移,故C错误。反应①正反应方向为气体体积的减小的方向,
2
反应②为反应前后气体体积不变的反应,因此温度升高,平衡移动,对于反应②气体的平均相对分子质量不变,
反应①平衡逆向移动,气体的物质的量增大,气体总质量恒定,故气体的平均相对分子质量减小,故 a点大于c
点,D正确。
14.【答案】D【解析】A.HgS溶解过程吸热,故温度升高,溶解度增大,T 下c(Hg2+)或c(S2-)更大,所以温度T
1 1
>T ,A正确;B.曲线上点均为溶解平衡点,T2下增大c(S2-),溶解平衡逆向移动,c(Hg2+)减小,故可使e点迁
2
移到c点,故B正确;C.T 下g点处,离子积Qc=c(Hg2+)×c(S2-)>K ,处于过饱和状态,故会析出HgS沉淀,
1 sp
故C正确;D.T 下K (HgS)=10-2b,当c(S2-)=0.01mol·L-1时,c(Hg2+)=10-2b÷10-2=102-2bmol·L-1,故D错误。
2 sp
{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}16.(1)答案:将废钯催化剂粉碎(增大反应物接触面积,加快反应速率;或适当提高焙烧温度、适当增加空气流速
等,合理即可)。解析:根据化学反应速率的影响因素,增大反应物接触面积、提高温度、增加气体反应物流
速等都能加快反应速率。
(2)答案:作还原剂,将PdO还原为Pd单质。解析:因为本流程目的是回收钯单质,而焙烧后钯以PdO形式存在,
加入甲酸后生成单质钯,所以甲酸起到还原作用。
(3)答案:最佳温度为70℃,最佳固液比为3∶1。解析:从“浸取率-温度”和“浸取率-固液比”图像可知,70℃时浸
取率最高,固液比为3∶1 时浸取率最高。
(4)答案:阴离子。解析:“浸取”操作后生成可溶性二元强酸H PdCl ,则溶液中存在H+和PdCl 2-等离子,“离
2 4 4
子交换除杂”过程要除去阳离子杂质,PdCl 2-留在树脂中经后续操作最终得到Pd单质,所以应使用阴离子交换
4
树脂。
(5)答案:Fe3+、Cu2+。解析:废钯催化剂中含Fe、Cu等元素,经过前面步骤转化为阳离子,且未被除去,所以流
出液中除H+外主要阳离子是Fe3+、Cu2+。
(6)根据流程可知,反应物是Pd(NH ) Cl 和N H ·H O,产物是Pd单质,N H ·H O作还原剂被氧化为N ,根据元
3 2 2 2 4 2 2 4 2 2
素守恒配平得到该方程式 N H H O+2PdNH Cl =2Pd+N +4NH Cl+H O
2 4 2 3 2 2 2 4 2
(7)
{#{QQABSYA8wgiwwhSACA5KAw10CAoQkIOjJYokAQARKARKABNABIA=}#}16.【解析】A为制备氯气的装置,该方法制备的氯气中有HCl和水蒸气杂质,可通过饱和食盐水和浓硫酸除去,B为
反应装置,实验过程中需要注意三氯化硼熔点为-107℃,沸点为12.5℃,易水解。
(1)甲指向的是球形冷凝管,用高锰酸钾和浓盐酸制备的氯气的离子方程式为
2MnO -+16H++10Cl-==2Mn2++5Cl +8H O;
4 2 2
(2)所制Cl 中有HCl和水蒸气杂质,三氯化硼易水解,需防止水蒸气进入B,由于HCl不影响BCl 的制备可不
2 3
除,仪器连接顺序为fgdebc(或debc);
(3)反应温度70℃左右,最佳加热方式为水浴加热;易与血红蛋白结合,使人体缺氧气而中毒的气体是CO,程
式为 ;
(4)达到滴定终点时过量的SCN-与指示剂电离出的Fe3+生成红色物质,则终点现象为:滴入最后半滴标准液,
溶液由无色变为红色,且半分钟不褪色;
则BCl 的含量为
3
因为K AgSCN