文档内容
高途高中化学
点睛卷
2024
天津市--------------------------- 高途高中化学点睛卷 ---------------------------
绝密 启用前
2024年天津市一般高中学业水平等级性考试化学模考卷
本试卷分为第一卷(选择题)和第二卷(非选择题)两部分,共100分,考试时间60分钟。
第一卷1至4页,第二卷5至9页。
第I卷
本卷共12题,每题3分,共36分。在每题给出的四个选项中,只有一项为哪一项最符
合题目要求。
以下数据可供解题时参考:相对原子质量:H-1 C-12 O-16 Fe-56 S-32 Li-7
1、日常生活、生产、医疗与化学有着密切联系。下列说法错误的是
A. 广泛用于新能源汽车行业的储氢合金是一种新型合金,在室温下吸、放氢的速率快
B. 火星车使用的热控保温材料纳米气凝胶可产生丁达尔效应
C. 发展新能源,主要是把煤、石油转化为气态燃料来提高能源的利用率
D. 港珠澳大桥水下钢柱镶铝块防腐的方法为“牺牲阳极的阴极保护法”
2、下列化学用语表达正确的是
A.基态Cr原子价电子排布式为3d44s2 B.SO
2
的价层电子对互斥模型:
1H O 2H O 2H
C.1 2 和1 2 互为同位素 D.中子数为2的氢原子:1
3、元素周期律的发现是近代化学史上的一座里程碑。下列事实不能用元素周期律解释的是
A.气态氢化物的沸点:H O>H S
2 2
B.Na CO 溶液中加硫酸,产生气泡
2 3
C.Cl 从NaBr溶液中置换出Br
2 2
D.常温下,形状和大小相同的Mg、Al与同浓度盐酸反应,Mg条更剧烈
4、下列常见物质及用途,正确的是
A. SO 具有还原性,可用于漂白纸浆
2
B. 明矾可用于自来水的消毒杀菌
C. Si N 可用于制作高温结构陶瓷
3 4
D. 金属钠具有强还原性,可与TiCl 溶液反应制取金属Ti
4
2--------------------------- 高途高中化学点睛卷 ---------------------------
5、已知完全分解1molH O 放出热量为98kJ,在含有少量I-的溶液中H O 分解的机理为反
2 2 2 2
应I:H
2
O
2
(aq)+I-(aq)IO-(aq)+H
2
O(l) △H
1
;
反应II:H
2
O
2
(aq)+IO-(aq)O
2
(g)+I-(aq)+H
2
O(l) △H
2
。
在一定温度下,其反应过程能量变化如图所示,下列有关该反应的说法不正确的是
A.反应I是焓减小的反应 B.H O 分解产生氧气的决速步是反应I
2 2
C.I-、IO-都是催化剂 D.△H +△H =-196kJ•mol-1
1 2
6、化合物M具有生物活性,其结构如图所示。下列关于M的说法正确的是
A.含有3个手性碳原子 B.能发生加聚反应和氧化反应
C.分子中含有3种官能团 D.1molM最多与5molH 发生加成反应
2
7、25℃时,下列各组离子中可以在水溶液中大量共存的是
A.H +、K +、Fe2+、MnO- B.H、K、NO 、CO2
4 3 3
C.OH、K、Mg2 、NO D.Na、K +、Cl、NO-
3 3
8、下列实验仪器或装置以及药品选择正确的是
B.观察氯化钠的焰色 C.实验室制备
A.测定醋酸溶液浓度 D.灼烧碎海带成灰
试验 NH
3
3--------------------------- 高途高中化学点睛卷 ---------------------------
9、常温下,下列有关电解质溶液的叙述正确的是
已知:[K (CH COOH)=1×10-5][K (NH ·H O)=1×10-5]
a 3 b 3 2
A.向0.1mol·L-1的HF溶液中滴加NaOH溶液至中性:c(Na+)=c(F-)=c(H+)=c(OH-)
B.0.1mol·L-1的NaHS溶液中:c(HS-)+c(S2-)=0.1mol·L-1
C.CH COONa和CH COOH等浓度混合,混合后溶液中:
3 3
c(OH-)+c(CH COO-)c(HC O
)>c(C O
2
)
2 2 4 2 2 4 2 4 2 4
10、下列关于元素及其化合物的性质说法不正确的是
A.氯气通入冷的石灰乳中制得漂白粉
B.高温下C与SiO 反应可制备粗硅
2
C.植物油中含有碳碳双键,具有还原性,能使酸性高锰酸钾溶液褪色
D.由于四水合铜离子
CuH
2
O
4
2为蓝色,则铜盐溶液均为蓝色
11、设N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 1molNiNH 2中键的数目为12N
3 4 A
B.44gCHCHO中sp3
杂化的碳原子数目为1N
3 A
C.标准状况下,11.2LHF中含有的电子数目为5N
A
D.常温下,将56gFe投入足量浓硝酸中,反应转移电子数目为3N
A
12、全固态锂电池以比容量高、安全、轻便等优势成为电动汽车的理想电池。近期,研究者
以硅和石墨为基体,分别负载 Li 和 S 作为电池电极,以 Li PS 为固体电解质进行充放电
3 4
实验,发现该 Li-S电池具有高离子电导率。该电池的装置如图所示,下列说法正确的是
A.Li 和 S无需基体负载,也能正常放电产生电流
B.充电时,阴极电极反应式为:S+2e-+2Li+=Li S
2
C.放电时,Li+从Li电极经 Li PS 固体电解质迁移到 S 电极
3 4
D.用该电池电解饱和食盐水时,若生成 22.4LH ,则需要消耗 14gLi
2
4--------------------------- 高途高中化学点睛卷 ---------------------------
第II卷
注意事项:
1. 用黑色墨水的钢笔或签字笔将 写在答题卡上;
2. 本卷共4题,共64分。
13、(15分)根据物质结构与性质的内在联系,回答下列问题:
(1)基态Si原子的电子排布式为______;该原子价层电子的运动状态有_____种。
(2)硅元素能够形成多种化合物,其中,熔点:SiO ____SiCl (填“>”或“<”),原因是________。
2 4
(3)非金属元素在人们的日常生活中发挥了很大作用,其中,N、O、S的第一电离能由大到
小的顺序为___________(用元素符号表示),SCN立体构型为_______。
(4)Mn的一种配合物的化学式为
Mn(CO) CH CN
,其中Mn原子的配位数为______。
5 3
(5)超导材料TiN具有NaCl型结构(如图),晶胞参数(晶胞边长)为anm,其中阴离子
N3
采用面心立方最密堆积方式,该氮化钛的密度__________g/cm3(列出计算式即可)。
14、(18分)加兰他敏是一种天然活性生物碱,临床上广泛应用于阿尔茨海默病及重症肌肉
无力等疾病的治疗。其合成路线如图(Ph-表示苯基C H -):
6 5
5--------------------------- 高途高中化学点睛卷 ---------------------------
已知:CH COOH+SOCl →CH COCl+SO +HCl
3 2 3 2
回答下列问题:
(1)I(加兰他敏)中的含氧官能团名称为________;E→H的反应类型________。
(2)C的化学名称为________;1molC与浓溴水反应最多消耗________molBr 。
2
(3)写出D→E的反应方程式__________________。
(4)G的结构简式是________。
(5)化合物D有多种同分异构体,写出1种同时符合下列条件的D的同分异构体的结构简式
(不包括立体异构)______________。
①分子中含有2个苯环且每个苯环上都只有2个互为对位的取代基;
②能发生银镜反应,且1molD与足量的Na CO 溶液反应,消耗Na CO 的物质的量为2mol。
2 3 2 3
(6)根据上述路线信息,设计由乙醇和苯胺为原料制备具有止痛、退热和防腐作用的乙酰苯
胺( )的合成路线(无机试剂任选)________。
15、(17分)焦亚硫酸钠(Na S O )是一种可溶于水的白色或淡黄色小晶体,食品级焦亚硫酸
2 2 5
钠可作为贮存水果的保鲜剂等。某化学研究兴趣小组欲自制焦亚硫酸钠并探究其部分化学性
质等。
(1)制备Na S O ,如图(夹持及加热装置略)
2 2 5
可用试剂:饱和Na SO 溶液、浓NaOH溶液、浓H SO 、苯、Na SO 固体焦亚硫酸钠的析
2 3 2 4 2 3
出原理:NaHSO (饱和溶液)→Na S O (晶体)+H O(1)。
3 2 2 5 2
①F中盛装的试剂是_____。E装置的作用是____。
②通入N 的作用是_____。
2
③Na S O 晶体在装置_____中得到,再经离心分离,干燥后可得纯净的样品。
2 2 5
6--------------------------- 高途高中化学点睛卷 ---------------------------
(2)设计实验探究Na S O 的性质,完成表中填空:
2 2 5
预测Na S O 的性质 探究Na S O 性质的操作及现象
2 2 5 2 2 5
探究一 Na S O 的溶液呈酸性 用适量蒸馏水溶解少量Na S O 固体于试管中,①
2 2 5 2 2 5
取少量Na S O 晶体于试管中,滴加1mL2mol•L-1酸性
探究二 Na S O 晶体具有还原性 2 2 5
2 2 5 KMnO 溶液,剧烈反应,溶液紫红色很快褪去
4
①补充步骤①的操作与现象:______________________(提供:pH试纸、蒸馏水及实验必需
的玻璃仪器)。
②探究二中反应的离子方程式为__________________。
(3)试设计检验Na S O 晶体在空气中已被氧化的实验方案____________________。
2 2 5
16、(14分)氨基甲酸铵(H NCOONH )为尿素生产过程的中间产物,易分解。
2 4
已知:
Ⅰ.N (g)+3H (g)⇌ 2NH (g) ΔH =-92kJ·mol-1
2 2 3 1
Ⅱ.C(s)+O (g)⇌ CO (g) ΔH =-394kJ·mo1-1
2 2 2
Ⅲ.N (g)+3H (g)+C(s)+O (g)⇌ H NCOONH (s) ΔH =-646kJ·mol-1
2 2 2 2 4 3
Ⅳ.H NCOONH (s)⇌ 2NH (g)+CO (g) ΔH
2 4 3 2 4
回答下列问题:
(1)NH 的空间构型为___________。NH 的键角大于PH , 分析原因:___________。
3 3 3
(2)ΔH =___________。 T℃下在某密闭容器中加入H NCOONH (s),假设只发生反应Ⅳ,达
4 2 4
平衡时测得NH 的浓度为c ;保持温度不变,加压(缩小容器的体积),测得新的平衡条件下
3 1
NH 的浓度为c ,则c ___________c (填“>”“<”或“=”)。反应Ⅳ在___________(填“高温”“低
3 2 1 2
温”或“任意温度”)条件下能够自发进行。
(3)某温度下在一刚性的密闭容器中,充入等物质的量N 和H 发生反应Ⅰ,起始压强为1MPa,
2 2
10min 末达平衡,测得平衡时压强为0.8MPa,则10min内v(N )=___________MPa/min。此
2
时平衡常数K =___________。对于该条件下的反应,下列说法错误的是___________。
p
A.当N 的体积分数不变时,说明反应已经达到化学平衡状态
2
B.温度升高化学反应速率加快,化学平衡常数增大
C.其他条件不变时,若适当增加N 的用量,可以提高H 的平衡转化率
2 2
D.使用合适的催化剂可以加快化学反应速率,但ΔH 不变
1
7--------------------------- 高途高中化学点睛卷 ---------------------------
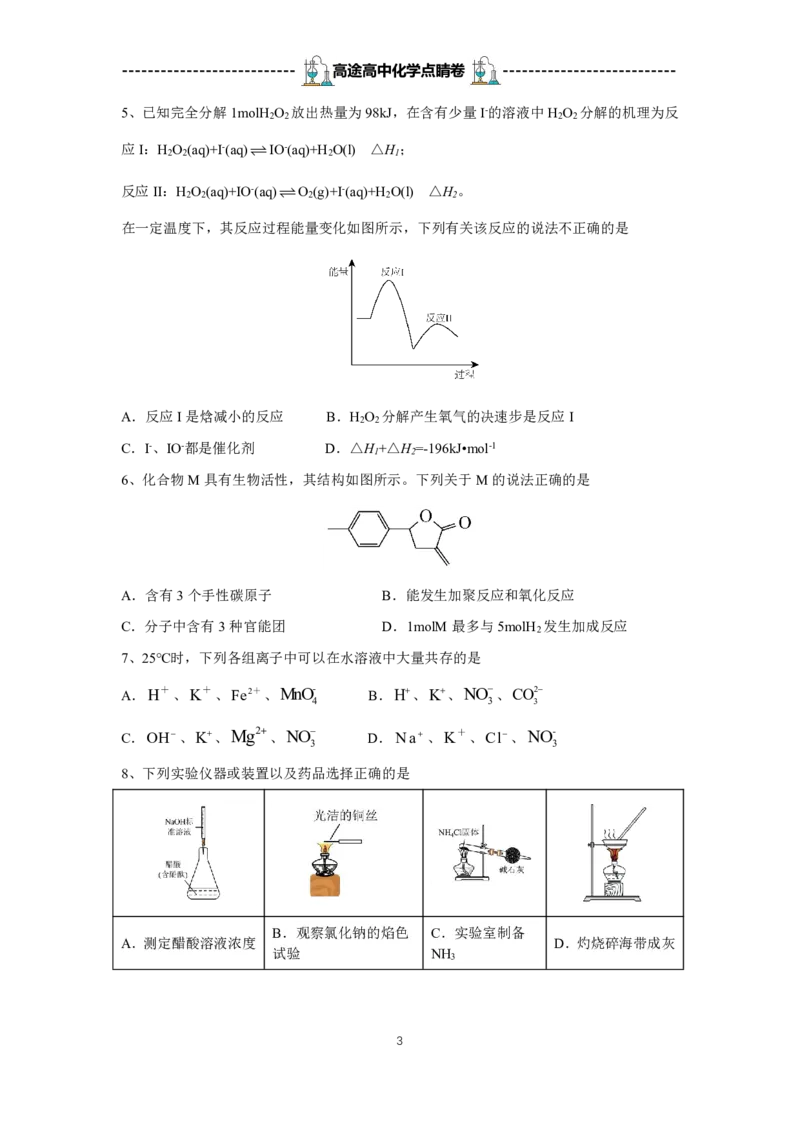
(4)在一定的条件 下,将AmolN 和BmolH 充入某体积固定的密闭容器中合成NH ,在不
2 2 3
同的催化剂(甲或乙)下发生反应,反应相同时间后H 的转化率与温度的关系如图:
2
某学习小组的同学通过讨论得出结论: 200°C时, a点对应的转化率(5%)不是使用催化剂
甲下H 的平衡转化率。判断依据是:___________。
2
8--------------------------- 高途高中化学点睛卷 ---------------------------
2024 年天津市一般高中学业水平等级性考试化学模考卷
参考答案
1、【答案】C
【解析】A. 广泛用于新能源汽车行业的储氢合金是一种新型合金,在室温下吸、放氢的速
率快,故A正确;
B. 纳米气凝胶具有胶体的性质,能产生丁达尔效应,故B正确;
C. 发展新能源的概念是指开发可再生、无污染的新型能源,比如氢能源、太阳能等,故C
错误;
D. 钢柱、铝块、海水构成的原电池中,较活泼的铝被氧化,可看作阳极,钢柱被保护,故
此防腐的方法为牺牲阳极的阴极保护法,故D正确。故答案选C。
2、【答案】B
【解析】A.根据洪特规则的特例,基态Cr原子价电子排布式为3d54s1,A错误;
622
B.SO 的中心原子孤电子对数= 1、价层电子对数=2+1=3,则二氧化硫的价层电
2
2
子对互斥模型为: ,B正确;
C.同位素是指质子数相同而中子数不同的同一元素的不同原子互称为同位素,故C错误;
D.中子数为2的氢原子表示为:3H ,D错误;故答案选B。
1
3、【答案】A
【详解】A.水分之间存在氢键,故水的沸点高于H S,与元素周期律无关,A符合题意;
2
B.碳酸钠加入硫酸生成二氧化碳气体,说明硫酸酸性强于碳酸,硫酸与碳酸均为最高价含
氧酸,非金属元素的非金属性越强,其最高价含氧酸的酸性越强,B不符合题意;
C.同主族元素,从上到下,非金属性减弱,单质的氧化性减弱,氯气氧化性强于溴,则氯
气与溴化钠制取溴单质,C不符合题意;
D.同周期元素,从左到右,金属性减弱,则Mg、Al与酸反应时,Mg的反应更加剧烈,D
不符合题意;故答案为:A。
4、【答案】C
A. SO 漂白时不涉及氧化还原反应,故A错误;
2
9--------------------------- 高途高中化学点睛卷 ---------------------------
B. 明矾主要成分为十二水硫酸铝钾[KAlSO 12H O],溶于水电离出的Al3+进行水解反应
4 2 2
生成Al(OH) (胶体),净水的原理是利用胶体的吸附性使水中细小的悬浮物颗粒集成较大的
3
颗粒而沉降,从而除去水中的悬浮物,达到净水的目的;但不具备消毒杀菌的能力,故B
错误;
C. 新型陶瓷中的高温结构陶瓷一般用碳化硅、氮化硅和某些金属氧化物等在高温下烧结而
成,故C正确;
D. 钠是活泼金属,可与水快速反应,故不能从盐的水溶液中置换出金属单质,应与熔融TiCl
4
反应制取金属Ti,故D错误;故答案选C。
5、【答案】C
【详解】A.从图中可以看出,反应I中生成物的总能量低于反应物的总能量,所以该反应
是焓减小的反应,A正确;
B.从图中可以看出,反应Ⅰ的活化能大,则H O 分解产生氧气的决速步是反应I,B正确;
2 2
I
C.将两步反应加和,总反应为2H O (aq)2H O(aq)+O (g),则I-是该反应的催化剂,IO-
2 2 2 2
是催化剂的中间产物,C不正确;
I
D.依题意得2H O (aq)2H O(aq)+O (g) △H=-196kJ•mol-1,依据盖斯定律,将反应Ⅰ+Ⅱ
2 2 2 2
I
得,2H O (aq)2H O(aq)+O (g) △H=△H +△H =-196kJ•mol-1,D正确;故选C。
2 2 2 2 1 2
6、【答案】B
【详解】A. 由M的结构知,分子中含有1个手性碳原子,A错误;
B.含有碳碳双键,能发生加聚反应,含有碳碳双键、苯环上连有甲基,能发生氧化反应,
B正确;
C.分子中含有碳碳双键和酯基两种官能团,C错误;
D.苯环和碳碳双键能与氢气发生加成反应,1molM最多与4mol H 发生加成反应,D错误;
2
故选B。
7、【答案】D
【详解】A.酸性条件下,高锰酸根离子与亚铁离子发生氧化还原反应不能大量共存,A错
误;
10--------------------------- 高途高中化学点睛卷 ---------------------------
B.H和CO2产生二氧化碳气体,不能大量共存,B错误;
3
C.
OH和Mg2
产生沉淀,不能大量共存,C错误;
D. 各离子之间不反应,可以大量共存,D正确。
8、【答案】A
【详解】A. 利用氢氧化钠溶液测定醋酸溶液的浓度,氢氧化钠标准液盛放于碱式滴定管,
终点为碱性,选用酚酞作指示剂,故A正确;
B. 铜也具有焰色,与钠元素的焰色发生冲突,不能观察到钠元素的焰色,故B错误;
C.NH Cl不稳定,受热分解产生NH 、HCl,两种气体在试管口遇冷会重新化合形成NH Cl
4 3 4
固体,因此不能用加热NH Cl固体的方法制取NH ,C错误;
4 3
D. 灼烧固体应在坩埚中,不能使用蒸发皿,故D错误。故答案选A。
9、【答案】D
【解析】A.向0.1mol·L-1的HF溶液中演加NaOH溶液至中性,所得为NaF、HF的混合溶
液,溶质主要为NaF、含少量HF,按电荷守恒可知:c(Na+)=c(F-)>c(H+)=c(OH-),A错误;
B.NaHS 溶液中 HS-既电离又水解 ,按物料守恒可知,0.1mol·L-1的 NaHS 溶液中:
c(H S)+c(HS-)+c(S2-)=0.1mol·L-1,B错误;
2
C.溶液中存在电荷守恒:c(OH-)+c(CH COO-)=c(Na+)+c(H+),由于CH COOH 的电离作用
3 3
大于CH COO-的水解作用,Na+不水解,所以c(CH COOH)<c(Na+),则溶液中微粒浓度关
3 3
系为:c(OH-)+c(CH COO-)>c(CH COOH)+c(H+),C错误;
3 3
D.H C O 难电离,一级电离为主,则0.1mol·L-1的H C O 溶液中:c(H C O )>c(HC O )
2 2 4 2 2 4 2 2 4 2 4
>c(C O
2
),D正确;故答案选D。
2 4
10、【答案】D
【详解】A.氯气通入冷的石灰乳中发生歧化反应生成氯化钙和次氯酸钙制得漂白粉,A正
确;
B.高温下C与SiO 反应生成CO和Si,C与SiO 反应可制备粗硅,故B正确;
2 2
C.植物油中含有碳碳双键,具有还原性,能发生氧化反应,使酸性高锰酸钾溶液褪色,选
项C正确;
D.氯化铜溶液中含有 CuCl 2 , CuCl 2 是黄色的,CuCl 溶液由于同时含有
4 4 2
11--------------------------- 高途高中化学点睛卷 ---------------------------
[Cu(H O)]2+和 CuCl 2以及Cl和H O的混合配离子,通常为黄绿色或绿色,选项D
2 4 4 2
错误,故答案选D。
11、【答案】B
【详解】A.
NiNH
3
4
2中含有12个N-H键和4个配位键也是键,故1mol
NiNH
3
4
2
中键的数目为
16N
,A错误;
A
B.CH
CHO中甲基中碳原子采用sp3杂化,醛基上碳原子采用sp2杂化,故44gCHCHO中sp3
3 3
杂化的碳原子数目为 44g ×1N mol-1= 1N ,B正确;
44gmol-1 A A
C.标准状况下HF为液体,故无法计算11.2LHF中含有的电子数目,C错误;
D.常温下Fe遇到浓硝酸将发生钝化,将56gFe投入足量浓硝酸中,无法计算反应转移电
子数目,D错误;故答案为:B。
12、【答案】C
【详解】A.硅和石墨为基体,分别负载 Li 和 S 作为电池电极,硫不导电,所以需用石
墨为载体,故A错误;
B.充电时,Li电极为阴极,阴极电极反应式为:Li++e-=Li,故B错误;
C.放电时,Li为负极、S为正极,阳离子由负极向正极移动,Li+从Li电极经 Li PS 固体
3 4
电解质迁移到 S 电极,故C正确;
D.没有明确是否为标准状况,22.4LH 的物质的量不一定是1mol,所以消耗Li的质量不一
2
定是14g,故D错误;故选C。
13、【答案】(1)1s22s22p63s23p2 4 (2)> 二氧化硅为共价晶体,而四氯化硅为分子晶体,
共价晶体的熔点大于分子晶体 (3)N>O>S;直线形 (4)6 (5) 248 1021
a3N
A
【详解】(1)硅为14号元素,基态Si原子的电子排布式为1s22s22p63s23p2;该原子价层电
子排布为3s23p2,其电子运动状态有4种。
(2)二氧化硅为共价晶体,而四氯化硅为分子晶体,共价晶体熔点高于分子晶体,则熔点:
SiO >SiCl ;
2 4
(3)同周期元素,从左到右第一电离能呈增大的趋势,但氮原子的2p轨道为半充满的稳定
结构,第一电离能比相邻元素大,同主族元素,从上到下第一电离能依次减小,则N、O、
S的第一电离能由大到小的顺序为N>O>S;硫氰酸根离子的价电子数和原子个数与二氧
12--------------------------- 高途高中化学点睛卷 ---------------------------
化碳相同,硫氰酸根与二氧化碳互为等电子体,等电子体具有相同的空间结构,二氧化碳的
空间结构为直线形,则硫氰酸根的空间构型也为直线形,故答案为: N>O>S;直线形;
(4)由化学式可知,Mn原子的配位数为6;
1 1 1
(5)根据“均摊法”,晶胞中含8 +6 4个N3、12 14个Ti3+,则晶体密度
8 2 4
4M
N 248
为 A 1021gcm3= 1021gcm3。
a3 a3N
A
14、【答案】(1)羟基、醚键 取代反应 (2)对羟基苯乙酸或4-羟基苯乙酸 2
(3) +SOCl → +SO +HCl (4)
2 2
(5) 或 或
(6)
【分析】A与KCN发生取代反应生成B,B经酸化生成C,C在题给条件下发生取代反应
生成D,结合E的结构分析可知D为 ,D与SOCl 发生取代反应生成E,E与G反
2
应生成H,结合H的结构简式可知该反应为取代反应,G的结构简式为: ,
H经一系列处理得到I,据此解答。
【详解】(1)由I的结构简式可知其所含的含氧官能团为羟基、醚键,由以上分析可知E→H
发生取代反应,故答案为:羟基、醚键;取代反应;
13--------------------------- 高途高中化学点睛卷 ---------------------------
(2)由C的结构简式可知其名称为对羟基苯乙酸或4-羟基苯乙酸,其中酚羟基的邻对位氢
原子可与溴单质发生取代反应,1molC中含2mol酚羟基邻位氢,能与2mol溴单质发生取
代反应,故答案为:对羟基苯乙酸或4-羟基苯乙酸;2。
15、【答案】(1) 浓NaOH溶液 防倒吸 排尽空气,防止Na S O 被氧化 D
2 2 5
(2) 用玻璃棒醮取少量Na S O 溶液点在pH试纸上,试纸变红
2 2 5
2 2
5S
2
O5 +4MnO4+2H+=10SO4 +4Mn2++H
2
O
(3)取少量Na S O 晶体于试管中,加入适量水溶解,滴加足量稀盐酸,振荡,再滴加几滴氯
2 2 5
化钡溶液,有白色沉淀生成
【分析】根据图可知:装置A中浓硫酸与亚硫酸钠溶液反应生成SO ,装置D中盛放饱和
2
Na SO 溶液,和SO 反应得到NaHSO 饱和溶液,从而析出Na S O 晶体;二氧化硫有毒,
2 3 2 3 2 2 5
装置F为尾气吸收装置,装置E防止倒吸。
【详解】(1)①根据仪器的结构可知A为三颈烧瓶;装置F中盛放浓NaOH溶液吸收未反
应的尾气,SO 极易溶液NaOH溶液,所以装置E用来防倒吸;
2
②Na S O 易被空气中的氧气氧化,所以要先用氮气排净装置中的空气;
2 2 5
③装置D中盛放饱和Na SO 溶液,和SO 反应得到NaHSO 饱和溶液,从而析出Na S O
2 3 2 3 2 2 5
晶体;
(2)①探究一验证Na S O 的溶液呈酸性,可以通过测定pH值确定,具体操作为:用玻璃
2 2 5
棒醮取少量Na S O 溶液点在pH试纸上,试纸变红;
2 2 5
②探究二中Na S O 与酸性KMnO 溶液发生氧化反应反应,KMnO 被还原为Mn2+,Na S O
2 2 5 4 4 2 2 5
被氧化为硫酸钠,根据电子守恒、元素守恒可得离子反应为:
5S O
2
+4MnO
+2H+=10SO
2
+4Mn2++H O;
2 5 4 4 2
(3)Na S O 晶体在空气中被氧化会生成硫酸钠,若检验到硫酸根则可以证明晶体被氧化,
2 2 5
具体操作为:取少量Na S O 晶体于试管中,加入适量水溶解,滴加足量稀盐酸,振荡,再
2 2 5
滴加几滴氯化钡溶液,有白色沉淀生成。
16、【答案】(1)三角锥形 中心原子均为sp3杂化,且都只有一对孤电子对,电负性N>P,
NH 中的键合电子(共用电子对)离中心原子更近,排斥力更大,键角越大
3
(2)+160kJ·mol-l = 高温 (3)0.01 12.5(MPa)-2 B
(4)催化剂不能使平衡发生移动,该反应为放热反应,温度升高平衡逆向移动,则a点为200℃
时使用催化剂甲下的平衡转化率应高于b点的转化率
14--------------------------- 高途高中化学点睛卷 ---------------------------
【详解】(1)NH 中心原子氮原子形成3个共价键且含有1对孤电子对,为sp3杂化,空间
3
构型为三角锥形;NH 的键角大于PH ,原因为:中心原子均为sp3杂化,且都只有一对孤
3 3
电子对,电负性N>P,NH 中的键合电子(共用电子对)离中心原子更近,排斥力更大,键角
3
越大;
(2)已知:Ⅰ.N (g)+3H (g)⇌ 2NH (g) ΔH =-92kJ·mol-1
2 2 3 1
Ⅱ.C(s)+O (g)⇌ CO (g) ΔH =-394kJ·mo1-1
2 2 2
Ⅲ.N (g)+3H (g)+C(s)+O (g)⇌ H NCOONH (s) ΔH =-646kJ·mol-1
2 2 2 2 4 3
由盖斯定律可知,Ⅰ+Ⅱ-Ⅲ得到反应Ⅳ.H NCOONH (s)⇌ 2NH (g)+CO (g),故
2 4 3 2
ΔH =ΔH +ΔH -ΔH =+160kJ·mol-1;
4 1 2 3
反应Ⅳ的平衡常数为:K=c2(NH )c(CO ),密闭容器中加入H NCOONH (s),保持温度不变,
3 2 2 4
加压平衡常数不变,则新的平衡条件下NH 的浓度为c =c ;反应Ⅳ为吸热的熵增反应,故
3 2 1
在高温条件下能够自发进行;
(3)刚性的密闭容器中,充入等物质的量N 和H 发生反应Ⅰ,假设投料均为1mol,起始压
2 2
强为1MPa;10min 末达平衡,测得平衡时压强为0.8MPa,则总的物质的量为1.6mol,总
的物质的量减小0.4mol,根据N (g)+3H (g)⇌ 2NH (g)可知生成氨气0.4mol、消耗氮气、氢
2 2 3
气分别为0.2mol、0.6mol,平衡时氮气、氢气、氨气分别为0.8mol、0.4mol、0.4mol,则10min
0.42
1 0.8 0.8MPa
内v(N 2 )= 1MPa 2 0.8MPa 1.6 =0.01 MPa/min。此时平衡常数K p = 0.8 1.6 0.43 =12.5 MPa-2。
10min 0.8MPa 0.8MPa
1.6 1.6
A.当N 的体积分数不变时,说明正逆反应速率相等,平衡不再移动,反应已经达到化学
2
平衡状态,A正确;
B.反应为放热反应,温度升高化学反应速率加快,平衡逆向移动,化学平衡常数减小,B
错误;
C.其他条件不变时,若适当增加N 的用量,平衡正向移动,可以提高H 的平衡转化率,
2 2
C正确;
D.使用合适的催化剂可以加快化学反应速率,但不该反应的焓变,故ΔH 不变,D正确;
1
故选B;
(4)催化剂不能使平衡发生移动,该反应为放热反应,温度升高平衡逆向移动,则a点为
200℃时使用催化剂甲下的平衡转化率应高于b点的转化率,与图像不符,故200°C时, a
点对应的转化率(5%)不是使用催化剂甲下H 的平衡转化率。
2
15