文档内容
专题 06 化学变化中的能量变化和反应机理
考点 三年考情(2022-2024) 命题趋势
高考中有关化学反应的热效应内容的考查
在选择题和主观题中都会涉及,在选择题
◆化学反应中的能量变化:2024安徽卷、
中考查的主要形式有两种:一是考查简单
2024湖南卷、2023湖北卷、2022天津卷、
的化学反应能量变化形式和能源对自然环
2022广东卷、2022浙江卷、2022重庆卷
考点1 化学反 境和社会发展的影响;二是以陌生的化学
◆化学反应历程、机理:2024浙江卷、
应中的能量变 反应机理图为载体进行考查,涉及的知识
2024甘肃卷、2024北京卷、2024广东卷、
化 点较多,如氧化还原反应、化学键的判
2024河北卷、2023新课标卷、2023湖南
断、方程式的书写等。随着新高考单科卷
卷、2023浙江卷、2022湖南卷、2022山东
的实行,对应化学反应的热效应的考查也
卷
会有所增加,有关焓变的比较和热化学方
程式的判断会增加考查。
考法01 化学反应中的能量变化
1. (2024·安徽卷)某温度下,在密闭容器中充入一定量的X(g),发生下列反应:X(g) Y(g)(ΔH <0),
1
Y(g) Z(g)(ΔH<0),测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意的是
2
A B.
.C. D.
【答案】B
【分析】由图可知,反应初期随着时间的推移X的浓度逐渐减小、Y和Z的浓度逐渐增大,后来随着时间
的推移X和Y的浓度逐渐减小、Z的浓度继续逐渐增大,说明X(g) Y(g)的反应速率大于Y(g) Z(g)的
反应速率,则反应X(g) Y(g)的活化能小于反应Y(g) Z(g)的活化能。
【解析】A.X(g) Y(g)和Y(g) Z(g) 的∆H都小于0,而图像显示Y的能量高于X,即图像显示X(g)
Y(g)为吸热反应,A项不符合题意;
B.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都小于0,且X(g) Y(g)的活化能小于Y(g) Z(g)的活
化能,B项符合题意;
C.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都小于0,但图像上X(g) Y(g)的活化能大于Y(g)
Z(g)的活化能,C项不符合题意;
D.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都大于0,且X(g) Y(g)的活化能大于Y(g) Z(g)的活
化能,D项不符合题意;
选B。
2. (2024·湖南卷)近年来,我国新能源产业得到了蓬勃发展,下列说法错误的是
A. 理想的新能源应具有资源丰富、可再生、对环境无污染等特点
B. 氢氧燃料电池具有能量转化率高、清洁等优点
C. 锂离子电池放电时锂离子从负极脱嵌,充电时锂离子从正极脱嵌
D. 太阳能电池是一种将化学能转化为电能的装置
【答案】D
【解析】A.理想的新能源应具有可再生、无污染等特点,故A正确;
B.氢氧燃料电池利用原电池将化学能转化为电能,对氢气与氧气反应的能量进行利用,减小了直接燃烧
的热量散失,产物无污染,故具有能量转化率高、清洁等优点,B正确;
C.脱嵌是锂从电极材料中出来的过程,放电时,负极材料产生锂离子,则锂离子在负极脱嵌,则充电时,
锂离子在阳极脱嵌,C正确;
D.太阳能电池是一种将太阳能能转化为电能的装置,D错误;
本题选D。
3.(2023·湖北卷)2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进入到高质量发
展新阶段。下列不能作为火箭推进剂的是
A.液氮-液氢 B.液氧-液氢 C.液态 -肼 D.液氧-煤油
【答案】A【解析】A.虽然氮气在一定的条件下可以与氢气反应,而且是放热反应,但是,由于 键能很大,
该反应的速率很慢,氢气不能在氮气中燃烧,在短时间内不能产生大量的热量和大量的气体,因此,液氮-
液氢不能作为火箭推进剂,A符合题意;
B.氢气可以在氧气中燃烧,反应速率很快且放出大量的热、生成大量气体,因此,液氧-液氢能作为火箭
推进剂,B不符合题意;
C.肼和 在一定的条件下可以发生剧烈反应,该反应放出大量的热,且生成大量气体,因此,液态
-肼能作为火箭推进剂,C不符合题意;
D.煤油可以在氧气中燃烧,反应速率很快且放出大量的热、生成大量气体,因此,液氧-煤油能作为火箭
推进剂,D不符合题意;
综上所述,本题选A。
4.(2022·天津卷)一定条件下,石墨转化为金刚石吸收能量。下列关于石墨和金刚石的说法正确的是
A.金刚石比石墨稳定
B.两物质的碳碳 键的键角相同
C.等质量的石墨和金刚石中,碳碳 键数目之比为4∶3
D.可以用X射线衍射仪鉴别金刚石和石墨
【答案】D
【解析】A.石墨转化为金刚石吸收能量,则石墨能量低,根据能量越低越稳定,因此石墨比金刚石稳定,
故A错误;
B.金刚石是空间网状正四面体形,键角为109°28′,石墨是层内正六边形,键角为120°,因此碳碳 键的
键角不相同,故B错误;
C.金刚石是空间网状正四面体形,石墨是层内正六边形,层与层之间通过范德华力连接,1mol金刚石有
2mol碳碳 键,1mol石墨有1.5mol碳碳 键,因此等质量的石墨和金刚石中,碳碳 键数目之比为
3∶4,故C错误;
D.金刚石和石墨是两种不同的晶体类型,因此可用X射线衍射仪鉴别,故D正确。
综上所述,答案为D。
5.(2021·广东卷)“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征系列运
载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是
A.煤油是可再生能源
B. 燃烧过程中热能转化为化学能
C.火星陨石中的 质量数为20
D.月壤中的 与地球上的 互为同位素
【答案】C
【解析】A.煤油来源于石油,属于不可再生能源,故A错误;
B.氢气的燃烧过程放出热量,将化学能变为热能,故B错误;
C.元素符号左上角数字为质量数,所以火星陨石中的 20Ne 质量数为20,故C正确;
D.同位素须为同种元素,3He 和 3H的质子数不同,不可能为同位素关系,故D错误;故选C。
6.(2022·浙江卷)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O H O H O
2 2 2 2 2
24
能量/kJmol-1 218 39 10 0 0 136 242
9
可根据HO(g)+HO(g)=H O (g)计算出H O 中氧氧单键的键能为214kJmol-1。下列说法不正确的是
2 2 2 2
A.H 的键能为436kJmol-1
2
B.O 的键能大于H O 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量:HOOClCHCOOCH CH
2 2 3 2 2 3
D. 与OH-反应、 与18OH-反应,两者所得醇和羧酸盐均不同
【答案】D
【解析】
【解析】A.步骤Ⅰ是氢氧根离子与酯基中的 作用生成羟基和O-,A正确;
B.步骤Ⅰ加入氢氧根离子使平衡Ⅰ正向移动,氢氧根离子与羧基反应使平衡Ⅱ也正向移动,使得酯在
NaOH溶液中发生的水解反应不可逆,B正确;
C.从信息②可知,随着取代基R上Cl个数的增多,水解相对速率增大,原因为Cl电负性较强,对电子的
吸引能力较强,使得酯基的水解速率增大,F的电负性强于Cl,FCH 对电子的吸引能力更强,因此酯的水
2
解速率 ,C正确;D. 与氢氧根离子反应,根据信息①可知,第一步反应后18O既存在于羟基中也存在于
O-中,随着反应进行,最终18O存在于羧酸盐中,同理 与18OH-反应,最终18O存在于羧
酸盐中,两者所得醇和羧酸盐相同,D错误;
故答案选D。
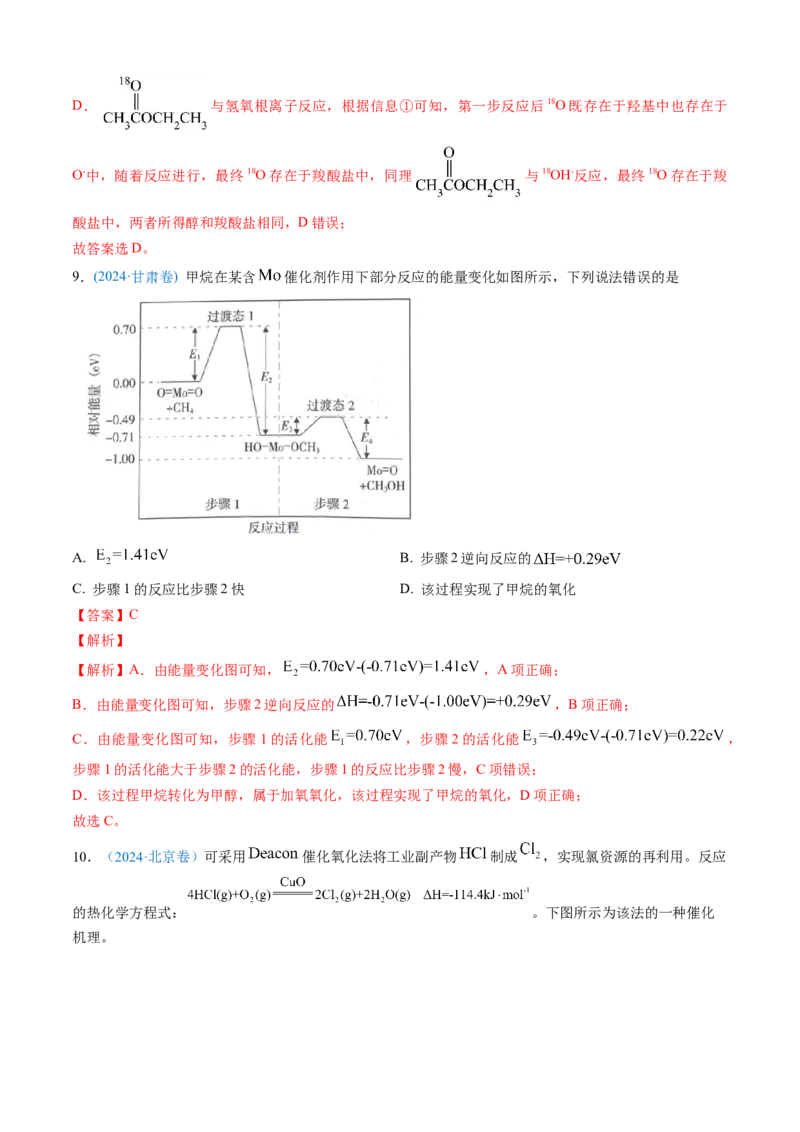
9.(2024·甘肃卷) 甲烷在某含 催化剂作用下部分反应的能量变化如图所示,下列说法错误的是
A. B. 步骤2逆向反应的
C. 步骤1的反应比步骤2快 D. 该过程实现了甲烷的氧化
【答案】C
【解析】
【解析】A.由能量变化图可知, ,A项正确;
B.由能量变化图可知,步骤2逆向反应的 ,B项正确;
C.由能量变化图可知,步骤1的活化能 ,步骤2的活化能 ,
步骤1的活化能大于步骤2的活化能,步骤1的反应比步骤2慢,C项错误;
D.该过程甲烷转化为甲醇,属于加氧氧化,该过程实现了甲烷的氧化,D项正确;
故选C。
10.(2024·北京卷)可采用 催化氧化法将工业副产物 制成 ,实现氯资源的再利用。反应
的热化学方程式: 。下图所示为该法的一种催化
机理。下列说法不正确的是( )
A.Y为反应物 ,W为生成物
B.反应制得 ,须投入
C.升高反应温度, 被 氧化制 的反应平衡常数减小
D.图中转化涉及的反应中有两个属于氧化还原反应
【答案】B
【解析】结合反应机理分析,X、Y、Z、W依次是 、 、 、 ,A正确; 在反应中作
催化剂,会不断循环,适量即可,B错误;总反应为放热反应,其他条件一定,升温平衡逆向移动,平衡
常数减小.C正确;图中涉及的两个氧化还原反应是 和 ,D正确。
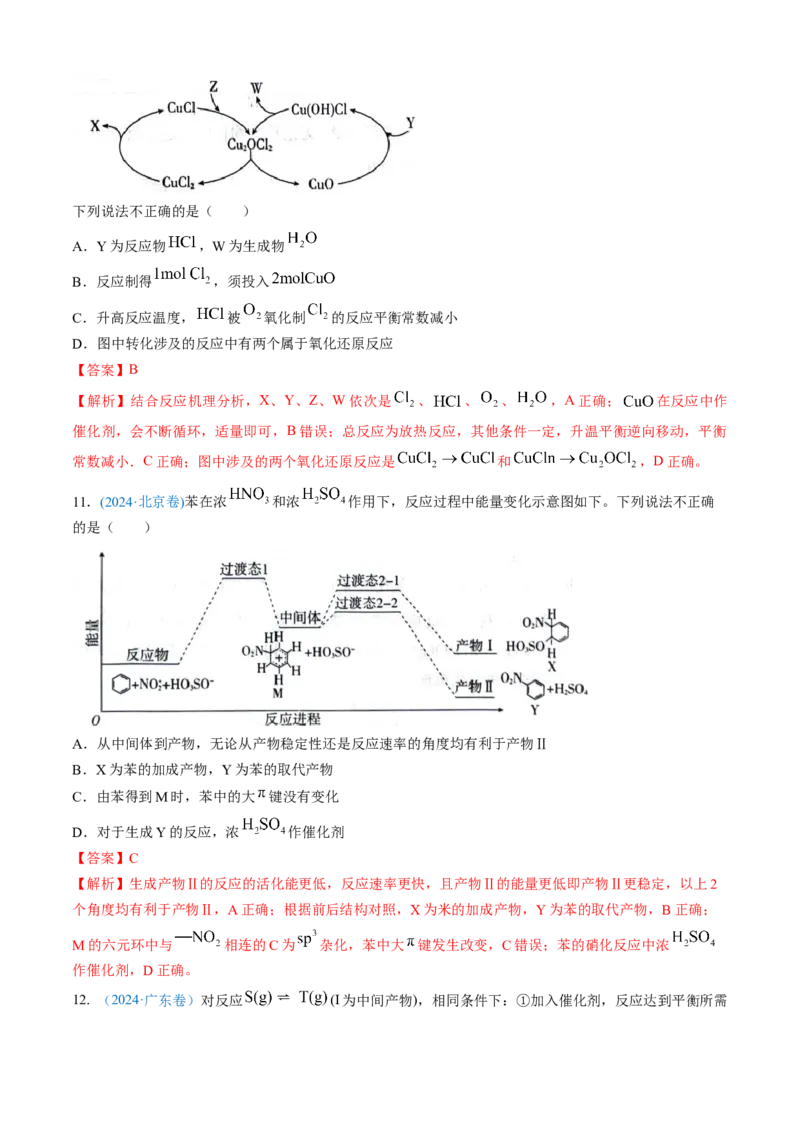
11.(2024·北京卷)苯在浓 和浓 作用下,反应过程中能量变化示意图如下。下列说法不正确
的是( )
A.从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ
B.X为苯的加成产物,Y为苯的取代产物
C.由苯得到M时,苯中的大 键没有变化
D.对于生成Y的反应,浓 作催化剂
【答案】C
【解析】生成产物Ⅱ的反应的活化能更低,反应速率更快,且产物Ⅱ的能量更低即产物Ⅱ更稳定,以上2
个角度均有利于产物Ⅱ,A正确;根据前后结构对照,X为米的加成产物,Y为苯的取代产物,B正确;
M的六元环中与 相连的C为 杂化,苯中大 键发生改变,C错误;苯的硝化反应中浓
作催化剂,D正确。
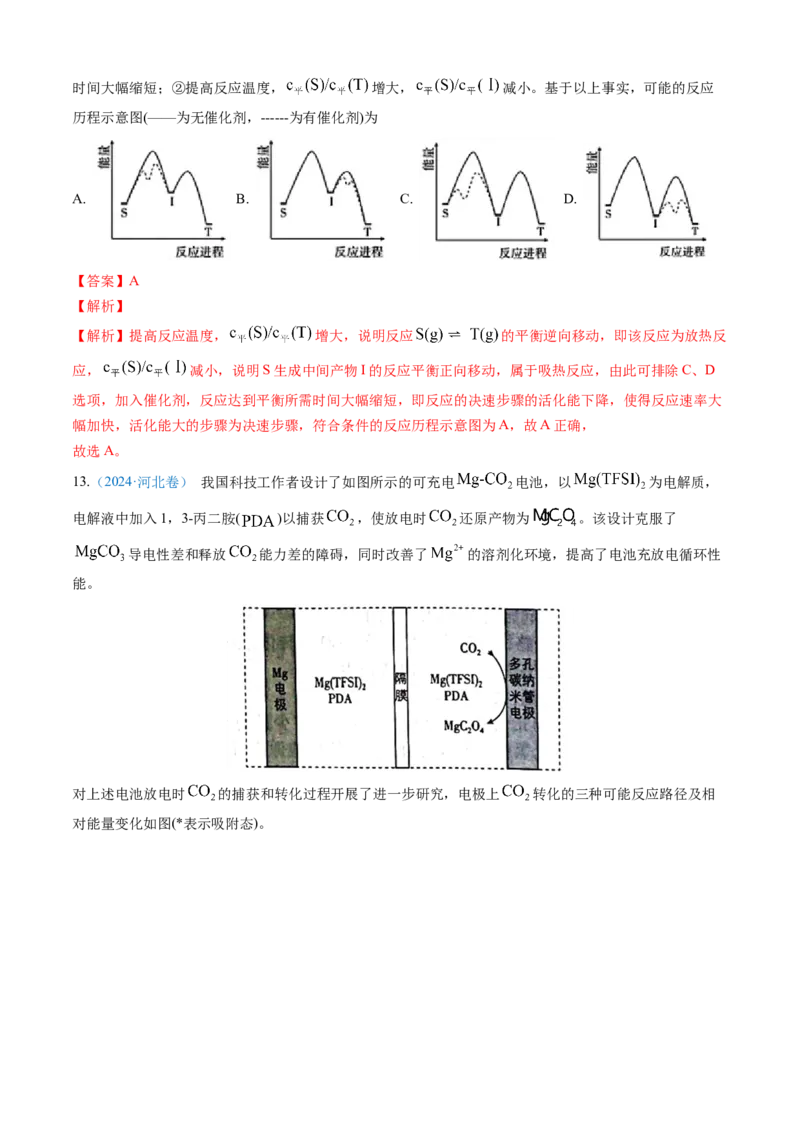
12. (2024·广东卷)对反应 (I为中间产物),相同条件下:①加入催化剂,反应达到平衡所需时间大幅缩短;②提高反应温度, 增大, 减小。基于以上事实,可能的反应
历程示意图(——为无催化剂,------为有催化剂)为
A. B. C. D.
【答案】A
【解析】
【解析】提高反应温度, 增大,说明反应 的平衡逆向移动,即该反应为放热反
应, 减小,说明S生成中间产物I的反应平衡正向移动,属于吸热反应,由此可排除C、D
选项,加入催化剂,反应达到平衡所需时间大幅缩短,即反应的决速步骤的活化能下降,使得反应速率大
幅加快,活化能大的步骤为决速步骤,符合条件的反应历程示意图为A,故A正确,
故选A。
13.(2024·河北卷) 我国科技工作者设计了如图所示的可充电 电池,以 为电解质,
电解液中加入1,3-丙二胺( )以捕获 ,使放电时 还原产物为 。该设计克服了
导电性差和释放 能力差的障碍,同时改善了 的溶剂化环境,提高了电池充放电循环性
能。
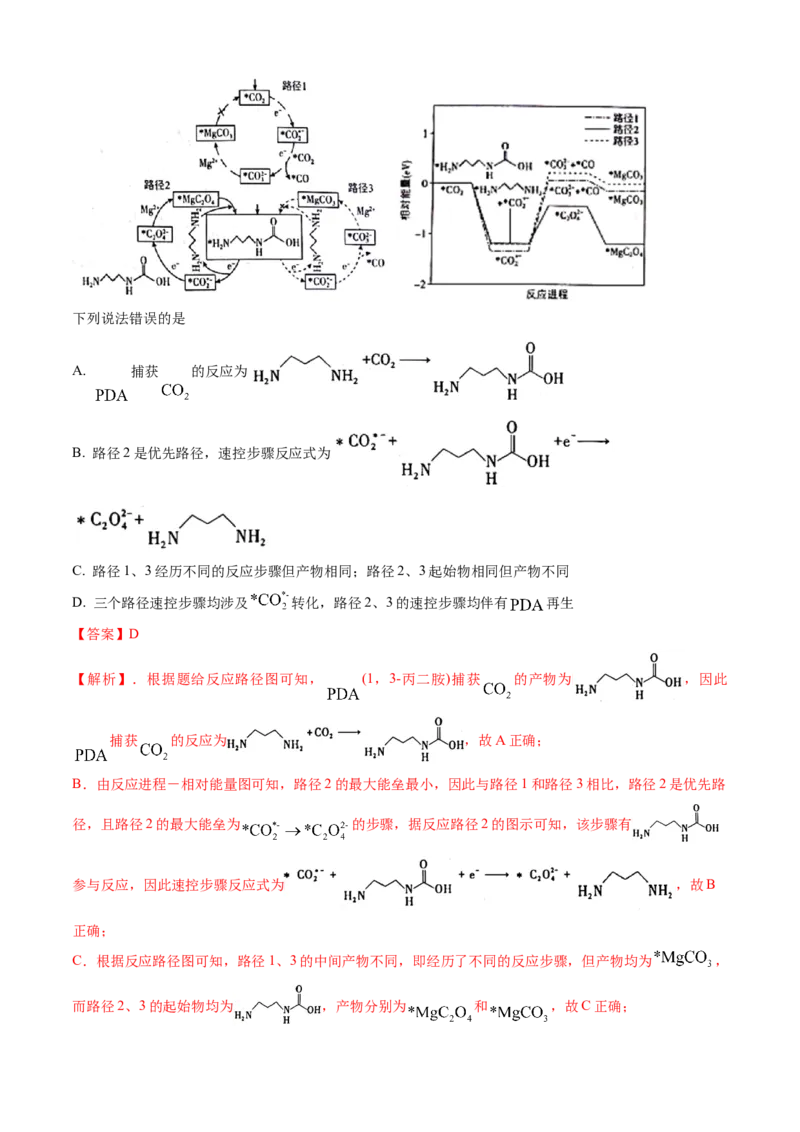
对上述电池放电时 的捕获和转化过程开展了进一步研究,电极上 转化的三种可能反应路径及相
对能量变化如图(*表示吸附态)。下列说法错误的是
A. 捕获 的反应为
B. 路径2是优先路径,速控步骤反应式为
C. 路径1、3经历不同的反应步骤但产物相同;路径2、3起始物相同但产物不同
D. 三个路径速控步骤均涉及 转化,路径2、3的速控步骤均伴有 再生
【答案】D
【解析】.根据题给反应路径图可知, (1,3-丙二胺)捕获 的产物为 ,因此
捕获 的反应为 ,故A正确;
B.由反应进程-相对能量图可知,路径2的最大能垒最小,因此与路径1和路径3相比,路径2是优先路
径,且路径2的最大能垒为 的步骤,据反应路径2的图示可知,该步骤有
参与反应,因此速控步骤反应式为 ,故B
正确;
C.根据反应路径图可知,路径1、3的中间产物不同,即经历了不同的反应步骤,但产物均为 ,
而路径2、3的起始物均为 ,产物分别为 和 ,故C正确;D.根据反应路径与相对能量的图像可知,三个路径的速控步骤中 都参与了反应,且由B项分析可
知,路径2的速控步骤伴有 再生,但路径3的速控步骤为 得电子转化为 和 ,没有
的生成,故D错误;
故答案为:D。
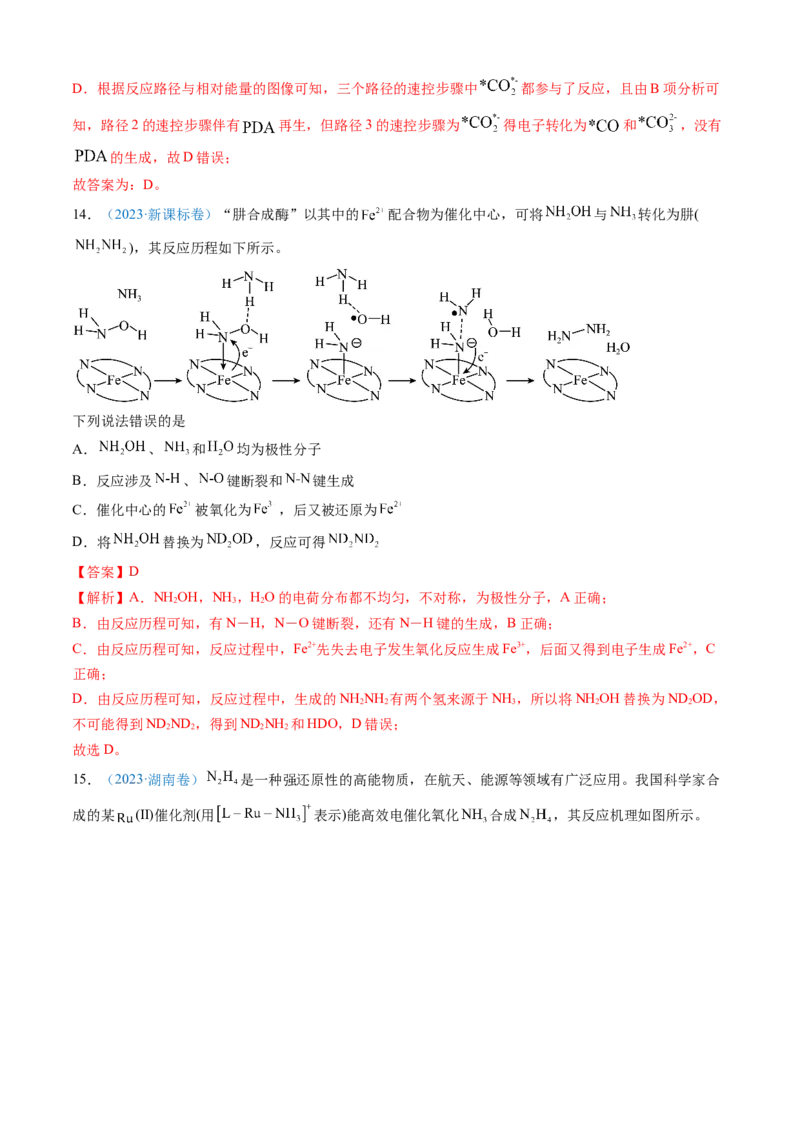
14.(2023·新课标卷)“肼合成酶”以其中的 配合物为催化中心,可将 与 转化为肼(
),其反应历程如下所示。
下列说法错误的是
A. 、 和 均为极性分子
B.反应涉及 、 键断裂和 键生成
C.催化中心的 被氧化为 ,后又被还原为
D.将 替换为 ,反应可得
【答案】D
【解析】A.NH OH,NH ,HO的电荷分布都不均匀,不对称,为极性分子,A正确;
2 3 2
B.由反应历程可知,有N-H,N-O键断裂,还有N-H键的生成,B正确;
C.由反应历程可知,反应过程中,Fe2+先失去电子发生氧化反应生成Fe3+,后面又得到电子生成Fe2+,C
正确;
D.由反应历程可知,反应过程中,生成的NH NH 有两个氢来源于NH ,所以将NH OH替换为ND OD,
2 2 3 2 2
不可能得到ND ND ,得到ND NH 和HDO,D错误;
2 2 2 2
故选D。
15.(2023·湖南卷) 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合
成的某 (Ⅱ)催化剂(用 表示)能高效电催化氧化 合成 ,其反应机理如图所示。下列说法错误的是
A. (Ⅱ)被氧化至 (Ⅲ)后,配体 失去质子能力增强
B.M中 的化合价为
C.该过程有非极性键的形成
D.该过程的总反应式:
【答案】B
【解析】A. (Ⅱ)被氧化至 (Ⅲ)后, 中的 带有更多的正电荷,其与N原子成键后,
吸引电子的能力比 (Ⅱ)强,这种作用使得配体 中的 键极性变强且更易断裂,因此其失去
质子( )的能力增强,A说法正确;
B. (Ⅱ)中 的化合价为+2,当其变为 (Ⅲ)后, 的化合价变为+3, (Ⅲ)失去2个质子后,N原
子产生了1个孤电子对, 的化合价不变;M为 ,当 变为M时,N原子
的孤电子对拆为2个电子并转移给 1个电子,其中 的化合价变为 ,因此,B说法不正确;
C.该过程M变为 时,有 键形成, 是非极性键,C说法正确;
D.从整个过程来看, 4个 失去了2个电子后生成了1个 和2个 , (Ⅱ)是催化剂,因此,
该过程的总反应式为 ,D说法正确;综上所述,本题选B。
16.(2023·浙江卷)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知 和
的相对能量为0],下列说法不正确的是A.
B.可计算 键能为
C.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
【答案】C
【分析】对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。
【解析】A.催化剂能降低活化能,但是不能改变反应的焓变,因此 ,A正确;
B.已知 的相对能量为0,对比两个历程可知, 的相对能量为 ,则 键
能为 ,B正确;
C.催化剂不能改变反应的平衡转化率,因此相同条件下, 的平衡转化率:历程Ⅱ=历程Ⅰ,C错误;
D.活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最低,所以速率最快的一步
反应的热化学方程式为: ,D正确;
故答案为:C。
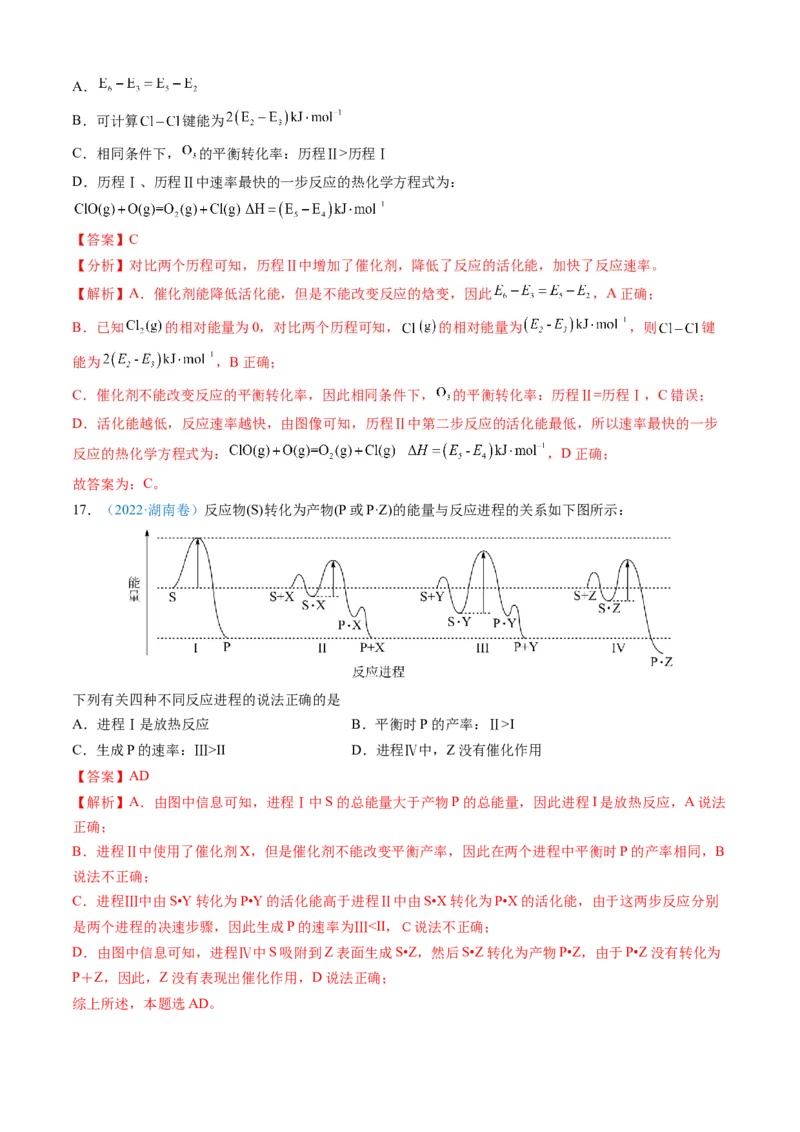
17.(2022·湖南卷)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是
A.进程Ⅰ是放热反应 B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
【答案】AD
【解析】A.由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A说法
正确;
B.进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产率相同,B
说法不正确;
C.进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X的活化能,由于这两步反应分别
是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;
D.由图中信息可知,进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为
P+Z,因此,Z没有表现出催化作用,D说法正确;
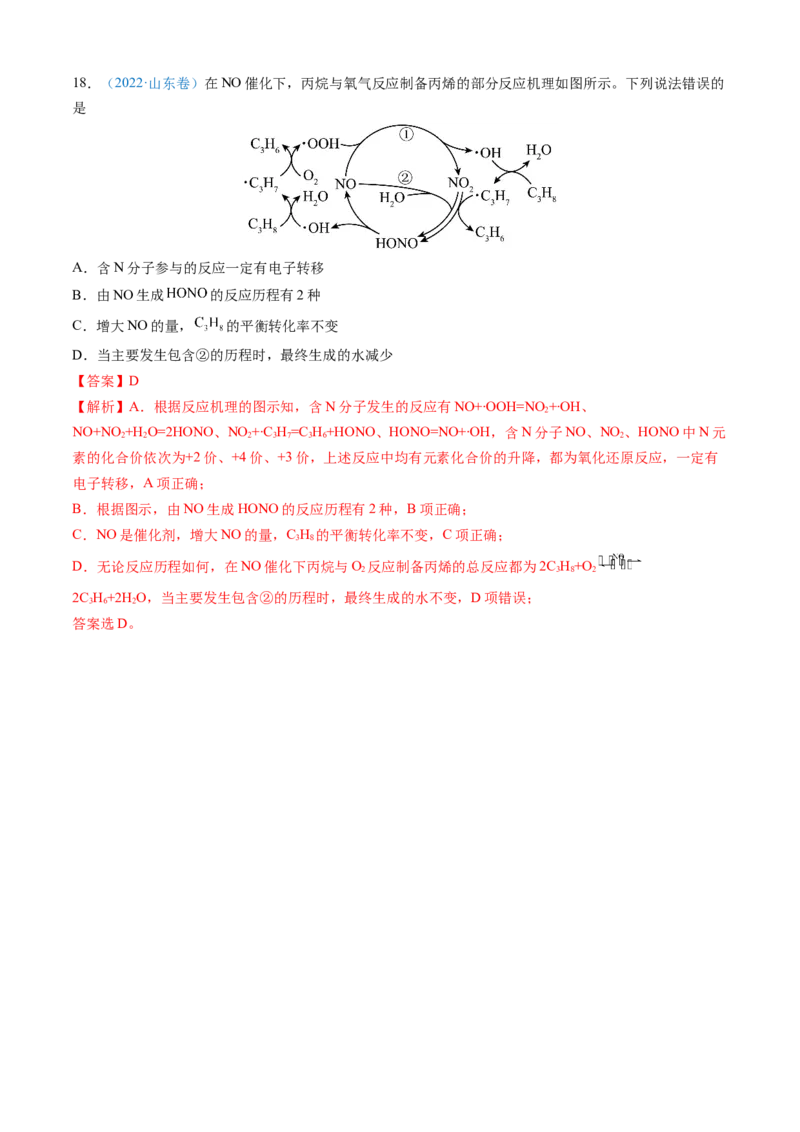
综上所述,本题选AD。18.(2022·山东卷)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的
是
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A.根据反应机理的图示知,含N分子发生的反应有NO+∙OOH=NO+∙OH、
2
NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子NO、NO 、HONO中N元
2 2 2 3 7 3 6 2
素的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,一定有
电子转移,A项正确;
B.根据图示,由NO生成HONO的反应历程有2种,B项正确;
C.NO是催化剂,增大NO的量,C H 的平衡转化率不变,C项正确;
3 8
D.无论反应历程如何,在NO催化下丙烷与O 反应制备丙烯的总反应都为2C H+O
2 3 8 2
2C H+2H O,当主要发生包含②的历程时,最终生成的水不变,D项错误;
3 6 2
答案选D。