文档内容
湖北省高中名校联盟 届高三第四次联合测评
2025
化学试卷参考答案与解析
一、选择题:本题共15小题,每小题3分,共45分。
题号
1 2 3 4 5 6 7 8
答案
C A B D D C B A
题号
9 10 11 12 13 14 15
答案
C A B C B D C
解析 绸缎和宣纸都属于有机高分子材料 均错误 泥胚的主要成分为硅酸盐 属于传统的无
1.C 【 】 ,A、B ; ,
机非金属材料 项正确 银锭头面主要成分为金属 属于金属材料 项错误
,C ; , ,D 。
解析 石油经分馏后得到柴油 汽油 煤油等轻质油和石蜡等重油 重油经催化裂化 裂解可得到
2.A 【 】 、 、 , 、
乙烯等化工原料 项错误
,A 。
解析 草木灰的主要成分为 其中只有钾元素一种植物营养元素 不属于复合肥 项错误
3.B 【 】 K2CO3, , ,B 。
解析 氨化的饱和盐水通 生成的碳酸氢钠以沉淀的形式析出 不能拆为离子 离子方程式应
4.D 【 】 CO2 , ,
为 + + 项错误
Na +H2O+NH3+CO2 NaHCO3↓+NH4,D 。
解析 所含中子数为 N 项错误 的 溶液 体积未知 无法计算 +的数
5.D 【 】0.5 mol CH4 3 A,A ;pH=2 HF , , H
目 项错误 中含有 中所含的共价键数目为 N 项错误 价层
,B ;1 mol SiC 4 mol C—Si,4 g SiC 0.4 A,C ;SiF4
电子对数为 标准状况下 价层电子对数为 N 项正确
4, ,28 L SiF4 5 A,D 。
解析 该物质含有碳碳双键 且碳碳双键两端 所连的 可以位于双键的同侧或异侧 因此存在
6.C 【 】 , C H ,
顺反异构体 项正确 该物质中的酰胺基和酚羟基可以与 反应 该物质最多可消耗
,A ; NaOH ,1 mol 2 mol
项正确 所有碳原子可能处于同一平面 项错误 该物质能被酸性 溶液氧化成苯甲
NaOH,B ; ,C ; KMnO4
酸 项正确
,D 。
解析 由题干中的信息和结构中成键特点可推断出 分别为 离子半径 2-
7.B 【 】 W、X、Y、Z H、O、S、K。 S >
+ 项错误 该物质中含有过氧键 因此受热易分解 项正确 的非金属性强 的稳定性大于
K ,A ; , ,B ;O ,H2O
项错误 的 模型为平面三角形 项错误
H2S,C ;SO2 VSEPR ,D 。
解析 氯苯与亚硫酰氯反应生成化合物 和 碱石灰的目的为防止空气中的水蒸气进入装置
8.A 【 】 Z HCl,
使亚硫酰氯水解 同时吸收生成的 若换为无水氯化钙 不能吸收 项错误
, HCl, , HCl,A 。
解析 邻氨基苯酚和对氨基苯酚常温条件均为固体 邻氨基苯酚与六元瓜环形成的超分子也为固
9.C 【 】 ,
体 因此操作 和 都为过滤 操作 将溶于甲醇中的邻氨基苯酚 减压 旋转 蒸发 项错误
, 1 2 , 3 ( / ) ,C 。
化学试卷参考答案与解析 第 页 共 页
1 ( 5 )解析 聚磷酸铵m越大 水溶性越差 项错误
10.A 【 】 , ,A 。
解析 焰色试验的原理为电子从较高能量的激发态跃迁到较低能量的激发态甚至是基态时 以
11.B 【 】 ,
光的形式释放能量 产生发射光谱 项错误
, ,B 。
解析 体心的 +周围有 个 2- 体内的每个 2-周围有 个 +和 个 3+ 因此 +和 2-的
12.C 【 】 Cu 4 S , S 2 Cu 2 Ga , Cu S
配位数都为 项错误
4,C 。
解析 -l 的 和 溶液中铵根离子的浓度不同 铵根离子会水解 因此
13.B 【 】0.1 mol·L NH4F (NH4)2CO3 , ,
不能达到实验目的 项错误 溶液中存在平衡 2- 橙色 2- 黄色 +
,A ;K2Cr2O7 Cr2O7 ( )+H2O2CrO4 ( )+2H ,
加入 溶液可以改变溶液中 +的浓度 探究浓度对化学平衡的影响 项正确 项中没有控制
NaOH H , ,B ;C
-和 -浓度相同 不能根据沉淀产生的先后顺序比较 和 的 K 大小 项错误 将 溴丁
Cl I , AgCl AgI sp ,C ; 1-
烷与 乙醇溶液共热时挥发出的乙醇也会使酸性高锰酸钾溶液褪色 应先将产生的气体通入水中
KOH ,
洗气 再通入酸性高锰酸钾溶液中 项错误
, ,D 。
解析 电极 为阴极 阴极附近电解水生成 和 - 生成的 -会通过阴离子交换膜移向电
14.D 【 】 a , H2 OH , OH
极 项正确 海水呈弱碱性 同时左室生成的 -移入右室 因此右室溶液显碱性 催化剂表面发
b,A ; , OH , ,
生反应的离子方程式为 3- - 4- 项错误
:4[Fe(CN)6] +4OH 4[Fe(CN)6] +2H2O+O2↑,D 。
解析 反应过程中 +与 2- 配位 2- 浓度越大 2- 与 +配位越多 因此曲线 代表
15.C 【 】 Ag SO3 ,SO3 ,SO3 Ag , Ⅱ
δ 5- 随c 2- 的变化 项正确 3- 2- 5-的平衡常数
([Ag(SO3)3] ) (SO3 ) ,A ;[Ag(SO3)2] +SO3 [Ag(SO3)3]
c 5-
K ([Ag(SO3)3] ) 当 c 2- -1 时 c 3-
= c 5- c 2- , ( SO3 ) = 0. 5 mol · L , ([ Ag ( SO3 )2 ] ) =
([Ag(SO3)3] )· (SO3 )
c 5- K 1 项正确 点时 c 2- -1 c -
([Ag(SO3)3] ), =c
2-
= 2,B ;a (SO3 )= 0. 01 mol·L , ([Ag(SO3)] )=
(SO3 )
-1 -1 因此 c 2- c - 项错误 当 c 2-
0.075×0.075 mol·L =0.0056 mol·L , (SO3 )> ([Ag(SO3)] ),C ; (SO3 )=
c 5- c 5-
-1 时 根据 K ([Ag(SO3)3] ) 可推出 ([Ag(SO3)3] ) 此时
1 mol·L , = c 5- c 2- = 2, c 5- = 2,
([Ag(SO3)3] )· (SO3 ) ([Ag(SO3)3] )
c - 几乎为 根据元素守恒 c 3- c 5- -1 可
([Ag(SO3)] ) 0, ([Ag(SO3)2] )+ ([Ag(SO3)3] )= 0.075 mol·L ,
推出 5-的浓度约为 -1 项正确
[Ag(SO3)3] 0.05mol·L ,D 。
二、非选择题:本题共4小题,共55分。
分 除标注外 每空 分
16.(14 )( , 2 )
定容 分
(1) (1 )
酸式滴定管 或移液管
(2) ( )
(3)18.00
2+ 或 或
(4)Mn ( MnSO4; MnBr2)
- - +
(5)2MnO4+6Br +8H 2MnO2↓+3Br2+4H2O
否 分
(6) (1 )
化学试卷参考答案与解析 第 页 共 页
2 ( 5 )两种条件下对应的化学反应不同 未能很好的做到变量的控制
, 。
或在不同的酸度条件下 还原产物不同 未能很好的做到变量的控制
( ,KMnO4 , 。)
生成的 胶体具有较强的吸附性 会吸附 - 使醋酸的电离平衡正向移动 导致溶液
(7) MnO2 , CH3COO , ,
中 溶液逐渐澄清
pH<1.21,
解析
【 】
配制 -1 溶液的操作步骤 计算 称量 溶解 移液 洗涤转移 轻轻摇动
(1) 0.01 mol·L KMnO4 : → → → → → →
定容 摇匀等
→ 。
量取 溶液所用的仪器为酸式滴定管 或移液管
(2) 10.00 mL KMnO4 ( )。
该小组探究酸度对 氧化 反应速率的影响 因此要控制其它反应物的浓度相同 实验中
(3) KMnO4 KBr , ,
取的 和 的物质的量相同 需要控制两组实验溶液体积相同 因此x
KMnO4 KBr , , =18.00。
实验 中紫色褪去 无沉淀生成 被还原为 2+
(4) ① , ,KMnO4 Mn 。
实验 中生成的棕黑色沉淀为 该过程中反应的离子方程式为 - - +
(5) ② MnO2, :2MnO4+6Br +8H
2MnO2↓+3Br2+4H2O。
两种条件下对应的化学反应不同 未能很好的做到变量的控制 不能根据实验现象比较反应的速
(6) , ,
率 因此该实验设计方案不合理
, 。
反应中生成的 胶体 会吸附 - 使醋酸的电离平衡正向移动 导致溶液中
(7) MnO2 , CH3COO , , pH<1.21,
溶液逐渐澄清
。
分 每空 分
17.(14 )( 2 )
(1)
+ +
(2)2Ag+H2O2+2H 2Ag +2H2O
(3)Si3N4+16HF3SiF4↑+4NH4F
氢氟酸会与硅单质反应 导致硅的回收率下降
,
答 氢氟酸易挥发 具有强腐蚀性 也给分
( “ , ” )
(4)CAB
硝酸氧化酸浸金属过程中会被还原为氮氧化合物 污染环境
(5) ,
增大硫酸浓度 硫酸的电离度减小 c + 减小 反应速率下降 相同时间内铝浸出率下降
(6) , , (H ) , ,
解析
【 】
的电子式为
(1)N2H4 : 。
氧化酸浸 中 和 被氧化溶解 发生反应的离子方程式为 +
(2)“ ” Ag Cu ,Ag 2Ag+H2O2+2H
+
2Ag +2H2O。
与氢氟酸反应生成气体和盐分别为 和 该反应的化学方程式为
(3)Si3N4 SiF4 NH4F, Si3N4+16HF
但过量的氢氟酸会与硅单质反应 导致硅的回收率下降
3SiF4↑+4NH4F; , 。
中含有电负性较高的 原子 使 变成吸电子基团 将整个有机物的电子云朝着 方向
(4)C F , -CF3 , -CF3
化学试卷参考答案与解析 第 页 共 页
3 ( 5 )转移 使 基团更容易电离出氢离子 故其酸性最强 和 中含有烷基 烷基为推电子基团使得
, -SO3H , ;A B ,
整个有机物的电子云朝着 方向移动 使 基团更不容易电离出氢离子 烷基越长推电子
-SO3H , -SO3H ,
效应越大 因此 上述三种物质的酸性大小为
。 , :C>A>B。
硝酸可以溶解 但硝酸氧化酸浸金属过程中会被还原为氮氧化合物 污染环境
(5) Al、Ag、Cu, , 。
硫酸的第二步电离存在电离平衡 增大硫酸浓度 硫酸的电离度减小 c + 减小 反应速率下降
(6) , , , (H ) , ,
相同时间内铝浸出率下降
。
分 除标注外 每空 分
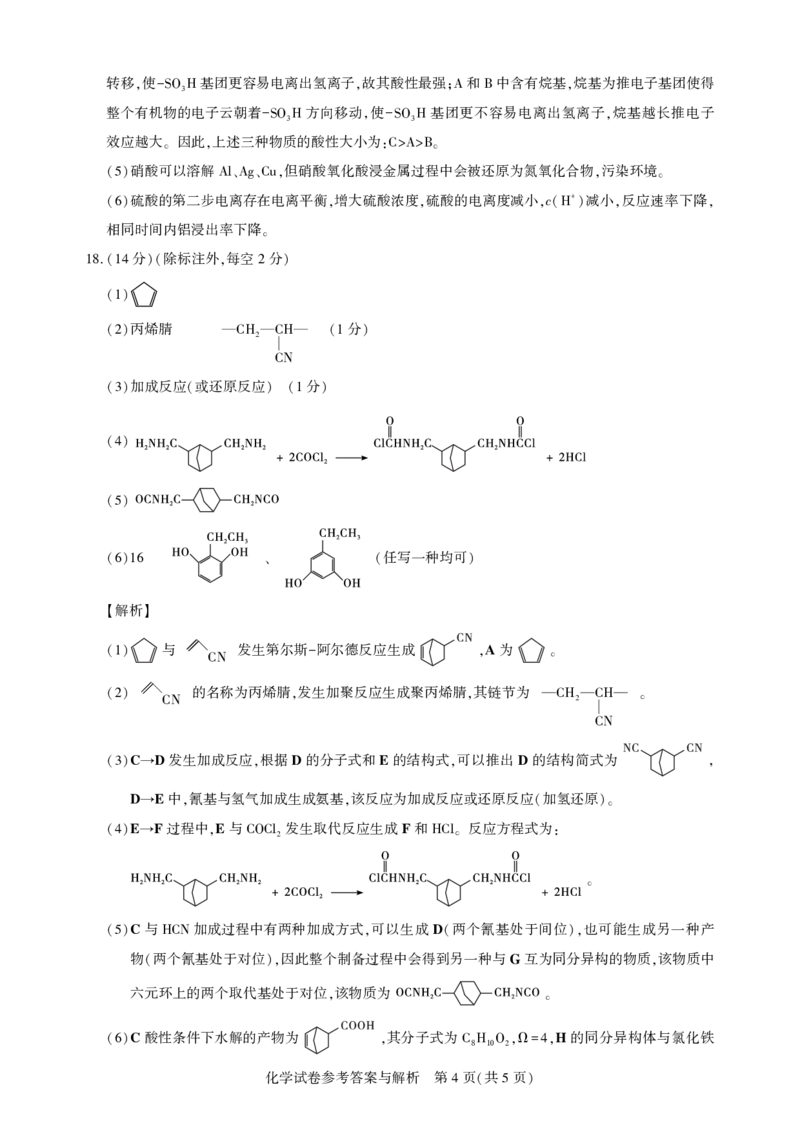
18.(14 )( , 2 )
(1)
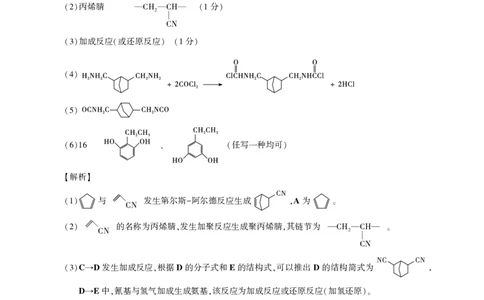
丙烯腈 分
(2) CH2 CH (1 )
CN
加成反应 或还原反应 分
(3) ( ) (1 )
(4)
(5)
任写一种均可
(6)16 、 ( )
解析
【 】
与 发生第尔斯 阿尔德反应生成 A为
(1) - , 。
CN
的名称为丙烯腈 发生加聚反应生成聚丙烯腈 其链节为
(2)
CN
, , CH2 CH 。
CN
C D发生加成反应 根据D的分子式和E的结构式 可以推出 D 的结构简式为
(3) → , , ,
D E中 氰基与氢气加成生成氨基 该反应为加成反应或还原反应 加氢还原
→ , , ( )。
E F过程中 E与 发生取代反应生成F和 反应方程式为
(4) → , COCl2 HCl。 :
。
C与 加成过程中有两种加成方式 可以生成 D 两个氰基处于间位 也可能生成另一种产
(5) HCN , ( ),
物 两个氰基处于对位 因此整个制备过程中会得到另一种与G互为同分异构的物质 该物质中
( ), ,
六元环上的两个取代基处于对位 该物质为
, 。
C酸性条件下水解的产物为 其分子式为 H 的同分异构体与氯化铁
(6) , C8H10O2,Ω=4,
化学试卷参考答案与解析 第 页 共 页
4 ( 5 )溶液显色 说明含酚羟基 除去苯环 还含有 个碳和 个羟基 其同分异构体分两大类情况 第一
, , , 2 1 , ,
类为苯环上的 个取代基分别为 个酚羟基和 个 这一类共有 种 第二类为苯环上
3 2 1 -CH2CH3, 6 ;
的 个取代基为 个酚羟基 个 和 个 这一类有 种 共 种 其中核磁共振
3 1 、1 -CH3 1 -CH2OH, 10 , 16 。
氢谱有 组峰 且峰面积之比为 的结构简式为
5 , 3 ∶ 2 ∶ 2 ∶ 2 ∶ 1 、 。
分 除标注外 每空 分
19.(13 )( , 2 )
分
(1)B (1 )
(2)-480
(3)①M
p2
②
12
反应 和 都为吸热反应 温度升高 平衡均正向移动 但温度升高对反应 的影响更大 导致
③ Ⅰ Ⅱ , , , Ⅰ ,
的物质的量分数降低
CO2
和 和 对 具有较强的吸附性
(4)La Ce La Ce H2 。
解析
【 】
燃料反应器中太阳能转化为化学能 在空气反应器中 该反应为放热反应 化学能转化为热能 利
(1) , , , ,
用热能发电过程中热能中蒸汽推动蒸汽轮机 将热能转化为机械能 因此该过程中没有化学能直
, ,
接转化为电能的过程
。
的燃烧热为 则反应 H 式
(2)CO 283 kJ/mol, Ⅳ:2CO(g)+O2(g)2CO2(g) Δ =-566 kJ/mol,Ⅲ =
式 式 式 H H H H
(Ⅰ -Ⅱ )×2+Ⅳ ,Δ 3=(Δ 1-Δ 2)×2+Δ =-480 kJ/mol。
合成甲醇反应方程式n n n n 根据图中 和 物
(3)① (CO) ∶ (H2)= 1 ∶ 2、 (CO2) ∶ (H2)= 1 ∶ 3, CO CO2
质的量分数 可以计算出理论所需 物质的量分数 如 时 和 的物质的量分数分别
, H2 , 500℃ ,CO CO2
约为 和 则理论所需 物质的量分数为 约为 则 为理论所需 物质的
0 0.1, H2 :0×2+0.1×3 0.3, M H2
量分数 达到平衡时 体系中只有 四种气体 物质的量分数为
。 ②600℃ , CH4、CO2、H2、CO ,CH4 1-
c c2
2 2
则反应 的平衡常数 K (CO)· (H2) 0.1 p·(0.5p) p 反应
0.1-0.1-0.5=0.3, Ⅰ p= c = = 。 ③ Ⅰ
(CH4) (0.3p) 12
和 都为吸热反应 温度升高 平衡均正向移动 但温度升高对反应 的影响更大 导致 的物
Ⅱ , , , Ⅰ , CO2
质的量分数降低
。
从表中的数据可以看出 使用 % 和 % 两种催化剂 转化率和 产率
(4) , CZA-3 La CZA-3 Ce ,H2 CH3OH
均大于 催化剂 因此有利于提高该催化剂催化活性的稀土元素有 和 其可以提高该催
CZA , La Ce;
化剂活性的原因可能为 和 对 具有较强的吸附性
La Ce H2 。
化学试卷参考答案与解析 第 页 共 页
5 ( 5 )