文档内容
专题32 晶体结构与性质
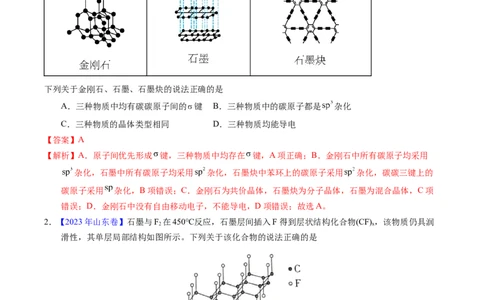
1.【2023年北京卷】中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是
A.三种物质中均有碳碳原子间的 键 B.三种物质中的碳原子都是 杂化
C.三种物质的晶体类型相同 D.三种物质均能导电
【答案】A
【解析】A.原子间优先形成 键,三种物质中均存在 键,A项正确;B.金刚石中所有碳原子均采用
杂化,石墨中所有碳原子均采用 杂化,石墨炔中苯环上的碳原子采用 杂化,碳碳三键上的
碳原子采用 杂化,B项错误;C.金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体,C项
错误;D.金刚石中没有自由移动电子,不能导电,D项错误;故选A。
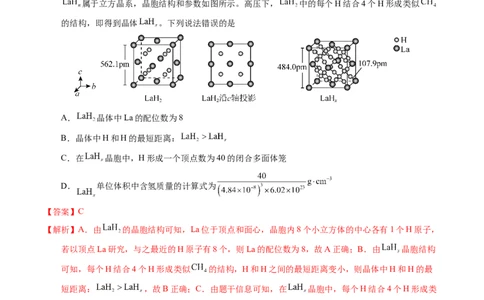
2.【2023年山东卷】石墨与F 在450℃反应,石墨层间插入F得到层状结构化合物(CF) ,该物质仍具润
2 x
滑性,其单层局部结构如图所示。下列关于该化合物的说法正确的是
A.与石墨相比,(CF) 导电性增强
x
B.与石墨相比,(CF) 抗氧化性增强
x
C.(CF) 中 的键长比 短
x
D.1mol(CF) 中含有2xmol共价单键
x
【答案】B【解析】A.石墨晶体中每个碳原子上未参与杂化的1个2p轨道上电子在层内离域运动,故石墨晶体能导
电,而(CF) 中没有未参与杂化的2p轨道上的电子,故与石墨相比,(CF) 导电性减弱,A错误;B.
x x
(CF) 中C原子的所有价键均参与成键,未有未参与成键的孤电子或者不饱和键,故与石墨相比,
x
(CF) 抗氧化性增强,B正确;C.已知C的原子半径比F的大,故可知(CF) 中 的键长比 长,
x x
C错误;D.由题干结构示意图可知,在(CF) 中C与周围的3个碳原子形成共价键,每个C-C键被2
x
个碳原子共用,和1个F原子形成共价键,即1mol(CF) 中含有2.5xmol共价单键,D错误;故答案为:
x
B。
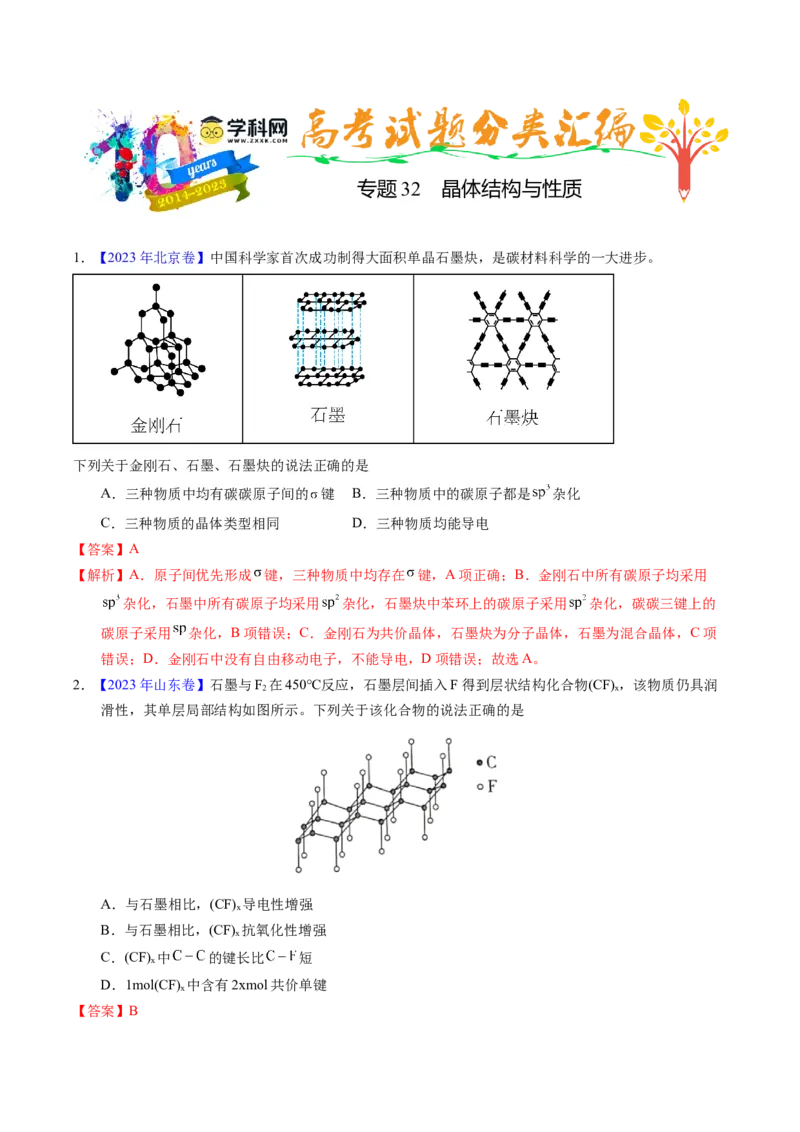
3.【2023年湖北卷】镧La和H可以形成一系列晶体材料 ,在储氢和超导等领域具有重要应用。
属于立方晶系,晶胞结构和参数如图所示。高压下, 中的每个H结合4个H形成类似
的结构,即得到晶体 。下列说法错误的是
A. 晶体中La的配位数为8
B.晶体中H和H的最短距离:
C.在 晶胞中,H形成一个顶点数为40的闭合多面体笼
D. 单位体积中含氢质量的计算式为
【答案】C
【解析】A.由 的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中心各有1个H原子,
若以顶点La研究,与之最近的H原子有8个,则La的配位数为8,故A正确;B.由 晶胞结构
可知,每个H结合4个H形成类似 的结构,H和H之间的最短距离变小,则晶体中H和H的最
短距离: ,故B正确;C.由题干信息可知,在 晶胞中,每个H结合4个H形成类
似 的结构,这样的结构有8个,顶点数为4 8=32,且不是闭合的结构,故C错误;D.1个
晶胞中含有5 8=40个H原子,含H质量为 g,晶胞的体积为(484.0 10-10cm)3=(4.84 10-
8)3cm3,则 单位体积中含氢质量的计算式为 ,故D正确;答案选
C。
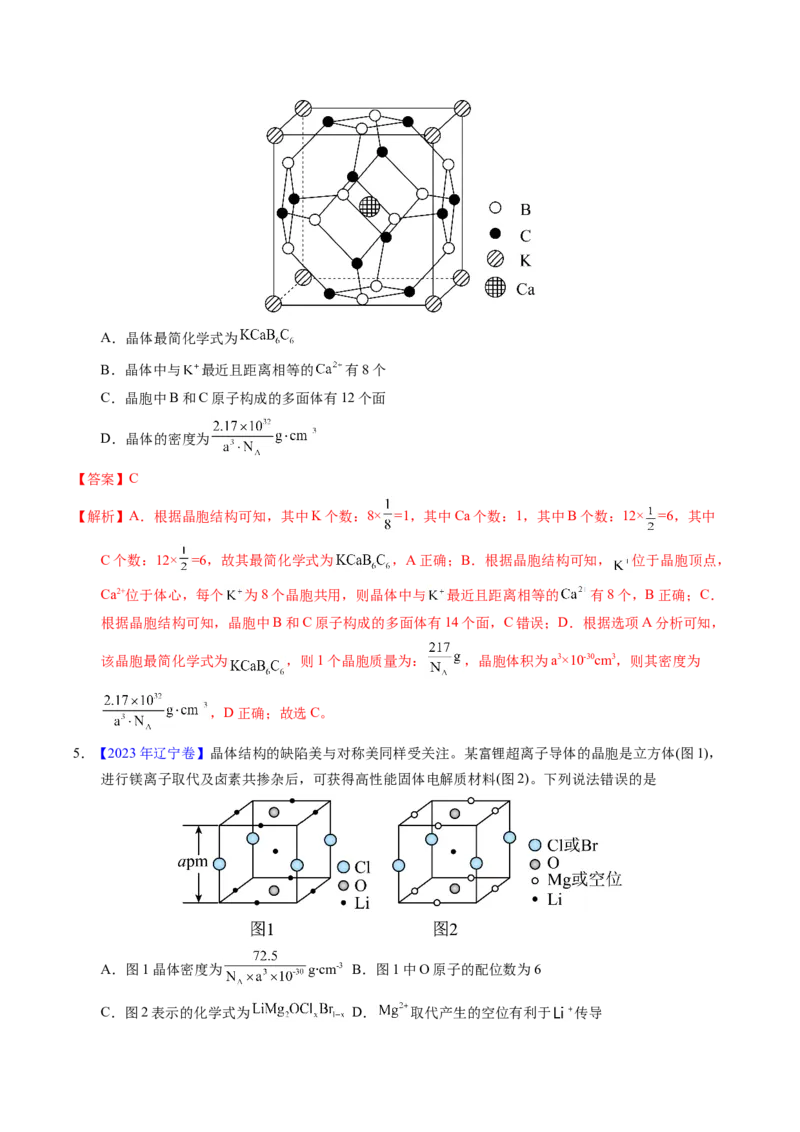
4.【2023年湖北卷】科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为 。
阿伏加德罗常数的值为 。下列说法错误的是A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有8个
C.晶胞中B和C原子构成的多面体有12个面
D.晶体的密度为
【答案】C
【解析】A.根据晶胞结构可知,其中K个数:8× =1,其中Ca个数:1,其中B个数:12× =6,其中
C个数:12× =6,故其最简化学式为 ,A正确;B.根据晶胞结构可知, 位于晶胞顶点,
Ca2+位于体心,每个 为8个晶胞共用,则晶体中与 最近且距离相等的 有8个,B正确;C.
根据晶胞结构可知,晶胞中B和C原子构成的多面体有14个面,C错误;D.根据选项A分析可知,
该晶胞最简化学式为 ,则1个晶胞质量为: ,晶胞体积为a3×10-30cm3,则其密度为
,D正确;故选C。
5.【2023年辽宁卷】晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),
进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
A.图1晶体密度为 gcm-3 B.图1中O原子的配位数为6
∙
C.图2表示的化学式为 D. 取代产生的空位有利于 传导【答案】C
【解析】A.根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的质量为
g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密度为 g÷(a3×10-
30cm3)= g/cm3,A项正确;B.图1晶胞中,O位于面心,与O等距离最近的Li有6个,
O原子的配位数为6,B项正确;C.根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,
Cl或Br:4× =1,Mg的个数小于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br
x 1-
,C项错误;D.进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代产
x
生的空位有利于Li+的传导,D项正确;答案选C。
6.【2023年广东卷】化学处处呈现美。下列说法正确的是
A.舞台上干冰升华时,共价键断裂
B.饱和 溶液可析出无水蓝色晶体
C.苯分子的正六边形结构,单双键交替呈现完美对称
D.晨雾中的光束如梦如幻,是丁达尔效应带来的美景
【答案】D
【解析】A.舞台上干冰升华物理变化,共价键没有断裂,A错误;B.饱和 溶液可析出的蓝色晶
体中存在结晶水为五水硫酸铜,B错误;C.苯分子的正六边形结构,六个碳碳键完全相同呈现完美
对称,C错误;D.晨雾中由于光照射胶体粒子散射形成的光束如梦如幻,是丁达尔效应带来的美景,
D正确;故选D。
7.(2021·辽宁真题)单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下列说法错误
的是
A.S位于元素周期表p区 B.该物质的化学式为
C.S位于H构成的八面体空隙中 D.该晶体属于分子晶体
【答案】D
【解析】A.S的价电子排布式为:3s23p4,故S位于元素周期表p区,A正确;B.由该物质形成晶体的晶
胞可知:S个数为 ,H个数为: ,故H、S原子个数比为3:1,故该物质的化学式为 ,B正确;C.S位于H构成的八面体空隙中,如图所示 ,C正确;D.
由于该晶体是一种新型超导材料,说明其是由阴、阳离子构成的,故该晶体属于离子晶体,D错误;
故答案为:D。
8.(2021·天津真题)下列各组物质的晶体类型相同的是
A.SiO 和SO B.I 和NaCl C.Cu和Ag D.SiC和MgO
2 3 2
【答案】C
【解析】A.SiO 为原子晶体,SO 为分子晶体,晶体类型不同,故A错误;B.I 为分子晶体,NaCl为离
2 3 2
子晶体,晶体类型不同,故B错误;C.Cu和Ag都为金属晶体,晶体类型相同,故C正确;D.SiC
为原子晶体,MgO为离子晶体,晶体类型不同,故D错误;故选C。
9.【2022年上海卷】下列属于原子晶体的是
A. B.金刚石 C.NaCl D.氦气
【答案】B
【解析】A. 由分子构成,熔点低, 是分子晶体,故不选A;B.金刚石由碳原子直接构成,熔点
高、硬度大,属于原子晶体,故选B;C.NaCl有Na+、Cl-构成,属于离子晶体,故不选C;D.氦气
由分子构成,熔点低,属于分子晶体,故不选D;选B。
10.(2021·湖北真题)某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶
胞结构图,图b表示晶胞的一部分。下列说法正确的是
A.该晶胞的体积为a3×10-36cm-3 B.K和Sb原子数之比为3∶1
C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 apm
【答案】B
【解析】A.该晶胞的边长为 ,故晶胞的体积为 ,A项错误;B.该
晶胞中K的个数为 ,Sb的个数为 ,故K和Sb原子数之比为3∶1,B项
正确;C.以面心处Sb为研究对象,与Sb最邻近的K原子数为8,C项错误;D.K和Sb的最短距离为晶胞体对角线长度的 ,即 ,D项错误。故选B。
11.【2021年江苏卷】通过下列实验可从I,的CCl 溶液中回收I。
2 4 2
下列说法正确的是
A.NaOH溶液与I 反应的离子方程式:I+2OH-=I-+IO +H O
2 2 2
B.通过过滤可将水溶液与CCl 分离
4
C.向加酸后的上层清液中滴加AgNO 溶液生成AgI沉淀,1个AgI晶胞(如图)中含14个I-
3
D.回收的粗碘可通过升华进行纯化
【答案】D
【解析】A.选项所给离子方程式元素不守恒,正确离子方程式为:3I+6OH-=5I-+IO +3H O,A错误;
2 2
B.水溶液与CCl 不互溶,二者应分液分离,B错误;C.根据均摊法,该晶胞中所含I-的个数为
4
=4,C错误;D.碘易升华,回收的粗碘可通过升华进行纯化,D正确;综上所述答案为
D。
12.【2022年山东卷】 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
键、 键。下列说法错误的是
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取 杂化 D.晶体中所有原子的配位数均相同
【答案】A
【解析】Al和Ga均为第ⅢA元素,N属于第ⅤA元素,AlN、GaN的成键结构与金刚石相似,则其为共
价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。AlN、GaN晶体中,N原子
与其相邻的原子形成3个普通共价键和1个配位键。A.因为AlN、GaN为结构相似的共价晶体,由
于Al原子的半径小于Ga,N—Al的键长小于N—Ga的,则N—Al的键能较大,键能越大则其对应的
共价晶体的熔点越高,故GaN的熔点低于AlN,A说错误;B.不同种元素的原子之间形成的共价键为极性键,故两种晶体中所有化学键均为极性键,B说法正确;C.金刚石中每个C原子形成4个共
价键(即C原子的价层电子对数为4),C原子无孤电子对,故C原子均采取sp3杂化;由于AlN、
GaN与金刚石互为等电子体,则其晶体中所有原子均采取sp3杂化,C说法正确;D.金刚石中每个C
原子与其周围4个C原子形成共价键,即C原子的配位数是4,由于AlN、GaN与金刚石互为等电子
体,则其晶体中所有原子的配位数也均为4,D说法正确。综上所述,本题选A。
13.【2022年山东卷】 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组
成变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是
A.每个 晶胞中 个数为x
B.每个 晶胞完全转化为 晶胞,转移电子数为8
C.每个 晶胞中0价Cu原子个数为
D.当 转化为 时,每转移 电子,产生 原子
【答案】BD
【解析】A.由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,位于体内的铜离子和亚铜
离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化合价代数
和为0可得2a+b=4×2,解得a=4x,故A错误;B.由题意可知,NaSe转化为Cu Se的电极反应式为
2 2-x
NaSe-2e-+(2-x)Cu=Cu Se+2Na+,由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,
2 2-x
则每个晶胞中含有4个NaSe,转移电子数为8,故B正确;C.由题意可知,Cu Se转化为NaCuSe
2 2-x
的电极反应式为Cu Se+ e-+Na+=NaCuSe+(1-x)Cu,由晶胞结构可知,位于顶点和面心的硒离子个数为
2-x
8× +6× =4,则每个晶胞中含有4个NaCuSe,晶胞中0价铜而个数为(4-4x),故C错误;D.由题意
可知,NaCu Se转化为NaCuSe的电极反应式为NaCu Se+(1-y) e-+ Na+=NaCuSe+(1-x)Cu,所以每转
y 2-x y 2-x
移(1-y)电子,产生(1-x)mol铜,故D正确;故选BD。
14.【2022年湖北卷】 在高温高压下可转变为具有一定导电性、高硬度的非晶态碳玻璃。下列关于该
碳玻璃的说法错误的是
A.具有自范性 B.与 互为同素异形体C.含有 杂化的碳原子 D.化学性质与金刚石有差异
【答案】A
【解析】A.自范性是晶体的性质,碳玻璃为非晶态,所以没有自范性,A错误;B.碳玻璃和 均是由
碳元素形成的不同的单质,所以是同素异形体,B正确;C.碳玻璃具有高硬度,与物理性质金刚石
类似,因而结构具有一定的相似性,所以含有 杂化的碳原子形成化学键,C正确;D.金刚石与碳
玻璃属于同素异形体,性质差异主要表现在物理性质上,化学性质上也有着活性的差异,D正确;故
选A。
15.【2022年湖北卷】某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误的是
A. 的配位数为6 B.与 距离最近的是
C.该物质的化学式为 D.若 换为 ,则晶胞棱长将改变
【答案】B
【解析】A. 配位数为与其距离最近且等距离的F-的个数,如图所示, 位于体心,F-位于面心,
所以 配位数为6,A正确;B. 与 的最近距离为棱长的 , 与 的最近距离为棱长的
,所以与 距离最近的是 ,B错误;C. 位于顶点,所以 个数= =1,F-位于面心,F-
个数= =3, 位于体心,所以 个数=1,综上,该物质的化学式为 ,C正确;D.
与 半径不同,替换后晶胞棱长将改变,D正确;故选B。
16.(2021.1·浙江真题)铝硅酸盐型分子筛中有许多笼状空穴和通道(如图),其骨架的基本结构单元是硅
氧四面体和铝氧四面体,化学组成可表示为M[(AlO )·(SiO)]·zHO(M代表金属离子)。
a 2 x 2 y 2
下列推测不正确的是
A.常采用水玻璃、偏铝酸钠在强酸溶液中反应后结晶制得分子筛B.若a=x/2,则M为二价阳离子
C.调节y/x(硅铝比)的值,可以改变分子筛骨架的热稳定性
D.分子筛中的笼状空穴和通道,可用于筛分分子
【答案】A
【解析】A.偏铝酸钠在强酸性溶液中不能稳定存在容易形成Al3+,不可以利用偏铝酸钠在强酸性溶液中
制备分子筛,A错误;B.设M的化合价为m,则根据正负化合价代数和为0计算,m× +x×(-1)=0,
解得m=+2,B正确;C.调节硅铝比可以改变分子筛的空间结构,从而改变分子筛的稳定性,C正确;
D.调节硅铝比可以调节分子筛的孔径,根据分子筛孔径的大小可以筛分不同大小的分子,D正确;
故答案选A。
17.(2014·上海高考真题)BeCl 熔点较低,易升华,溶于醇和醚,其化学性质与AlCl 相似。由此可推测
2 3
BeCl
2
A.熔融态不导电 B.水溶液呈中性
C.熔点比BeBr 高 D.不与氢氧化钠溶液反应
2
【答案】A
【解析】A.BeCl 熔点较低,易升华,溶于醇和醚,说明该化合物形成的晶体是分子晶体,熔融态不导电,
2
A正确;B.该化合物的化学性质与AlCl 相似,而氯化铝溶液显酸性,因此其水溶液也呈酸性,B不
3
正确;C.BeCl 与BeBr 形成的晶体均是分子晶体,后者的相对分子质量大,熔点高于BeCl ,C不正
2 2 2
确;D.氯化铝能与氢氧化钠溶液反应生成偏铝酸钠和水,则该化合物也与氢氧化钠溶液反应,D不
正确;答案选A。
18.(2018·上海高考真题)下列过程中,仅克服分子间作用力的是( )
A.氯化钾熔融 B.碳酸钠溶于水 C.碘升华 D.晶体硅熔融
【答案】C
【解析】A.KCl是离子化合物,KCl熔融时需要克服离子键的作用,A选项不满足题意;B.碳酸钠是离
子化合物,碳酸钠溶于水时需要克服离子键的作用,B选项不满足题意;C.碘单质属于分子晶体,
碘单质升华是物理变化,碘升华仅克服分子间的作用力,C选项满足题意;D.晶体硅属于原子晶体,
晶体硅熔融破坏的是共价键,D选项不满足题意;答案选C。
19.(2008·四川高考真题)下列说法中正确的是( )
A.离子晶体中每个离子的周围均吸引着6个带相反电荷的离子
B.金属导电的原因是在外加电场的作用下金属产生自由电子,电子定向运动
C.分子晶体的熔沸点低,常温下均呈液态或气态
D.原子晶体中的各相邻原子都以共价键相结合
【答案】D
【解析】A、离子所带电荷数和离子半径的大小不同,每个离子周围均吸引带相反电荷的离子数目不同,
一个NaCl晶胞为立方体,Na+离子在立方体中心的话,离它最近的Cl-离子在立方体六个面的中央,
CsCl的晶胞也是立方体,Cs+离子在立方体中心的话,离它最近的Cl-离子就在立方体的八个顶点上,
错误;B、金属里本来就存在有自由电子,在金属未通电的情况下,金属中的电子是在做热运动,即无规则运动,在外加电场的作用下自由电子做定向移动,而不是产生了自由电子,错误;C、分子晶
体存在常温下呈固态的物质,例如S、白磷、红磷、C 等都属于分子晶体,在常温下为固态,错误;
60
D、原子晶体中原子间作用力为共价键,所以D选项是正确的。答案选D。
20.(2012·上海高考真题)氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是(
)
A.AlON和石英的化学键类型相同
B.AlON和石英晶体类型相同
C.AlON和Al O 的化学键类型不同
2 3
D.AlON和Al O 晶体类型相同
2 3
【答案】D
【解析】原子晶体中相邻的原子间形成共价键。常见的原子晶体有金刚石、二氧化硅(石英)晶体等。是
离子晶体,Al O 结构粒子为阴、阳离子,离子间作用力为离子键。所以D的描述是错误的。
2 3
21.(2008·海南高考真题)已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则下面
表示该化合物的化学式正确的( )
A.ZXY B.ZXY C.ZXY D.ZXY
3 2 6 4 8 8 12
【答案】A
【解析】本题主要考查了晶体结构的计算及其应用,较易。根据晶体结构的计算方法可知,一个晶胞中含
1个Z原子,X原子数为 1,Y原子数为 3。所以化学式为ZXY ,综上所述,本题正
3
确答案为A。
22.(2007·江苏高考真题)下列说法正确的是
A.原子晶体中只存在非极性共价键
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属元素和非金属元素形成的化合物一定是离子化合物
【答案】B
【解析】A.原子晶体也可能含有极性键,例如二氧化硅中的Si-O键,A不正确;B.稀有气体形成的晶
体属于分子晶体,B正确;C.干冰升华是物理变化,破坏的是分子间作用力,化学键不变,C不正确;
D.金属元素和非金属元素形成的化合物不一定是离子化合物,也可能是共价化合物,例如氯化铝是
共价化合物,D不正确;答案选B。