文档内容
试卷类型:A
2025-2026 学年度第一学期高三年级期中教学质量检测试卷
化学
注意事项:
1.考生答卷前,务必将自己的姓名、座位号写在答题卡上。将条形码粘贴在规定区域。本试
卷满分100分,考试时间75分钟。
2.做选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡的规定区域内,写在本试卷上无效。
4.考试结束后,将答题卡交回。
可能用到的相对原子质量:B-11 C-12 N-14 O-16 S-32 Fe-56 Ag-108
一、选择题:(本题共 15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项符合题目要求)。
1. 下列有关物质性质与用途对应关系错误的是
A. 单晶硅熔点高,可用于制造芯片 B. 金属铝具有还原性,可用于冶炼金属
C. 浓硫酸具有吸水性,可用作干燥剂 D. 乙炔燃烧火焰温度高,可用于切割金属
【答案】A
【解析】
【详解】A.单晶硅用于制造芯片主要因其半导体性质,而非熔点高,熔点高与用途无直接关联,A错误;
B.金属铝还原性强,可通过铝热反应冶炼金属(如Fe、Mn等),B正确;
C.浓硫酸吸水性使其可干燥中性/酸性气体(如H、CO),C正确;
2 2
D.乙炔燃烧产生高温氧炔焰(约3000℃),可熔化金属进行切割,D正确;
故选A。
2. 下列图示中,实验操作或方法符合规范的是
A.溶解氯化钠固体 B.量取20.00mL草酸溶液
第1页/共22页
学科网(北京)股份有限公司C.收集二氧化碳气体 D.观察钠与水的反应
.
A A B. B C. C D. D
【答案】B
【解析】
【详解】A.溶解氯化钠固体应在烧杯中进行,用玻璃棒搅拌,不能在试管中溶解,A错误;
B.量取20.00 mL草酸溶液需用酸式滴定管,B正确;
C.二氧化碳密度比空气大,应用向上排空气法收集,导管需伸入集气瓶底部且还需要一个短管出气,该
装置无出气导管,C错误;公众号:高中试卷君
D.观察钠与水反应时,不能将脸凑近烧杯口,应保持安全距离,防止液体飞溅伤人,D错误;
故选B。
3. 下列化学科普实验所涉及物质的性质或应用描述正确的是
选项 科普试验 性质或应用
A 焰色试验 Na和K的焰色均为紫色
B 漂白实验 和 均可使品红溶液永久褪色
C 蛋清变性 醋酸铅溶液和甲醛溶液均可使蛋白质变性
D 铜板刻蚀 氯化铁溶液和浓硫酸均可在常温下刻蚀铜板
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.钠的焰色反应为黄色,钾需透过蓝色钴玻璃观察呈紫色,现象描述错误,A错误;
B. 的漂白是暂时性, 需生成HClO才有漂白性且为永久性,但 本身不直接漂白,B错误;
C.醋酸铅(重金属盐)和甲醛均能使蛋白质不可逆变性,性质与现象正确,C正确;
D.铜在常温浓硫酸中表现出惰性,加热才能反应,故浓硫酸无法腐蚀铜电路板,而 溶液可以,D
第2页/共22页
学科网(北京)股份有限公司错误;
故选C。
4. 下列化学用语或图示表达正确的是
A. 的电子式: B. 的VSEPR模型:
C. 的球棍模型为 D. 反-2-丁烯的结构简式为
【答案】B
【解析】
【详解】A. 的电子式中,每个氧原子应含有两对孤对电子,正确电子式为 ,A错误;
B. 中心B原子价层电子对数=3(成键电子对)+0(孤对电子)=3,VSEPR模型为平面三角形,B正
确;
C. (乙炔)的球棍模型需用“棍”表示化学键,“球”表示原子,图片3仅显示四个球相连,未体现化
学键(棍),为空间填充模型而非球棍模型,C错误;
D.反-2-丁烯中两个甲基应在双键两侧,图片4中两个甲基在双键同侧,为顺-2-丁烯结构简式,D错误;
故答案选B。
5. 加热时,浓硫酸与木炭发生反应: (浓) 。设 为阿伏加德罗
常数的值。下列说法正确的是
A. 含质子数为
B. 常温常压下, 含σ键数目为
C. 的稀硫酸中含 数目为
D. 与 充分反应得到 的分子数为
【答案】A
【解析】
【详解】A.12g的12C的物质的量为1mol,每个12C原子含有6个质子,因此总质子数为6N ,A正确;
A
B.常温常压下,6.72L CO 的物质的量小于0.3mol,每个CO 分子含2个σ键,总σ键数小于0.6N ,B错
2 2 A
第3页/共22页
学科网(北京)股份有限公司误;
C.pH=1的稀硫酸中, 浓度为0.1mol/L,1L溶液中 数目为0.1N ,而非0.2N ,C错误;
A A
D.SO 与O 生成SO 的反应为可逆反应,无法完全转化,实际生成的SO 分子数小于N ,D错误;
2 2 3 3 A
故选A。
6. 下列方程式与所给事实不相符的是
A. 海水提溴过程中,用氯气氧化苦卤得到溴单质:
B. 用绿矾( )将酸性工业废水中的 转化为
C. 用 溶液能有效除去误食的
D. 用 溶液将水垢中的 转化为溶于酸的 :
【答案】D
【解析】
【详解】A.氯气氧化苦卤得到溴单质,发生置换反应,离子方程式正确,A正确;
B. 可以将 氧化成 ,离子方程式正确,B正确;
C. 结合 生成 沉淀,可以阻止 被人体吸收,离子方程式正确,C正确;
D. 与 反应属于沉淀的转化, 不能拆分,正确的离子方程式为CaSO+
4
=CaCO + ,D错误;
3
本题选D。
7. 下列实验产生的废液中,可能大量存在的粒子组是
选
实验 粒子组
项
A 稀硝酸与铜片制
B 硫酸与 制
第4页/共22页
学科网(北京)股份有限公司C 浓盐酸与 制
D 双氧水与 溶液制
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.稀硝酸与铜反应生成 和NO,NO难溶于水,无法大量存在,A不符合题意;
B.70%硫酸与NaSO 反应生成SO ,溶液中应含 ,但 在强酸性条件下会转化为
2 3 2
SO 和HO,无法大量存在,B不符合题意;
2 2
C.浓盐酸与KMnO 反应生成Cl ,产物为 、 、 和 ,这些离子在酸性环境中稳定共存,无
4 2
后续反应干扰,C符合题意;
D.FeCl 催化HO 分解生成O,溶液中应含Fe3+而非Fe2+,D不符合题意;
3 2 2 2
故选C。
8. 丁香挥发油中含丁香色原酮(K)、香草酸(M),其结构简式如下:
下列说法正确的是
A. K中含手性碳原子 B. M中碳原子都是 杂化
C. K、M均能与 反应 D. K、M共有四种含氧官能团
【答案】D
【解析】
【详解】A.由图知,K中环上碳原子均为sp2杂化,饱和碳原子均为甲基碳原子,所以不含手性碳原子,
A错误;
B.M中环上碳原子和羧基上的碳原子均为sp2杂化,甲基碳原子为 杂化,B错误;
第5页/共22页
学科网(北京)股份有限公司C.由于酸性:羧酸>碳酸>苯酚> ,所以K中的酚羟基不能与 溶液反应,K中不含能与
溶液反应的官能团,M中羧基可与 溶液反应,C错误;
D.K、M 中共有羟基、醚键、羰基、羧基四种含氧官能团,D正确;
故选D。
9. 依据下列事实进行的推测正确的是
选
事实 推测
项
A 固体与浓硫酸反应可制备 气体 NaI固体与浓硫酸反应可制备HI气体
B 电解熔融的氯化钠可得到钠 电解熔融的氯化铝可得到铝
C 盐酸和 溶液反应是吸热反应 盐酸和 溶液反应是吸热反应
D 的沸点高于 的沸点高于
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.浓硫酸具有强氧化性,与NaI反应时会将碘离子氧化为I,无法制得HI气体,A错误;
2
B.AlCl 为共价化合物,熔融态不导电,工业上电解Al O 制铝,B错误;
3 2 3
C.HCl与NaOH的中和反应是典型的放热反应,与NaHCO 反应的吸热性无关,C错误;
3
D.HO分子间存在氢键,使水的沸点高于HS,HF分子间存在氢键,使其沸点高于HCl,D正确;
2 2
故选D。
10. 下列实验操作、现象和结论相对应的是
实验操作、现象 结论
A 用蓝色石蕊试纸检验某无色溶液,试纸变红 该溶液是酸溶液
B 用酒精灯灼烧织物产生类似烧焦羽毛的气味 该织物含蛋白质
C 乙醇和浓硫酸加热,产生的气体使溴水褪色 该气体是乙烯
D 氯化镁溶液中滴入氢氧化钠溶液,生成沉淀 氢氧化钠的碱性比氢氧化镁强
A. A B. B C. C D. D
第6页/共22页
学科网(北京)股份有限公司【答案】B
【解析】
【详解】A.用蓝色石蕊试纸检验某无色溶液,试纸变红,该溶液显酸性,但不一定是酸溶液,也有可能
是显酸性的盐溶液,A项不符合题意;
的
B.动物纤维主要成分是蛋白质,灼烧后有类似烧焦羽毛 味道,若用酒精灯灼烧织物产生类似烧焦羽毛
的味道,说明该织物含有动物纤维,含有蛋白质,B项符合题意;
C.乙醇和浓硫酸加热,会产生很多产物,如加热温度在170℃,主要产物为乙烯;如加热温度在140℃,
主要产物为二乙醚;同时乙醇可在浓硫酸下脱水生成碳单质,继续和浓硫酸在加热条件下产生二氧化碳、
二氧化硫等,其中的产物二氧化硫也能使溴水褪色,不能说明产生的气体就是乙烯,C项不符合题意;
D.氯化镁溶液中滴入氢氧化钠溶液,会发生复分解反应,生成难溶的氢氧化镁,与氢氧化钠和氢氧化镁
的碱性无关,不能由此得出氢氧化钠的碱性比氢氧化镁强,D项不符合题意;
故选B。
11. 一种高聚物 被称为“无机橡胶”,可由如图所示的环状三聚体制备。X、Y和Z都是短周期
元素,X、Y价电子数相等,X、Z电子层数相同,基态Y的 轨道半充满,Z的最外层只有1个未成对
电子,下列说法正确的是
A. X、Z的第一电离能: B. X、Y的简单氢化物的键角:
C. 最高价含氧酸的酸性: D. X、Y、Z均能形成多种氧化物
【答案】D
【解析】
【分析】X、Y价电子数相等,X、Y属于同一主族,且X形成5个键,Y形成3个键,基态Y的 轨道
半充满,则X为P元素,Y为N元素,X、Z电子层数相同, Z的最外层只有1个未成对电子,Z形成1
个键,Z为Cl元素,以此分析。
【详解】A.第一电离能同周期从左到右有增大趋势,第一电离能:Cl>P,A错误;
B.X、Y的简单氢化物分别为:PH 和NH ,电负性:N>P,共用电子对距N近,成键电子对斥力N-H大
3 3
第7页/共22页
学科网(北京)股份有限公司于P-H,键角:NH >PH,B错误;
3 3
C.元素的非金属性越强,其最高价含氧酸酸性越强,非金属性:Cl>N>P,酸性:HClO>HNO >H PO ,
4 3 3 4
C错误;公众号:高中试卷君
D.P、N、Cl均能形成多种氧化物,D正确;
答案选D。
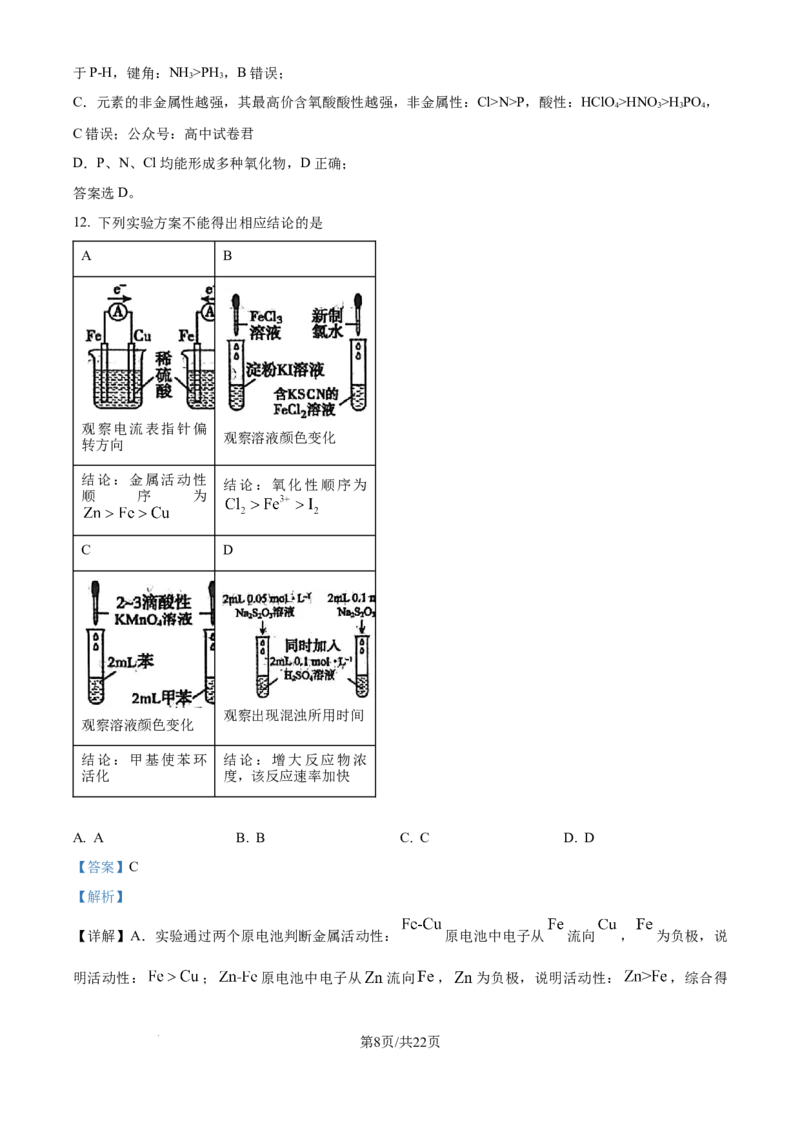
12. 下列实验方案不能得出相应结论的是
A B
观察电流表指针偏
观察溶液颜色变化
转方向
结论:金属活动性
结论:氧化性顺序为
顺 序 为
C D
观察出现混浊所用时间
观察溶液颜色变化
结论:甲基使苯环 结论:增大反应物浓
活化 度,该反应速率加快
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.实验通过两个原电池判断金属活动性: 原电池中电子从 流向 , 为负极,说
明活动性: ; 原电池中电子从 流向 , 为负极,说明活动性: ,综合得
第8页/共22页
学科网(北京)股份有限公司活动性: ,A正确;
B.KI和FeCl 发生氧化还原反应产生FeCl 和I,溶液变为蓝色,证明氧化性:Fe3+>I,向含 的
2 2 2 2
溶液中滴加氯水, 将 氧化为 ,溶液变红,证明氧化性 ,综合氧化性:
,B正确;
C.酸性 溶液氧化甲苯中的甲基,而苯不反应,因此苯环使甲基活化,而非甲基使苯环活化,C
错误;
D.实验中仅 浓度不同,其他条件相同,浓度大的试管先出现浑浊,说明增大反应物浓度加快反
应速率,D正确;
故答案选C。
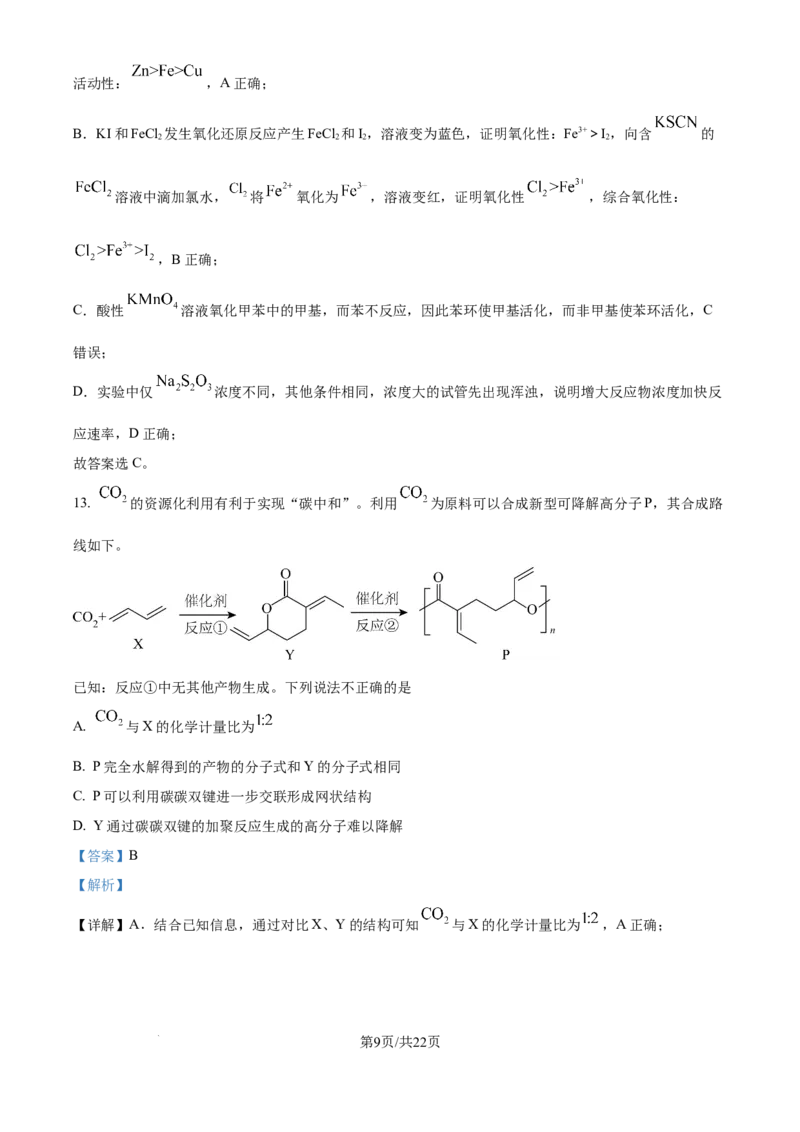
13. 的资源化利用有利于实现“碳中和”。利用 为原料可以合成新型可降解高分子P,其合成路
线如下。
已知:反应①中无其他产物生成。下列说法不正确的是
A. 与X的化学计量比为
B. P完全水解得到的产物的分子式和Y的分子式相同
C. P可以利用碳碳双键进一步交联形成网状结构
D. Y通过碳碳双键的加聚反应生成的高分子难以降解
【答案】B
【解析】
【详解】A.结合已知信息,通过对比X、Y的结构可知 与X的化学计量比为 ,A正确;
第9页/共22页
学科网(北京)股份有限公司B.P完全水解得到的产物结构简式为 ,分子式为 ,Y的分子式为
,二者分子式不相同,B错误;
C.P的支链上有碳碳双键,可进一步交联形成网状结构,C正确;
D.Y形成的聚酯类高分子主链上含有大量酯基,易水解,而Y通过碳碳双键加聚得到的高分子主链主要
为长碳链,与聚酯类高分子相比难以降解,D正确;
故选B。
14. 兴趣小组设计了从 中提取 的实验方案,下列说法正确的是
A. 还原性:
B. 按上述方案消耗 可回收
C. 反应①的离子方程式是
D. 溶液①中的金属离子是
【答案】C
【解析】
【详解】A.根据金属活动性顺序,还原性: ,故A错误;
B.按上述方案,根据得失电子守恒,消耗 生成1molCu,1molCu可回收2molAg,故B错误;
C.反应①是 和盐酸反应生成氯化铜和氯化铵,反应的离子方程式是
,故C正确;
D.氯化铵溶液显酸性,在酸性条件下,氧气能将 氧化为 ,所以溶液①中的金属离子是 ,
故D错误;
第10页/共22页
学科网(北京)股份有限公司选C。
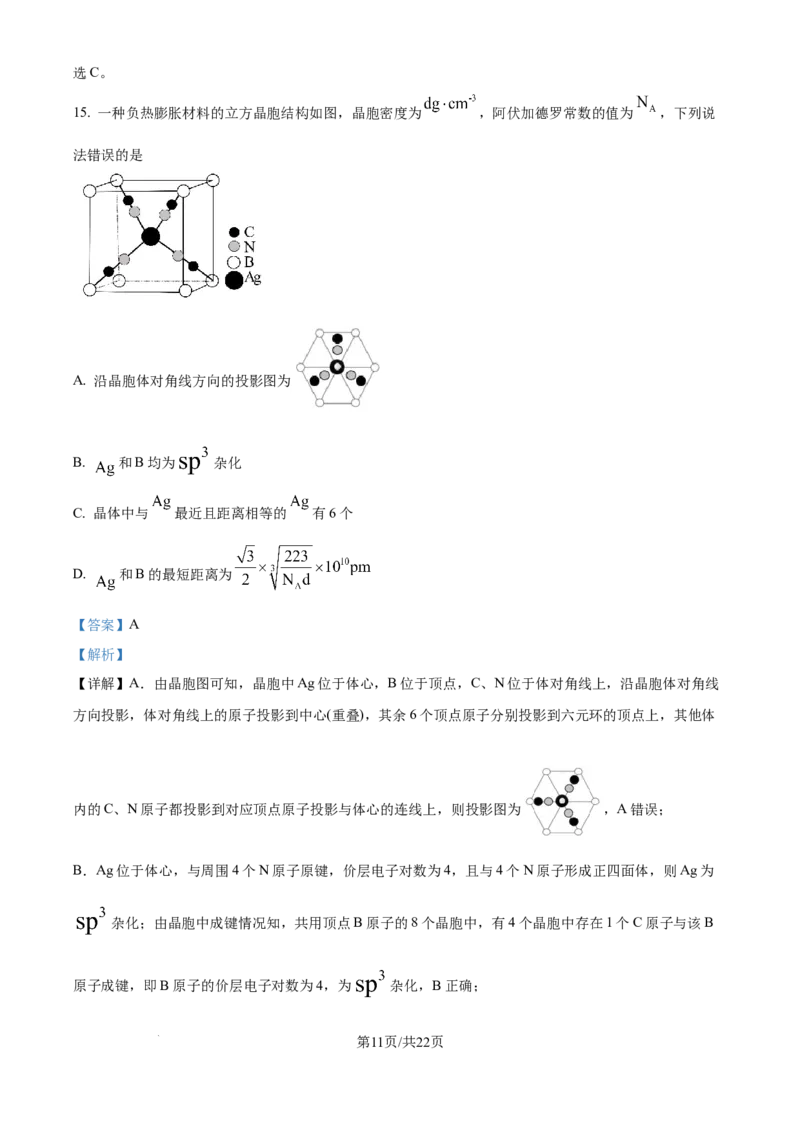
15. 一种负热膨胀材料的立方晶胞结构如图,晶胞密度为 ,阿伏加德罗常数的值为 ,下列说
法错误的是
A. 沿晶胞体对角线方向的投影图为
B. 和B均为 杂化
C. 晶体中与 最近且距离相等的 有6个
D. 和B的最短距离为
【答案】A
【解析】
【详解】A.由晶胞图可知,晶胞中Ag位于体心,B位于顶点,C、N位于体对角线上,沿晶胞体对角线
方向投影,体对角线上的原子投影到中心(重叠),其余6个顶点原子分别投影到六元环的顶点上,其他体
内的C、N原子都投影到对应顶点原子投影与体心的连线上,则投影图为 ,A错误;
B.Ag位于体心,与周围4个N原子原键,价层电子对数为4,且与4个N原子形成正四面体,则Ag为
杂化;由晶胞中成键情况知,共用顶点B原子的8个晶胞中,有4个晶胞中存在1个C原子与该B
原子成键,即B原子的价层电子对数为4,为 杂化,B正确;
第11页/共22页
学科网(北京)股份有限公司C.晶胞中Ag位于体心,与 最近且距离相等的 就是该晶胞上、下、左、右、前、后6个相邻的晶
胞体心中的 原子,为6个,C正确;
D.B位于顶点,其个数为 ,Ag、C、N均位于晶胞内,个数分别为1、4、4,由晶胞密度可知晶
胞参数a= , 和B的最短距离为体对角线的一半,即
,D正确;
故选A。
二、非选择题:(本题共4小题,共55分)。
16. Fe单质及其化合物应用广泛。回答下列问题:
(1)在元素周期表中,基态 原子的价层电子排布式_____。基态 原子与基态 离子未成对电子数
之比为_____。
(2)尿素分子 与 形成配离子的硝酸盐 俗称尿素铁,既
可作铁肥,又可作缓释氮肥。
①元素C、N、O中,第一电离能最大的是_____。
②尿素分子中,C原子采取的轨道杂化方式为_____。
③八面体配离子 中 的配位数为6,碳氮键的键长均相等,则与 配位的原
子是_____(填元素符号)。
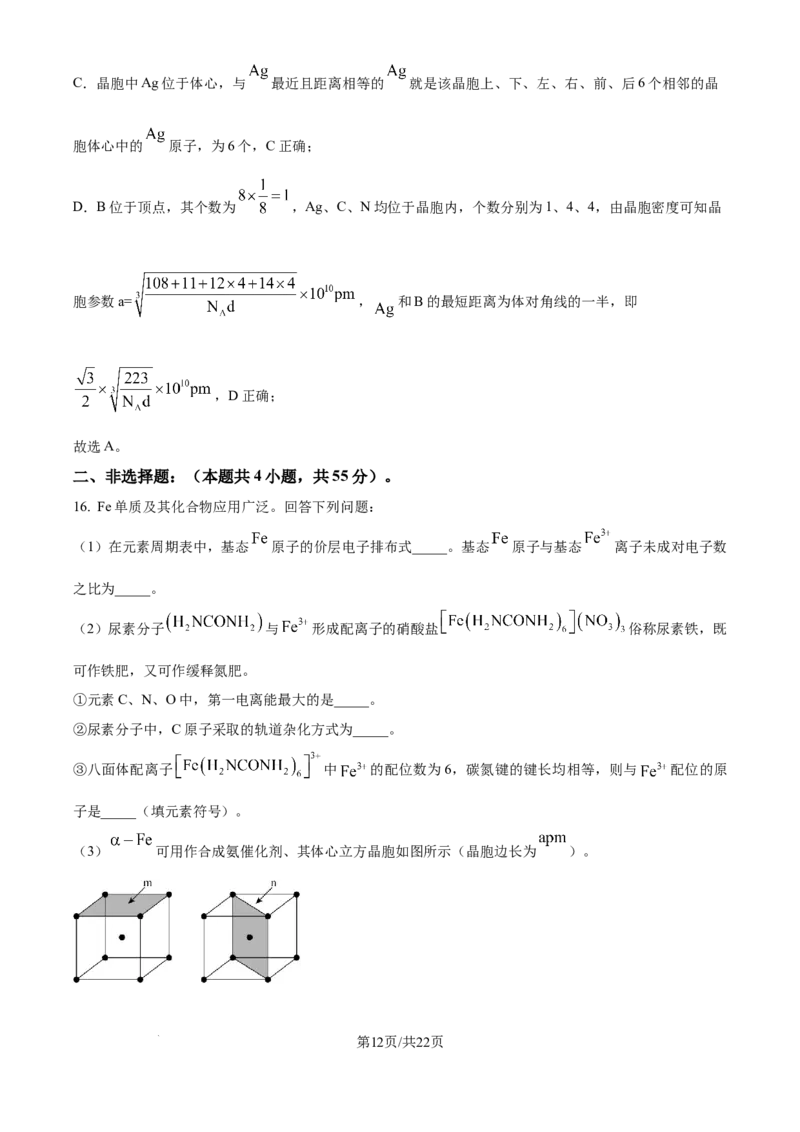
(3) 可用作合成氨催化剂、其体心立方晶胞如图所示(晶胞边长为 )。
第12页/共22页
学科网(北京)股份有限公司① 晶胞中 原子的半径为_____ 。
②研究发现, 晶胞中阴影所示 , 两个截面的催化活性不同,截面单位面积含有Fe原子个数越
多,催化活性越低。m,n截面中,催化活性较低的是_____,该截面单位面积含有的Fe原子为_____个
。
【答案】(1) ①. ②. 4:5
(2) ①. N ②. ③. O
(3) ①. ②. n ③.
【解析】
【小问1详解】
Fe为26号元素,位于元素周期表中第四周期VIII族基态Fe原子电子排布式为 ,故价电子排
布式为 ;基态 原子未成对电子数为4,基态 离子价电子排布式为 ,未成对电子数为
5,比值为4:5。
【小问2详解】
①同周期元素从左到右,第一电离能呈增大趋势,但N原子2p轨道为半充满稳定结构,第一电离能:
N>O>C,故答案为N;
②尿素分子中C原子形成3个 键,无孤电子对,采取的轨道杂化方式为 杂化;
③八面体配离子 中 的配位数为6,碳氮键的键长均相等,因此N原子不会参
与形成配位键,说明C=O中O原子参与配位,所以与配位的原子是O。
【小问3详解】
① 为体心立方晶胞,晶胞边长为a pm,体对角线长度为 ,体心立方晶胞中Fe原子半径r
与体对角线关系为4r= ,因此Fe原子的半径为 。
第13页/共22页
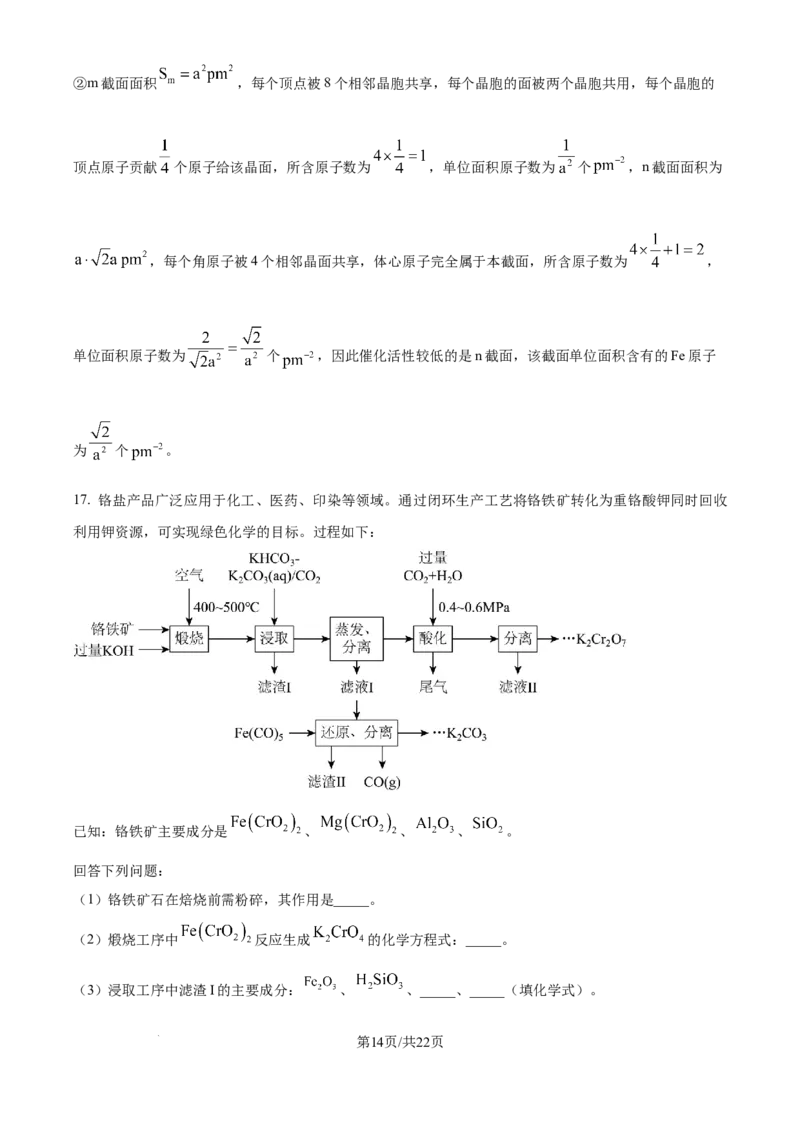
学科网(北京)股份有限公司②m截面面积 ,每个顶点被8个相邻晶胞共享,每个晶胞的面被两个晶胞共用,每个晶胞的
顶点原子贡献 个原子给该晶面,所含原子数为 ,单位面积原子数为 个 ,n截面面积为
,每个角原子被4个相邻晶面共享,体心原子完全属于本截面,所含原子数为 ,
单位面积原子数为 个 ,因此催化活性较低的是n截面,该截面单位面积含有的Fe原子
为 个 。
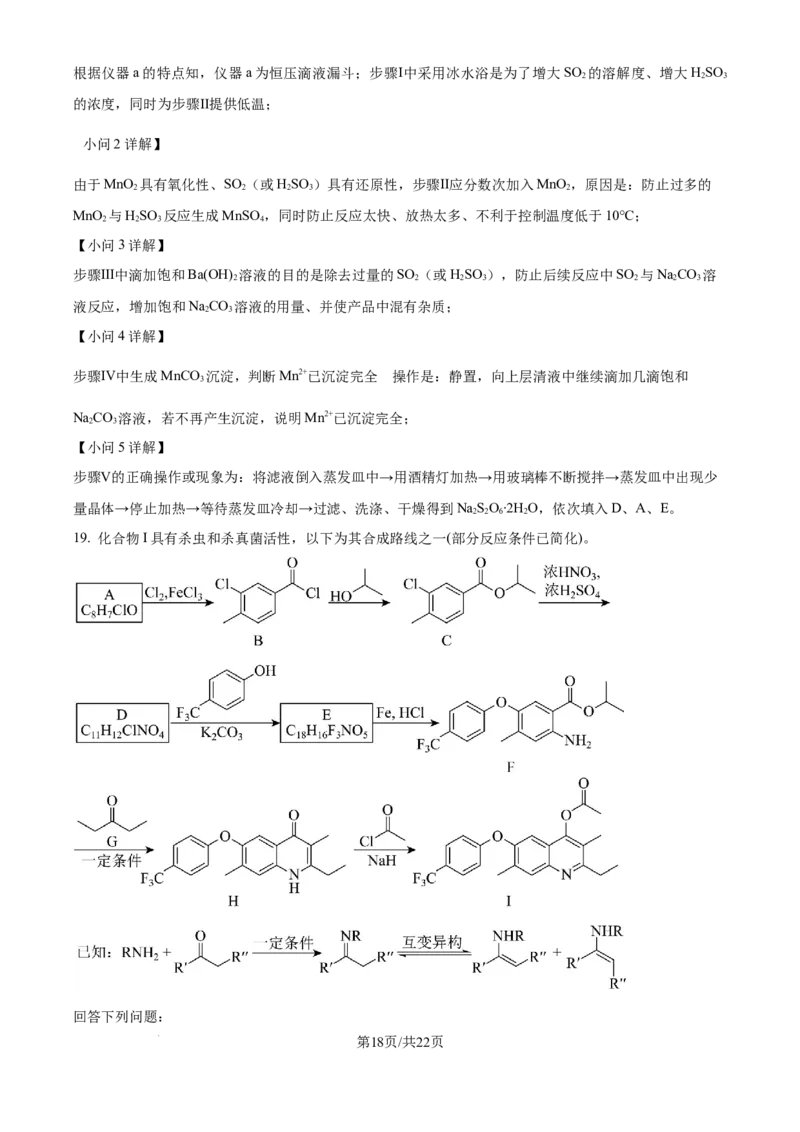
17. 铬盐产品广泛应用于化工、医药、印染等领域。通过闭环生产工艺将铬铁矿转化为重铬酸钾同时回收
利用钾资源,可实现绿色化学的目标。过程如下:
已知:铬铁矿主要成分是 、 、 、 。
回答下列问题:
(1)铬铁矿石在焙烧前需粉碎,其作用是_____。
(2)煅烧工序中 反应生成 的化学方程式:_____。
(3)浸取工序中滤渣I的主要成分: 、 、_____、_____(填化学式)。
第14页/共22页
学科网(北京)股份有限公司(4)酸化工序中需加压的原因:_____。
(5)滤液Ⅱ的主要成分:_____(填化学式)。
(6)补全还原、分离工序中发生反应的化学方程式_____。
_____+_____= _____+_____+_____CO
(7)滤渣Ⅱ可返回_____工序。(填工序名称)
【答案】(1)增大接触面积,提高煅烧速率
(2)
(3) ①. ②. MgO
(4)加大压强,可以增大CO 的溶解度,使液体中CO 浓度增大,保证酸化反应充分进行
2 2
(5)
(6) (7)浸取
【解析】
【分析】铬铁矿主要成分是 、 、 、 ,与过量KOH在空气中煅烧,生
成 、 、 MgO 、 、 , ; 通 入 浸 取 , 生 成
, 、MgO不反应,故滤渣Ⅰ为 , 、MgO;通过蒸发
浓缩、冷却结晶、过滤分离出 固体,滤液Ⅰ中含有 ,将 中加水溶解,并通入过
量CO 酸化,将 转化为 ,同时副产物 生成,将 与 分离,滤液
2
Ⅱ的主要溶质为 ; 做还原剂,将滤液Ⅰ中剩余的 还原为 ,自身转化
为 进入滤渣Ⅱ,KOH进一步处理得 ,循环使用。公众号:高中试卷君
【小问1详解】
铬铁矿石在焙烧前需粉碎,其作用是增大接触面积,提高煅烧速率。
【小问2详解】
第15页/共22页
学科网(北京)股份有限公司煅烧工序中 与过量KOH在空气中煅烧生成 、 ,化学方程式为
。
【小问3详解】
根据分析可得浸取工序中滤渣I的主要成分: , 、MgO,故答案为 、
MgO。
【小问4详解】
向 中加水溶解,并通入过量CO 酸化,将 转化为 ,加大压强,可以增大CO 的
2 2
溶解度,使液体中CO 浓度增大,保证酸化反应充分进行。
2
【小问5详解】
将 与 分离,滤液Ⅱ的主要溶质为 。
【小问6详解】
做还原剂,将滤液Ⅰ中剩余的 还原为 ,自身转化为 ,铁元素由0
价升高到+3价,Cr由+6价降低到+3价,根据得失电子守恒,原子守恒,化学方程式
。
【小问7详解】
做还原剂,将滤液Ⅰ中剩余的 还原为 ,自身转化为 进入滤渣Ⅱ,
回到“浸取”工序循环使用,以回收其中的铬元素。
18. 某兴趣小组设计了利用 和 生成 ,再与 反应制备 的方
案:
(1)采用下图所示装置制备 ,仪器a的名称为_______;步骤I中采用冰水浴是为了_______;
第16页/共22页
学科网(北京)股份有限公司是
(2)步骤Ⅱ应分数次加入 ,原因 _______;
(3)步骤Ⅲ滴加饱和 溶液的目的是_______;
(4)步骤Ⅳ生成 沉淀,判断 已沉淀完全的操作是_______;
(5)将步骤Ⅴ中正确操作或现象的标号填入相应括号中_______。
A.蒸发皿中出现少量晶体
B.使用漏斗趁热过滤
C.利用蒸发皿余热使溶液蒸干
D.用玻璃棒不断搅拌
E.等待蒸发皿冷却
【答案】(1) ①. 恒压滴液漏斗 ②. 增大SO 的溶解度、增大HSO 的浓度,同时为步骤Ⅱ提供低
2 2 3
温
(2)防止过多的MnO 与HSO 反应生成MnSO ,同时防止反应太快、放热太多、不利于控制温度低于
2 2 3 4
10℃
(3)除去过量的SO (或HSO )
2 2 3
(4)静置,向上层清液中继续滴加几滴饱和NaCO 溶液,若不再产生沉淀,说明Mn2+已沉淀完全
2 3
(5)D、A、E
【解析】
【分析】步骤Ⅱ中 MnO 与 HSO 在低于 10℃时反应生成 MnS O ,反应的化学方程式为
2 2 3 2 6
MnO +2H SO =MnSO+2H O,步骤Ⅲ中滴加饱和Ba(OH) 除去过量的SO (或HSO ),步骤Ⅳ中滴入饱
2 2 3 2 6 2 2 2 2 3
和NaCO 溶液发生反应MnS O+Na CO=MnCO↓+Na SO ,经过滤得到NaSO 溶液,步骤Ⅴ中NaSO
2 3 2 6 2 3 3 2 2 6 2 2 6 2 2 6
溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到NaSO∙2H O。
2 2 6 2
【小问1详解】公众号:高中试卷君
第17页/共22页
学科网(北京)股份有限公司根据仪器a的特点知,仪器a为恒压滴液漏斗;步骤Ⅰ中采用冰水浴是为了增大SO 的溶解度、增大HSO
2 2 3
的浓度,同时为步骤Ⅱ提供低温;
【
小问2详解】
由于MnO 具有氧化性、SO (或HSO )具有还原性,步骤Ⅱ应分数次加入MnO ,原因是:防止过多的
2 2 2 3 2
MnO 与HSO 反应生成MnSO ,同时防止反应太快、放热太多、不利于控制温度低于10℃;
2 2 3 4
【小问3详解】
步骤Ⅲ中滴加饱和Ba(OH) 溶液的目的是除去过量的SO (或HSO ),防止后续反应中SO 与NaCO 溶
2 2 2 3 2 2 3
液反应,增加饱和NaCO 溶液的用量、并使产品中混有杂质;
2 3
【小问4详解】
的
步骤Ⅳ中生成MnCO 沉淀,判断Mn2+已沉淀完全 操作是:静置,向上层清液中继续滴加几滴饱和
3
NaCO 溶液,若不再产生沉淀,说明Mn2+已沉淀完全;
2 3
【小问5详解】
步骤Ⅴ的正确操作或现象为:将滤液倒入蒸发皿中→用酒精灯加热→用玻璃棒不断搅拌→蒸发皿中出现少
量晶体→停止加热→等待蒸发皿冷却→过滤、洗涤、干燥得到NaSO∙2H O,依次填入D、A、E。
2 2 6 2
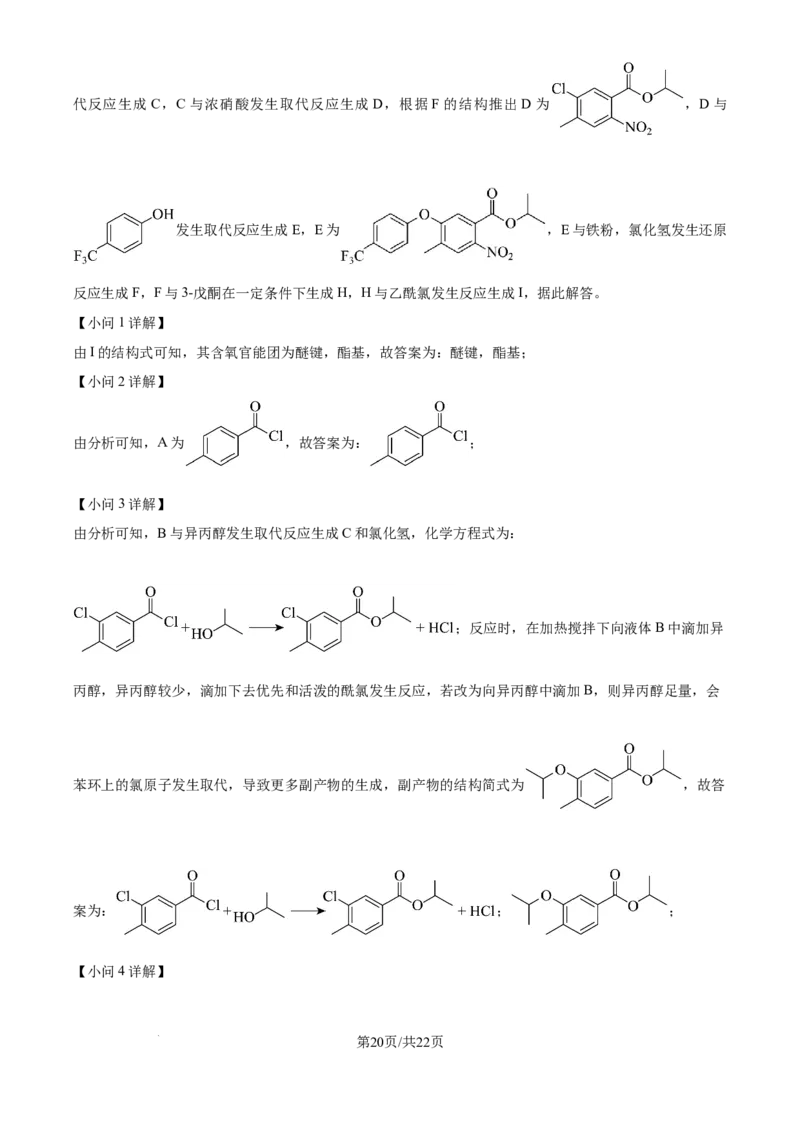
19. 化合物I具有杀虫和杀真菌活性,以下为其合成路线之一(部分反应条件已简化)。
回答下列问题:
第18页/共22页
学科网(北京)股份有限公司(1)I中含氧官能团的名称是_______。
(2)A的结构简式为_______。
(3)由B生成C的化学方程式为_______。反应时,在加热搅拌下向液体B中滴加异丙醇;若改为向异丙
醇中滴加B则会导致更多副产物的生成,副产物可能的结构简式为_______(写出一种即可)。
(4)由D生成E的反应类型为_______。
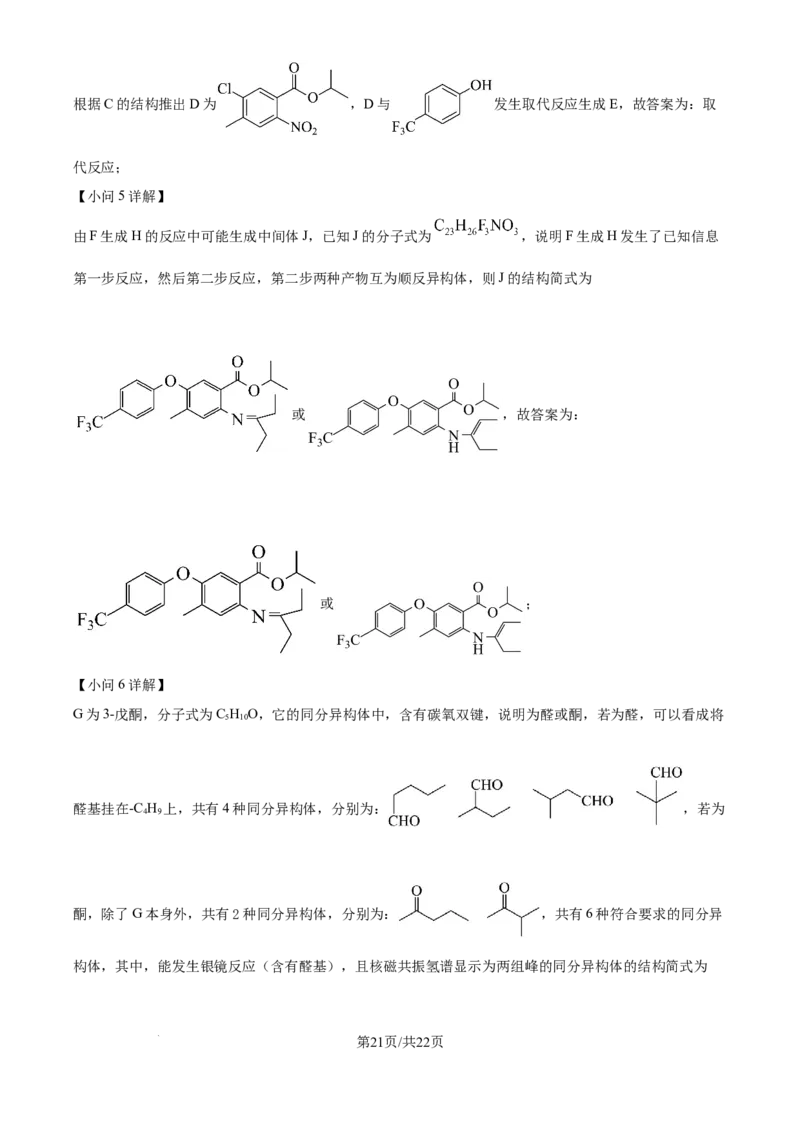
(5)由F生成H的反应中可能生成中间体J,已知J的分子式为 ,则J的结构简式为
_______(写出一种即可)。
(6)G的同分异构体中,含有碳氧双键的还有_______种(不考虑立体异构);其中,能发生银镜反应,且
核磁共振氢谱显示为两组峰的同分异构体的结构简式为_______。
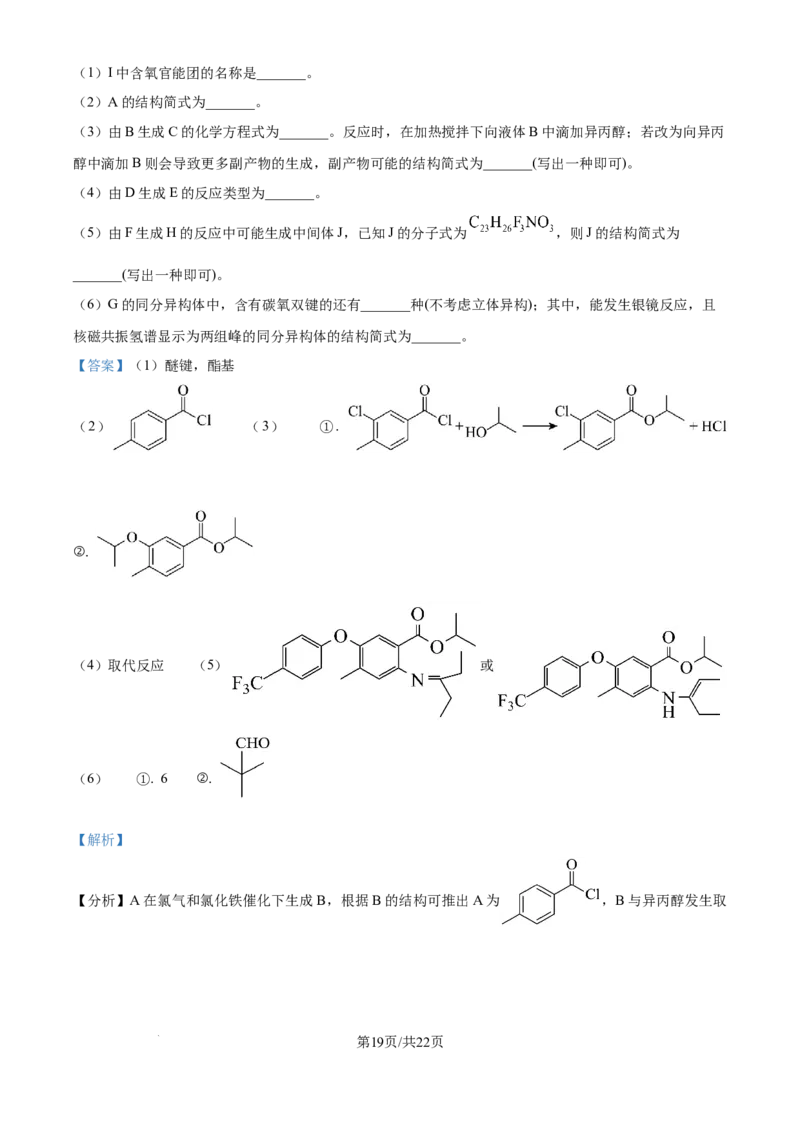
【答案】(1)醚键,酯基
(2) (3) ①.
②.
(4)取代反应 (5) 或
(6) ①. 6 ②.
【解析】
【分析】A在氯气和氯化铁催化下生成B,根据B的结构可推出A为 ,B与异丙醇发生取
第19页/共22页
学科网(北京)股份有限公司代反应生成C,C与浓硝酸发生取代反应生成D,根据F的结构推出D为 ,D与
发生取代反应生成E,E为 ,E与铁粉,氯化氢发生还原
反应生成F,F与3-戊酮在一定条件下生成H,H与乙酰氯发生反应生成I,据此解答。
【小问1详解】
由I的结构式可知,其含氧官能团为醚键,酯基,故答案为:醚键,酯基;
【小问2详解】
由分析可知,A为 ,故答案为: ;
【小问3详解】
由分析可知,B与异丙醇发生取代反应生成C和氯化氢,化学方程式为:
;反应时,在加热搅拌下向液体B中滴加异
丙醇,异丙醇较少,滴加下去优先和活泼的酰氯发生反应,若改为向异丙醇中滴加B,则异丙醇足量,会
苯环上的氯原子发生取代,导致更多副产物的生成,副产物的结构简式为 ,故答
案为: ; ;
【小问4详解】
第20页/共22页
学科网(北京)股份有限公司根据C的结构推出D为 ,D与 发生取代反应生成E,故答案为:取
代反应;
【小问5详解】
由F生成H的反应中可能生成中间体J,已知J的分子式为 ,说明F生成H发生了已知信息
第一步反应,然后第二步反应,第二步两种产物互为顺反异构体,则J的结构简式为
或 ,故答案为:
或 ;
【小问6详解】
G为3-戊酮,分子式为C H O,它的同分异构体中,含有碳氧双键,说明为醛或酮,若为醛,可以看成将
5 10
醛基挂在-C H 上,共有4种同分异构体,分别为: ,若为
4 9
酮,除了G本身外,共有2种同分异构体,分别为: ,共有6种符合要求的同分异
构体,其中,能发生银镜反应(含有醛基),且核磁共振氢谱显示为两组峰的同分异构体的结构简式为
第21页/共22页
学科网(北京)股份有限公司,故答案为:6; 。
第22页/共22页
学科网(北京)股份有限公司