文档内容
六安一中 2025 届高三综合模拟卷
化学试卷(二)
时间:75分钟 满分:100分
可能用到的相对原子质量:H:1 Li:7 C:12 O:16
一、选择题:本题共14小题,每小题3分,共42分。
1. 中华优秀传统文化涉及很多化学知识。下列说法错误的是
的
A. “世间丝、麻、裘、褐皆具素质”,文中 “裘”的主要成分是蛋白质
B. 《神农本草经》中“石胆……能化铁为铜、成金银”描述的是湿法炼铜
C. “凿开混沌得乌金,不辞辛苦出山林”,其中“乌金”的主要成分是煤炭
D. 《本草纲目拾遗》中有对强水的记载:性最猛烈,能蚀五金。强水属于强电解质
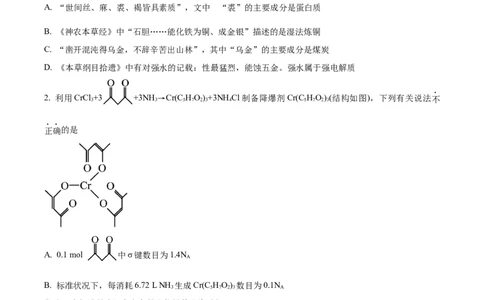
2. 利用CrCl +3 +3NH→Cr(C HO)+3NHCl制备降爆剂Cr(C HO)(结构如图),下列有关说法不
3 3 5 7 2 3 4 5 7 2 3
正确的是
A. 0.1 mol 中σ键数目为1.4N
A
B. 标准状况下,每消耗6.72 L NH 生成Cr(C HO) 数目为0.1N
3 5 7 2 3 A
C. 2 mol Cr(C HO) 中含有的配位键数目为6N
5 7 2 3 A
D. 1 L 0.1 mol·L-1 NH Cl溶液含有的 数目为0.1N
4 A
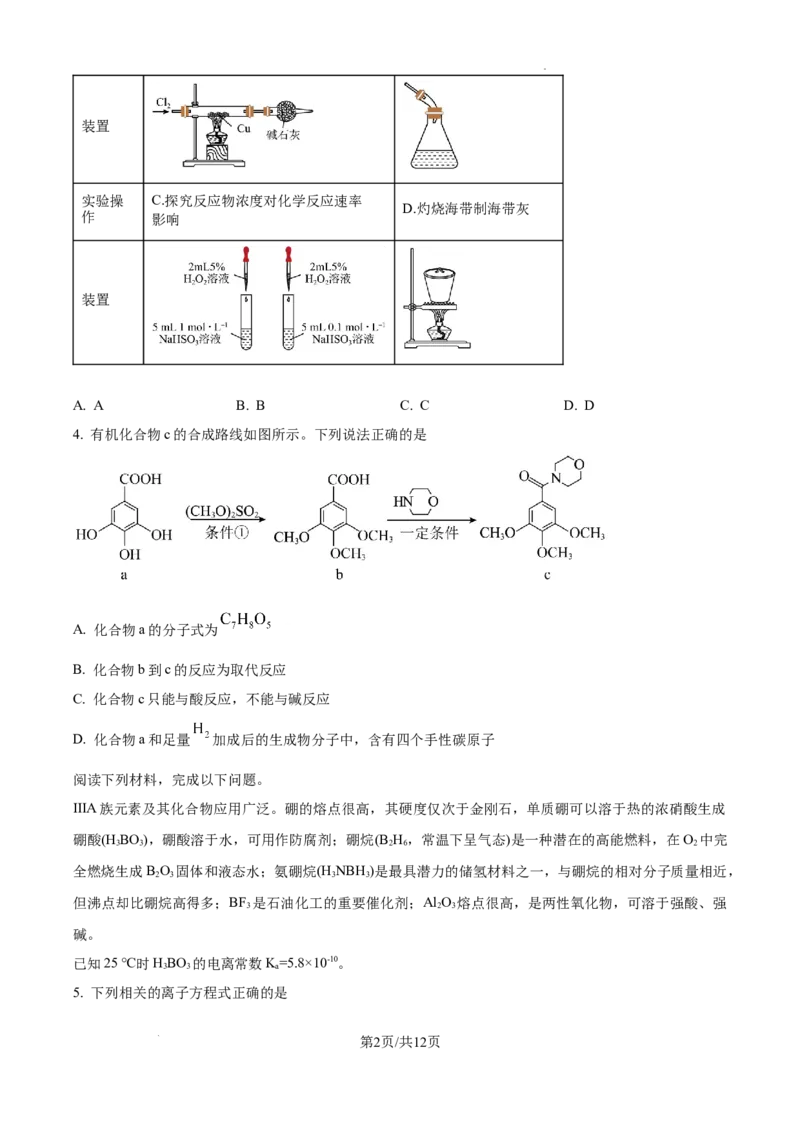
3. 下列实验操作对应的装置正确的是
实验操 B.石油分馏时接收馏出
A.氯气和铜的反应
作 物
第1页/共12页
学科网(北京)股份有限公司装置
实验操 C.探究反应物浓度对化学反应速率 的
D.灼烧海带制海带灰
作 影响
装置
A. A B. B C. C D. D
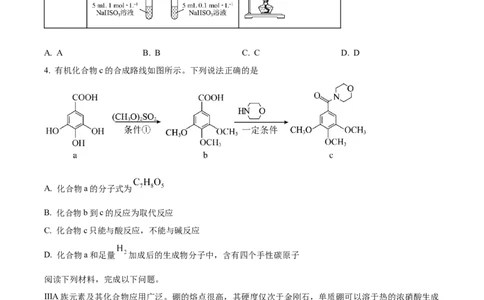
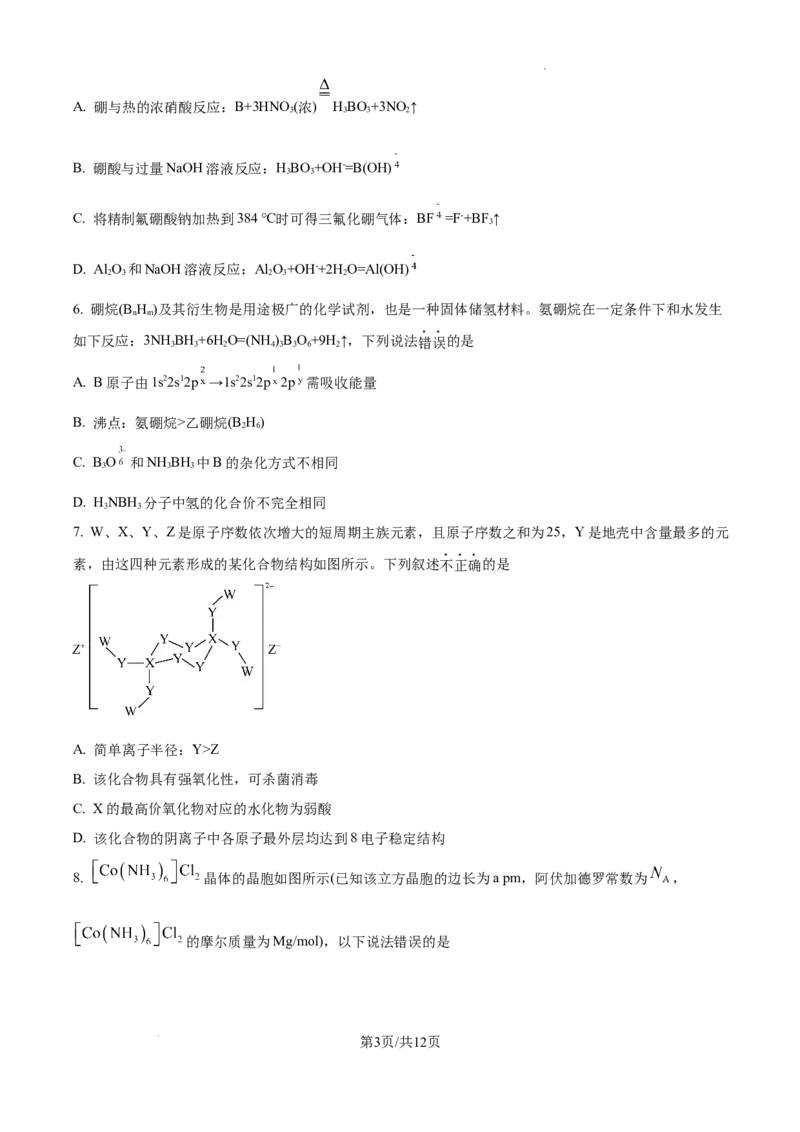
4. 有机化合物c的合成路线如图所示。下列说法正确的是
A. 化合物a的分子式为
B. 化合物b到c的反应为取代反应
C. 化合物c只能与酸反应,不能与碱反应
D. 化合物a和足量 加成后的生成物分子中,含有四个手性碳原子
阅读下列材料,完成以下问题。
ⅢA族元素及其化合物应用广泛。硼的熔点很高,其硬度仅次于金刚石,单质硼可以溶于热的浓硝酸生成
硼酸(H BO),硼酸溶于水,可用作防腐剂;硼烷(B H,常温下呈气态)是一种潜在的高能燃料,在O 中完
3 3 2 6 2
全燃烧生成B O 固体和液态水;氨硼烷(H NBH )是最具潜力的储氢材料之一,与硼烷的相对分子质量相近,
2 3 3 3
但沸点却比硼烷高得多;BF 是石油化工的重要催化剂;Al O 熔点很高,是两性氧化物,可溶于强酸、强
3 2 3
碱。
已知25 ℃时HBO 的电离常数K=5.8×10-10。
3 3 a
5. 下列相关的离子方程式正确的是
第2页/共12页
学科网(北京)股份有限公司A. 硼与热的浓硝酸反应:B+3HNO (浓) HBO+3NO↑
3 3 3 2
B. 硼酸与过量NaOH溶液反应:HBO+OH-=B(OH)
3 3
C. 将精制氟硼酸钠加热到384 ℃时可得三氟化硼气体:BF =F-+BF ↑
3
D. Al O 和NaOH溶液反应:Al O+OH-+2H O=Al(OH)
2 3 2 3 2
6. 硼烷(B H )及其衍生物是用途极广的化学试剂,也是一种固体储氢材料。氨硼烷在一定条件下和水发生
n m
如下反应:3NH BH+6H O=(NH )B O+9H ↑,下列说法错误的是
3 3 2 4 3 3 6 2
A. B原子由1s22s12p →1s22s12p 2p 需吸收能量
B. 沸点:氨硼烷>乙硼烷(B H)
2 6
C. B O 和NH BH 中B的杂化方式不相同
3 3 3
D. HNBH 分子中氢的化合价不完全相同
3 3
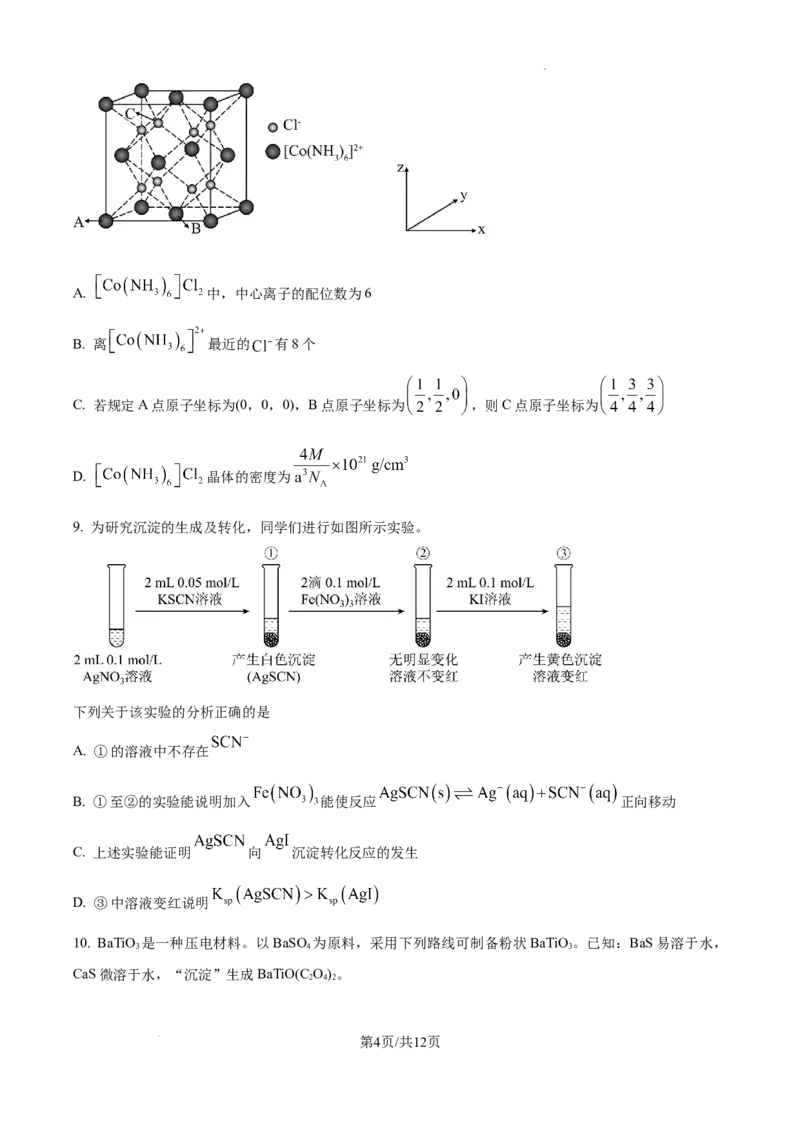
7. W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数之和为25,Y是地壳中含量最多的元
素,由这四种元素形成的某化合物结构如图所示。下列叙述不正确的是
A. 简单离子半径:Y>Z
B. 该化合物具有强氧化性,可杀菌消毒
C. X的最高价氧化物对应的水化物为弱酸
D. 该化合物的阴离子中各原子最外层均达到8电子稳定结构
8. 晶体的晶胞如图所示(已知该立方晶胞的边长为a pm,阿伏加德罗常数为 ,
的摩尔质量为Mg/mol),以下说法错误的是
第3页/共12页
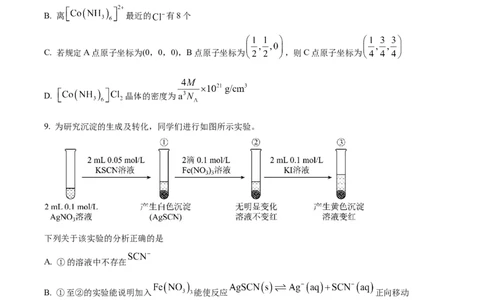
学科网(北京)股份有限公司A. 中,中心离子的配位数为6
B. 离 最近的 有8个
C. 若规定A点原子坐标为(0,0,0),B点原子坐标为 ,则C点原子坐标为
D. 晶体的密度为
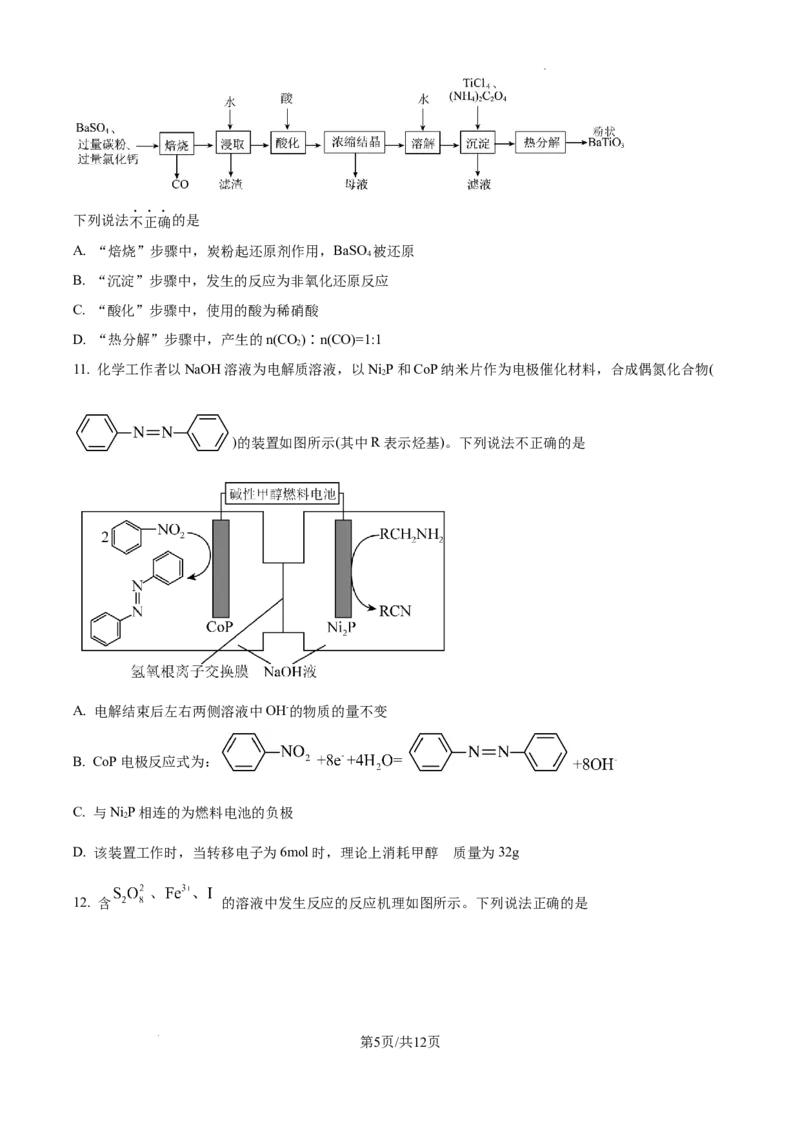
9. 为研究沉淀的生成及转化,同学们进行如图所示实验。
下列关于该实验的分析正确的是
A. ①的溶液中不存在
B. ①至②的实验能说明加入 能使反应 正向移动
C. 上述实验能证明 向 沉淀转化反应的发生
D. ③中溶液变红说明
10. BaTiO 是一种压电材料。以BaSO 为原料,采用下列路线可制备粉状BaTiO 。已知:BaS易溶于水,
3 4 3
CaS微溶于水,“沉淀”生成BaTiO(C O)。
2 4 2
第4页/共12页
学科网(北京)股份有限公司下列说法不正确的是
A. “焙烧”步骤中,炭粉起还原剂作用,BaSO 被还原
4
B. “沉淀”步骤中,发生的反应为非氧化还原反应
C. “酸化”步骤中,使用的酸为稀硝酸
D. “热分解”步骤中,产生的n(CO)∶n(CO)=1:1
2
11. 化学工作者以NaOH溶液为电解质溶液,以Ni P和CoP纳米片作为电极催化材料,合成偶氮化合物(
2
)的装置如图所示(其中R表示烃基)。下列说法不正确的是
A. 电解结束后左右两侧溶液中OH-的物质的量不变
B. CoP电极反应式为:
C. 与Ni P相连的为燃料电池的负极
2
的
D. 该装置工作时,当转移电子为6mol时,理论上消耗甲醇 质量为32g
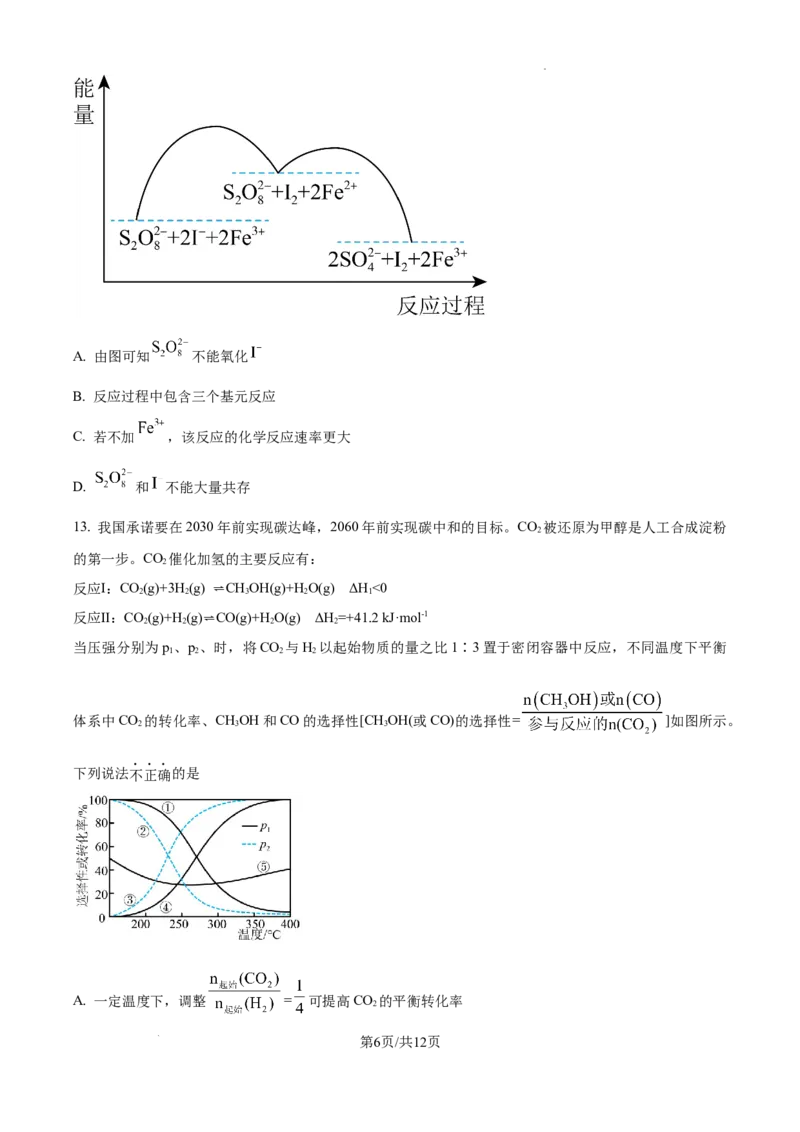
12. 含 的溶液中发生反应的反应机理如图所示。下列说法正确的是
第5页/共12页
学科网(北京)股份有限公司A. 由图可知 不能氧化
B. 反应过程中包含三个基元反应
C. 若不加 ,该反应的化学反应速率更大
D. 和 不能大量共存
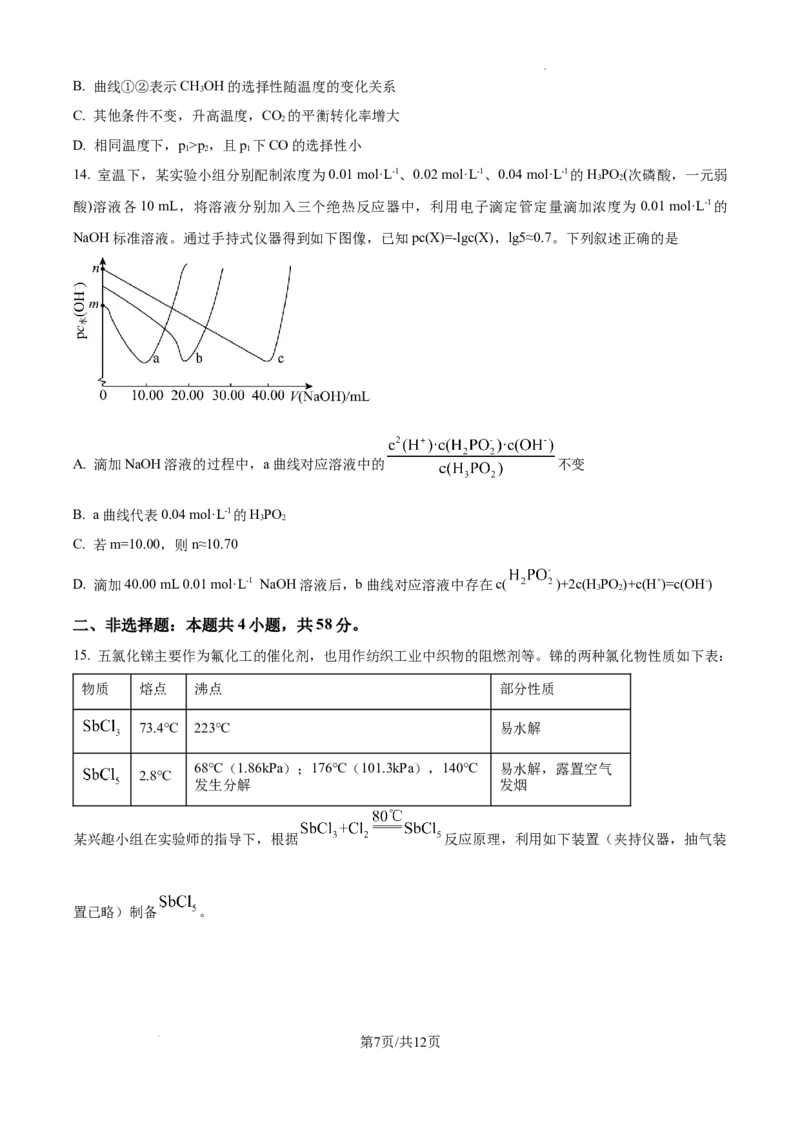
13. 我国承诺要在2030年前实现碳达峰,2060年前实现碳中和的目标。CO 被还原为甲醇是人工合成淀粉
2
的第一步。CO 催化加氢的主要反应有:
2
反应Ⅰ:CO
2
(g)+3H
2
(g) ⇌CH
3
OH(g)+H
2
O(g) ΔH
1
<0
反应Ⅱ:CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) ΔH
2
=+41.2 kJ·mol-1
当压强分别为p 、p 、时,将CO 与H 以起始物质的量之比1∶3置于密闭容器中反应,不同温度下平衡
1 2 2 2
体系中CO 的转化率、CHOH和CO的选择性[CHOH(或CO)的选择性= ]如图所示。
2 3 3
下列说法不正确的是
A. 一定温度下,调整 = 可提高CO 的平衡转化率
2
第6页/共12页
学科网(北京)股份有限公司B. 曲线①②表示CHOH的选择性随温度的变化关系
3
C. 其他条件不变,升高温度,CO 的平衡转化率增大
2
D. 相同温度下,p>p,且p 下CO的选择性小
1 2 1
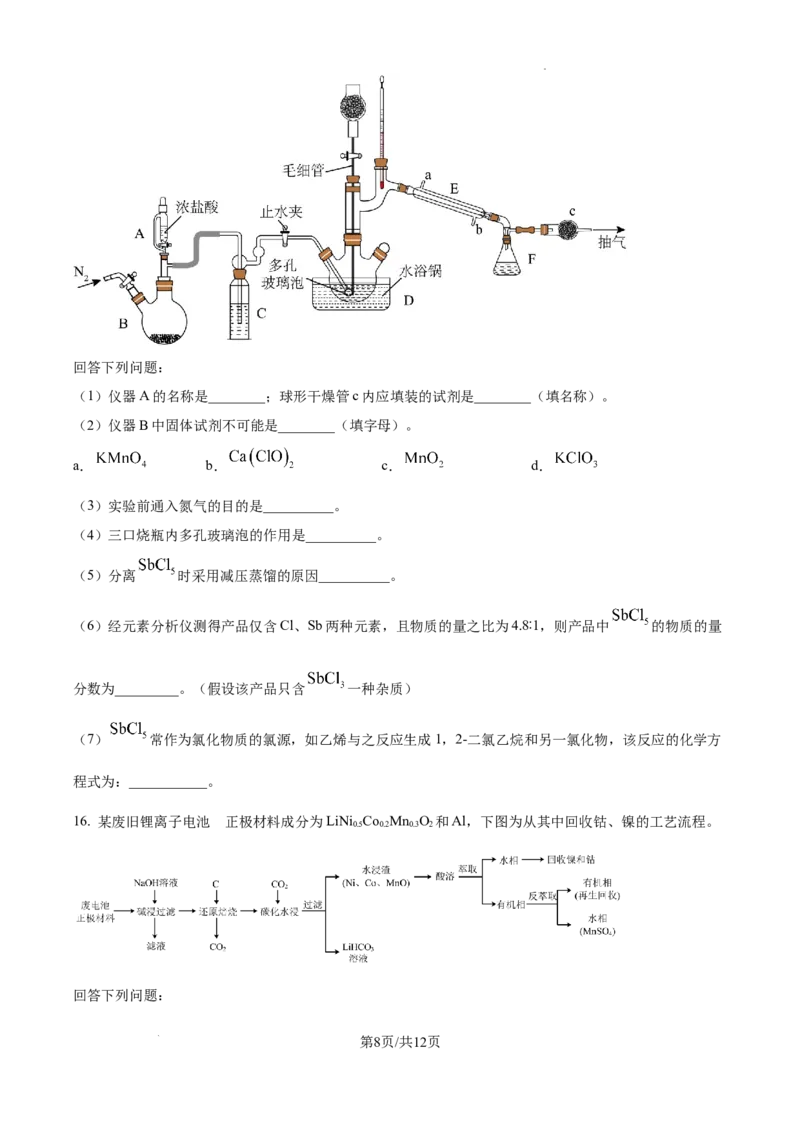
14. 室温下,某实验小组分别配制浓度为0.01 mol·L-1、0.02 mol·L-1、0.04 mol·L-1的HPO (次磷酸,一元弱
3 2
酸)溶液各10 mL,将溶液分别加入三个绝热反应器中,利用电子滴定管定量滴加浓度为 0.01 mol·L-1的
NaOH标准溶液。通过手持式仪器得到如下图像,已知pc(X)=-lgc(X),lg5≈0.7。下列叙述正确的是
A. 滴加NaOH溶液的过程中,a曲线对应溶液中的 不变
B. a曲线代表0.04 mol·L-1的HPO
3 2
C. 若m=10.00,则n≈10.70
D. 滴加40.00 mL 0.01 mol·L-1 NaOH溶液后,b曲线对应溶液中存在c( )+2c(H PO )+c(H+)=c(OH-)
3 2
二、非选择题:本题共4小题,共58分。
15. 五氯化锑主要作为氟化工的催化剂,也用作纺织工业中织物的阻燃剂等。锑的两种氯化物性质如下表:
物质 熔点 沸点 部分性质
73.4℃ 223℃ 易水解
68℃(1.86kPa);176℃(101.3kPa),140℃ 易水解,露置空气
2.8℃
发生分解 发烟
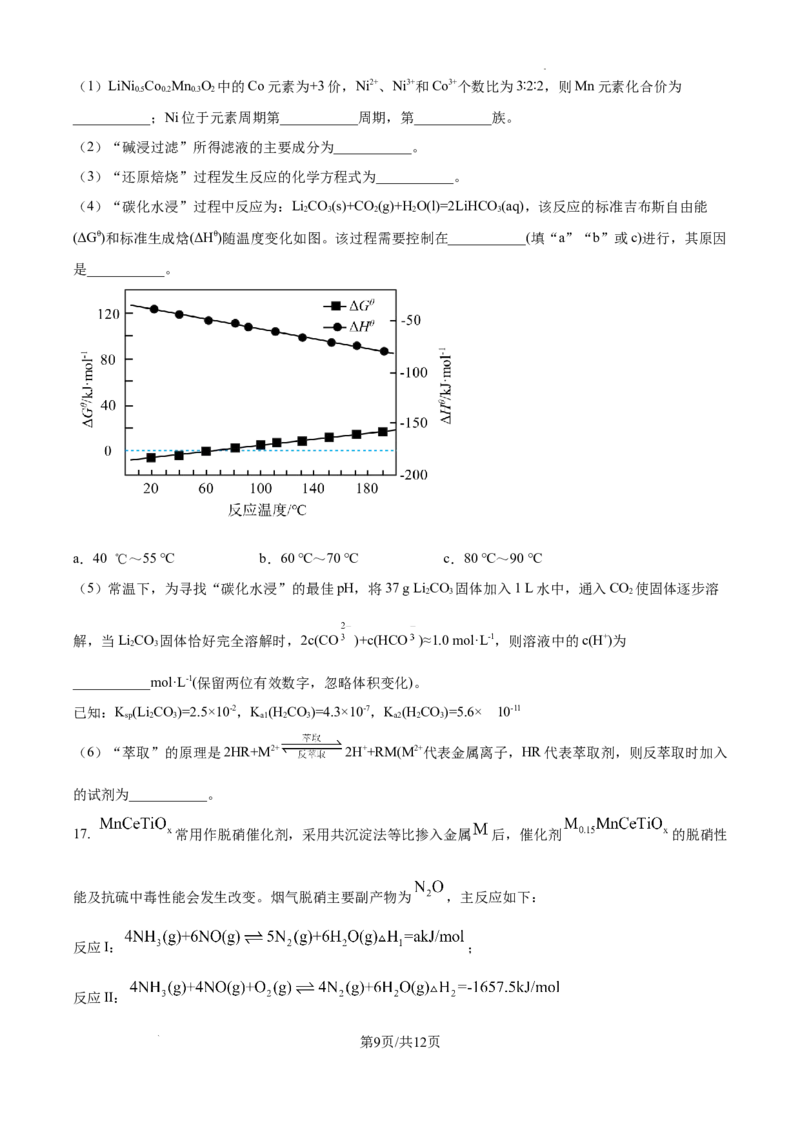
某兴趣小组在实验师的指导下,根据 反应原理,利用如下装置(夹持仪器,抽气装
置已略)制备 。
第7页/共12页
学科网(北京)股份有限公司回答下列问题:
(1)仪器A的名称是________;球形干燥管c内应填装的试剂是________(填名称)。
(2)仪器B中固体试剂不可能是________(填字母)。
a. b. c. d.
(3)实验前通入氮气的目的是__________。
(4)三口烧瓶内多孔玻璃泡的作用是__________。
(5)分离 时采用减压蒸馏的原因__________。
(6)经元素分析仪测得产品仅含Cl、Sb两种元素,且物质的量之比为4.8∶1,则产品中 的物质的量
分数为_________。(假设该产品只含 一种杂质)
(7) 常作为氯化物质的氯源,如乙烯与之反应生成1,2-二氯乙烷和另一氯化物,该反应的化学方
程式为:___________。
的
16. 某废旧锂离子电池 正极材料成分为LiNi Co Mn O 和Al,下图为从其中回收钴、镍的工艺流程。
0.5 0.2 0.3 2
回答下列问题:
第8页/共12页
学科网(北京)股份有限公司(1)LiNi Co Mn O 中的Co元素为+3价,Ni2+、Ni3+和Co3+个数比为3∶2∶2,则Mn元素化合价为
0.5 0.2 0.3 2
___________;Ni位于元素周期第___________周期,第___________族。
(2)“碱浸过滤”所得滤液的主要成分为___________。
(3)“还原焙烧”过程发生反应的化学方程式为___________。
(4)“碳化水浸”过程中反应为:LiCO(s)+CO(g)+HO(l)=2LiHCO (aq),该反应的标准吉布斯自由能
2 3 2 2 3
(ΔGθ)和标准生成焓(ΔHθ)随温度变化如图。该过程需要控制在___________(填“a”“b”或c)进行,其原因
是___________。
a.40 ℃~55 ℃ b.60 ℃~70 ℃ c.80 ℃~90 ℃
(5)常温下,为寻找“碳化水浸”的最佳pH,将37 g LiCO 固体加入1 L水中,通入CO 使固体逐步溶
2 3 2
解,当LiCO 固体恰好完全溶解时,2c(CO )+c(HCO )≈1.0 mol·L-1,则溶液中的c(H+)为
2 3
___________mol·L-1(保留两位有效数字,忽略体积变化)。
已知:K (Li CO)=2.5×10-2,K (H CO)=4.3×10-7,K (H CO)=5.6× 10-11
sp 2 3 a1 2 3 a2 2 3
(6)“萃取”的原理是2HR+M2+ 2H++RM(M2+代表金属离子,HR代表萃取剂,则反萃取时加入
的试剂为___________。
17. 常用作脱硝催化剂,采用共沉淀法等比掺入金属 后,催化剂 的脱硝性
能及抗硫中毒性能会发生改变。烟气脱硝主要副产物为 ,主反应如下:
反应I: ;
反应II:
第9页/共12页
学科网(北京)股份有限公司(1)已知: 。则 ___________。
(2)某条件下对于反应I, , ,k 、k 为速率常数。
正 逆
升高温度时,k 增大m倍,k 增大n倍,则m___________ n(填“>”“<”或“=”)。
正 逆
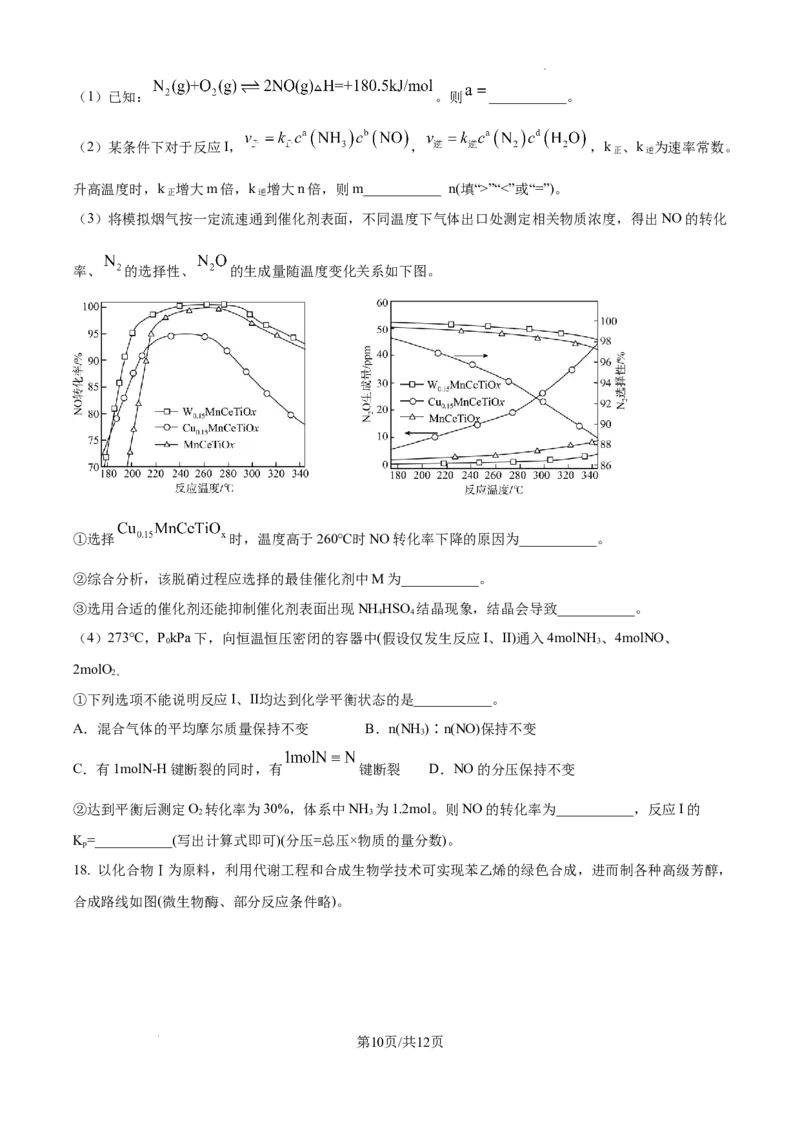
(3)将模拟烟气按一定流速通到催化剂表面,不同温度下气体出口处测定相关物质浓度,得出NO的转化
率、 的选择性、 的生成量随温度变化关系如下图。
①选择 时,温度高于260℃时NO转化率下降的原因为___________。
②综合分析,该脱硝过程应选择的最佳催化剂中M为___________。
③选用合适的催化剂还能抑制催化剂表面出现NH HSO 结晶现象,结晶会导致___________。
4 4
(4)273℃,PkPa下,向恒温恒压密闭的容器中(假设仅发生反应I、II)通入4molNH 、4molNO、
0 3
2molO
2。
①下列选项不能说明反应I、Ⅱ均达到化学平衡状态的是___________。
A.混合气体的平均摩尔质量保持不变 B.n(NH )∶n(NO)保持不变
3
C.有1molN-H键断裂的同时,有 键断裂 D.NO的分压保持不变
②达到平衡后测定O 转化率为30%,体系中NH 为1.2mol。则NO的转化率为___________,反应I的
2 3
K=___________(写出计算式即可)(分压=总压×物质的量分数)。
p
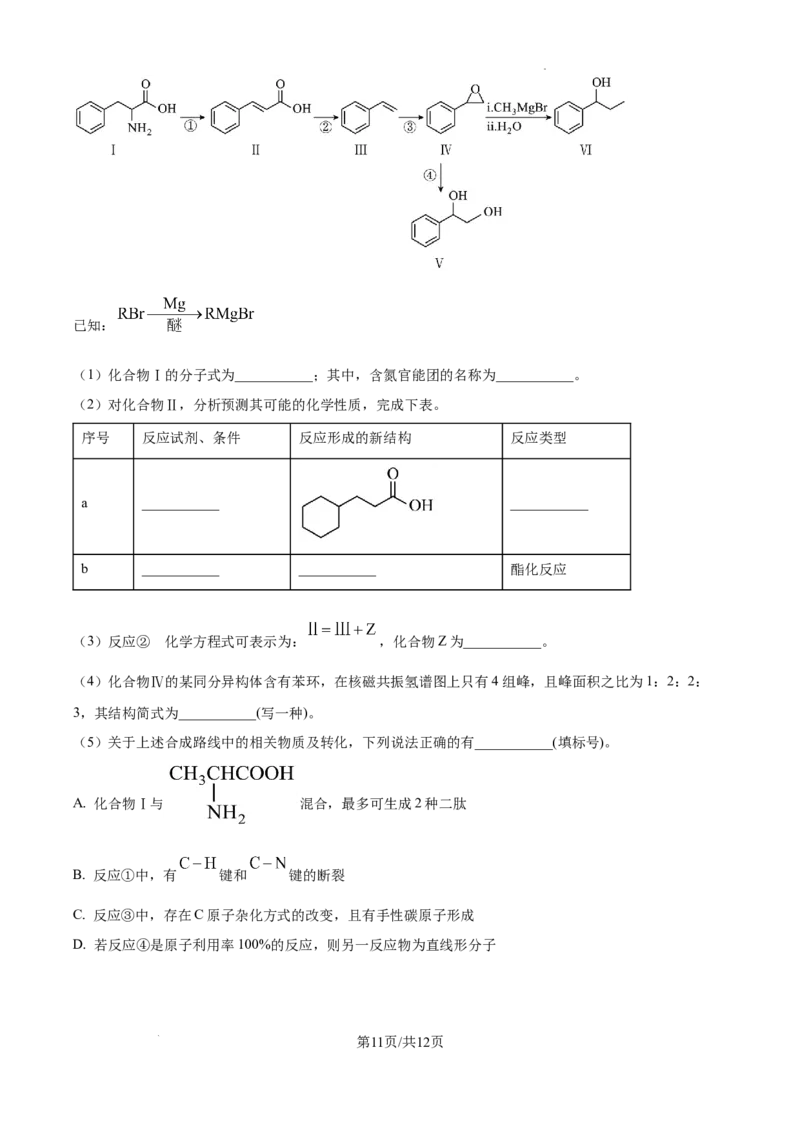
18. 以化合物Ⅰ为原料,利用代谢工程和合成生物学技术可实现苯乙烯的绿色合成,进而制各种高级芳醇,
合成路线如图(微生物酶、部分反应条件略)。
第10页/共12页
学科网(北京)股份有限公司已知:
(1)化合物Ⅰ的分子式为___________;其中,含氮官能团的名称为___________。
(2)对化合物Ⅱ,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a ___________ ___________
b ___________ ___________ 酯化反应
的
(3)反应② 化学方程式可表示为: ,化合物Z为___________。
(4)化合物Ⅳ的某同分异构体含有苯环,在核磁共振氢谱图上只有4组峰,且峰面积之比为1:2:2:
3,其结构简式为___________(写一种)。
(5)关于上述合成路线中的相关物质及转化,下列说法正确的有___________(填标号)。
A. 化合物Ⅰ与 混合,最多可生成2种二肽
B. 反应①中,有 键和 键的断裂
C. 反应③中,存在C原子杂化方式的改变,且有手性碳原子形成
D. 若反应④是原子利用率100%的反应,则另一反应物为直线形分子
第11页/共12页
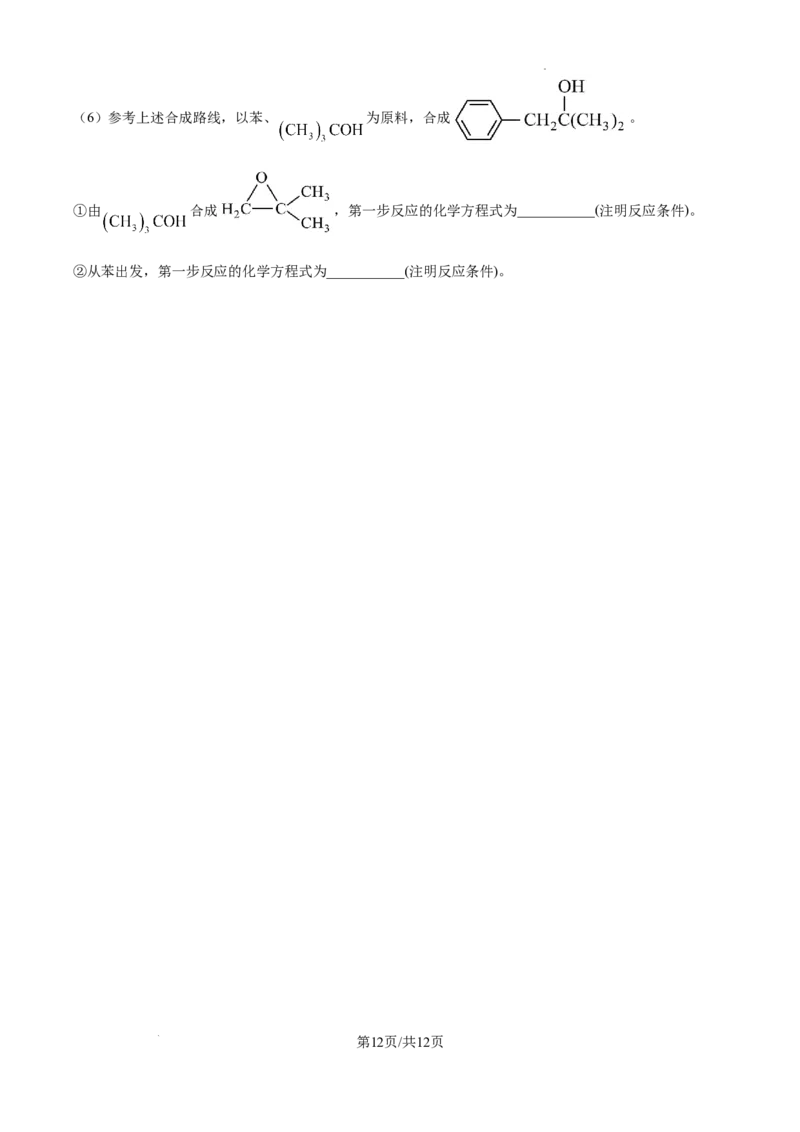
学科网(北京)股份有限公司(6)参考上述合成路线,以苯、 为原料,合成 。
①由 合成 ,第一步反应的化学方程式为___________(注明反应条件)。
②从苯出发,第一步反应的化学方程式为___________(注明反应条件)。
第12页/共12页
学科网(北京)股份有限公司