文档内容
专题54 化学平衡的建立与移动(B)
1.【2023年辽宁卷】某小组进行实验,向 蒸馏水中加入 ,充分振荡,溶液呈浅棕色,再加入
锌粒,溶液颜色加深;最终紫黑色晶体消失,溶液褪色。已知 为棕色,下列关于颜色变化
的解释错误的是
选项 颜色变化 解释
A 溶液呈浅棕色 在水中溶解度较小
B 溶液颜色加深 发生了反应:
C 紫黑色晶体消失 ( )的消耗使溶解平衡 右移
D 溶液褪色 与有色物质发生了置换反应
【答案】D
【解析】A.向10mL蒸馏水中加入0.4gI,充分振荡,溶液呈浅棕色,说明I 的浓度较小,因为I 在水中
2 2 2
溶解度较小,A项正确;B.已知 (aq)为棕色,加入0.2g锌粒后,Zn与I 反应生成ZnI,生成的I-与
2 2
I 2 发生反应I-+I 2⇌ ,生成 使溶液颜色加深,B项正确;C.I 2 在水中存在溶解平衡I 2 (s)⇌I 2 (aq),Zn
与I 反应生成的I-与I(aq)反应生成 ,I(aq)浓度减小,上述溶解平衡向右移动,紫黑色晶体消失,C
2 2 2
项正确;D.最终溶液褪色是Zn与有色物质发生了化合反应,不是置换反应,D项错误;答案选D。
2.【2022年天津卷】向恒温恒容密闭容器中通入2mol 和1mol ,反应
达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断错误的是
A. 的平衡浓度增大 B.反应平衡常数增大
C.正向反应速率增大 D. 的转化总量增大
【答案】B
【解析】A.平衡后,再通入一定量 ,平衡正向移动, 的平衡浓度增大,A正确;B.平衡常数是
与温度有关的常数,温度不变,平衡常数不变,B错误;C.通入一定量 ,反应物浓度增大,正向
反应速率增大,C正确;D.通入一定量 ,促进二氧化硫的转化, 的转化总量增大,D正确;
故选B。
3.(2021·北京真题)NO
2
和N
2
O
4
存在平衡:2NO
2
(g)⇌N
2
O
4
(g) △H<0。下列分析正确的是A.1 mol平衡混合气体中含1 mol N原子
B.断裂2 mol NO 中的共价键所需能量小于断裂1 mol N O 中的共价键所需能量
2 2 4
C.恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的
D.恒容时,水浴加热,由于平衡正向移动导致气体颜色变浅
【答案】B
【解析】A.1molNO 含有1molN原子,1molN O 含有2molN原子,现为可逆反应,为NO 和NO 的混
2 2 4 2 2 4
合气体,1 mol平衡混合气体中所含原子大于1 mol N,A项错误;B.反应2NO
2
(g)⇌N
2
O
4
(g)为放热反
应,故完全断开2molNO 分子中的共价键所吸收的热量比完全断开1molN O 分子中的共价键所吸收
2 2 4
的热量少,B项正确;C.气体体积压缩,颜色变深是因为体积减小,浓度变大引起的,C项错误;
D.放热反应,温度升高,平衡逆向移动,颜色加深,D项错误;答案选B。
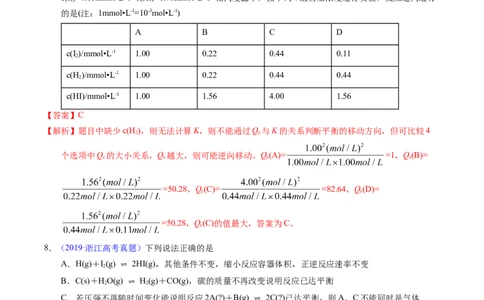
4.【2022年广东卷】恒容密闭容器中, 在不同温度下达平衡时,
各组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
【答案】C
【解析】A.从图示可以看出,平衡时升高温度,氢气的物质的量减少,则平衡正向移动,说明该反应的
正反应是吸热反应,即ΔH>0,故A错误; B.从图示可以看出,在恒容密闭容器中,随着温度升高
氢气的平衡时的物质的量减少,则平衡随着温度升高正向移动,水蒸气的物质的量增加,而a曲线表
示的是物质的量不随温度变化而变化,故B错误;C.容器体积固定,向容器中充入惰性气体,没有
改变各物质的浓度,平衡不移动,故C正确;D.BaSO 是固体,向平衡体系中加入BaSO,不能改
4 4
变其浓度,因此平衡不移动,氢气的转化率不变,故D错误;故选C。
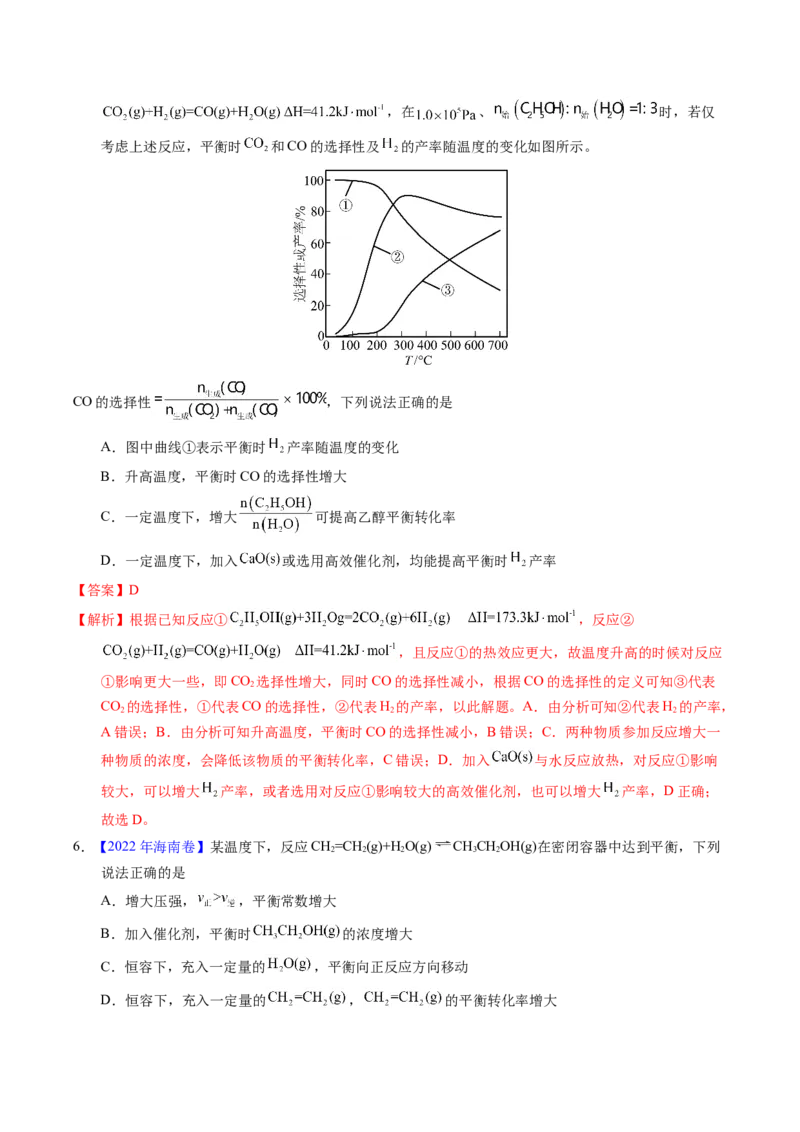
5.【2022年江苏卷】乙醇-水催化重整可获得 。其主要反应为
,,在 、 时,若仅
考虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】D
【解析】根据已知反应① ,反应②
,且反应①的热效应更大,故温度升高的时候对反应
①影响更大一些,即CO 选择性增大,同时CO的选择性减小,根据CO的选择性的定义可知③代表
2
CO 的选择性,①代表CO的选择性,②代表H 的产率,以此解题。A.由分析可知②代表H 的产率,
2 2 2
A错误;B.由分析可知升高温度,平衡时CO的选择性减小,B错误;C.两种物质参加反应增大一
种物质的浓度,会降低该物质的平衡转化率,C错误;D.加入 与水反应放热,对反应①影响
较大,可以增大 产率,或者选用对反应①影响较大的高效催化剂,也可以增大 产率,D正确;
故选D。
6.【2022年海南卷】某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,下列
2 2 2 3 2
说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大【答案】C
【解析】A.该反应是一个气体分子数减少的反应,增大压强可以加快化学反应速率,正反应速率增大的
幅度大于逆反应的,故v > v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A
正 逆
不正确;B.催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CHCHOH(g)的浓度,B
3 2
不正确;C.恒容下,充入一定量的HO(g),HO(g)的浓度增大,平衡向正反应方向移动,C正确;
2 2
D.恒容下,充入一定量的CH=CH (g),平衡向正反应方向移动,但是CH=CH (g)的平衡转化率减
2 2 2 2
小,D不正确;综上所述,本题选C。
7.(2020·北京高考真题)一定温度下,反应I
2
(g)+H
2
(g)⇌2Hl(g)在密闭容器中达到平衡时,测得
c(I )=0.11mmol•L-1,c(HI)=0.78mmol•L-1。相同度温下,按下列4组初始浓度进行实验,反应逆向进行
2
的是(注:1mmol•L-1=10-3mol•L-1)
A B C D
c(I )/mmol•L-1 1.00 0.22 0.44 0.11
2
c(H)/mmol•L-1 1.00 0.22 0.44 0.44
2
c(HI)/mmol•L-1 1.00 1.56 4.00 1.56
【答案】C
【解析】题目中缺少c(H),则无法计算K,则不能通过Q 与K的关系判断平衡的移动方向,但可比较4
2 c
个选项中Q 的大小关系,Q 越大,则可能逆向移动。Q(A)= =1,Q(B)=
c c c c
=50.28,Q(C)= =82.64,Q(D)=
c c
=50.28,Q(C)的值最大,答案为C。
c
8.(2019·浙江高考真题)下列说法正确的是
A.H(g)+I 2 (g) ⇌ 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
B.C(s)+H 2 O(g) ⇌ H 2 (g)+CO(g),碳的质量不再改变说明反应已达平衡
C.若压强不再随时间变化能说明反应2A(?)+B(g) ⇌ 2C(?)已达平衡,则A、C不能同时是气体
D.1 mol N 和3 mol H 反应达到平衡时H 转化率为10%,放出的热量为Q;在相同温度和压强下,
2 2 2 1
当2 mol NH 分解为N 和H 的转化率为10%时,吸收的热量为Q,Q 不等于Q
3 2 2 2 2 1
【答案】B
【解析】A.该可逆反应的反应前后气体计量数不发生变化,当缩小反应容器体积,相当于加压,正逆反
应速率同等程度增加,错误;B.在建立平衡前,碳的质量不断改变,达到平衡时,质量不变,因而
碳的质量不再改变说明反应已达平衡,正确;C.即使A,C物质均为气体,反应前后气体体积也会
发生变化,当压强不随时间变化时,仍能说明反应达到平衡,错误;D.易知N
2
(g)+3H
2
(g)⇌2NH
3
(g)
ΔH,合成氨气实际参与反应n(H )=3×10%=0.3mol,因而Q=0.3/3×|ΔH|=0.1|ΔH|,分解氨气时实际消
2 1耗的n(NH )=2×10%=0.2mol,Q=0.2/2×|ΔH|=0.1|ΔH|,则Q=Q ,错误。故答案选B。
3 2 1 2
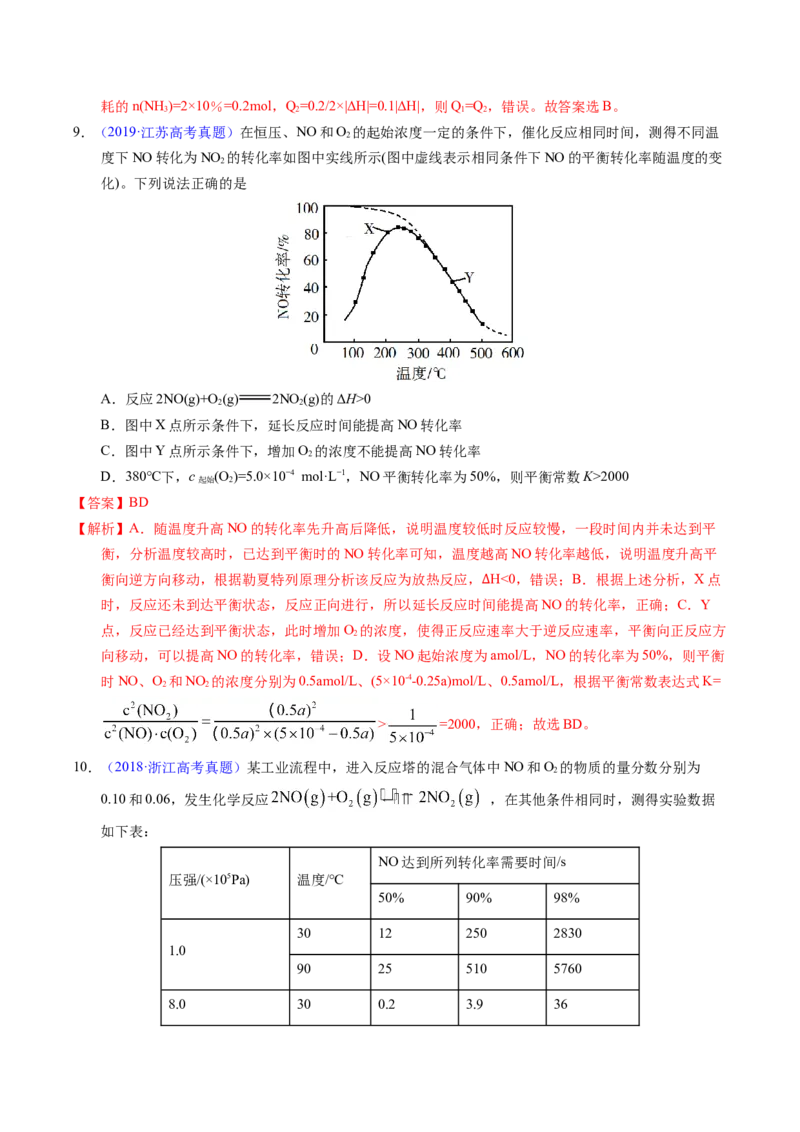
9.(2019·江苏高考真题)在恒压、NO和O 的起始浓度一定的条件下,催化反应相同时间,测得不同温
2
度下NO转化为NO 的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变
2
化)。下列说法正确的是
A.反应2NO(g)+O (g) 2NO (g)的ΔH>0
2 2
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O 的浓度不能提高NO转化率
2
D.380℃下,c (O )=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
起始 2
【答案】BD
【解析】A.随温度升高NO的转化率先升高后降低,说明温度较低时反应较慢,一段时间内并未达到平
衡,分析温度较高时,已达到平衡时的NO转化率可知,温度越高NO转化率越低,说明温度升高平
衡向逆方向移动,根据勒夏特列原理分析该反应为放热反应, H<0,错误;B.根据上述分析,X点
时,反应还未到达平衡状态,反应正向进行,所以延长反应时间能提高NO的转化率,正确;C.Y
∆
点,反应已经达到平衡状态,此时增加O 的浓度,使得正反应速率大于逆反应速率,平衡向正反应方
2
向移动,可以提高NO的转化率,错误;D.设NO起始浓度为amol/L,NO的转化率为50%,则平衡
时NO、O 和NO 的浓度分别为0.5amol/L、(5×10-4-0.25a)mol/L、0.5amol/L,根据平衡常数表达式K=
2 2
> =2000,正确;故选BD。
10.(2018·浙江高考真题)某工业流程中,进入反应塔的混合气体中NO和O 的物质的量分数分别为
2
0.10和0.06,发生化学反应 ,在其他条件相同时,测得实验数据
如下表:
NO达到所列转化率需要时间/s
压强/(×105Pa) 温度/℃
50% 90% 98%
30 12 250 2830
1.0
90 25 510 5760
8.0 30 0.2 3.9 3690 0.6 7.9 74
根据表中数据,下列说法正确的是
A.升高温度,反应速率加快
B.增大压强,反应速率变慢
C.在1.0×105Pa、90℃条件下,当转化率为98%时的反应已达到平衡
D.若进入反应塔的混合气体为amol,反应速率以v=Δn/Δt表示,则在8.0×105Pa、30℃条件下转化率
从50%增至90%时段NO的反应速率为4a/370mol/s
【答案】D
【解析】A.相同压强时,温度高时达到相同转化率需要的时间多,升高温度,反应速率越小,A错误;
B.相同温度,压强高时达到相同转化率需要的时间少,增大压强,反应速率变快,错误;C.在此条
件下,当转化率为98%时需要的时间较长,不确定反应是否达到了平衡,错误;D.在amol混合气体
进入反应塔,题目所示的外界环境下,NO的反应速率为v=∆n/∆t= =
mol/s,正确。综上所述,本题正确答案为D。
11.(2017·天津高考真题)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g) Ni(CO) (g)。230℃时,
4
该反应的平衡常数K=2×10−5。已知:Ni(CO) 的沸点为42.2℃,固体杂质不参与反应。
4
第一阶段:将粗镍与CO反应转化成气态Ni(CO) ;
4
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A.增加c(CO),平衡向正向移动,反应的平衡常数增大
B.第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C.第二阶段,Ni(CO) 分解率较低
4
D.该反应达到平衡时,v [Ni(CO) ]=4v (CO)
生成 4 生成
【答案】B
【解析】A.平衡常数只与温度有关,与浓度无关,错误;B.50℃时,Ni(CO) 以气态存在,有利于分离,
4
从而促使平衡正向移动,正确;C.230℃时,Ni(CO) 分解的平衡常数K =1/K =1/(2×10−5)
4 逆 正
=5×104,可知分解率较高,错误; D.平衡时,应该是4v [Ni(CO) ]=v (CO),错误;正确答案:
生成 4 生成
B
12.(2015·福建高考真题)在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列
判断不正确的是A.a=6.00
B.同时改变反应温度和蔗糖的浓度,v可能不变
C.b<318.2
D.不同温度时,蔗糖浓度减少一半所需的时间相同
【答案】D
【解析】A.根据表格的数据可知:温度不变时,蔗糖的浓度越大,水解的速率越快。根据浓度与速率的
变化关系可知:在328.2T时,蔗糖的浓度每减小0.100mol/L,水解速率减小1.50mmol/(L∙min),所以
在温度是328.2T、浓度是0.400mol/L时,水解的速率是a=7.50-1.50=6.00 mmol/(L∙min),A正确;B.
根据表格数据可知:升高温度,水解速率增大,增大浓度,水解速率也增大,若同时改变反应物的浓
度和反应的温度,则二者对水解反应速率的影响因素可能相互抵消,使反应速率可能不发生改变,B
正确;C.在物质的浓度不变时,升高温度,水解速率增大,降低温度,水解速率减小。由于在物质
的浓度是0.600mol/L时,温度是318.2T时水解速率是3.60mmol/(L∙min),现在该反应的速率是2.16
mmol/(L∙min)<3.60 mmol/(L∙min),说明反应温度低于318.2 T。即b<318.2,C正确;D.不同温度时,
蔗糖浓度减少,所以速率减慢,但是温度不同,在相同的浓度时的反应速率不相同,D错误;故答案
选D。
13.(2018·江苏高考真题)一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生
反应2SO2(g)+ O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
A.v< v,c< 2c B.K> K ,p> 2p
1 2 2 1 1 3 2 3
C.v< v,α (SO ) >α (SO ) D.c> 2c ,α (SO )+α (SO )<1
1 3 1 2 3 2 2 3 2 3 3 2
【答案】CD
【解析】对比容器的特点,将容器1和容器2对比,将容器1和容器3对比。容器2中加入4molSO 等效
3于在相同条件下反应物投入量为4molSO 和2molO ,容器2中起始反应物物质的量为容器1的两倍,
2 2
容器2相当于在容器1达平衡后增大压强,将容器的体积缩小为原来的一半,增大压强化学反应速率
加快,υ υ,增大压强平衡向正反应方向移动,平衡时c 2c,p 2p,α (SO )+α (SO ) 1,
2 1 2 1 2 1 1 2 2 3
容器1和容器2温度相同,K=K ;容器3相当于在容器1达到平衡后升高温度,升高温度化学反应速
1 2
率加快,υ υ,升高温度平衡向逆反应方向移动,平衡时c c,p p,α (SO ) α (SO ),K
3 1 3 1 3 1 3 2 1 2 3
K。据此分析解答。根据上述分析,A.υ υ,c 2c,错误;B.K K,p 2p,p p,则p
1 2 1 2 1 3 1 2 1 3 1 2
2p,错误;C.υ υ,α (SO ) α (SO ),正确;D.c 2c,c c,则c 2c,α
3 3 1 3 2 1 2 2 1 3 1 2 3 1
(SO )+α (SO ) 1,α (SO ) α (SO ),则α (SO )+α (SO ) 1,正确;答案选CD。
2 2 3 3 2 1 2 2 3 3 2
14.(2009·北京高考真题)已知H(g)+I (g) 2HI(g)∆H<0,有相同容积的定容密封容器甲和乙,甲中
2 2
加入H 和I(g)各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓
2 2
度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度 B.甲中加入0.1mol He,乙不改变
C.甲降低温度,乙不变 D.甲增加0.1molH,乙增加0.1mol I
2 2
【答案】C
【解析】在相同温度、相同容积下,甲、乙容器中达平衡时是完全全等的等效平衡;A.甲、乙提高相同
温度时,平衡均向逆反应方向移动,且达平衡时二者仍等效,HI浓度仍相等,A不选;B.加入稀有
气体时,由于各物质浓度不变,平衡不移动,二者HI浓度仍相等,B不选;C.甲降低温度平衡向着
正反应方向移动,达平衡时HI浓度增大,而乙中HI浓度不变,C选;D.根据反应的特点,甲中增
加0.1molH,乙中增加0.1molI ,平衡都正向移动,达平衡时HI浓度仍相等,D不选;答案选C。
2 2
15.(2013·上海高考真题)某恒温密闭容器中,可逆反应A(s) B+C(g)-Q达到平衡。缩小容器体积,
重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A ﹕n(C) =1﹕1
)消耗 消耗
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q
【答案】BC
【解析】A.若B是气体,平衡常数K=c(B)·c(C),若c(C) 不变,则c(B)也不变,可得K不变、若B是非
气体,平衡常数K=c(C),此时C(g)的浓度不变,因此A错误;B.根据平衡时的v(正)=v(逆)可
知B正确(注意:不是浓度消耗相等);C.若B是气体,平衡时加入B,平衡向逆向移动,正确;
D.由于反应是可逆反应,因此达到平衡时放出热量小于Q,错误;故选BC。
16.(2008·全国高考真题)在相同温度和压强下,对反应CO(g)+H(g) CO(g)+HO(g)进行甲、乙、
2 2 2
丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO H CO HO
2 2 2甲 amol amol 0mol 0mol
乙 2amol amol 0mol 0mol
丙 0mol 0mol amol amol
丁 amol 0mol amol amol
上述四种情况达到平衡后,n(CO)的大小顺序是
A.乙=丁>丙=甲 B.乙>丁>甲>丙
C.丁>乙>丙=甲 D.丁>丙>乙>甲
【答案】A
【解析】
假设丙、丁中的CO、HO(g)全部转化为CO、H,再与甲、乙比较:
2 2 2
CO(g)+H (g) CO(g)+H O(g)
2 2 2
丙开始时 0mol 0mol anol anol
丙假设全转化 anol anol 0mol 0mol
丁开始时 amol 0mol amol amol
丁假设全转化 2amol amol 0mol 0mol
通过比较,甲、丙的数值一样,乙、丁的数值一样,则说明甲和丙属于等效平衡,乙和丁为等效平衡,因
为乙或丁相当于比甲多加入二氧化碳,则增大反应物的量,平衡正向移动,则生成一氧化碳的物质的
量比甲多,故选A。
17.(2016·江苏高考真题)一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H(g)+CO(g)
2
CHOH(g) 达到平衡。下列说法正确的是( )
3
A.该反应的正反应放热
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C.达到平衡时,容器Ⅱ中c(H)大于容器Ⅲ中c(H)的两倍
2 2
D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
【答案】D
【解析】A.对比Ⅰ、Ⅲ,如温度相同,0.1mol/L的CHOH相当于0.20mol/L的H 和0.1mol/L的CO,为
3 2
等效平衡,但Ⅲ温度较高,平衡时CHOH较低,说明升高温度平衡逆向移动,正反应为放热反应,
3
错误;B.对比Ⅰ、Ⅱ,在相同温度下反应,但Ⅱ浓度较大,由方程式2H
2
(g)+CO(g)⇌CH
3
OH(g)可知,增大浓度,平衡正向移动,该反应正向为体积减小的反应,增大浓度转化率会增大,则容器Ⅰ中反应
物转化率比容器Ⅱ中的小,错误;C.Ⅱ浓度较大,Ⅲ温度较高,增大浓度平衡正向移动,升高温度
平衡逆向移动,Ⅲ的转化率降低,Ⅲ中相当于起始C(H)为Ⅱ的一半,平衡时Ⅱ中C(H)小于Ⅲ中的两
2 2
倍,错误;D.对比Ⅰ、Ⅲ,Ⅲ温度较高,浓度相当,升高温度,反应速率增大,正确;故选D。
18.(2014·江苏高考真题)一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CHOH(g)
3
CHOCH (g)+HO(g)
3 3 2
起始物质的量(mol) 平衡物质的量(mol)
容器编号 温度(℃)
CHOH(g) CHOCH (g) HO(g)
3 3 3 2
I 387 0.20 0.080 0.080
Ⅱ 387 0.40
Ⅲ 207 0.20 0.090 0.090
下列说法正确的是
A.该反应的正方应为吸热反应
B.达到平衡时,容器I中的CHOH体积分数比容器Ⅱ中的小
3
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CHOH 0.1mol、CHOCH 0.15mol和HO 0.10mol,则反应将向正反应方
3 3 3 2
向进行
【答案】D
【解析】A、容器I与容器Ⅲ相比甲醇的起始物质的量相等,但温度不同,温度较低时生成物的物质的量
多,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应,A错误;B、反应前后体积不
变,因此容器Ⅱ与容器I相比平衡等效,因此达到平衡时,容器I中的CHOH体积分数和容器Ⅱ中的
3
相等, B不正确;C、容器I中温度高,反应速率快,因此容器I中反应达到平衡所需时间比容器Ⅲ
中的少,C不正确;D、根据容器I表中数据可知,平衡时生成物的浓度均是0.080mol/L,则根据反应
的化学方程式可知消耗甲醇的浓度是0.16mol/L,所以平衡时甲醇的浓度是0.04mol/L,所以该温度下
的平衡常数K= =4。若起始时向容器I中充入CHOH 0.1mol、CHOCH 0.15mol和
3 3 3
HO 0.10mol,则此时 =1.5<4,所以反应将向正反应方向进行,D正确,答案选D。
2
19.(2007·江苏高考真题)一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);△H>0。现将1molA和
2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,
t 时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
1A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙
中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C
的体积分数的2倍
D.保持温度和乙中的压强不变,t 时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情
2
况分别如图2和图3所示(t 前的反应速率变化已省略)
1
【答案】D
【解析】根据等效平衡分析,4molC和2molD相当于2molA和4molB,但是乙容器的容积是甲的2倍,即
物质的量浓度相同,所以在相同条件下达到相同平衡状态,A.保持温度和活塞位置不变,在甲中再
加入1molA和2molB,相当于增大压强,平衡向逆反应反向移动,达到平衡时甲中C的浓度小于原来
的2倍,甲中C的浓度小于乙中C的浓度的2倍,错误;B.保持活塞位置不变,升高温度,平衡向
逆反应方向移动,甲、乙中B的体积分数都增大,错误;C.保持温度不变,移动活塞P,使乙的容
积和甲相等,相当于增大乙的压强,平衡向逆反应方向移动,减小甲的压强平衡向正反应方向移动,
达到新的平衡后,乙中C的体积分数小于甲中C的体积分数的2倍,错误;D.甲中温度和体积不变
充入稀有气体,没有改变气体的浓度,对反应速率没有影响,可以用图2表示,乙中温度和压强不变,
充入稀有气体,相当于增大容器体积,气体浓度减小,反应速率减小,生成物的浓度减小的程度大些,
化学平衡正向移动,可以用图3表示,正确,答案选D。
20.(2012·天津高考真题)已知2SO (g) + O(g) 2SO (g);ΔH=-197 kJ·mol-1。向同温、同体积的三
2 2 3
个密闭容器中分别充入气体:(甲) 2 mol SO 和1 mol O ;(乙) 1 mol SO 和0.5 mol O;(丙) 2 mol
2 2 2 2
SO 。恒温、恒容下反应达平衡时,下列关系一定正确的是
3
A.容器内压强P:P =P > 2P
甲 丙 乙
B.SO 的质量m:m =m > 2m
3 甲 丙 乙
C.c(SO )与c(O)之比k:k =k > k
2 2 甲 丙 乙
D.反应放出或吸收热量的数值Q:Q =Q > 2Q
甲 丙 乙
【答案】B
【解析】由给的数据利用归一法可知甲和丙是等效平衡。A.如果平衡不移动,p =p =2p ,但乙加入的
甲 丙 乙
物质的量是甲、丙的一半,恒容下相当于减压,平衡左移,压强变大,所以应该是p =p <2p ,错
甲 丙 乙
误;B.根据分析,平衡左移,三氧化硫的量减少,所以m =m >2m ,正确;C.加入的量均为
甲 丙 乙
2∶1,反应的量为2∶1,三者剩余的量也一定相等,为2∶1,c(SO )与c(O)之比k不变,所以k =k
2 2 甲
=k ,错误;D.因为甲和丙是在不同的方向建立起的等效平衡,若转化率均为50%时,反应热的数
丙 乙值应相等,但该反应的转化率不一定是50%,所以Q 和Q 不一定相等,项错。答案选B。
甲 丙
21.(2011·四川高考真题)可逆反应1X(g)+2Y(g) 2Z(g) 、2M(g) N(g)+P(g)分别在密闭容器
的两个反应室中进行,反应室之间有无摩擦,可滑动的密封隔板。反应开始和达到平衡状态时有关物
理量的变化如图所示:
下列判断正确的是:
A.反应1的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(I)时,X的转化率为
D.在平衡(I)和平衡(II)中,M的体积分数相等
【答案】B
【解析】A.降温由平衡(I)向平衡(II)移动,同时X、Y、Z的物质的量减少,说明平衡向右移动,正反应
放热,错误。B.达平衡(I)时的压强于开始时的体系的压强之比为:2.8:3=14:15,正确;C.达平衡(I)
时,反应①的总物质的量由3.0 mol减小为2.8 mol,X(g)+2Y(g)⇌⇌2Z(g)该反应正反应气体总量减小,
设反应的X的物质的量为△n(X),利用差量可得:1:1=△n(X):(3.0-2.8),解之得:
△n(X)=0.2mol,则X的转化率为 ×100%=20%,错误;D.由平衡(I)到平衡(II),由于反应过
程温度降低,化学反应②发生移动,M的量发生变化,M体积分数是不会相等的,错误;故答案:
B。
22.【2022年海南卷】某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应:
回答问题:
(1)已知:电解液态水制备 ,电解反应的 。由此计算 的燃烧热(焓)
_______ 。
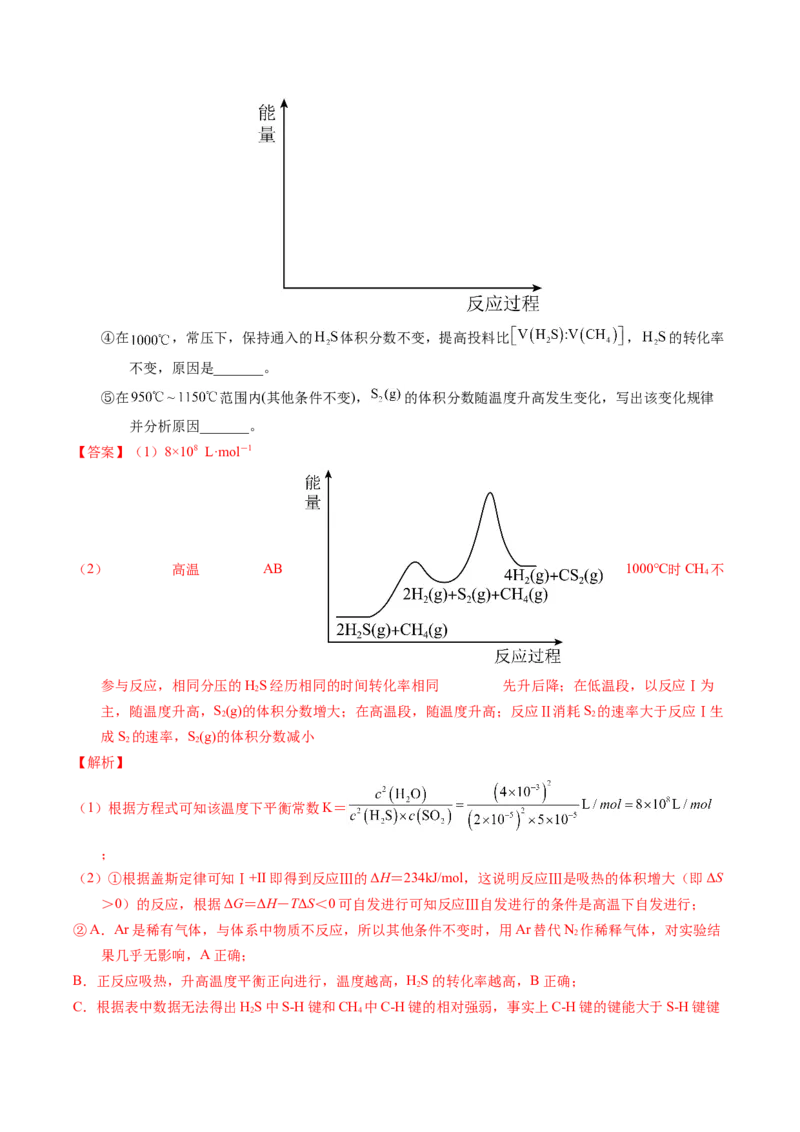
(2)已知: 的平衡常数(K)与反应温度(t)之间的关系如图1所示。①若反应为基元反应,且反应的 与活化能(Ea)的关系为 。补充完成该反应过程的能量变化
示意图(图2)_______。
②某研究小组模拟该反应,温度t下,向容积为10L的抽空的密闭容器中通入 和 ,
反应平衡后测得容器中 。则 的转化率为_______,反应温度t约为_______℃。
(3)在相同条件下, 与 还会发生不利于氧循环的副反应:
,在反应器中按 通入反应物,在不同温
度、不同催化剂条件下,反应进行到2min时,测得反应器中 、 浓度( )如下表所
示。
t=350℃ t=400℃
催化剂催化剂
10.8 12722 345.2 42780
Ⅰ
催化剂
9.2 10775 34 38932
Ⅱ
在选择使用催化剂Ⅰ和350℃条件下反应, 生成 的平均反应速率为___ ;
若某空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃的反应条件,原因是_______。
【答案】(1)-286
(2) 50%或0.5 660.2(或660.1或660.3,
其他答案酌情给分)
(3) 5.4 相同催化剂,400℃的反应速率更快,相同温度,催化剂Ⅱ副产物浓度低,甲烷与甲
醇比例高
【解析】
(1)电解液态水制备 ,电解反应的 ,由此可以判断,2mol 完全燃烧消
耗 ,生成液态水的同时放出的热量为572kJ ,故1mol 完全燃烧生成液态水放出的热
量为286kJ,因此, 的燃烧热(焓) -286 。
(2)①由 的平衡常数(K)与反应温度(t)之间的关系图可知,K随
着温度升高而减小,故该反应为放热反应。若反应为基元反应,则反应为一步完成,由于反应的
与活化能(Ea)的关系为 ,由图2信息可知 =a ,则 a ,该反应为放
热反应,生成物的总能量小于反应物的,因此该反应过程的能量变化示意图为:。
②温度t下,向容积为10L的抽空的密闭容器中通入 和 ,反应平衡后测得容器中
,则 的转化率为 ,根据C元素守恒可知, 的平衡量为
, 和 是按化学计量数之比投料的,则 的平衡量为 , 的平衡量是
的2倍,则 , 的平衡浓度分别为
、 、 、 ,则该反应的平衡常数K=
,根据图1中的信息可知,反应温度t约为660.2℃。
(3)在选择使用催化剂Ⅰ和350℃条件下反应,由表中信息可知, 的浓度由0增加到10.8
,因此, 生成 的平均反应速率为 ;由表中信
息可知,在选择使用催化剂Ⅰ和350℃条件下反应, 的浓度由0增加到10.8
,, : =12722:10.8 1178;在选择使用催化剂Ⅱ和350℃的反应条件下,
的浓度由0增加到9.2 , : =10775:9.2 1171;在选择使用催化剂Ⅰ
和400℃条件下反应, 的浓度由0增加到345.2 , : =
42780:345.2 124;在选择使用催化剂Ⅱ和400℃的反应条件下, 的浓度由0增加到34
, : =38932:34 1145。因此,若某空间站的生命保障系统实际选择使用催
化剂Ⅱ和400℃的反应条件的原因是:相同催化剂,400℃的反应速率更快,相同温度,催化剂Ⅱ副产
物浓度低,甲烷与甲醇比例高。
23.【2022年6月浙江卷】主要成分为 的工业废气的回收利用有重要意义。
(1)回收单质硫。将三分之一的 燃烧,产生的 与其余 混合后反应:。在某温度下达到平衡,测得密闭系统中各组分浓度分别为
、 、 ,计算该温度下的平衡
常数 _______。
(2)热解 制 。根据文献,将 和 的混合气体导入石英管反应器热解(一边进料,另一边出
料),发生如下反应:
Ⅰ
Ⅱ
总反应:
Ⅲ
投料按体积之比 ,并用 稀释;常压,不同温度下反应相同时间后,测得 和
体积分数如下表:
105
温度/ 950 1000 1100 1150
0.5 1.5 3.6 5.5 8.5
0.0 0.0 0.1 0.4 1.8
请回答:
①反应Ⅲ能自发进行的条件是_______。
②下列说法正确的是_______。
A.其他条件不变时,用Ar替代 作稀释气体,对实验结果几乎无影响
B.其他条件不变时,温度越高, 的转化率越高
C.由实验数据推出 中的 键强于 中的 键
D.恒温恒压下,增加 的体积分数, 的浓度升高
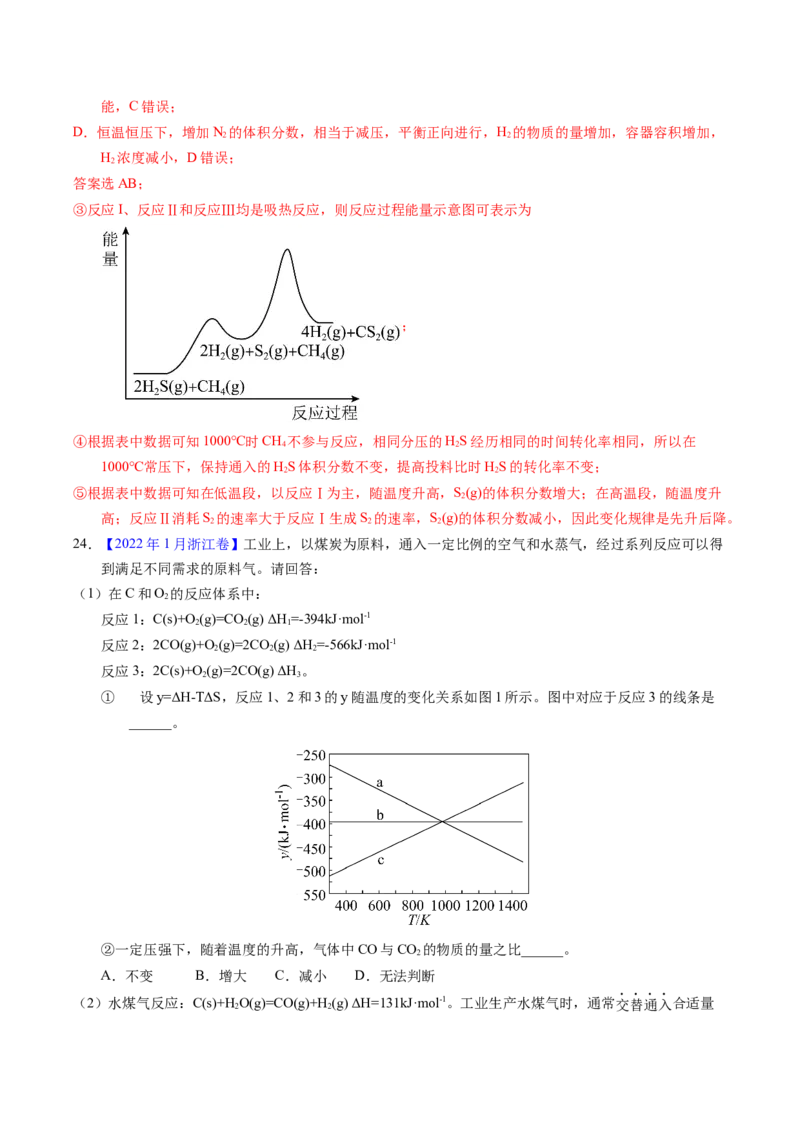
③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过程能量示意
图_______。④在 ,常压下,保持通入的 体积分数不变,提高投料比 , 的转化率
不变,原因是_______。
⑤在 范围内(其他条件不变), 的体积分数随温度升高发生变化,写出该变化规律
并分析原因_______。
【答案】(1)8×108 L·mol-1
(2) 高温 AB 1000℃时CH 不
4
参与反应,相同分压的HS经历相同的时间转化率相同 先升后降;在低温段,以反应Ⅰ为
2
主,随温度升高,S(g)的体积分数增大;在高温段,随温度升高;反应Ⅱ消耗S 的速率大于反应Ⅰ生
2 2
成S 的速率,S(g)的体积分数减小
2 2
【解析】
(1)根据方程式可知该温度下平衡常数K=
;
(2)①根据盖斯定律可知Ⅰ+Ⅱ即得到反应Ⅲ的ΔH=234kJ/mol,这说明反应Ⅲ是吸热的体积增大(即ΔS
>0)的反应,根据ΔG=ΔH-TΔS<0可自发进行可知反应Ⅲ自发进行的条件是高温下自发进行;
②A.Ar是稀有气体,与体系中物质不反应,所以其他条件不变时,用Ar替代N 作稀释气体,对实验结
2
果几乎无影响,A正确;
B.正反应吸热,升高温度平衡正向进行,温度越高,HS的转化率越高,B正确;
2
C.根据表中数据无法得出HS中S-H键和CH 中C-H键的相对强弱,事实上C-H键的键能大于S-H键键
2 4能,C错误;
D.恒温恒压下,增加N 的体积分数,相当于减压,平衡正向进行,H 的物质的量增加,容器容积增加,
2 2
H 浓度减小,D错误;
2
答案选AB;
③反应I、反应Ⅱ和反应Ⅲ均是吸热反应,则反应过程能量示意图可表示为
;
④根据表中数据可知1000℃时CH 不参与反应,相同分压的HS经历相同的时间转化率相同,所以在
4 2
1000℃常压下,保持通入的HS体积分数不变,提高投料比时HS的转化率不变;
2 2
⑤根据表中数据可知在低温段,以反应Ⅰ为主,随温度升高,S(g)的体积分数增大;在高温段,随温度升
2
高;反应Ⅱ消耗S 的速率大于反应Ⅰ生成S 的速率,S(g)的体积分数减小,因此变化规律是先升后降。
2 2 2
24.【2022年1月浙江卷】工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得
到满足不同需求的原料气。请回答:
(1)在C和O 的反应体系中:
2
反应1:C(s)+O(g)=CO (g) ΔH =-394kJ·mol-1
2 2 1
反应2:2CO(g)+O(g)=2CO (g) ΔH =-566kJ·mol-1
2 2 2
反应3:2C(s)+O(g)=2CO(g) ΔH 。
2 3
① 设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是
______。
②一定压强下,随着温度的升高,气体中CO与CO 的物质的量之比______。
2
A.不变 B.增大 C.减小 D.无法判断
(2)水煤气反应:C(s)+HO(g)=CO(g)+H (g) ΔH=131kJ·mol-1。工业生产水煤气时,通常交替通入合适量
2 2的空气和水蒸气与煤炭反应,其理由是________。
(3)一氧化碳变换反应:CO(g)+HO(g)=CO(g)+H(g) ΔH=-41kJ·mol-1。
2 2 2
①一定温度下,反应后测得各组分的平衡压强(即组分的物质的量分数×总压):p(CO)=0.25MPA.
p(H O)=0.25MPA.p(CO)=0.75MPa和p(H )=0.75MPa,则反应的平衡常数K的数值为________。
2 2 2
②维持与题①相同的温度和总压,提高水蒸气的比例,使CO的平衡转化率提高到90%,则原料气中
水蒸气和CO的物质的量之比为________。
③生产过程中,为了提高变换反应的速率,下列措施中合适的是________。
A.反应温度愈高愈好 B.适当提高反应物压强
C.选择合适的催化剂 D.通入一定量的氮气
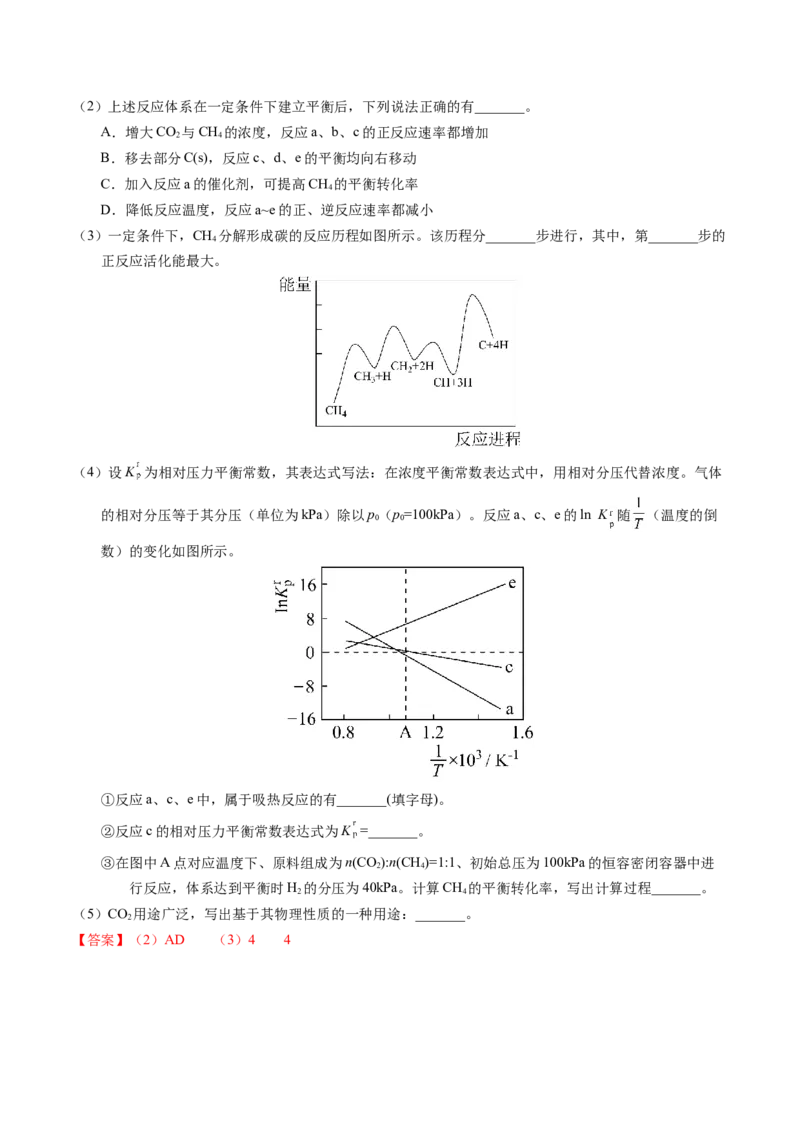
④以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,能量-反应过
程如图2所示。
用两个化学方程式表示该催化反应历程(反应机理):步骤Ⅰ:________;步骤Ⅱ:________。
【答案】(1) a B
(2)水蒸气与煤炭反应吸热,氧气与煤炭反应放热,交替通入空气和水蒸气有利于维持体系热量平衡,
保持较高温度,有利于加快化学反应速率
(3) 9.0 1.8:1 BC M+HO=MO+H MO+CO=M+CO
2 2 2
【解析】
(1)①由已知方程式:(2×反应1-反应2)可得反应3,结合盖斯定律得:
,反应1前后气体分子数不变,升温y不变,对
应线条b,升温促进反应2平衡逆向移动,气体分子数增多,熵增,y值增大,对应线条c,升温促进
反应3平衡逆向移动,气体分子数减少,熵减, y值减小,对应线条a,故此处填a;
②温度升高,三个反应平衡均逆向移动,由于反应2焓变绝对值更大,故温度对其平衡移动影响程度大,
故CO 物质的量减小,CO物质的量增大,所以CO与CO 物质的量比值增大,故答案选B;
2 2
(2)由于水蒸气与煤炭反应吸热,会引起体系温度的下降,从而导致反应速率变慢,不利于反应的进行,
通入空气,利用煤炭与O 反应放热从而维持体系温度平衡,维持反应速率,故此处填:水蒸气与煤炭
2
反应吸热,氧气与煤炭反应放热,交替通入空气和水蒸气有利于维持体系热量平衡,保持较高温度,
有利于加快反应速率;
(3)①该反应平衡常数K= ;
②假设原料气中水蒸气为x mol,CO为1 mol,由题意列三段式如下:,则平衡常数K= ,解得x=1.8,故水蒸气
与CO物质的量之比为1.8:1;
③A.反应温度过高,会引起催化剂失活,导致反应速率变慢,A不符合题意;
B.适当增大压强,可加快反应速率,B符合题意;
C.选择合适的催化剂有利于加快反应速率,C符合题意;
D.若为恒容条件,通入氮气对反应速率无影响,若为恒压条件,通入氮气后,容器体积变大,反应物浓
度减小,反应速率变慢,D不符合题意;
故答案选BC;
④水分子首先被催化剂吸附,根据元素守恒推测第一步产生H,第二步吸附CO产生CO,对应反应历程
2 2
依次为:M+HO=MO+H 、MO+CO=M+CO 。
2 2 2
25.(2013·江苏高考真题)一定条件下存在反应:CO(g)+HO(g) CO(g)+H(g),其正反应放热。现
2 2 2
有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和
1molH O,在II中充入1molCO 和1mol H,在III中充入2molCO和2molH O,700℃条件下开始反应。
2 2 2 2
达到平衡时,下列说法正确的是
A.容器I、II中正反应速率相同
B.容器I、III中反应的平衡常数相同
C.容器I中CO的物质的量比容器II中的多
D.容器I中CO的转化率与容器II中CO 的转化率之和等于1
2
【答案】C
【解析】A.容器I中反应正向进行,反应放热温度升高,容器II中反应逆向进行,反应吸热温度降低,
所以容器I中正反应速率大于II中正反应速率,错误;B.容器III反应物是容器I中的2倍,容器III
放热多温度高,所以平衡常数不同,错误;C.容器I的温度比容器II高,升高温度平衡逆向移动,
容器I中CO的物质的量比容器II中的多,正确;D.若容器I、II在恒温、恒容的条件下进行,为等
效平衡,容器I中CO的转化率与容器II中CO 的转化率之和等于1,但反应在恒容绝热密闭容器中进
2
行,容器I中温度升高,平衡逆向移动,CO的转化率减小,容器II中温度降低,平衡正向移动,CO
2
的转化率减小,则容器I中CO的转化率与容器II中CO 的转化率之和小于1,错误;答案选C。
2
26.(2021·广东真题)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO
4 2 2
利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4
e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
A.增大CO 与CH 的浓度,反应a、b、c的正反应速率都增加
2 4
B.移去部分C(s),反应c、d、e的平衡均向右移动
C.加入反应a的催化剂,可提高CH 的平衡转化率
4
D.降低反应温度,反应a~e的正、逆反应速率都减小
(3)一定条件下,CH 分解形成碳的反应历程如图所示。该历程分_______步进行,其中,第_______步的
4
正反应活化能最大。
(4)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体
的相对分压等于其分压(单位为kPa)除以p(p=100kPa)。反应a、c、e的ln K 随 (温度的倒
0 0
数)的变化如图所示。
①反应a、c、e中,属于吸热反应的有_______(填字母)。
②反应c的相对压力平衡常数表达式为K =_______。
③在图中A点对应温度下、原料组成为n(CO):n(CH)=1:1、初始总压为100kPa的恒容密闭容器中进
2 4
行反应,体系达到平衡时H 的分压为40kPa。计算CH 的平衡转化率,写出计算过程_______。
2 4
(5)CO 用途广泛,写出基于其物理性质的一种用途:_______。
2
【答案】(2)AD (3)4 4(4)①ac ② ③68% (5)做冷冻剂
【解析】根据盖斯定律计算未知反应的反应热;根据影响化学反应速率和化学平衡的因素判断反应速率的
变化及转化率的变化;根据图像及曲线高低判断反应进程和活化能的相对大小;根据平衡时反应物的
分压计算平衡转化率;根据CO 的物理性质推测CO 的用途。
2 2
(2)A.增大CO 和CH 的浓度,对于反应a、b、c来说,均增大了反应物的浓度,反应的正反应速率增
2 4
大,A正确;
B.移去部分C(s),没有改变反应体系中的压强,反应的正逆反应速率均不变,平衡不移动,B错误;
C.催化剂可以同等条件下增大正逆反应速率,只能加快反应进程,不改变反应的平衡状态,平衡转化率
不变,C错误;
D.降低温度,体系的总能量降低,正、逆反应速率均减小,D正确;
故答案选AD;
(3)由图可知,反应过程中能量变化出现了4个峰,即吸收了4次活化能,经历了4步反应;且从左往右
看4次活化能吸收中,第4次对应的峰最高,即正反应方向第4步吸收的能量最多,对应的正反应活
化能最大。
(4)①随着温度的升高,反应a和c的ln K 增大,说明K 的数值增大,反应向正反应方向进行,反应a
和c为吸热反应,同理反应e的ln K 减小,说明K 的减小,反应向逆反应方向进行,反应e为放热
反应,故答案为ac;
②用相对分压代替浓度,则反应c的平衡常数表达式K = ;
③由图可知,A处对应反应c的ln K =0,即K = =1,解方程的p2(H )=p(CH),已知反应平衡时
2 4
p(H )=40kPa,则有p(CH)=16kPa,且初始状态时p(CH)= ×100kPa=50kPa,故CH 的平衡转化率为
2 4 4 4
×100%=68%;
(5)固态CO 即为干冰,干冰用于制冷或人工降雨均是利用其物理性质。
2
27.(2021.1·浙江真题)“氯碱工业”以电解饱和食盐水为基础制取氯气等产品, 氯气是实验室和工业上
的常用气体。请回答:
(3)在一定温度下,氯气溶于水的过程及其平衡常数为:
Cl
2
(g)⇌Cl
2
(aq) K
1
=c(Cl
2
)/pCl
2
(aq) + H
2
O(l)⇌H+ (aq)+Cl- (aq) + HClO(aq) K
2
其中p为Cl(g)的平衡压强,c(Cl )为Cl 在水溶液中的平衡浓度。
2 2 2
①Cl
2
(g)⇌Cl
2
(aq)的焓变ΔH
1
______0。(填”>”、“=”或“<”)
②平衡常数K 的表达式为K=______。
2 2
③氯气在水中的溶解度(以物质的量浓度表示)为c,则c=______。(用平衡压强p和上述平衡常数表示,
忽略HClO的电离)
(4)工业上,常采用“加碳氯化”的方法以高钛渣(主要成分为TiO)为原料生产TiCl ,相应的化学方程式为;
2 4
I.TiO
2
(s)+2Cl
2
(g)⇌TiCl
4
(g)+O
2
(g) ΔH
I
=181 mol·L-1,K
I
=-3.4×10-29
II.2C(s)+O
2
(g)⇌2CO(g) ΔH
II
= - 221 mol·L-1,K
II
=1.2×1048
结合数据说明氯化过程中加碳的理由______ 。
(5)在一定温度下,以I 为催化剂,氯苯和Cl 在CS 中发生平行反应,分别生成邻二氯苯和对二氯苯,
2 2 2
两产物浓度之比与反应时间无关。反应物起始浓度均为0.5 mol·L-1,反应30 min测得氯苯15%转化为
邻二氯苯,25%转化为对二氯苯。保持其他条件不变,若要提高产物中邻二氯苯的比例,可采用的措
施是______。
A.适当提高反应温度 B.改变催化剂
C.适当降低反应温度 D.改变反应物浓度
【答案】
(3)①< ② ③K p +
1
(4)反应I + II得: TiO(s)+2Cl (g) + 2C(s) =TiCl (g)+ 2CO(g),K=KK =4.1×1019远大于K,反应II使
2 2 4 I II 1
TiO 氯化为TiCl 得以实现;ΔH=ΔH+ΔH = -40kJ·mol-1,反应II 可为反应I提供所需的能量
2 4 I II
(5)AB
【解析】
(3)①Cl 2 (g) ⇌ Cl 2 (aq)表示的是氯气的溶解平衡,氯气在常温下可溶于水,该过程是自发的,由于该过
程的熵变小于0,因此,其焓变ΔH<0。
1
②由化学方程式Cl 2 (aq) + H 2 O(l) ⇌ H+ (aq)+Cl- (aq) + HClO(aq)可知,其平衡常数K 2 的表达式为K 2 =
,注意水为液态,其不出现在表达式中。
③Cl 2 (g) ⇌ Cl 2 (aq) 与Cl 2 (aq) + H 2 O(l) ⇌ H+ (aq)+Cl- (aq) + HClO(aq) 相加可以得到Cl 2 (g) + H 2 O(l) ⇌
H+ (aq)+Cl- (aq) + HClO(aq),因此,该反应的平衡常数为 ;氯气在水中的溶解度(以物质的量浓
度表示)为c,根据物料守恒可知,c= + c(HClO)+ c(Cl-),由于HCl是强电解质,若忽略
水的电离和次氯酸的电离,则 ,由K = 可知
2
= ,由K =c(Cl)/p可知, = ,则 = ,因此,
1 2c= K p + 。
1
(4)已知:I . TiO 2 (s)+2Cl 2 (g) ⇌ TiCl 4 (g)+O 2 (g) ΔH I =181 mol ·L-1,K I =-3.4 ×10-29;II. 2C(s)+O 2 (g) ⇌
2CO(g) ΔH = - 221 mol ·L-1,K =1.2×1048。根据盖斯定律可知,I + II得: TiO(s)+2Cl (g) + 2C(s)
II II 2 2
=TiCl (g)+ 2CO(g),则K=KK =4.1 ×1019远大于K ,反应II的发生可以减小反应I的平衡体系中氧气
4 I II 1
的浓度,从而使TiO 氯化为TiCl 得以实现;反应I为吸热反应,而ΔH=ΔH+ΔH = -40kJ·mol-1,说明
2 4 I II
TiO(s)+2Cl (g) + 2C(s) =TiCl (g)+ 2CO(g)为放热反应,则反应II 可为反应I提供所需的能量。
2 2 4
(5) 15%生成邻二氯苯,说明该反应活化能大,25%生成对二氯苯,说明该反应活化能小,温度改变对
活化能的影响大,即升高温度,邻二氯苯产量增大的多,比例增大;降低温度邻二氯苯产量减少的多,
比例减少,故A正确、C错误;选择合适的催化剂,降低生成邻二氯苯的反应的活化能,故B正确;
D中改变反应物的浓度,并不能改变两种产物的比例,故D错误,综上所述,选AB。
28.(2020·全国高考真题)天然气的主要成分为CH,一般还含有C H 等烃类,是重要的燃料和化工原
4 2 6
料。
(1)乙烷在一定条件可发生如下反应:C H(g)= C H(g)+H(g) ΔH,相关物质的燃烧热数据如下表所示:
2 6 2 4 2
物质 C H(g) C H(g) H(g)
2 6 2 4 2
燃烧热ΔH/( kJ·mol−1) -1560 -1411 -286
①ΔH=_________kJ·mol−1。
②提高该反应平衡转化率的方法有_________、_________。
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的
平衡常数K =_________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
p
(2)高温下,甲烷生成乙烷的反应如下:2CH C H+H 。反应在初期阶段的速率方程为:r=k×
4 2 6 2
,其中k为反应速率常数。
①设反应开始时的反应速率为r,甲烷的转化率为α时的反应速率为r,则r=_____ r。
1 2 2 1
②对于处于初期阶段的该反应,下列说法正确的是_________。
A.增加甲烷浓度,r增大 B.增加H 浓度,r增大
2
C.乙烷的生成速率逐渐增大 D.降低反应温度,k减小
【答案】(1)①137 ②升高温度 减小压强(增大体积) ③ (2)①1-α
② AD
【解析】
(1)①由表中燃烧热数值可知:
①C H(g)+ O(g)=2CO (g) +3H O(l) ∆H= -1560kJ∙mol-1;②C H(g)+3O(g)=2CO (g) +2H O(l) ∆H=
2 6 2 2 2 1 2 4 2 2 2 2
-1411kJ∙mol-1;③H(g)+ O(g)=HO(l) ∆H= -286kJ∙mol-1;根据盖斯定律可知,①-②-③得C H(g)
2 2 2 3 2 6=C H(g) + H(g),则∆H= ∆H-∆H-∆H=( -1560kJ∙mol-1)-( -1411kJ∙mol-1)- ( -286kJ∙mol-1)=137kJ∙mol-1,故
2 4 2 1 2 3
答案为137;
②反应C H(g) C H(g) + H(g)为气体体积增大的吸热反应,升高温度、减小压强平衡都向正反应方向
2 6 2 4 2
移动,故提高该反应平衡转化率的方法有升高温度、减小压强(增大体积);
③设起始时加入的乙烷和氢气各为1mol,列出三段式,
C H(g) C H(g) + H(g)
2 6 2 4 2
起始(mol) 1 0 1
转化(mol) α α
平衡(mol) 1- 1+
平衡时,C H、C H 和H 平衡分压分别为 p、 p和 p,则反应的平衡常数为K=
2 6 2 4 2 p
;
(2) ①根据r=k× ,若r= kc,甲烷转化率为 甲烷的浓度为c(1- ),则r= kc(1- ),所以
1 2
r=(1- )r;
2 1
②A.增大反应物浓度反应速率增大,故A说法正确;
B.由速率方程可知,初期阶段的反应速率与氢气浓度无关,故B说法错误;
C.反应物甲烷的浓度逐渐减小,结合速率方程可知,乙烷的生成速率逐渐减小,故C说法错误;
D.化学反应速率与温度有关,温度降低,反应速率常数减小,故D正确。
答案选AD。
29.(2016·全国高考真题)元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)−(绿色)、Cr O2−
4 2 7
(橙红色)、CrO2−(黄色)等形式存在,Cr(OH) 为难溶于水的灰蓝色固体,回答下列问题:
4 3
(1)Cr3+与Al3+的化学性质相似,在Cr (SO ) 溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是
2 4 3
_________。
(2)CrO2−和Cr O2−在溶液中可相互转化。室温下,初始浓度为1.0 mol·L−1的NaCrO 溶液中c
4 2 7 2 4
(Cr O2−)随c(H+)的变化如图所示。
2 7
①用离子方程式表示NaCrO 溶液中的转化反应____________。
2 4
②由图可知,溶液酸性增大,CrO2−的平衡转化率__________(填“增大“减小”或“不变”)。根
4
据A点数据,计算出该转化反应的平衡常数为__________。③升高温度,溶液中CrO2−的平衡转化率减小,则该反应的ΔH_________(填“大于”“小于”或
4
“等于”)。
【答案】(1)开始有灰蓝色固体生成,随后沉淀消失;
(2)①2CrO2-+2H+ Cr O2-+H O; ② 增大;1014;③< ;
4 2 7 2
【解析】
(1)Cr3+与Al3+的化学性质相似,可知Cr(OH) 是两性氢氧化物,能溶解在强碱NaOH溶液中。在Cr
3 2
(SO ) 溶液中逐滴加入NaOH溶液直至过量,首先发生反应产生Cr(OH) 灰蓝色固体,当碱过量
4 3 3
时,可观察到沉淀消失。故观察到的现象是开始有灰蓝色固体生成,随后沉淀消失。
(2)①随着H+浓度的增大,CrO2-转化为Cr O2-的离子反应式为2CrO2-+2H+ Cr O2-+H O。
4 2 7 4 2 7 2
②溶液酸性增大,平衡2CrO2-+2H+ Cr O2-+H O正向进行,CrO2−的平衡转化率增大;A点Cr O2-的
4 2 7 2 4 2 7
浓度为0.25mol/L,根据Cr元素守恒可知CrO2-的浓度为0.5mol/L;H+浓度为1×10-7mol/L;此时该转
4
化反应的平衡常数为 = =1014;③升高温度,溶液中CrO2−的平衡转化率减
4
小,平衡逆向移动,说明正方向放热,则该反应的ΔH<0;
30.(2017·浙江高考真题)(一) 十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C H )→四氢萘
10 18
(C H )→萘(C H)”的脱氢过程释放氢气。已知:
10 12 10 8
C H (l) C H (l)+3H(g) △H
10 18 10 12 2 1
C H (l) C H(l)+2H(g) △H
10 12 10 8 2 2
△H>△H>0;C H →C H 的活化能为Ea,C H →C H 的活化能为Ea,十氢萘的常压沸点为
1 2 10 18 10 12 1 10 12 10 8 2
192℃;在192℃,液态十氢萘的脱氢反应的平衡转化率约为9%。请回答:
(1)有利于提高上述反应平衡转化率的条件是_______________。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)研究表明,将适量十氢萘置于恒容密闭反应器中,升高温度带来高压,该条件下也可显著释氢,理
由是_____________________________________________________。
(3)温度335℃,在恒容密闭反应器中进行高压液态十氢萘(1.00 mol)催化脱氢实验,测得C H 和
10 12
C H 的产率x 和x(以物质的量分数计)随时间变化关系,如图1所示。
10 8 1 2
①在8 h时,反应体系内氢气的量为___________________mol(忽略其他副反应)。
②x 显著低于x 的原因是____________________________。
1 2③在图2中绘制“C H →C H →C H”的“能量~反应过程”示意图____。
10 18 10 12 10 8
【答案】(1)C (2) 温度升高,加快反应速率;温度升高使平衡正移的作用大于压强增大使平衡逆
移的作用。 (3)①1.95 ②催化剂显著降低了C H →C H 的活化能,反应生成的C H 快速
10 12 10 8 10 12
转化为C H ③
10 8
【解析】
Ⅰ.(1)C H (l) C H (l)+3H(g) △H,C H (l) C H(l)+2H(g) △H,△H>△H>0;均
10 18 10 12 2 1 10 12 10 8 2 2 1 2
为吸热反应,且都属于气体的物质的量增大的反应。
A.升高温度,平衡正向移动,平衡转化率增大,但增大压强,平衡逆向移动,平衡转化率减小,故A错
误;B.降低温度,平衡逆向移动,平衡转化率减小,故B错误;C.升高温度,平衡正向移动,平衡
转化率增大,减小压强,平衡正向移动,平衡转化率增大,故C正确;D.降低温度,平衡逆向移动,
平衡转化率减小,故D错误;故选C;
(2)总反应为该反应为吸热反应,升高温度,平衡正向移动,平衡转化率增大,平衡常数增大,当温度
达到192℃时,十氢萘气化,浓度增大,平衡正向移动,生成氢气量显著增加,故答案为反应吸热,
温度升高,平衡正向移动。与此同时,温度升高导致十氢萘气化,浓度增大,平衡正向移动,生成氢
气量显著增加;
(3)①温度335℃,在8 h时,十氢萘为1.00 mol,测得C H 和C H 的产率x=0.027,x=0.374,即生成
10 12 10 8 1 2
C H 和C H 的物质的量分别为0.027mol,0.374mol,设反应的C H 的物质的量为a,反应C H 的
10 12 10 8 10 18 10 12
物质的量为b,根据反应
C H (l) C H (l)+3H(g)
10 18 10 12 2
1 1 3
a a 3a
C H (l) C H(l)+2H(g),
10 12 10 8 2
1 1 2
b b 2b
则a-b=0.027,b=0.374,则a=0.401,因此生成的氢气的物质的量分数为3a+2b=3×0.401+2×0.374=1.951,则
氢气的量为1.951mol,故答案为1.951;
②反应2的活化能比反应1小,相同温度下反应2更快,所以相同时间内,生成的四氢萘大部分都转化为
萘,故x 显著低于x,故答案为反应2的活化能比反应1小,相同温度下反应2更快,所以相同时间
1 2
内,生成的四氢萘大部分都转化为萘,故x 显著低于x;
1 2
③C H (l) C H (l)+3H(g) △H,C H (l) C H(l)+2H(g) △H,△H>△H>0;上述反应
10 18 10 12 2 1 10 12 10 8 2 2 1 2
均为吸热反应,生成物的总能量大于反应物,“C H →C H →C H”的“能量~反应过程” 示意图
10 18 10 12 10 8为 ,故答案为 ;
31.(2018·海南高考真题)过氧化氢(H O)是重要的化工产品,广泛应用于绿色化学合成.医疗消毒等领
2 2
域。
回答下列问题:
(1)已知:H(g)+ O(g)=HO(l) △H=-286 kJ·mol¯1
2 2 2 1
H(g)+O(g)=HO(l) △H=-188 kJ·mol¯1
2 2 2 2 2
过氧化氢分解反应2HO(l)=2HO(l)+O(g)的△H=______kJ·mol¯1。不同温度下过氧化氢分解反应的平衡
2 2 2 2
常数K _____K (填大于、小于或等于)。
(313K) (298K)
(2)100℃时,在不同金属离子存在下,纯过氧化氢24 h的分解率见下表:
离子 加入量(mg·L¯1) 分解率% 离子 加入量(mg·L¯1) 分解率%
无 0 2 Fe3+ 1.0 15
Al3+ 10 2 Cu2+ 0.1 86
Zn2+ 10 10 Cr3+ 0.1 96
由上表数据可知,能使过氧化氢分解反应活化能降低最多的离子是_______。贮运过氧化氢时,可选
用的容器材质为_________(填标号)。
A.不锈钢 B.纯铝 C.黄铜 D.铸铁
(3)过氧化氢的Ka=2.24×10¯12,HO 的酸性________HO (填大于、小于或等于)。
1 2 2 2
研究表明,过氧化氢溶液中HO -的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分
2
解率与pH的关系如图所示。一定浓度的过氧化氢,pH增大分解率增大的原因是
___________________:相同pH下,过氧化氢浓度越大分解率越低的原因是
__________________________________________。
【答案】(1)-196 小于 (2)Cr3+ B (3)大于 pH升高,c( )增大,分解速率
加快 HO 浓度越大,其电离度越小,分解率越小
2 2
【解析】(1)已知:① H(g)+ O(g)=HO(l) △H=-286 kJ·mol¯1
2 2 2 1
②H(g)+O(g)=HO(l) △H=-188 kJ·mol¯1
2 2 2 2 2
根据盖斯定律,①×2-②×2得:2HO(l)=2HO(l)+O(g)的△H=2△H-2△H=-196kJ·mol¯1。
2 2 2 2 1 2
该反应为放热反应,温度升高,化学平衡常数减小,所以K Kw,故HO 电离出氢离子浓度大于水电离出的氢离子浓度,故HO 的酸性>H O;
1 2 2 2 2 2
pH增大,氢离子浓度减小,反应正向进行,HO -的浓度增加,分解速率加快;
2
过氧化氢浓度越高,其电离程度越低,故分解率越小。
故答案为:大于;pH升高,c( )增大,分解速率加快;HO 浓度越大,其电离度越小,分解率越小。
2 2
32.(2012·重庆高考真题)尿素[CO(NH )]是首个由无机物人工合成的有机物.
2 2
(1)工业上尿素由CO 和NH 在一定条件下合成,其反应方程式为 .
2 3
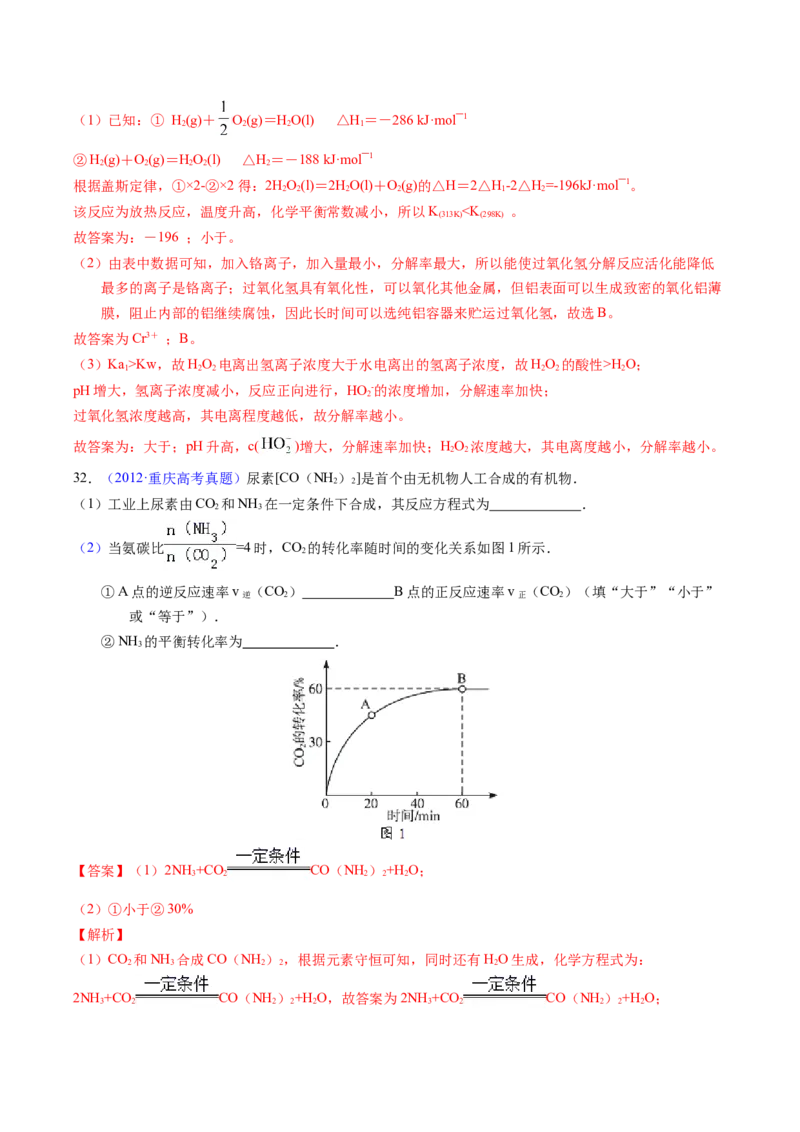
(2)当氨碳比 =4时,CO 的转化率随时间的变化关系如图1所示.
2
①A点的逆反应速率v (CO) B点的正反应速率v (CO)(填“大于”“小于”
逆 2 正 2
或“等于”).
②NH 的平衡转化率为 .
3
【答案】(1)2NH +CO CO(NH )+H O;
3 2 2 2 2
(2)①小于②30%
【解析】
(1)CO 和NH 合成CO(NH ),根据元素守恒可知,同时还有HO生成,化学方程式为:
2 3 2 2 2
2NH +CO CO(NH )+H O,故答案为2NH +CO CO(NH )+H O;
3 2 2 2 2 3 2 2 2 2(2)①由CO 的转化率随时间变化图可知在A点时反应还未达到平衡状态,反应仍将继续正向进行,故v
2
(CO)小于B点平衡时的化学反应速率,故答案为小于;
逆 2
②设CO 的初始物质的量为a,则NH 的初始物质的量为4a,由图可知,CO 的转化率为60%,故转化的
2 3 2
二氧化碳为a×60%=0.6a,根据方程式可知,转化的NH 的物质的量为0.6a×2=1.2a,故平衡时氨气的
3
转化率定为 ×100%=30%,
故答案为30%;