文档内容
专题59 水的电离与溶液的 pH
1.【2022年1月浙江卷】已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA.NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为
2 2
0.013%
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【答案】B
【解析】A.在等浓度的NaA.NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,故
2
A错误;B.溶液中c(H+)=10-3mol/L,HA电离程度较小,溶液中c(HA)≈0.1mol/L,K =
2 2 a1
,c(HA-)=1.3×10-5mol/L,c(HA-)≈c(HA) ,则HA的电离度
2 电离 2
0.013%,故B正确;C.向HA溶液中加入NaOH溶液至pH=11,
2
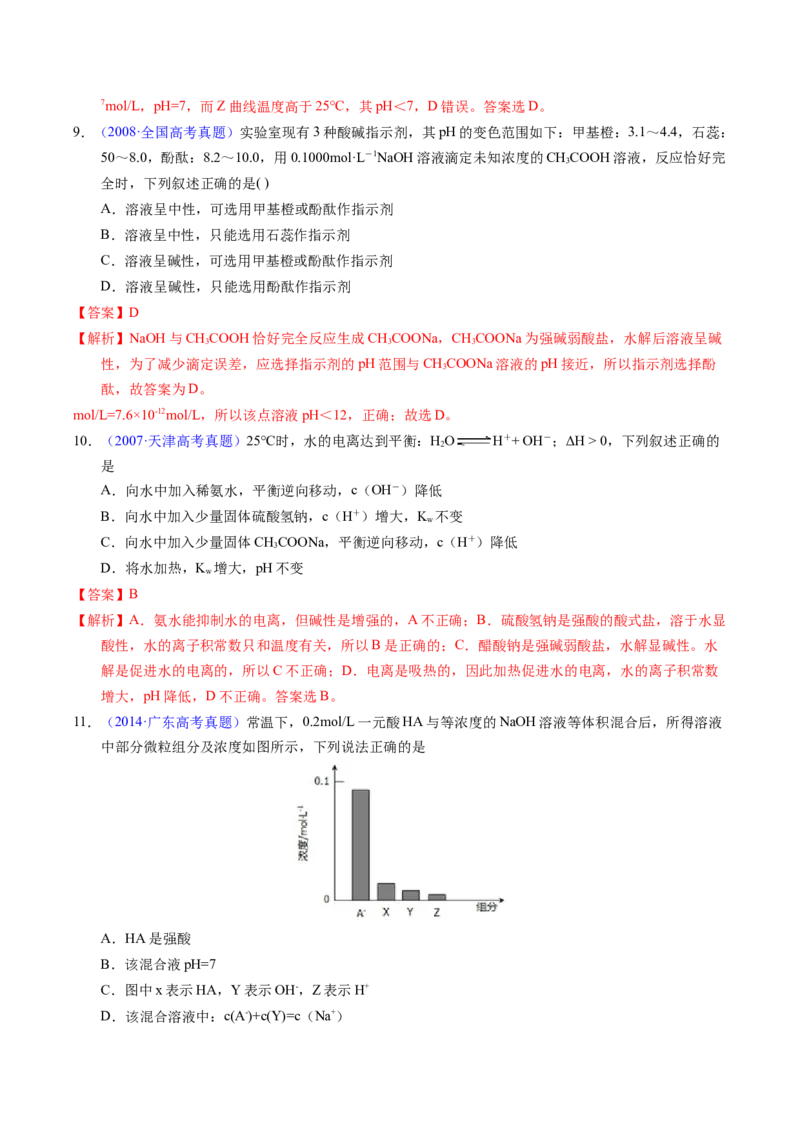
,则c(A2-)c(OH−)
B.随温度升高,CHCOONa溶液的c(OH−)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO−、Cu2+水解平衡移动
3 4 3
方向不同
【答案】C
【解析】水的电离为吸热过程,升高温度,促进水的电离;盐类水解为吸热过程,升高温度促进盐类水解,
据此解题;A.水的电离为吸热过程,升高温度,平衡向着电离方向移动,水中c(H+).c(OH-)=Kw增大,
故pH减小,但c(H+)=c(OH-),不符合题意;B.水的电离为吸热过程,升高温度,促进水的电离,所
以c(OH-)增大,醋酸根水解为吸热过程,CHCOOH-+H O CHCOOH+OH-,升高温度促进盐类水解,
3 2 3
所以c(OH-)增大,不符合题意;C.升高温度,促进水的电离,(H+)增大;升高温度,促进铜离子水解
Cu2++2H O Cu(OH) +2H+,(H+)增大,两者共同作用使pH发生变化,符合题意;D.盐类水解为吸
2 2
热过程,升高温度促进盐类水解,不符合题意;综上所述,本题应选C。
4.(2019·上海高考真题)25℃时,0.005mol/LBa(OH) 中H+浓度是( )
2
A.1× mol/L B.1× mol/L
C.5× mol/L D.5× mol/L
【答案】A
【解析】溶液中的氢氧根离子浓度为0.01mol/L,根据水的离子积常数计算,氢离子浓度为
mol/L。故选A 。
5.(2017·上海高考真题)下列物质的水溶液呈酸性,并且使水的电离平衡向正方向移动的是:
A.NaCO B.NH Cl C.HSO D.NaHCO
2 3 4 2 4 3
【答案】B
【解析】A.NaCO 是强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,促进水电离,错误;B.氯化铵是
2 3
强酸弱碱盐,铵根离子水解,溶液显酸性,促进水的电离,正确;C.硫酸完全电离生成氢离子而导
致溶液中c(H+)增大,溶液显酸性,抑制水的电离,错误;D.碳酸氢钠是强碱弱酸酸式盐,碳酸氢根离子水解程度大于电离程度,溶液显碱性,促进水的电离,错误;故选B。
6.(2017·浙江高考真题)下列说法不正确的是
A.pH<7的溶液不一定呈酸性
B.在相同温度下,物质的量浓度相等的氨水、NaOH溶液,c(OH-)相等
C.在相同温度下,pH相等的盐酸、CHCOOH溶液,c(Cl-)=c(CHCOO-)
3 3
D.氨水和盐酸反应后的溶液,若c(Cl―)=c(NH +),则溶液呈中性
4
【答案】B
【解析】A.pH<7的溶液不一定呈酸性,只有当溶液中c(OH-)<c(H+)时溶液显酸性,A正确;B.氢氧
化钠是强碱,完全电离,一水合氨是弱碱,部分电离,在相同温度下,物质的量浓度相等的氨水、
NaOH溶液,c(OH-)不相等,前者小于后者,B错误;C.盐酸、CHCOOH溶液中存在电荷守恒:
3
c(H+)=c(OH-)+c(Cl-)、c(H+)=c(OH-)+c(CHCOO-),因此在相同温度下,pH相等的盐酸、CHCOOH
3 3
溶液,c(Cl-)=c(CHCOO-),C正确;D.氨水和盐酸反应后的溶液中存在电荷守恒:c(NH +)
3 4
+c(H+)=c(OH-)+c(Cl-),若c(Cl―)=c(NH +),则c(H+)=c(OH-),溶液呈中性,D正确。答案选B。
4
7.(2017·浙江高考真题)下列物质的水溶液不能使酚酞变红的是
A.NaOH B.NaCO C.NaCl D.NH
2 3 3
【答案】C
【解析】A.NaOH是强碱,溶液显碱性,能使酚酞变红,不选;B.NaCO 属于强碱弱酸盐,水解后溶
2 3
液显碱性,能使酚酞变红,不选;C.NaCl是强酸强碱盐,溶液显中性,不能使酚酞变红,选;D.
NH 的水溶液显碱性,能使酚酞变红,不选;故选C。
3
8.(2013·全国高考真题)下图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是
A.两条曲线间任意点均有c(H+)×c(OH-)=K
w
B.M区域内任意点均有c(H+)<c(OH-)
C.图中T<T
1 2
D.XZ线上任意点均有pH=7
【答案】D
【解析】A、由图像知,两曲线上的任意点均是平衡点,且温度一定,所以其水的离子积是一个常数,A
正确;B、XZ连线的斜率是1,存在c(H+)=c(OH-),在X、Z连线的上方,c(H+)<c
(OH-),在X、Z连线的下方,c(H+)>c(OH-),B正确;C、水的电离是吸热反应,升温促进
水电离,c(H+)、c(OH-)及K 都增大,所以T<T,C正确;D、X曲线在25℃时c(H+)=10-
w 1 27mol/L,pH=7,而Z曲线温度高于25℃,其pH<7,D错误。答案选D。
9.(2008·全国高考真题)实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1~4.4,石蕊:
50~8.0,酚酞:8.2~10.0,用0.1000mol·L-1NaOH溶液滴定未知浓度的CHCOOH溶液,反应恰好完
3
全时,下列叙述正确的是( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
【答案】D
【解析】NaOH与CHCOOH恰好完全反应生成CHCOONa,CHCOONa为强碱弱酸盐,水解后溶液呈碱
3 3 3
性,为了减少滴定误差,应选择指示剂的pH范围与CHCOONa溶液的pH接近,所以指示剂选择酚
3
酞,故答案为D。
mol/L=7.6×10-12mol/L,所以该点溶液pH<12,正确;故选D。
10.(2007·天津高考真题)25℃时,水的电离达到平衡:HO H++ OH-;ΔH > 0,下列叙述正确的
2
是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,K 不变
w
C.向水中加入少量固体CHCOONa,平衡逆向移动,c(H+)降低
3
D.将水加热,K 增大,pH不变
w
【答案】B
【解析】A.氨水能抑制水的电离,但碱性是增强的,A不正确;B.硫酸氢钠是强酸的酸式盐,溶于水显
酸性,水的离子积常数只和温度有关,所以B是正确的;C.醋酸钠是强碱弱酸盐,水解显碱性。水
解是促进水的电离的,所以C不正确;D.电离是吸热的,因此加热促进水的电离,水的离子积常数
增大,pH降低,D不正确。答案选B。
11.(2014·广东高考真题)常温下,0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液
中部分微粒组分及浓度如图所示,下列说法正确的是
A.HA是强酸
B.该混合液pH=7
C.图中x表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)【答案】D
【解析】A、0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,得到的溶液为0.1mol/L的NaA溶
液,若HA为强酸,则溶液为中性,且c(A-)=0.1mol/L,与图不符,所以HA为弱酸,A错误;B、根
据A的分析,可知该溶液的pH>7,B错误;C、A-水解使溶液显碱性,所以溶液中的粒子浓度的大
小关系是c(Na+)>c(A-)>c(OH-)>c(HA)>c(H+),所以X是OH-,Y是HA,Z表示H+,C错误;
D、根据元素守恒,有c(A-)+c(HA)=c(Na+),D正确;答案选D。
12.(2014·海南高考真题)NaOH溶液滴定盐酸实验中,不必用到的是
A.酚酞 B.圆底烧瓶 C.锥形瓶 D.碱式滴定管
【答案】B
【解析】在酸碱中和滴定中要用滴定管滴加试剂,待测溶液盛装在锥形瓶中,用指示剂酚酞来判断滴定终
点。因此不使用的仪器是圆底烧瓶。答案选B。
13.(2008·上海高考真题)常温下,某溶液中由水电离出来的c(H+)=1.0×10-13mol·L-1,该溶液可能是( )
①二氧化硫 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
【答案】A
【解析】依据常温下溶液中由水电离出来的c(H+)=1.0×10-13mol·L-1,说明水的电离受到抑制,溶液为强
酸或强碱溶液。①二氧化硫溶于水生成了亚硫酸,亚硫酸电离出氢离子,会抑制水的电离,故①正确;
②氯化铵是强酸弱碱盐,铵根离子会发生水解,水解的本质是促进水的电离,故②错误;③硝酸钠是
强酸强碱盐,溶液为中性,水的电离程度不会减小,故③错误;④氢氧化钠为强碱,会抑制水的电离,
故④正确。综上所述,本题正确答案为A。
14.(2012·上海高考真题)常温下a mol/L CH COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判
3
断一定错误的是
A.若c(OH-)>c(H+),a=b B.若c(K+)>c(CHCOO-),a>b
3
C.若c(OH-)=c(H+),a>b D.若c(K+)<c(CHCOO-),a<b
3
【答案】D
【解析】A.若c(OH−)>c(H+),溶液为醋酸钾溶液或醋酸钾和KOH的混合液,则a b,不符合题意;B.
若c(K+)>c(CHCOO−),由电荷守恒c(CHCOO−)+ c(OH−)= c(H+)+ c(K+)可知,c(OH−)>c(H+),则
3 3 ⩽
a b,若当a>b,也就是弱酸强碱中和时,弱酸过量,溶液可能呈酸性、中性或碱性,醋酸过量的极
少,所以过量的醋酸电离出的H+小于醋酸根水解产生的OH−,有可能成立,不符合题意;C.若
⩽
c(OH−)=c(H+),溶液显中性,一定为醋酸和醋酸钾的混合液,则a>b,不符合题意;D.若c(K+)<
c(CHCOO−),由电荷守恒可知c(CHCOO−)+ c(OH−)= c(H+)+ c(K+),c(OH−)<c(H+),则a>b,符合题意;
3 3
答案选D。
15.(2015·广东高考真题)一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是(
)A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
【答案】C
【解析】A.温度升高,水的离子积常数增大,水溶液中,氢离子和氢氧根离子浓度都增大,将不在曲线
上,A错误;B.b点c(H+)=c(OH-)=1.0×10-7,故K =1.0×10-7×1.0×10-7=1.0×10-14,B错误;C.加入
w
FeCl ,由于氯化铁为强酸弱碱盐,在溶液中Fe3+水解结合水电离出的OH-,促进水的电离平衡右移,
3
最终使溶液中氢离子浓度增大,氢氧根离子浓度减小,可以由b到a点,符合图象变化趋势,C正确;
D.由c点到d点,水的离子积常数减小,温度不变,K 不变,故不能利用稀释使其形成此变化,D
w
错误;故合理选项是C。
16.(2008·全国高考真题)常温下,取浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液
的pH等于12,则原溶液的浓度为
A.0.01mol·L-1 B.0.017mol·L-1
C.0.05mol·L-1 D.0.50mol·L-1
【答案】C
【解析】设NaOH和HCl的物质的量浓度均为c,NaOH和HCl溶液以3:2体积比相混合,体积分别为
3V、2V,酸碱混合后pH=12,则碱过量,剩余的氢氧根离子浓度为:c(OH−)=0.01 mol·L-1,则:
c(OH−)= =0.01 mol·L-1,解得:c=0.05mol·L-1,正确,答案选C。
17.(2010·天津高考真题)下列液体均处于25℃,有关叙述正确的是
A.某物质的溶液pH < 7,则该物质一定是酸或强酸弱碱盐
B.pH= 4.5的番茄汁中c(H+)是pH= 6.5的牛奶中c(H+)的100倍
C.AgCl在同浓度的CaCl 和NaCl溶液中的溶解度相同
2
D.pH= 5.6的CHCOOH与CHCOONa混合溶液中,c(Na+) > c(CH COO-)
3 3 3
【答案】B
【解析】A、某物质的溶液pH<7,则该物质可能是酸或强酸弱碱盐或弱酸弱碱盐或NaHSO 等,弱酸弱碱
4
盐的水溶液有可能也显酸性,A错误;B、pH=4.5的番茄汁中c(H+)=1.0×10-4.5mol/L,pH=6.5的牛
奶中c(H+)=1.0×10-6.5mol/L,前者c(H+)是后者的100倍,B正确;C、浓度相同的CaCl 和NaCI溶
2
液中的Cl-浓度不同,前者c(Cl-)是后者的2倍,根据氯化银的溶解平衡判断,氯离子浓度增大,平
衡左移,氯化银的溶解度减小,所以AgCl在同浓度的CaCl 和NaCI溶液中的溶解度不同,前者较小,
2C错误;D、pH=5.6的CHCOOH与CHCOONa混合溶液显酸性,说明醋酸的电离大于醋酸根离子
3 3
的水解程度,所以c(Na+)<c(CHCOO-),D错误;答案选B。
3
18.(2009·四川高考真题)关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列
说法不正确的是
A.c(NH+):③>①
4
B.水电离出的c(H+):②>①
C.①和②等体积混合后的溶液:c(H+)=c(OH )+c(NH·H O)
3 2
D.①和③等体积混合后的溶液:c(NH+)>c(Cl )>c(OH )>c(H+)
4
【答案】B
【解析】A.氯化铵为强电解质完全电离后产生大量的NH +,氨水为弱电解质只有少量的NH +产生,A正确;
4 4
B.在水中加入酸和碱都抑制水的电离,但是盐类水解促进水的电离,不正确。C.盐酸和氨水混合后
恰好完全反应,但因生成的盐为强酸弱碱盐,溶液显酸性,而多余的H+为水解产生,此等式可表示溶
液中的质子守恒,正确。D.①和③等体积混合后的溶液显碱性,氯化铵是强电解质,而一水合氨是
弱电解质,故离子浓度的大小顺序为c(NH+)>c(Cl−)>c(OH−)>c(H+),D正确。故选B。
4
19.(2007·全国高考真题)室温时,下列混合溶液的pH一定小于7的是
A.pH=3的盐酸和pH=11的氨水等体积混合
B.pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合
C.pH=3的醋酸和pH=11的的氢氧化钡溶液等体积混合
D.pH=3的硫酸和pH=11的氨水等体积混合
【答案】C
【解析】A.一水合氨为弱电解质,溶液中只能部分电离出氢氧根离子,pH=3的盐酸中氯化氢浓度为0.
001mol/L,而pH=11的氨水中一水合氨浓度远远大于0.01mol/L,两溶液等体积混合后氨水过量,
溶液显示碱性,溶液的pH一定大于7,错误;B.盐酸是强酸,氢氧化钡是强碱,完全电离,所以pH
=3的盐酸和pH=11的氢氧化钡溶液等体积混合,二者恰好完全反应产生水,所以溶液的pH=7,错
误;C.pH=3的醋酸中,醋酸为弱电解质,醋酸的物质的量浓度大于0.001mol/L,pH=11的氢氧
化钠溶液中氢氧化钠的浓度为0.001mol/L,两溶液等体积混合后醋酸过量,溶液显示酸性,溶液的
pH一定小于7,正确;D.一水合氨为弱电解质,溶液中只能部分电离出氢氧根离子,pH=3的硫酸中
硫酸浓度为0.001mol/L,而pH=11的氨水中一水合氨浓度远远大于0.01mol/L,两溶液等体积混合
后氨水过量,溶液显示碱性,溶液的pH一定大于7,错误;综上所述,答案为C。
20.(2012·上海高考真题)水中加入下列溶液对水的电离平衡不产生影响的是( )
A.NaHSO 溶液 B.KF溶液 C.KAl(SO ) 溶液 D.NaI溶液
4 4 2
【答案】D
【解析】水的电离H
2
O⇌H++OH-,加入酸或碱抑制水的电离,加入能水解的盐促进水的电离。A.硫酸氢
钠在水溶液中完全电离,电离出氢离子和硫酸根离子和钠离子,溶液呈酸性,水的电离H
2
O⇌H++OH-,抑制了水的电离,水的电离向逆反应方向移动,错误;B.KF为强电解质,电离出钾离子和氟
离子,钾不水解,氟离子水解生成氢氟酸,促进水的电离,错误;C.KAl(SO ) 为强电解质,电离
4 2
出钾离子和铝离子和硫酸根离子,钾离子、硫酸根离子不水解,铝离子水解生成氢氧化铝,促进水的
电离,错误;D.NaI为强电解质,在溶液中电离出钠离子和碘离子,这两种离子都不水解,对水的
电离平衡无影响,正确;答案选D
21.(2007·广东高考真题)下列可用于测定溶液pH且精确度最高的是( )
A.酸碱指示剂 B.pH计 C.精密pH试纸 D.广泛pH试纸
【答案】B
【解析】A.酸碱指示剂只能大概知道溶液的酸碱性,不能定量,错误;B.pH计能读到小数点后面两位
小数,正确;C.精密pH试纸能测到0.2数量级,错误;D.广泛pH试纸仅能读出整数,错误;答案
选B。
22.(2008·海南高考真题)用pH试纸测定溶液pH的正确操作是( )
A.将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照
B.将一小块试纸用蒸馏水润湿后放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比
色卡对照
C.将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照
D.将一小条试纸先用蒸馏水润湿后,在待测液中蘸一下,取出后与标准比色卡对照
【答案】A
【解析】A.将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照,
A正确;B.用pH试纸测定溶液pH值时,若用蒸馏水润湿试纸,相当于把待测液加水稀释,导致所
测的pH值可能不准,故试纸是不能事先润湿的,B不正确;C.不能将试纸在待测液中蘸一下,这样
会污染试剂,C不正确;D.不能将试纸用蒸馏水润湿,D不正确。本题选A。
23.(2014·山东高考真题)已知某温度下CHCOOH和NH ·H O的电离常数相等,现向10mL浓度为
3 3 2
0.1mol·L-1的CHCOOH溶液中滴加相同浓度的氨水,在滴加过程中( )
3
A.水的电离程度始终增大
B. 先增大再减小
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10mL时,c(NH +)=c(CHCOO-)
4 3
【答案】D
【解析】A.酸溶液、碱溶液抑制了水的电离,溶液显示中性前,随着氨水的加入,溶液中氢离子浓度逐
渐减小,水的电离程度逐渐增大;当氨水过量后,随着溶液中氢氧根离子浓度逐渐增大,水的电离程
度逐渐减小,所以滴加过程中,水的电离程度先增大后减小,错误;B.由CHCOONH 的水解常数
3 4
K= ,随着氨水的加入,c(H+)逐渐减小,K 不变,则 始终减小,
h h
错误;C.n(CHCOOH)与n(CHCOO-)之和为0.001mol,始终保持不变,由于溶液体积逐渐增大,
3 3所以c(CHCOOH)与c(CHCOO-)之和逐渐减小,错误;D.当加入氨水的体积为10mL时,醋酸
3 3
和一水合氨的物质的量相等,由于二者的电离常数相等,所以溶液显示中性,c(H+)=c(OH-),根
据电荷守恒可知:c(NH +)=c(CHCOO-),正确;故答案为D。
4 3
24.(2011·四川高考真题)25℃时,在等体积的①pH=0的HSO 溶液、②0.05mol/L的Ba(OH) 溶液、③
2 4 2
pH=10的NaS溶液、④pH=5的NH NO 溶液中,发生电离的水的物质的量之比是
2 4 3
A.1:10:1010:109 B.1:5:5×109:5×10
C.1:20:1010:109 D.1:10:104:109
【答案】A
【解析】
①中pH=0的HSO 中c(H+)=1.0 mol·L-1,c(OH-)=1.0×10-14mol·L-1,水电离程度为1.0×10-14mol·L-
2 4
1;
②中c(OH-)=0.1 mol·L-1,c(H+)=1.0×10-13mol·L-1,水电离程度为1.0×10-13mol·L-1;
③中c(OH-)=1.0×10-4mol·L-1,水的电离程度为1.0×10-4mol·L-1;
④中c(H+)=1.0×10-5mol·L-1,水的电离程度为1.0×10-5mol·L-1;
故①②③④中水的电离程度之比为:1.0×10-14mol·L-1:1.0×10-13mol·L-1:1.0×10-4mol·L-1:1.0×10-
5mol·L-1=1:10:1010:109,正确。
答案选A。
25.(2013·上海高考真题)374℃、22.1Mpa以上的超临界水具有很强的溶解有机物的能力,并含有较多
的H+和OH-,由此可知超临界水
A.显中性,pH等于7 B.表现出非极性溶剂的特性
C.显酸性,pH小于7 D.表现出极性溶剂的特性
【答案】B
【解析】A.25℃时,水的pH=7,水的电离是吸热过程,升高温度促进水的电离,在374℃时,超临界水
显中性,pH<7,A错误;B.超临界水具有很强的溶解有机物的能力,根据相似相溶原理,说明超临
界水表现出非极性溶剂的特性,B正确;C.25℃时,水的pH=7,水的电离是吸热过程,升高温度促
进水的电离,在374℃时,超临界水中H+与OH-浓度相等,显中性,pH<7,C错误;D.超临界水具
有很强的溶解有机物的能力,根据相似相溶原理,说明超临界水表现出非极性溶剂的特性,D错误;
答案选B。
26.(2013·全国高考真题)室温时,M(OH) (S) M2+(aq)+2OH-(aq) Ksp=a,c(M2+)="b" mol·L-1时,溶液的
2
pH等于( )
1 b 1 1
A. lg( ) B. lg( )
2 a 2 2
1 1 1 b
C.14+ lg( ) D.14+ lg( )
2 2 2 a
【答案】C
a
【解析】根据Ksp=a= c(M2+)·c(OH-)2,c(M2+)=b mol·L-1,解得c(OH-)2=( )。本题是碱性环境,先求出
b1 a
c(OH-),根据水的离子积,在求出c(H+),在求出溶液的pH=14+ lg( )。
2 b
27.(2011·上海高考真题)常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积
混合得到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是
A.b不可能显碱性 B.a可能显酸性或碱性
C.a不可能显酸性 D.b可能显碱性或酸性
【答案】AB
【解析】根据pH都为11的氨水、氢氧化钠溶液,氢氧化钠的浓度小,再讨论pH为3的某酸溶液,利用
等体积混合反应后溶液中的溶质来分析溶液的酸碱性。A.pH为3的某酸溶液,为强酸时与等体积
pH为11的氢氧化钠恰好完全反应,生成强酸强碱盐,则溶液为中性;酸为弱酸时酸过量,则溶液一
般为酸性,即b不可能显碱性,正确;B.某酸溶液为强酸时与等体积pH为11的氨水反应时氨水过
量,则a可能显碱性;若为弱酸时恰好完全反应,生成弱酸弱碱盐,当弱酸酸根离子的水解小于弱碱
中离子的水解,则a可能显酸性,正确;C.若为pH=3弱酸与等体积pH为11的氨水恰好完全反应时,
生成弱酸弱碱盐,当弱酸酸根离子的水解小于弱碱中离子的水解,则a可能显酸性,错误;D.若酸
为pH=3弱酸与等体积pH为11的氢氧化钠溶液反应时酸过量,则溶液一般为酸性,即b不可能显碱
性,错误。答案选AB。
28.(2012·广东高考真题)对于常温下pH为2的盐酸,传述正确的是( )
A.c(H+)=c(Cl﹣)+c(OH﹣)
B.与等体积pH=12的氨水混合后所得溶液显酸性
C.由HO电离出的c(H+)=1.0×10﹣12mol•L﹣1
2
D.与等体积0.01 mol•L﹣1乙酸钠溶液混合后所得溶液中:c(Cl﹣)=c(CHCOO﹣)
3
【答案】AC
【解析】A、常温下PH为2的盐酸溶液中电荷守恒可知,c(H+)=c(Cl﹣)+c(OH﹣),正确;B、一水
合氨是弱电解质存在电离平衡,与等体积PH=12的氨水混合后,一水合氨会继续电离出氢氧根离子,
氨水过量,显碱性,错误;C、常温下PH为2的盐酸溶液中c(H+)=0.01mol/L;c(H+)水=c(OH
﹣)水=K /c(H+)=1.0×10﹣12mol•L﹣1;正确;D,反应后生成乙酸和氯化钠,水溶液为酸性,醋酸是
W
弱电解质存在电离平衡,c(Cl﹣)>c(CHCOO﹣),错误;故选AC.
3
29.(2012·全国高考真题)已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的一元酸
W
HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.a=b
B.混合溶液的PH=7
C.混合溶液中,c(H+)= mol.L-1
D.混合溶液中c(H+)+c(B+)=c(OH-)+C(A-)
【答案】C
【解析】A.没有给具体的温度和酸、碱的强弱,A错误;B.由于没有给具体的温度,pH=7,不一定是中性,B错误;C.判断溶液呈中性的依据只能是c(H+)=c(OH-),此时c(H+)= mol·L-1,C正确;
D.根据电荷守恒,不论溶液是酸性、中性、还是碱性,都成立,D错误;故合理选项为C。
30.(2010·海南高考真题)常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该
混合溶液的pH等于
A.1.7 B.2.0 C.12.0 D.12.4
【答案】B
【解析】
设溶液的体积都是1L,则氢氧化钠的物质的量为1L×0.1mol•L-1=0.1mol,
硫酸的物质的量为1L×0.06mol•L-1=0.06mol,H+的物质的量为0.06mol×2=0.12mol,
则当酸碱发生中和时H+和OH-的物质的量分别为0.12mol和0.1mol,
则硫酸过量,过量的H+的物质的量为0.12mol-0.1mol=0.02mol,
则反应后溶液中H+的物质的量浓度为c(H+)= =0.01mol•L-1,
pH=-lg10-2=2.0,故选B.