文档内容
专题60 酸碱中和滴定及曲线
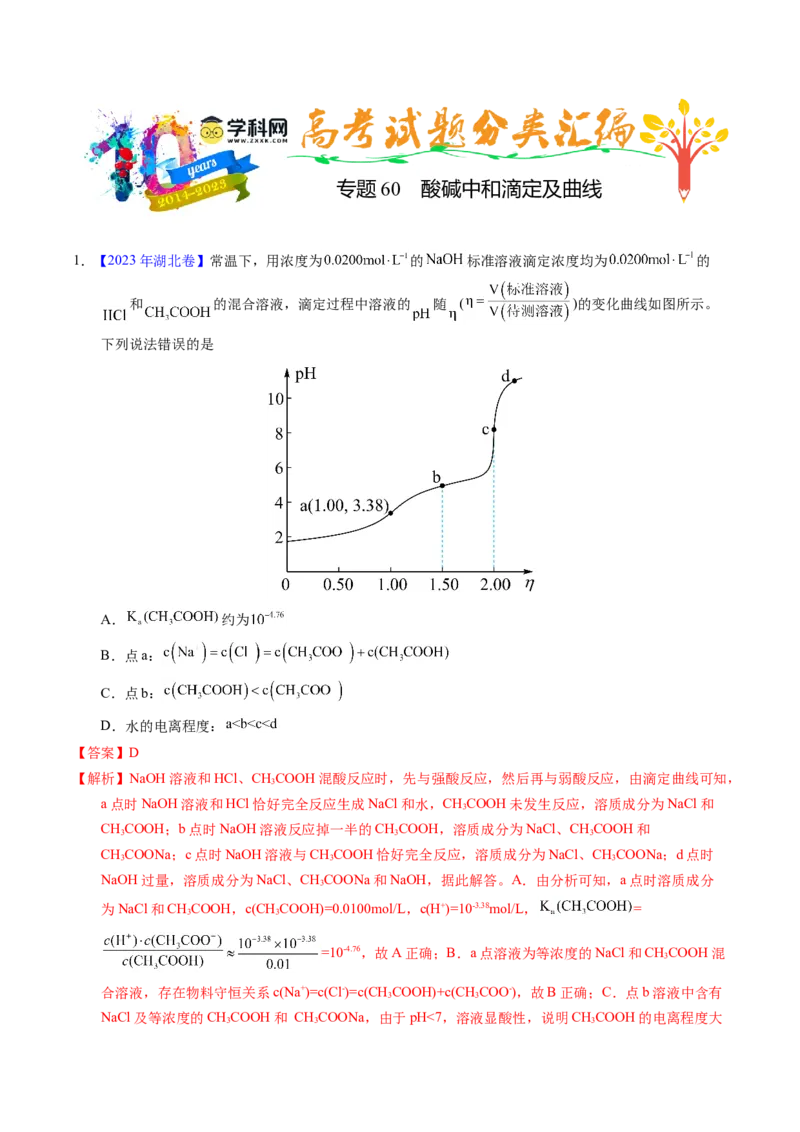
1.【2023年湖北卷】常温下,用浓度为 的 标准溶液滴定浓度均为 的
和 的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。
下列说法错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
【答案】D
【解析】NaOH溶液和HCl、CHCOOH混酸反应时,先与强酸反应,然后再与弱酸反应,由滴定曲线可知,
3
a点时NaOH溶液和HCl恰好完全反应生成NaCl和水,CHCOOH未发生反应,溶质成分为NaCl和
3
CHCOOH;b点时NaOH溶液反应掉一半的CHCOOH,溶质成分为NaCl、CHCOOH和
3 3 3
CHCOONa;c点时NaOH溶液与CHCOOH恰好完全反应,溶质成分为NaCl、CHCOONa;d点时
3 3 3
NaOH过量,溶质成分为NaCl、CHCOONa和NaOH,据此解答。A.由分析可知,a点时溶质成分
3
为NaCl和CHCOOH,c(CHCOOH)=0.0100mol/L,c(H+)=10-3.38mol/L, =
3 3
=10-4.76,故A正确;B.a点溶液为等浓度的NaCl和CHCOOH混
3
合溶液,存在物料守恒关系c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-),故B正确;C.点b溶液中含有
3 3
NaCl及等浓度的CHCOOH和 CHCOONa,由于pH<7,溶液显酸性,说明CHCOOH的电离程度大
3 3 3于CHCOO-的水解程度,则c(CHCOOH)d,故D错误;答案选D。
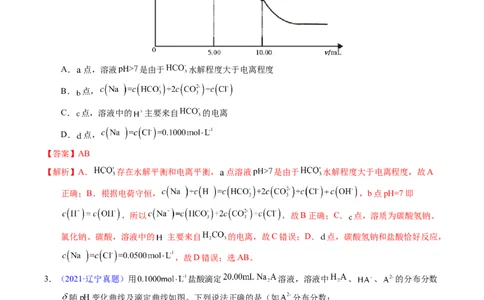
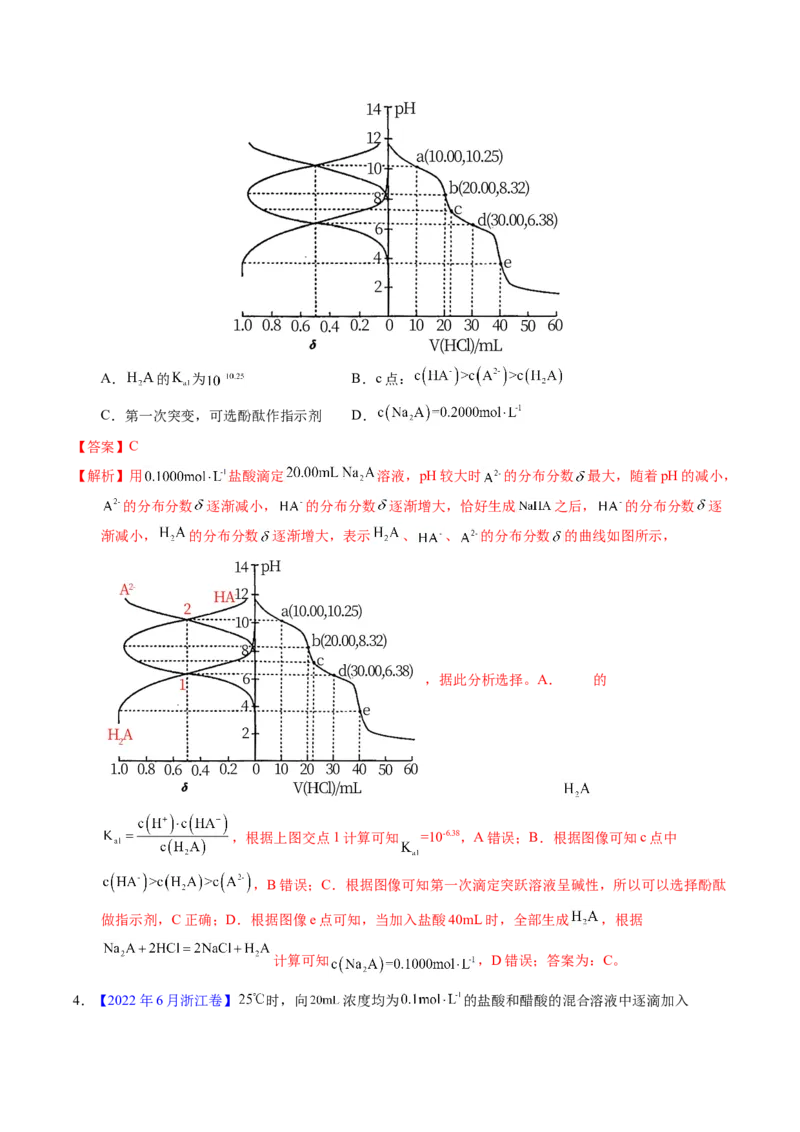
2.(2021·海南真题)25℃时,向 的 溶液中滴加 的盐酸,溶
液的 随加入的盐酸的体积 变化如图所示。下列有关说法正确的是
A. 点,溶液 是由于 水解程度大于电离程度
B. 点,
C. 点,溶液中的 主要来自 的电离
D. 点,
【答案】AB
【解析】A. 存在水解平衡和电离平衡, 点溶液 是由于 水解程度大于电离程度,故A
正确;B.根据电荷守恒, ,b点pH=7即
,所以 ,故B正确;C. 点,溶质为碳酸氢钠、
氯化钠、碳酸,溶液中的 主要来自 的电离,故C错误;D. 点,碳酸氢钠和盐酸恰好反应,
,故D错误;选AB。
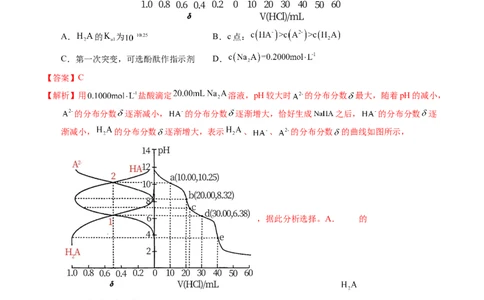
3.(2021·辽宁真题)用 盐酸滴定 溶液,溶液中 、 、 的分布分数
随pH变化曲线及滴定曲线如图。下列说法正确的是(如 分布分数:
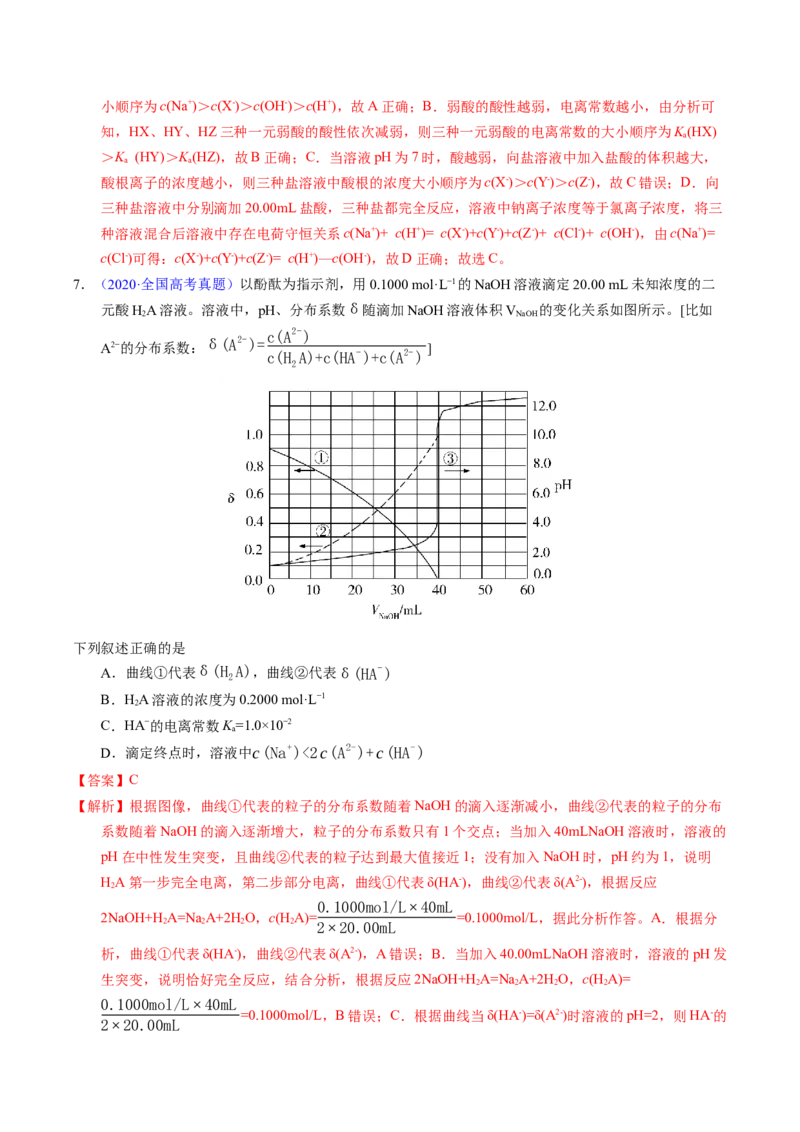
)A. 的 为 B.c点:
C.第一次突变,可选酚酞作指示剂 D.
【答案】C
【解析】用 盐酸滴定 溶液,pH较大时 的分布分数 最大,随着pH的减小,
的分布分数 逐渐减小, 的分布分数 逐渐增大,恰好生成 之后, 的分布分数 逐
渐减小, 的分布分数 逐渐增大,表示 、 、 的分布分数 的曲线如图所示,
,据此分析选择。A. 的
,根据上图交点1计算可知 =10-6.38,A错误;B.根据图像可知c点中
,B错误;C.根据图像可知第一次滴定突跃溶液呈碱性,所以可以选择酚酞
做指示剂,C正确;D.根据图像e点可知,当加入盐酸40mL时,全部生成 ,根据
计算可知 ,D错误;答案为:C。
4.【2022年6月浙江卷】 时,向 浓度均为 的盐酸和醋酸的混合溶液中逐滴加入的 溶液(醋酸的 ;用 的 溶液滴定 等浓度的盐酸,滴
定终点的 突跃范围4.3~9.7)。下列说法不正确的是
A.恰好中和时,溶液呈碱性
B.滴加 溶液至 的过程中,发生反应的离子方程式为:
C.滴定过程中,
D. 时,
【答案】B
【解析】A.恰好中和时,生成氯化钠溶液和醋酸钠溶液,其中醋酸根离子会水解,溶液显碱性,A正确;
B.滴加 溶液至 的过程中,若只发生反应的离子方程式: ,则滴加NaOH
溶液的体积为20mL,则根据电离常数, 的醋酸中,c(H+)≈c(CH COO-)= =
3
= >1.0×10-4.3,故用氢氧化钠滴定的过程中,醋酸也参加了反应,则离子
方程式为:H++OH-=H O和CHCOOH+OH-=CH COO-+H O,B错误;C.滴定前盐酸和醋酸的浓度相
2 3 3 2
同,故滴定过程中,根据物料守恒可知: ,C正确;D.向
浓度均为 的盐酸和醋酸的混合溶液中逐滴加入 的 溶液,当盐酸的体积为
20ml时,溶液为氯化钠和醋酸的混合溶液,显酸性,需要再滴加适量的氢氧化钠,当加入的NaOH溶
液的体积为30mL时,溶液为NaCl和等浓度的CHCOONA.CHCOOH,根据Ka=1.8×10-5>Kh=
3 3
可知,此时溶液仍然呈酸性,需继续滴加NaOH溶液,故有
,D正确;故答案为:B。
5.【2022年1月浙江卷】某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如
3
图曲线:下列说法正确的的是
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO
1
+H+=CO ↑+H O
2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO )=c(OH-)-c(H+)
2 3 3 2 3
【答案】C
【解析】A.碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,则碳酸钠溶液的起始pH较
大,甲曲线表示碳酸钠溶液中滴加盐酸,碳酸钠与盐酸反应先生成碳酸氢钠,碳酸氢根离子再与氢离
子反应产生碳酸,进而产生二氧化碳,则图中丁线表示向NaCO 溶液中滴加盐酸,乙、丙线表示向
2 3
NaHCO 溶液中滴加盐酸,A项错误;B.由图示可知,当滴加盐酸的体积为20mL时,碳酸根离子恰
3
好完全转化为碳酸氢根子,而V> 20mL,VmL时(a点、b点),没有二氧化碳产生,则所发生的反应
1 1
为碳酸氢根离子与氢离子结合生成碳酸,离子方程式表示为:HCO +H+=H CO,B项错误;C.根据
2 3
pH-V(HCl)图,滴定分析时,c点的pH在9左右,符合酚酞的指示范围,可用酚酞作指示剂;d点的
pH在4左右,符合甲基橙的指示范围,可用甲基橙作指示剂指示滴定终点,C项正确;D.根据电荷
守恒和物料守恒,则NaCO 中存在c(OH-)-c(H+)=2c(H CO)+c(HCO ), NaHCO 溶液中满足
2 3 2 3 3
c(HCO)-c(CO )=c(OH-)-c(H+),D项错误;答案选C。
2 3
6.(2021·湖南真题)常温下,用 的盐酸分别滴定20.00mL浓度均为 三种一元
弱酸的钠盐 溶液,滴定曲线如图所示。下列判断错误的是
A.该 溶液中:
B.三种一元弱酸的电离常数:
C.当 时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
【答案】C
【解析】由图可知,没有加入盐酸时,NaX、NaY、NaZ溶液的pH依次增大,则HX、HY、HZ三种一元
弱酸的酸性依次减弱。A.NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为c(Na+)>c(X-)>c(OH-)>c(H+),故A正确;B.弱酸的酸性越弱,电离常数越小,由分析可
知,HX、HY、HZ三种一元弱酸的酸性依次减弱,则三种一元弱酸的电离常数的大小顺序为K(HX)
a
>K (HY)>K(HZ),故B正确;C.当溶液pH为7时,酸越弱,向盐溶液中加入盐酸的体积越大,
a a
酸根离子的浓度越小,则三种盐溶液中酸根的浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;D.向
三种盐溶液中分别滴加20.00mL盐酸,三种盐都完全反应,溶液中钠离子浓度等于氯离子浓度,将三
种溶液混合后溶液中存在电荷守恒关系c(Na+)+ c(H+)= c(X-)+c(Y-)+c(Z-)+ c(Cl-)+ c(OH-),由c(Na+)=
c(Cl-)可得:c(X-)+c(Y-)+c(Z-)= c(H+)—c(OH-),故D正确;故选C。
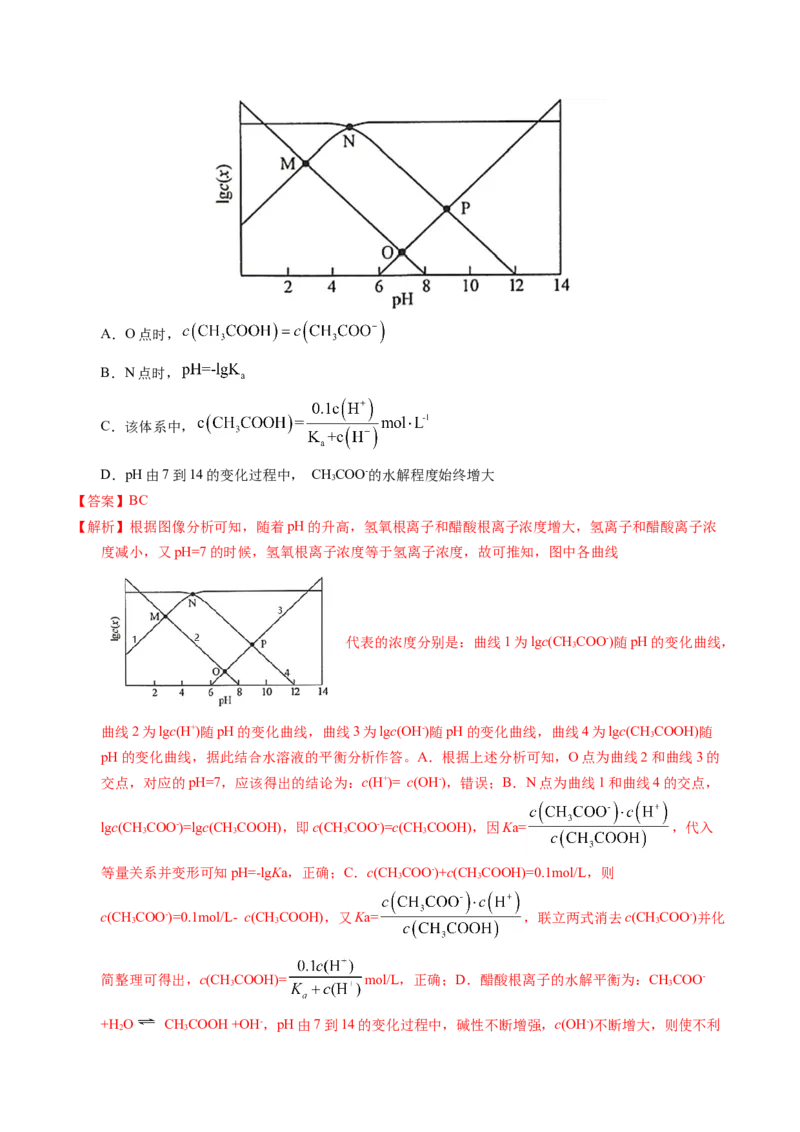
7.(2020·全国高考真题)以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二
元酸HA溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V 的变化关系如图所示。[比如
2 NaOH
c(A2-)
δ(A2-)=
A2−的分布系数: ]
c(H A)+c(HA-)+c(A2-)
2
下列叙述正确的是
A.曲线①代表δ(H A),曲线②代表δ(HA-)
2
B.HA溶液的浓度为0.2000 mol·L−1
2
C.HA−的电离常数K=1.0×10−2
a
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
【答案】C
【解析】根据图像,曲线①代表的粒子的分布系数随着NaOH的滴入逐渐减小,曲线②代表的粒子的分布
系数随着NaOH的滴入逐渐增大,粒子的分布系数只有1个交点;当加入40mLNaOH溶液时,溶液的
pH在中性发生突变,且曲线②代表的粒子达到最大值接近1;没有加入NaOH时,pH约为1,说明
HA第一步完全电离,第二步部分电离,曲线①代表δ(HA-),曲线②代表δ(A2-),根据反应
2
0.1000mol/L×40mL
2NaOH+H A=Na A+2HO,c(H A)= =0.1000mol/L,据此分析作答。A.根据分
2 2 2 2 2×20.00mL
析,曲线①代表δ(HA-),曲线②代表δ(A2-),A错误;B.当加入40.00mLNaOH溶液时,溶液的pH发
生突变,说明恰好完全反应,结合分析,根据反应2NaOH+H A=Na A+2HO,c(H A)=
2 2 2 2
0.1000mol/L×40mL
=0.1000mol/L,B错误;C.根据曲线当δ(HA-)=δ(A2-)时溶液的pH=2,则HA-的
2×20.00mLc(A2-)⋅c(H+)
电离平衡常数K= =c(H+)=1×10-2,C正确;D.用酚酞作指示剂,酚酞变色的pH范围
a c(HA-)
为8.2~10,终点时溶液呈碱性,c(OH-)>c(H+),溶液中的电荷守恒为c(Na+)+c(H+)=2c(A2-)+c(HA-)
+c(OH-),则c(Na+)>2c(A2-)+c(HA-),D错误;答案选C。
8.(2020·浙江高考真题)室温下,向 盐酸中滴加 溶
液,溶液的pH随 溶液体积的变化如图。已知 。下列说法不正确的是( )
A. 与盐酸恰好完全反应时,
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D. 时,
【答案】C
【解析】A. 与盐酸恰好完全反应时溶液中的溶质为NaCl,呈中性,室温下 ,正确;B.选
择变色范围在pH突变范围内的指示剂,可减小实验误差,B正确;C.甲基橙的变色范围在pH突变
范围外,误差更大,错误;D. 时,溶液中的溶质为氯化钠和氢氧化钠,且
c(NaOH)= =0.02mol/L,即溶液中c(OH-)=0.02mol,则
c(H+)=5×10-13 mol/L,pH=-lgc(H+)=12.3,正确;故答案为C。
9.(2020·山东高考真题)25℃时,某混合溶液中 ,
1gc( CH COOH)、1gc(CHCOO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。K 为CHCOOH
3 3 a 3
的电离常数,下列说法正确的是A.O点时,
B.N点时,
C.该体系中,
D.pH由7到14的变化过程中, CHCOO-的水解程度始终增大
3
【答案】BC
【解析】根据图像分析可知,随着pH的升高,氢氧根离子和醋酸根离子浓度增大,氢离子和醋酸离子浓
度减小,又pH=7的时候,氢氧根离子浓度等于氢离子浓度,故可推知,图中各曲线
代表的浓度分别是:曲线1为lgc(CHCOO-)随pH的变化曲线,
3
曲线2为lgc(H+)随pH的变化曲线,曲线3为lgc(OH-)随pH的变化曲线,曲线4为lgc(CHCOOH)随
3
pH的变化曲线,据此结合水溶液的平衡分析作答。A.根据上述分析可知,O点为曲线2和曲线3的
交点,对应的pH=7,应该得出的结论为:c(H+)= c(OH-),错误;B.N点为曲线1和曲线4的交点,
lgc(CHCOO-)=lgc(CHCOOH),即c(CHCOO-)=c(CHCOOH),因Ka= ,代入
3 3 3 3
等量关系并变形可知pH=-lgKa,正确;C.c(CHCOO-)+c(CHCOOH)=0.1mol/L,则
3 3
c(CHCOO-)=0.1mol/L- c(CHCOOH),又Ka= ,联立两式消去c(CHCOO-)并化
3 3 3
简整理可得出,c(CHCOOH)= mol/L,正确;D.醋酸根离子的水解平衡为:CHCOO-
3 3
+H O CHCOOH +OH-,pH由7到14的变化过程中,碱性不断增强,c(OH-)不断增大,则使不利
2 3于醋酸根离子的水解平衡,会使其水解程度减小,错误;答案选BC。
10.(2019·全国高考真题)NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸HA的K =1.1×10−3 ,
2 a1
K =3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错
a2
误的是
A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2−的导电能力之和大于HA−的
C.b点的混合溶液pH=7
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)
【答案】C
【解析】邻苯二甲酸氢钾为二元弱酸酸式盐,溶液呈酸性,向邻苯二甲酸氢钾溶液中加入氢氧化钠溶液,
两者反应生成邻苯二甲酸钾和邻苯二甲酸钠,溶液中离子浓度增大,导电性增强,邻苯二甲酸钾和邻
苯二甲酸钠为强碱弱酸盐,邻苯二甲酸根在溶液中水解使溶液呈碱性。A.向邻苯二甲酸氢钾溶液中
加入氢氧化钠溶液,两者反应生成邻苯二甲酸钾和邻苯二甲酸钠,溶液中Na+和A2—的浓度增大。由
图像可知,溶液导电性增强,说明导电能力与离子浓度和种类有关,正确;B.a点和b点K+的物质
的量相同,K+的物质的量浓度变化不明显,HA—转化为A2—,b点导电性强于a点,说明Na+和A2—的
导电能力强于HA—,正确;C.b点邻苯二甲酸氢钾溶液与氢氧化钠溶液恰好完全反应生成邻苯二甲
酸钾和邻苯二甲酸钠,邻苯二甲酸钾为强碱弱酸盐,A2—在溶液中水解使溶液呈碱性,溶液pH>7,
错误;D.b点邻苯二甲酸氢钾溶液与氢氧化钠溶液恰好完全反应生成等物质的量的邻苯二甲酸钾和
邻苯二甲酸钠,溶液中c(Na+)和c(K+)相等,c点是继续加入氢氧化钠溶液后,得到邻苯二甲酸
钾、邻苯二甲酸钠、氢氧化钠的混合溶液,则溶液中c(Na+)>c(K+),由图可知,a点到b点加入
氢氧化钠溶液的体积大于b点到c点加入氢氧化钠溶液的体积,则溶液中c(K+)>c(OH—),溶液
中三者大小顺序为c(Na+)>c(K+)>c(OH—),正确。故选C。
11.(2019·上海高考真题)用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,用甲基橙作指示剂,下列说法
正确的是( )
A.可以用酚酞代替指示剂
B.滴定前用待测液润洗锥形瓶
C.若氢氧化钠吸收少量CO,不影响滴定结果
2
D.当锥形瓶内溶液由橙色变为红色,且半分钟内不褪色,即达到滴定终点
【答案】C
【解析】A.酚酞的变色范围在8.2-10.0,指示剂变色,碱没有完全反应,故不能使用酚酞做指示剂,错误;
B.滴定前不能用待测液润洗锥形瓶,否则待测液的体积变大,影响测定结果,错误;C.氢氧化钠吸收少量二氧化碳后变为碳酸钠,当甲基橙做指示剂时,反应后都生成氯化钠,不影响盐酸的体积,所
以不影响滴定结果,正确;D.甲基橙在碱性溶液中显黄色,随着滴定的进行,溶液的颜色逐渐变为
橙色,滴定终点颜色为黄色变为橙色,且半分钟内不变色,若变为红色,说明盐酸已经过量,错误;
答案选C。
12.(2018·全国高考真题)用0.100 mol·L-1 AgNO 滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所
3
示。下列有关描述错误的是( )
A.根据曲线数据计算可知K (AgCl)的数量级为10-10
sp
B.曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=K (AgCl)
sp
C.相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a
D.相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动
【答案】C
【解析】本题应该从题目所给的图入手,寻找特定数据判断题目中的沉淀滴定的具体过程。注意:横坐标
是加入的硝酸银溶液的体积,纵坐标是氯离子浓度的负对数。A.选取横坐标为50mL的点,此时向
50mL 0.05mol/L的Cl-溶液中,加入了50mL 0.1mol/L的AgNO 溶液,所以计算出此时溶液中过量的
3
Ag+浓度为0.025mol/L(按照银离子和氯离子1:1沉淀,同时不要忘记溶液体积变为原来2倍),由图
示得到此时Cl-约为1×10-8mol/L(实际稍小),所以K (AgCl)约为0.025×10-8=2.5×10-10,所以其数量
SP
级为10-10,正确;B.由于K (AgCl)极小,所以向溶液滴加硝酸银就会有沉淀析出,溶液一直是氯化
SP
银的饱和溶液,所以c(Ag+)·c(Cl-)=K (AgCl),正确;C.滴定的过程是用硝酸银滴定氯离子,所以滴
SP
定的终点应该由原溶液中氯离子的物质的量决定,将50mL 0.05mol/L的Cl-溶液改为50mL 0.04mol/L
的Cl-溶液,此时溶液中的氯离子的物质的量是原来的0.8倍,所以滴定终点需要加入的硝酸银的量也
是原来的0.8倍,因此应该由c点的25mL变为25×0.8=20mL,而a点对应的是15mL,错误;D.卤化
银从氟化银到碘化银的溶解度应该逐渐减小,所以K (AgCl)应该大于K (AgBr),将50mL 0.05mol/L
SP SP
的Cl-溶液改为50mL 0.05mol/L的Br-溶液,这是将溶液中的氯离子换为等物质的量的溴离子,因为银
离子和氯离子或溴离子都是1:1沉淀的,所以滴定终点的横坐标不变,但是因为溴化银更难溶,所以
终点时,溴离子的浓度应该比终点时氯离子的浓度更小,所以有可能由a点变为b点,正确;故答案
选C。
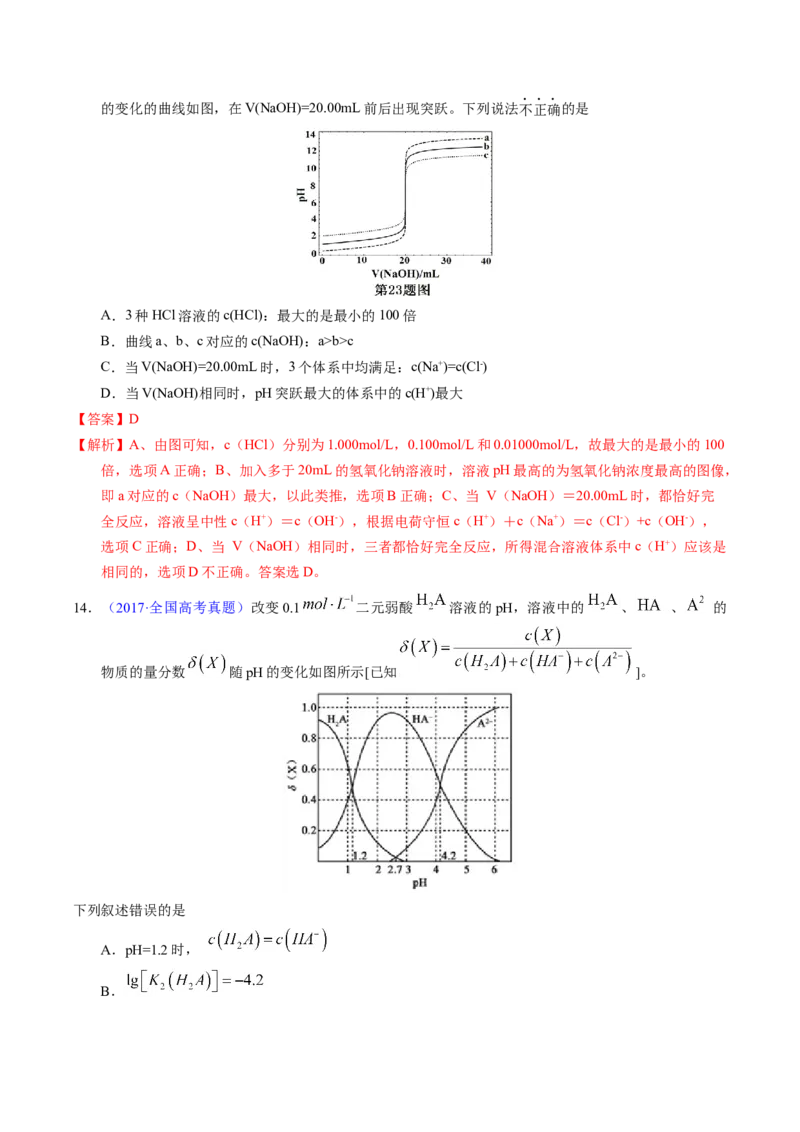
13.(2018·浙江高考真题)常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度
为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。下列说法不正确的是
A.3种HCl溶液的c(HCl):最大的是最小的100倍
B.曲线a、b、c对应的c(NaOH):a>b>c
C.当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)
D.当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
【答案】D
【解析】A、由图可知,c(HCl)分别为1.000mol/L,0.100mol/L和0.01000mol/L,故最大的是最小的100
倍,选项A正确;B、加入多于20mL的氢氧化钠溶液时,溶液pH最高的为氢氧化钠浓度最高的图像,
即a对应的c(NaOH)最大,以此类推,选项B正确;C、当 V(NaOH)=20.00mL时,都恰好完
全反应,溶液呈中性c(H+)=c(OH-),根据电荷守恒c(H+)+c(Na+)=c(Cl-)+c(OH-),
选项C正确;D、当 V(NaOH)相同时,三者都恰好完全反应,所得混合溶液体系中c(H+)应该是
相同的,选项D不正确。答案选D。
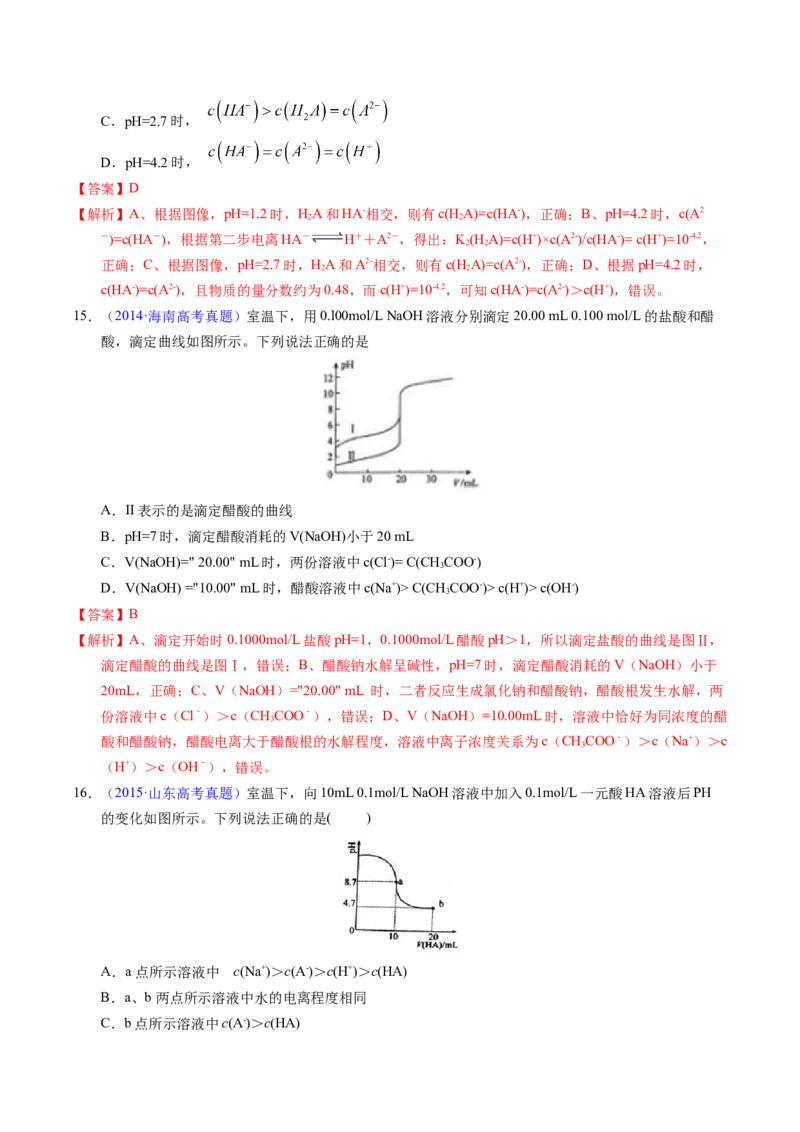
14.(2017·全国高考真题)改变0.1 二元弱酸 溶液的pH,溶液中的 、 、 的
物质的量分数 随pH的变化如图所示[已知 ]。
下列叙述错误的是
A.pH=1.2时,
B.C.pH=2.7时,
D.pH=4.2时,
【答案】D
【解析】A、根据图像,pH=1.2时,HA和HA-相交,则有c(HA)=c(HA-),正确;B、pH=4.2时,c(A2
2 2
-)=c(HA-),根据第二步电离HA- H++A2-,得出:K(H A)=c(H+)×c(A2-)/c(HA-)= c(H+)=10-4.2,
2 2
正确;C、根据图像,pH=2.7时,HA和A2-相交,则有c(HA)=c(A2-),正确;D、根据pH=4.2时,
2 2
c(HA-)=c(A2-),且物质的量分数约为0.48,而c(H+)=10-4.2,可知c(HA-)=c(A2-)>c(H+),错误。
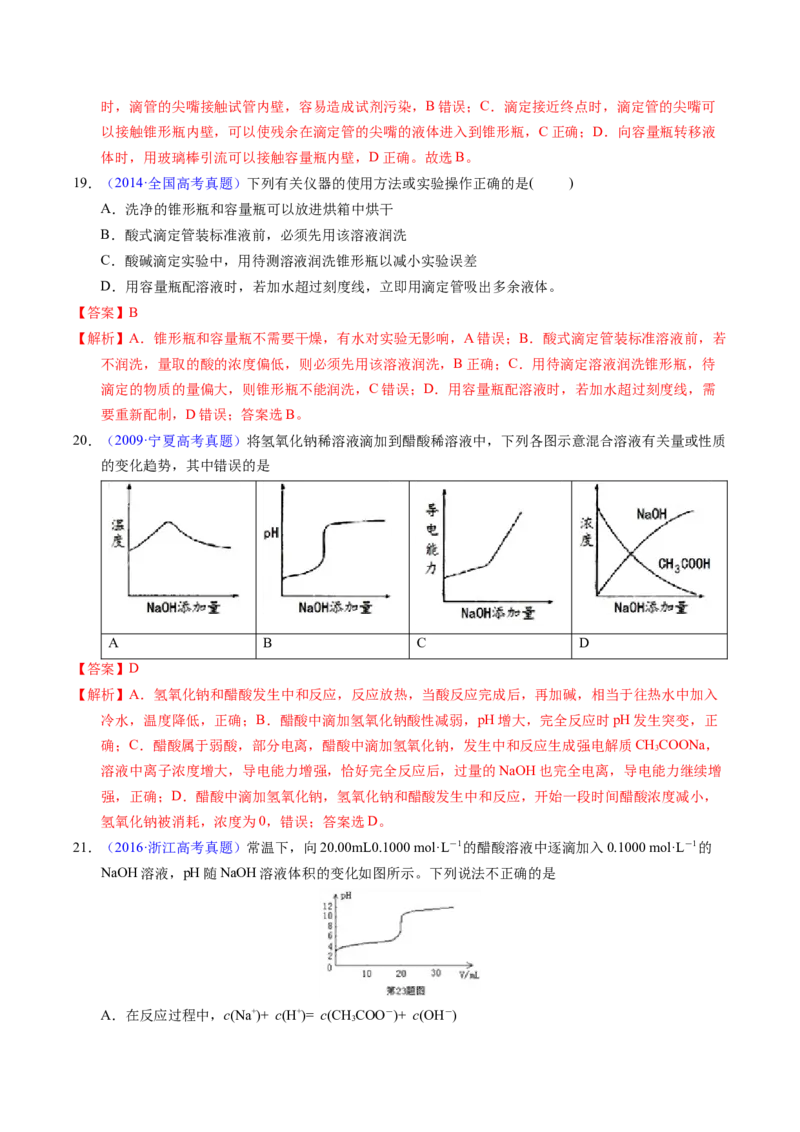
15.(2014·海南高考真题)室温下,用0.l00mol/L NaOH溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋
酸,滴定曲线如图所示。下列说法正确的是
A.II表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20 mL
C.V(NaOH)=" 20.00" mL时,两份溶液中c(Cl-)= C(CH COO-)
3
D.V(NaOH) ="10.00" mL时,醋酸溶液中c(Na+)> C(CH COO-)> c(H+)> c(OH-)
3
【答案】B
【解析】A、滴定开始时0.1000mol/L盐酸pH=1,0.1000mol/L醋酸pH>1,所以滴定盐酸的曲线是图Ⅱ,
滴定醋酸的曲线是图Ⅰ,错误;B、醋酸钠水解呈碱性,pH=7时,滴定醋酸消耗的V(NaOH)小于
20mL,正确;C、V(NaOH)="20.00" mL 时,二者反应生成氯化钠和醋酸钠,醋酸根发生水解,两
份溶液中c(Cl﹣)>c(CHCOO﹣),错误;D、V(NaOH)=10.00mL时,溶液中恰好为同浓度的醋
3
酸和醋酸钠,醋酸电离大于醋酸根的水解程度,溶液中离子浓度关系为c(CHCOO﹣)>c(Na+)>c
3
(H+)>c(OH﹣),错误。
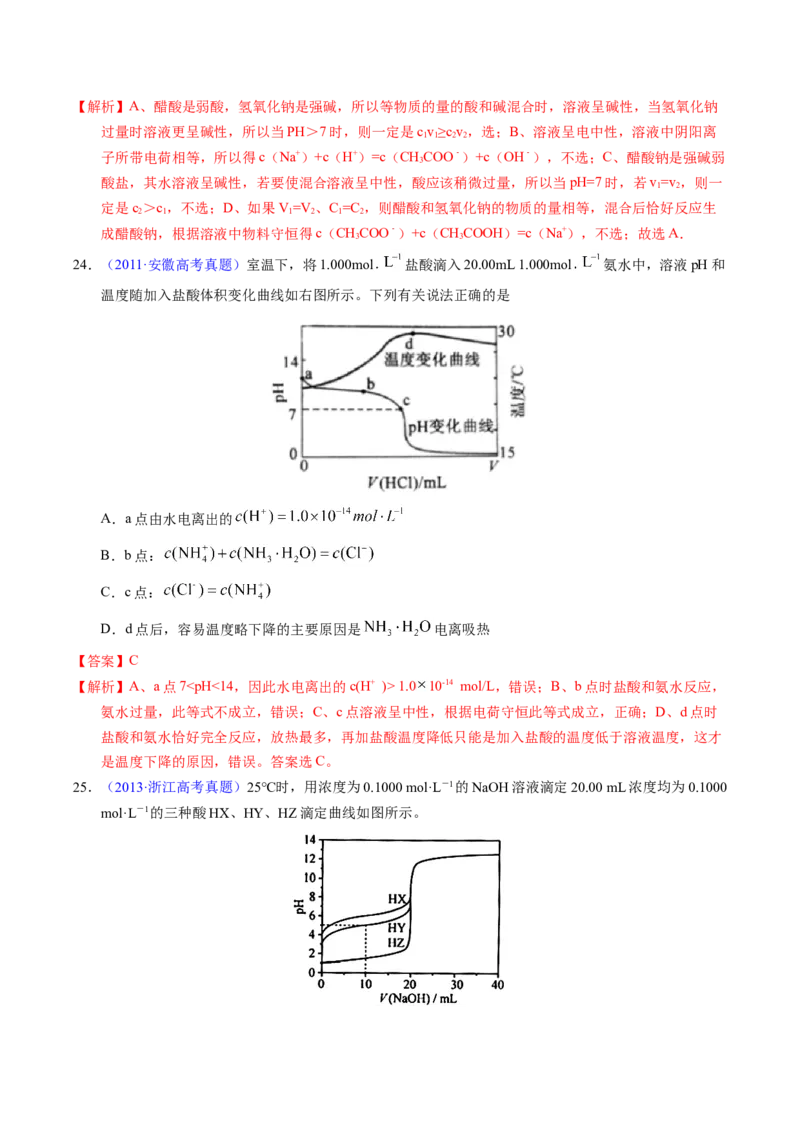
16.(2015·山东高考真题)室温下,向10mL 0.1mol/L NaOH溶液中加入0.1mol/L一元酸HA溶液后PH
的变化如图所示。下列说法正确的是( )
A.a 点所示溶液中 c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b 两点所示溶液中水的电离程度相同
C.b点所示溶液中c(A-)>c(HA)D.pH=7时,c(Na+)=c(A-)+c(HA)
【答案】C
【解析】A.a点时消耗0.1mol/L一元酸HA10mL,酸碱恰好中和生成盐,溶液pH=8.7,溶液显碱性,则
该盐为强碱弱酸盐,说明HA为弱酸,NaA溶液水解呈碱性,应为c(HA)>c(H+),错误;B.a点A-水
解,促进水的电离,b点时HA过量,溶液呈酸性,HA电离出H+,抑制水的电离,错误;C.b点加
入0.1mol/L一元酸HA溶液20mL,HA过量一倍,溶液存在NaA和HA,此时溶液的pH=4.7,溶液呈
酸性,说明HA电离程度大于A-水解程度,则存在c(A-)>c(HA),正确;D.pH=7时,c(H+)=c(OH-),
由电荷守恒可知c(Na+)+c(H+)=c(A-)+c(OH-),则c(Na+)=c(A-),错误;答案选C。
17.(2016·全国高考真题)298 K时,在20.0 mL 0.10mol·L-1氨水中滴入0.10mol·L-1的盐酸,溶液的pH
与所加盐酸的体积关系如图所示。已知0.10 mol·L-1 氨水的电离度为1.32%,下列有关叙述正确的是
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH +)=c(Cl-)=c(H+)=c(OH-)
4
D.N点处的溶液中pH<12
【答案】D
【解析】A.强酸弱碱相互滴定时,由于生成强酸弱碱盐使溶液显酸性,而石蕊的变色范围为5-8,无法控
制滴定终点,应选择甲基橙作指示剂,错误;B.如果M点盐酸体积为20.0mL,则二者恰好完全反应
生成氯化铵,氯化铵中铵根离子水解导致该点溶液应该呈酸性,要使溶液呈中性,则氨水应该稍微过
量,所以盐酸体积小于20.0mL,错误;C.M处溶液呈中性,则存在c(H+)=c(OH-),根据电荷
守恒得c(NH +)=c(Cl-),该点溶液中溶质为氯化铵和一水合氨,铵根离子水解而促进水电离、一
4
水合氨抑制水电离,铵根离子水解和一水合氨电离相互抑制,水的电离程度很小,该点溶液中离子浓
度大小顺序是c(NH +)=c(Cl-)>c(H+)=c(OH-),错误;D.N点为氨水溶液,氨水浓度为
4
0.10mol•L-1,该氨水电离度为1.32%,则该溶液中c(OH-)=0.10mol/L×1.32%=1.32×10-3 mol/L,c
(H+)=
18.(2016·海南高考真题)下列有关实验操作的叙述错误的是
A.过滤操作中,漏斗的尖端应接触烧杯内壁
B.从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁
C.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
D.向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁
【答案】B
【解析】A.过滤操作中,漏斗的尖端应接触烧杯内壁,使液体顺利流下,A正确;B.从滴瓶中取用试剂时,滴管的尖嘴接触试管内壁,容易造成试剂污染,B错误;C.滴定接近终点时,滴定管的尖嘴可
以接触锥形瓶内壁,可以使残余在滴定管的尖嘴的液体进入到锥形瓶,C正确;D.向容量瓶转移液
体时,用玻璃棒引流可以接触容量瓶内壁,D正确。故选B。
19.(2014·全国高考真题)下列有关仪器的使用方法或实验操作正确的是( )
A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B.酸式滴定管装标准液前,必须先用该溶液润洗
C.酸碱滴定实验中,用待测溶液润洗锥形瓶以减小实验误差
D.用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体。
【答案】B
【解析】A.锥形瓶和容量瓶不需要干燥,有水对实验无影响,A错误;B.酸式滴定管装标准溶液前,若
不润洗,量取的酸的浓度偏低,则必须先用该溶液润洗,B正确;C.用待滴定溶液润洗锥形瓶,待
滴定的物质的量偏大,则锥形瓶不能润洗,C错误;D.用容量瓶配溶液时,若加水超过刻度线,需
要重新配制,D错误;答案选B。
20.(2009·宁夏高考真题)将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量或性质
的变化趋势,其中错误的是
A B C D
【答案】D
【解析】A.氢氧化钠和醋酸发生中和反应,反应放热,当酸反应完成后,再加碱,相当于往热水中加入
冷水,温度降低,正确;B.醋酸中滴加氢氧化钠酸性减弱,pH增大,完全反应时pH发生突变,正
确;C.醋酸属于弱酸,部分电离,醋酸中滴加氢氧化钠,发生中和反应生成强电解质CHCOONa,
3
溶液中离子浓度增大,导电能力增强,恰好完全反应后,过量的NaOH也完全电离,导电能力继续增
强,正确;D.醋酸中滴加氢氧化钠,氢氧化钠和醋酸发生中和反应,开始一段时间醋酸浓度减小,
氢氧化钠被消耗,浓度为0,错误;答案选D。
21.(2016·浙江高考真题)常温下,向20.00mL0.1000 mol·L-1的醋酸溶液中逐滴加入0.1000 mol·L-1的
NaOH溶液,pH随NaOH溶液体积的变化如图所示。下列说法不正确的是
A.在反应过程中,c(Na+)+ c(H+)= c(CHCOO-)+ c(OH-)
3B.pH=5时,c(CHCOO-)> c(Na+)> c(H+)> c(OH-)
3
C.pH=6时,c(Na+)+ c(H+)-c(OH-)+ c(CHCOOH)=0.1000 mol·Lˉ1
3
D.pH=7时,消耗NaOH溶液的体积小于20.00mL
【答案】C
【解析】A.根据电荷守恒可知:c(Na+)+c(H+)=c(CH COO-)+c(OH-),正确;B.pH=5时,溶液呈酸性,以
3
醋酸电离为主,所以离子浓度的大小为:c(CHCOO-)>c(Na+)>c(H+)>c(OH-),正确;C.根据电荷守
3
恒可知:c(Na+)+c(H+)=c(OH-)+c(CH COO-),两者混合pH=6,则氢氧化钠溶液的体积小于20.00mL,
3
物料守恒可知:c(CHCOO-)+c(CH COOH)>0.05mol/L,所以c(Na+)+c(H+)-c(OH-)+c(CH COOH)=0.05
3 3 3
mol/L, 错误;D.如果消耗NaOH溶液的体积为20.00mL,两者恰好完全反应生成醋酸钠,溶液水
解呈碱性,而溶液呈中性,所以消耗NaOH溶液的体积小于20.00mL,正确;故选C。
22.(2013·山东高考真题)某温度下,向一定体积 0.1mol/L 醋酸溶液中逐滴加入等浓度的NaOH溶液,
溶液中pOH (pOH = -lg[OH-])与pH的变化关系如图所示,则
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CHCOO-)>c(Na+)
3
C.M点和N点所示溶液中水的电离程度可能相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
【答案】C
【解析】A.醋酸是弱酸,加入NaOH后反应生成CHCOONa,CHCOONa是强电解质,M点溶质是
3 3
CHCOOH和CHCOONa,CHCOOH量较多,导电能力最弱,故错误;B.N点溶液显碱性,根据电
3 3 3
荷守恒,应是c(Na+)>c(CH COO-),故错误;C.M点的H+浓度等于N点OH-浓度,M点为醋酸和
3
醋酸钠的混合液,溶液呈酸性,水的电离受到抑制。N点对应的溶液呈碱性,若N点对应的是醋酸钠和
氢氧化钠的混合液时,水的电离程度相同;若N点恰好为醋酸钠溶液,则水的电离程度不同,正确;
D.Q点溶液显中性,消耗的NaOH的体积略小于醋酸溶液的体积,故错误。故选C。
23.(2011·全国高考真题)室温时,将浓度和体积分别为 、 的NaOH溶液和 、 的CHCOOH溶
3
液相混合,下列关于该混合溶液的叙述错误的是
A.若pH>7,则一定是cV=cV
1 1 2 2
B.在任何情况下都是c(Na+)+c(H+)=c(CH COO-)+c(OH-)
3
C.当pH=7时,若V=V ,则一定是c>c
1 2 1 2
D.若V=V ,c=c,则c(CHCOO-)+ c(CHCOOH)= c(Na+)
1 2 1 2 3 3
【答案】A【解析】A、醋酸是弱酸,氢氧化钠是强碱,所以等物质的量的酸和碱混合时,溶液呈碱性,当氢氧化钠
过量时溶液更呈碱性,所以当PH>7时,则一定是cv≥cv,选;B、溶液呈电中性,溶液中阴阳离
1 1 2 2
子所带电荷相等,所以得c(Na+)+c(H+)=c(CHCOO﹣)+c(OH﹣),不选;C、醋酸钠是强碱弱
3
酸盐,其水溶液呈碱性,若要使混合溶液呈中性,酸应该稍微过量,所以当pH=7时,若v=v,则一
1 2
定是c>c,不选;D、如果V=V 、C =C ,则醋酸和氢氧化钠的物质的量相等,混合后恰好反应生
2 1 1 2 1 2
成醋酸钠,根据溶液中物料守恒得c(CHCOO﹣)+c(CHCOOH)=c(Na+),不选;故选A.
3 3
24.(2011·安徽高考真题)室温下,将1.000mol 盐酸滴入20.00mL 1.000mol 氨水中,溶液pH和
温度随加入盐酸体积变化曲线如右图所示。下列有关说法正确的是
A.a点由水电离出的
B.b点:
C.c点:
D.d点后,容易温度略下降的主要原因是 电离吸热
【答案】C
【解析】A、a点7 1.0 10-14 mol/L,错误;B、b点时盐酸和氨水反应,
氨水过量,此等式不成立,错误;C、c点溶液呈中性,根据电荷守恒此等式成立,正确;D、d点时
盐酸和氨水恰好完全反应,放热最多,再加盐酸温度降低只能是加入盐酸的温度低于溶液温度,这才
是温度下降的原因,错误。答案选C。
25.(2013·浙江高考真题)25℃时,用浓度为0.1000 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.1000
mol·L-1的三种酸HX、HY、HZ滴定曲线如图所示。下列说法正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得K(HY)≈10-5
a
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>
c(OH-)>c(H+)
D.HY与HZ混合,达到平衡时:c(H+)= +c(Z-)+c(OH-)
【答案】B
【解析】浓度均为0.1000 mol/L的三种酸HX、HY、HZ,根据滴定曲线0点三种酸的pH可得到HZ是强酸
HY和HX是弱酸,但酸性:HY>HX。A选项:同温同浓度时,三种酸的导电性:HZ>HY>HX。B
选项:当NaOH溶液滴加到10 mL时,溶液中c(HY)≈c(Y—),即K(HY)≈c(H+)=10—pH=10—5。C选项:
a
用NaOH溶液滴定至HX恰好完全反应时,HY早被完全中和,所得溶液是NaY和NaX混合溶液;但
因酸性:HY>HX,即X—的水解程度大于Y—,溶液中c(Y—)>c(X—)。D选项:HY与HZ混合,溶液
的电荷守恒式为:c(H+)= c(Y—)+ c(Z—) +c(OH—),又根据 HY 的电离平衡常数:K(HY)=
a
即有:c(Y—)= ,所以达平衡后:c(H+)= + c(Z—) +c(OH—)
26.(2015·广东高考真题)准确移取20.00 mL某待测 HCl溶液于锥形瓶中,用0.100 0 mol·L-1 NaOH溶
液滴定。下列说法正确的是 ( )
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏大
【答案】BD
【解析】A.滴定管使用之前必须用NaOH标准液润洗,否则消耗的标准液体积偏大,测定酸的浓度偏大,
A错误;B.碱滴定酸,氢离子浓度逐渐减小,则随着NaOH溶液滴入,锥形瓶中溶液pH由小变大,
B正确;C.用酚酞作指示剂,滴定前锥形瓶中为无色溶液,则当锥形瓶中溶液由无色变红色且30s内
不褪去时,停止滴定,C错误;D.滴定终点时,发现滴定管尖嘴部分有悬滴,则消耗的标准液体积
偏大,则测定酸的浓度偏大,D正确;答案选BD。
27.(2012·江苏高考真题)250C时,有c(CHCOOH)+c(CH COO-)=0.1mol·L-1的一组醋酸、醋酸钠混合溶
3 3
液,溶液中c(CHCOOH)、c(CHCOO-)与pH 的关系如图7 所示。下列有关溶液中离子浓度关系的叙
3 3
述正确的是A.pH=5.5 的溶液中: c(CHCOOH)>c(CH COO-)>c(H+)>c(OH-)
3 3
B.W 点所表示的溶液中: c(Na+)+c(H+)= c(CHCOOH)+c(OH-)
3
C.pH =3.5 的溶液中: c(Na+) +c(H+) -c(OH-) +c(CHCOOH)=0.1mol·L-1
3
D.向W 点所表示的1.0L 溶液中通入0.05mol HCl 气体(溶液体积变化可忽略): c(H+)=
c(CHCOOH)+c(OH-)
3
【答案】BC
【解析】分析pH变化,可分析出降低的是醋酸浓度,升高的是醋酸根离子浓度。A选项错误,由图直接
看出离子浓度大于分子浓度;B选项正确,w点醋酸分子浓度大于醋酸根离子浓度,所以该关系是溶
液的电荷守恒;C选项正确,等式中的前3项即醋酸根离子浓度,该式即题中的等式关系;D选项错
误,理论上氯化氢与醋酸根离子全部反应,生成醋酸,醋酸是弱电解质,溶液中氢离子浓度较小,比
可能大于醋酸浓度。
28.(2012·上海高考真题)用滴定法测定NaCO(含NaCl杂质)的质量分数,下列操作会引起测定值偏高的
2 3
是( )
A.试样中加入酚酞作指示剂,用标准酸液进行滴定
B.滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定
C.锥形瓶用蒸馏水洗涤后,直接注入待测溶液进行滴定
D.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00 mL进行滴定
【答案】B
【解析】此实验过程中,待测值为c(Na CO),根据酸与NaCO 的反应可知:c(Na CO)·V =k·c ·V (k
2 3 2 3 2 3 待测液 酸 酸
为标准酸与NaCO 反应时的化学计量数之比)。A.加入酚酞对实验数据无影响;B.此操作使V 数
2 3 酸
值偏大,故使c(Na CO)偏大,最终所得NaCO 质量分数偏高;C.此操作对实验数据无影响;D.此
2 3 2 3
操作使c(Na CO)数值偏小,最终使所得NaCO 质量分数偏低。
2 3 2 3
29.(2013·天津高考真题)下列实验误差分析错误的是( )
A.用湿润的pH试纸测稀碱液的pH,测定值偏小
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小
【答案】B
【解析】A.湿润的pH值试纸可以稀释碱液,溶液中氢氧根离子浓度减小,测定的溶液碱性减弱,测定值偏小,正确;B.定容时俯视刻度线,导致所配溶液的体积偏小,结合c= 可知,所配溶液的浓度偏
大,错误;C.滴定前滴定管内无气泡,终点读数时有气泡,气体占据液体应占有的体积,会导致所
测溶液体积偏小,正确;D.测定中和反应的反应热时,将碱缓慢倒入酸中,导致热量损失过大,所
测温度值偏小,正确;故选B。
30.(2018·浙江高考真题)某兴趣小组用镀锌铁皮按下列流程制备七水合硫酸锌(ZnSO·7H O)
4 2
请回答:
(6)ZnSO ·7H O产品的纯度可用配位滴定法测定。
4 2
① 下列关于滴定分析,正确的是________________。
A.图2中,应将凡士林涂在旋塞的a端和旋塞套内的c端
B.滴定前,锥形瓶和滴定管均须用标准溶液润洗
C.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
D.滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
E.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡,则测得的体积比实际消耗的小
②图3中显示滴定终点时的度数是_____________mL。
【答案】(6)ADE 20.60
【解析】
(6)①A、在涂抹凡土林时不能将旋塞的小孔堵住,故涂抹在旋塞a端和旋塞套内的c端,选项A正确;
B、滴定前锥形瓶不能用标准液润洗,会使测定结果产生偏差,选项B错误;C、标准液装入滴定管时
直接倒入,借助其他玻璃仪器可能会产生污染试剂,产生误差,选项C错误;D、滴定时,用左手控
制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转,选项D正确;E、滴定前无气泡、滴定
后产生气泡,滴加的溶液比实际消耗的体积要小,选项E正确。答案选ADE;②滴定管的读数从上向
下,并且精确到小数点后两位。读数为20.60 mL。
31.(2013·江苏高考真题)硫酸镍铵[(NH )Ni (SO ) ·nH O]可用于电镀、印刷等领域。某同学为测定硫酸
4 x y 4 m 2
镍铵的组成,进行如下实验:①准确称取2. 3350 g 样品,配制成100. 00 mL 溶液A;②准确量取25.
00 mL 溶液A,用0. 04000 mol·L-1 的EDTA(Na HY)标准溶液滴定其中的Ni2+(离子方程式为Ni2+
2 2
+H Y2-=NiY2-+2H+),消耗EDTA 标准溶液31. 25 mL;③另取25. 00 mL溶液A,加足量的NaOH 溶
2
液并充分加热,生成NH 56. 00 mL(标准状况)。
3(1)若滴定管在使用前未用EDTA 标准溶液润洗,测得的Ni2+含量将_________(填“偏高”、或“偏
低”或“不变”)。
(2)氨气常用__________________检验,现象是________________。
(3)通过计算确定硫酸镍铵的化学式(写出计算过程)。________
【答案】(1)偏高 (2)湿润的红色石蕊试纸 试纸颜色由红变蓝 (3)(NH )Ni(SO )·10H O
4 2 4 2 2
【解析】
(1)若滴定管在使用前未用EDTA标准液润洗,EDTA标准液的浓度就会偏低,则滴定消耗的EDTA标准
液的体积偏大,测得的Ni2+含量将偏高。
(2)氨气的检验有两种常用的方法:①湿润的红色石蕊试纸,现象是试纸由红色变为蓝色;②浓盐酸,
现象是用玻璃棒蘸取浓盐酸,靠近待测气体,产生白烟。
(3)25.00mL溶液中
n(Ni2+)=0.04000 mol·L-1×31. 25 mL×10-3L·mL-1=1.250×10-3mol
n(NH +)=n(NH )= =2.500×10-3mol
4 3
根据电荷守恒,n(SO 2-)= = =2.500×10-3mol
4
m(Ni2+)=59 g·mol-1×1. 250×10-3mol=0.07375 g
m(NH +)=18g·mol-1×2. 500×10-3mol=0.04500 g
4
m(SO2-)=96g·mol-1×2. 500×10-3mol=0.2400 g
4
n(H O)= =1.250×10-2mol
2
x :y :m:n= n(NH +):n(Ni2+):n(SO 2-):n(H O)=2:1:2:10
4 4 2
硫酸镍铵的化学式为(NH )Ni(SO )·10H O
4 2 4 2 2
32.(2017·江苏高考真题)砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措
施之一。
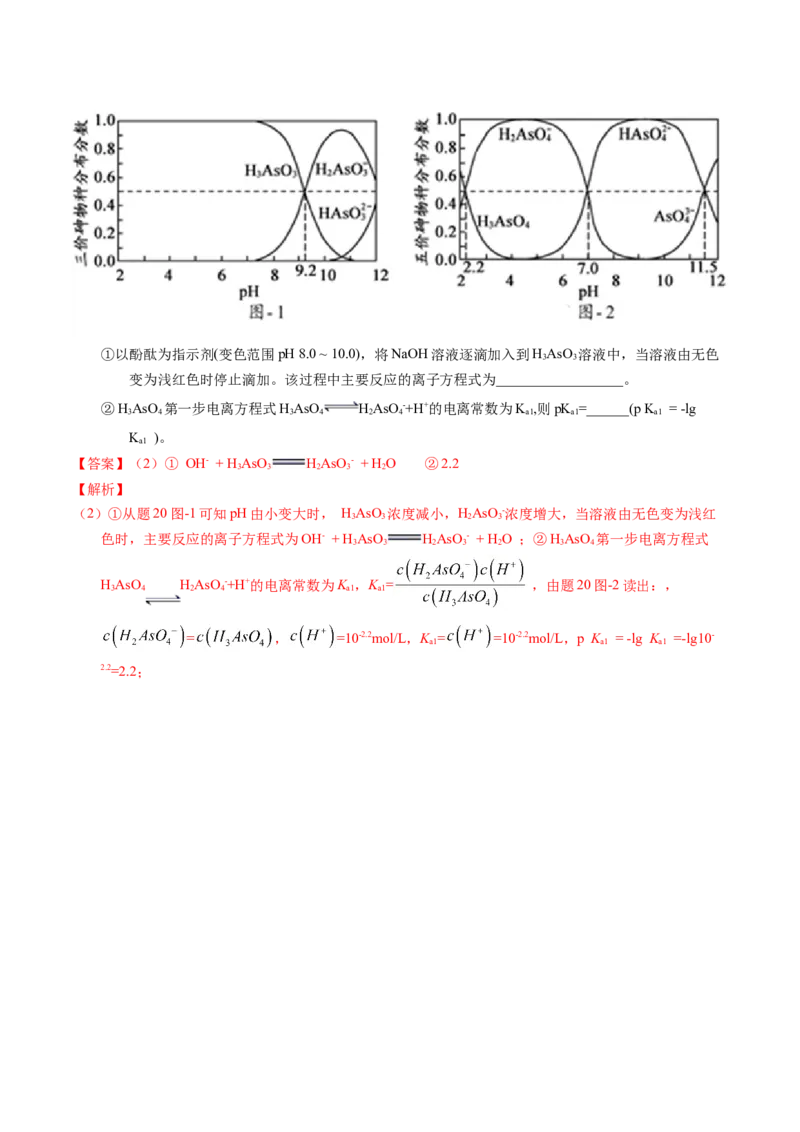
(2)HAsO 和HAsO 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)
3 3 3 4
与pH的关系分别如图- 1和图- 2所示。①以酚酞为指示剂(变色范围pH 8.0 ~ 10.0),将NaOH溶液逐滴加入到HAsO 溶液中,当溶液由无色
3 3
变为浅红色时停止滴加。该过程中主要反应的离子方程式为__________________。
②HAsO 第一步电离方程式HAsO HAsO -+H+的电离常数为K ,则pK =______(p K = -lg
3 4 3 4 2 4 a1 a1 a1
K )。
a1
【答案】(2)① OH- + H AsO HAsO - + H O ②2.2
3 3 2 3 2
【解析】
(2)①从题20图-1可知pH由小变大时, HAsO 浓度减小,HAsO -浓度增大,当溶液由无色变为浅红
3 3 2 3
色时,主要反应的离子方程式为OH- + H AsO HAsO - + H O ;②HAsO 第一步电离方程式
3 3 2 3 2 3 4
HAsO HAsO -+H+的电离常数为K ,K = ,由题20图-2读出:,
3 4 2 4 a1 a1
= , =10-2.2mol/L,K = =10-2.2mol/L,p K = -lg K =-lg10-
a1 a1 a1
2.2=2.2;