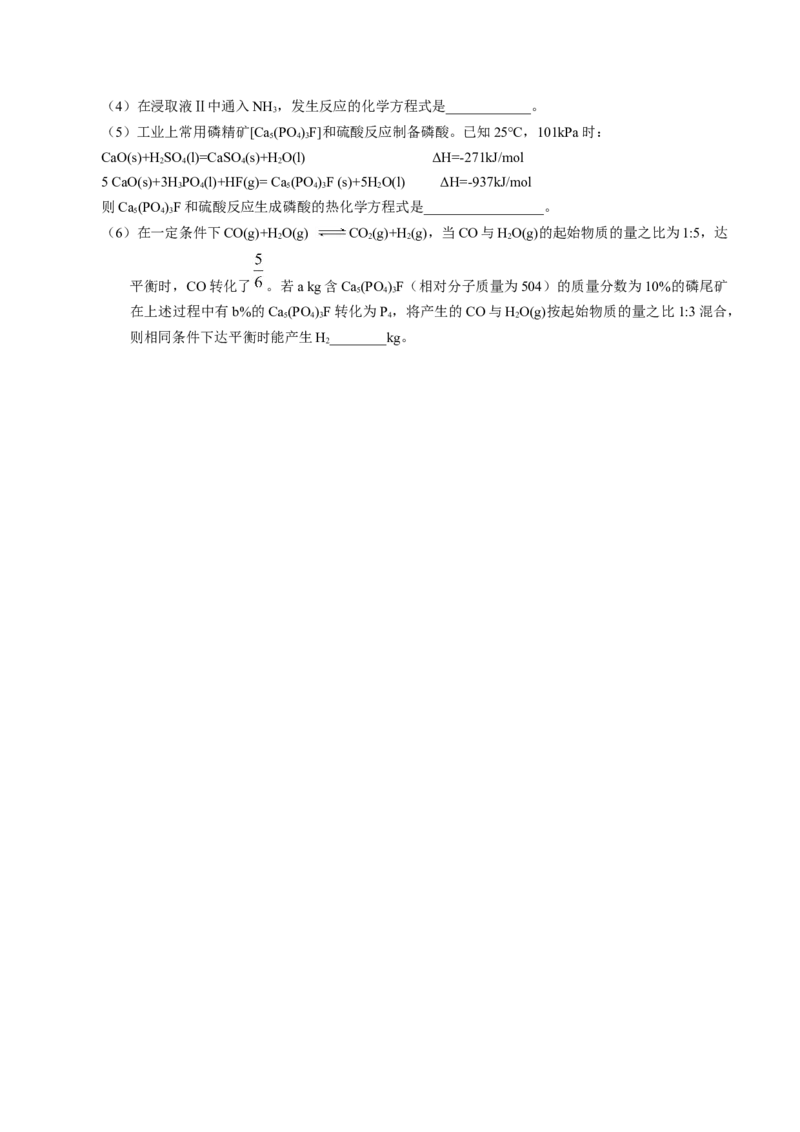文档内容
专题95 工艺流程——污染处理载体
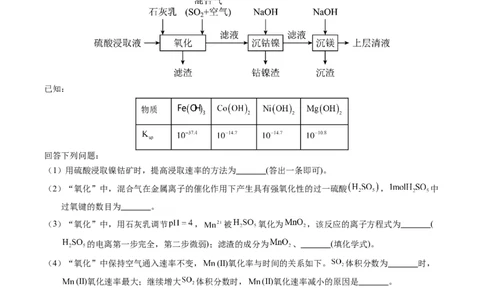
1.【2023年辽宁卷】某工厂采用如下工艺处理镍钴矿硫酸浸取液含( 和
)。实现镍、钴、镁元素的回收。
已知:
物质
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为 (答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸 , 中
过氧键的数目为 。
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为 (
的电离第一步完全,第二步微弱);滤渣的成分为 、 (填化学式)。
(4)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如下。 体积分数为 时,
(Ⅱ)氧化速率最大;继续增大 体积分数时, (Ⅱ)氧化速率减小的原因是 。(5)“沉钴镍”中得到的 (Ⅱ)在空气中可被氧化成 ,该反应的化学方程式为 。
(6)“沉镁”中为使 沉淀完全 ,需控制 不低于 (精确至0.1)。
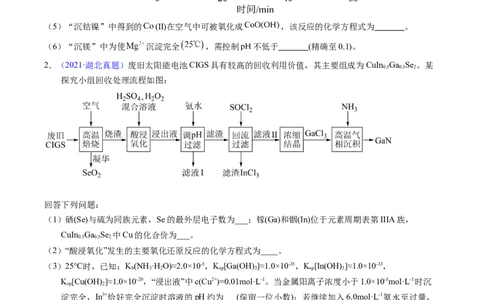
2.(2021·湖北真题)废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为CuIn Ga Se 。某
0.5 0.5 2
探究小组回收处理流程如图:
回答下列问题:
(1)硒(Se)与硫为同族元素,Se的最外层电子数为___;镓(Ga)和铟(In)位于元素周期表第IIIA族,
CuIn Ga Se 中Cu的化合价为___。
0.5 0.5 2
(2)“酸浸氧化”发生的主要氧化还原反应的化学方程式为____。
(3)25℃时,已知:K(NH ·H O)≈2.0×10-5,K [Ga(OH)]≈1.0×10-35,K [In(OH) ]≈1.0×10-33,
b 3 2 sp 3 sp 3
K [Cu(OH) ]≈1.0×10-20,“浸出液”中c(Cu2+)=0.01mol·L-1。当金属阳离子浓度小于1.0×10-5mol·L-1时沉
sp 2
淀完全,In3+恰好完全沉淀时溶液的pH约为___(保留一位小数);若继续加入6.0mol·L-1氨水至过量,
观察到的实验现象是先有蓝色沉淀,然后___;为探究Ga(OH) 在氨水中能否溶解,计算反应
3
Ga(OH) +NH·H O [Ga(OH)]-+NH 的平衡常数K=___。
3 3 2 4
(已知:Ga3++4OH- [Ga(OH)]- K′= ≈1.0×1034)
4
(4)“滤渣”与SOCl 混合前需要洗涤、干燥,检验滤渣中SO 是否洗净的试剂是___;“回流过滤”中
2
SOCl 的作用是将氢氧化物转化为氯化物和___。
2
(5)“高温气相沉积”过程中发生的化学反应方程式为___。3.【2021年重庆卷】电镀在工业生产中具有重要作用,某电镀厂生产的废水经预处理后含有 和少
量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
已知: K (CuS)=6.3 ×10-36和K (NiS)=3.0×10-19
sp sp
回答下列问题:
(1) 中Cr元素的化合价为_______。
(2)还原池中有Cr3+生成,反应的离子方程式为_______。
(3)沉淀1为Cr(OH) ,其性质与Al(OH) 相似,则Cr(OH) 与NaOH溶液反应的化学方程式_______。
3 3 3
(4)NaS溶液呈碱性的原因是_______(用离子方程式表示),沉淀2为_______。
2
(5)若废水中还含有Cd2+,pH=4时Cd2+的浓度为_______mol·L-1,用该结果说明Cd2+影响上述流程进行分
离的原因是_______(设HS平衡浓度为1.0× 10-6mol·L-1。已知:HS的K=1.0×10-7,K=7.0×10-15,
2 2 1 2
Ksp(CdS)=7.0×10-27)
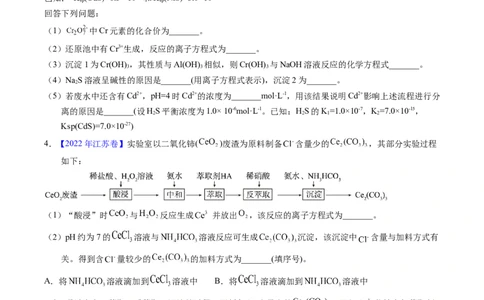
4.【2022年江苏卷】实验室以二氧化铈( )废渣为原料制备 含量少的 ,其部分实验过程
如下:
(1)“酸浸”时 与 反应生成 并放出 ,该反应的离子方程式为_______。
(2)pH约为7的 溶液与 溶液反应可生成 沉淀,该沉淀中 含量与加料方式有
关。得到含 量较少的 的加料方式为_______(填序号)。
A.将 溶液滴加到 溶液中 B.将 溶液滴加到 溶液中
(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的 。已知 能被有机萃取剂
(简称HA)萃取,其萃取原理可表示为
(水层)+3HA(有机层) (有机层)+ (水层)
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是_______。
②反萃取的目的是将有机层 转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或
采取的实验操作有_______(填两项)。
③与“反萃取”得到的水溶液比较,过滤 溶液的滤液中,物质的量减小的离子有
_______(填化学式)。(4)实验中需要测定溶液中 的含量。已知水溶液中 可用准确浓度的 溶液滴定。
以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
。请补充完整实验方案:①准确量取 溶液[ 约为 ],
加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后
定容;②按规定操作分别将 和待测 溶液装入如图所示的滴定管中:
③_______。
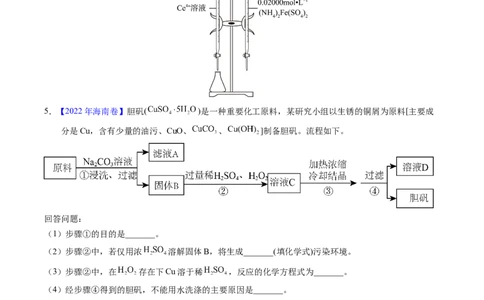
5.【2022年海南卷】胆矾( )是一种重要化工原料,某研究小组以生锈的铜屑为原料[主要成
分是Cu,含有少量的油污、CuO、 、 ]制备胆矾。流程如下。
回答问题:
(1)步骤①的目的是_______。
(2)步骤②中,若仅用浓 溶解固体B,将生成_______(填化学式)污染环境。
(3)步骤②中,在 存在下Cu溶于稀 ,反应的化学方程式为_______。
(4)经步骤④得到的胆矾,不能用水洗涤的主要原因是_______。
(5)实验证明,滤液D能将 氧化为 。
ⅰ.甲同学认为不可能是步骤②中过量 将 氧化为 ,理由是_______。
ⅱ.乙同学通过实验证实,只能是 将 氧化为 ,写出乙同学的实验方案及结果_______(不要求写具体
操作过程)。
6.(2021.1·浙江真题)某兴趣小组用铬铁矿[Fe(CrO )]制备KCr O 晶体,流程如下:
2 2 2 2 7已知:4Fe (CrO ) + 10Na CO+7O 8NaCrO +4NaFeO+10CO
2 2 2 3 2 2 4 2 2
2H++2CrO Cr O +H O
2 2
相关物质的溶解度随温度变化如下图。
请回答:
(1)步骤I,将铬铁矿粉碎有利于加快高温氧化的速率,其理由是______。
(2)下列说法正确的是______。
A.步骤II,低温可提高浸取率
B.步骤II,过滤可除去NaFeO 水解产生的Fe(OH)
2 3
C.步骤III,酸化的目的主要是使NaCrO 转变为NaCr O
2 4 2 2 7
D.步骤IV,所得滤渣的主要成分是NaSO 和NaCO
2 4 2 3
(3)步骤V,重结晶前,为了得到杂质较少的KCr O 粗产品,从下列选项中选出合理的操作(操作不能重
2 2 7
复使用)并排序:溶解KCl →______→______→______→______→重结晶。
a.50℃蒸发溶剂;
b.100℃ 蒸发溶剂;
c.抽滤;
d.冷却至室温;
e.蒸发至溶液出现晶膜,停止加热;
f.蒸发至溶液中出现大量晶体,停止加热。
(4)为了测定KCr O 产品的纯度,可采用氧化还原滴定法。
2 2 7
①下列关于滴定分析的操作,不正确的是______。
A.用量筒量取25.00mL待测液转移至锥形瓶B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
②在接近终点时,使用“半滴操作”可提高测量的准确度。其方法是:将旋塞稍稍转动,使半滴溶液悬
于管口,用锥形瓶内壁将半滴溶液沾落,______继续摇动锥形瓶,观察颜色变化。(请在横线上补
全操作)
(5)该小组用滴定法准确测得产品中KCr O 的质量分数为98.50%。某同学还用分光光度法测定产品纯度
2 2 7
(K Cr O 溶液的吸光度与其浓度成正比例),但测得的质量分数明显偏低。分析其原因,发现配制
2 2 7
KCr O 待测水溶液时少加了一种试剂。该试剂是______,添加该试剂的理由是______。
2 2 7
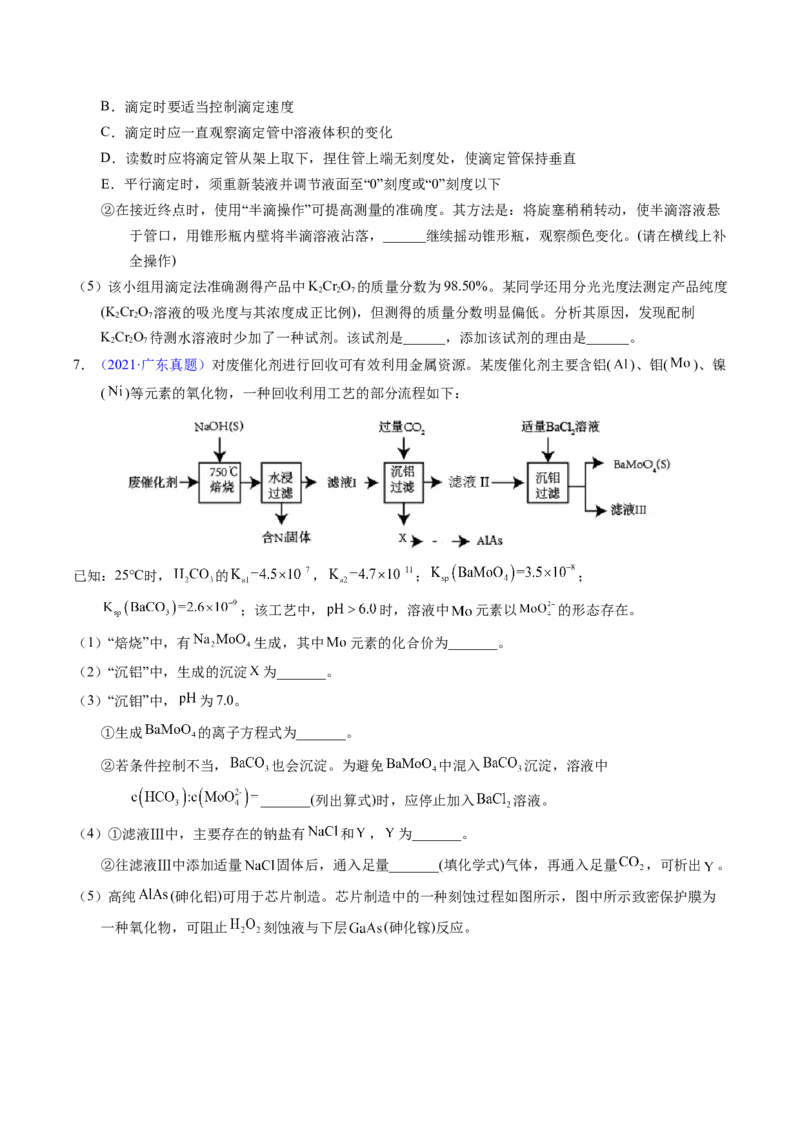
7.(2021·广东真题)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、镍
( )等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的 , ; ;
;该工艺中, 时,溶液中 元素以 的形态存在。
(1)“焙烧”中,有 生成,其中 元素的化合价为_______。
(2)“沉铝”中,生成的沉淀 为_______。
(3)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
②若条件控制不当, 也会沉淀。为避免 中混入 沉淀,溶液中
_______(列出算式)时,应停止加入 溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有 和 , 为_______。
②往滤液Ⅲ中添加适量 固体后,通入足量_______(填化学式)气体,再通入足量 ,可析出 。
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为
一种氧化物,可阻止 刻蚀液与下层 (砷化镓)反应。①该氧化物为_______。
②已知: 和 同族, 和 同族。在 与上层 的反应中, 元素的化合价变为+5价,
则该反应的氧化剂与还原剂物质的量之比为_______。
8.【2016江苏卷】实验室以一种工业废渣(主要成分为MgCO 、MgSiO 和少量Fe、Al的氧化物)为原
3 2 4
料制备MgCO ·3H O。实验过程如下:
3 2
(1)酸溶过程中主要反应的热化学方程式为
MgCO (s)+2H+(aq)===Mg2+(aq)+CO (g)+HO(l) ΔH=-50.4 kJ·mol–1
3 2 2
MgSiO(s)+4H+(aq)===2 Mg2+(aq)+H SiO(s)+HO(l) ΔH=-225.4 kJ·mol–1
2 4 2 3 2
酸溶需加热的目的是______;所加HSO 不宜过量太多的原因是_______。
2 4
(2)加入HO 氧化时发生发应的离子方程式为___________。
2 2
(3)用下图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。
①实验装置图中仪器A的名称为_______。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有
机萃取剂,______、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO ·3H O的实验方案:边搅拌边向溶液中滴加氨水,
3 2______,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO ·3H O。
3 2
[已知该溶液中pH=8.5时Mg(OH) 开始沉淀;pH=5.0时Al(OH) 沉淀完全]。
2 3
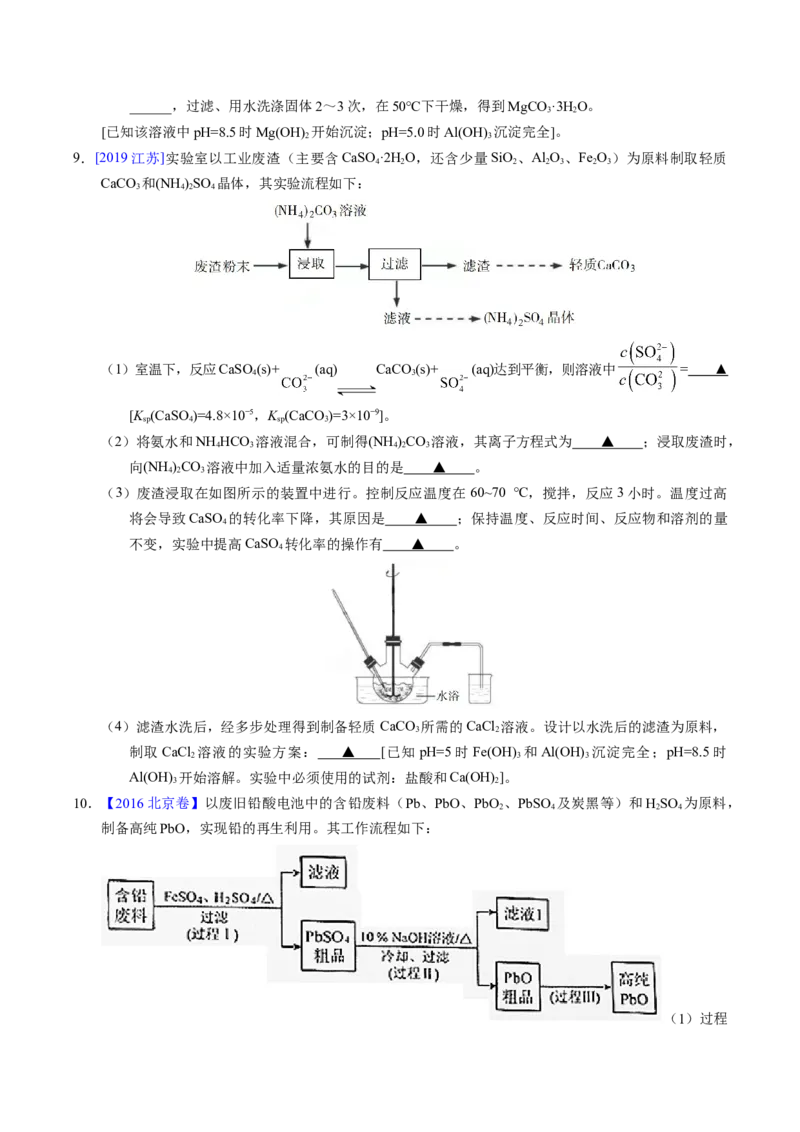
9.[2019江苏]实验室以工业废渣(主要含CaSO·2H O,还含少量SiO 、Al O 、Fe O )为原料制取轻质
4 2 2 2 3 2 3
CaCO 和(NH )SO 晶体,其实验流程如下:
3 4 2 4
(1)室温下,反应CaSO(s)+ (aq) CaCO (s)+ (aq)达到平衡,则溶液中 = ▲
4 3
[K (CaSO)=4.8×10−5,K (CaCO)=3×10−9]。
sp 4 sp 3
(2)将氨水和NH HCO 溶液混合,可制得(NH )CO 溶液,其离子方程式为 ▲ ;浸取废渣时,
4 3 4 2 3
向(NH )CO 溶液中加入适量浓氨水的目的是 ▲ 。
4 2 3
(3)废渣浸取在如图所示的装置中进行。控制反应温度在 60~70 ℃,搅拌,反应3小时。温度过高
将会导致CaSO 的转化率下降,其原因是 ▲ ;保持温度、反应时间、反应物和溶剂的量
4
不变,实验中提高CaSO 转化率的操作有 ▲ 。
4
(4)滤渣水洗后,经多步处理得到制备轻质CaCO 所需的CaCl 溶液。设计以水洗后的滤渣为原料,
3 2
制取CaCl 溶液的实验方案: ▲ [已知pH=5时Fe(OH) 和Al(OH) 沉淀完全;pH=8.5时
2 3 3
Al(OH) 开始溶解。实验中必须使用的试剂:盐酸和Ca(OH) ]。
3 2
10.【2016北京卷】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO 、PbSO 及炭黑等)和HSO 为原料,
2 4 2 4
制备高纯PbO,实现铅的再生利用。其工作流程如下:
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO 反应生成PbSO 的化学方程式是__________。
2 4
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO +4H++SO2−=2Fe3++PbSO+2H O
2 4 4 2
ii: ……
①写出ii的离子方程式:________________。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO 溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO ,溶液变红。
4 2
b.______________。
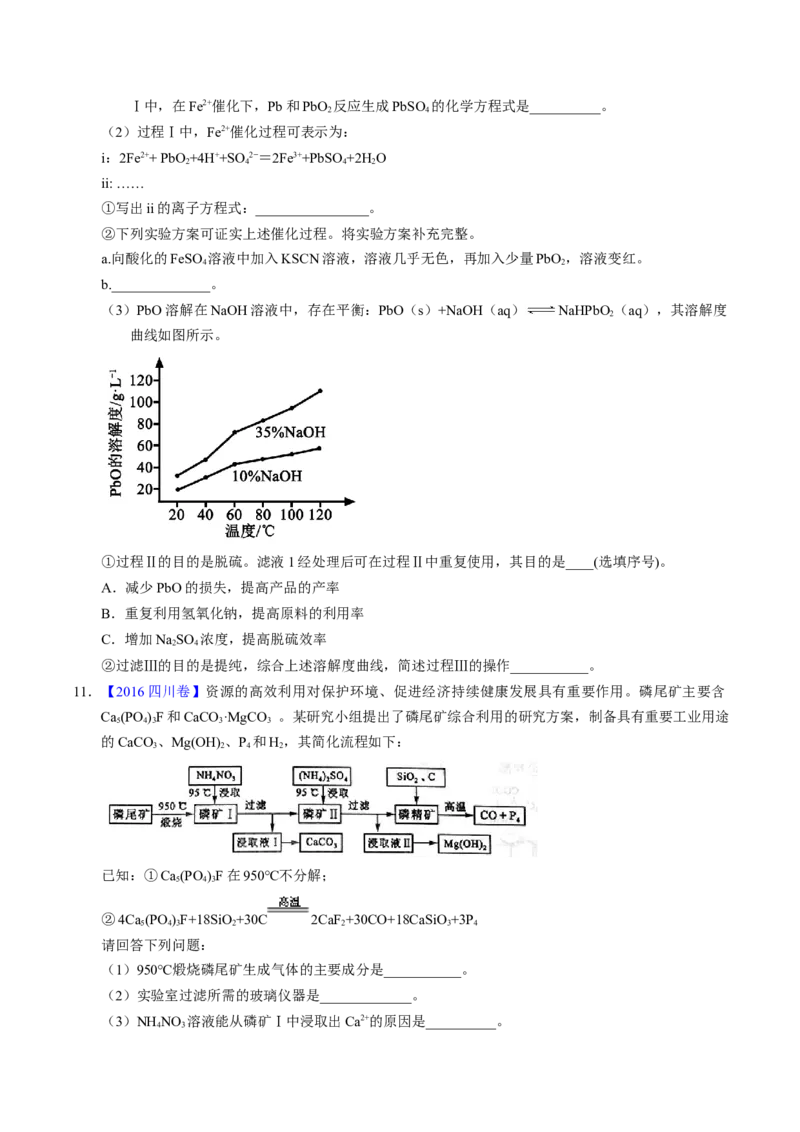
(3)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq) NaHPbO (aq),其溶解度
2
曲线如图所示。
①过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是____(选填序号)。
A.减少PbO的损失,提高产品的产率
B.重复利用氢氧化钠,提高原料的利用率
C.增加NaSO 浓度,提高脱硫效率
2 4
②过滤Ⅲ的目的是提纯,综合上述溶解度曲线,简述过程Ⅲ的操作___________。
11.【2016四川卷】资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。磷尾矿主要含
Ca (PO )F和CaCO ·MgCO 。某研究小组提出了磷尾矿综合利用的研究方案,制备具有重要工业用途
5 4 3 3 3
的CaCO 、Mg(OH) 、P 和H,其简化流程如下:
3 2 4 2
已知:①Ca (PO )F在950℃不分解;
5 4 3
②4Ca (PO )F+18SiO +30C 2CaF +30CO+18CaSiO +3P
5 4 3 2 2 3 4
请回答下列问题:
(1)950℃煅烧磷尾矿生成气体的主要成分是___________。
(2)实验室过滤所需的玻璃仪器是_____________。
(3)NH NO 溶液能从磷矿Ⅰ中浸取出Ca2+的原因是__________。
4 3(4)在浸取液Ⅱ中通入NH ,发生反应的化学方程式是____________。
3
(5)工业上常用磷精矿[Ca (PO )F]和硫酸反应制备磷酸。已知25℃,101kPa时:
5 4 3
CaO(s)+H SO (l)=CaSO (s)+HO(l) ΔH=-271kJ/mol
2 4 4 2
5 CaO(s)+3H PO (l)+HF(g)= Ca (PO )F (s)+5HO(l) ΔH=-937kJ/mol
3 4 5 4 3 2
则Ca (PO )F和硫酸反应生成磷酸的热化学方程式是_________________。
5 4 3
(6)在一定条件下CO(g)+HO(g) CO(g)+H(g),当CO与HO(g)的起始物质的量之比为1:5,达
2 2 2 2
平衡时,CO转化了 。若a kg含Ca (PO )F(相对分子质量为504)的质量分数为10%的磷尾矿
5 4 3
在上述过程中有b%的Ca (PO )F转化为P ,将产生的CO与HO(g)按起始物质的量之比1:3混合,
5 4 3 4 2
则相同条件下达平衡时能产生H________kg。
2