文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(黑龙江、甘肃、吉林、
安徽、江西、贵州、广西)
黄金卷 02
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Si 28 Cl 35.5 Na 23 Ti 48 Cu 64
第Ⅰ卷
一、单项选择题:共15题,每题3分,共45分。每题只有一个选项最符合题意。
1.神舟十六号载人飞船顺利发射,我国航天航空事业再次迎来飞速发展。下列有关说法错误的是
A.飞船采用的太阳能刚性电池阵:将太阳能转化为电能
B.航天员的航天服使用的多种合成纤维:有机高分子材料
C.飞船返回舱使用的高温结构陶瓷:新型无机非金属材料
D.火箭燃料偏二甲肼(CH ) N-NH :属于烃类
3 2 2
2.ClO 在工业上可用于淀粉及油脂的漂白及自来水的消毒,制备ClO 的一种方法为:5NaClO 4HCl
2 2 2
5NaCl4ClO 2H O,下列有关化学用语表达正确的是
2 2
A.中子数为8的氧原子:16O B.Na的结构示意图:
8
C.HCl的电子式: D.ClO 的空间填充模型:
2
3.设N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.1mol金属钠生成Na O ,转移的电子数为2N
2 2 A
B.60g二氧化硅晶体中含有N 个SiO 分子
A 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002C.乙烯和丙烯的混合物共28g,含有的氢原子数为4N
A
D.由1molCH COONa和少量CH COOH形成的中性溶液中,CH COO-数目小于N
3 3 3 A
4.下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 配制FeCl 溶液 将FeCl 固体溶于浓盐酸后再稀释
3 3
B 提纯含有少量乙酸的乙酸乙酯 加NaOH溶液后分液
C 实验室制NH 加热使氯化铵固体分解
3
D 由MgCl 溶液制备无水MgCl 将MgCl 溶液加热蒸干
2 2 2
A.A B.B C.C D.D
5.下列有关物质的性质和用途说法不正确的是
A.利用高纯单质硅的半导体性能,可以制成光电池
B.石灰石在高温下的分解产物可与SO 反应,可用于减少燃煤烟气中的SO
2 2
C.Na O 与CO 反应放出氧气,可用于制作呼吸面具
2 2 2
D.二氧化硅导电能力强,可用于制造光导纤维
6.W、X、Y、Z、M五种短周期主族元素,原子序数依次增大。W的核外电子数等于其周期数,XW 分
3
子呈三角锥形,Y的核外电子数等于W、X核外电子数之和,在同周期元素中M的第一电离能最小。下列
说法正确的是
A.M Y与M Y 含有的化学键类型完全相同
2 2 2
B.X、Y、Z三种元素的电负性顺序为:X 0
D.对于反应②,增加CuO的量,平衡正移
15.为研究用AgNO 溶液将混合溶液中的Cl和CrO2沉淀分离,绘制了25℃时AgCl和Ag CrO 两种难溶
3 4 2 4
化合物的溶解平衡曲线。其中,pAg lgc Ag ,其余离子类推。两条相交的溶解平衡曲线把图像分成
了X、Y、Z、M四个区域。下列说法中不正确的是
A.K Ag CrO 约为11012,K AgCl的数量级为1010
sp 2 4 sp
B.M区域内可析出Ag CrO 沉淀,而不析出AgCl沉淀
2 4
C.向Cl、CrO2均为0.1mol/L的混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀
4
c
CrO2
4
D.向Ag CrO 、AgCl混合固体和水的溶解平衡体系中加少量水, 增大
2 4 c2 Cl
第Ⅱ卷
二、非选择题:共4题,共55分。
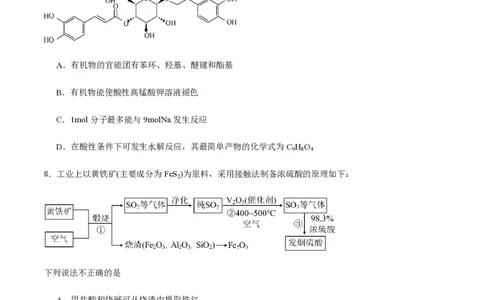
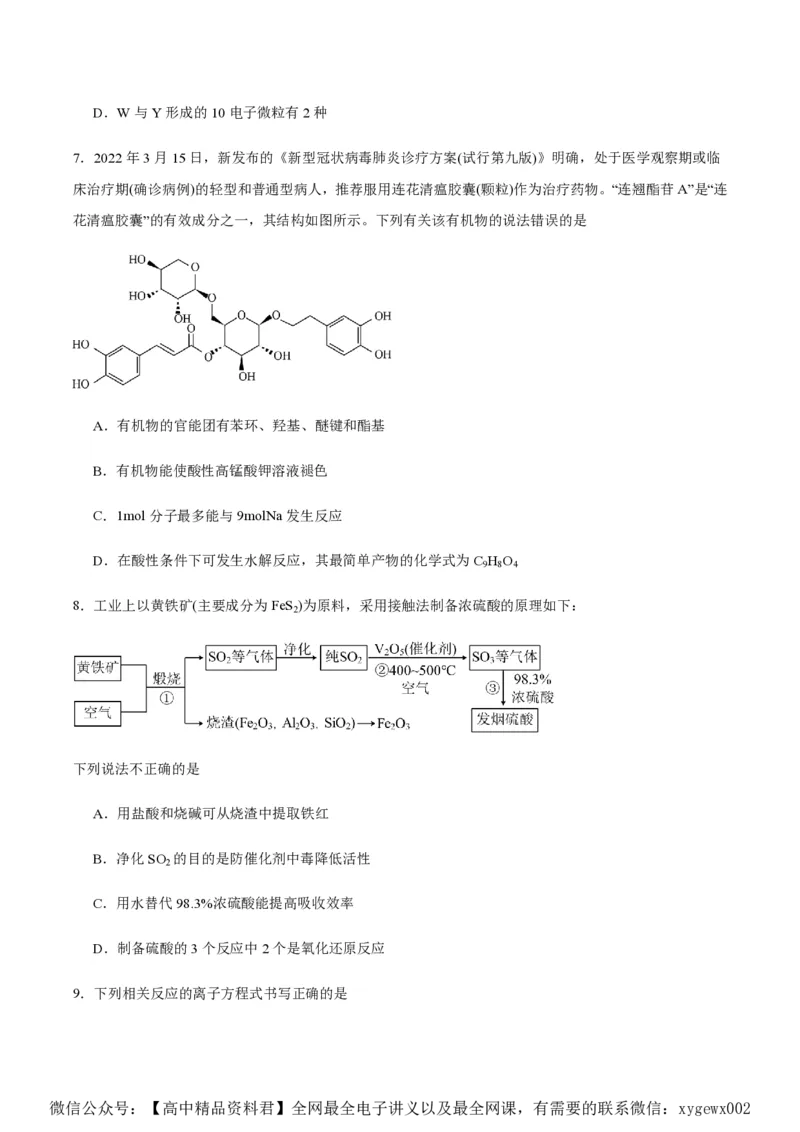
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx00216.(14分)氯化亚铜(CuCl)微溶于水,易被氧化,广泛应用于医药等行业。以废铜渣(铜单质的质量分数为
64%,CuO的质量分数为8%,其他杂质不含铜元素)为原料制备CuCl流程如下:
【资料】CuCl固体难溶于水,与Cl-反应生成可溶于水的离子[CuCl ]-。
2
(1)用Na SO 固体配制100 mL0.50 mol/LNa SO 溶液时,需要的玻璃仪器有烧杯、玻璃棒、胶体滴管、
2 3 2 3
(填仪器名称);
(2)“溶解”步骤装置如图所示。
①“溶解”制备硫酸铜的化学程式为2Cu+2H SO +O =2CuSO +2H O 、 。
2 4 2 4 2
②通入热空气的目的是 ;
(3)“还原”过程中所得的氧化产物为 ,NaCl的用量对铜的沉淀率的影响如图所示。
n(NaCl)
>1.1时,CuCl的沉淀率下降的原因是 ;
n(Cu2+)
(4)准确称取所制备的氯化亚铜样品0.50 g,将其置于过量的FeCl 溶液中,待样品完全溶解后过滤,将
3
滤液及洗涤液一并转移到锥形瓶中,加入指示剂2滴,立刻滴入0.20 mol/LCe(SO ) 标准溶液,至恰好反应
4 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002时,消耗Ce(SO ) 标准溶液20.00 mL。(已知:FeCl +CuCl=FeCl +CuCl 、Ce4++Fe2+=Ce3++Fe3+,且杂质不
4 2 3 2 2
参与反应。)
①样品中CuCl的质量分数为 。(写出计算过程)
②若操作过程缺少“将洗涤液一并转移到瓶中”的步骤,会导致CuCl的质量分数 (填“偏大”或“偏
小”)。
17.(13分)一种在常温、常压下催化电解实现工业合成氨反应的工艺为:
2N g6H Ol=4NH g3O g H 1530kJmol1,该反应可分两步完成:
2 2 3 2 1
反应Ⅰ:N g3H g=2NH g H 92.4kJmol1
2 2 3 2
反应Ⅱ:2H Ol=2H gO g ΔH
2 2 2 3
请回答下列问题:
(1)ΔH = kJmol1。
3
(2)将1.00molN 和3.00molH 充入到3L的恒容密闭容器中模拟反应Ⅰ:
2 2
①该反应中物质浓度随时间变化的曲线如图所示,0~10nin内,vH molL1min1。
2
②不同温度和压强下测得平衡时混合物中氨的体积分数与温度的关系如图所示:
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002则B、C两点的平衡常数K K (填“>”、“<”、“=”或“不确定”);B点时N 的转化率= (保
B C 2
留2位有效数字)。
(3)从图乙中获知反应Ⅰ存在着高温降低平衡产率与低温降低反应速率等调控矛盾。在提高合成氨的产率的
工业生产中,通常从以下多个视角来综合考虑合理的工业生产条件:
反应速率的视角:①加入催化剂;②提高温度(控制在催化剂的活性温度内)
平衡移动和原料的转化率的视角:③ ,④ 。
(4)科学家为避免直接破坏NN键而消耗大量热能,通过新型催化剂降低了反应路径中决速步的能垒,
使该反应在常温、常压下采用电化学方法也能实现,反应装置如图所示,阴极上的电极反应式
为 。
18.(14分)金属钛有“生物金属、海洋金属、太空金属”的美称。有些含钛的化合物在耐高温、环保或者抑
菌方面有着重要的应用,钛元素也被称为“健康钛”。
(1)Ti元素位于元素周期表的 区,基态原子电子排布式为 。
(2)TiCl 与SiCl 互为等电子体。SiCl 可以与N-甲基咪唑 发生反应。
4 4 4
①TiCl 分子的空间构型为 。
4
②N-甲基咪唑分子中碳原子的杂化轨道类型为 ,C、N、Si的电负性由大到小的顺序为 ,1个
含有 个π键。
(3)TiCl 可以与胺形成配合物,如TiCl (CH NH ) 、TiCl (H NCH CH NH )。
4 4 3 2 2 4 2 2 2 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002① TiCl (H NCH CH NH )中提供电子对形成配位键的原子是 。
4 2 2 2 2
②乙二胺(H NCH CH NH )能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳
2 2 2 2
定性较差的是 (填“Mg2+”或“Cu2+”)。
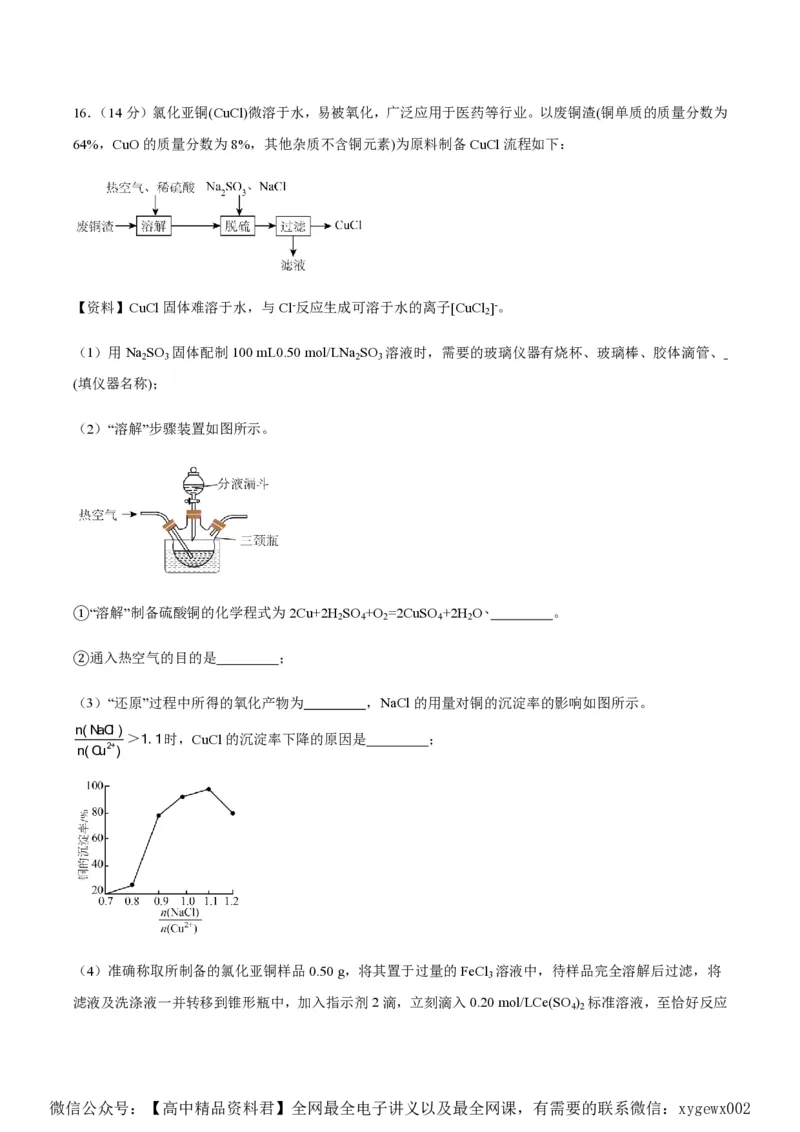
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积方式,X-
射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为a pm,则r(N3-)为 pm。该氮化钛的密度为
g·cm-3(N 为阿伏加德罗常数的值,只列计算式)。
A
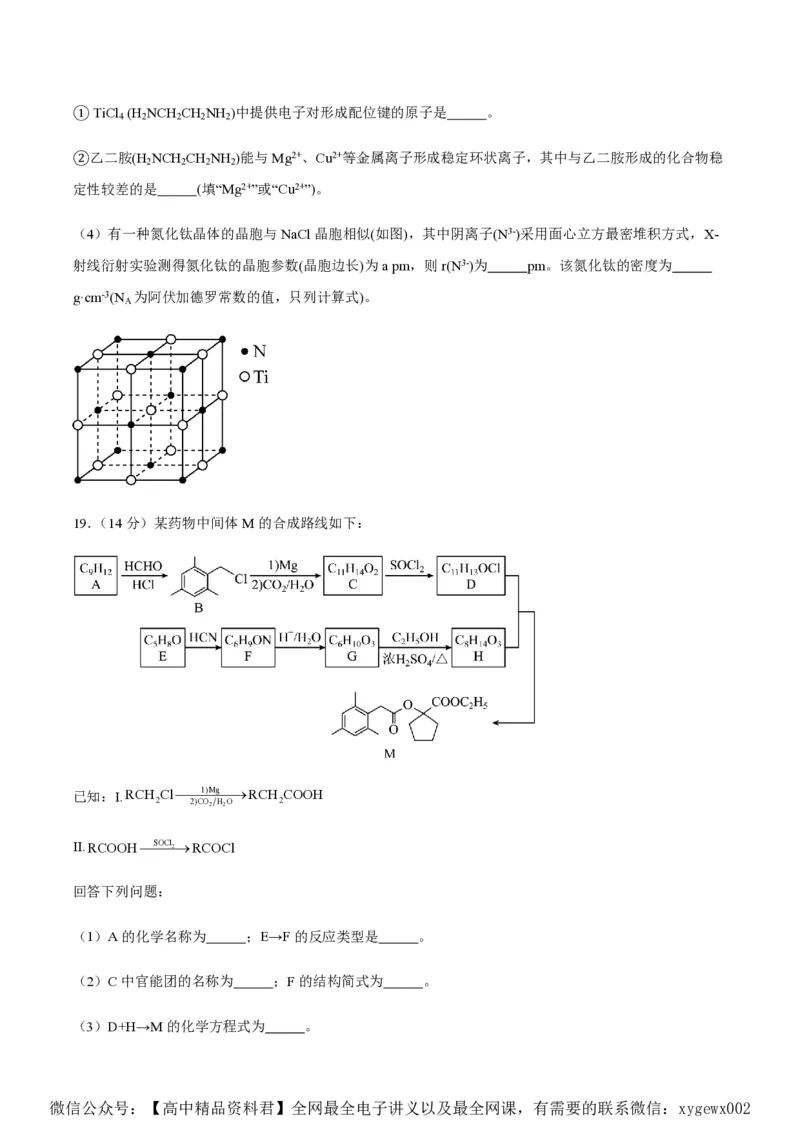
19.(14分)某药物中间体M的合成路线如下:
已知:I.RCH Cl1)MgRCH COOH
2 2)CO2 H2O 2
II.RCOOHSOCl2RCOCl
回答下列问题:
(1)A的化学名称为 ;E→F的反应类型是 。
(2)C中官能团的名称为 ;F的结构简式为 。
(3)D+H→M的化学方程式为 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(4)写出同时满足下列条件的C的同分异构体的结构简式 (任写一种)。
①属于芳香族化合物②与C具有相同官能团③含有四种化学环境的氢
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002