文档内容
合肥一中 2026 届高三 10 月份教学质量测评
化学参考答案
1. C
【详解】碳纤维属于无机材料,玻璃钢属于复合材料,金属材料指的是金属单质以及合金。
2.A
【详解】A.石膏在豆腐制作中的主要作用是使豆浆中的蛋白质发生凝聚和沉淀,形成豆腐的质
地和形状,与石膏的溶解性无关,A错误;
B.B与H形成的简单化合物中,B显正价,B的电负性小于H,NaBH 中H为-1价,体现出强
还原性,易被氧化为0价,所以NaBH 可用作还原剂,B正确; 4
C.聚四氟乙烯性质稳定,被称为塑料王。4具有抗酸碱、自润滑等性能,可用于制作滴定管活
塞,C正确;
D.ClO 具有强氧化性,可用于自来水消毒
2
3.D
【详解】A.图示装置将水倒入混合液中,不符合浓硫酸稀释原则,无法安全有效检验Cu2+,A
不符合题意;
B.检验葡萄糖需要在碱性溶液中进行,水解后没有加NaOH中和硫酸,不能检验水解产物具有还
原性,B错误;
C.图中锌直接与硫酸铜溶液接触反应,不能达到化学能转化为电能的目的,应该将两侧溶液调
换,锌与硫酸锌溶液一侧,铜与硫酸铜溶液一侧,C错误;
D. Cu NH SO H O在乙醇中的溶解度小于在水中的溶解度,加入乙醇,可以降低其溶解
[度,( 用玻3)4璃]棒摩4⋅擦2试管壁后,可析出晶体,D正确;
4.A
【分析】如题图,腺嘌呤核苷酸从左到右分为三部分:磷酸、核糖、碱基(腺嘌呤)。腺嘌呤核
苷酸初步水解可生成磷酸和腺嘌呤核苷(核糖+碱基),腺嘌呤核苷酸完全水解可生成磷酸、核
糖、碱基(腺嘌呤)。
合肥一中2026届高三10月份教学质量 测评·化学参考答案 第1页(共7页)【详解】A.腺嘌呤核苷酸是腺嘌呤核苷(核糖+碱基)的磷酸酯,可发生酯的水解反应,属于取
代反应;腺嘌呤核苷酸的核糖部分有羟基,且与羟基相连的碳原子的邻位碳原子上有氢(即
β-H),可发生消去反应,同时存在α-H,也能发生氧化反应,A正确;
B.与足量H 加成仅发生在碱基的不饱和键,核糖部分五元环上的4个碳原子均为手性碳原子,
2
加成后碱基部分新增3个手性碳原子( ),共7个,B错误;
C.腺嘌呤核苷酸的磷酸部分可电离出2个H+,且有一个酯键,故1 mol腺嘌呤核苷酸最多能与
3 mol NaOH反应,C错误;
D.完全水解生成的碱基为腺嘌呤( ),分子式为C H N ,D错误;
5 5 5
故选A。
5.D
【详解】
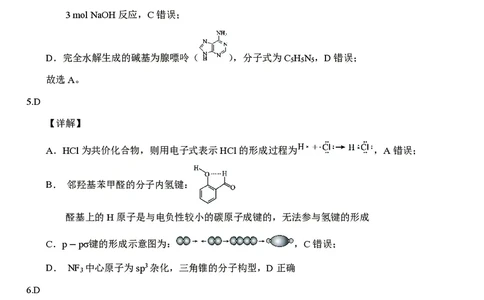
A.HCl为共价化合物,则用电子式表示HCl的形成过程为 ,A错误;
B. 邻羟基苯甲醛的分子内氢键:
醛基上的H原子是与电负性较小的碳原子成键的,无法参与氢键的形成
C.p pσ键的形成示意图为: ,C错误;
D. N−F 中心原子为sp3杂化,三角锥的分子构型,D正确
3
6.D
【详解】A.向Mg HCO 溶液中加入过量的NaOH溶液,氢氧化镁的溶解度比碳酸镁小,应生
成氢氧化镁,正确的( 离子3反)2应为:Mg HCO OH Mg CO H O,A错
2+ − − 2−
误。 +2 3 +4 = (OH)2 ↓+2 3 +2 2
B. SO 通入Ba(NO ) 溶液时, 酸性条件下将SO 氧化为 ,自身被还原为NO,正确离
2 3 2 2
− 2−
子方程式应为3Ba +3SO +2NNOO3 +2H O=3BaSO ↓+2NO ↑+S4OH4 ,B错误;
2
2+ − +
C.向 溶液中滴入2 3 使 反应完4全,此时
2−
NH4Al(SO4)2 Ba(OH)2 SO4 𝑛𝑛(NH4Al(SO4)2):𝑛𝑛(Ba(OH)2)=
合肥一中2026届高三10月份教学质量 测评·化学参考答案 第2页(共7页),离子方程式为 Ba OH Al SO +NH BaSO Al OH
2+ − 3+ 2− +
1:2,C错误; 2 +4 + +2 4 4 =2 4 ↓+ ( )3 ↓+NH3·
D.含H2氟O牙膏可以防龋齿是利用沉淀转化,形成更难溶的沉淀保护牙齿,该方程是书写正确,D
正确;
故选D。
7.B
A.[MEA]L 和NaCl均为离子晶体,熔点较低的[MEA]L的离子键较弱,A正确
B.C在反应过程中作还原剂,不能用来推断非金属性,B错误
C.强酸制取弱酸,C正确
D.镀锡马口铁镀层破坏后加速铁的腐蚀是因为形成原电池,因铁活泼会更快腐蚀,D正确
8.B
解析:I基态原子的简化电子排布式为[Kr]4d105s25p5,A错误;与一个CH NH+ 最近且等距离的I-
3 3
有12个,B错误;根据晶胞的解雇若 Pb2+处于晶胞的各顶角位置,则碘离子处于棱心处,
D错误。
9.D
【解析】【详解】A.过程中存在H O 中O-O非极性键的断裂,以及O 中非极性键的形成;还存
2 2 2
在O−H极性键的断裂,以及O−C极性键的形成,A正确;
B. 过程中Ti的化学键(Ti−O)始终是4个,与分子形成的配位键不会改变Ti的化合价,故Ti
元素的化合价不变,B正确;
C. 根据反应原理,可写出总反应
D. I的部分结构来自于H O ,属于中间产物,物质III为催化剂
2 2
10.B
【详解】地壳中含量最高的为氧元素,故Y为氧元素,RY是常见干燥剂为CaO,故R为钙元
素,分布在不同周期,X为第一周期,故为氢元素,Z、W在第三周期且属于硅酸盐,故W
为硅元素, Z的3P有2个空轨道为Al。
A.原子半径顺序应为Al(Z)>Si(W)>O(Y),而选项A中为W>Z>Y,错误;
B. SiO 的熔点高于H O,正确;
2 2
合肥一中2026届高三10月份教学质量 测评·化学参考答案 第3页(共7页)C.X(H)和R(Ca)形成的化合物CaH₂中,H显-1价,显负价,错误;
D.两性的氢氧化铝只溶于较强的酸碱,不能溶于硅酸,D错误;
故选B。
11.D
答案解析:X参与两个反应,v(X)=v(M) +v(N)=1 mol·L -1 ·s -1,A错误;反应开始后c(M)> c(N),说
明反应 的速率大于反应 ,则反应 的活化能小于反应 ,B 错误;根据B 选项说明k 大于
1
k ,平衡①后的任意时刻,v②(正)均大于①v (逆) ,C错误;若加②催化剂,k 变大,k 不变,则反应
2 1 2 1 2
的速率提高,反应 的速率不变,反应 的选择性提高,则 c(M)的最大值增大,D正确。 ①
12.D ② ①
【详解】A.葫芦脲CB[5]和其它分子结合后才是超分子,本身不是超分子,故A错误;
B.阿霉素进入CB[7]内腔的包含作用属于超分子相互作用,如疏水作用、范德华力等,而非共
价键,B错误;
C.题干描述CB[n]“内部刷了油(疏水)、外部刷了糖浆(亲水)”,说明内部空腔为疏水环境,
外部为亲水环境,化学微环境不同,C错误;
D.主客体因为大小匹配形成超分子,体现识别功能,故D正确;
13.D
【分析】该装置有外接电源为电解池,电极B中Mn2+转化为MnO ,B为阳极,发生氧化反应
2
Mn2++2H O-2e-=MnO +4H+;电极A为阴极,发生还原反应
2 2
LiMn O +3e-+8H+=Li++↓2Mn2++4H O。
2 4 2
【详解】A.电极A处LiMn O 生成Li+和Mn2+,Mn元素价态从+3.5降为+2,发生还原反应,
2 4
故电极A为阴极,A错误;
B.电极B为阳极,Mn2+被氧化为MnO ,溶液含H SO 呈酸性,电极反应式应为
2 2 4
Mn2++2H O-2e-=MnO +4H+,B错误;
2 2
C.电极A生成Mn2+发生反↓应LiMn O +3e-+8H+=Li++2Mn2++4H O),电极B消耗Mn2+生成
2 4 2
MnO ,根据分析、结合两极上电子数守恒,则生成量大于消耗量,Mn2+浓度增大,C错
2
误;
D.电解后溶液含Li+和Mn2+,调节pH可使Mn2+转化为Mn(OH) 沉淀除去,剩余Li+与Na CO
2 2 3
合肥一中2026届高三10月份教学质量 测评·化学参考答案 第4页(共7页)反应生成Li CO ,D正确;
2 3
故选D。
14.C
解析:根据As(III)水溶液中含砷的各物质的分布分数知,当H AsO 与H AsO -相等时溶液的
3 3 2 3
c(H+)⋅c(H AsO-)
pH=9.2,则H AsO 的K = 2 3 =10-9.2;根据As(V)水溶液中含砷的各物质的分
3 3 a1
c(H AsO )
3 3
布分数知,当H AsO 与H AsO -相等时溶液的pH在2~3之间,H AsO -与HAsO 2-相等时溶
3 4 2 4 2 4 4
c(H+)⋅c(H AsO-)
液的pH=6.8,则H AsO 的K = 2 4 >10-3,故H AsO 为中强酸,A错误;
3 3 a1 3 4
c(H AsO )
3 4
pH=10时,As(V)的主要存在形式为HAsO 2-,正确的反应的离子方程式为:H AsO -+ClO-
4 2 3
+OH-= HAsO 2-+Cl-+H O,B错误;
4 2
c(HAsO2-)⋅c(H AsO )
C项,H AsO -+ H AsO - HAsO 2-+H AsO 的K= 4 3 3 =
2 4 2 3 4 3 3 c(H AsO-)⋅c(H AsO-)
2 4 2 3
c(HAsO2-)⋅c(H AsO )⋅c(H+) K (H AsO ) 10-6.8
4 3 3 = a2 3 4 = =102.4,C项正确
c(H AsO-)⋅c(H AsO-)⋅c(H+) K (H AsO ) 10-9.2
2 4 2 3 a1 3 3
Ca (A O ) 沉淀在溶液中存在沉淀溶解平衡:Ca (A O ) 3Ca2++2A O 3-,
3 S 4 2 3 S 4 2 S 4
2 4
Ksp[Ca (AsO ) ]=c3(Ca2+)c2(AsO3-)=c3(Ca2+)[ c(Ca2+)]2 = c5(Ca2+),
3 4 2 4 3 9
9 9
c5(Ca2+)= Ksp[Ca (AsO ) ]= ×10−21.2,用0.1mol·L-1Na CO 溶液浸泡Ca (A O ) 沉淀,
4 3 4 2 4 2 3 3 S 4 2
9 9
Qc5(CaCO )=c5(Ca2+)c5(CO2-)= ×10−21.2×(0.1)5 = ×10−26.2 >(10−8.6)5,故有CaCO 沉淀生
3 3 4 4 3
成,D错误;
15.(14分,每空2分)
(1)FeS +5O−+2H O=Fe(OH) +2SO2−+OH−
2 2 2 3 4
(2)SOCl 可与水发生水解生成HCl,HCl可抑制Al3+在加热时的水解;
2
(3)弱
(4)SeO
2
(5)<
合肥一中2026届高三10月份教学质量 测评·化学参考答案 第5页(共7页)(6)bc 1:1
16. (14分,每空2分)
低温焙烧
(1)3MnO +3NH HSO 3MnSO +N NH H O
2 4 4 4 2 3 2
↑+ ↑+6
(2)用稀硫酸吸收低温焙烧时生成的NH ,形成(NH ) SO 溶液,处理后所得(NH ) SO 导入“低温
3 4 2 4 4 2 4
焙烧”循环使用
(3)Mn HCO MnCO +CO +H O
3 2 2
2+ −
(4)H O 将+-22价硫3(S=2-或HS-)氧↓化为单质↑ 硫,促进Co2+浸出
2 2
(5) SiO CaSO 加热时,边搅拌边加入3.0mol·L-1 H SO 至固体不再溶解,过滤,向滤液中分批
2 4 2 4
加入稍过量铁粉,充分反应后,加入3.0mol·L-1 H SO 至固体完全溶解,将所得溶液蒸发浓
2 4
缩、降温结晶
(合理即可)
17. (15分,除标注外,每空2分)
(1)三颈烧瓶
70∼80C
(2)4NaHCO +FeCl +H Y NaFeY⋅3H O+4CO ↑+H O+3NaCl
3 3 4 2 2 2
(3) 加乙醇后再降温结晶 AgNO 溶液和稀硝酸
3
(4) pH越小,溶液中H+浓度越大,会抑制反应H Y4H+ +Y4−的发生,使Y4−浓度减小,导致
4
NaFeY⋅3H O的产率减小。
2
(5) d 2.8⁄a (3分)
18. (15分,除标注外,每空2分)
(1)低温、减压或通入更多的氨气(合理即可)
(2)P >P >P 42%
3 2 1
2.88×0.36
(3)副反应受空气(或氧1气.38 )的×0.影8 响更大,增大空气的量时,使得副反应的平衡正向移动的程度大
于主反应
合肥一中2026届高三10月份教学质量 测评·化学参考答案 第6页(共7页)(4)第一步的反应速率比第二步慢,过程中生成的 立即被第二步反应消耗
合肥一中2026届高三10月份教学质量 测评·化学参考答案 第7页(共7页)