文档内容
1
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司目 录 contents
反应历程与机理.......................................................................................................3
化学反应与能量.....................................................................................................17
反应速率与化学平衡.............................................................................................29
反应速率与平衡图像突破.....................................................................................45
化学反应原理综合.................................................................................................62
2
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司反应历程与机理
年份 试卷 考点
2023 广东卷 反应历程、化学平衡、反应速率、相关图像
2023 新课标卷 反应历程、极性分子、氧化还原、相关图像
2023 江苏卷 反应机理、平衡常数、电子转移、相关图像
2023 湖北卷 反应历程、化合价、非极性键、相关图像
2023 浙江卷 反应历程、转化率、热化学方程式、相关图像
2022 山东卷 反应历程、电子转移、转化率、相关图像
2022 湖南卷 反应历程、电子式、原子利用率、活化能、相关图像
2022 浙江卷 反应机理、焓变、活化能与反应速率、相关图像
2021 山东卷 反应历程、化学平衡、反应速率、相关图像
2021 湖南卷 反应机理、氧化还原反应、反应速率、相关图像
2021 湖南卷 反应历程、氧化还原、反应速率、相关图像
化学反应机理试题是高考热点题型,通常以图示的形式来描述某一化学变化所经由的全部反应,主要考查
反应热、活化能、催化剂对反应历程的影响与能量变化,反应历程分析等,试题思维转化大,要求考生具
有较强的迁移运用能力和创新思维,具有一定的难度。
1.基元反应与过渡态理论
(1)基元反应、过渡态理论及活化能
①基元反应:研究发现,大多数化学反应并不是经过简单碰撞就能完成,往往要经过多个反应步骤才能实
现。每一步反应都称为基元反应。
3
原创精品资源学科网独家享有版权,侵权必究!
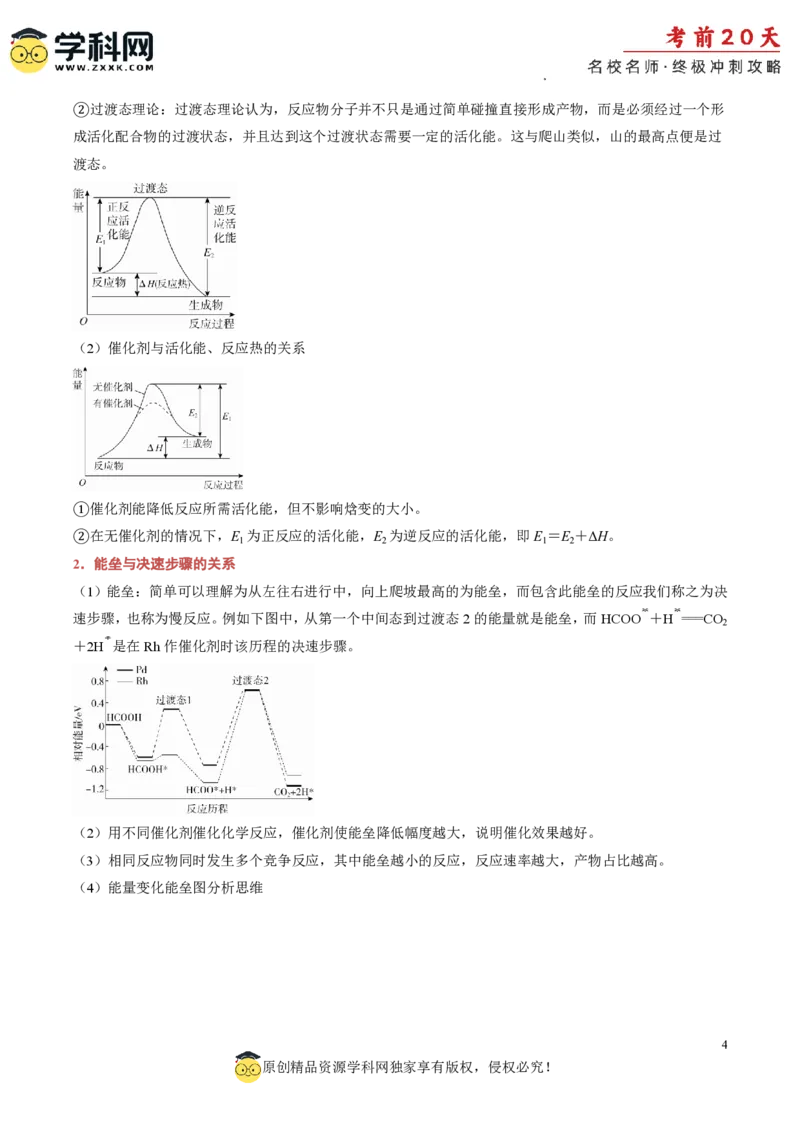
学科网(北京)股份有限公司②过渡态理论:过渡态理论认为,反应物分子并不只是通过简单碰撞直接形成产物,而是必须经过一个形
成活化配合物的过渡状态,并且达到这个过渡状态需要一定的活化能。这与爬山类似,山的最高点便是过
渡态。
(2)催化剂与活化能、反应热的关系
①催化剂能降低反应所需活化能,但不影响焓变的大小。
②在无催化剂的情况下,E 为正反应的活化能,E 为逆反应的活化能,即E =E +ΔH。
1 2 1 2
2.能垒与决速步骤的关系
(1)能垒:简单可以理解为从左往右进行中,向上爬坡最高的为能垒,而包含此能垒的反应我们称之为决
速步骤,也称为慢反应。例如下图中,从第一个中间态到过渡态2的能量就是能垒,而HCOO +H ===CO
2
+2H 是在Rh作催化剂时该历程的决速步骤。
(2)用不同催化剂催化化学反应,催化剂使能垒降低幅度越大,说明催化效果越好。
(3)相同反应物同时发生多个竞争反应,其中能垒越小的反应,反应速率越大,产物占比越高。
(4)能量变化能垒图分析思维
4
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司3.催化剂与化学反应的关系
(1)化学反应中,反应分子原有的某些化学键,必须解离并形成新的化学键,这需要一定的活化能。在某
些难以发生化学反应的体系中,加入有助于反应分子化学键重排的第三种物质(催化剂),可降低反应的活化
能。催化剂能改变反应的途径、降低反应的活化能、加快反应速率,但不能改变反应热的符号与数值、不
能改变平衡的移动方向。图甲虚线表示催化剂对反应的影响,图乙为催化反应历程示意图。
(2)催化反应机理题的解题思路
①通览全图,找准一“剂”三“物”
一“剂” 催化剂在机理图中多数是以完整的循环出现的,以催化剂粒子为主体的多个物种一定在机
指催化剂 理图中的主线上
反应物 通过一个箭头进入整个历程的物质一般是反应物
三“物”指反应物、
生成物 通过一个箭头最终脱离整个历程的物质多是产物
生成物、中间物
通过一个箭头脱离整个历程,但又生成的是中间体,通过两个箭头进入整
种(或中间体)
中间体
个历程的中间物质也是中间体,中间体有时在反应历程中用“[ ]”标出
②逐项分析得答案
根据第一步由题给情境信息,找出催化剂、反应物、生成物、中间体,再结合每一选项设计的问题逐项分
析判断,选出正确答案。
4.化学反应历程类试题解题模板
5
原创精品资源学科网独家享有版权,侵权必究!
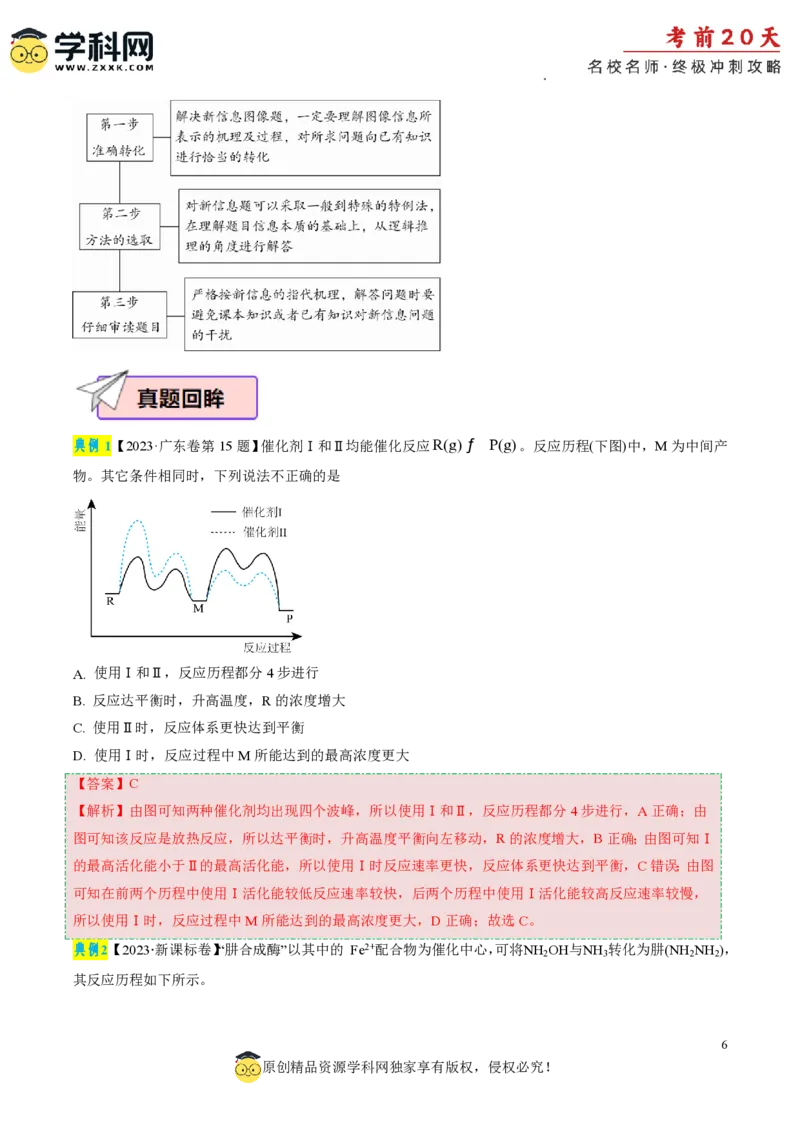
学科网(北京)股份有限公司典例1【2023·广东卷第15题】催化剂Ⅰ和Ⅱ均能催化反应R(g)ƒ P(g)。反应历程(下图)中,M为中间产
物。其它条件相同时,下列说法不正确的是
A. 使用Ⅰ和Ⅱ,反应历程都分4步进行
B. 反应达平衡时,升高温度,R的浓度增大
C. 使用Ⅱ时,反应体系更快达到平衡
D. 使用Ⅰ时,反应过程中M所能达到的最高浓度更大
【答案】C
【解析】由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;由
图可知该反应是放热反应,所以达平衡时,升高温度平衡向左移动,R的浓度增大,B正确;由图可知Ⅰ
的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平衡,C错误;由图
可知在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ活化能较高反应速率较慢,
所以使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确;故选C。
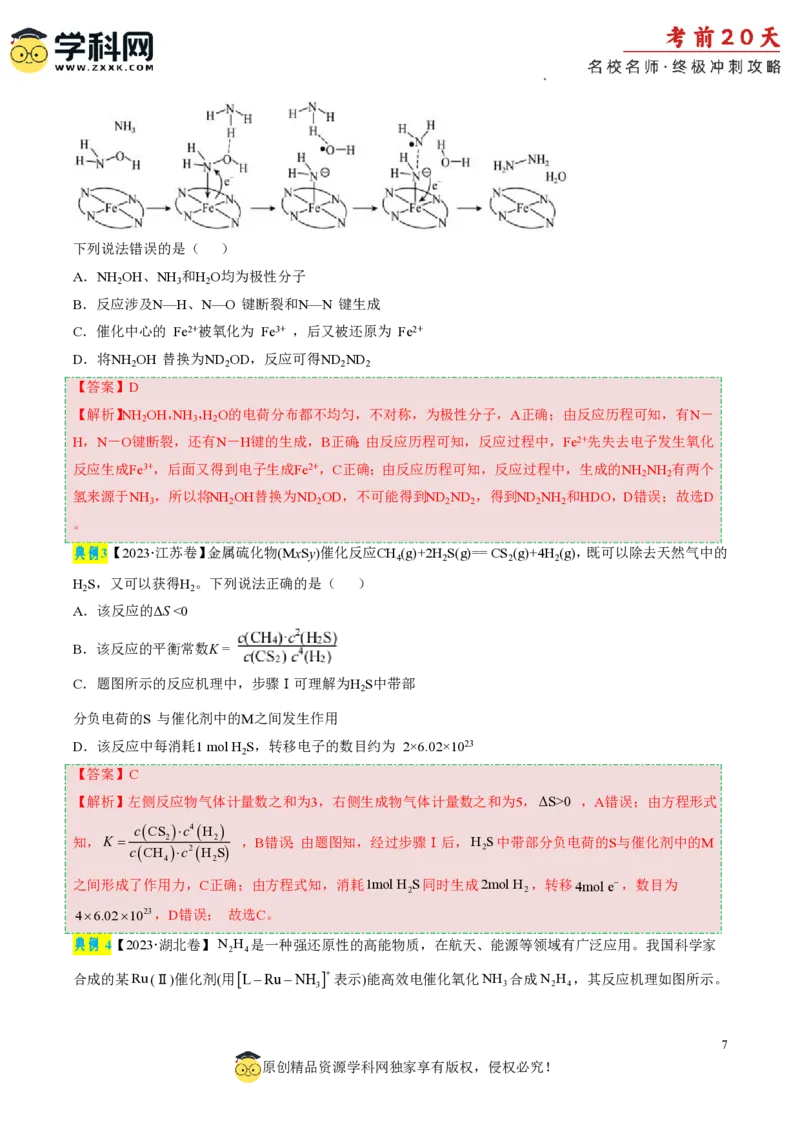
典例2【2023·新课标卷】“肼合成酶”以其中的 Fe2+配合物为催化中心,可将NH OH与NH 转化为肼(NH NH ),
2 3 2 2
其反应历程如下所示。
6
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司下列说法错误的是( )
A.NH OH、NH 和H O均为极性分子
2 3 2
B.反应涉及N—H、N—O 键断裂和N—N 键生成
C.催化中心的 Fe2+被氧化为 Fe3+ ,后又被还原为 Fe2+
D.将NH OH 替换为ND OD,反应可得ND ND
2 2 2 2
【答案】D
【解析】NH OH,NH ,H O的电荷分布都不均匀,不对称,为极性分子,A正确;由反应历程可知,有N-
2 3 2
H,N-O键断裂,还有N-H键的生成,B正确;由反应历程可知,反应过程中,Fe2+先失去电子发生氧化
反应生成Fe3+,后面又得到电子生成Fe2+,C正确;由反应历程可知,反应过程中,生成的NH NH 有两个
2 2
氢来源于NH ,所以将NH OH替换为ND OD,不可能得到ND ND ,得到ND NH 和HDO,D错误;故选D
3 2 2 2 2 2 2
。
典例3【2023·江苏卷】金属硫化物(MxSy)催化反应CH (g)+2H S(g)== CS (g)+4H (g),既可以除去天然气中的
4 2 2 2
H S,又可以获得H 。下列说法正确的是( )
2 2
A.该反应的ΔS <0
B.该反应的平衡常数K =
C.题图所示的反应机理中,步骤Ⅰ可理解为H S中带部
2
分负电荷的S 与催化剂中的M之间发生作用
D.该反应中每消耗1 mol H S,转移电子的数目约为 2×6.02×1023
2
【答案】C
【解析】左侧反应物气体计量数之和为3,右侧生成物气体计量数之和为5,ΔS>0 ,A错误;由方程形式
cCS c4H
知,K 2 2 ,B错误;由题图知,经过步骤Ⅰ后,H S中带部分负电荷的S与催化剂中的M
cCH c2H S 2
4 2
之间形成了作用力,C正确;由方程式知,消耗1mol H S同时生成2mol H ,转移4mol e,数目为
2 2
46.021023,D错误; 故选C。
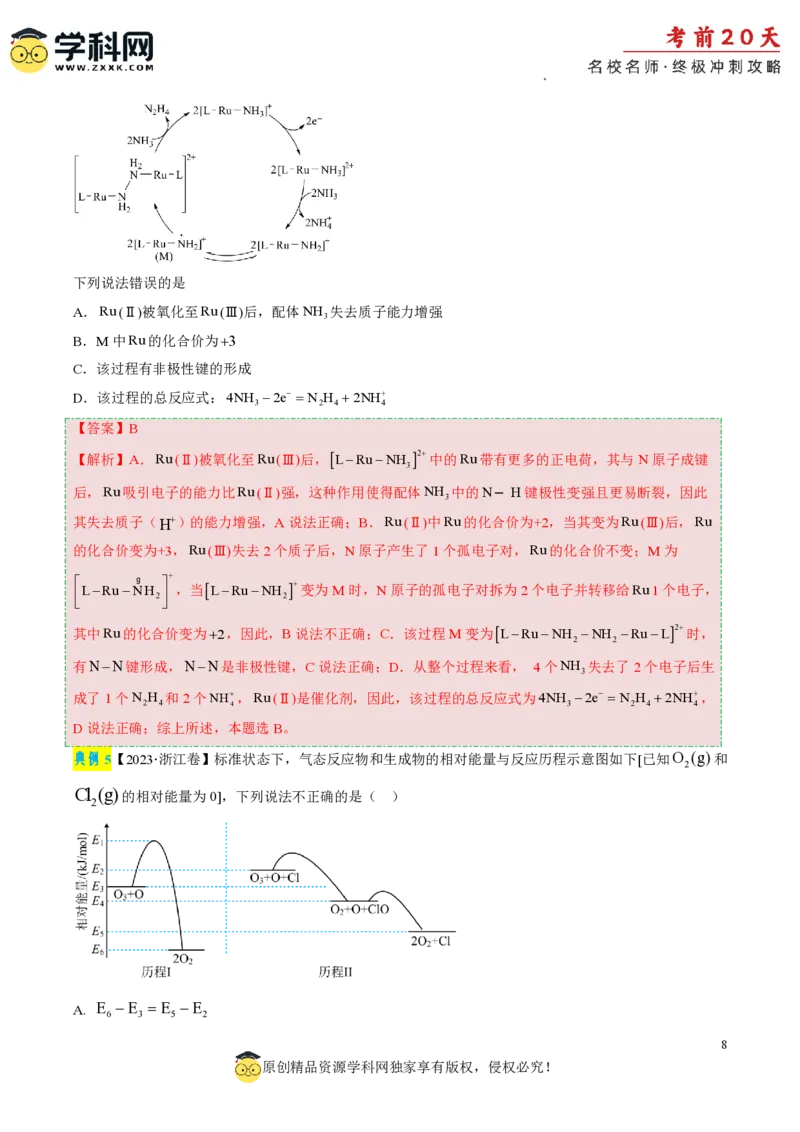
典例4【2023·湖北卷】N H 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家
2 4
合成的某Ru(Ⅱ)催化剂(用LRuNH 表示)能高效电催化氧化NH 合成N H ,其反应机理如图所示。
3 3 2 4
7
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司下列说法错误的是
A.Ru(Ⅱ)被氧化至Ru(Ⅲ)后,配体NH 失去质子能力增强
3
B.M中Ru的化合价为3
C.该过程有非极性键的形成
D.该过程的总反应式:4NH 2e N H 2NH
3 2 4 4
【答案】B
【解析】A.Ru(Ⅱ)被氧化至Ru(Ⅲ)后,LRuNH 2中的Ru带有更多的正电荷,其与N原子成键
3
后,Ru吸引电子的能力比Ru(Ⅱ)强,这种作用使得配体NH 中的N— H键极性变强且更易断裂,因此
3
其失去质子(H)的能力增强,A说法正确;B.Ru(Ⅱ)中Ru的化合价为+2,当其变为Ru(Ⅲ)后,Ru
的化合价变为+3,Ru(Ⅲ)失去2个质子后,N原子产生了1个孤电子对,Ru的化合价不变;M为
LRuN g H ,当LRuNH 变为M时,N原子的孤电子对拆为2个电子并转移给Ru1个电子,
2 2
其中Ru的化合价变为2,因此,B说法不正确;C.该过程M变为LRuNH NH RuL2时,
2 2
有NN键形成,NN是非极性键,C说法正确;D.从整个过程来看, 4个NH 失去了2个电子后生
3
成了1个N H 和2个NH,Ru(Ⅱ)是催化剂,因此,该过程的总反应式为4NH 2e N H 2NH,
2 4 4 3 2 4 4
D说法正确;综上所述,本题选B。
典例5【2023·浙江卷】标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知O (g)和
2
Cl (g)的相对能量为0],下列说法不正确的是( )
2
A. E E E E
6 3 5 2
8
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司B. 可计算ClCl键能为2E E kJmol1
2 3
C. 相同条件下,O 的平衡转化率:历程Ⅱ>历程Ⅰ
3
D. 历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
ClO(g)O(g)=O (g)Cl(g) ΔHE E kJmol1
2 5 4
【答案】C
【分析】对比两个历程可知,历程Ⅱ中增加了催化剂,降低了反应的活化能,加快了反应速率。
【解析】催化剂能降低活化能,但是不能改变反应的焓变,因此E E E E ,A正确;已知Cl (g)的
6 3 5 2 2
相对能量为0,对比两个历程可知,Cl g的相对能量为E -E kJmol1,则ClCl键能为
2 3
2E -E kJmol1,B正确;催化剂不能改变反应的平衡转化率,因此相同条件下,O 的平衡转化率:
2 3 3
历程Ⅱ=历程Ⅰ,C错误;活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最低,
所以速率最快的一步反应的热化学方程式为:ClO(g)O(g)=O (g)Cl(g) ΔH E -E kJmol1,D正
2 5 4
确;故选C。
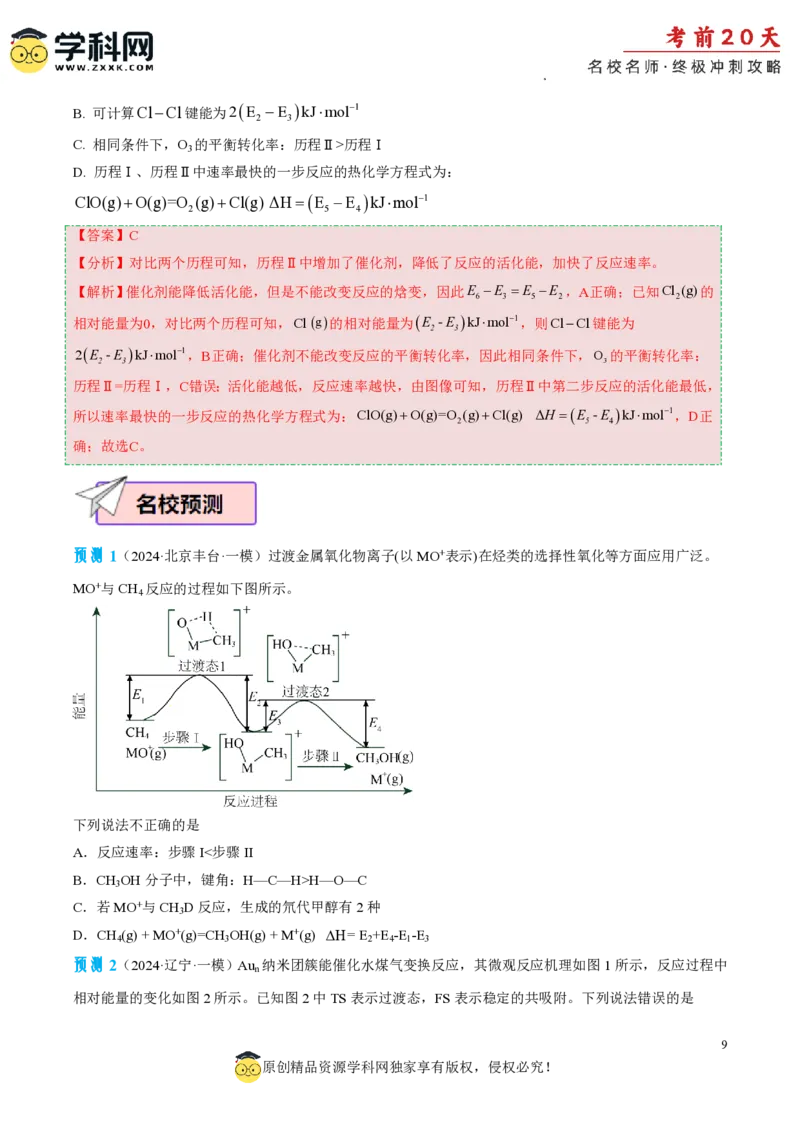
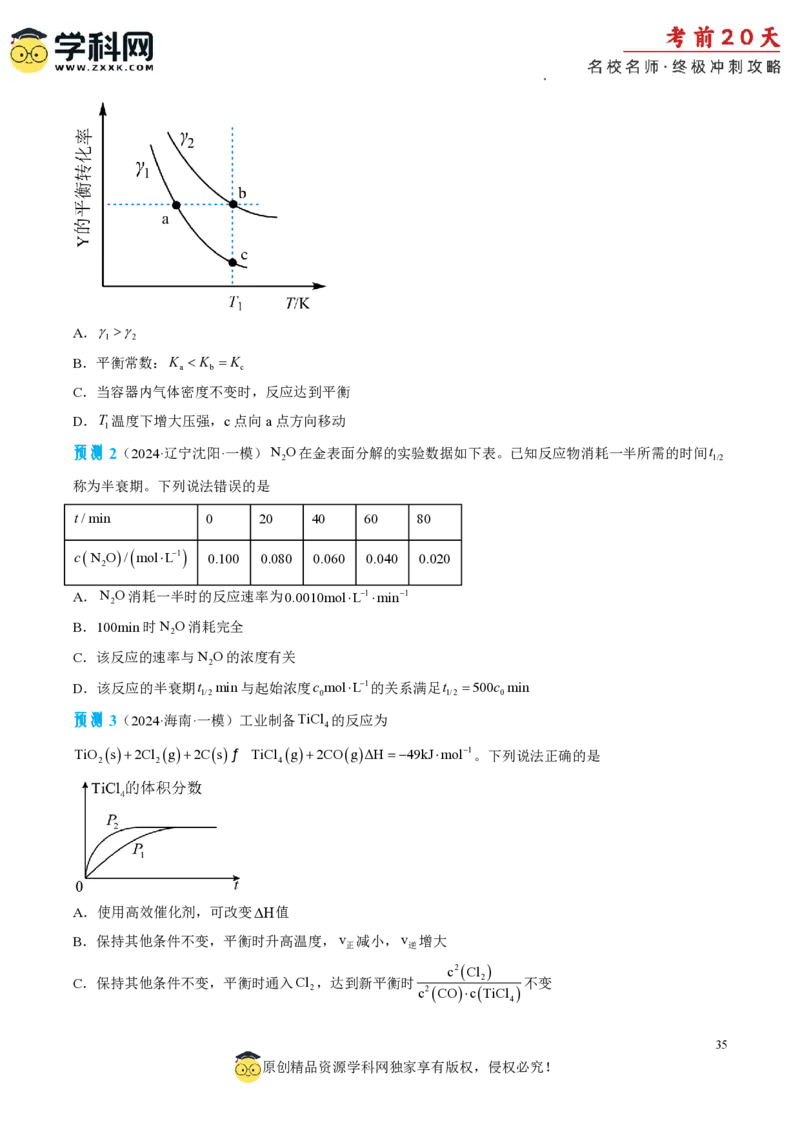
预测1(2024·北京丰台·一模)过渡金属氧化物离子(以MO+表示)在烃类的选择性氧化等方面应用广泛。
MO+与CH 反应的过程如下图所示。
4
下列说法不正确的是
A.反应速率:步骤I<步骤II
B.CH OH分子中,键角:H—C—H>H—O—C
3
C.若MO+与CH D反应,生成的氘代甲醇有2种
3
D.CH (g) + MO+(g)=CH OH(g) + M+(g) H= E +E -E -E
4 3 2 4 1 3
预测2(2024·辽宁·一模)Au 纳米团簇能催化水煤气变换反应,其微观反应机理如图1所示,反应过程中
n
相对能量的变化如图2所示。已知图2中TS表示过渡态,FS表示稳定的共吸附。下列说法错误的是
9
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司Au
n
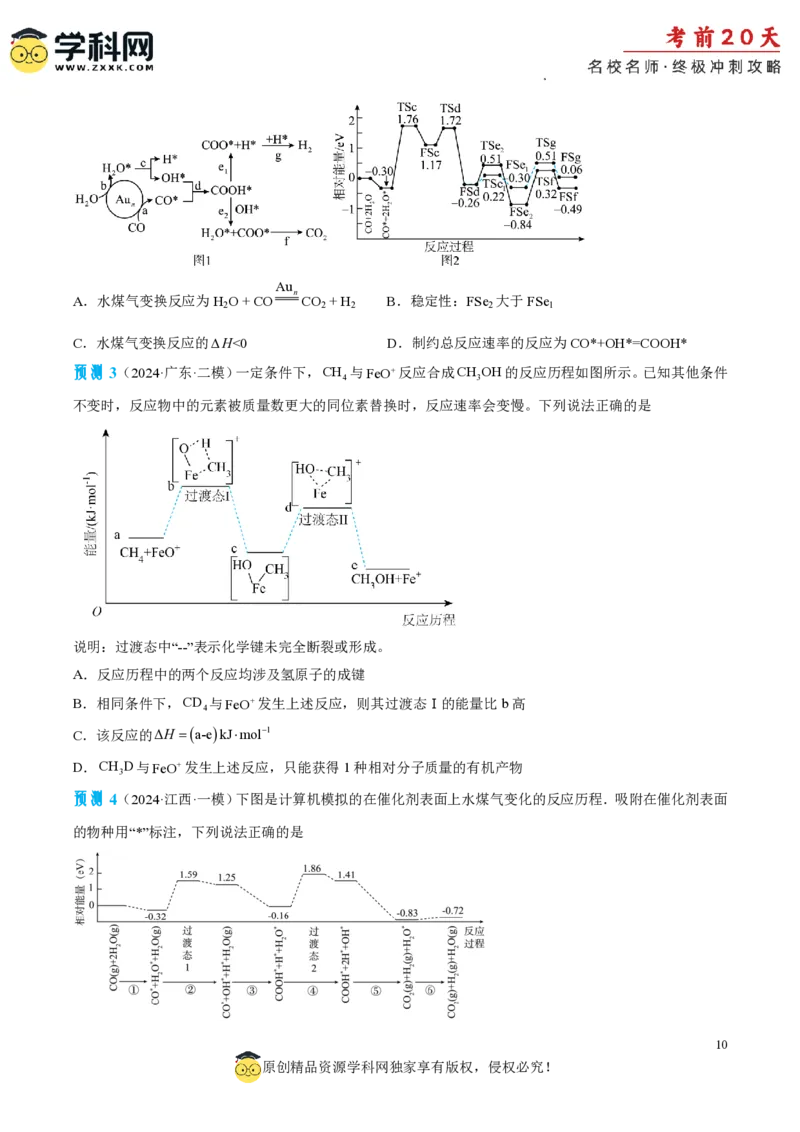
A.水煤气变换反应为H O + CO CO + H B.稳定性:FSe 大于FSe
2 2 2 2 1
C.水煤气变换反应的H<0 D.制约总反应速率的反应为CO*+OH*=COOH*
预测3(2024·广东·二模)一定条件下,CH 与FeO反应合成CH OH的反应历程如图所示。已知其他条件
4 3
不变时,反应物中的元素被质量数更大的同位素替换时,反应速率会变慢。下列说法正确的是
说明:过渡态中“--”表示化学键未完全断裂或形成。
A.反应历程中的两个反应均涉及氢原子的成键
B.相同条件下,CD 与FeO发生上述反应,则其过渡态Ⅰ的能量比b高
4
C.该反应的ΔH a-ekJmol1
D.CH D与FeO发生上述反应,只能获得1种相对分子质量的有机产物
3
预测4(2024·江西·一模)下图是计算机模拟的在催化剂表面上水煤气变化的反应历程.吸附在催化剂表面
的物种用“*”标注,下列说法正确的是
10
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A.①表示CO和H O从催化剂表面脱离的过程
2
B.②和④中化学键变化相同,因此吸收的能量相同
C.由图可知CO(g)H O(g)CO (g)H (g)为吸热反应
2 2 2
D.由图可知,决定反应速率的步骤是②
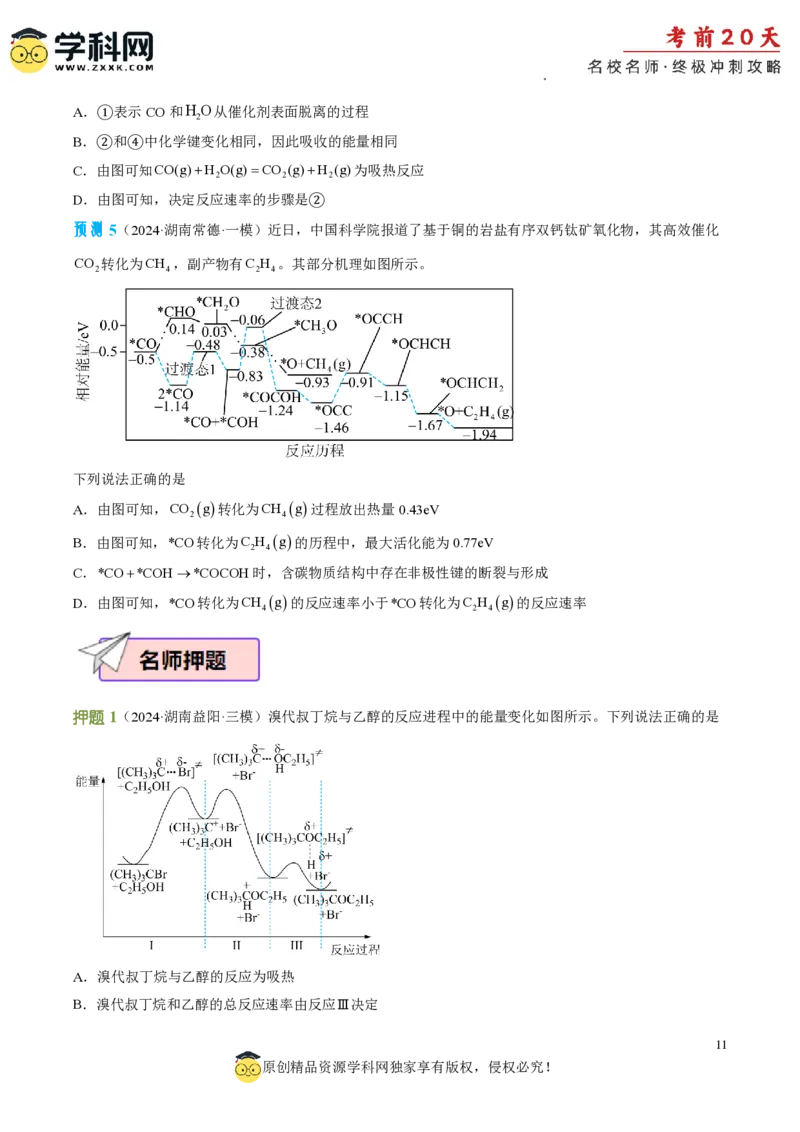
预测5(2024·湖南常德·一模)近日,中国科学院报道了基于铜的岩盐有序双钙钛矿氧化物,其高效催化
CO 转化为CH ,副产物有C H 。其部分机理如图所示。
2 4 2 4
下列说法正确的是
A.由图可知,CO g转化为CH g过程放出热量0.43eV
2 4
B.由图可知,*CO转化为C H g的历程中,最大活化能为0.77eV
2 4
C.*CO*COH*COCOH时,含碳物质结构中存在非极性键的断裂与形成
D.由图可知,*CO转化为CH g的反应速率小于*CO转化为C H g的反应速率
4 2 4
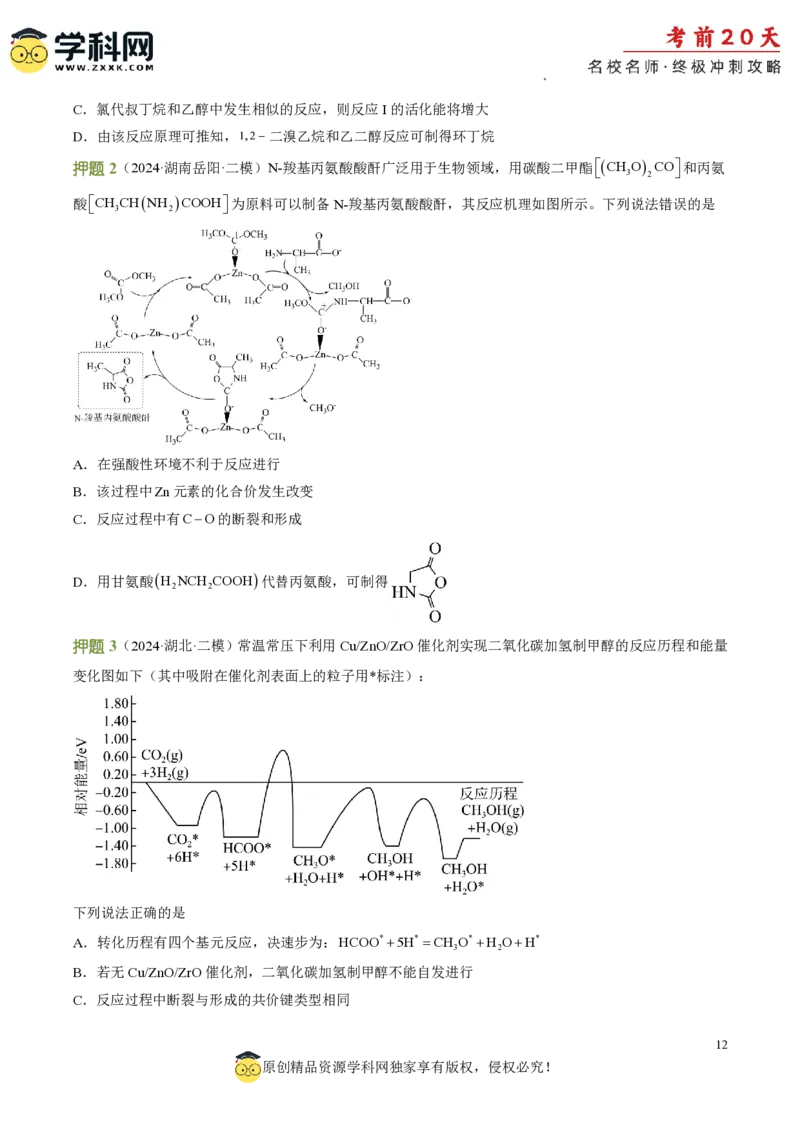
押题1(2024·湖南益阳·三模)溴代叔丁烷与乙醇的反应进程中的能量变化如图所示。下列说法正确的是
A.溴代叔丁烷与乙醇的反应为吸热
B.溴代叔丁烷和乙醇的总反应速率由反应Ⅲ决定
11
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司C.氯代叔丁烷和乙醇中发生相似的反应,则反应I的活化能将增大
D.由该反应原理可推知,1,2二溴乙烷和乙二醇反应可制得环丁烷
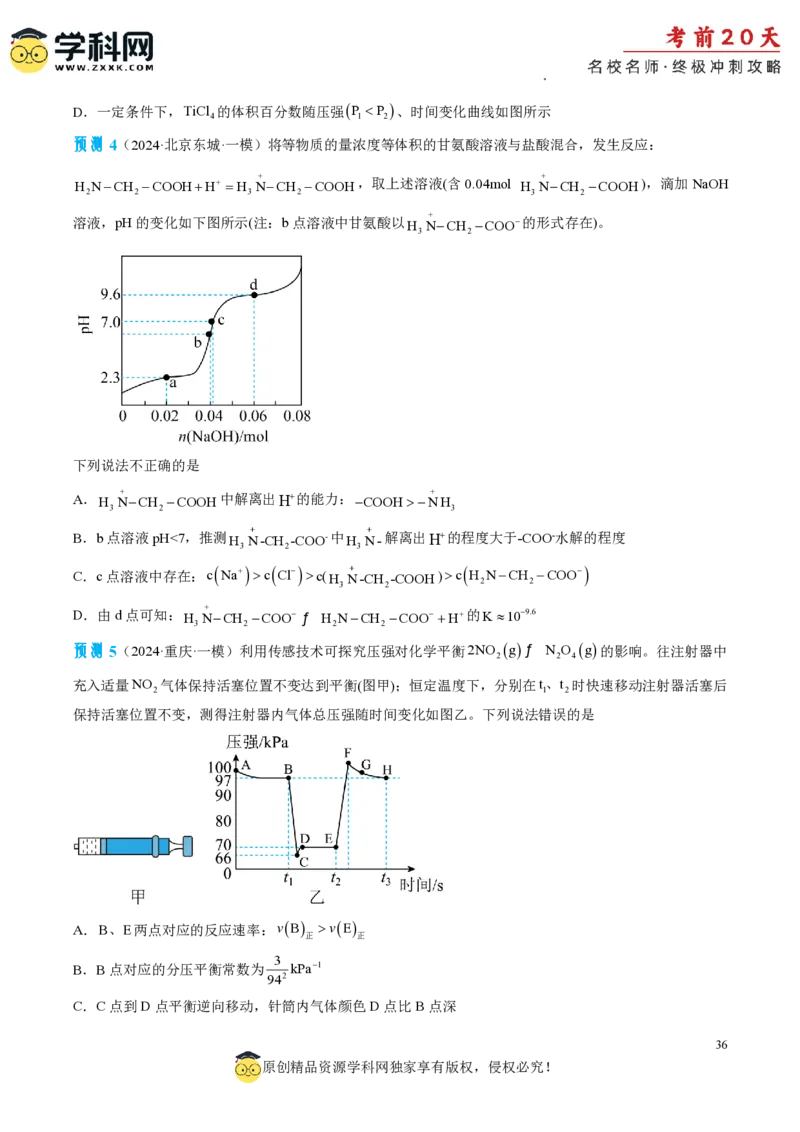
押题2(2024·湖南岳阳·二模)N-羧基丙氨酸酸酐广泛用于生物领域,用碳酸二甲酯CH O CO和丙氨
3 2
酸
CH
3
CHNH
2
COOH
为原料可以制备N-羧基丙氨酸酸酐,其反应机理如图所示。下列说法错误的是
A.在强酸性环境不利于反应进行
B.该过程中Zn元素的化合价发生改变
C.反应过程中有CO的断裂和形成
D.用甘氨酸H NCH COOH代替丙氨酸,可制得
2 2
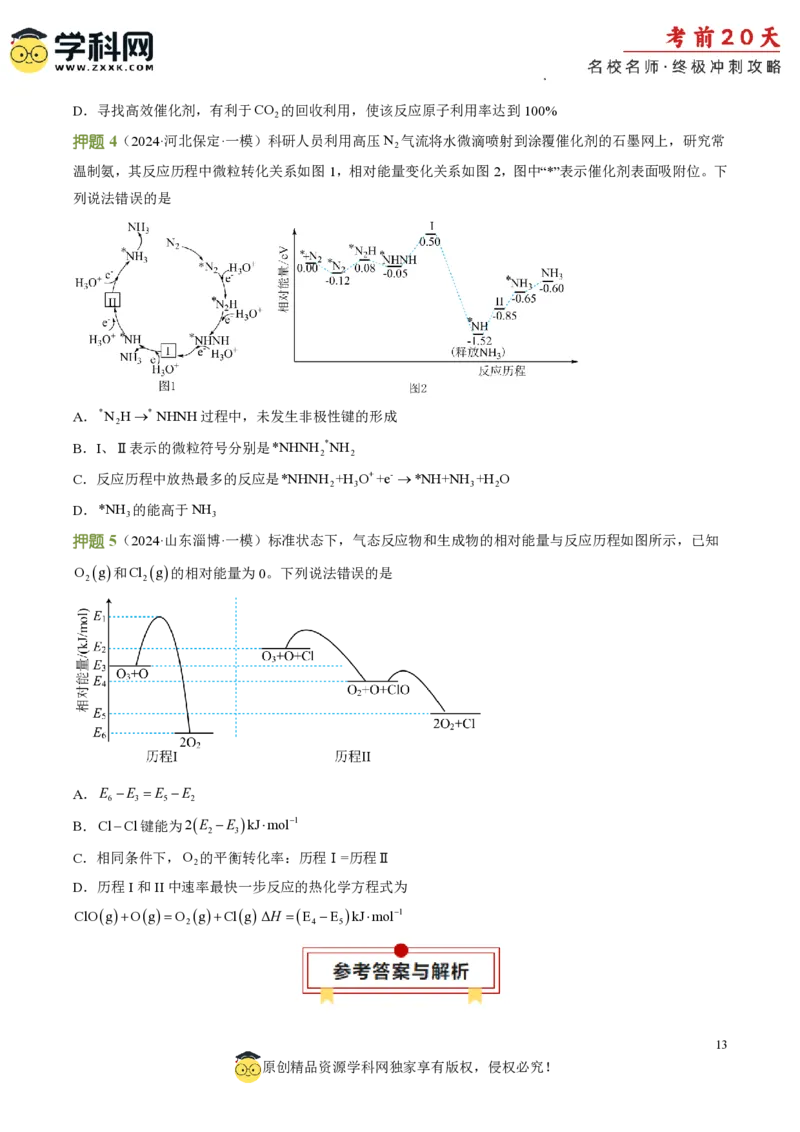
押题3(2024·湖北·二模)常温常压下利用Cu/ZnO/ZrO催化剂实现二氧化碳加氢制甲醇的反应历程和能量
变化图如下(其中吸附在催化剂表面上的粒子用*标注):
下列说法正确的是
A.转化历程有四个基元反应,决速步为:HCOO*5H* CH O*H OH*
3 2
B.若无Cu/ZnO/ZrO催化剂,二氧化碳加氢制甲醇不能自发进行
C.反应过程中断裂与形成的共价键类型相同
12
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司D.寻找高效催化剂,有利于CO 的回收利用,使该反应原子利用率达到100%
2
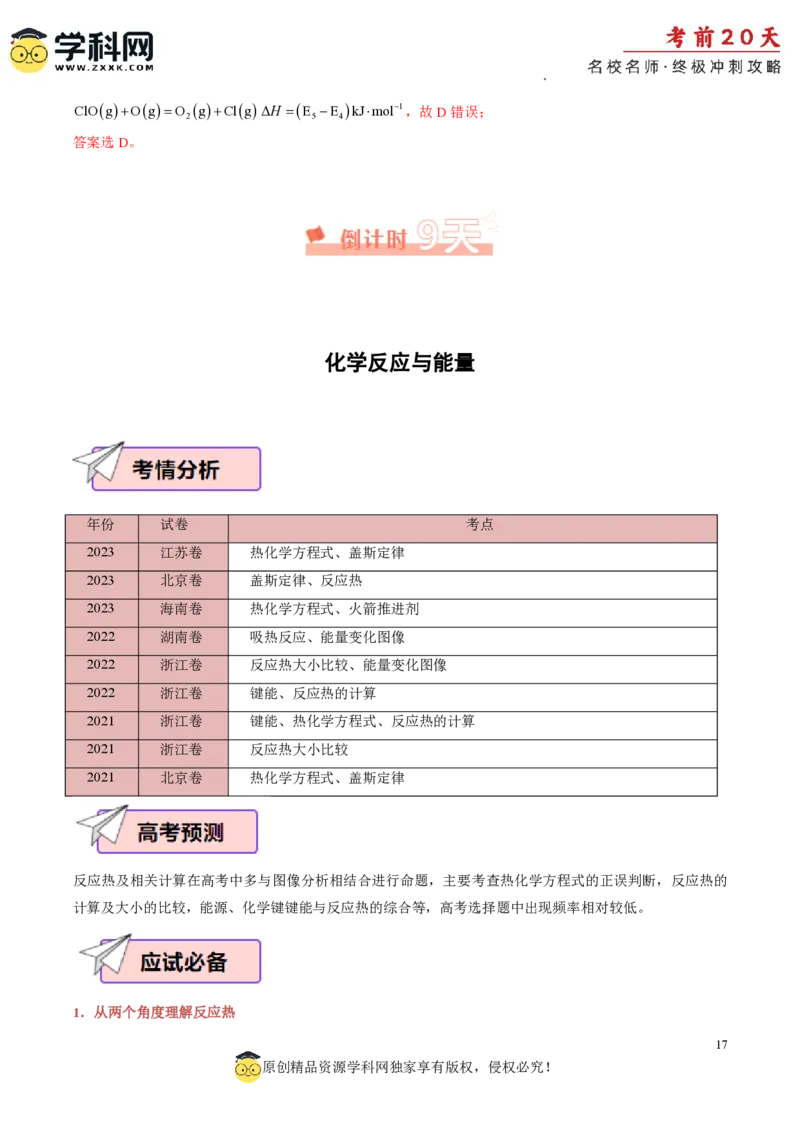
押题4(2024·河北保定·一模)科研人员利用高压N 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常
2
温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位。下
列说法错误的是
A.*N H* NHNH过程中,未发生非极性键的形成
2
B.I、Ⅱ表示的微粒符号分别是*NHNH *NH
2 2
C.反应历程中放热最多的反应是*NHNH +H O++e- *NH+NH +H O
2 3 3 2
D.*NH 的能高于NH
3 3
押题5(2024·山东淄博·一模)标准状态下,气态反应物和生成物的相对能量与反应历程如图所示,已知
O g和Cl g的相对能量为0。下列说法错误的是
2 2
A.E E E E
6 3 5 2
B.ClCl键能为2E E kJmol1
2 3
C.相同条件下,O 的平衡转化率:历程Ⅰ=历程Ⅱ
2
D.历程I和II中速率最快一步反应的热化学方程式为
ClOgOgO gClg ΔH E E kJmol1
2 4 5
13
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司名校预测
预测1
【答案】D
【解析】A.步骤I的活化能大于步骤II,反应速率步骤I更小,故A正确;
B.O原子上有两对孤对电子,排斥力较大,键角H—C—H>H—O—C,故B正确;
C.根据反应机理可知,若MO+与CHD 反应,生成的氘代甲醇可能为CHD OD或CD OH,共两种,故C
2 2 3
正确;
D.根据反应历程能量变化图所示,总反应的反应热为E -E +E -E ,故D错误;
1 2 3 4
答案选D。
预测2
【答案】D
【解析】A.由图1可知,反应物为H O 和 CO,生成物为CO 和 H ,故水煤气变换反应为H O +
2 2 2 2
Au
n
CO CO + H ,A正确;
2 2
B.物质的能量越低越稳定,FSe 的能量比FSe 的低,故稳定性:FSe 大于FSe ,B正确;
2 1 2 1
C.由图2可知,反应物总能量高于生成物总能量,故水煤气变换反应的H<0,C正确;
D.制约总反应速率的反应为活化能最大的反应,由图1、2可知,活化能最大的反应为H O=OH+H,D
2
错误;
答案选D。
预测3
【答案】B
【解析】A.根据图知,反应历程中的第一个反应涉及氢原子的成键,第二个反应没涉及氢原子的成键,A
错误;
B.已知其他条件不变时,反应物中的元素被质量数更大的同位素替换时,反应速率会变慢,所以相同条件
下,CD 与FeO发生上述反应,反应速率会变慢,则其过渡态Ⅰ的能量比b高,B正确;
4
C.该反应的H e-akJmol1,即生成物的能量减去反应物的能量,C错误;
D.根据图可知,CH D与FeO发生上述反应,可以获得CH OD、CH DOH有机产物,D错误;
3 3 2
故选B。
预测4
【答案】B
【解析】A.由图可知,①表示CO和H O在催化剂表面吸附的过程,故A错误;
2
B.②和④中化学键变化相同,断裂的均为H-O键,②中吸收能量[1.25-(-0.32)]eV=1.57eV,④中吸收能量
14
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司为[1.41-(-0.16)]eV=1.57eV,两者吸收的能量相同,故B正确;
C.由图可知,CO(g)和H O(g)的总能量大于CO (g)+H (g)的总能量,因此反应CO(g)+H O(g)=CO (g)+H (g)
2 2 2 2 2 2
为放热反应,故C错误;
D.由图可知,相同条件下,④的活化能为(1.86+0.16)eV=2.02eV,②的活化能为(1.59+0.32)eV=1.91eV,④
的活化能大于②,则反应速率④<②,决定反应速率的步骤是④,故D错误;
故选:B。
预测5
【答案】B
【解析】A.图中没有给出CO g的能量,则无法计算CO g转化为CH g过程放出的热量,A错误;
2 2 4
B.由图可知,*CO转化为C H g的历程中,最大活化能*CO*COH*COCOH时的需要的活化能,则
2 4
最大活化能为0.77eV,B正确;
C.*CO*COH*COCOH时,不存在非极性键的断裂,C错误;
D.由图可知,*CO转化为CH g的最大活化能为0.19eV,结合选项B可知,*CO转化为CH g的最大
4 4
活化能较小,反应速率较快,D错误;
故选B。
名师押题
押题1
【答案】C
【解析】A.根据反应过程中反应物的总能量高于生成物的总能量,该反应为放热反应,A错误;
B.由图可知,反应Ⅰ的活化能最大,所以溴代叔丁烷和乙醇的总反应速率由反应Ⅰ决定,B错误;
C.由图可知,反应Ⅰ中碳卤键会断裂,C-Cl的键长小于C-Br,所以C-Cl的键能大,断裂需要的能量多,
反应Ⅰ的活化能将增大,C正确;
D.由该反应原理可知醇在反应过程中断裂羟基的O-H键,卤代烃断裂碳卤键,会生成醚键,所以1,2二
溴乙烷和乙二醇反应不能制得环丁烷,D错误;
故选C。
押题2
【答案】B
【解析】A.在强酸性溶液中,碳酸二甲酯会发生水解,同时CH CH(NH )COO-浓度降低,不利于反应进行,A
3 2
正确;
B.碳酸二甲酯(CH O) CO]与Zn(CH COO) 形成的是配位键,整个过程中均未有元素化合价发生变化,B
3 2 3 2
错误;
C.该过程中存在N—H、C—O等极性键的断裂和生成,C正确;
15
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司D.若用甘氨酸(H NCH COOH)代替丙氨酸,则根据转化关系,最后可得到 ,D正确;
2 2
故答案为:B。
押题3
【答案】A
【解析】A.由图可知,转化历程有四个基元反应;活化能越大,反应越慢,为决速步,决速步为
HCOO*5H* CH O*H OH*,故A正确;
3 2
B.催化剂能改变反应的速率,不能决定反应是否自发进行,无Cu/ZnO/ZrO催化剂,二氧化碳加氢制甲醇
依然能自发进行,故B错误;
C.反应过程中断裂与形成的共价键类型不相同,故C错误;
D.反应产物还有水生成,原子利用率不可能达到100%,故D错误。
答案选A。
押题4
【答案】D
【解析】
A.*N H*NHNH过程中,有极性键的形成,未发生非极性键的形成,A正确;
2
B.由图1可知,I、Ⅱ表示的微粒符号分别是*NHNH 、*NH ,B正确;
2 2
C.反应历程中放热最多的反应是I和H O+、e-的反应,反应方程式为
3
*NHNH +H O++e- *NH+NH +H O,C正确;
2 3 3 2
D.由图2可知,*NH 的能量低于NH ,D错误;
3 3
故选D。
押题5
【答案】D
【解析】A.由图可知,Cl原子是历程Ⅱ的催化剂,催化剂不能改变反应的反应热,则历程Ⅰ、Ⅱ的反应
热相等,即△H=E -E =E -E ,故A正确;
6 3 5 2
B.Cl (g)的相对能量为0,由图可知Cl(g)的相对能力为(E -E )kJ/mol,断裂化学键吸收热量,Cl (g)→2Cl(g)
2 2 3 2
吸收能量为2(E -E )kJ/mol,则Cl-Cl键能为2(E -E )kJ/mol,故B正确;
2 3 2 3
C.催化剂不能改变反应的始态和终态,不能改变反应物的平衡转化率,即相同条件下O 的平衡转化率:
3
历程Ⅱ=历程Ⅰ,故C正确;
D.由图可知,历程Ⅱ中第二步反应的活化能小于第一步反应的活化能,反应的活化能越低,反应速率越快,
则历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
16
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司ClOgOgO gClg ΔH E E kJmol1,故D错误;
2 5 4
答案选D。
化学反应与能量
年份 试卷 考点
2023 江苏卷 热化学方程式、盖斯定律
2023 北京卷 盖斯定律、反应热
2023 海南卷 热化学方程式、火箭推进剂
2022 湖南卷 吸热反应、能量变化图像
2022 浙江卷 反应热大小比较、能量变化图像
2022 浙江卷 键能、反应热的计算
2021 浙江卷 键能、热化学方程式、反应热的计算
2021 浙江卷 反应热大小比较
2021 北京卷 热化学方程式、盖斯定律
反应热及相关计算在高考中多与图像分析相结合进行命题,主要考查热化学方程式的正误判断,反应热的
计算及大小的比较,能源、化学键键能与反应热的综合等,高考选择题中出现频率相对较低。
1.从两个角度理解反应热
17
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司能量
示意图
微观 宏观
图像 a表示断裂旧化学键吸收的能量; a表示反应物形成活化分子吸收的能量(正反应的活化能);
分析 b表示形成新化学键放出的能量; b表示活化分子形成生成物释放的能量(逆反应的活化能);
c表示反应热 c表示反应热
ΔH的计
ΔH=H(生成物)-H(反应物) ΔH=E(反应物总键能)-E(生成物总键能)
算
2.热化学方程式书写与判断的注意事项
(1)注意ΔH的符号和单位:吸热反应的ΔH为“+”,放热反应的ΔH为“-”;ΔH的单位为kJ·mol-1。
(2)注意测定条件:绝大多数反应的反应热是在25 ℃、101 kPa下测定的,此时可不注明温度和压强。
(3)注意热化学方程式中的化学计量数:热化学方程式中的化学计量数可以是整数,也可以是分数。
(4)注意物质的聚集状态:气体用“g”,液体用“l”,固体用“s”,溶液用“aq”。热化学方程式中不用“↑”和
“↓”。
(5)注意ΔH的数值与符号:如果化学计量数加倍,则ΔH也要加倍。逆反应的反应热与正反应的反应热
数值相等,但符号相反。
(6)对于具有同素异形体的物质,除了要注明聚集状态外,还要注明物质的名称。例如:S(单斜,s)===S(正
交,s) ΔH=-0.33 kJ·mol-1。
3.反应热(ΔH)的大小比较
对于放热反应来说,ΔH=-Q kJ·mol-1,虽然“-”仅表示放热的意思,但在比较大小时要将其看成真正意
义上的“负号”,即放热越多,ΔH反而越小。如:
(1)同一反应,生成物状态不同时,例如A(g)+B(g)===C(g) ΔH <0,A(g)+B(g)===C(l) ΔH <0,因为
1 2
C(g)===C(l) ΔH <0,则ΔH =ΔH -ΔH ,所以ΔH <ΔH 。
3 3 2 1 2 1
(2)同一反应,反应物状态不同时,例如S(g)+O (g)===SO (g) ΔH <0,S(s)+O (g)===SO (g) ΔH <0,
2 2 1 2 2 2
,ΔH +ΔH =ΔH ,则ΔH =ΔH -ΔH ,又ΔH <0,所以ΔH <ΔH 。
2 3 1 3 1 2 3 1 2
3.根据盖斯定律计算ΔH的方法
18
原创精品资源学科网独家享有版权,侵权必究!
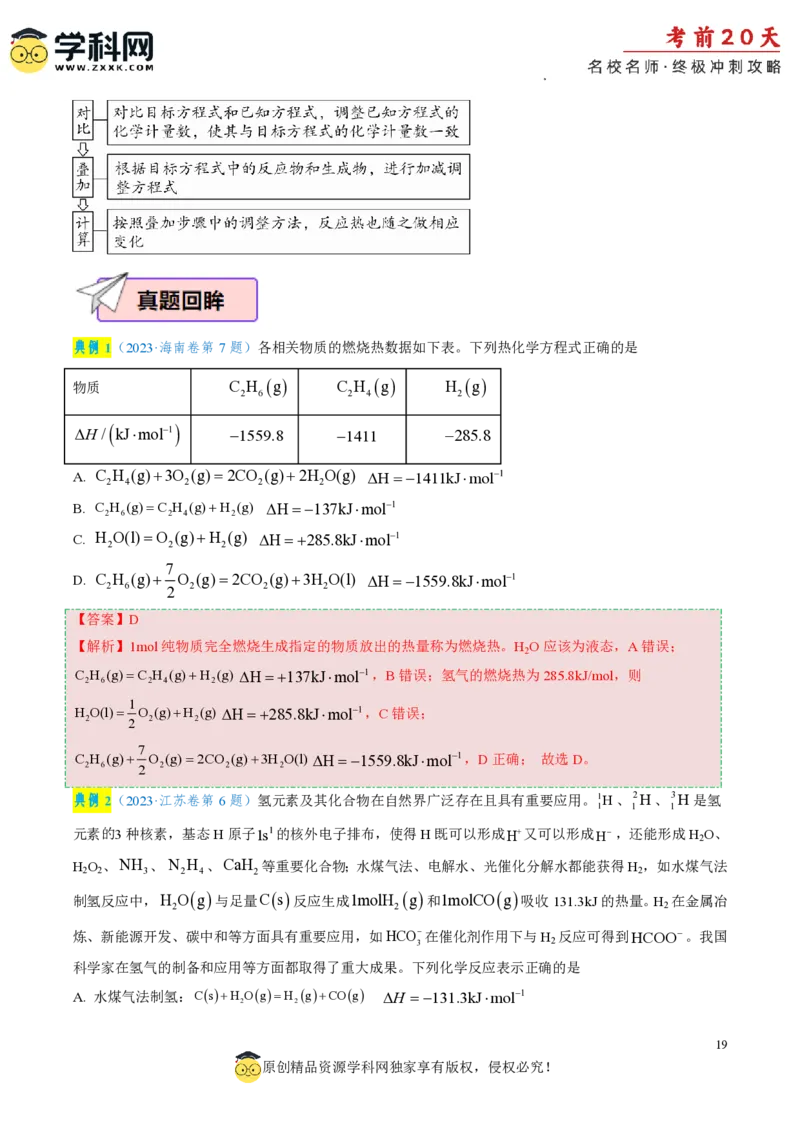
学科网(北京)股份有限公司典例1(2023·海南卷第7题)各相关物质的燃烧热数据如下表。下列热化学方程式正确的是
物质 C H g C H g H g
2 6 2 4 2
H /
kJmol1
1559.8 1411 285.8
A. C H (g)3O (g)2CO (g)2H O(g) H1411kJmol1
2 4 2 2 2
B. C H (g)C H (g)H (g) H137kJmol1
2 6 2 4 2
C. H O(l)O (g)H (g) H285.8kJmol1
2 2 2
7
D. C H (g) O (g)2CO (g)3H O(l) H1559.8kJmol1
2 6 2 2 2 2
【答案】D
【解析】1mol纯物质完全燃烧生成指定的物质放出的热量称为燃烧热。H O应该为液态,A错误;
2
C H (g)C H (g)H (g) H137kJmol1,B错误;氢气的燃烧热为285.8kJ/mol,则
2 6 2 4 2
1
H O(l) O (g)H (g) H285.8kJmol1,C错误;
2 2 2 2
7
C H (g) O (g)2CO (g)3H O(l) H1559.8kJmol1,D正确; 故选D。
2 6 2 2 2 2
典例2(2023·江苏卷第6题)氢元素及其化合物在自然界广泛存在且具有重要应用。1H、2H、3H是氢
1 1 1
元素的3种核素,基态H原子1s1的核外电子排布,使得H既可以形成H又可以形成H,还能形成H O、
2
H O 、NH 、 N H 、CaH 等重要化合物;水煤气法、电解水、光催化分解水都能获得H ,如水煤气法
2 2 3 2 4 2 2
制氢反应中,H Og 与足量Cs 反应生成1molH g 和1molCOg 吸收131.3kJ的热量。H 在金属冶
2 2 2
炼、新能源开发、碳中和等方面具有重要应用,如HCO在催化剂作用下与H 反应可得到HCOO。我国
3 2
科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
A. 水煤气法制氢:CsH OgH gCOg H 131.3kJmol1
2 2
19
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司催化剂
B. HCO催化加氢生成HCOO的反应:HCOH HCOOH O
3 3 2 2
C. 电解水制氢的阳极反应:2H O2e H 2OH
2 2
D. CaH 与水反应:CaH 2H OCaOH H
2 2 2 2 2
【答案】B
【解析】水煤气法制氢的反应为吸热反应,其热化学方程式为CsH OgH gCOg
2 2
H +131.3kJmol1,A错误;由题意可知HCO在催化剂作用下与H 反应可得到HCOO,根据原
3 2
催化剂
子守恒可得离子方程式为HCOH HCOOH O,B正确;电解水制氢的阳极反应为
3 2 2
4OH 4e O 2H O,C错误;CaH 与水反应化学方程式为CaH 2H OCaOH 2H ,
2 2 2 2 2 2 2
CaH 2H OCaOH H 中H原子不守恒,D错误。 故选B。
2 2 2 2
典例3(2022·浙江卷)相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图所示:
下列推理不正确的是
A.2ΔH ≈ΔH ,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH <ΔH ,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH <ΔH ,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH -ΔH <0,ΔH -ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
【答案】A
【解析】2ΔH ≈ΔH ,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比,但是不能是存在相互
1 2
作用的两个碳碳双键,A错误;ΔH <ΔH ,即单双键交替的物质能量低,更稳定,说明单双键交替的两
2 3
个碳碳双键间存在相互作用,有利于物质稳定,B正确;由图示可知,反应I为: (l)+H (g)→ (l)ΔH
2 1
反应IV为: +3H (g)→ (l)ΔH ,故反应I是1mol碳碳双键加成,如果苯环上有三个完全独立的
2 4
碳碳三键,则3ΔH =ΔH ,现3ΔH <ΔH ,说明苯分子中不存在三个完全独立的碳碳双键,C正确;
1 4 1 4
由图示可知,反应I为: (l)+H (g)→ (l)ΔH 反应III为: (l)+2H (g)→ (l)ΔH 反应IV
2 1 2 3
20
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司为: +3H (g)→ (l)ΔH ,ΔH -ΔH <0即 (l)+H (g)→ (l)ΔH<0,ΔH -ΔH >0即
2 4 3 1 2 4 3
+H (g)→ (l)ΔH>0,则说明 具有的总能量小于 ,能量越低越稳定,则说明苯分子具有
2
特殊稳定性,D正确;故选A。
典例4(2022·浙江卷)标准状态下,下列物质气态时的相对能量如下表:
H O H O
2
物质(g) O H HO HOO H O
2
2 2 2
能量/kJmol-1 249 218 39 10 0 0 -136 -242
可根据HO(g)+HO(g)=H O (g)计算出H O 中氧氧单键的键能为214kJmol-1。下列说法不正确的是
2 2 2 2
A.H 的键能为436kJmol-1 B.O 的键能大于H O 中氧氧单键的键能的两倍
2 2 2 2
C.解离氧氧单键所需能量:HOO0,ΔH >0 B. ΔH =ΔH +ΔH
1 2 3 1 2
C. ΔH >ΔH ,ΔH >ΔH D. ΔH =ΔH +ΔH
1 2 3 2 2 3 4
【答案】C
【解析】一般的烯烃与氢气发生的加成反应为放热反应,但是,由于苯环结构的特殊性决定了苯环结构
的稳定性,苯与氢气发生加成反应生成1,3-环己二烯时,破坏了苯环结构的稳定性,因此该反应为吸热
反应。环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放热反应,因此,H<0,H<0 ,A不正
1 2
确;
苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊的共价键,因此,其与氢气完全加
21
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司成的反应热不等于环己烯、1,3-环己二烯分别与氢气发生的加成反应的反应热之和,即H H H ,B
3 1 2
不正确;环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放反应,H<0,H<0,由于1mol 1,3-环
1 2
己二烯与氢气完全加成后消耗的氢气是等量环己烯的2倍,故其放出的热量更多,其H H ;苯与氢气
1 2
发生加成反应生成1,3-环己二烯的反应为吸热反应(ΔH >0),根据盖斯定律可知,苯与氢气完全加成
4
的反应热H =H +H ,因此H H ,C正确;根据盖斯定律可知,苯与氢气完全加成的反应热
3 4 2 3 2
H =H +H ,因此H H -H ,D不正确。综上所述,本题选C。
3 4 2 2 3 4
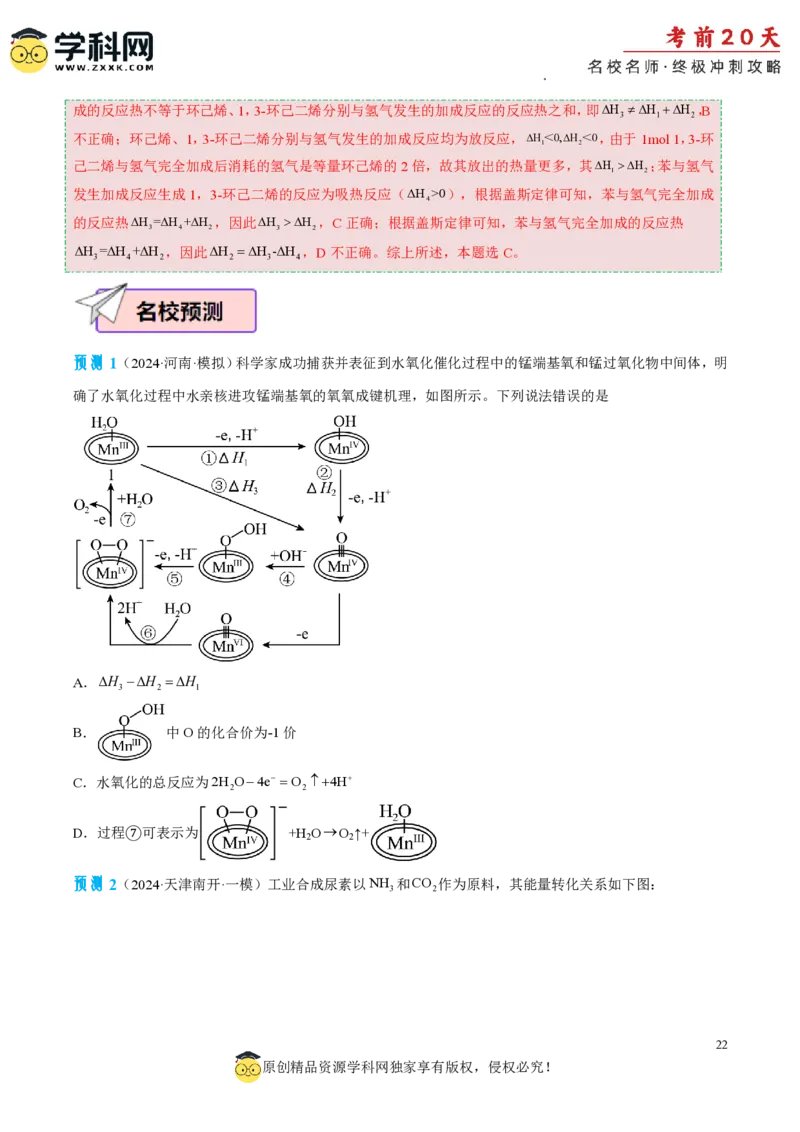
预测1(2024·河南·模拟)科学家成功捕获并表征到水氧化催化过程中的锰端基氧和锰过氧化物中间体,明
确了水氧化过程中水亲核进攻锰端基氧的氧氧成键机理,如图所示。下列说法错误的是
A.H H H
3 2 1
B. 中O的化合价为-1价
C.水氧化的总反应为2H O4e O 4H
2 2
D.过程⑦可表示为 +H OO ↑+
2 2
预测2(2024·天津南开·一模)工业合成尿素以NH 和CO 作为原料,其能量转化关系如下图:
3 2
22
原创精品资源学科网独家享有版权,侵权必究!
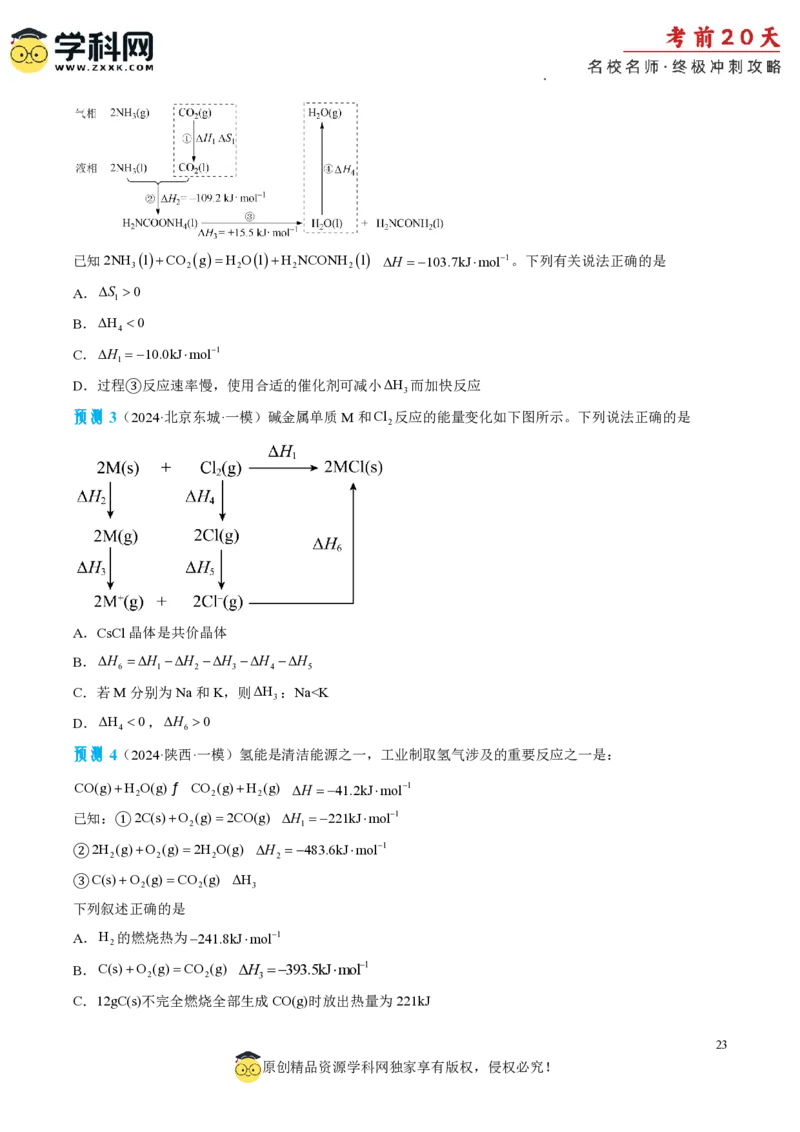
学科网(北京)股份有限公司已知2NH lCO gH OlH NCONH l H 103.7kJmol1。下列有关说法正确的是
3 2 2 2 2
A.S 0
1
B.H 0
4
C.H 10.0kJmol1
1
D.过程③反应速率慢,使用合适的催化剂可减小ΔH 而加快反应
3
预测3(2024·北京东城·一模)碱金属单质M和Cl 反应的能量变化如下图所示。下列说法正确的是
2
A.CsCl晶体是共价晶体
B.H H H H H H
6 1 2 3 4 5
C.若M分别为Na和K,则ΔH :Nav ,则平衡向正反应方向移动;反之向逆反应方向
正 逆
移动。
(3)依据变化过程中速率变化的性质判断
若平衡移动过程中,正反应速率增大的程度小于(大于)逆反应速率增大的程度,则平衡向逆(正)反应方向移
动。
(4)依据浓度商(Q)规则判断
若某温度下QK,反应向逆反应方向进行。
4.化学平衡常数
cpC·cqD
(1)表达式:对于反应mA(g)+nB(g) pC(g)+qD(g),K= 。
cmA·cnB
实例:
化学方程式 平衡常数 关系式
c2NH3 K = K1
N (g)+3H (g)2NH (g) K = 2
2 2 3 1
cN2·c3H2
1
K =
1 3 3 K1
N (g)+ H (g)NH (g)
2 2 3
2 2
cN2·c3H2
2NH (g)N (g)+3H (g) K =
3 2 2 3
c2NH3
(2)意义
①K值越大,正反应进行的程度越大,反应物的转化率越大。
②K只受温度影响,与反应物或生成物的浓度变化无关,吸热反应,升高温度,K增大,放热反应,升高
温度,K减小。
典例1(2023·江苏卷第13题)二氧化碳加氢制甲烷过程中的主要反应为
CO g4H gCH g2H Og H 164.7kJmol1
2 2 4 2
CO gH gCOgH Og H 41.2kJmol1
2 2 2
在密闭容器中,1.01105Pa、n CO :n H 1:4时,CO 平衡转化率、在催化剂作用下反应相
起始 2 起始 2 2
n CH
同时间所测得的CO 实际转化率随温度的变化如题图所示。CH 的选择性可表示为 生成 4 100%。
2 4 n CO
反应 2
下列说法正确的是
31
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A. 反应2COg2H gCO gCH g 的焓变H205.9kJmol1
2 2 4
B. CH 的平衡选择性随着温度的升高而增加
4
C. 用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
n H
起始 2
D. 450℃时,提高 的值或增大压强,均能使CO 平衡转化率达到X点的值
n CO 2
起始 2
【答案】D
【解析】由盖斯定律可知反应2COg2H gCO gCH g
的焓变
2 2 4
H241.2kJmol1164.7kJmol1 247.1kJmol1,A错误;
CO g4H gCH g2H Og 为放热反应,升高温度平衡逆向移动,CH 的含量降低,故CH
2 2 4 2 4 4
的平衡选择性随着温度的升高而降低,B错误;由图可知温度范围约为450~550℃时二氧化碳实际转化率
n H
起始 2
趋近于平衡转化率,此时为最适温度,温度继续增加,催化剂活性下降,C错误;450℃时,提高
n CO
起始 2
的值可提高二氧化碳的平衡转化率,增大压强反应I平衡正向移动,可提高二氧化碳的平衡转化率,均能
使CO 平衡转化率达到X点的值,D正确。 故选D。
2
典例2(2023·海南卷第13题)工业上苯乙烯的生产主要采用乙苯脱氢工艺:
C H CH CH (g)ƒ C H CHCH (g)H (g)。某条件下无催化剂存在时,该反应的正、逆反应速率
6 5 2 3 6 5 2 2
v随时间t的变化关系如图所示。下列说法正确的是
A. 曲线①表示的是逆反应的v-t关系
B. t 时刻体系处于平衡状态
2
C. 反应进行到t 时,Q K (Q为浓度商)
1
32
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司D. 催化剂存在时,v 、v 都增大
1 2
【答案】BD
【解析】反应为乙苯制备苯乙烯的过程,开始反应物浓度最大,生成物浓度为0,所以曲线①表示的是正
反应的v-t关系,曲线表示的是逆反应的v-t关系,故A错误;t 时,正逆反应速率相等,体系处于平衡
2
状态,故B正确;反应进行到t 时,反应正向进行,故Q<K,故C错误;催化剂能降低反应的活化能,
1
使反应的v 、v 都增大,故D正确;故选BD。
1 2
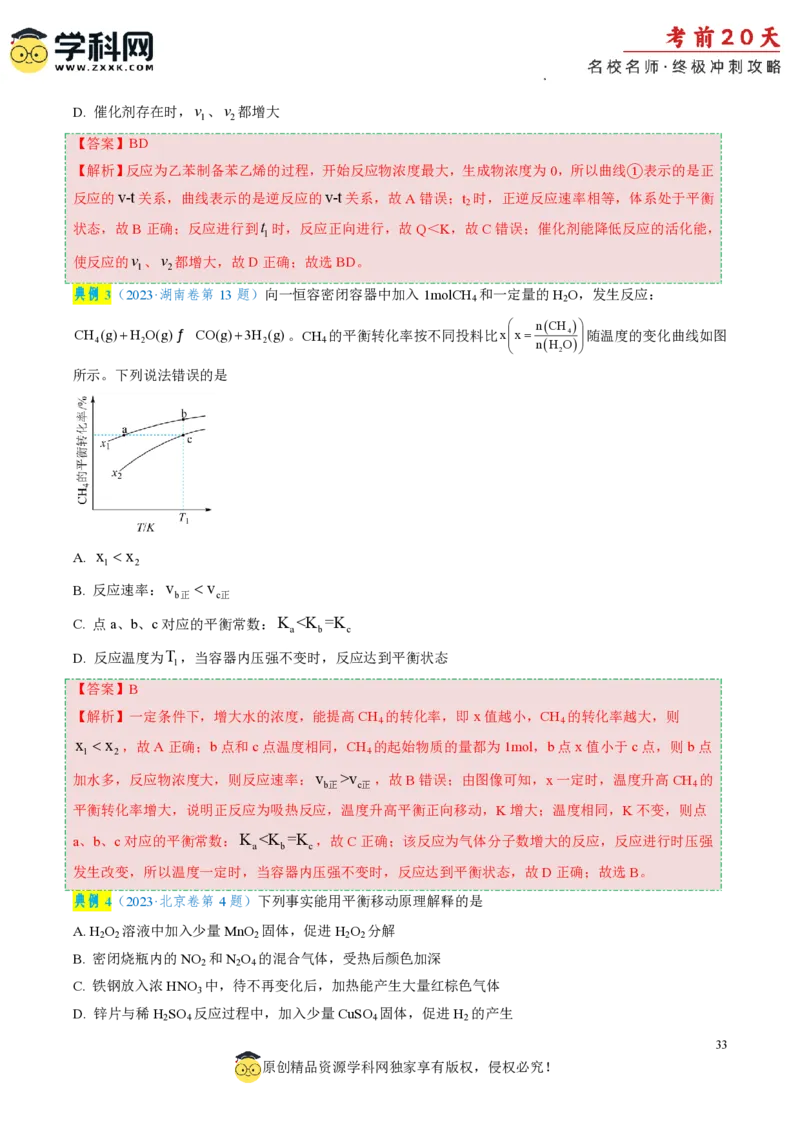
典例3(2023·湖南卷第13题)向一恒容密闭容器中加入1molCH 和一定量的H O,发生反应:
4 2
nCH
CH (g)H O(g)ƒ CO(g)3H (g)。CH 的平衡转化率按不同投料比xx 4 随温度的变化曲线如图
4 2 2 4 nH O
2
所示。下列说法错误的是
A. x x
1 2
B. 反应速率:v v
b正 c正
C. 点a、b、c对应的平衡常数:K v ,故B错误;由图像可知,x一定时,温度升高CH 的
b正 c正 4
平衡转化率增大,说明正反应为吸热反应,温度升高平衡正向移动,K增大;温度相同,K不变,则点
a、b、c对应的平衡常数:K γA,
2 1 2 1
错误;
B.该反应正向为放热反应,温度越高,K越小,故K >K =K ,B错误;
a b c
C.由于产物之一为固体,容器恒容,若反应未平衡,气体总质量会改变,气体密度会改变,故当容器内气
体密度不变时,反应达到平衡,C正确;
D.正向反应气体体积数减小,温度一定,增大压强,平衡正向移动,Y的转化率升高,温度不变,不会向
a点方向移动,D错误;
本题选C。
预测2
【答案】C
【解析】A.从表中可知,20min时,N O浓度为0.080 molL1,而在60min时,N O浓度变为原来的一半,
2 2
(0.0800.040)mol/L
因此N O消耗一半时的反应速率= =0.0010molL1min1,A正确;
2 40min
B.由表中数据可知,每20minN O浓度消耗0.020mol/L,因此当100min时N O消耗完全,B正确;
2 2
C.由表中数据可知,该反应匀速进行,与起始浓度无关,C错误;
D.结合选项A的解析,N O起始浓度为0.080 molL1时,40分钟达到半衰期,代入关系式验证,可得:
2
40min=500×0.080,D正确。
因此,本题选C。
预测3
【答案】C
【解析】A.催化剂只会改变反应速率,不能改变H,A错误;
B.该反应的正反应是放热反应,保持其他条件不变,平衡时升高温度,v 、v 都增大,B错误;
正 逆
c2COcTiCl
C.该反应的化学平衡常数K= 4 ,化学平衡常数只与温度有关,保持其他条件不变,平衡时
c2Cl
2
通入Cl ,即增大了反应物的浓度,化学平衡正向移动,但由于温度不变,因此化学平衡常数不变,达到新
2
40
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司c2Cl
平衡时 2 不变,C正确;
c2COcTiCl
4
D.该反应为体积分数增大的反应,压强增大平衡逆向移动,一定条件下,TiCl 的体积百分数随压强
4
P P 、时间变化曲线应该P 条件下体积分数更大,D错误;
1 2 1
故答案为:C。
预测4
【答案】C
+
【分析】甘氨酸溶液与盐酸混合,发生反应:H N-CH -COOH+H+=H N-CH -COOH,向反应后的溶液中
2 2 3 2
+ +
加氢氧化钠溶液,依次发生H N-CH -COOH+OH-=H N-CH -COO-+H O、
3 2 3 2 2
+
H N-CH -COO-+OH-=H N-CH -COO-+H O。
3 2 2 2 2
+
【解析】A.甘氨酸溶液与盐酸混合,发生反应:H N-CH -COOH+H+=H N-CH -COOH,生成物为
2 2 3 2
+ +
H N-CH -COOH,再向其中加氢氧化钠溶液,继续反应,b点溶液中甘氨酸以H N-CH -COO-的形式存
3 2 3 2
+
在,即-COOH更容易和氢氧化钠溶液反应,所以解离出H+的能力:-COOH>-NH ,故A正确;
3
+ +
B.b点溶液中甘氨酸以H N-CH -COO-的形式存在,-COO-水解使溶液有呈碱性的趋势、H N-电离使溶
3 2 3
+ +
液有呈酸性的趋势,b点溶液pH<7,所以H N-CH -COO-中H N-解离出H的程度大于-COO-水解的程度,
3 2 3
故B正确;
C.c点n(NaOH)>0.04mol,而溶液中n(Cl-)=0.04mol,所以n(NaOH)>n(Cl-),即c(NaOH)>c(Cl-),甘氨酸
+
溶液与盐酸混合,发生反应:H N-CH -COOH+H+=H N-CH -COOH,向反应后的溶液中加氢氧化钠溶液,b
2 2 3 2
+ +
点溶液中甘氨酸以H N-CH -COO-的形式存在,此时H N-CH -COOH与氢氧化钠恰好完全反应:
3 2 3 2
+ +
H N-CH -COOH+OH-=H N-CH -COO-+H O,再加氢氧化钠溶液,发生反应:
3 2 3 2 2
H N + -CH -COO-+OH-=H N-CH -COO-+H O,生成H N-CH -COO-,所以c点溶液中应是存在:
3 2 2 2 2 2 2
c(H N-CH -COO-)> c(H N + -CH -COOH),故C错误;
2 2 3 2
+ +
D.b点0.04molNaOH与0.04molH N-CH -COOH反应,生成0.04mol H N-CH -COO-,再加的
3 2 3 2
0.02molNaOH与0.02molH N + -CH -COO-反应,生成0.02molH N-CH -COO-,即d点溶液中
3 2 2 2
H N-CH -COO-与H N + -CH -COO-的物质的量相等,又pH=9.6,即c(H+)=10-9.6mol/L,所以
2 2 3 2
c(H N-CH -COO-)c(H+)
H N + -CH -COO- ƒ H N-CH -COO-+H+的K= 2 + 2 c(H+)=10-9.6 ,故D正确;
3 2 2 2 c(H N-CH -COO-)
3 2
41
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司故答案为:C。
预测5
【答案】C
【解析】A.压强越大、反应速率越快,则B、E两点对应的正反应速率:v(B) >v(E) ,A正确;
正 正
2NO gƒ N O g
2 2 4
起始kPa 100 0 100 100
B.根据物质的量之比等于压强之比, 解得x=3,二氧
变化kPa 2x x 97 100x
平衡kPa 1002x x
3
化氮的分压为94kPa,四氧化二氮的分压为3kPa,K = kPa-1,B正确;
p 942
C.t 时快速拉动注射器活塞,针筒内气体体积增大,压强迅速减小,C点到D点平衡逆向移动,但是平衡
1
移动的影响小于浓度减小的影响,所以针筒内气体颜色D比B点浅,C错误;
D.t 时快速推动注射器活塞,针筒内气体体积减小,压强迅速增大,保持活塞位置不变后,平衡向着正向
2
m
移动,混合气体的物质的量减小,故E、F、H三点中,H点的气体的物质的量最小,根据n= 可知,H
M
点的气体平均相对分子质量最大,D正确;
答案选C。
名师押题
押题1
【答案】B
【分析】速率方程为v=kcα(H )·cβ(Br )·cγc(HBr),将表中数据代入速率方程可得到①vk0.1α0.1β2γ ②,
2 2
8vk0.1α0.4β2γ,③16vk0.2α0.4β2γ,④2vk0.4α0.1β4γ,由①②得到
3 3
β ,②③得到α1,①④得到γ1,对于⑤4vk0.2α0.1βcγ与①,将α1,β ,γ1
2 2
代入,解得c=1,据此分析解题。
【解析】A.根据分析,α的值为1,A正确;
B.根据分析,c的值为1,B错误;
3
C.由于v=kcα(H )·cβ(Br )·cγc(HBr),α1,β ,γ1,速率与H (g)和Br (g)的浓度成正比,与HBr(g)
2 2 2 2
2
的浓度成反比,反应体系的三种物质中,Br (g)的浓度对反应速率影响最大,C正确;
2
D.由于γ1,增大HBr(g)的浓度,cγc(HBr)减小,在反应体系中保持其他物质浓度不变,增大HBr(g)浓
度,会使反应速率降低,D正确;
答案选B。
42
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司押题2
【答案】C
【分析】反应Ⅰ为吸热反应,反应Ⅱ和反应Ⅲ是放热反应,升高温度反应Ⅰ平衡正向移动,反应Ⅱ和反应Ⅲ
平衡逆向移动,CO和H 的摩尔分数增大,且H 的摩尔分数大于CO,曲线b代表H ,a代表CO,以此
2 2 2
解答。
【解析】A.由盖斯定律可知,反应Ⅰ+反应Ⅲ可得反应Ⅱ,CO g4H gCH g2H Og
2 2 4 2
ΔH =ΔH +ΔH =42.1kJmol1-206.0kJmol1=-163.9kJmol1,该反应为放热反应,低温下有利于反应Ⅱ正
2 1 3
向进行,A正确;
B.由分析可知,曲线b代表H ,B正确;
2
C.由分析可知,曲线b代表H ,a代表CO,当x(CO)=x(CO )时,温度高于500℃,x(H )>x(H O),反应I
2 2 2 2
xCOxH O xH O
的平衡常数K = 2 = 2 1,p点温度低于500℃,反应I是吸热反应,温度降低平衡常
p xCO xH xH
2 2 2
数减小,则P点时反应I的K <1,C错误;
p
D.由图可知,高温时反应I进行程度很大,反应II、III程度很小接近于0,CH 含量很少接近于0,则平
4
衡不受压强影响,适当增大体系压强,nCO保持不变,D正确;
故选C。
押题3
【答案】D
【解析】A.由图看出,随着温度升高,CH OH的选择性(S-CH OH)逐渐降低,反应①向逆方向进行,因
3 3
此正反应H 0;同时,随着温度升高,前期CO 的平衡转化率逐渐降低,此阶段体系发生的反应主要是
1 2
反应①,后期CO 的平衡转化率逐渐升高,此阶段体系发生的反应主要是反应②,因此H 0,A错误;
2 2
B.温度太低,反应不能正常进行,反应速率减小,不利于甲醇的合成,B错误;
C.T℃时,根据CO 的平衡转化率为30%,得出两个反应共消耗0.3mol CO ,又因为CH OH的选择性为
2 2 3
80%,可知0.3mol CO 中有80%即0.24mol发生反应①转化为CH OH,根据反应方程式
2 3
CO (g)+3H (g)⇌CH OH(g)+H O(g),消耗氢气0.72mol,有0.06mol CO 发生反应②,根据方程式
2 2 3 2 2
0.78mol
CO (g)+H (g)⇌CO(g)+H O(g),消耗氢气0.06mol,H 共消耗0.78mol,转化率为 100%26%,C
2 2 2 2 3mol
错误;
D.根据方程式,反应①消耗氢气0.72mol的同时,生成水和甲醇都是0.24mol,反应②氢气0.06mol的同
时,生成水和一氧化碳都是0.06mol,此时,体系中剩余未反应的CO 0.7mol,氢气剩余2.22mol,CO有
2
0.06mol,H O共有0.3mol,甲醇0.24mol,反应②的
2
43
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司nH O nCO
2 p p
n总 n总 nCOnH O 0.06mol0.3mol
K 2 1.16102,D正确;
p nCO nH nCO nH 0.7mol2.22mol
2 p 2 p 2 2
n总 n总
本题选D。
押题4
【答案】D
【解析】A.根据盖斯定律,反应Ⅲ=反应Ⅱ-反应Ⅰ,则H H H 206.1kJmol1,A错误;
3 2 1
B.温度升高,反应Ⅰ正向移动,反应Ⅱ和Ⅲ逆向移动,可知c线为CO,a为CO ,b为CH ,649℃时,
2 4
反应平衡时nH 1.2mol,转换为氢气为0.8mol,生成的H O小于0.8mol,nCOnCO ,平衡常数:
2 2 2
0.8 2
K 1,B错误;
1.2 3
C.由图像可知,250℃~649℃范围内,随着温度的升高,平衡时nH 增大,平衡逆向移动,则平衡时nH O
2 2
不断减小;649℃~900℃范围内,随着温度的升高,平衡时nH 减小,平衡正向移动,则平衡时nH O不
2 2
断增大,C错误;
D.高温时反应I进行程度很大,反应II、III程度很小,CH 含量很少,平衡不受压强影响,适当增大体系
4
压强,nCO保持不变,D正确;
答案选D。
押题5
【答案】C
【解析】A.由图可知M,的起始浓度为0.5mol L,反①应的速率v kc2M,反②应的速率v k c2M,k 、k
1 1 2 2 1 2
为速率常数,则同一反应体系中反应①、②的速率之比始终不变,所以Y、Z的浓度变化之比始终不变,A
错误;
B.①MN XZ②MN XY,则体系中始终有cYcZΔcM,由图可知,30min时
0.2mol/L
ΔcM0.5mol/L0.300mol/L0.2mol/L,M的平均反应速率为 6.7103mol/Lmin,B
30min
错误;
C.30min时,cZ0.125mol/L,则cY0.2mol/L0.125mol/L0.075mol/L,即反应开始后,体系
中Y和Z的浓度之比为0.075mol L:0.125mol L3:5,当反应能进行到底时,cYcZ0.5mol/L,
5 3
则cZ 0.5mol/L0.3125mol/L,cY 0.5mol/L0.1875mol/L,反应结束时N转化为
35 35
0.1875mol L
Y的特化率为 100%37.5%,C正确;
0.5mol L
44
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司D.30min时,vY:vZΔcY:ΔcZ3:5,即vYvZ、v v ,反应的活化能越高,反应速率
2 1
越慢,所以反应①的活化能小于反应②的活化能,D错误;
故选C。
反应速率与平衡图像突破
年份 试卷 考点
2023 江苏卷 转化率-温度图像
2023 海南卷 速率-时间图像
2023 湖南卷 转化率-温度图像
2023 重庆卷 物质体积分数-温度图像
2022 广东卷 浓度-时间图像
2022 湖南卷 压强-时间图像
2022 江苏卷 产率-温度图像
2022 河北卷 1
lnk~
T图像
2021 湖南卷 反应速率-时间图像
2021 河北卷 浓度-时间图像
2021 广东卷 浓度-时间图像
2021 湖北卷 pc—pOH图像
2021 辽宁卷 反应物浓度-催化剂浓度-图像
本专题主要从食物营养、合成药物、常见材料、自然资源利用、生产条件优化、废物回收利用和毒害物质
45
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司处理、环境保护等情境选材,考查学生解决问题的能力。会延续以往的命题风格,试题外观特征和考查要
求不会发生大的变化,与时代的变化和发展的关系会越来越紧密。关注生成生活、关注社会热点和焦点中
的化学知识,特别是绿色化学理念、碳中和碳达峰和常见的环境问题。
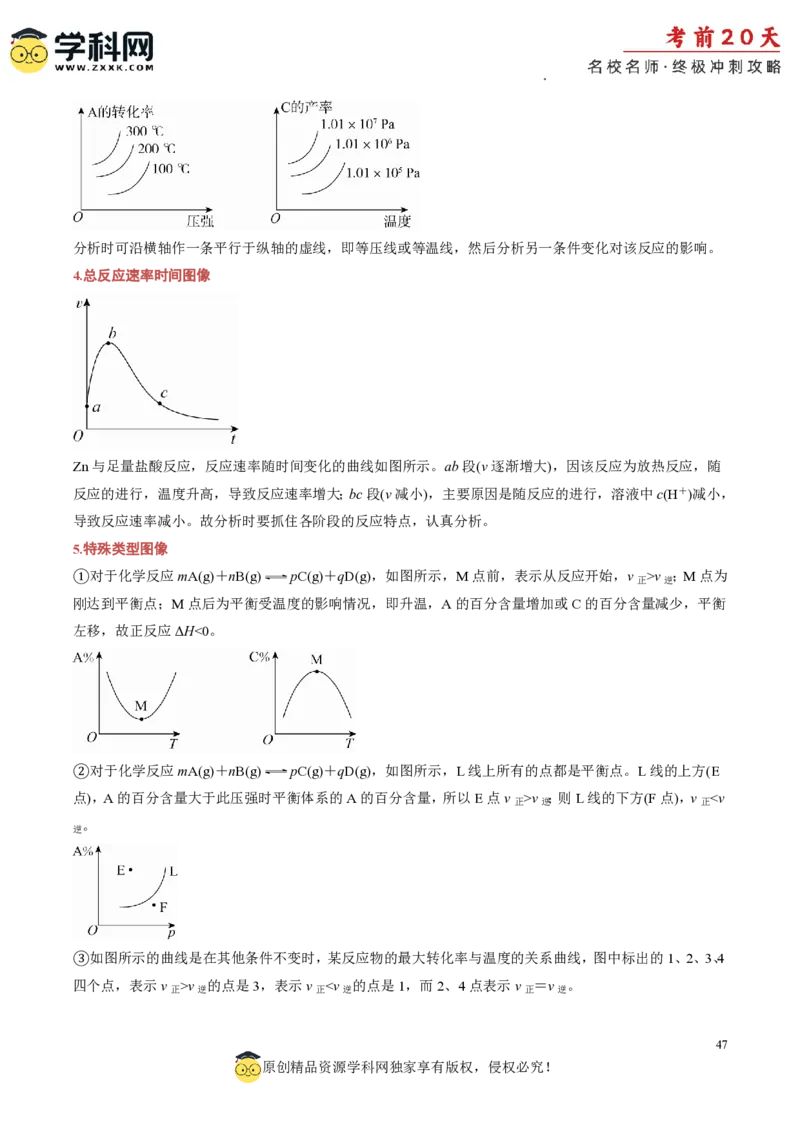
1.速率时间图像
反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0
①t 时增大反应物的浓度,正反应速率瞬间增大,然后逐渐减小,而逆反应速率逐渐增大;
1
②t 时升高温度,正反应和逆反应速率均增大,吸热反应的正反应速率增大得多;
2
③t 时减小压强,容器容积增大,浓度变小,正反应速率和逆反应速率均减小,正反应的反应速率减小得
3
多;
④t 时使用催化剂,正反应速率和逆反应速率均瞬间增大但仍相等。
4
2.转化率(或含量)时间图像
反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0
①图甲表示压强对反应物转化率的影响,对于气体反应物化学计量数之和大于气体生成物化学计量数之和
的反应,压强越大,反应物的转化率越大;
②图乙表示温度对反应物转化率的影响,对于吸热反应,温度越高,反应物的转化率越大;
③图丙表示催化剂对反应物转化率的影响,催化剂只能改变化学反应速率,不能改变反应物的转化率。
3.恒压(温)线
反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0
46
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司分析时可沿横轴作一条平行于纵轴的虚线,即等压线或等温线,然后分析另一条件变化对该反应的影响。
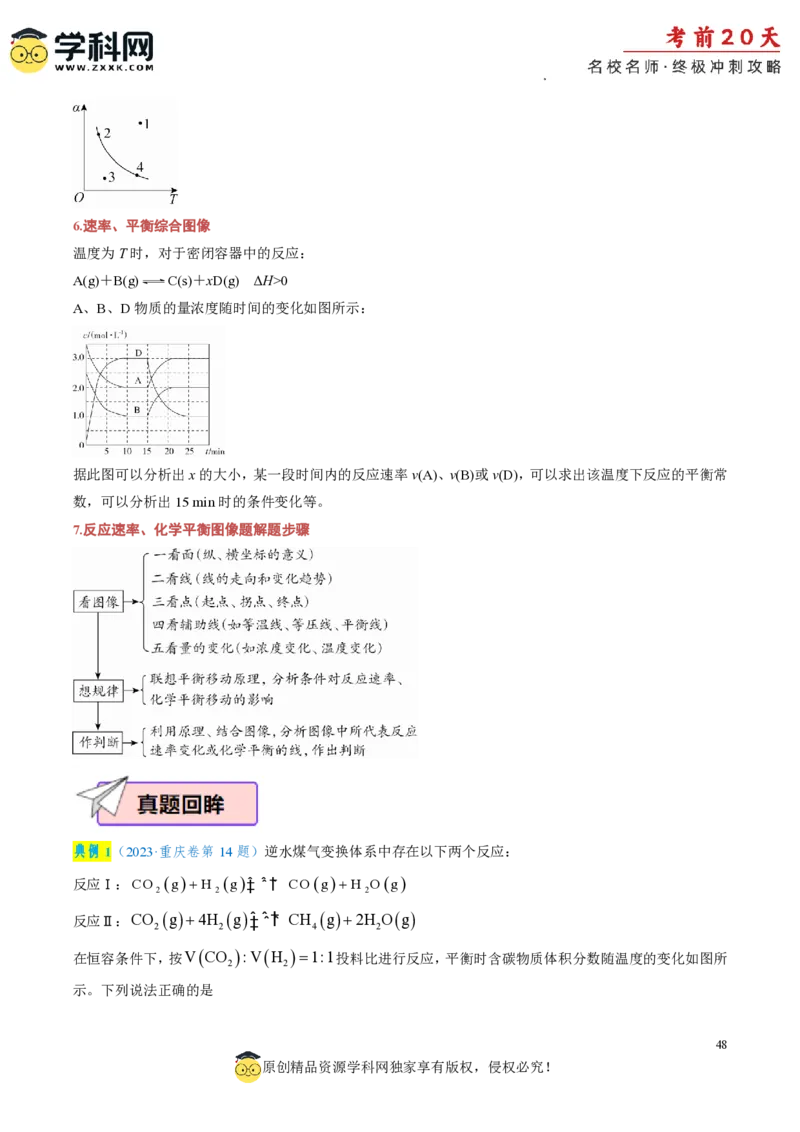
4.总反应速率时间图像
Zn与足量盐酸反应,反应速率随时间变化的曲线如图所示。ab段(v逐渐增大),因该反应为放热反应,随
反应的进行,温度升高,导致反应速率增大;bc段(v减小),主要原因是随反应的进行,溶液中c(H+)减小,
导致反应速率减小。故分析时要抓住各阶段的反应特点,认真分析。
5.特殊类型图像
①对于化学反应mA(g)+nB(g) pC(g)+qD(g),如图所示,M点前,表示从反应开始,v >v ;M点为
正 逆
刚达到平衡点;M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,平衡
左移,故正反应ΔH<0。
②对于化学反应mA(g)+nB(g) pC(g)+qD(g),如图所示,L线上所有的点都是平衡点。L线的上方(E
点),A的百分含量大于此压强时平衡体系的A的百分含量,所以E点v >v ;则L线的下方(F点),v v 的点是3,表示v 0
A、B、D物质的量浓度随时间的变化如图所示:
据此图可以分析出x的大小,某一段时间内的反应速率v(A)、v(B)或v(D),可以求出该温度下反应的平衡常
数,可以分析出15 min时的条件变化等。
7.反应速率、化学平衡图像题解题步骤
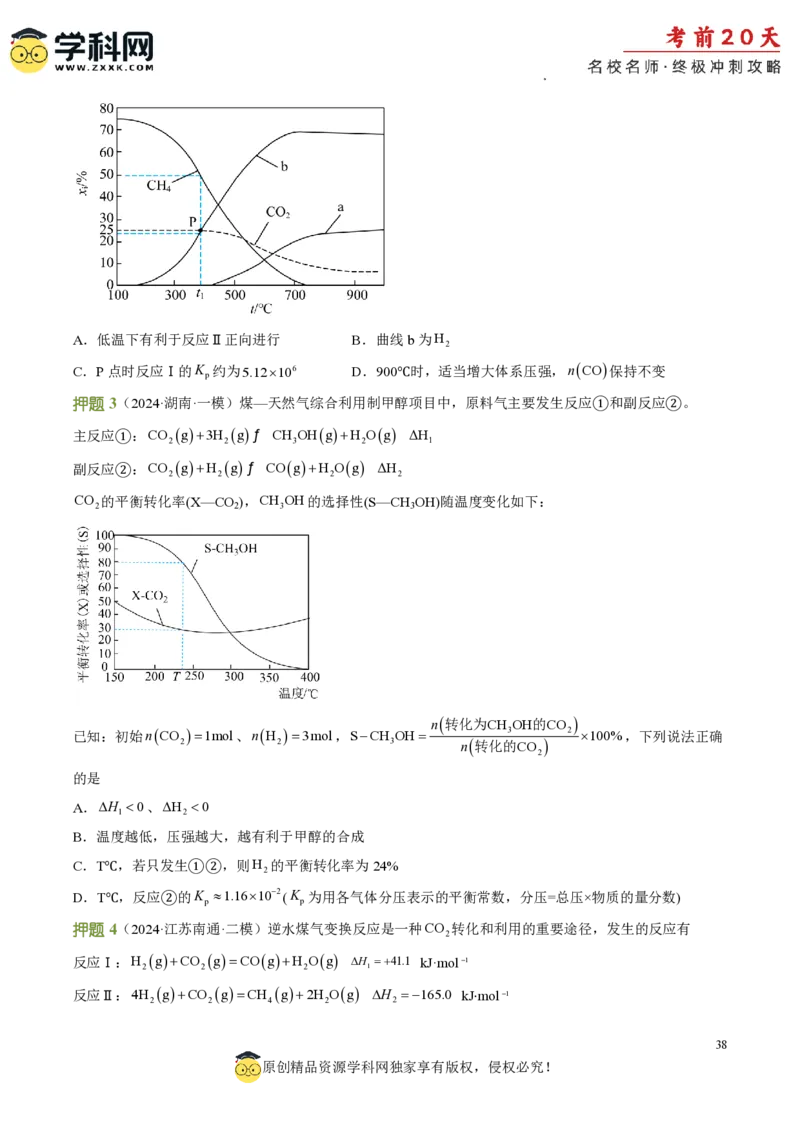
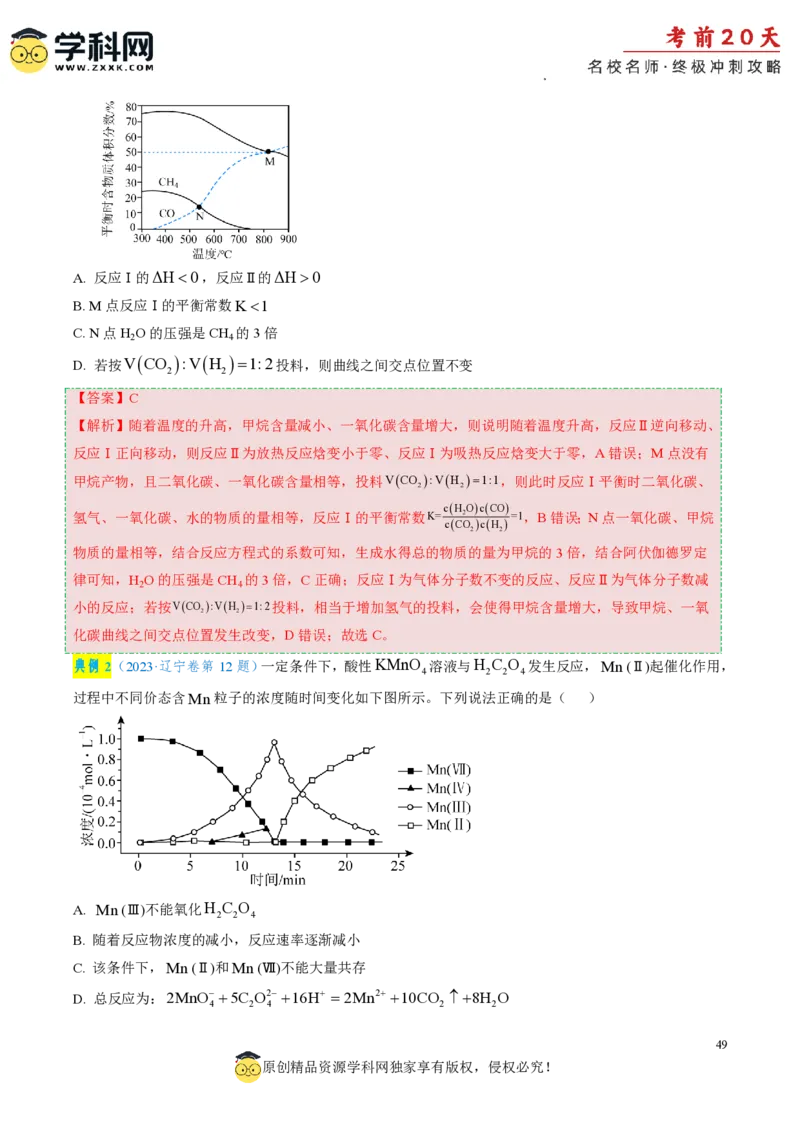
典例1(2023·重庆卷第14题)逆水煤气变换体系中存在以下两个反应:
反应Ⅰ:CO g H g‡ˆ ˆˆ†ˆ COg H Og
2 2 2
反应Ⅱ:CO g4H g ‡ ˆ ˆ ˆ † ˆ CH g2H Og
2 2 4 2
在恒容条件下,按VCO :VH 1:1投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所
2 2
示。下列说法正确的是
48
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A. 反应Ⅰ的ΔH0,反应Ⅱ的ΔH0
B. M点反应Ⅰ的平衡常数K1
C. N点H O的压强是CH 的3倍
2 4
D.
若按VCO :VH 1:2投料,则曲线之间交点位置不变
2 2
【答案】C
【解析】随着温度的升高,甲烷含量减小、一氧化碳含量增大,则说明随着温度升高,反应Ⅱ逆向移动、
反应Ⅰ正向移动,则反应Ⅱ为放热反应焓变小于零、反应Ⅰ为吸热反应焓变大于零,A错误;M点没有
甲烷产物,且二氧化碳、一氧化碳含量相等,投料VCO :VH 1:1,则此时反应Ⅰ平衡时二氧化碳、
2 2
cH OcCO
氢气、一氧化碳、水的物质的量相等,反应Ⅰ的平衡常数K= 2 =1,B错误;N点一氧化碳、甲烷
cCO cH
2 2
物质的量相等,结合反应方程式的系数可知,生成水得总的物质的量为甲烷的3倍,结合阿伏伽德罗定
律可知,H O的压强是CH 的3倍,C正确;反应Ⅰ为气体分子数不变的反应、反应Ⅱ为气体分子数减
2 4
小的反应;若按VCO :VH 1:2投料,相当于增加氢气的投料,会使得甲烷含量增大,导致甲烷、一氧
2 2
化碳曲线之间交点位置发生改变,D错误;故选C。
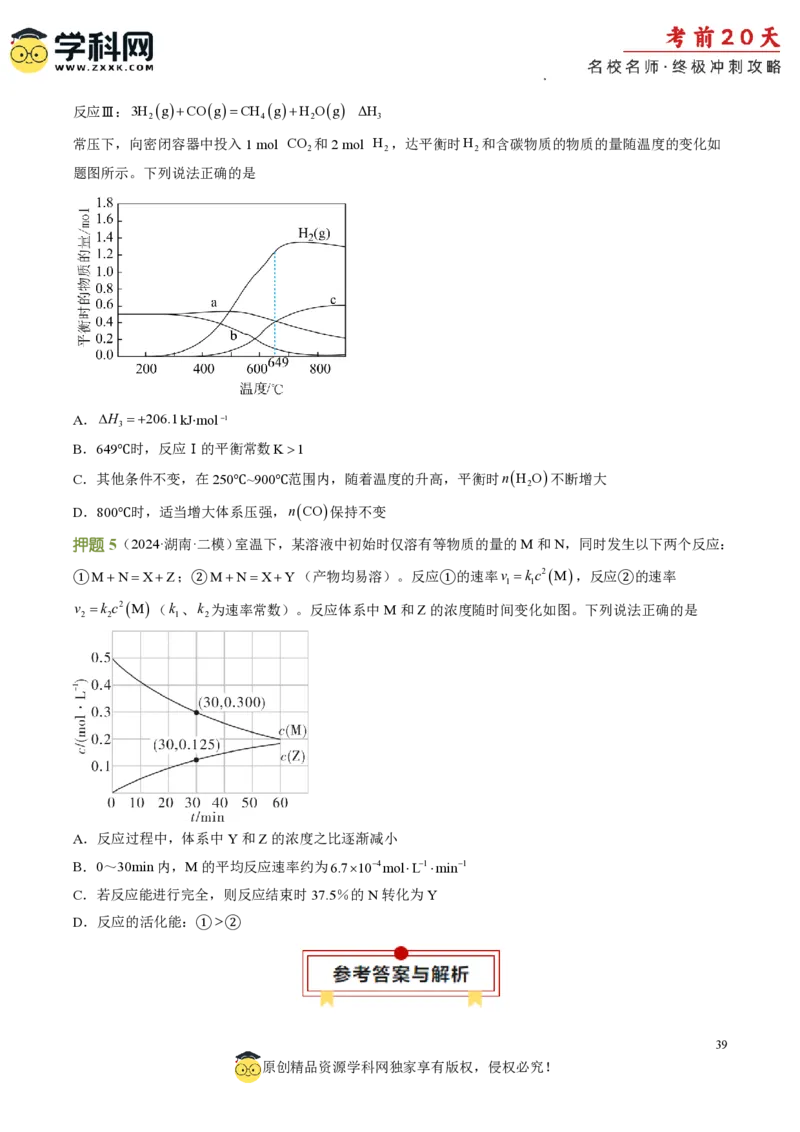
典例2(2023·辽宁卷第12题)一定条件下,酸性KMnO 溶液与H C O 发生反应,Mn(Ⅱ)起催化作用,
4 2 2 4
过程中不同价态含Mn粒子的浓度随时间变化如下图所示。下列说法正确的是( )
A. Mn(Ⅲ)不能氧化H C O
2 2 4
B. 随着反应物浓度的减小,反应速率逐渐减小
C. 该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
D. 总反应为:2MnO 5C O2 16H 2Mn2 10CO 8H O
4 2 4 2 2
49
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司【答案】C
【解析】开始一段时间(大约13min前)随着时间的推移Mn(VII)浓度减小直至为0,Mn(III)浓度增大直
至达到最大值,结合图像,此时间段主要生成Mn(III),同时先生成少量Mn(IV)后Mn(IV)被消耗;后来
(大约13min后)随着时间的推移Mn(III)浓度减少,Mn(II)的浓度增大;据此作答。由图像可知,随着
时间的推移Mn(III)的浓度先增大后减小,说明开始反应生成Mn(III),后Mn(III)被消耗生成Mn(II),Mn(III)
能氧化H C O ,A项错误;随着反应物浓度的减小,到大约13min时开始生成Mn(II),Mn(II)对反应起
2 2 4
催化作用,13min后反应速率会增大,B项错误;由图像可知,Mn(VII)的浓度为0后才开始生成Mn(II),
该条件下Mn(II)和Mn(VII)不能大量共存,C项正确;H C O 为弱酸,在离子方程式中应以化学式保留,
2 2 4
总反应为2MnO -+5H C O +6H+=2Mn2++10CO ↑+8H O,D项错误;故选C。
4 2 2 4 2 2
典例3(2022·湖南卷)向体积均为1L的两恒容容器中分别充入2mol X和1mol Y发生反应:
2X(g)+Y(g)ƒ Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图
所示。下列说法正确的是
A. ΔH>0 B. 气体的总物质的量:n 12 D. 反应速率:v ν ,平衡常数增大
正 逆
B.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低
C.温度不变,若恒压下向平衡体系中充入惰性气体,平衡不移动
D.若投料比n(H ):n(CO )=3:1,则图中 M点乙烯的体积分数为7.7%
2 2
押题1(2024·湖南益阳·三模)工业上常用CO 和H 为原料合成甲醇CH OH,过程中发生如下反应:
2 2 3
CO (g)3H (g)ƒ CH OH(g)H O(g) H51kJ/mol。在T、T 温度下,向2L刚性容器中充入1molCO
2 2 3 2 1 2 2
和一定物质的量的H ,随着充入H 的物质的量的不同,平衡时容器中CH OH的体积分数变化曲线如图所
2 2 3
示。下列说法错误的是
A.a3 B.T T
1 2
C.平衡常数K(M)=K(N) D.该反应在高温高压条件下自发进行
押题2(2024·湖南长沙·一模)二氧化碳催化加氢制甲醇,有利于减少温室气体一氧化碳。其原理为
CO g3H gƒ CH OHgH Og。在起始物n(H )/n(CO )=3时,在不同条件下达到平衡,设体系
2 2 3 2 2 2
中甲醇的物质的量分数为xCH OH,在T=250℃下的xCH OH~ p、在p5105Pa下的xCH OH~T
3 3 3
曲线如图所示。下列说法正确的是
55
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A.图中对应等压过程的曲线是a
B.该反应在高温下能自发进行
C.当xCH OH0.10时,CO 的平衡转化率a33.3%
3 2
D.温度压强一定时,增大起始物nH /nCO ,可提高平衡时的xCH OH
2 2 3
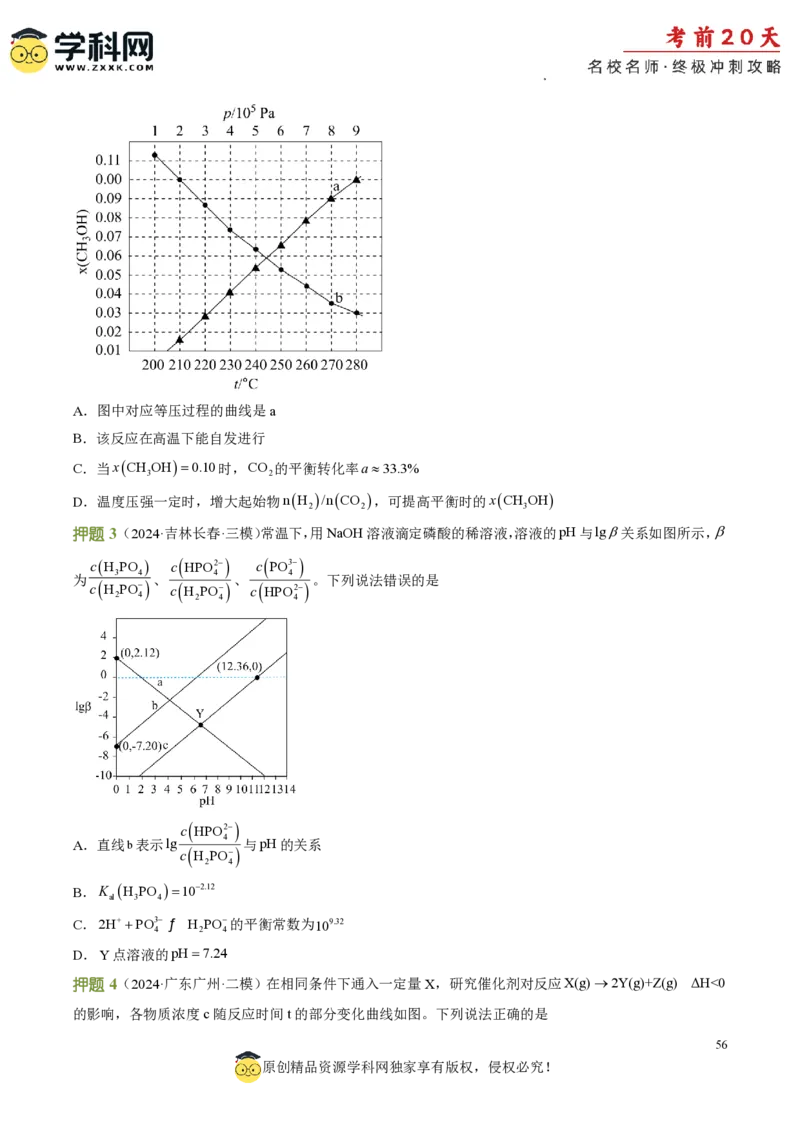
押题3(2024·吉林长春·三模)常温下,用NaOH溶液滴定磷酸的稀溶液,溶液的pH与lg关系如图所示,
cH PO c HPO2 c PO3
3 4 4 4
为 、 、 。下列说法错误的是
c H PO c H PO c HPO2
2 4 2 4 4
c
HPO2
A.直线b表示lg 4 与pH的关系
c
H
PO
2 4
B.K H PO 102.12
al 3 4
C.2H PO3 ƒ H PO的平衡常数为109.32
4 2 4
D.Y点溶液的pH7.24
押题4(2024·广东广州·二模)在相同条件下通入一定量X,研究催化剂对反应X(g)2Y(g)+Z(g) ΔH<0
的影响,各物质浓度c随反应时间t的部分变化曲线如图。下列说法正确的是
56
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.使用催化剂Ⅰ,2 min时,v(X)=1.0 molL-1min-1
D.c曲线可表示使用催化剂I时Z的浓度随t的变化
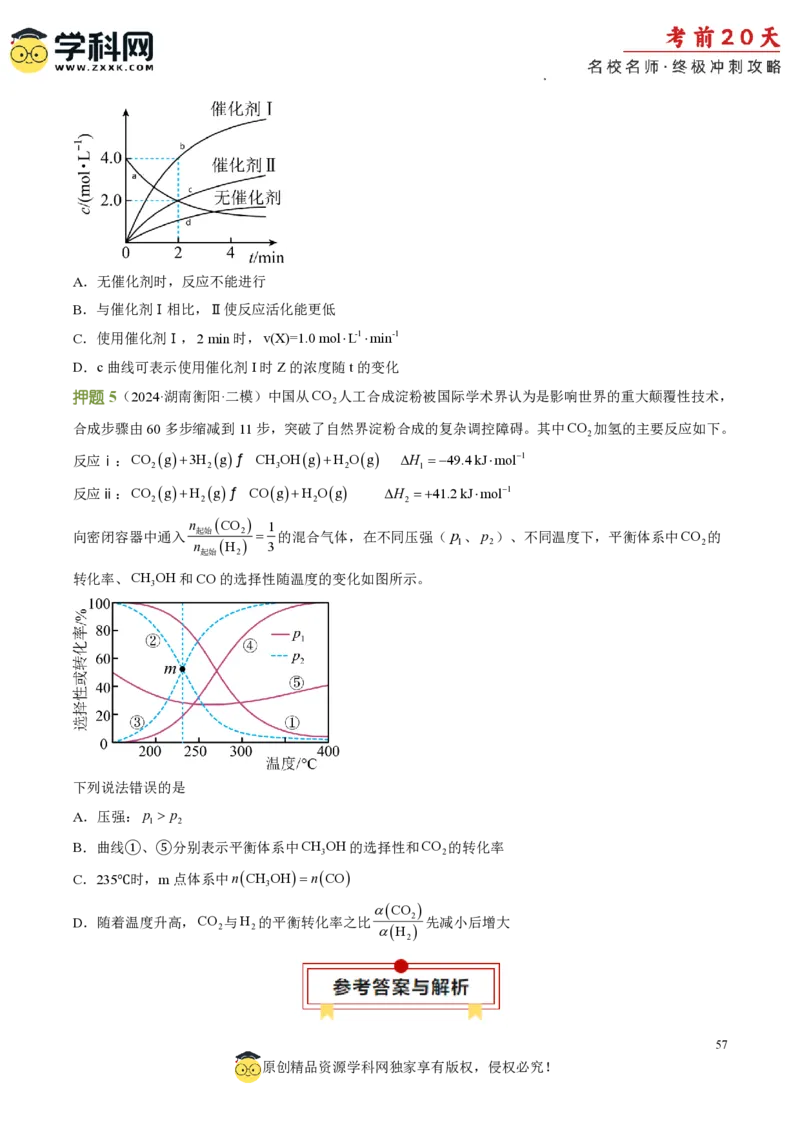
押题5(2024·湖南衡阳·二模)中国从CO 人工合成淀粉被国际学术界认为是影响世界的重大颠覆性技术,
2
合成步骤由60多步缩减到11步,突破了自然界淀粉合成的复杂调控障碍。其中CO 加氢的主要反应如下。
2
反应ⅰ:CO g3H gƒ CH OHgH Og H 49.4kJmol1
2 2 3 2 1
反应ⅱ:CO gH gƒ COgH Og H 41.2kJmol1
2 2 2 2
n CO 1
向密闭容器中通入 起始 2 的混合气体,在不同压强(p 、p )、不同温度下,平衡体系中CO 的
n H 3 1 2 2
起始 2
转化率、CH OH和CO的选择性随温度的变化如图所示。
3
下列说法错误的是
A.压强:p p
1 2
B.曲线①、⑤分别表示平衡体系中CH OH的选择性和CO 的转化率
3 2
C.235℃时,m点体系中nCH OHnCO
3
CO
D.随着温度升高,CO 与H 的平衡转化率之比 2 先减小后增大
2 2 H
2
57
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司名校预测
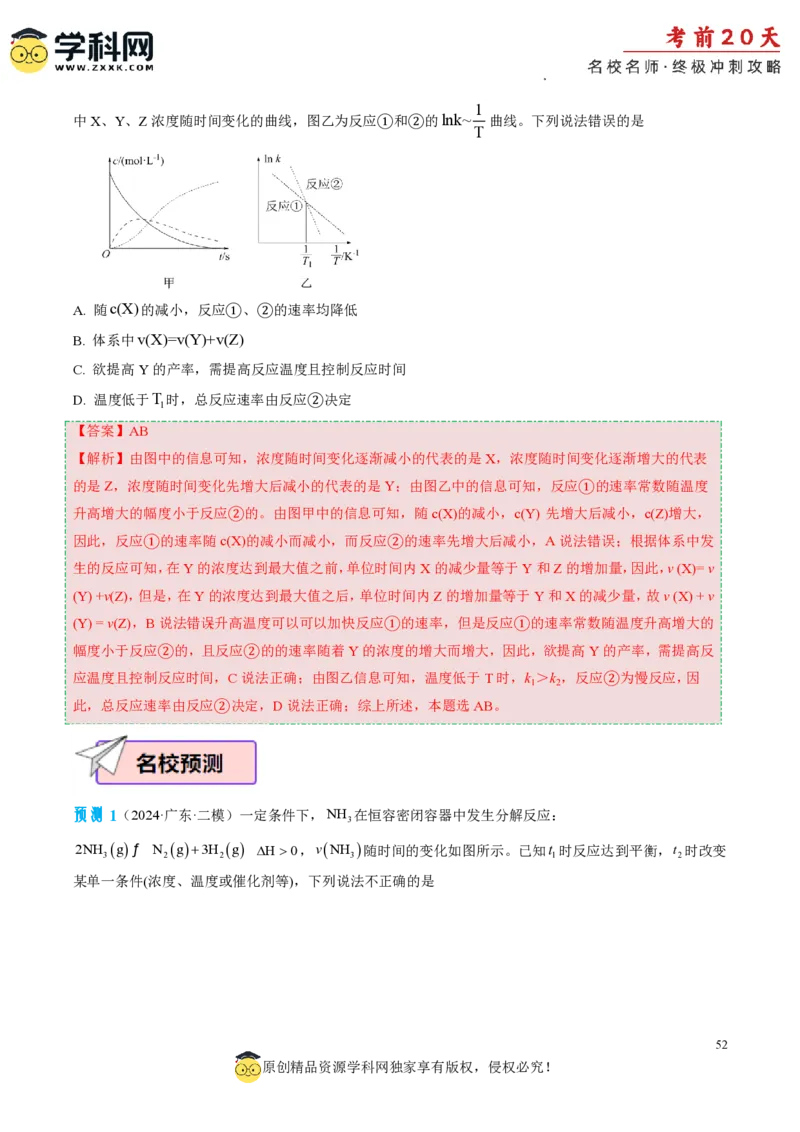
预测1
【答案】D
【解析】A.由图可知,0到t 的过程为氨气分解形成平衡的过程,反应中氢气的浓度不断增大,故A正确;
1
B.由图可知,t 时反应达到平衡,正逆反应速率相等,则t 到t 的过程中,反应速率的关系为
1 1 2
2v H =3v NH ,故B正确;
正 2 逆 3
C.由图可知,t 条件改变的瞬间,逆反应速率增大,可能是通入氮气,增大了生成物氮气的浓度,故C正
2
确;
D.由图可知,t 条件改变的瞬间,逆反应速率增大,随后减小,说明平衡向逆反应方向移动,该反应是吸
2
热反应,若改变条件为升高温度,平衡向正反应方向移动,与图示不符合,所以改变条件不可能是升高温
度,温度不变,平衡常数不变,则反应的平衡常数K 等于K ,故D错误;
Ⅰ Ⅱ
故选D。
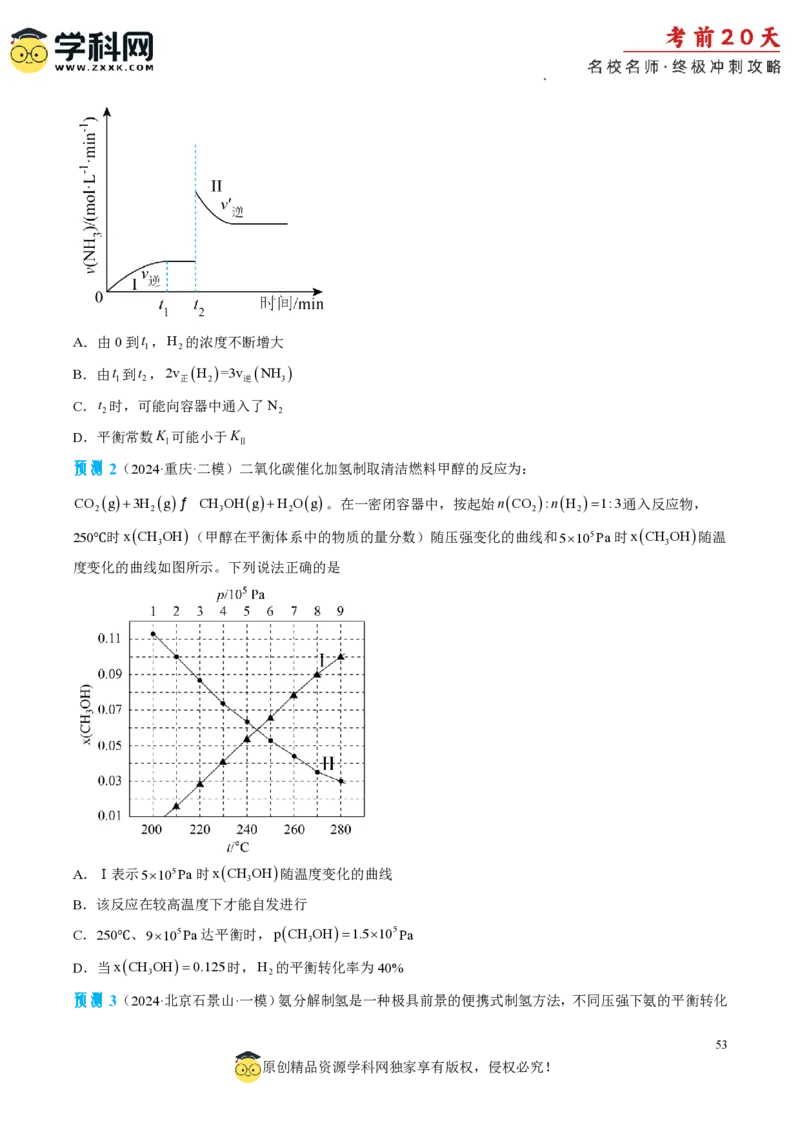
预测2
【答案】D
【分析】由CO g3H gƒ CH OHgH Og可知,该反应是气体分子数减少的反应,恒温加压平
2 2 3 2
衡右移,甲醇在平衡体系中的物质的量分数增大,所以曲线Ⅰ表示甲醇的物质的量分数随压强的变化曲线,
曲线Ⅱ表示甲醇的物质的量分数随温度的变化曲线。
【解析】A.该反应是气体分子数减少的反应,甲醇在平衡体系中的物质的量分数随压强的增大而增大,则
曲线Ⅰ表示甲醇的物质的量分数随压强的变化曲线,曲线Ⅱ表示甲醇的物质的量分数随温度的变化曲线,
故A错误;
B.曲线Ⅱ表示甲醇的物质的量分数随温度的变化曲线,图像显示温度升高xCH OH变小,说明该反应的
3
正反应是放热反应,H0,又该反应是气体分子数减少的反应,S 0,根据G=H-TS可知,该反应
在较低的温度下能自发进行,故B错误;
C.读图可知250℃、9105Pa时,xCH OH0.1,则pCH OH0.19105Pa9104Pa,故C错误;
3 3
D.xCH OH0.125,设起始通入a molCO 和3a molH ,三段式表示
3 2 2
CO g +3H g ƒ CH OHg +H Og
2 2 3 2
起始mol a 3a 0 0
,n(总)=a(1-x)+a(3-3x)+ax+ax=4a-2ax,则
转化mol ax 3ax ax ax
平衡mol a1-x a3-3x ax ax
ax x 30.4a
= =0.125,解得x0.4,H 的平衡转化率为 100%40%,故D正确;
4a-2ax 4-2x 2 3a
故答案为:D。
预测3
58
原创精品资源学科网独家享有版权,侵权必究!
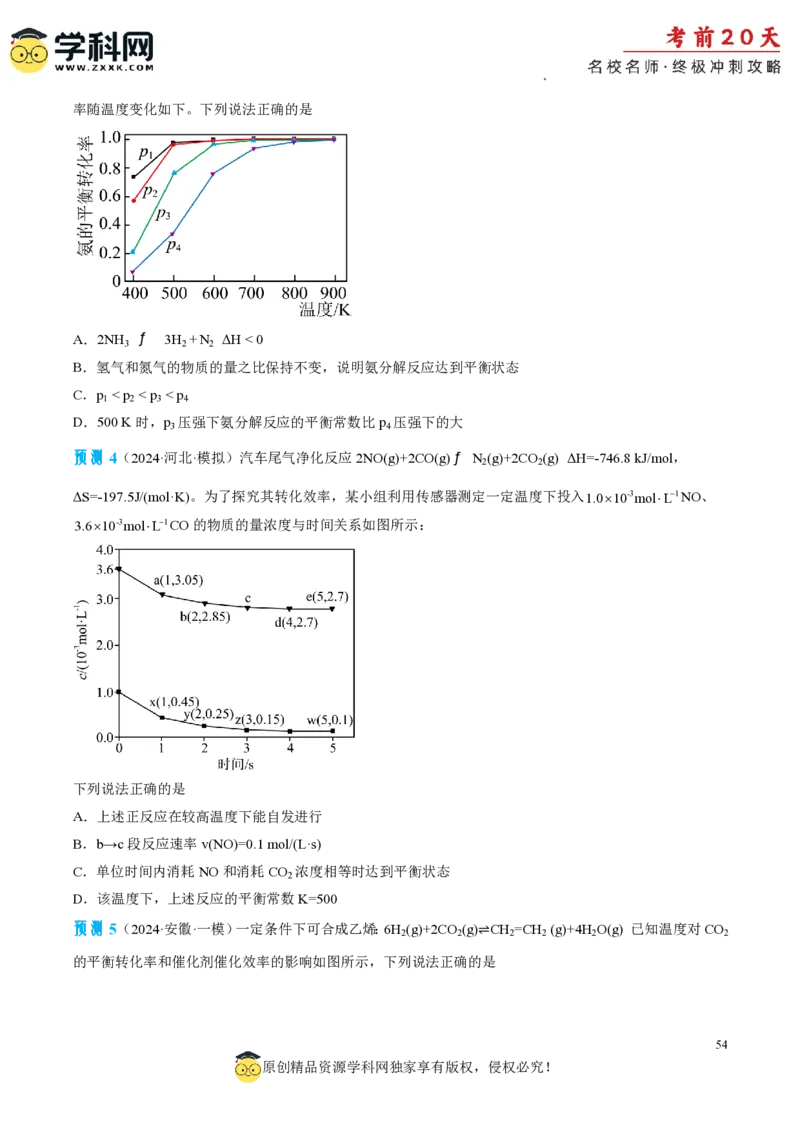
学科网(北京)股份有限公司【答案】C
【解析】A.温度升高,氨的平衡转化率上升,2NH ƒ 3H +N 平衡正向移动,ΔH > 0,故A错误;
3 2 2
B.氢气和氮气的物质的量之比始终为3:1,不能说明反应到达平衡状态,故B错误;
C.2NH ƒ 3H +N 为气体分子数增大的反应,增大压强,平衡逆向移动,氨的平衡转化率下降,因此p
3 2 2 1
< p < p < p ,故C正确;
2 3 4
D.平衡常数只与温度有关,500 K时无论压强是多少,K为定值,故D错误;
故选C。
预测4
【答案】C
【解析】A.根据反应可知ΔH<0,ΔS<0,当较低温度时满足ΔG=ΔH-TΔS<0,反应能自发进行,故A错误;
B.由曲线与纵坐标交点可知,曲线abcde表示CO,曲线xyzw表示NO,则b→c段反应速率
0.25103mol/L0.15103mol/L
vNO 0.1103mol/Ls,故B错误;
1s
C.当单位时间内消耗NO和消耗CO 浓度相等时,说明正逆反应速率相等,反应达到平衡状态,故C正
2
确;
D.曲线abcde表示CO,曲线xyzw表示NO,则该温度下,达到平衡时,c(CO)2.7103molL-1,
1 1
c(NO)0.1103molL-1,c(N ) cNO 1.01030.1103 molL-1 0.45103molL-1,
2 2 2
c2(CO )c(N )
c(CO )2c(N )=0.9103molL-1,上述反应的平衡常数K= 2 2 =5000,故D错误;
2 2 c2(NO)c2(CO)
故答案选C。
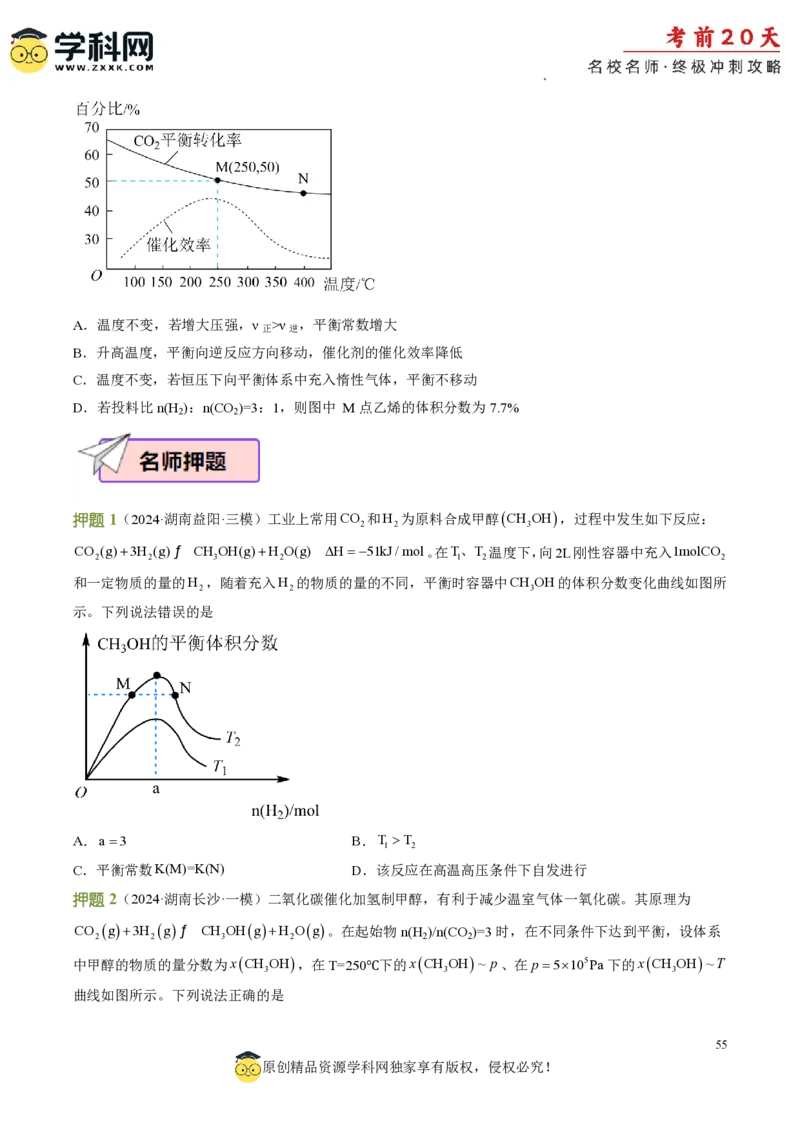
预测5
【答案】D
【解析】A.平衡常数只与温度有关,温度不变,若增大压强,ν >ν ,平衡常数不变,故A错误;
正 逆
B.升高温度,CO 的平衡转化率降低,可知平衡向逆反应方向移动;根据图示,催化剂的催化效率先升高
2
后降低,故B错误;
C.温度不变,若恒压下向平衡体系中充入惰性气体,体积增大,相当于减压,平衡逆向移动,故C错误;
D.若投料比n(H ):n(CO )=3:1,图中 M点CO 的平衡转化率为50%
2 2 2
6H g 2CO g ƒ CH =CH g 4H Og
2 2 2 2 2
初始mol 3a a 0 0
转化mol 1.5a 0.5a 0.25a a
平衡mol 1.5a 0.5a 0.25a a
0.25a
乙烯的体积分数为 100%7.7%,故D正确;
3.25a
选D。
59
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司名师押题
押题1
【答案】D
【解析】A.投料比符合方程式中的气体系数比时,达到平衡时产物的体积分数最大,所以a=3,A正确;
B.由题可知该反应是放热反应,升高温度高反应会逆向移动,所以T T ,B正确;
1 2
C.平衡常数受温度影响,M、N点温度相同,平衡常数相等,C正确;
D.该反应H<0,S<0,所以该反应在低温条件下自发进行,与压强无关,D错误;
故选D。
押题2
【答案】C
【解析】A.总反应为气体体积减小反应,当其他条件不变,增大压强时,平衡正向移动,xCH OH增大,
3
则a为250℃下的xCH OH~ p曲线,b为p5105Pa下的xCH OH~T 曲线,b线为等压过程的曲线,
3 3
故A错误;
B.由A中分析可知,b为p5105Pa下的xCH OH~T 曲线,随温度升高,xCH OH减小,可知升温
3 3
使平衡逆向移动,正向为放热反应,该反应在低温下能自发进行,故B错误;
C.起始物n(H )/n(CO )=3,设n(H )=3mol,n(CO )=1mol,设二氧化碳的变化量为x,根据已知条件列三段
2 2 2 2
式:
CO g + 3H g ƒ CH OHg + H Og
2 2 3 2
起始/mol 1 3 0 0
转化/mol x 3x x x
某时刻/mol 1-x 3-3x x x
x 1
xCH OH0.10时,即 100%0.10,解得:x= ,CO 的平衡转化率a33.3%,故C正
3 x+x+1-x+3-3x 3 2
确;
D.温度压强一定时,增大起始物nH /nCO ,等同于nCO 一定时,增大氢气的浓度,平衡时的
2 2 2
xCH OH减小,故D错误;
3
故选:C。
押题3
【答案】C
c(H+)c H PO c H PO
【分析】电离常数的表达式K H PO 2 4 ,随着pH增大,c(H+)减小, 2 4 减小,
al 3 4 cH PO cH PO
3 4 3 4
60
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司cH PO cH PO c(H+)c HPO2
c H
3
PO
4
增大,图像中曲线a表示lg
c H
3
PO
4
与pH的关系;K
a2
H
3
PO
4
c H PO
4 ,
2 4 2 4 2 4
c(H+)c PO3 c HPO2 c PO3
K H PO 4 ,在pH相等时,K H PO K H PO ,即lg 4 >lg 4 ,
a3 3 4 c HPO2 a2 3 4 a3 3 4 c H PO c HPO2
4 2 4 4
c
HPO2
c
PO3
故曲线b表示lg 4 与pH的关系,曲线c表示lg 4 与pH的关系;
c
H
PO
c
HPO2
2 4 4
c
HPO2
【解析】A.由上述分析可知,直线b表示lg 4 与pH的关系,故A正确;
c
H
PO
2 4
c(H+)c H PO
B.K H PO 2 4 ,在图像中找(0,2.12)的点,此时c(H+)=1mol/L,故
al 3 4 cH PO
3 4
c(H+)c H PO c H PO
K H PO 2 4 = 2 4 =102.12,故B正确;
al 3 4 cH PO cH PO
3 4 3 4
c(H+)c HPO2
C.在b线上找(0,-7.20)的点,K H PO 4 =107.20,根据c线上(0,12.36),
a2 3 4 c H PO
2 4
c(H+)c PO3 c H PO
K H PO 4 =1012.36,2H PO3 ƒ H PO的平衡常数K= 2 4 ,
a3 3 4 c HPO2 4 2 4 c2(H+)c PO3
4 4
c2(H+)c PO3 1 1
K H PO K H PO = 4 ,则K= = 1019.56,故C
a2 3 4 a3 3 4 c H PO K H PO K H PO 107.201012.36
2 4 a2 3 4 a3 3 4
错误;
c PO3 cH PO c PO3 K cH PO c(H+) K c(H+)
D.Y点 c HPO 4 2 = c H 3 PO 4 , c HPO 4 2 = c(H a3 +) , c H 3 PO 4 = K ,即 c(H a3 +) = K ,
4 2 4 4 2 4 a1 a1
c(H+)= K K = 10-12.3610-2.12 =10-7.24,故pH=7.24,故D正确。
a3 a1
答案选C。
押题4
【答案】D
【分析】由图可知,X为反应物,随着反应进行X的量减小,在0~2min 内X的浓度变化了2.0mol/L,结
合化学方程式可知,YZ的浓度变化分别为4.0mol/L、2.0mol/L,则b为为Y浓度变化曲线、c为Z浓度变
化曲线;
【解析】A.催化剂改变反应速率,但是不影响反应进行的程度,A错误;
B.由图可知,催化剂Ⅰ比催化剂Ⅱ催化效果好,说明催化剂Ⅰ使反应活化能更低,反应更快,则Ⅱ使反应
活化能更高,B错误;
61
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司C.由分析可知,使用催化剂Ⅰ,0~2min 内X的平均反应速率为:
2
v(X)= molL-1min-1=1.0 molL-1min-1,不是2 min时的反应速率,C错误;
2
D.由分析可知,c曲线可表示使用催化剂Ⅰ时Z的浓度随t的变化,D正确;
故选D。
押题5
【答案】D
【分析】反应I为放热反应,升高温度,平衡向逆反应方向移动,甲醇的选择性减小,反应Ⅱ为吸热反应,
升高温度,平衡向正反应方向移动,一氧化碳的选择性增大,则曲线①、②表示甲醇的选择性,曲线③、
④表示一氧化碳的选择性,曲线⑤表示二氧化碳的转化率。
【解析】A.由分析可知,曲线①、②表示甲醇的选择性,反应Ⅰ为气体体积减小的反应,增大压强,平
衡向正反应方向移动,甲醇的选择性增大,由图可知,p 条件下甲醇的选择性大于p 条件下甲醇的选择性,
1 2
则压强p 大于p ,故A正确;
1 2
B.由分析知,曲线①、⑤分别表示平衡体系中CH OH的选择性和CO 的转化率,故B正确;
3 2
C.235℃时,甲醇和一氧化碳选择性相同,两个反应分别生成甲醇和一氧化碳的量相同,故m点体系中
n(CH OH)=n(CO),C正确;
3
D.随着温度升高,反应i放热会逆向移动,反应ii吸热会正向移动,反应ii中二氧化碳和氢气反应比是
1:1,氢气消耗少于反应i,故反应ii进行程度越大,氢气转化率越低且二氧化碳转化率越高,故CO 与H
2 2
的平衡转化率之比增大,故D错误;
故选D。
化学反应原理综合
年份 试卷 考点
62
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司2023 广东卷 电子轨道表示式、离子方程式、消耗速率、平衡转化率
2023 浙江卷 平衡移动原理、影响平衡移动的因素、盖斯定律、转化率
2023 湖北卷 反应历程、基元反应、平衡常数、反应速率和化学平衡影响因素
2023 湖南卷 盖斯定律、平衡常数、催化剂与反应速率、能量转化
2023 浙江卷 盖斯定律、平衡常数、温度对反应速率和化学平衡影响因素
2023 海南卷 转化率、吸热反应、平衡常数计算
2023 重庆卷 热化学方程式、平衡常数、反应速率、晶胞的计算
2022 海南卷 燃烧热、转化率、反应速率计算及其影响因素
2022 湖北卷 盖斯定律、平衡状态、反应速率和化学平衡影响因素
2022 湖南卷 吸热反应、平衡常数、离子方程式、阴极反应式
2022 辽宁卷 自发反应、温度对反应速率和化学平衡的影响、电子排布式
2022 山东卷 焓变的计算、平衡常数、产率 、压强对化学平衡的影响
2022 河北卷 热化学方程式、平衡常数、电极反应式
2021 广东卷 反应历程、盖斯定律、吸热反应、平衡常数
2021 河北卷 热化学方程式、电极反应式、分压的相关计算
2021 湖北卷 平衡常数、反应速率计算、浓度对化学平衡的影响、
2021 湖南卷 反应热的计算、反应速率的计算、平衡常数、电极反应式
2021 辽宁卷 盖斯定律、平衡常数、化学平衡的影响因素、
2021 浙江卷 平衡常数、电解饱和食盐水、浓度与反应速率、
化学反应原理综合题是高考必考题型,题目通常结合图像、表格、数据等信息,围绕一个主题,以“拼盘”的
形式呈现,每个小题有一定的相对独立性,主要考查盖斯定律的应用、化学反应速率和化学平衡分析、化
学平衡常数的表达与计算、反应条件的分析选择、生产生活中的实际应用、电化学等命题点,在近几年考
题中,主要以“多因素影响”考查出现,要求考生具有较强的综合分析判断能力,信息量大,难度较高。
一、盖斯定律的应用
63
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司二、反应速率与速率常数
1.含义
速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相同的浓度条件下,可用速率
常数大小来比较化学反应的反应速率。
化学反应速率与反应物浓度(或浓度的次方)成正比,而速率常数是其比例常数,在恒温条件下,速率常数不
随反应物浓度的变化而改变。因此,可以应用速率方程求出该温度下任意浓度时的反应速率。
2.速率方程
一定温度下,化学反应速率与反应物浓度以其化学计量数为指数的幂的乘积成正比。
对于反应:aA(g)+bB(g) gG(g)+hH(g),则v =k ·ca(A)·cb(B)(其中k 为正反应的速率常数),v =k
正 正 正 逆
·cg(G)·ch(H)(其中k 为逆反应的速率常数)。
逆 逆
3.速率常数与化学平衡常数之间的关系
一定温度下,可逆反应:aA(g)+bB(g) gG(g)+hH(g),达到平衡状态时,v =k ·ca(A)·cb(B),v =k
正 正 逆
k正 cg(G)·ch(H)
·cg(G)·ch(H),因平衡时v =v ,则k ·ca(A)·cb(B)=k ·cg(G)·ch(H), = =K。
逆 正 逆 正 逆
k逆 ca(A)·cb(B)
三、转化率、产率等计算与变化判断
1.三段式突破平衡的有关计算
mA(g) + nB(g) pC(g) + qD(g)
起始 /
a b 0 0
mol· L-1
变化 /
mx nx px qx
mol· L-1
平衡 /
a-mx b-nx px qx
mol· L-1
mx
(1)v = 。
A
Δt
mx
(2)转化率α = ×100%。
A
a
64
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(px)p·(qx)q
(3)K= 。
(a-mx)m·(b-nx)n
(4)生成物的产率:实际产量占理论产量的百分数。一般来说,转化率越高,原料利用率越高,产率越高。
产物实际质量
产率= ×100%。
理论产量
平衡量
(5)混合物中某组分的百分含量= ×100%。
平衡总量
2.平衡移动与转化率的关系
在一恒容密闭容器中通入a mol A、b mol B发生反应aA(g)+bB(g) cC(g),达到平衡后,改变下列条件,
分析转化率的变化情况:
(1)再通入b mol B,α(A)增大,α(B)减小。
(2)再通入a mol A、b mol B,若a+b>c,α(A)增大、α(B)增大;若a+b=c,α(A)不变、α(B)不变;若a+
bα >α
3 III II I
C.三组实验中,反应速率都随反应进程一直减小
D.体系由橙红色转变为淡蓝色所需时间:t >t >t
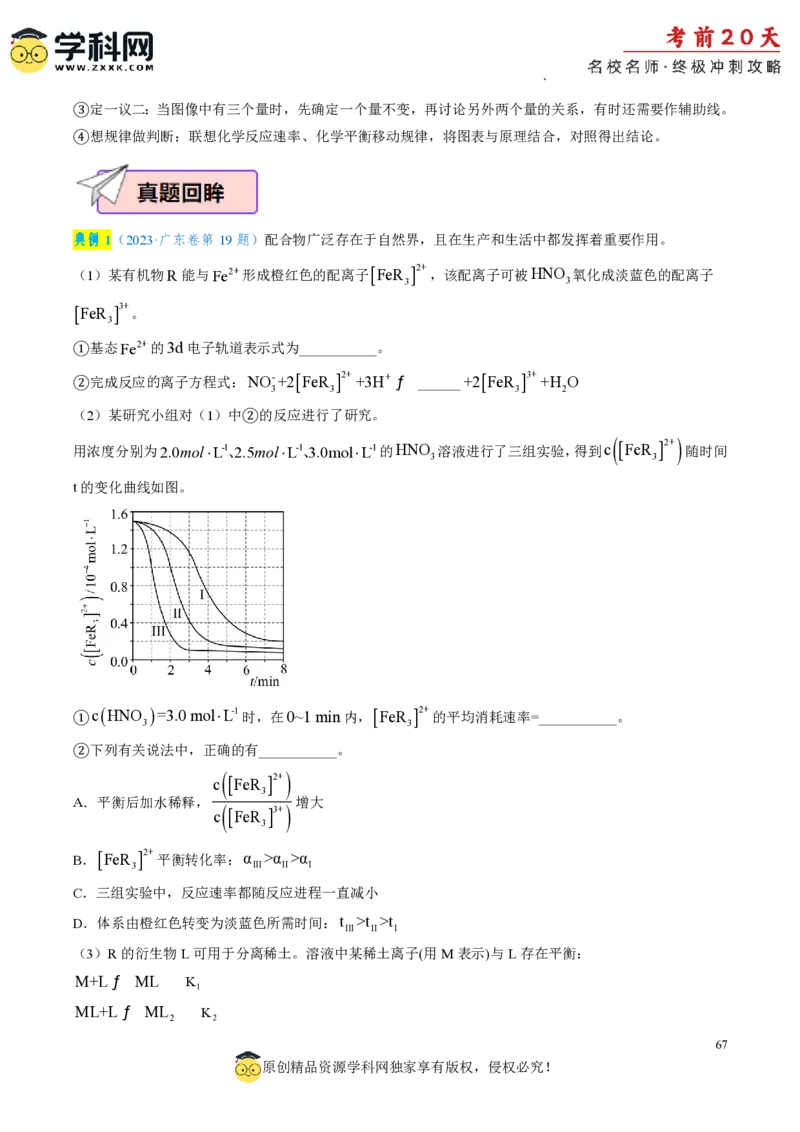
III II I
(3)R的衍生物L可用于分离稀土。溶液中某稀土离子(用M表示)与L存在平衡:
M+Lƒ ML K
1
ML+Lƒ ML K
2 2
67
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司研究组配制了L起始浓度c ( L)=0.02 molL-1、M与L起始浓度比c (M)/c (L)不同的系列溶液,反应平
0 0 0
衡后测定其核磁共振氢谱。配体L上的某个特征H在三个物种L、ML、ML 中的化学位移不同,该特征
2
H对应吸收峰的相对峰面积S(体系中所有特征H的总峰面积计为1)如下表。
c (M)/c (L) S(L) S(ML) SML
0 0 2
0 1.00 0 0
a x <0.01 0.64
b <0.01 0.40 0.60
【注】核磁共振氢谱中相对峰面积S之比等于吸收峰对应H的原子数目之比;“<0.01”表示未检测到。
①c (M)/c (L)=a时,x= ___________。
0 0
②c (M)/c (L)=b时,平衡浓度比c ML :c (ML)=___________。
0 0 平 2 平
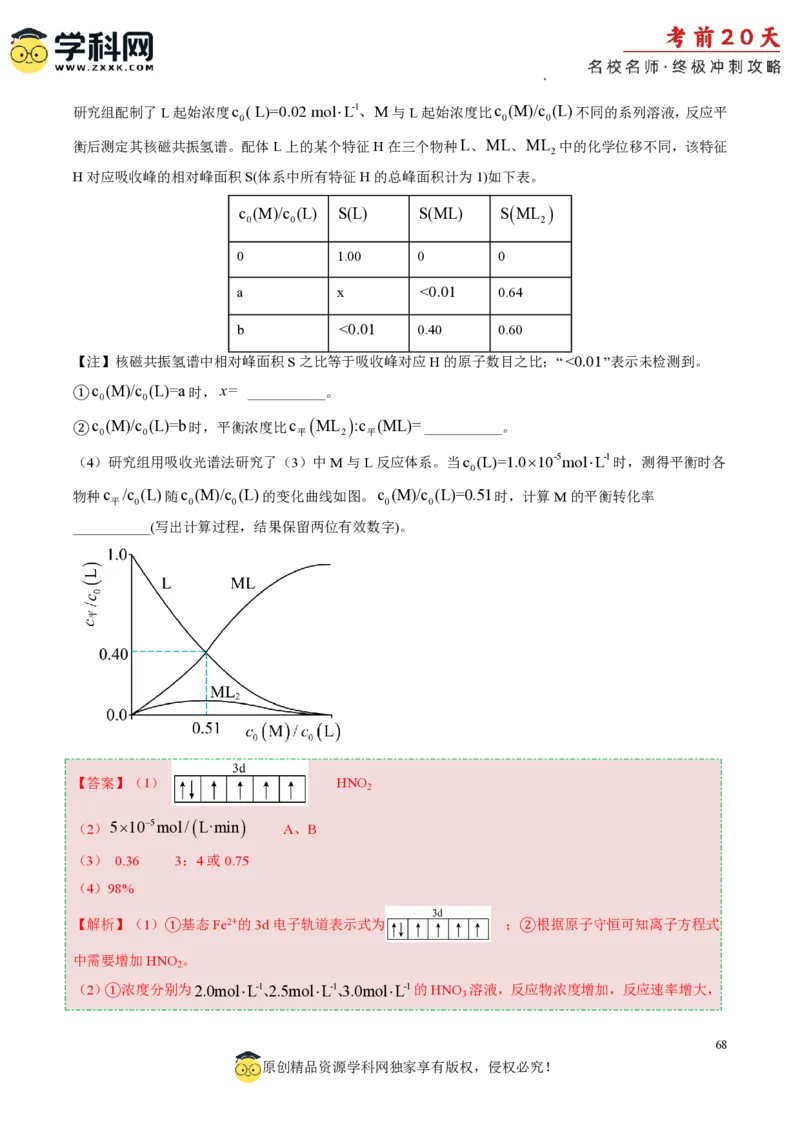
(4)研究组用吸收光谱法研究了(3)中M与L反应体系。当c (L)=1.010-5molL-1时,测得平衡时各
0
物种c /c (L)随c (M)/c (L)的变化曲线如图。c (M)/c (L)=0.51时,计算M的平衡转化率
平 0 0 0 0 0
___________(写出计算过程,结果保留两位有效数字)。
【答案】(1) HNO
2
(2)5105mol/L·min
A、B
(3) 0.36 3:4或0.75
(4)98%
【解析】(1)①基态Fe2+的3d电子轨道表示式为 ;②根据原子守恒可知离子方程式
中需要增加HNO 。
2
(2)①浓度分别为2.0molL-1、2.5molL-1、3.0molL-1的HNO 溶液,反应物浓度增加,反应速率增大,
3
68
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司据此可知三者对应的曲线分别为Ⅰ、Ⅱ、Ⅲ;cHNO =3.0 molL-1时,在0~1 min内,观察图像可
3
(1.5-1.0)104molL-1
知FeR 2+ 的平均消耗速率为 5105mol/(Lmin);②对于反应
3 1min
NO-+2FeR 2+ +3H+ ƒ HNO +2FeR 3+ +H O,加水稀释,平衡往粒子数增加的方向移动,
3 3 2 3 2
c
FeR
2+
FeR 2+ 含量增加,FeR 3+ 含量减小, 3 增大,A正确;HNO 浓度增加,FeR 2+ 转化
3 3 c FeR 3+ 3 3
3
率增加,故α >α >α ,B正确;观察图像可知,三组实验反应速率都是前期速率增加,后期速率减小,C
III II I
错误;硝酸浓度越高,反应速率越快,体系由橙红色转变为淡蓝色所需时间越短,故t 0,升高温
度,平衡右移,CH 平衡转化率增大;降低压强,平衡右移,CH 平衡转化率增大,故有利于提高CO 平
4 4 2
衡转化率的条件是高温低压;答案选C;
(2)已知:Ⅰ:CH (g)CO (g)ƒ 2CO(g)2H (g) ΔH 247kJmol1,K
4 2 2 1 1
Ⅱ:CO (g)H (g)ƒ CO(g)H O(g) ΔH 41kJmol1,K
2 2 2 2 2
根据盖斯定律,由Ⅰ+Ⅱ×2得反应CH (g)3CO (g)ƒ 4CO(g)2H O(g);
4 2 2
故∆H=△H +2△H =+329kJ·mol-1,K K K 2;
1 2 1 2
(3)根据流程可知,Fe O 转化为Fe,Fe又转化为Fe O ,Fe O 可循环利用;CaCO 受热分解生成CaO
3 4 3 4 3 4 3
和CO , CaO又与CO 反应生成CaCO ,CaO也可循环利用,A错误;过程ⅱ,CaO吸收CO 使CO 浓
2 2 3 2 2
度降低,促进Fe O 氧化CO的平衡正移,B正确;过程ⅱCaO吸收CO 而产生的H O最终未被CaO吸
3 4 2 2
收,在过程ⅲ被排出,C正确;焓变只与起始物质的量有关,与过程无关,故相比于反应Ⅰ,该流程的总
cCO
反应还原1molCO 需吸收的能量一样多,D错误;故选BC;通入He,CaCO 分解平衡正移,导致 2
2 3 c(CO)
增大,促进Fe还原CO 平衡正移,故过程ⅱ平衡后通入He,测得一段时间内CO物质的量上升;
2
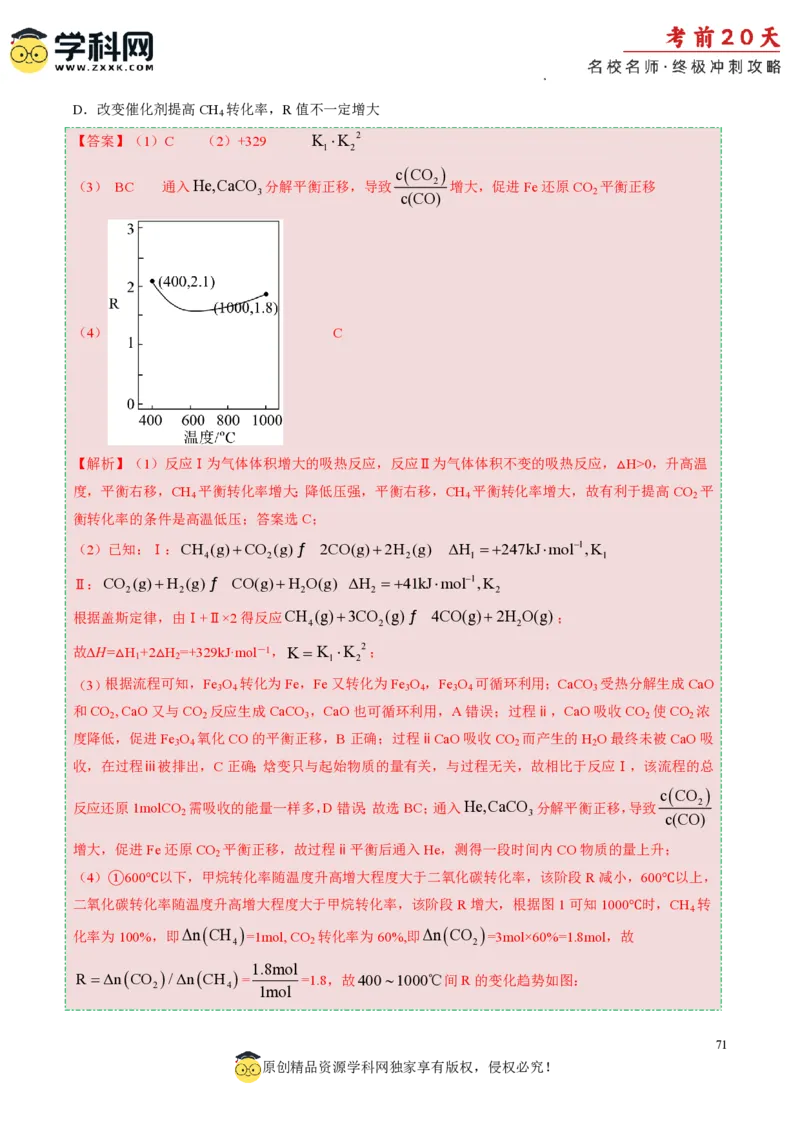
(4)①600℃以下,甲烷转化率随温度升高增大程度大于二氧化碳转化率,该阶段R减小,600℃以上,
二氧化碳转化率随温度升高增大程度大于甲烷转化率,该阶段R增大,根据图1可知1000℃时,CH 转
4
化率为100%,即ΔnCH
=1mol, CO
转化率为60%,即ΔnCO
=3mol×60%=1.8mol,故
4 2 2
1.8mol
R ΔnCO /ΔnCH = =1.8,故4001000℃间R的变化趋势如图:
2 4 1mol
71
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司②R值提高是由于催化剂X选择性地提高反应Ⅱ的速率,使单位时间内反应Ⅱ中CO 的转化率增大,
2
ΔnCO 增大的倍数比ΔnCH
大,则R提高,A正确;根据表中数据可知,温度越低,CH 转化率
2 4 4
越小,而R越大,ΔnCO 增大的倍数比ΔnCH
大,含氢产物中H O占比越高,B正确;温度升高,CH
2 4 2 4
转化率增加,CO 转化率也增大,且两个反应中的CO 转化率均增大,增大倍数多,故R值增大,C错误;
2 2
改变催化剂使反应有选择性按反应Ⅰ而提高CH 转化率,若CO 转化率减小,则R值不一定增大,D正
4 2
确;答案选C。
典例3(2023·辽宁卷第18题)硫酸工业在国民经济中占有重要地位。
(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO ·5H O)取精华法”。借助现代仪器分析,该制备过
4 2
程中CuSO ·5H O分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。
4 2
700℃左右有两个吸热峰,则此时分解生成的氧化物有SO 、_______和_______(填化学式)。
2
(2)铅室法使用了大容积铅室制备硫酸(76%以下),副产物为亚硝基硫酸,主要反应如下:
NO +SO +H O=NO+H SO
2 2 2 2 4
2NO+O =2NO
2 2
(ⅰ)上述过程中NO 的作用为_______。
2
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是_______(答出两点即可)。
(3)接触法制硫酸的关键反应为SO 的催化氧化:
2
SO (g)+ 1 O (g)ƒ SO (g) ΔH=-98.9kJ·mol-1
2 2 2 3
72
原创精品资源学科网独家享有版权,侵权必究!
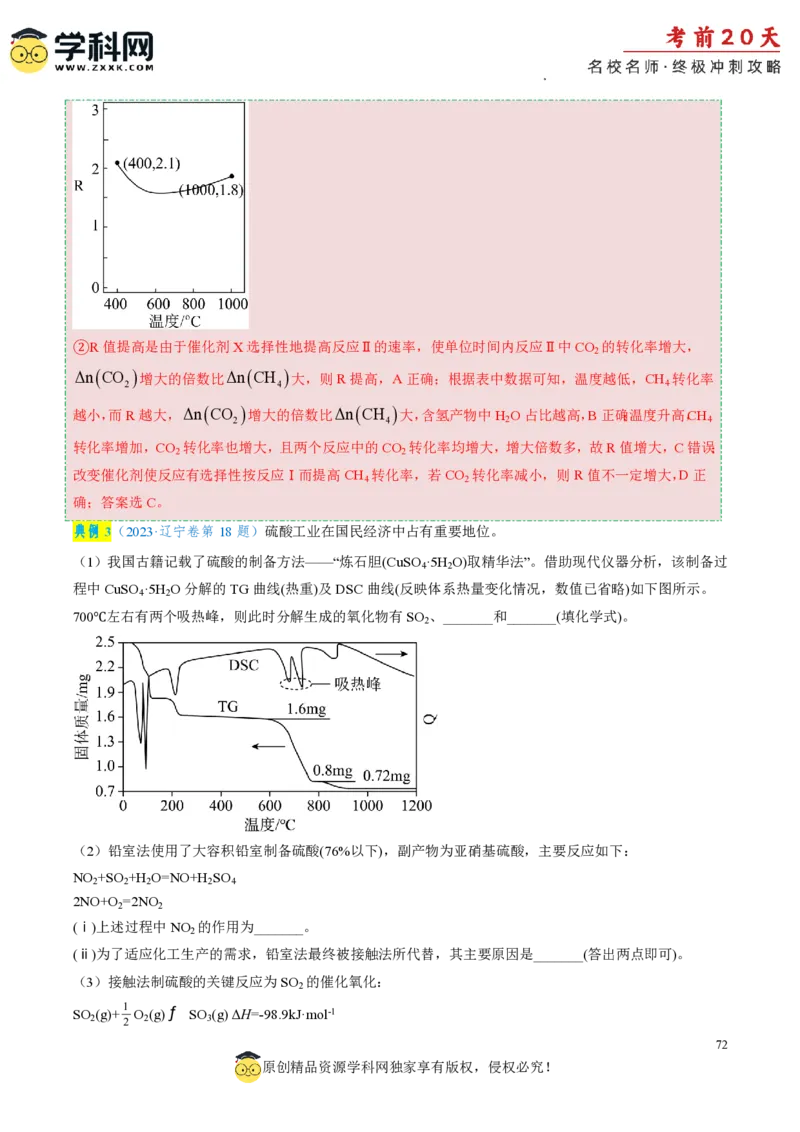
学科网(北京)股份有限公司(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度
的关系如下图所示,下列说法正确的是_______。
a.温度越高,反应速率越大
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同α下的最大速率,选择最佳生产温度
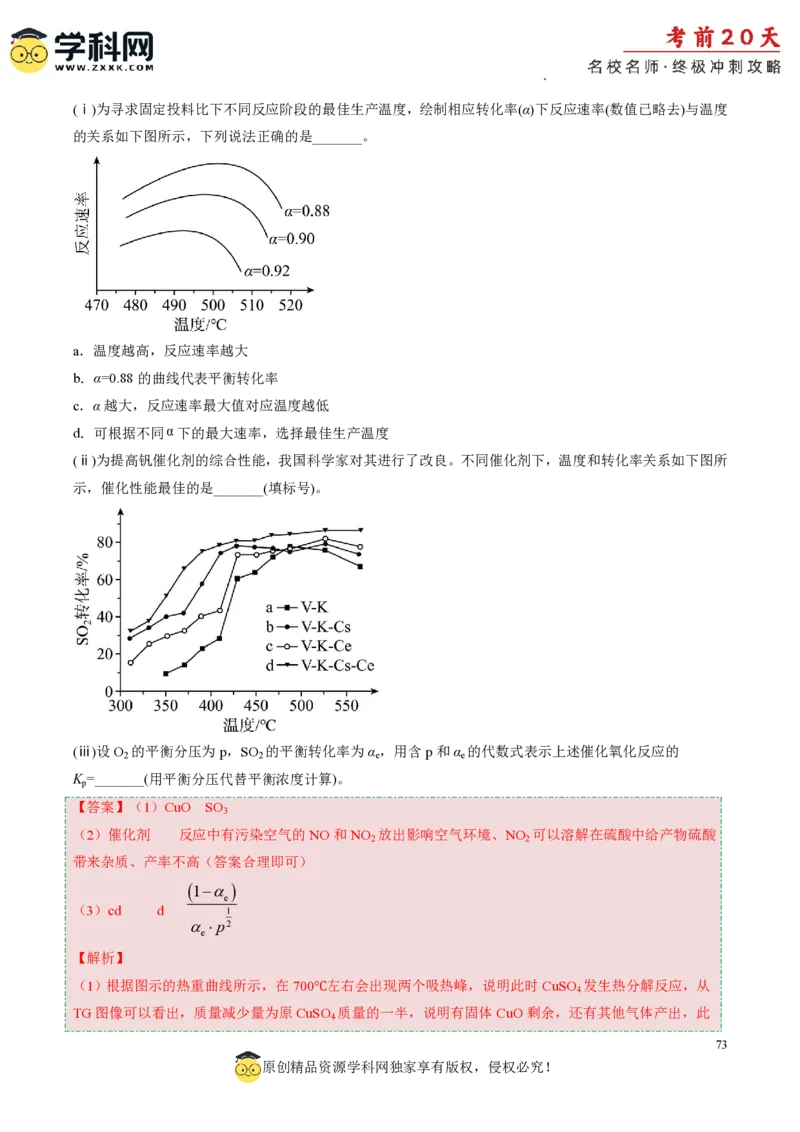
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所
示,催化性能最佳的是_______(填标号)。
(ⅲ)设O 的平衡分压为p,SO 的平衡转化率为α ,用含p和α 的代数式表示上述催化氧化反应的
2 2 e e
K =_______(用平衡分压代替平衡浓度计算)。
p
【答案】(1)CuO SO
3
(2)催化剂 反应中有污染空气的NO和NO 放出影响空气环境、NO 可以溶解在硫酸中给产物硫酸
2 2
带来杂质、产率不高(答案合理即可)
1
e
(3)cd d 1
p2
e
【解析】
(1)根据图示的热重曲线所示,在700℃左右会出现两个吸热峰,说明此时CuSO 发生热分解反应,从
4
TG图像可以看出,质量减少量为原CuSO 质量的一半,说明有固体CuO剩余,还有其他气体产出,此
4
73
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司700 ℃
时气体产物为SO 、SO 、O ,可能出现的化学方程式为3CuSO =====3CuO+2SO ↑+SO ↑+O ↑,结合反
2 3 2 4 2 3 2
应中产物的固体产物质量和气体产物质量可以确定,该反应的产物为CuO、SO 、SO 、O ,故答案为
2 3 2
CuO、SO 。
3
(2)(i)根据所给的反应方程式,NO 在反应过程中线消耗再生成,说明NO 在反应中起催化剂的作用;
2 2
(ii)近年来,铅室法被接触法代替因为在反应中有污染空气的NO和NO 放出影响空气环境、同时作为催
2
化剂的NO 可以溶解在硫酸中给产物硫酸带来杂质影响产品质量、产率不高(答案合理即可)。
2
(3)(i)a.根据不同转化率下的反应速率曲线可以看出,随着温度的升高反应速率先加快后减慢,a错误;
b.从图中所给出的速率曲线可以看出,相同温度下,转化率越低反应速率越快,但在转化率小于88%的
时的反应速率图像并没有给出,无法判断α=0.88的条件下是平衡转化率,b错误;
c.从图像可以看出随着转化率的增大,最大反应速率不断减小,最大反应速率出现的温度也逐渐降低,c
正确;
d.从图像可以看出随着转化率的增大,最大反应速率出现的温度也逐渐降低,这时可以根据不同转化率
选择合适的反应温度以减少能源的消耗,d正确;故选cd;
(ii)为了提高催化剂的综合性能,科学家对催化剂进行了改良,从图中可以看出标号为d的催化剂
V-K-Cs-Ce对SO 的转化率最好,产率最佳,故选d;
2
n(SO )
3 p(总)
p(SO )
3
n(总)
(iii)利用分压代替浓度计算平衡常数,反应的平衡常数K = 1 = =
p n(SO ) 1
p(SO
2
)p2(O
2
)
2 p(总)p2(O )
n(总) 2
n(SO )
3
1 ;设SO 初始量为m mol,则平衡时n(SO )=m·α ,n(SO )=m-m·α =m(1-α ),K =
2 2 e 3 e e p
n(SO ) p2(O )
2 2
m1 1
e e
1 = 1 。
m p2(O ) p2
e 2 e
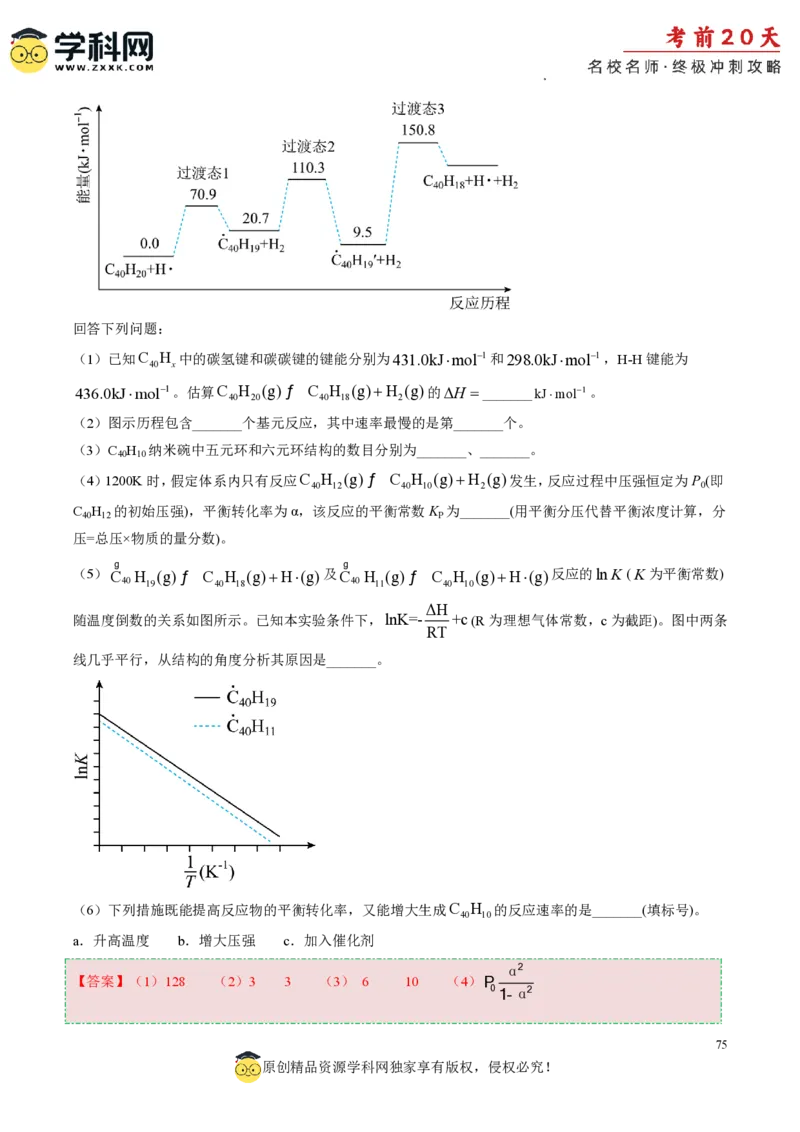
典例4(2023·湖北卷第19题)纳米碗C H 是一种奇特的碗状共轭体系。高温条件下,C H 可以由C H
40 10 40 10 40 20
分子经过连续5步氢抽提和闭环脱氢反应生成。C H (g)HC H (g)H (g)的反应机理和能量变
40 20 40 18 2
化如下:
74
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司回答下列问题:
(1)已知C H 中的碳氢键和碳碳键的键能分别为431.0kJmol1和298.0kJmol1,H-H键能为
40 x
436.0kJmol1。估算C H (g)ƒ C H (g)H (g)的H _______kJmol1。
40 20 40 18 2
(2)图示历程包含_______个基元反应,其中速率最慢的是第_______个。
(3)C H 纳米碗中五元环和六元环结构的数目分别为_______、_______。
40 10
(4)1200K时,假定体系内只有反应C H (g)ƒ C H (g)H (g)发生,反应过程中压强恒定为P (即
40 12 40 10 2 0
C H 的初始压强),平衡转化率为α,该反应的平衡常数K 为_______(用平衡分压代替平衡浓度计算,分
40 12 P
压=总压×物质的量分数)。
g g
(5)C H (g)ƒ C H (g)H(g)及C H (g)ƒ C H (g)H(g)反应的lnK (K为平衡常数)
40 19 40 18 40 11 40 10
ΔH
随温度倒数的关系如图所示。已知本实验条件下,lnK=- +c(R为理想气体常数,c为截距)。图中两条
RT
线几乎平行,从结构的角度分析其原因是_______。
(6)下列措施既能提高反应物的平衡转化率,又能增大生成C H 的反应速率的是_______(填标号)。
40 10
a.升高温度 b.增大压强 c.加入催化剂
α2
【答案】(1)128 (2)3 3 (3) 6 10 (4)P
01-α2
75
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(5)在反应过程中,断裂和形成的化学键相同 (6)a
【解析】
(1)由C H 和C H 的结构式和反应历程可以看出,C H 中断裂了2根碳氢键,C H 形成了1根
40 20 40 18 40 20 40 18
碳碳键,所以C H (g)ƒ C H (g)H (g)的H 4312298436 kJmol1=+128kJmol1;
40 20 40 18 2
g
(2)由反应历程可知,包含3个基元反应,分别为:C H Hgƒ C H H ,
40 20 40 19 2
g g g
C H H ƒ C H 'H ,C H 'H ƒ C H HgH ,其中第三个的活化能最大,反应速率
40 19 2 40 19 2 40 19 2 40 18 2
最慢;
(3)由C H 的结构分析,可知其中含有1个五元环,10个六元环,每脱两个氢形成一个五元环,则
40 20
C H 总共含有6个五元环,10个六元环;
40 10
(4)1200K时,假定体系内只有反应C H (g)ƒ C H (g)H (g)发生,反应过程中压强恒定为P (即
40 12 40 10 2 0
C H 的初始压强),平衡转化率为α,设起始量为1mol,则根据信息列出三段式为:
40 12
C H (g) ƒ C H (g) H(g)
40 12 40 10 2
起始量(mol) 1 0 0
变化量(mol)
平衡量(mol) 1
1-α α α
则P(C H )=P ,P(C H )=P ,P(H)=P ,该反应的平衡常数
40 12 0 1+α 40 10 0 1+α 2 0 1+α
α α
P P
0 1+α 0 1+α α2
K = =P(C H )=P ;
p 1-α 40 12 01-α2
P
0 1+α
g g
(5)C H (g)ƒ C H (g)H(g)及C H (g)ƒ C H (g)H(g)反应的lnK (K为平衡常数)随
40 19 40 18 40 11 40 10
ΔH
温度倒数的关系如图。图中两条线几乎平行,说明斜率几乎相等,根据lnK=- +c(R为理想气体常数,c
RT
为截距)可知,斜率相等,则说明焓变相等,因为在反应过程中,断裂和形成的化学键相同;
(6)由反应历程可知,该反应为吸热反应,升温,反应正向进行,提高了平衡转化率反应速率也加快,a
符合题意;由化学方程式可知,该反应为正向体积增大的反应,加压,反应逆向进行,降低了平衡转化
率,b不符合题意;加入催化剂,平衡不移动,不能提高平衡转化率,c不符合题意;故答案为a。
典例5(2023·湖南卷第16题)聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
21
①C H C H g O g8CO g5H OgΔH 4386.9kJmol1
6 5 2 5 2 2 2 2 1
76
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司②C H CHCH g10O g8CO g4H OgΔH 4263.1kJmol1
6 5 2 2 2 2 2
1
③H g O gH OgΔH 241.8kJmol1
2 2 2 2 3
计算反应④C H C H gƒ C H CHCH gH g 的H _______kJmol1;
6 5 2 5 6 5 2 2 4
(2)在某温度、100kPa下,向反应器中充入1mol气态乙苯发生反应④,其平衡转化率为50%,欲将平
衡转化率提高至75%,需要向反应器中充入_______mol水蒸气作为稀释气(计算时忽略副反应);
(3)在913K 、100kPa下,以水蒸气作稀释气。Fe O 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如
2 3
下两个副反应:
⑤C H C H (g)ƒ C H (g)CH CH (g)
6 5 2 5 6 6 2 2
⑥C H C H (g)H (g)ƒ C H CH (g)CH (g)
6 5 2 5 2 6 5 3 4
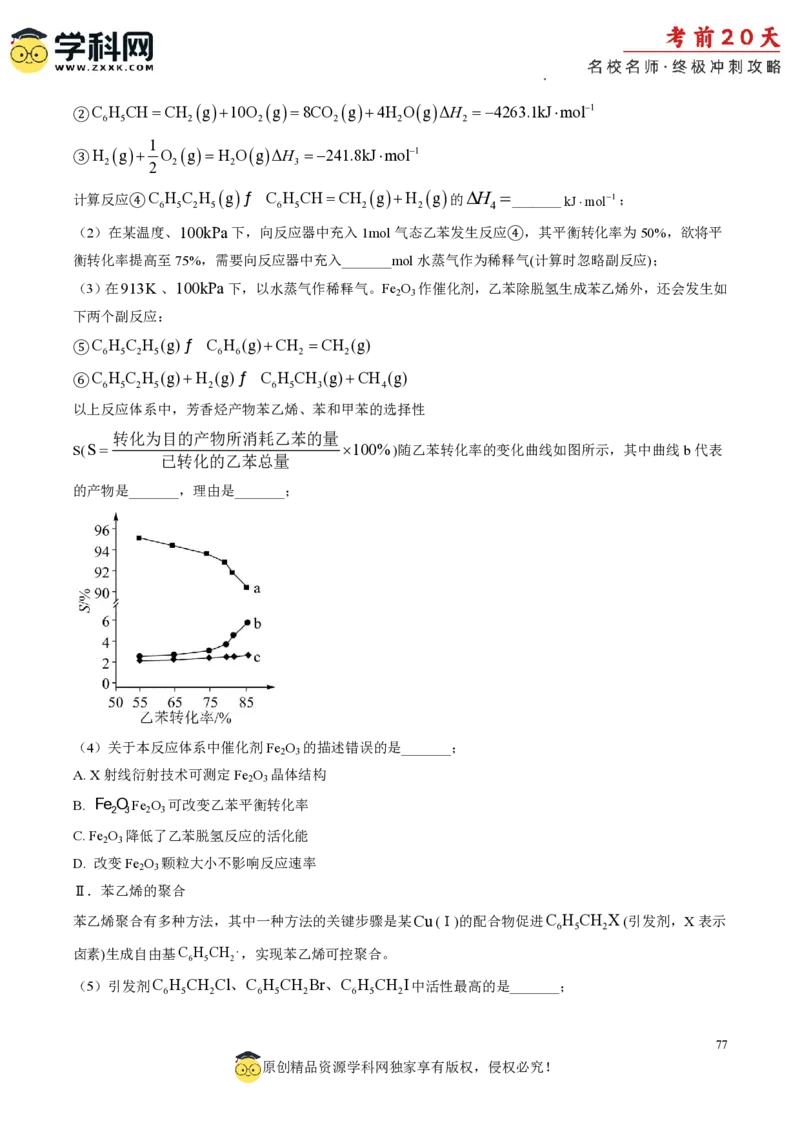
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性
转化为目的产物所消耗乙苯的量
S(S 100%)随乙苯转化率的变化曲线如图所示,其中曲线b代表
已转化的乙苯总量
的产物是_______,理由是_______;
(4)关于本反应体系中催化剂Fe O 的描述错误的是_______;
2 3
A. X射线衍射技术可测定Fe O 晶体结构
2 3
B. Fe OFe O 可改变乙苯平衡转化率
2 3 2 3
C. Fe O 降低了乙苯脱氢反应的活化能
2 3
D. 改变Fe O 颗粒大小不影响反应速率
2 3
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某Cu(Ⅰ)的配合物促进C H CH X(引发剂,X表示
6 5 2
卤素)生成自由基C H CH ·,实现苯乙烯可控聚合。
6 5 2
(5)引发剂C H CH Cl、C H CH Br、C H CH I中活性最高的是_______;
6 5 2 6 5 2 6 5 2
77
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(6)室温下,①Cu在配体L的水溶液中形成CuL ,其反应平衡常数为K;②CuBr在水中的溶
2
度积常数为K 。由此可知,CuBr在配体L的水溶液中溶解反应的平衡常数为_______(所有方程式中计量
sp
系数关系均为最简整数比)。
【答案】(1)+118 (2)5 (3)苯 反应④为主反应,反应⑤⑥为副反应,苯乙烯的选择性
最大;在恒温恒压下,随乙苯转化率的增大,反应⑤正向移动,反应⑥不移动,则曲线b代表产物苯
(4)BD (5)C H CH Cl (6)K∙K
6 5 2 sp
【解析】
(1)根据盖斯定律,将①-②-③可得C H C H (g)⇌C H CH=CH (g)+H (g)
6 5 2 5 6 5 2 2
∆H =-4386.9kJ/mol-(-4263.1kJ/mol)-(-241.8kJ/mol)=+118kJ/mol;
4
(2)设充入H O(g)物质的量为xmol;在某温度、100kPa下,向反应器中充入1mol气态乙苯发生反应
2
C H C H (g)ƒ C H CH=CH (g)H (g)
6 5 2 5 6 5 2 2
n(起始)(mol) 1 0 0
④。乙苯的平衡转化率为50%,可列三段式 ,此时平
n(转化)(mol) 0.5 0.5 0.5
n(平衡)(mol) 0.5 0.5 0.5
衡时混合气体总物质的量为1.5mol,此时容器的体积为V;当乙苯的平衡转化率为75%,可列三段式
C H C H (g)ƒ C H CH=CH (g)H (g)
6 5 2 5 6 5 2 2
n(起始)(mol) 1 0 0
,此时乙苯、苯乙烯、H 物质的量之和为1.75mol,混
n(转化)(mol) 0.75 0.75 0.75 2
n(平衡)(mol) 0.25 0.75 0.75
合气的总物质的量为(1.75+x)mol,在恒温、恒压时,体积之比等于物质的量之比,此时容器的体积为
0.75
( )2
0.5 1.75+x
( )2 V
1.75+x V 1.5
V;两次平衡温度相同,则平衡常数相等,则 = ,解得x=5;
1.5 0.5 0.25
V 1.75+x
V
1.5
(3)曲线a芳香烃产物的选择性大于曲线b、c芳香烃产物的选择性,反应④为主反应,反应⑤⑥为副
反应,则曲线a代表产物苯乙烯的选择性;反应④⑤的正反应为气体分子数增大的反应,反应⑥的正反
应是气体分子数不变的反应;在913K、100kPa(即恒温恒压)下以水蒸气作稀释气,乙苯的转化率增大,
即减小压强,反应④⑤都向正反应方向移动,反应⑥平衡不移动,故曲线b代表的产物是苯;答案为:
苯;反应④为主反应,反应⑤⑥为副反应,苯乙烯的选择性最大;在恒温恒压下,随乙苯转化率的增大,
反应⑤正向移动,反应⑥不移动,则曲线b代表产物苯;
(4)测定晶体结构最常用的仪器是X射线衍射仪,即用X射线衍射技术可测定Fe O 晶体结构,A项正
2 3
确;
催化剂不能使平衡发生移动,不能改变乙苯的平衡转化率,B项错误;催化剂能降低反应的活化能,加快
反应速率,故Fe O 可降低乙苯脱氢反应的活化能,C项正确;催化剂颗粒大小会影响接触面积,会影响
2 3
78
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司反应速率,D项错误;故选BD。
(5)电负性Cl>Br>I,则极性C—Cl键>C—Br键>C—I键,则C H CH Cl更易生成自由基,即活性
6 5 2
最高的是C H CH Cl;答案为:C H CH Cl;
6 5 2 6 5 2
c{[Cu(L) ]+}
(6)Cu+在配体L的水溶液中形成[Cu(L) ]+,则Cu++2L⇌[Cu(L) ]+的平衡常数K= 2 ;CuBr
2 2 c(Cu+)c2(L)
在水中的溶度积常数K =c(Cu+)∙c(Br-);CuBr在配体L的水溶液中溶解反应为CuBr+2L⇌[Cu(L) ]++Br-,
sp 2
c{[Cu(L) ]+}c(Br-) c{[Cu(L) ]+}c(Br-)c(Cu+)
该反应的平衡常数为 2 = 2 =K∙K 。
c2(L) c2(L)c(Cu+) sp
预测1(2024·湖南长沙·二模)我国提出2060年前实现碳中和,为有效降低大气CO 中的含量,以CO 为
2 2
原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。CO 在固体催化剂表面加氢合成甲烷过程中
2
发生如下反应:
Ⅰ.主反应:CO g4H gƒ CH g2H Og H 156.9kJmol1
2 2 4 2 1
Ⅱ.副反应:CO gH gƒ COgH Og H 41.1kJmol1
2 2 2 2
(1)已知:Ⅲ.2H gO g2H Og H 395.6kJmol1
2 2 2 3
Ⅳ.CH g2O gCO g2H Og H 。
4 2 2 2 4
(2)CO 加氢合成甲烷时,通常控制温度为500℃左右,其可能的原因为___________。
2
A.反应速率快 B.平衡转化率高
C.催化剂活性高 D.主反应催化剂选择性好
(3)500℃时,向1L恒容密闭容器中充入4molCO 和12molH ,初始压强为p,20min时主、副反应都达
2 2
到平衡状态,测得cH O5molL1,体系压强为 3 p,则0~20min内vCH molL1min1,
2 4 4
CH 平衡浓度
平衡时CH 选择性= (CH 选择性 4 100%,计算保留三位有效数字,下同),副反应
4 4 CO 转化浓度
2
的K 。
c
(4)以CO 催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为
2
3CH OHg ƒ C H g3H Og。该反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知
3 3 6 2
Ea
Arhenius经验公式Rlnk=- +C,(Ea为活化能,k为速率常数,R和C为常数)。当改变外界条件时,实验
T
数据如图中的曲线b所示,则实验可能改变的外界条件是 。
79
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(5)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为NH 配体:四面体中心为硼原
3
子,顶点均为氢原子。若其摩尔质量为188gmol1,则M元素为 (填元素符号):在该化合物中,M
离子的价电子排布式为 。
预测2(2024·吉林·三模)甲醇用途广泛,可用作溶剂、防冻剂、燃料,也可用于生产生物柴油,利用合成
气(主要成分为CO、CO 和H )可以合成甲醇,涉及的反应如下,回答下列问题:
2 2
反应ⅰ:CO(g)+2H (g)ƒ CH OH(g) △H =−91.5kJ∙mol−1
2 3 1
反应ii:CO (g)+3H (g)ƒ CH OH(g)+H O(g) △H =−49.9kJ∙mol−1
2 2 3 2 2
反应iii:CO (g)+H (g)ƒ CO(g)+H O(g) △H =+41.6kJ∙mol−1
2 2 2 3
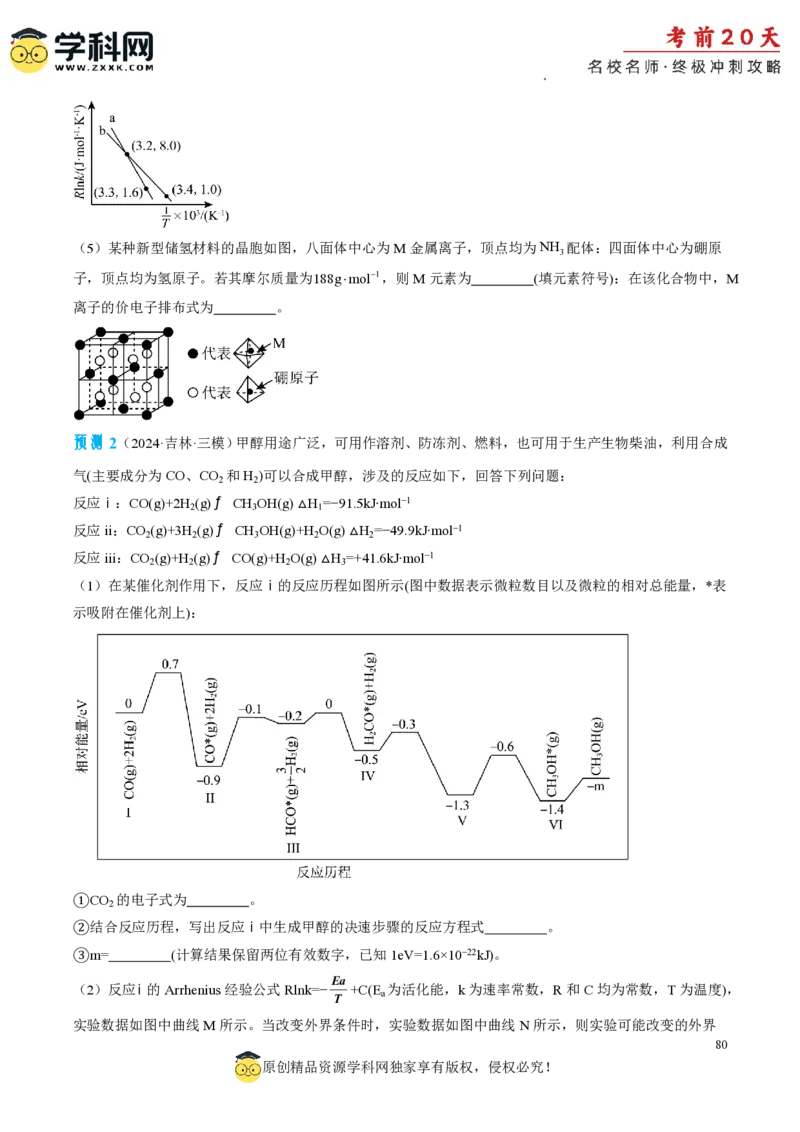
(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表
示吸附在催化剂上):
①CO 的电子式为 。
2
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式 。
③m= (计算结果保留两位有效数字,已知1eV=1.6×10−22kJ)。
Ea
(2)反应ⅰ的Arrhenius经验公式Rlnk=− +C(E 为活化能,k为速率常数,R和C均为常数,T为温度),
T a
实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界
80
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司条件是 。
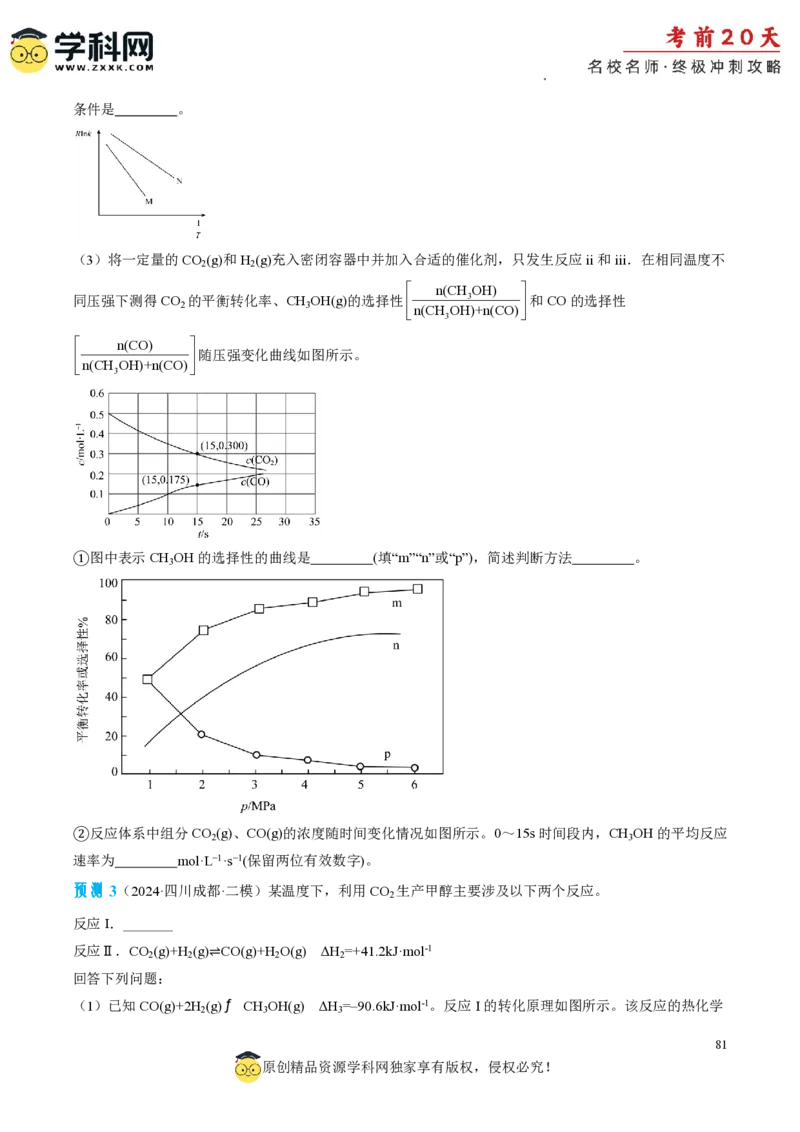
(3)将一定量的CO (g)和H (g)充入密闭容器中并加入合适的催化剂,只发生反应ii和iii.在相同温度不
2 2
n(CH OH)
同压强下测得CO 2 的平衡转化率、CH 3 OH(g)的选择性 n(CH OH 3 )+n(CO) 和CO的选择性
3
n(CO)
随压强变化曲线如图所示。
n(CH OH)+n(CO)
3
①图中表示CH OH的选择性的曲线是 (填“m”“n”或“p”),简述判断方法 。
3
②反应体系中组分CO (g)、CO(g)的浓度随时间变化情况如图所示。0~15s时间段内,CH OH的平均反应
2 3
速率为 mol·L−1·s−1(保留两位有效数字)。
预测3(2024·四川成都·二模)某温度下,利用CO 生产甲醇主要涉及以下两个反应。
2
反应I._______
反应Ⅱ.CO (g)+H (g)⇌CO(g)+H O(g) ΔH =+41.2kJ·mol-1
2 2 2 2
回答下列问题:
(1)已知CO(g)+2H (g)ƒ CH OH(g) ΔH =–90.6kJ·mol-1。反应I的转化原理如图所示。该反应的热化学
2 3 3
81
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司方程式为 ,在 条件下反应I可自发发生。
(2)若在恒压条件下密闭容器中发生反应I和Ⅱ,平衡后再充入惰性气体,反应Ⅱ平衡将 移动(填“正
向”、“逆向”或“不”)。
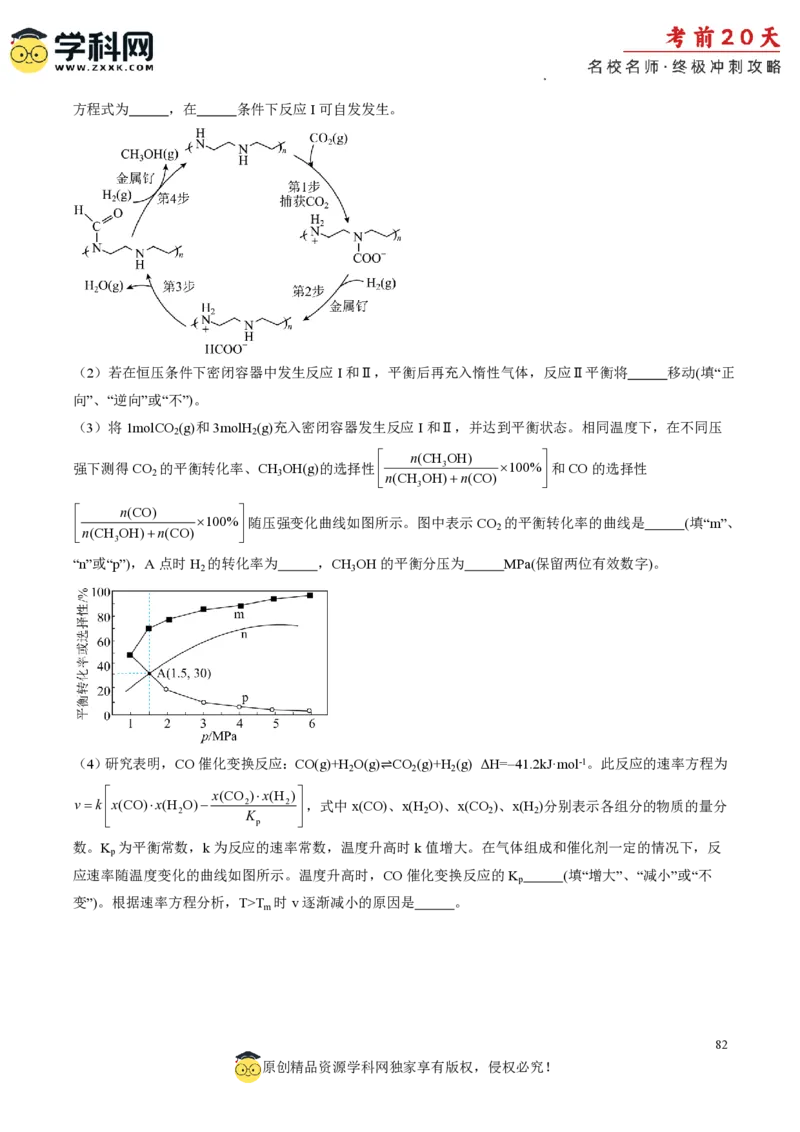
(3)将1molCO (g)和3molH (g)充入密闭容器发生反应I和Ⅱ,并达到平衡状态。相同温度下,在不同压
2 2
n(CH OH)
强下测得CO
2
的平衡转化率、CH
3
OH(g)的选择性
n(CH OH
3
)n(CO)
100%
和CO的选择性
3
n(CO)
n(CH OH)n(CO) 100% 随压强变化曲线如图所示。图中表示CO 2 的平衡转化率的曲线是 (填“m”、
3
“n”或“p”),A点时H 的转化率为 ,CH OH的平衡分压为 MPa(保留两位有效数字)。
2 3
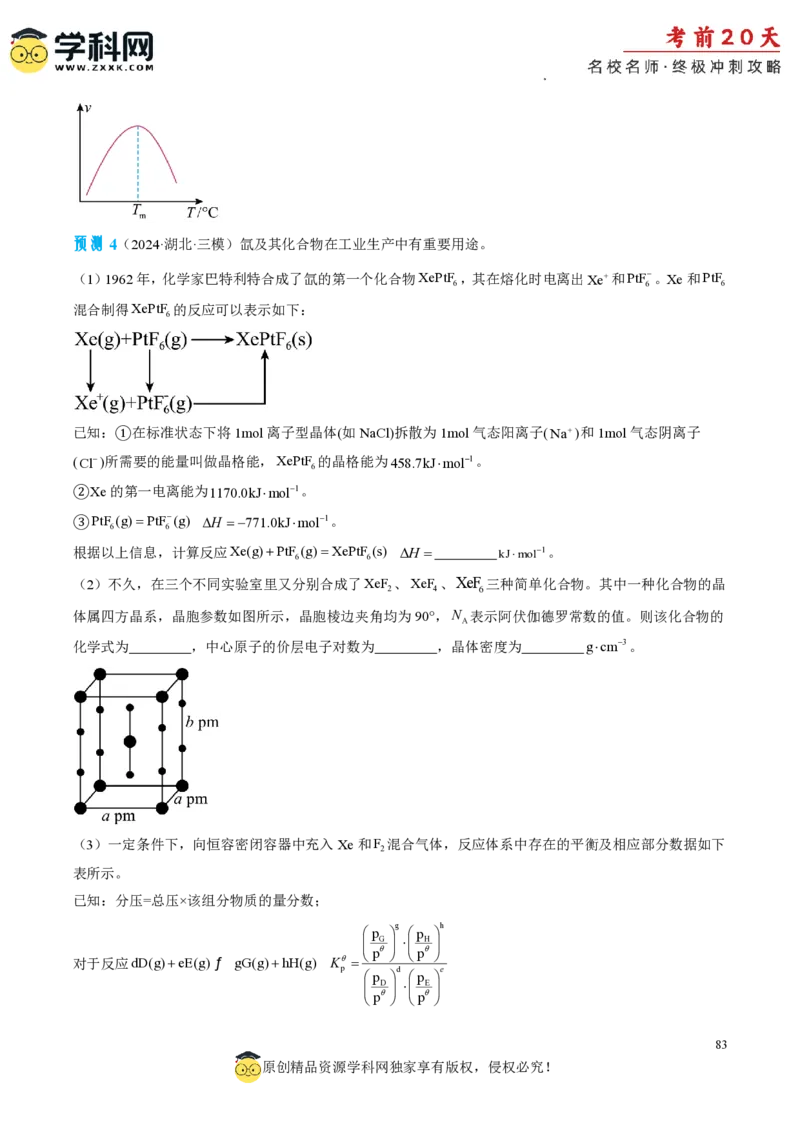
(4)研究表明,CO催化变换反应:CO(g)+H O(g)⇌CO (g)+H (g) ΔH=–41.2kJ·mol-1。此反应的速率方程为
2 2 2
x(CO )x(H )
vkx(CO)x(H O) 2 2 ,式中x(CO)、x(H O)、x(CO )、x(H )分别表示各组分的物质的量分
2 K
p
2 2 2
数。K 为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反
p
应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的K (填“增大”、“减小”或“不
p
变”)。根据速率方程分析,T>T 时v逐渐减小的原因是 。
m
82
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司预测4(2024·湖北·三模)氙及其化合物在工业生产中有重要用途。
(1)1962年,化学家巴特利特合成了氙的第一个化合物XePtF ,其在熔化时电离出Xe和PtF。Xe和PtF
6 6 6
混合制得XePtF 的反应可以表示如下:
6
已知:①在标准状态下将1mol离子型晶体(如NaCl)拆散为1mol气态阳离子(Na)和1mol气态阴离子
(Cl)所需要的能量叫做晶格能,XePtF 的晶格能为458.7kJmol1。
6
②Xe的第一电离能为1170.0kJmol1。
③PtF(g)PtF(g) H 771.0kJmol1。
6 6
根据以上信息,计算反应Xe(g)PtF(g)XePtF(s) H kJmol1。
6 6
(2)不久,在三个不同实验室里又分别合成了XeF 、XeF 、XeF 三种简单化合物。其中一种化合物的晶
2 4 6
体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,N 表示阿伏伽德罗常数的值。则该化合物的
A
化学式为 ,中心原子的价层电子对数为 ,晶体密度为 gcm3。
(3)一定条件下,向恒容密闭容器中充入Xe和F 混合气体,反应体系中存在的平衡及相应部分数据如下
2
表所示。
已知:分压=总压×该组分物质的量分数;
g h
p p
G H
p
p
对于反应dD(g)eE(g)ƒ gG(g)hH(g) K
p d e
p p
D E
p
p
83
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司其中p100kPa,p 、p 、p 、p 为各组分的平衡分压。
G H D E
标准压强平衡常数K
p
K(523K) K(673K)
p p
反应平衡
反应I:Xe(g)F (g)ƒ XeF (g) ΔH 8.8104 360
2 2 1
反应II:Xe(g)2F (g)ƒ XeF (g) ΔH
2 4 2
反应III:Xe(g)3F (g)ƒ XeF(g) ΔH K(III)
2 6 3 p
nF
①ΔH 0(填“>”或“<”)。为提高平衡混合物中XeF g的含量,应 投料比xx 2 (填
1 2 n(Xe)
“增大”或“减小”)。
②673K时充入23.77molXe和45.28molF ,达平衡时容器内总压强p2.477103kPa,各产物的物质的量如
2
下表所示:
化学式 XeF XeF XeF
2 4 6
物质的量/mol 3.60 19.80 0.36
则F 平衡转化率 F (保留三位有效数字),K(III) 。
2 平 2 p
预测5(2024·广东·二模)含硫化合物在能源、材料及环境等工业领域均有广泛的应用。
Ⅰ.工业废气H S分解可制取H 。
2 2
(1)已知热化学方程式:
ⅰ.S g2O g2SO g ΔH
2 2 2 1
ⅱ.2H gO g2H Og ΔH
2 2 2 2
ⅲ.2H Sg3O g2SO g2H Og ΔH
2 2 2 2 3
H S热分解反应2H SgS g2H g的H (用含ΔH 、ΔH 、ΔH 的式子表示)。
2 2 2 2 4 1 2 3
(2)一定温度下,2mol H S在体积为VL的恒容密闭容器中发生上述分解反应,ts时H 的产率为40%,
2 2
则0~ts内H S的平均分解速率为 molL1s1;H S充分分解达到平衡时,容器中H S和H 的分压
2 2 2 2
相等,则该温度下的平衡常数K 。
Ⅱ.KSCN可用于镀铬工业。常温下,用KSCN配制电镀液,溶液中Cr3与SCN发生第一、二步络合的反
应如下:
ⅳ.Cr3 SCN ƒ CrSCN 2 K 74.1
1
ⅴ.CrSCN 2 SCN ƒ CrSCN K 13.0
2 2
84
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(3)根据以上络合反应,下列说法正确的有___________(填字母)。
A.加水稀释后,溶液中离子的总数减少
B.加入少量FeCl 固体,溶液中含铬微粒总数不变
3
C.反应Cr3 2SCN ƒ CrSCN 的平衡常数K K K
2 3 1 2
D.溶液中c Cr3 减小,SCN与
CrSCN
2 浓度的比值减小
(4)常温下,某研究小组配制了起始浓度c Cr3 0.2molL1、c SCN 不同的系列溶液,测得平衡时
0 0
Cr3、
CrSCN
2 、
CrSCN
的浓度c
平
(含铬微粒)随c
平
SCN 的变化曲线如图所示,平衡后其他含
2
铬微粒CrSCN
x-3-
(3≤x≤6,图中未画出)总浓度为amol/L。
x
①c SCN 0.05molL1时,图中含铬微粒按浓度由大到小的顺序为 ;A点时,溶液中SCN的
平
平衡浓度为 (列出计算式即可)。
②在某电镀工艺中,Cr3的浓度需要在0.0162molL1以上,结合计算判断C点所对应的溶液能否用于该电
镀工艺 (写出计算过程)。
押题1(2024·山东济南·一模)天然气、石油钻探过程会释放出CO 、H S等气体。某种将CO 和H S共活
2 2 2 2
化的工艺涉及如下反应:
①CO gH Sgƒ COSgH Og ΔH 35.00kJmol1
2 2 2 1
②2CO g2H Sgƒ 2COgS g2H Og ΔH
2 2 2 2 2
③2H Sgƒ S g2H g ΔH 171.58kJmol1
2 2 2 3
④CO gH gƒ COgH Og ΔH 41.20kJmol1
2 2 2 4
回答下列问题:
(1)已知:298K时,18g气态水转化为液态水释放出44kJ的能量;H S(g)的标准摩尔燃烧焓(△H)为
2
-586kJ·mol-1,则COS(g)的标准摩尔燃烧焓(H)为 kJ·mol-1,反应②在 (填“高温”“低温”
85
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司或“任意温度”)下能自发进行。
(2)一定条件下,向起始压强为200kPa的恒容密闭容器中通入等物质的量的CO (g)和H S(g)混合气体,
2 2
发生上述反应,25min时,测得体系总压强为210kPa,S (g)的平均反应速率为 kPa·min-1.达到平衡
2
时,测得体系总压强为230kPa,2pCOS=2pH =pCO ,此时H S(g)的平衡转化率为 ,反应
2 2 2
②的标准平衡常数K (已知:分压=总压×该组分物质的量分数,对于反应
g h
p p
G H
dDgeEgƒ gGghHg,KΘ
pΘ
pΘ
,其中pΘ 100kPa,p 、p 、p 、p 为各组分
d d G H D E
p p
D E
pΘ
pΘ
的平衡分压)。
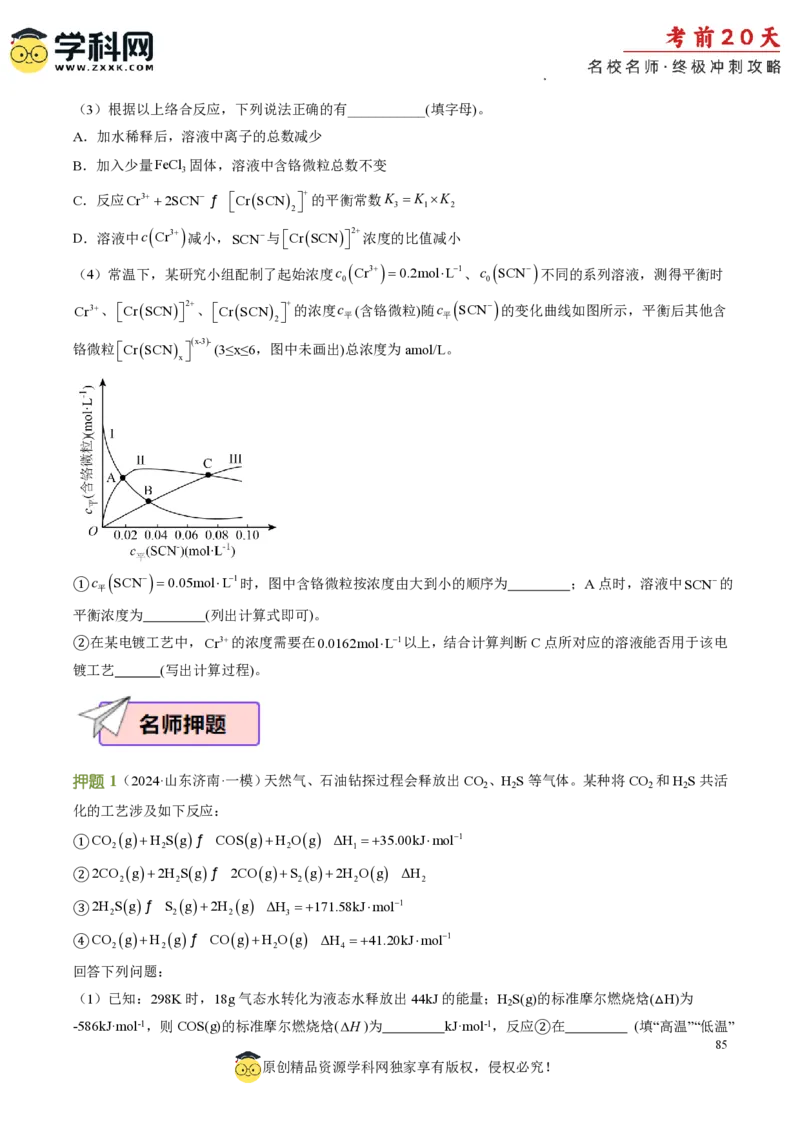
(3)将等物质的量的CO (g)和H S(g)混合气体充入恒压密闭容器中,发生上述反应,反应物的平衡转化率、
2 2
n COS
COS或H O的选择性与温度关系如图所示。COS的选择性= 生成 100%,H O的选择性
2 n H S 2
消耗 2
n H O
= 生成 2 100%。
n H S
消耗 2
①表示“COS的选择性”的曲线是 (填“曲线a”或“曲线b”);
②温度低于500℃时,H S的转化率与CO 的相等,原因是 。
2 2
押题2(2024·河北邢台·二模)工业废气中的二氧化碳加氢制甲醇是“碳中和”的一个重要研究方向,在催化
剂作用下,主要发生以下反应:
ⅰ.CO g3H gƒ CH OHgH Og ΔH 49kJmol1;
2 2 3 2 1
ⅱ.CO gH gƒ COgH Og ΔH 41kJmol1;
2 2 2 2
ⅲ.COg2H gƒ CH OHg ΔH 。
2 3 3
86
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(1)已知反应ⅲ正反应的活化能为EkJmol1,则其逆反应的活化能为 kJmol1(用含有E 的式
a a
子表示)。
(2)①一定温度下,向恒容密闭容器中通入物质的量之比为1:3的CO 与H ,发生以上3个反应,下列
2 2
能说明反应达到平衡状态的是 。
A.v CO v H O B.平衡常数不再发生变化
消耗 2 消耗 2
C.气体密度不再改变 D.测得CO的浓度保持不变
②若起始压强为200MPa,反应经tmin后达到平衡,此时体系压强为150MPa,H O的分压:
2
pH O40MPa,则tmin内反应的平均速率vCO MPa/min,CH OH的选择性为 %
2 3
nCH OH
选择性 3 ,反应ⅰ的平衡常数K (保留两位有效数字)。
消耗nCO
2
p
nH
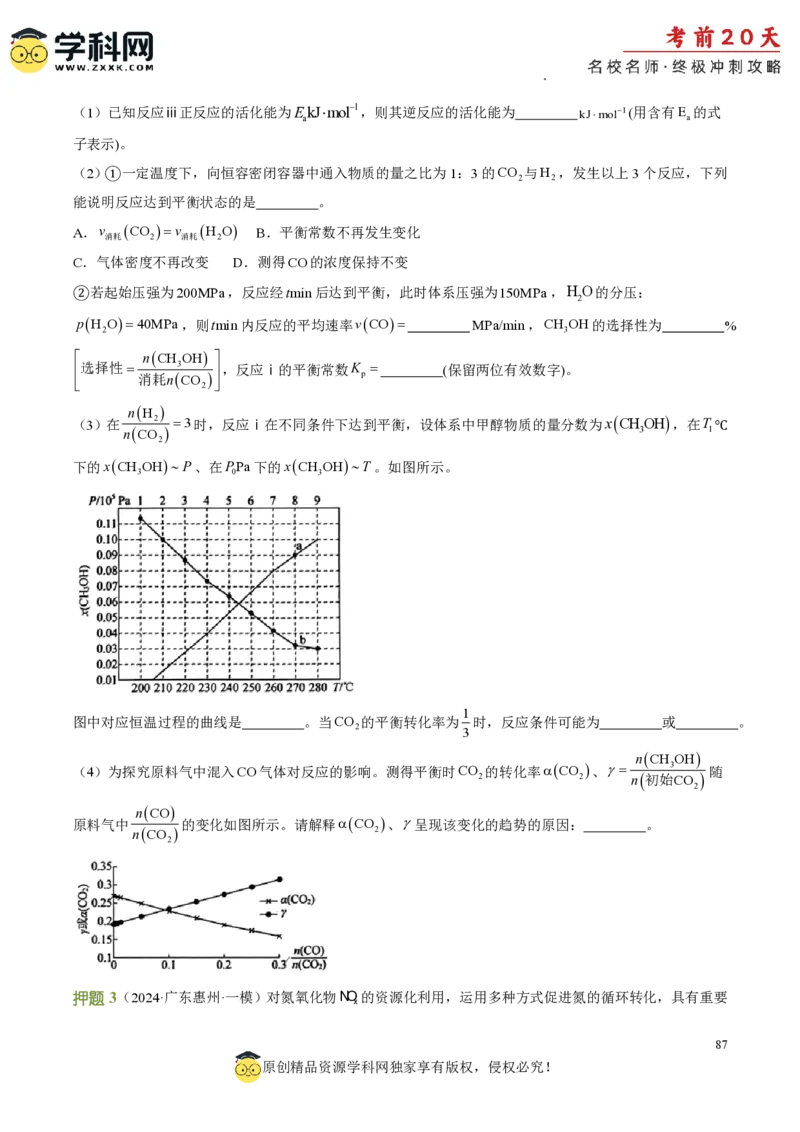
(3)在 2 3时,反应ⅰ在不同条件下达到平衡,设体系中甲醇物质的量分数为xCHOH ,在T ℃
nCO 3 1
2
下的xCH OHP、在PPa下的xCH OHT。如图所示。
3 0 3
1
图中对应恒温过程的曲线是 。当CO 的平衡转化率为 时,反应条件可能为 或 。
2 3
nCH OH
(4)为探究原料气中混入CO气体对反应的影响。测得平衡时CO 的转化率CO 、 3 随
2 2 n初始CO
2
nCO
原料气中 的变化如图所示。请解释CO 、呈现该变化的趋势的原因: 。
nCO 2
2
押题3(2024·广东惠州·一模)对氮氧化物NO的资源化利用,运用多种方式促进氮的循环转化,具有重要
x
87
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司的研究意义。
(1)已知a:N (g)O (g)2NO(g) H182.6kJmol1
2 2
b:C的燃烧热为393kJmol1;
c:CO (g)C(s)2CO(g) H172.4kJmol1
2
①请写出NO(g)与CO(g)反应生成两种无污染性气体的热化学方程式: 。
②将等物质的量的NO与CO混合气体分别通入体积均为1L的恒温密闭容器Ⅰ和绝热密闭容器Ⅱ中,反应
一段时间后两容器内达到平衡状态,下列说法正确的是 。
A.两容器内混合气体密度相等
B.NO转化率α α
Ⅰ Ⅱ
C.反应平衡常数K K
Ⅰ Ⅱ
(2)可利用钴氨配合物吸收NO,CoNH 2 对NO的配合能力很强,而CoNH 3 对NO的配合能力
3 6 3 6
极低。
①已知CoNH 3 的结构如图所示 ,1molCoNH 3 中含有σ键的数目
3 6 3 6
是 。
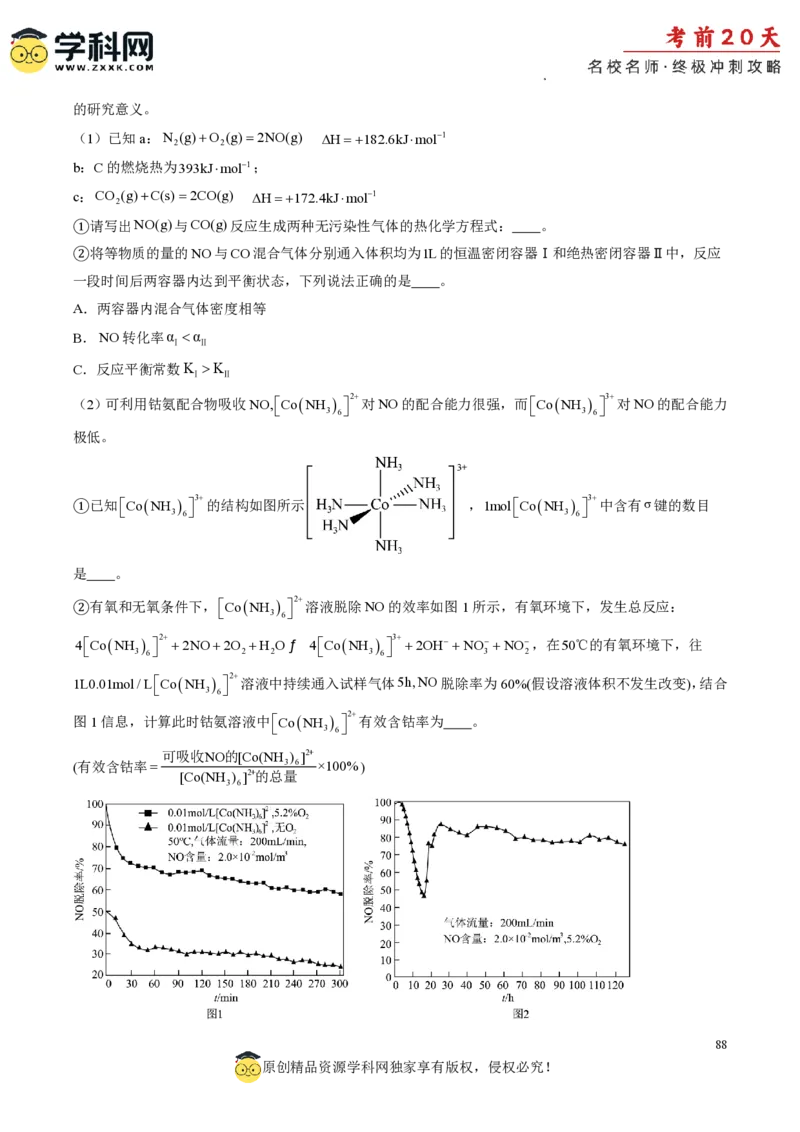
②有氧和无氧条件下,CoNH 2 溶液脱除NO的效率如图1所示,有氧环境下,发生总反应:
3 6
4CoNH 2 2NO2O H Oƒ 4CoNH 3 2OHNONO,在50℃的有氧环境下,往
3 6 2 2 3 6 3 2
1L0.01mol/LCoNH 2 溶液中持续通入试样气体5h,NO脱除率为60%(假设溶液体积不发生改变),结合
3 6
图1信息,计算此时钴氨溶液中CoNH 2 有效含钴率为 。
3 6
可吸收NO的[Co(NH ) ]2+
(有效含钴率 3 6 ×100%)
[Co(NH ) ]2+的总量
3 6
88
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司③钴氨溶液经过多次循环吸收NO后,其吸收NO的能力变化如图2所示,前16h内钴氨溶液吸收NO的能
力不断下降的原因是 。
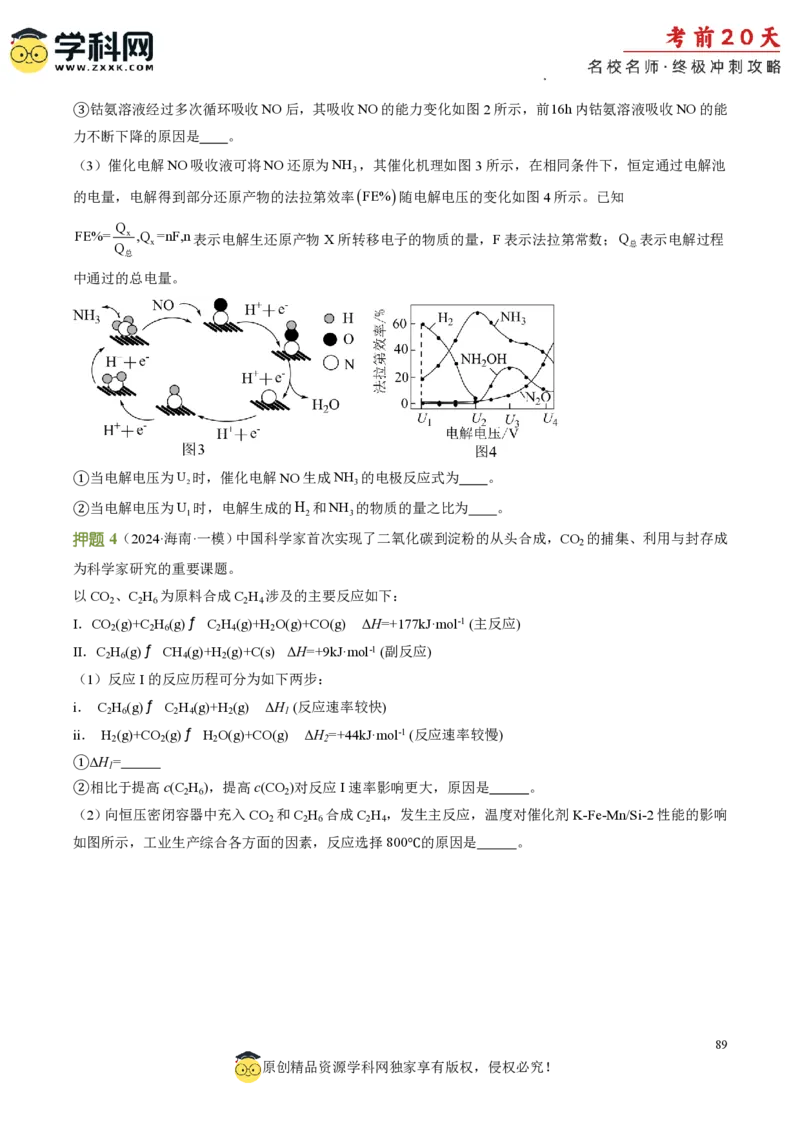
(3)催化电解NO吸收液可将NO还原为NH ,其催化机理如图3所示,在相同条件下,恒定通过电解池
3
的电量,电解得到部分还原产物的法拉第效率FE%随电解电压的变化如图4所示。已知
Q
FE%= x ,Q =nF,n表示电解生还原产物X所转移电子的物质的量,F表示法拉第常数;Q 表示电解过程
Q x 总
总
中通过的总电量。
①当电解电压为U 时,催化电解NO生成NH 的电极反应式为 。
2 3
②当电解电压为U 时,电解生成的H 和NH 的物质的量之比为 。
1 2 3
押题4(2024·海南·一模)中国科学家首次实现了二氧化碳到淀粉的从头合成,CO 的捕集、利用与封存成
2
为科学家研究的重要课题。
以CO 、C H 为原料合成C H 涉及的主要反应如下:
2 2 6 2 4
I.CO (g)+C H (g)ƒ C H (g)+H O(g)+CO(g) ΔH=+177kJ·mol-1 (主反应)
2 2 6 2 4 2
II.C H (g)ƒ CH (g)+H (g)+C(s) ΔH=+9kJ·mol-1 (副反应)
2 6 4 2
(1)反应I的反应历程可分为如下两步:
i. C H (g)ƒ C H (g)+H (g) ΔH (反应速率较快)
2 6 2 4 2 1
ii. H (g)+CO (g)ƒ H O(g)+CO(g) ΔH =+44kJ·mol-1 (反应速率较慢)
2 2 2 2
①∆H =
1
②相比于提高c(C H ),提高c(CO )对反应I速率影响更大,原因是 。
2 6 2
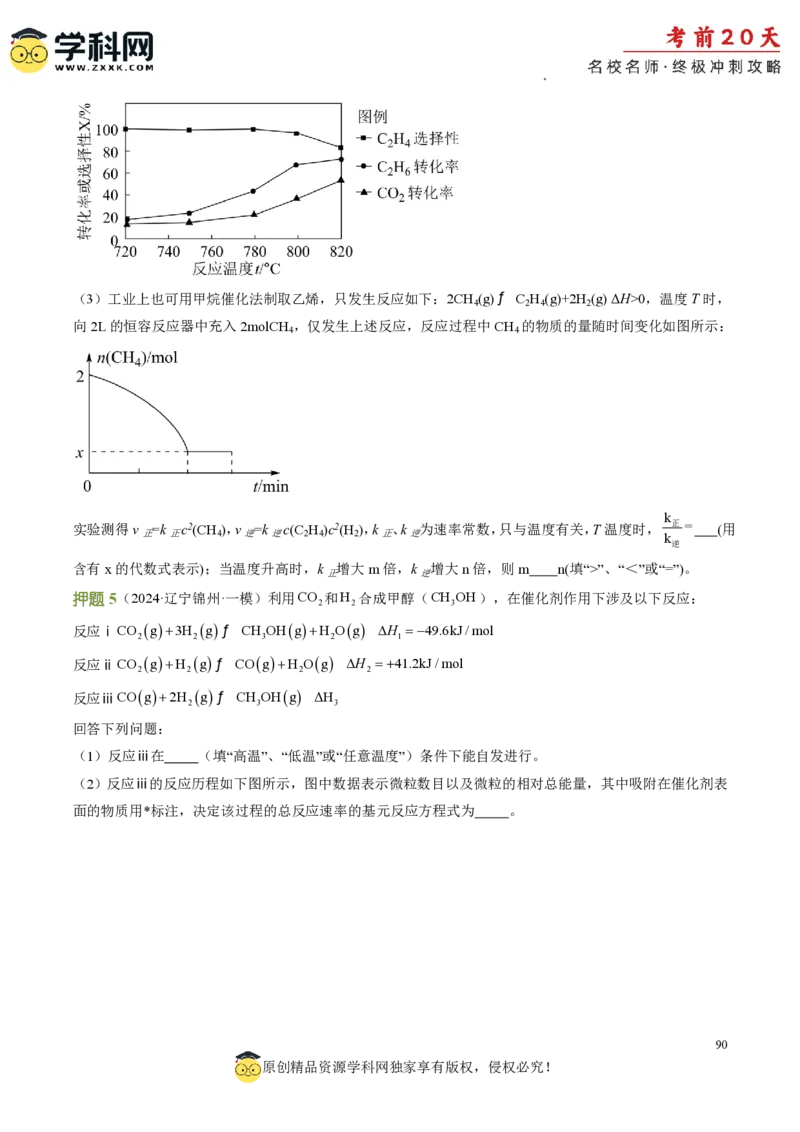
(2)向恒压密闭容器中充入CO 和C H 合成C H ,发生主反应,温度对催化剂K-Fe-Mn/Si-2性能的影响
2 2 6 2 4
如图所示,工业生产综合各方面的因素,反应选择800℃的原因是 。
89
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(3)工业上也可用甲烷催化法制取乙烯,只发生反应如下:2CH (g)ƒ C H (g)+2H (g) ΔH>0,温度T时,
4 2 4 2
向2L的恒容反应器中充入2molCH ,仅发生上述反应,反应过程中CH 的物质的量随时间变化如图所示:
4 4
k
实验测得v =k c2(CH ),v =k c(C H )c2(H ),k 、k 为速率常数,只与温度有关,T温度时, 正 = (用
正 正 4 逆 逆 2 4 2 正 逆 k
逆
含有x的代数式表示);当温度升高时,k 增大m倍,k 增大n倍,则m n(填“>”、“<”或“=”)。
正 逆
押题5(2024·辽宁锦州·一模)利用CO 和H 合成甲醇(CH OH),在催化剂作用下涉及以下反应:
2 2 3
反应ⅰCO g3H gƒ CH OHgH Og H 49.6kJ/mol
2 2 3 2 1
反应ⅱCO gH gƒ COgH Og H 41.2kJ/mol
2 2 2 2
反应ⅲCOg2H gƒ CH OHg ΔH
2 3 3
回答下列问题:
(1)反应ⅲ在 (填“高温”、“低温”或“任意温度”)条件下能自发进行。
(2)反应ⅲ的反应历程如下图所示,图中数据表示微粒数目以及微粒的相对总能量,其中吸附在催化剂表
面的物质用*标注,决定该过程的总反应速率的基元反应方程式为 。
90
原创精品资源学科网独家享有版权,侵权必究!
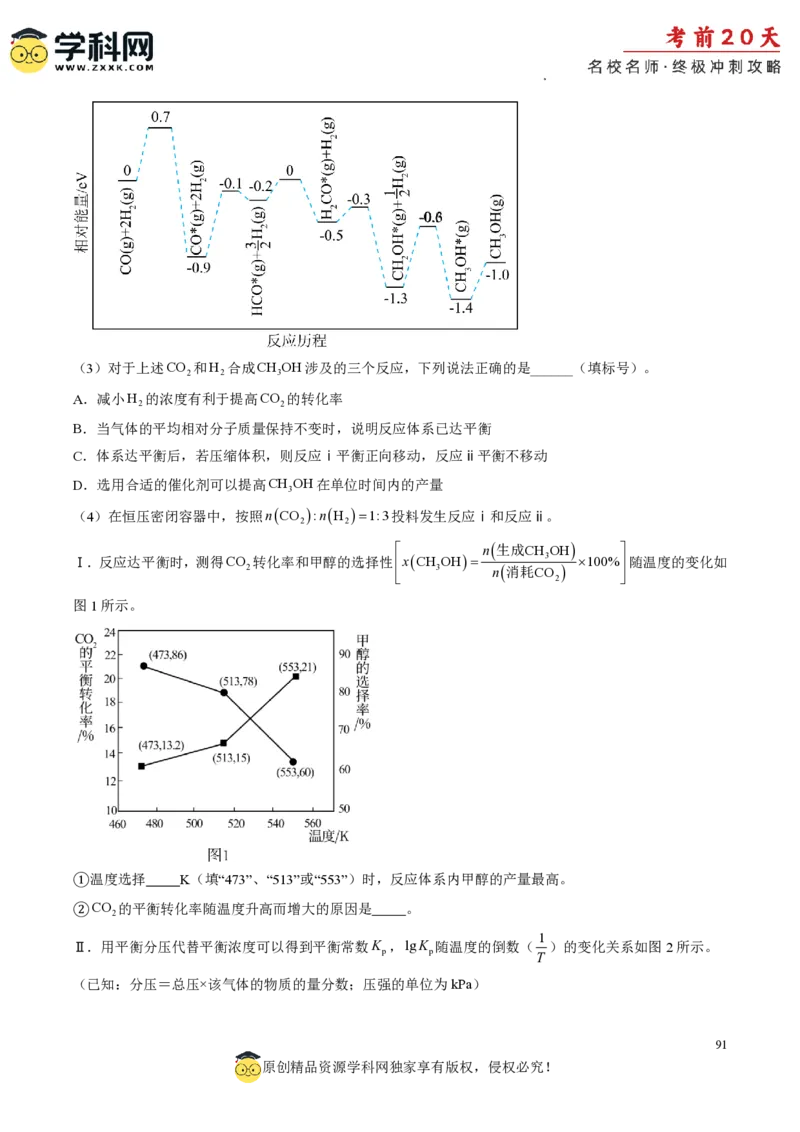
学科网(北京)股份有限公司(3)对于上述CO 和H 合成CH OH涉及的三个反应,下列说法正确的是______(填标号)。
2 2 3
A.减小H 的浓度有利于提高CO 的转化率
2 2
B.当气体的平均相对分子质量保持不变时,说明反应体系已达平衡
C.体系达平衡后,若压缩体积,则反应ⅰ平衡正向移动,反应ⅱ平衡不移动
D.选用合适的催化剂可以提高CH OH在单位时间内的产量
3
(4)在恒压密闭容器中,按照nCO :nH 1:3投料发生反应ⅰ和反应ⅱ。
2 2
n生成CH OH
Ⅰ.反应达平衡时,测得CO 转化率和甲醇的选择性xCH OH 3 100%随温度的变化如
2
3 n消耗CO
2
图1所示。
①温度选择 K(填“473”、“513”或“553”)时,反应体系内甲醇的产量最高。
②CO 的平衡转化率随温度升高而增大的原因是 。
2
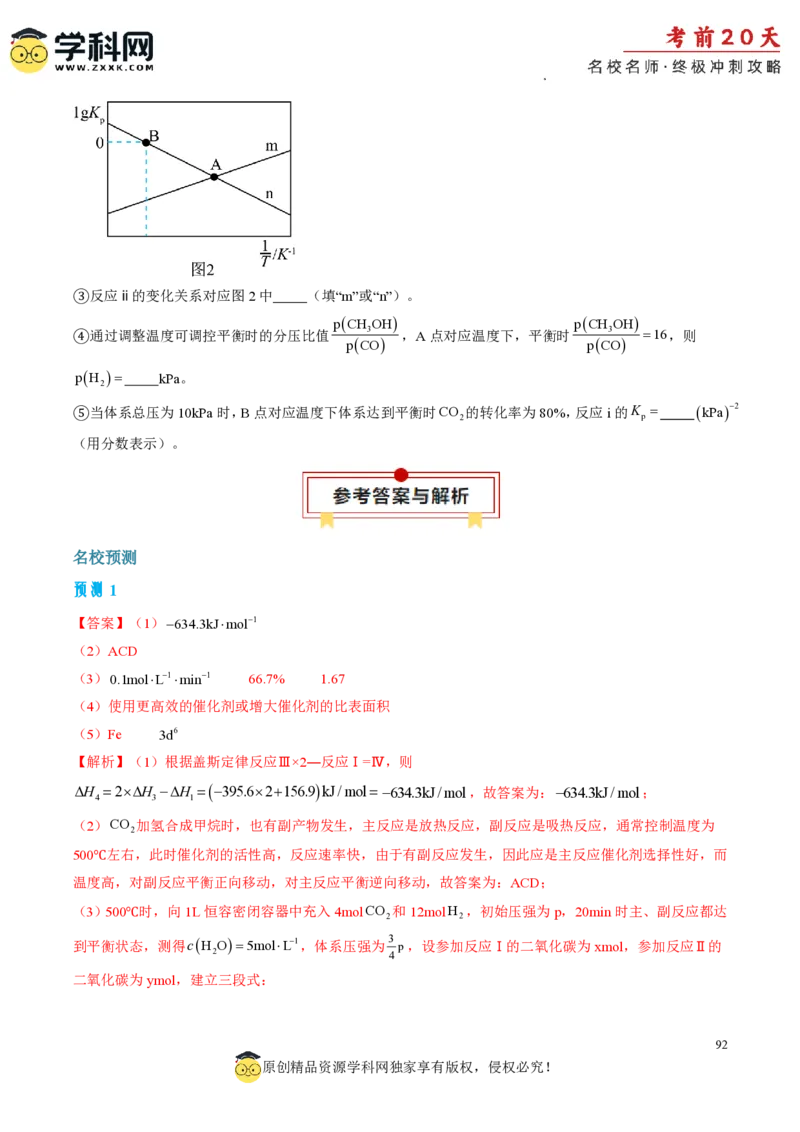
1
Ⅱ.用平衡分压代替平衡浓度可以得到平衡常数K ,lgK 随温度的倒数( )的变化关系如图2所示。
p p T
(已知:分压=总压×该气体的物质的量分数;压强的单位为kPa)
91
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司③反应ⅱ的变化关系对应图2中 (填“m”或“n”)。
pCH OH pCH OH
④通过调整温度可调控平衡时的分压比值 3 ,A点对应温度下,平衡时 3 16,则
pCO pCO
pH kPa。
2
⑤当体系总压为10kPa时,B点对应温度下体系达到平衡时CO 的转化率为80%,反应i的K kPa2
2 p
(用分数表示)。
名校预测
预测1
【答案】(1)634.3kJmol1
(2)ACD
(3)0.1molL1min1 66.7% 1.67
(4)使用更高效的催化剂或增大催化剂的比表面积
(5)Fe 3d6
【解析】(1)根据盖斯定律反应Ⅲ×2―反应Ⅰ=Ⅳ,则
H 2H H 395.62156.9kJ/mol 634.3kJ/mol,故答案为:634.3kJ/mol;
4 3 1
(2)CO 加氢合成甲烷时,也有副产物发生,主反应是放热反应,副反应是吸热反应,通常控制温度为
2
500℃左右,此时催化剂的活性高,反应速率快,由于有副反应发生,因此应是主反应催化剂选择性好,而
温度高,对副反应平衡正向移动,对主反应平衡逆向移动,故答案为:ACD;
(3)500℃时,向1L恒容密闭容器中充入4molCO 和12molH ,初始压强为p,20min时主、副反应都达
2 2
到平衡状态,测得cH O5molL1,体系压强为 3 p,设参加反应Ⅰ的二氧化碳为xmol,参加反应Ⅱ的
2 4
二氧化碳为ymol,建立三段式:
92
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司CO g +4H g ƒ CH g +2H Og
2 2 4 2
起始量mol 4 12 0 0
转化量mol x 4x x 2x
平衡量mol 4-x 12-4x x 2x
CO g +H g ƒ COg +H Og
2 2 2
起始量mol 4-x 12-4x 0 2x
转化量mol y y y y
平衡量mol 4-x-y 12-4x-y y 2x+y
3
p
则有2xy5,根据物质的量之比等于压强之比得到162x 4 ,解得x2,y1,则0~20min内
16 p
c 2mol 2
vCH 0.1mol/Lmin,平衡时CH 选择性 100% 66.7%,cCO 1molL1,
4 t 1L20min 4 12 2
cCOcH O 15
cH 3molL1,cCO1molL1,cH O5molL1副反应K = 2 = 1.67,故答案
2 2 c cCO cH 13
2 2
为:0.1mol/Lmin;66.7%;1.67;
(4)当改变外界条件时,实验数据如图中的曲线b所示,斜率降低,说明活化能降低,则实验可能改变的
外界条件是使用更高效的催化剂或增大催化剂的比表面积,故答案为:使用更高效的催化剂或增大催化剂
的比表面积;
1 1
(5)由图可知,黑球代表MNH ,位于顶点和面心,个数为8 +6 4,白球代表BH ,位于体内,
3 6 8 2 4
个数为8,则黑球:白球4:81:2,则化学式为MNH BH ,摩尔质量为188gmol1,则M的摩尔
3 6 4 2
质量为188176152gmol156gmol1,则M元素为Fe;MNH BH 中,NH 为分子,不带
3 6 4 2 3
电荷,BH带1个单位负电荷,则Fe为+2价,其价电子排布式为3d6,故答案为:Fe;3d6。
4
预测2
3
【答案】(1) CO*(g)+2H (g)=HCO*(g)+ H *(g) 0.95eV
2 2
2
(2)加入了高效催化剂
(3) m 反应ii是气体体积减小的反应,反应iii是气体体积不变的反应,增大压强时平衡正向移动,
CO 的平衡转化率增大,甲醇选择性增大,一氧化碳转化率减小,且甲醇选择性和一氧化碳选择性之和为1
2
0.0017
【解析】(1)①已知CO 是共价化合物,故CO 的电子式为 ;
2 2
②决速步骤指反应历程中反应速率最慢的反应,反应速率快慢由反应的活化能决定,活化能越大,反应速
率越慢,由反应历程图中数据可知,活化能=过渡态能量-起始态能量,各个步骤中活化能分别为:0.7eV、
0.8eV、0.2eV、0.2eV、0.7eV、(1.4-m)eV,其中最大的数值为[-0.1-(-0.9)]eV=0.8eV,该步骤的反应方程式为
93
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司3 3
CO*(g)+2H (g)=HCO*(g)+ H *(g),故答案为:CO*(g)+2H (g)=HCO*(g)+ H *(g);
2 2 2 2
2 2
③反应i CO(g)+2H (g)⇌CH OH(g)ΔH =-91.5kJ/mol,由图可知,1molCO(g)和2molH 的总能量与CH OH(g)
2 3 1 2 3
的总能量之差为91.5kJ,反应历程图中的E表示的是1个CO分子和2个H 分子的相对总能量与1个
2
91.5
CH OH分子的相对总能量之差为meV,相对总能量E═meV= ≈0.95eV,即m=0.95,故
3 6.0210231.61022
答案为:0.95eV;
(2)由图可知,曲线M的Rlnk随T的增大减小幅度大,曲线N的Rlnk随T的增大减小幅度小,即温度
一定时二者的活化能不相等,催化剂能降低反应的活化能,所以曲线N实验可能改变的外界条件是加入了
高效催化剂,故答案为:加入了高效催化剂;
(3)①反应ii是气体体积减小的反应,反应iii是气体体积不变的反应,增大压强时平衡正向移动,CO
2
的平衡转化率增大,CH OH(g)的选择性增大,CO的选择性减小,并且CH OH(g)的选择性增和CO的选择
3 3
性之和为100%,所以曲线n表示CO 的平衡转化率,曲线m表示CH OH(g)的选择性,曲线n表示CO(g)
2 3
的选择性,故答案为:m;反应ii是气体体积减小的反应,反应iii是气体体积不变的反应,增大压强时平
衡正向移动,CO 的平衡转化率增大,甲醇选择性增大,一氧化碳转化率减小,且甲醇选择性和一氧化碳选
2
择性之和为1;
②由题干图像信息可知,15s末CO 的浓度为0.3mol/L,CO的浓度为0.175mol/L,由三段式分析可知:
2
CO g +3H g ƒ CH OHg+H Og
2 2 3 2
起始浓度(mol/L) 0.5
转化浓度(mol/L)
15s末浓度(mol/L) 0.3
CO g +H g ƒ COg+H Og
2 2 2
起始浓度(mol/L) 0.5 0
,则15s内CH OH的浓度变化量为
转化浓度(mol/L) 0.175 3
15s末浓度(mol/L) 0.3 0.175
0.5-0.3-0.175=0.025mol/L,故0~15s时间段内,CH OH的平均反应速率为
3
c 0.025mol/L
=0.0017mol·L−1·s−1,故答案为:0.0017。
t 15s
预测3
【答案】(1)CO (g)+3H (g)ƒ CH OH(g)+H O(g) ∆H =-49.4kJ∙mol-1 低温
2 2 3 2 1
(2)正向
(3)n 24% 0.088
(4)减小 随温度升高,Kp减小使v减小的程度大于k增大使v增大的程度
【解析】(1)某温度下,利用CO 生产甲醇主要涉及以下两个反应:
2
反应I._______
反应Ⅱ.CO (g)+H (g)ƒ CO(g)+H O(g) ΔH =+41.2kJ·mol-1
2 2 2 2
94
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司已知反应:CO(g)+2H (g)ƒ CH OH(g) ΔH =–90.6kJ·mol-1。利用盖斯定律,将反应Ⅱ+已知反应,可得反
2 3 3
应I的的热化学方程式为CO (g)+3H (g)ƒ CH OH(g)+H O(g) ∆H =(+41.2kJ·mol-1)+( –
2 2 3 2 1
90.6kJ·mol-1)=-49.4kJ∙mol-1,该反应为气体体积缩小的放热反应,在低温条件下反应I可自发发生。
(2)若在恒压条件下密闭容器中发生反应I和Ⅱ,平衡后再充入惰性气体,则混合气的体积增大,各物质
的浓度减小,相当于原平衡体系减压,反应I的平衡逆向移动,H 的物质的量增大,H O(g)的物质的量减
2 2
小,对反应Ⅱ来说,相当于增大反应物浓度,同时减小生成物浓度,则反应Ⅱ平衡将正向移动。
(3)增大压强,反应Ⅰ的平衡正向移动,CH OH的选择性增大,此时H 的物质的量减小,H O(g)的物质
3 2 2
的量增大,反应Ⅱ的平衡逆向移动,CO的选择性减小,由于反应Ⅰ占主导地位,所以总的来说,CO 的平
2
衡转化率增大,因此图中m表示CH OH的选择性曲线,p表示H 的选择性曲线,表示CO 的平衡转化率
3 2 2
的曲线是n。
采集图中数据,可得出压强为1.5MPa时,将1molCO (g)和3molH (g)充入密闭容器发生反应I和Ⅱ,并达
2 2
到平衡状态,CO 的平衡转化率为30%,CO的选择性为30%,则CH OH的选择性为70%,由此可建立如
2 3
下三段式:
CO (g) 3H (g) ƒ CH OH(g) H O(g)
2 2 3 2
起始量(mol) 1 3 0 0
变化量(mol) 10.30.7 0.213 0.21 0.21
平衡量(mol) 0.7 2.28 0.21 0.3
CO (g) H (g) ƒ CO(g) H O(g)
2 2 2
起始量(mol) 1 3 0 0
变化量(mol) 10.30.3 0.09 0.09 0.09
平衡量(mol) 0.7 2.28 0.09 0.3
0.72mol
A点时H 的转化率为 100%=24%,CH OH的平衡分压为
2 3
3mol
0.21mol
1.5MPa≈0.088MPa。
(0.72.280.210.090.3)mol
(4)因为ΔH=–41.2kJ·mol-1<0,所以温度升高时,平衡逆向移动,CO催化变换反应的K 减小。根据速率
p
方程分析,升高温度,k增大,可使v增大,升高温度可使K 减小,K 减小可使v减小。T>T 时v逐渐
p p m
减小,表明K 减小对v的影响更大,原因是: 随温度升高,Kp减小使v减小的程度大于k增大使v增大
p
的程度。
预测4
【答案】(1)-59.7
338
(2) XeF 5
2 a2bN 1030
A
(3) < 减小 97.8% 36
【解析】(1)XePtF 的晶格能为458.7kJmol-1,则Xe+形成1molXePtF 晶体的热化学方程式:
6 6
Xe+g+PtF-g=XePtF sΔH=-458.7kJmol-1;Xe的第一电离能为1170.0kJmol1,则
6 6
95
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司Xe(g)=Xe+gΔH=+1170.0kJmol-1;根据盖斯定律,
Xeg+PtF g=XePtF sΔH=(-458.7+1170.0-771.0)kJmol-1 59.7kJmol-1
6 6
1 1
(2)图中大球的个数为8× +1=2,小球的个数为8× +2=4,根据粒子半径的大小判断大球应为Xe原子、
8 4
小球应为F原子,大球与小球个数比是1:2,则晶胞的化学式为XeF ;中心原子的价层电子对数为2+
2
812 2M
=5;该晶胞中含有2个XeF 分子,故晶胞的质量为m= g,晶胞的体积为V=a2b×10-30cm3,则密
2 2 N
A
m 2169 338
度为ρ= = g/cm3;
V N a2b10-30 N a2b10-30
A A
(3)①根据表格数据,第一个反应的温度升高,平衡常数K减小,说明平衡往逆向移动,该反应为放热
反应,故ΔH <0;根据表格中的三个方程式,F 比例越大,越容易转化为XeF 或XeF ,所以应该减小投料
1 2 4 6
中F /Xe的比值;
2
②根据反应i、ii、iii,达到平衡时,反应的F 物质的量为:n(F )3.6019.8020.36344.28mol,则F
2 2 2
44.28mol
平衡转化率 F 100%97.8%;
平 2 45.28mol
已知,达到平衡时,各物质总物质的量n =[3.60+19.80+0.36+(45.28-44.28)+(23.77-23.76)]mol=24.77mol,反
总
0.36
2.477103kPa
24.77
p
XeF6
100kPa
pθ
应III的平衡常数Kθ(III)= 36kPa。
p p p 3 0.01 1 3
Xe F2 2.477103kPa 2.477103kPa
pθ
pθ
24.77
24.77
100kPa 100kPa
预测5
【答案】(1)H H H
3 2 1
4 1
(2)
5Vt 2V
(3)BC
(4) c CrSCN 2 c CrSCN 2 c Cr3 74 1 .1 (或 K 1 ) C点 CrSCN 2 与 CrSCN 2
1
浓度相等,K 2 c SC 1 N,代入反应ⅳ,求得c CrSCN 2 5.7c Cr3 ,由
c Cr3 c CrSCN 2 c CrSCN c CrSCN x-3- 0.2molL1,求得
2 x
c Cr3
0.2a12.4
molL10.0162molL1,因此C点对应的溶液不能用于该电镀工艺
【解析】(1)由盖斯定律可知ⅲ-ⅰ-ⅱ得反应2H SgS g2H g,故H H H H ;
2 2 2 4 3 2 1
96
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(2)2H SgS g2H g,ts时H 的产率为40%,则0~ts内H S的平均分解速率为
2 2 2 2 2
240% 4
molL1s1= molL1s1;H S充分分解达到平衡时,容器中H S和H 的分压相等,由方程式
Vt 5Vt 2 2 2
可知,平衡时硫化氢、氢气的物质的量相等,均为2mol÷2=1mol,同时生成S 为1mol÷2=0.5mol,则则该温
2
1 2 0.5
V V 0.5 1
度下的平衡常数K = = ;
1 2 V 2V
V
(3)A.加水稀释后,离子浓度减小,促使平衡向生成离子数多的方向移动,溶液中离子的总数增大,A
错误;
B.加入少量FeCl 固体,根据铬元素守恒,溶液中含铬微粒总数不变,B正确;
3
C.ⅳ.Cr3 SCN ƒ CrSCN 2
ⅴ.CrSCN 2 SCN ƒ CrSCN
2
由盖斯定律可知,ⅳ+ⅴ得反应Cr3 2SCN ƒ CrSCN ,则其平衡常数K K K ,C正确;
2 3 1 2
c
CrSCN
2
c
SCN
1
D.K 1 c C r3 c SC N , c CrSCN 2 = K 1 c Cr3 ,溶液中c Cr3 减小,SCN与 CrSCN 2 浓度
的比值增大,D错误;
故选BC;
(4)①ⅳ.Cr3 SCN ƒ CrSCN 2 K 74.1
1
ⅴ.CrSCN 2 SCN ƒ CrSCN K 13.0
2 2
由平衡常数可知,初始生成
CrSCN
2 的进行程度更大,结合图可知,Ⅰ、Ⅱ、Ⅲ分别为Cr3、
CrSCN
2 、
CrSCN 的曲线,由图可知,当 c SCN 0.05molL1时,图中含铬微粒按浓度由大到小的顺序为
平
2
c
CrSCN
2
c
CrSCN
c Cr3 ;A点时,c
CrSCN
2
=c Cr3 ,
2
c
CrSCN
2
1 1 1
K = 74.1,溶液中SCN的平衡浓度为 (或 )。
1 c Cr3 c SCN c SCN 74.1 K 1
1
②C点 CrSCN 2 与 CrSCN 2 浓度相等, K 2 c SCN,代入反应ⅳ,求得
c
CrSCN
2
5.7c Cr3 ,由
c Cr3 c CrSCN 2 c CrSCN c CrSCN x-3- 0.2molL1,求得
2 x
97
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司c Cr3
0.2a12.4
molL10.0162molL1,因此C点对应的溶液不能用于该电镀工艺。
名师押题
押题1
【答案】(1)-577 高温
(2)0.4 80% 2.7
(3)曲线b 温度低于500℃时,反应③和反应④几乎不发生或者反应④正向进行的程度是反应③的
两倍
【解析】(1)298K时,18g气态水转化为液态水释放出44kJ的能量;H S(g)的标准摩尔燃烧焓(△H)为
2
-586kJ·mol-1,可得:⑤H Og=H OlΔH =-44kJmol1;
2 2 5
3
⑥H Sg+ O g=H OlSO gΔH =-586kJmol-1;
2 2 2 2 2 6
3
COS(g)的标准摩尔燃烧焓的反应为:COSg+ O g=CO g+SO gΔH ;根据盖斯定律可知,该反应
2 2 2 2 7
可由⑥-①-⑤得到,则
ΔH ΔH ΔH ΔH (-586kJmol-1)(35.00kJmol1)(-44kJmol1)577kJmol-1;反应②正向气体
7 6 1 5
分子数增加,ΔS>0,该反应可由③+2×④得到,则该反应
ΔHΔH +2ΔH (171.58kJmol-1)2(41.20kJmol1)253.98kJmol-1,H0,则反应在高温条件
3 4
下能自发进行。
(2)由反应可知①和④反应前后气体分子数相等,则反应前后不会导致压强变化,②和③反应前后气体
分子数均增加,且增加量恰好等于生成的S (g)的物质的量,根据压强之比等于气体物质的量的之比可得,
2
反应后体系内压强的增加量即为S (g)的分压,则p(S )210kPa-200kPa=10kPa,S (g)的平均反应速率为
2 2 2
10kPa
0.4kPamin1;
25min
设起始时CO (g)和H S(g)的物质的量均为1mol,则两者的起始分压均为100kPa,平衡时,测得体系总压强
2 2
为230kPa,则平衡时气体的物质的量之和为2.3mol,结合以上分析可得n (S )=0.3mol,其平衡分压为30
2
kPa,设平衡时n(H )=x,则n(COS)=x, n(CO )=2x,根据S原子守恒可得:2n(S )+ n(COS)+ n(H S) = n(H S)
2 2 2 2 平衡 2
,得n(H S) =(1-x-0.3×2)=(0.4-x)mol;根据氢原子守恒可得:2n(H S) +2n(H O)+2n(H )= 2n(H S) ,
初始 2 平衡 2 平衡 2 2 2 初始
则得2(0.4-x)+2 n(H O)+2x=2:解得:n(H O)=0.6mol,根据C原子守恒得:n(COS)+ n(CO ) + n(CO)= n(CO )
2 2 2 平衡 2
,可得:n(CO)=(1-3x)mol,在结合O原子守恒:n(COS)+ 2n(CO ) + n(CO)+ n(H O)= 2n(CO ) ,解
初始 2 平衡 2 2 初始
得:x=0.2,则平衡时各气体的物质的量:n(CO )=0.4 mol,n(COS)=0.2 mol,n(CO)=0.4 mol,n (S )=0.3mol,
2 2
n(H O)=0.6 mol,n(H S)=0.2 mol, n(H )=0.2 mol,总气体为2.3mol;此时H S(g)的平衡转化率为
2 2 2 2
98
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司 p 2 p 2 p
CO H2O S2
10.2 pΘ pΘ pΘ
100%80%;反应②的标准平衡常数KΘ =
1 p 2 p 2
CO2 H2S
pΘ
pΘ
0.4 2 0.6 2 00.3
p p p
2.3
总
2.3
总
2.3
总
pΘ pΘ pΘ
=2.7;
0.2 2 0.4 2
p p
2.3
总
2.3
总
pΘ pΘ
(3)①由反应可知COS只在反应①中生成,且该反应同时生成等量的水,而水在①②④中均生成,则
相同条件下,H O的选择性高于COS的选择性,故曲线b表示COS的选择性;
2
②温度低于500℃时,反应③和反应④几乎不发生或者反应④正向进行的程度是反应③的两倍,从而使
H S的转化率与CO 的相等。
2 2
押题2
【答案】(1)E 90
a
15
(2)AD 62.5 0.00046或4.6104
t
(3) a T ℃、9105Pa 210℃、PPa
1 0
nCO nCO
(4) 增大,与CO反应的H 变多,与CO 反应的H 变少,所以CO 降低, 增大,更
nCO 2 2 2 2 nCO
2 2
有利于反应ⅲ的正向进行,产生CH OH变多,所以升高
3
【解析】(1)由盖斯定律可知,反应ⅰ-反应ⅱ可得反应ⅲ,则
COg2H gƒ CH OHg ΔH =ΔH -ΔH 49kJmol141kJmol1 90kJmol1=正反应活化能-逆
2 3 3 1 2
反应活化能,已知反应ⅲ正反应的活化能为EkJmol1,则其逆反应的活化能为E +90kJmol1。
a a
(2)①A.v CO v H O说明正逆反应速率相等,说明反应达到平衡,A选;
消耗 2 消耗 2
B.一定温度下,平衡常数是定值,平衡常数不再发生变化,不能说明反应达到平衡,B不选;
C.该反应过程中气体总质量和总体积是定值,混合气体的平均密度是定值,当气体密度不再改变,不能说
明反应达到平衡,C不选;
D.测得CO的浓度保持不变,说明正逆反应速率相等,说明反应达到平衡,D选;
故选AD;
②根据已知条件列出“三段式”
99
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司CO g 3H g ƒ CH OHg H Og
2 2 3 2
起始mol 1 3 0 0
转化mol x 3x x x
平衡mol 1x 33x x x
CO g + H g ƒ COg + H Og
2 2 2
起始mol 1-x 3-3x 0 x
转化mol y y y y
平衡mol 1-x-y 3-3x-y y x+y
COg + 2H g ƒ CH OHg
2 3
起始mol y 3-3x-y x
转化mol z 2z z
平衡mol y-z 3-3x-y-2z x+z
4-2x-2z 150
若起始压强为200MPa,反应经tmin后达到平衡,此时体系压强为150MPa,则 = ,H O的分
4 200 2
x+y
压:pH O40MPa= 150Mpa,x+y=0.8mol,x+z=0.5mol,y-z=0.3mol,p(CH OH)=
2 4-2x-2z 3
x+z 0.5 1-x-y 0.2
150MPa 150MPa=25MPa,p(CO )= 150MPa 150MPa=10MPa,p(H )=
2 2
3 3 3 3
3-x+y-2x+z 1.2
150MPa 150MPa=60MPa,则tmin内反应的平均速率
3 3
0.3
150MPa 15 0.5mol
vCO 3 = MPa/min。CH OH的选择性为 100%=62.5%,反应ⅰ的平衡常数
t 3 0.8mol
tmin
0.5
40 150
3
K
p
1.2 3 0.2
0.00046或4.6104。
150 150
3 3
(3)反应ⅰ是气体体积减小的反应,恒温条件下增大压强,平衡正向移动,xCH OH增大,则图中对应
3
恒温过程的曲线是a,对应恒压过程的曲线是b,设起始物n(H )=3mol,n(CO )=1mol,平衡时二氧化
2 2
1 2
碳的物质的量为1mol- mol = mol,氢气的物质的量为3mol-1mol=2mol,CH OH和H O的物质的量为
3 3 3 2
1
mol
1 mol,气体的总物质的量为 1 mol+ 1 mol+ 2 mol+2mol= 10 mol,xCH OH= 3 =0.1,由图可知,反应
3 3 3 3 3 3 10
mol
3
条件可能为:T ℃、9105Pa或210℃、PPa。
1 0
nCO
(4)CO 、呈现该变化的趋势的原因是: 增大,与CO反应的H 变多,与CO 反应的H 变
2 nCO 2 2 2
2
nCO
少,所以CO 降低, 增大,更有利于反应ⅲ的正向进行,产生CH OH变多,所以升高。
2 nCO 3
2
100
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司押题3
【答案】(1)2NO(g)+ 2CO(g)=N (g)+2CO (g) △H=-748kJ/mol AC
2 2
(2) 24N 85.6% [Co(NH ) ]2+被氧化为[Co(NH ) ]3+,[Co(NH ) ]3+对NO的配位能力极低
A 3 6 3 6 3 6
(3)NO+5e—+5H+=NH +H O 15:2
3 2
【解析】(1)①由题意可知,碳燃烧的热化学方程式为C(s) +O (g)= CO (g) △H=—393kJ/mol,由盖斯定律
2 2
可知,反应b—a—c得到反应2NO(g)+ 2CO(g)=N (g)+2CO (g),则反应
2 2
△H=(—393kJ/mol)—(+182.6kJ/mol)—(+172.4kJ/mol)=-748kJ/mol;
②A.由质量守恒定律可知,反应前后气体的质量相等,则1L的恒温密闭容器Ⅰ和绝热密闭容器Ⅱ中混合
气体密度相等,故正确;
B.该反应为放热反应,则恒温密闭容器Ⅰ中反应温度小于绝热密闭容器Ⅱ,升高温度,平衡向逆反应方向
移动,一氧化氮的转化率减小,则一氧化氮转化率α 大于α ,故错误;
Ⅰ Ⅱ
C.该反应为放热反应,则恒温密闭容器Ⅰ中反应温度小于绝热密闭容器Ⅱ,升高温度,平衡向逆反应方向
移动,化学平衡常数减小,则反应平衡常数K 大于K ,故正确;故选AC;
Ⅰ Ⅱ
(2)①[Co(NH ) ]3+离子中配位键属于σ键、氮氢键属于σ键,则1mol[Co(NH ) ]3+离子中含有σ键的数目
3 6 3 6
1mol×24×N mol—1=24N ;
A A
②由题给信息可知,反应消耗一氧化氮的物质的量为
2×10—4m3/min×300min×2×10—2mol/m3×60%=0.00072mol,则钴氨溶液中[Co(NH ) ]2+有效含钴率为
3 6
0.01mol/L1L-0.00072mol2
×100%=85.6%;
0.01mol/L1L
③由图可知,前16h内钴氨溶液吸收NO的能力不断下降的原因是[Co(NH ) ]2+被氧化为[Co(NH ) ]3+,
3 6 3 6
[Co(NH ) ]3+对NO的配位能力极低;
3 6
(3)①由图可知,当电解电压为U 时,催化电解一氧化氮生成氨气的电极为阴极,酸性条件下一氧化氮
2
在阴极得到电子发生还原反应生成氨气和水,电极反应式为NO+5e—+5H+=NH +H O;
3 2
②由图可知,当电解电压为U 时,氢气和氨气的法拉第效率分别为60%和20%,则电解生成的氢气和氨气
1
60%Q 20%Q
的物质的量之比为 总: 总 =15:2。
2 5
押题4
【答案】(1)+133kJ/mol 反应ⅱ为反应Ⅰ的决速步,c(CO )增大,反应ii速率加快,从而提高反应I
2
速率
(2)温度低于800℃时,反应物的转化率不够高,温度高于800℃时,C H 选择性下降较为明显,而800℃
2 4
时反应物的转化率和C H 选择性都相对较高,有利于提高C H 的产率
2 4 2 4
(2-x)3
(3) >
4x2
【解析】(1)①由盖斯定律可知,反应Ⅰ—ii可得反应i,则反应∆H =(+177kJ/mol)—(+44kJ/mol)=
1
+133kJ/mol;
101
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司②化学反应速率取决于慢反应,由题意可知,反应i是快反应,反应ⅱ为慢反应,反应ⅱ是反应Ⅰ的决速
步,增大二氧化碳的浓度,反应ii速率加快,从而提高反应I速率,所以相比于增大乙烷的浓度,增大二氧
化碳的浓度对反应Ⅰ速率影响更大;
(2)由图可知,温度低于800℃时,反应物的转化率不够高,温度高于800℃时,乙烯选择性下降较为明显,
而800℃时乙烷的转化率和乙烯选择性都相对较高,有利于提高乙烯的产率,所以工业生产中综合各方面的
因素后,反应选择800℃,故答案为:温度低于800℃时,反应物的转化率不够高,温度高于800℃时,C H
2 4
选择性下降较为明显,而800℃时反应物的转化率和C H 选择性都相对较高,有利于提高C H 的产率;
2 4 2 4
k
(3)由反应达到平衡时,正逆反应速率相等可得:k c2(CH ) =k c(C H )c2(H ),整理可得: 正 =
正 4 逆 2 4 2 k
逆
cC H c2H
2 4 2 ,由图可知,平衡时甲烷的物质的量为xmol,由方程式可知,乙烯、氢气的物质的量分别
c2CH
4
0.5(2-x) 2-x
( )2
为0.5(2—x)mol、(2—x)mol,则 k 正 = 2 2 = (2-x)3 ;该反应为吸热反应,升高温度,平衡向正
k
逆 (
x
)2
4x2
2
反应方向移动,正反应速率大于逆反应速率,则正反应速率常数增大的倍数m大于逆反应速率常数增大的
(2-x)3
倍数n,故答案为: ;>。
4x2
押题5
【答案】(1)低温
3
(2)CO*(g)+2H (g)=HCO*(g)+ H (g)
2 2
2
(3)BD
(4) 553K 升高温度促进反应ⅱ平衡正向移动的程度大于促进反应ⅰ平衡逆向移动的程度 n 4
5
48
【解析】(1)由盖斯定律可知,反应ⅰ-反应ⅱ可得反应ⅲCOg2H gƒ CH OHg
2 3
ΔH ΔH ΔH -49.6kJ/mol-41.2kJ/mol=-90.8kJ/mol,该反应是气体体积减小的反应,S0,
3 1 2
ΔH-TΔS<0时反应能自发进行,则反应ⅲ在低温条件下能自发进行。
3
(2)CO*(g)+2H (g)=HCO*(g)+ H (g)的活化能最大,反应速率最慢,故为决速步。
2 2
2
(3)A.减小H 的浓度,反应ⅰ和反应ⅱ逆向移动,CO 的转化率减小,A错误;
2 2
B.上述CO 和H 合成CH OH涉及的三个反应过程中气体总质量不变,总物质的量减小,气体的平均相对
2 2 3
分子质量增大,当气体的平均相对分子质量保持不变时,说明反应体系已达平衡,B正确;
C.反应ⅰ是气体体积减小的反应,则体系达平衡后,若压缩体积,则反应ⅰ平衡正向移动,水蒸气浓度增
大,导致反应ⅱ平衡逆向移动,C错误;
102
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司D.选用合适的催化剂可以增大反应速率,可以提高CH OH在单位时间内的产量,D正确;
3
故选BD。
a
(4)①由题意可知,起始二氧化碳的物质的量为 mol,由图中数据可知,473K、513K、553K时,甲醇
4
a a
的物质的量分别为 mol×13.6%×86%≈0.029amol、 mol×15%×78%≈0.029amol、
4 4
a
mol×20%×60%=0.03amol,则553K条件下反应达到平衡时,反应体系内甲醇的产量最高;
4
②反应ⅰ为放热反应,反应ⅱ为吸热反应,CO 的平衡转化率随温度升高而增大的原因是:升高温度促进
2
反应ⅱ平衡正向移动的程度大于促进反应ⅰ平衡逆向移动的程度;
③反应ⅰ正反应为放热反应,升高温度平衡逆向移动,则平衡常数减小,而反应ⅱ正反应为吸热反应,升
1
高温度平衡正向移动,则平衡常数增大,即反应ⅰ的lnK 随着 增大而减小,即随着T的降低而增大,反
p
T
1
应ⅱ的lnK 随着 的增大而增大,即随着T的降低而减小,结合题干图示可知,反应ⅱ对应图2中n;
p
T
pCH OH
④通过调整温度可调控平衡时 3 的值,A点对应温度下,反应ⅰ和反应ⅱ的压力平衡常数相等,
pCO
pCH OHpH O pCOpH O pCH OH pCH OH
即 3 2 = 2 ,即得p2H 3 ,平衡时 3 16,则pH 4kPa;
pCO p3H pCO pH 2 pCO pCO 2
2 2 2 2
⑤根据已知条件列出“三段式”
CO g 3H g ƒ CH OHg H Og
2 2 3 2
起始mol 1 3 0 0
转化mol x 3x x x
平衡mol 1-x 3-3x x x
CO g H g ƒ COg H Og
2 2 2
起始mol 1-x 3-3x 0 x
转化mol y y y y
平衡mol 1-x-y 3-3x-y y y+x
CO 的转化率为80%,则x+y=0.8,y=0.8-x,图中B点反应ⅱ的平衡常数lnK =0,即K =1.00,则
2 p p
0.8 0.5
0.80.8-x 3.0 10kPa 3.0 10kPa 5
=1,解得x=0.5mol,y=0.3,故有反应ⅰ的K = = kPa2。
0.22.2-2x p 0.2 1.2 3 48
10kPa 10kPa
3.0 3.0
103
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司