文档内容
{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}绝密★启用前(广东卷)
化学参考答案
1.【答案】C
【解析】A项,纸的主要成分是纤维素,属于有机高分子材料;B项,粤绣中的“线”有棉麻的,主要成分是
纤维素,属于有机高分子材料,也有是丝毛的,主要成分是蛋白质,也属于有机高分子材料;C项,香油的主
要成分是油脂,不是有机高分子材料;D项,“藤”的主要成分是纤维素,属于有机高分子材料。
2.【答案】B
【解析】GaP、GaAs均为无机非金属材料,金属材料包括纯金属和合金,B项错误。
3.【答案】B
【解析】光导纤维主要成分的化学式为SiO ,无分子式,A项错误;PCl 的中心原子为sp3杂化,有3个方向
2 3
形成共价键,一个方向有一对孤电子对,价层电子对互斥模型为 ,B项正确;C原子编号错误,名称应
该是4-甲基-2-戊烯,C项错误;Co原子失去4s上的2个电子,变成Co2+,D项轨道表示式错误。
4.【答案】D
【解析】腐蚀电路板上的Cu,利用的是FeCl 溶液的氧化性,A项不符合题意;Mg2+是活泼金属的阳离子,在
3
水溶液中Mg2+难得到电子转化为单质镁,工业上常采用电解熔融的MgCl 制备单质镁,B项不符合题意;作干
2
燥剂是利用了浓硫酸的吸水性,C项不符合题意;等离子体含有能自由移动带电粒子,可应用于化学合成和材
料表面改性,D项符合题意。
5.【答案】C
【解析】氮氧化物在空气中可形成硝酸型酸雨,A项正确;氨气是sp3杂化,有一个杂化轨道上是孤对电子,
甲烷是也是sp3杂化,但四个杂化轨道全部参与成键,所以氨气分子的键角小于甲烷的键角,B项正确;该反应
的氧化产物和还原产物的质量比为4∶3,C项错误;NaNO 和NaNO 都不是NO 对应的盐(N的价态不同),
3 2 2
所以题中反应能说明NO 不是酸性氧化物,D项正确。
2
6.【答案】D
【解析】水垢中的的主要成分碳酸钙和氢氧化镁被醋酸溶解,A正确;SO 能杀菌且能防止营养物质被氧化,B
2
正确;碱性条件下,油脂能发生皂化反应,C正确;高温不利于提高氨气的平衡产率,D错误。
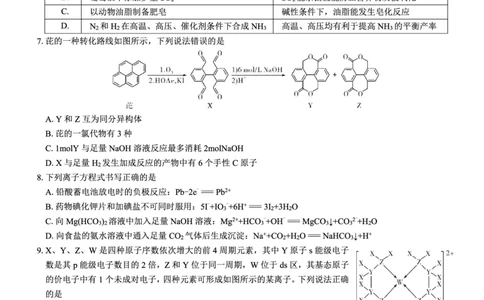
7.【答案】D
【解析】Y和Z只是碳氧双键的位置不同,互为同分异构体,A项正确;芘的一氯代物有3种,如图所示,B
项正确;Y与NaOH溶液反应,酯基先水解,生成了羧基和(醇)羟基,(醇)羟基不与NaOH反应,故1molY
与足量NaOH溶液反应最多消耗2molNaOH,C项正确;X与足量H 发生加成反应的产物中只有4个手性C
2
原子,D项错误。
化学参考答案(广东卷)第 1 页 (共 7 页)
{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}1
2
3
8.【答案】B
【解析】A 项的离子方程式为 Pb-2e-+SO 2-=PbSO ↓;C 项的离子方程式为 Mg2++2HCO -+4OH-=
4 4 3
Mg(OH) ↓+2CO 2-+2H O;D项的离子方程式为CO +NH ·H O+Na+=NaHCO ↓+NH +。
2 3 2 2 3 2 3 4
9.【答案】C
【解析】X为H,Y为C,Z为N,W为Cu元素,第二周期中的F和Ne的第一电离能都比Z要大,A项错误;
离子中的C和N原子都是sp3杂化,B项错误;W的配位数是4,配体数是2,配体种类是1,C项正确;W带
2个单位正电荷,是Cu2+,第三层是最外层,最外层电子数不是1,D项错误。
10.【答案】C
【解析】Fe作原电池的负极,电极上发生反应:Fe-2e-=Fe2+,Fe2++H S=FeS↓+2H+;碳作正极,电极反
2
应为O +4H++4e-=2H O,A、B项正确;通入空气是提供O ,O 不能增强电解质溶液的导电性,C项错误;
2 2 2 2
生成的FeS沉淀会附着在铁碳填料的表面,负极的表面积减小,反应速率减小,形成的微电池数量也在减小,
故工作一段时间后,H S的去除效率会降低,D项正确。
2
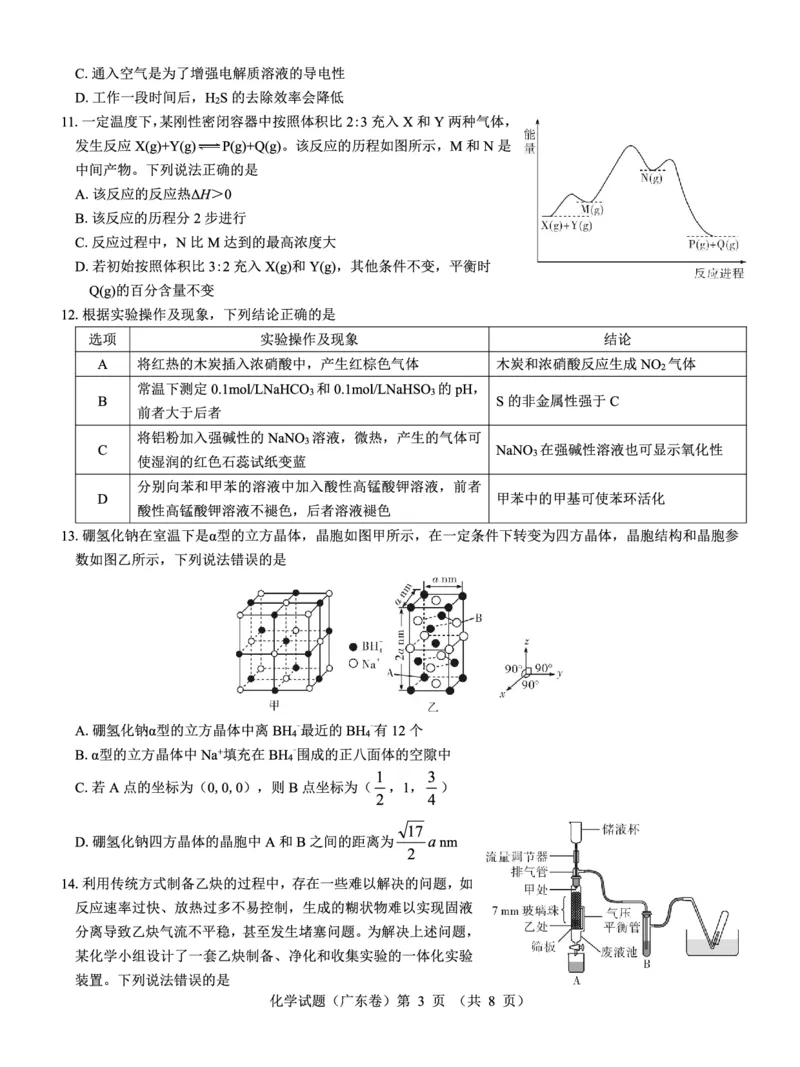
11.【答案】D
【解析】反应物总能量高于生成物,该反应为放热反应,ΔH<0,A项错误;图中有3个峰,则该反应的历程
分3步进行,B项错误;图中可知,中间产物N的能量比M的能量高,M(g)→N(g)活化能较高,为慢反应,
N(g)→P(g)+Q(g)活化能较低,为快反应,则反应过程中,M的最高浓度比N的大,C项错误;该反应是前后气
体分子数不变的反应,按照体积比3:2充入X(g)和Y(g),平衡时Q(g)的百分含量不变,D项正确。
12.【答案】C
【解析】产生的NO 气体也可能是浓硝酸受热分解生成的,A项错误;可以说明酸性:H SO >H CO ,但不能
2 2 3 2 3
说明非金属性:S>C,因为H SO 不是S的最高价含氧酸,B项错误;产生的气体是氨气,说明NaNO 在强
2 3 3
碱性溶液也显示氧化性,C项正确;实验说明甲苯中的苯环可使甲基活化,D项错误。
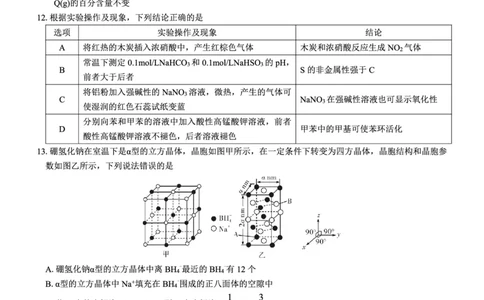
13.【答案】D
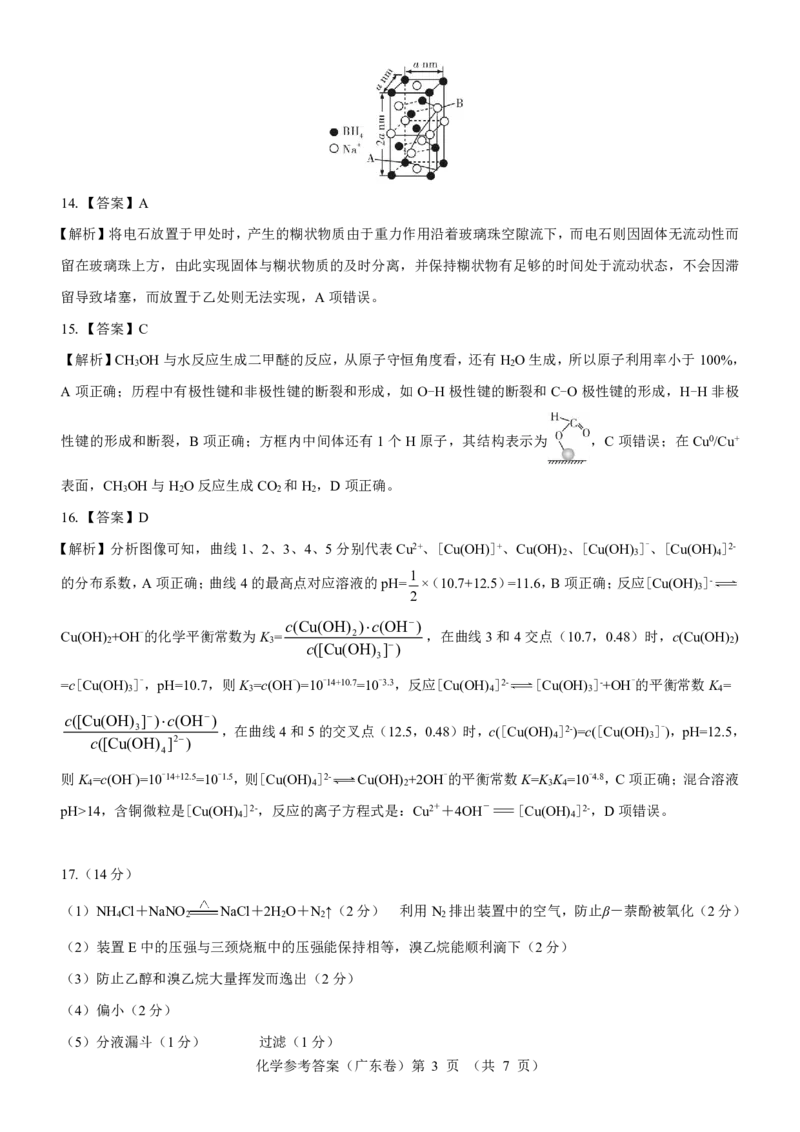
【解析】取甲图晶胞体心的BH -分析,离该BH -最近的BH -上中下层各有4个,共12个,A项正确;晶体是
4 4 4
由很多晶胞无隙并置组成的,Na+恰好填充在6个BH -围成的正八面体的空隙中,B项正确;根据原子的投影
4
1 3
容易判断B点坐标为( ,1, ),C项正确;如图所示,在四方晶体的晶胞中构造一个直角三角形,运用
2 4
3 1 14
几何相关知识可得AB2=(2a )2 a2 ( a)2,则AB= a(nm),D项错误。
4 2 2
化学参考答案(广东卷)第 2 页 (共 7 页)
{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}14.【答案】A
【解析】将电石放置于甲处时,产生的糊状物质由于重力作用沿着玻璃珠空隙流下,而电石则因固体无流动性而
留在玻璃珠上方,由此实现固体与糊状物质的及时分离,并保持糊状物有足够的时间处于流动状态,不会因滞
留导致堵塞,而放置于乙处则无法实现,A项错误。
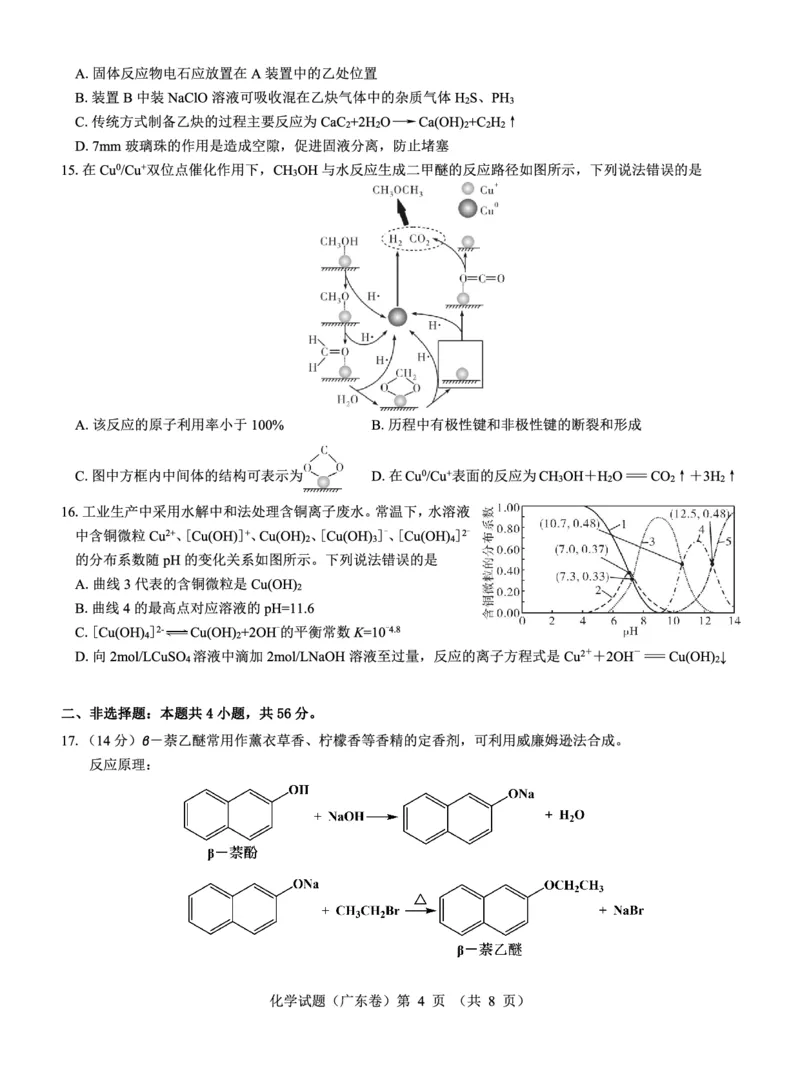
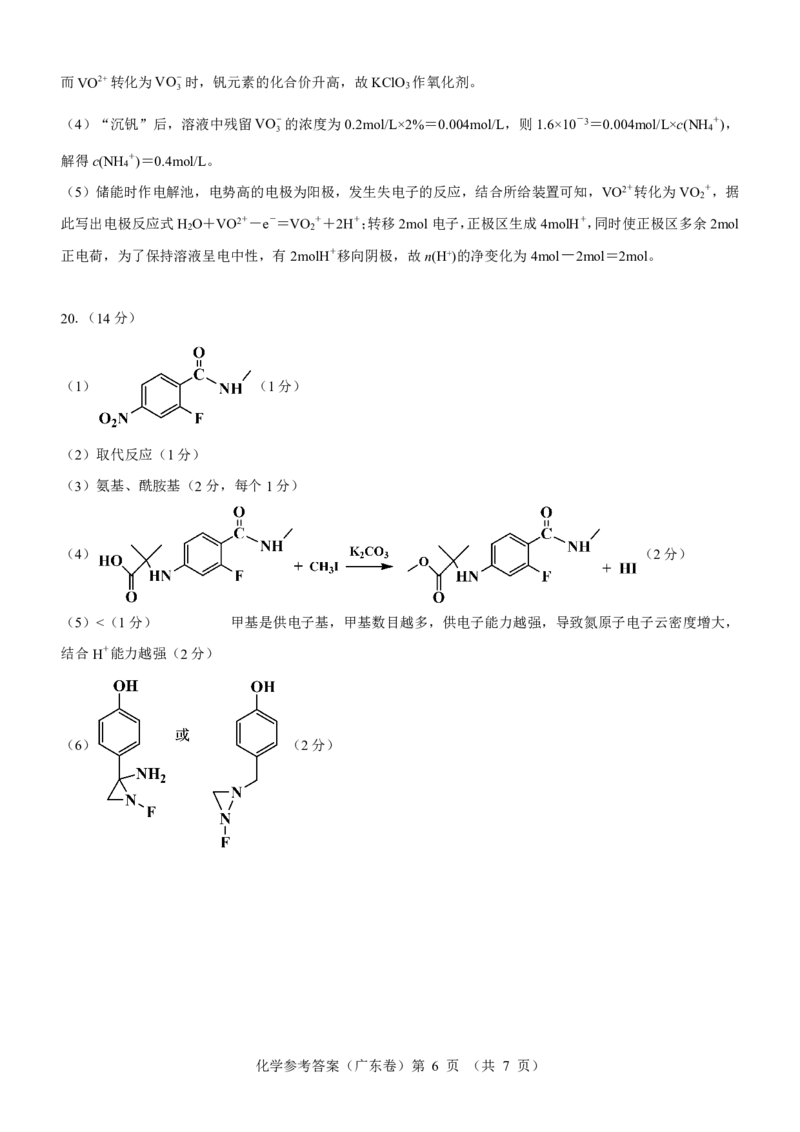
15.【答案】C
【解析】CH OH与水反应生成二甲醚的反应,从原子守恒角度看,还有H O生成,所以原子利用率小于100%,
3 2
A项正确;历程中有极性键和非极性键的断裂和形成,如O-H极性键的断裂和C-O极性键的形成,H-H非极
性键的形成和断裂,B项正确;方框内中间体还有1个H原子,其结构表示为 ,C项错误;在Cu0/Cu+
表面,CH OH与H O反应生成CO 和H ,D项正确。
3 2 2 2
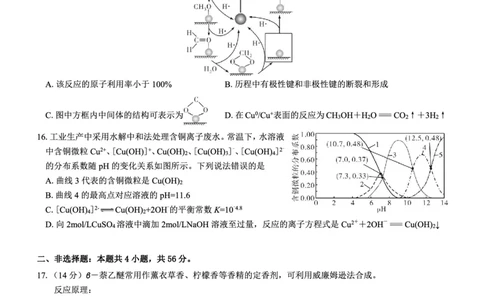
16.【答案】D
【解析】分析图像可知,曲线1、2、3、4、5分别代表Cu2+、[Cu(OH)]+、Cu(OH) 、[Cu(OH) ]-、[Cu(OH) ]2-
2 3 4
1
的分布系数,A项正确;曲线4的最高点对应溶液的pH= ×(10.7+12.5)=11.6,B项正确;反应[Cu(OH) ]-
3
2
c(Cu(OH) )c(OH)
Cu(OH) +OH-的化学平衡常数为K = 2 ,在曲线3和4交点(10.7,0.48)时,c(Cu(OH) )
2 3 c([Cu(OH) ]) 2
3
=c[Cu(OH) ]-,pH=10.7,则K =c(OH-)=10-14+10.7=10-3.3,反应[Cu(OH) ]2- [Cu(OH) ]-+OH-的平衡常数K =
3 3 4 3 4
c([Cu(OH) ])c(OH)
3 ,在曲线4和5的交叉点(12.5,0.48)时,c([Cu(OH) ]2-)=c([Cu(OH) ]-),pH=12.5,
c([Cu(OH) ]2) 4 3
4
则K =c(OH-)=10-14+12.5=10-1.5,则[Cu(OH) ]2- Cu(OH) +2OH-的平衡常数K=K K =10-4.8,C项正确;混合溶液
4 4 2 3 4
pH>14,含铜微粒是[Cu(OH) ]2-,反应的离子方程式是:Cu2++4OH-=[Cu(OH) ]2-,D项错误。
4 4
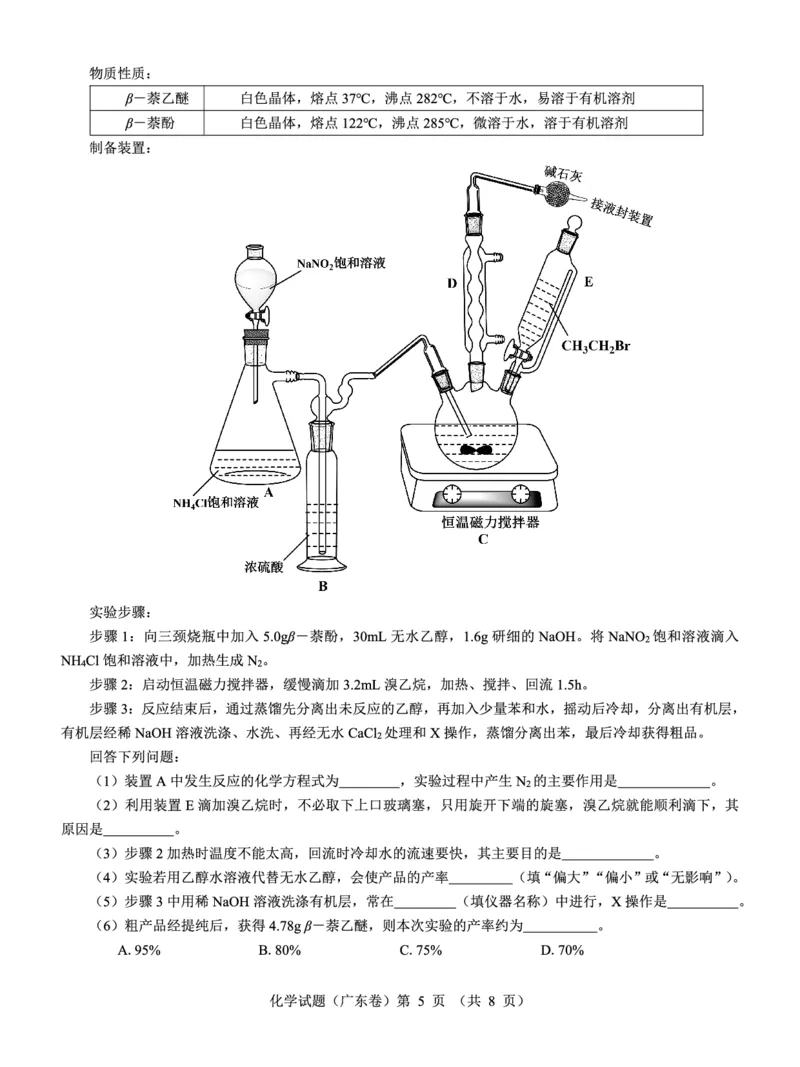
17.(14分)
(1)NH Cl+NaNO NaCl+2H O+N ↑(2分) 利用N 排出装置中的空气,防止β-萘酚被氧化(2分)
4 2 2 2 2
(2)装置E中的压强与三颈烧瓶中的压强能保持相等,溴乙烷能顺利滴下(2分)
(3)防止乙醇和溴乙烷大量挥发而逸出(2分)
(4)偏小(2分)
(5)分液漏斗(1分) 过滤(1分)
化学参考答案(广东卷)第 3 页 (共 7 页)
{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}(6)B(2分)
【解析】
(1)酚类易被氧化,又由于反应时间较长,为了避免β-萘酚长时间接触O 被氧化,需要将装置中的空气排尽。
2
(2)恒压滴液漏斗侧面的玻璃管能保证漏斗中的压强与三颈烧瓶中的压强一致,从而使溴乙烷能够顺利滴下。
(3)乙醇和溴乙烷的沸点均较低,为了防止二者大量挥发,加热温度不能太高,通冷却水的速度要快。
(4)溴乙烷在碱性水溶液中会发生水解反应,从而使产品的产率降低。
(5)洗涤液态有机物常在分液漏斗中进行,无水CaCl 吸水后生成的水合物受热易释放出水,因此在蒸馏之前
2
需要进行过滤。
5.0g 4.78g
(6)β-萘乙醚的理论产量为 172g/mol=5.97g,故产率为 ×100%=80%。
144g/mol 5.97g
18.(14分)
(1)+126.0(1分)
(2)①0.55(2分) 50%(2分) 加入稀释剂可减小C H 的分压,有利于平衡正向进行,故加入稀
3 8
释剂C H 平衡转化率高于不加稀释剂(2分)
3 8
②AC(2分)
(3)①不是(1分) ODHP工艺发生的反应和副反应均为放热反应,C H 的平衡转化率随温度升高应降
3 8
低,而不是升高(2分)
②0.01755n(2分)
【解析】
(1)根据盖斯定律,PDH工艺中的ΔH =-2217.8kJ/mol-(-2058.0kJ/mol)-(-285.8kJ/mol)=+126.0kJ/mol。
1
(2)①达到平衡时参与反应的C H 的物质的量为1mol×60%=0.6mol,利用“三段式”整理数据如下。
3 8
C H (g) C H (g)+H (g)
3 8 3 6 2
n(始)/mol 1 0 0
n(变)/mol 0.6 0.6 0.6
n(平)/mol 0.4 0.6 0.6
平衡时气体的总物质的量为0.4mol+0.6mol+0.6mol+1.1mol=2.7mol。
0.6
( 1.65MPa)2
p(C H )p(H ) 2.7
平衡常数K 3 6 2 0.55MPa 。
p p(C H ) 0.4
3 8 1.65MPa
2.7
若不加Ar,设达到平衡时C H 的转化率为,则参加反应的C H 的物质的量为1mol× = mol,利用
3 8 3 8
“三段式”整理数据如下。
化学参考答案(广东卷)第 4 页 (共 7 页)
{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}C H (g) C H (g)+H (g)
3 8 3 6 2
n(始)/mol 1 0 0
n(变)/mol
n(平)/mol(1-
)
[ 1.65MPa]2
(1)
由于温度不变,平衡常数不变,故 0.55MPa ,解得50%。
(1)
1.65MPa
(1)
②该反应是吸热反应,ΔH>0,观察表中数据,较高温度下,ΔG<0,据此可判断ΔS>0,A项正确;由方程式可
c(C H )
知无论反应是否达到平衡, 3 6 始终为1∶1,B项错误;恒温、恒容条件下,增大c(C H ),其平衡结果
3 8
c(H )
2
等效于加压,因此丙烷的平衡转化率减小,C项正确;催化剂不能改变平衡转化率,D项错误。
(3)①根据给出图像可知,随温度升高,C H 的转化率增大,而平衡转化率应随温度升高而降低,故390℃~
3 8
420℃之间C H 的转化率不是平衡转化率。
3 8
②发生副反应消耗的C H 物质的量为nmol/min×2min×4.5%×(1-87%)=0.0117nmol,根据副反应的方程式可知
3 8
3
生成C H 的物质的量为0.0117nmol× =0.01755nmol。
2 4
2
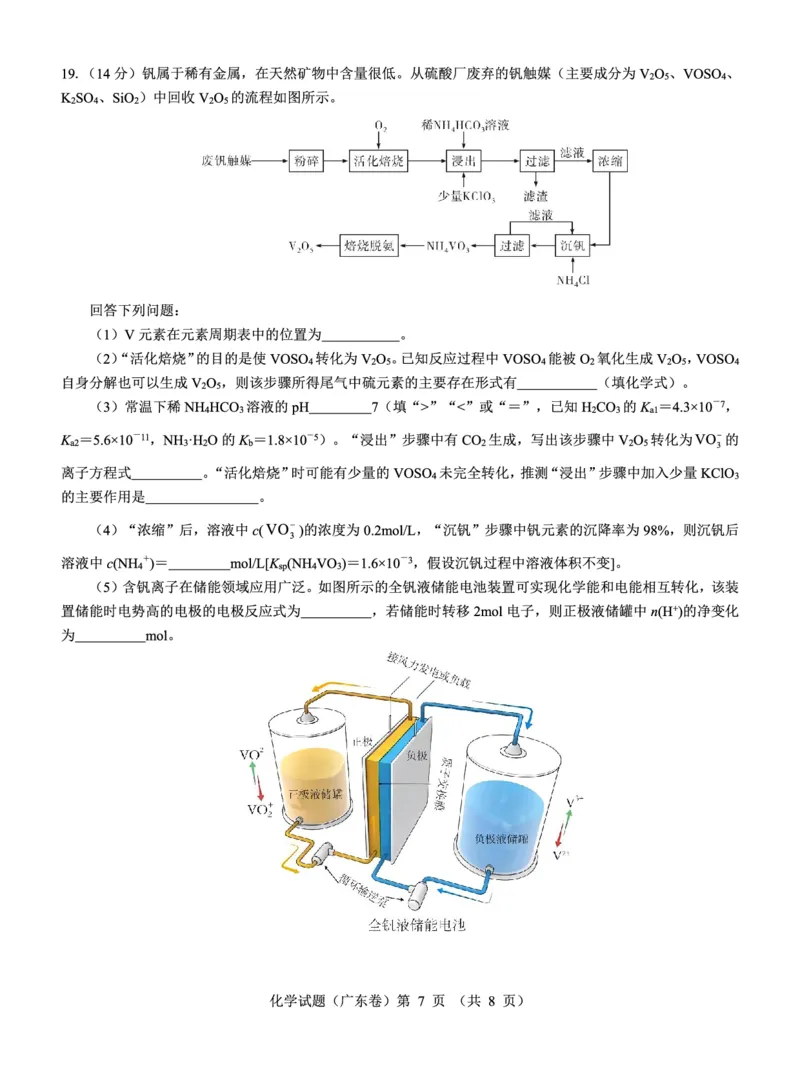
19.(14分)
(1)第四周期VB族(1分)
(2)SO 、SO (2分,每个1分)
3 2
(3)>(1分) V O +2HCO -=2VO -+2CO ↑+H O(2分)
2 5 3 3 2 2
将溶液中少量的VO2+氧化为VO(或作氧化剂)(2分)
3
(4)0.4(2分)
(5)H O+VO2+-e-=VO ++2H+(2分) 2(2分)
2 2
【解析】
(1)V是23号元素,位于第四周期VB族。
(2)VOSO 被O 氧化生成V O ,硫元素的化合价不变,因此会有SO 生成。VOSO 自身分解生成V O ,钒
4 2 2 5 3 4 2 5
元素的化合价升高,必有硫元素得电子生成SO 。
2
11014 11014
(3)NH +水解常数K = 5.61010,HCO -水解常数K = 2.3108,故HCO -的水
4 h 1.8105 3 h 4.3107 3
解能力稍强于NH +,溶液显弱碱性,pH>7。由题中信息可知,“浸出”的主要目的是将钒元素转化为VO,
4 3
化学参考答案(广东卷)第 5 页 (共 7 页)
{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}而VO2+转化为VO
3
时,钒元素的化合价升高,故KClO
3
作氧化剂。
(4)“沉钒”后,溶液中残留VO的浓度为0.2mol/L×2%=0.004mol/L,则1.6×10 -3=0.004mol/L×c(NH +),
3 4
解得c(NH +)=0.4mol/L。
4
(5)储能时作电解池,电势高的电极为阳极,发生失电子的反应,结合所给装置可知,VO2+转化为VO +,据
2
此写出电极反应式H O+VO2+-e-=VO ++2H+;转移2mol电子,正极区生成4molH+,同时使正极区多余2mol
2 2
正电荷,为了保持溶液呈电中性,有2molH+移向阴极,故n(H+)的净变化为4mol - 2mol=2mol。
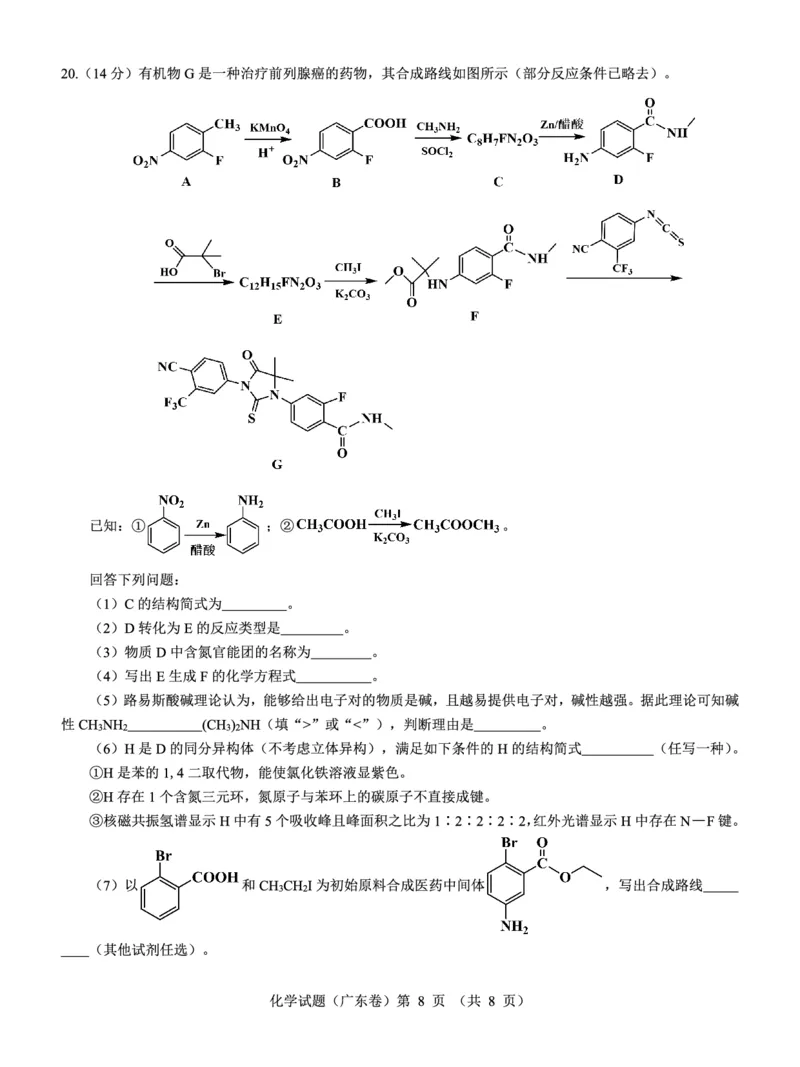
20.(14分)
(1) (1分)
(2)取代反应(1分)
(3)氨基、酰胺基(2分,每个1分)
(4) (2分)
(5)<(1分) 甲基是供电子基,甲基数目越多,供电子能力越强,导致氮原子电子云密度增大,
结合H+能力越强(2分)
(6) (2分)
化学参考答案(广东卷)第 6 页 (共 7 页)
{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}(7) (3分)
【解析】
(1)根据反应条件可知,C转化为D只是把硝基转化为氨基,因此只要把D中的氨基重新变回硝基,即可得
到C的结构简式。
(2)根据题中已知②的信息并结合F的结构简式,可知D转化为E时,D中氨基上的氢原子被“ ”
取代。
(3)根据D的结构简式可知,D中含有氨基、酰胺基、碳氟键,其中氨基和酰胺基为含氮官能团。
(4)根据D到E的转化并结合F的结构简式,可确定E的结构简式,进而写出方程式。
(5)见答案。
(6)能使氯化铁溶液显紫色,说明有酚羟基存在,因此另一个取代基含有2个N、1个C、1个F,再根据②、
③中的信息可确定符合条件的H的同分异构体。
(7)见答案。
化学参考答案(广东卷)第 7 页 (共 7 页)
{#{QQABKQCUggggQpAAAQhCQwEgCgOQkAEACagGwAAEMAIAgRFABAA=}#}