文档内容
专题22 金属有关的工艺流程
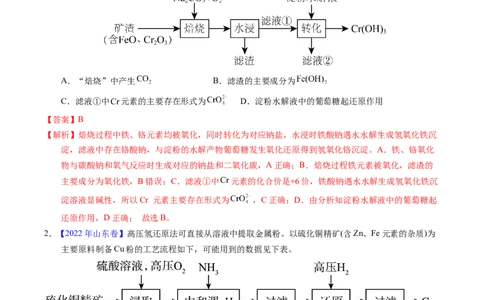
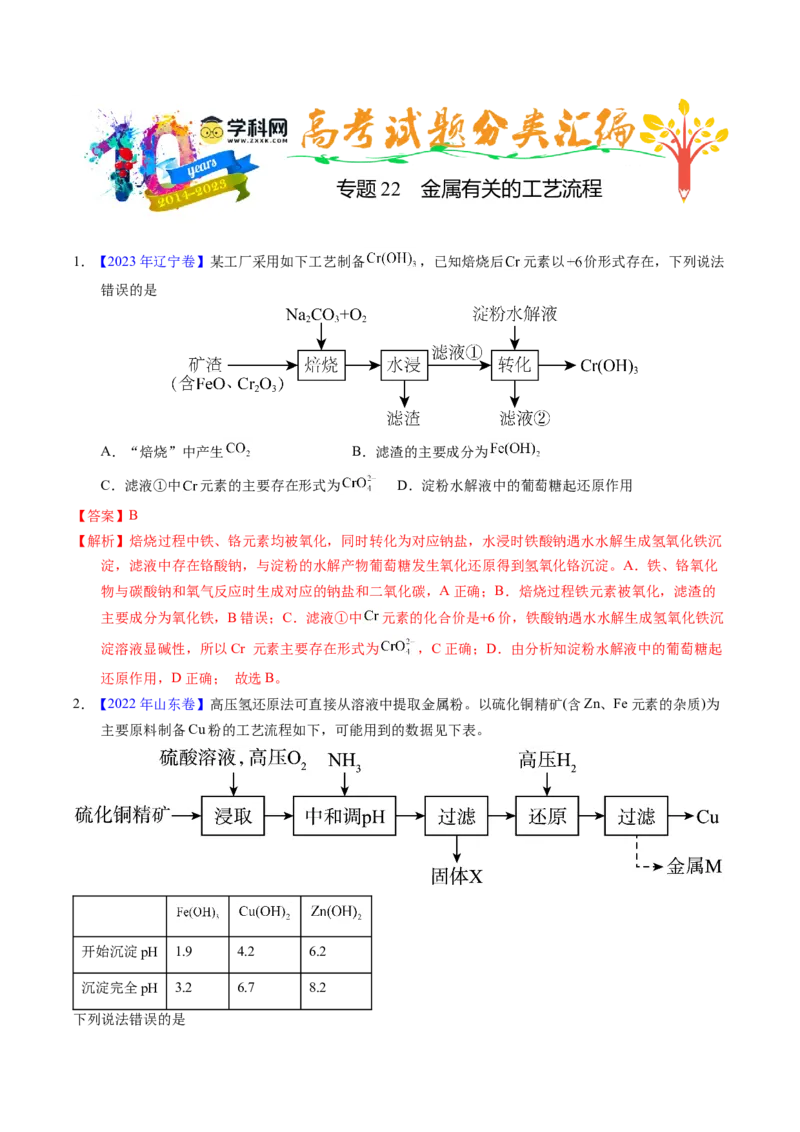
1.【2023年辽宁卷】某工厂采用如下工艺制备 ,已知焙烧后 元素以 价形式存在,下列说法
错误的是
A.“焙烧”中产生 B.滤渣的主要成分为
C.滤液①中 元素的主要存在形式为 D.淀粉水解液中的葡萄糖起还原作用
【答案】B
【解析】焙烧过程中铁、铬元素均被氧化,同时转化为对应钠盐,水浸时铁酸钠遇水水解生成氢氧化铁沉
淀,滤液中存在铬酸钠,与淀粉的水解产物葡萄糖发生氧化还原得到氢氧化铬沉淀。A.铁、铬氧化
物与碳酸钠和氧气反应时生成对应的钠盐和二氧化碳,A正确;B.焙烧过程铁元素被氧化,滤渣的
主要成分为氧化铁,B错误;C.滤液①中 元素的化合价是+6价,铁酸钠遇水水解生成氢氧化铁沉
淀溶液显碱性,所以Cr 元素主要存在形式为 ,C正确;D.由分析知淀粉水解液中的葡萄糖起
还原作用,D正确; 故选B。
2.【2022年山东卷】高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为
主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是A.固体X主要成分是 和S;金属M为Zn
B.浸取时,增大 压强可促进金属离子浸出
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
【答案】D
【解析】CuS精矿(含有杂质Zn、Fe元素)在高压O 作用下,用硫酸溶液浸取,CuS反应产生为CuSO 、
2 4
S、HO,Fe2+被氧化为Fe3+,然后加入NH 调节溶液pH,使Fe3+形成Fe(OH) 沉淀,而Cu2+、Zn2+仍以
2 3 3
离子形式存在于溶液中,过滤得到的滤渣中含有S、Fe(OH) ;滤液中含有Cu2+、Zn2+;然后向滤液中
3
通入高压H,根据元素活动性:Zn>H>Cu,Cu2+被还原为Cu单质,通过过滤分离出来;而Zn2+仍
2
然以离子形式存在于溶液中,再经一系列处理可得到Zn单质。A.经过上述分析可知固体X主要成分
是S、Fe(OH) ,金属M为Zn,A正确;B.CuS难溶于硫酸,在溶液中存在沉淀溶解平衡CuS(s)
3
Cu2+(aq)+S2-(aq),增大O 的浓度,可以反应消耗S2-,使之转化为S,从而使沉淀溶解平衡正向移动,
2
从而可促进金属离子的浸取,B正确;C.根据流程图可知:用NH 调节溶液pH时,要使Fe3+转化为
3
沉淀,而Cu2+、Zn2+仍以离子形式存在于溶液中,结合离子沉淀的pH范围,可知中和时应该调节溶液
pH范围为3.2~4.2,C正确;D.在用H 还原Cu2+变为Cu单质时,H 失去电子被氧化为H+,与溶液
2 2
中OH-结合形成HO,若还原时增大溶液的酸度,c(H+)增大,不利于H 失去电子还原Cu单质,因此
2 2
不利于Cu的生成,D错误;故合理选项是D。
3.【2022年福建卷】用铬铁合金(含少量 单质)生产硫酸铬的工艺流程如下:
下列说法错误的是
A.“浸出”产生的气体含有 B.“除杂”的目的是除去 元素
C.流程中未产生六价铬化合物 D.“滤渣2”的主要成分是
【答案】D
【解析】由流程可知,加入稀硫酸溶解,生成气体为氢气,溶液中含 加入NaS分
2
离出滤渣1含CoS和NiS, 不会沉淀,再加入草酸除铁生成FeC O,过滤分离出硫酸铬,
2 4
以此来解答。A.四种金属均与稀硫酸反应生成H,A正确;B.共有四种金属,由流程可知,沉铁
2
后分离出硫酸铬,则“除杂"的目的是除去Ni、Co元素,B正确;C.由上述分析可知,流程中未产
生六价铬化合物,C正确;D.“滤渣2”的主要成分是FeC O,D错误; 故本题选D。
2 4
4.(2021·福建真题)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:下列说法错误的是
A.FeSO 的分解产物X为FeO B.本流程涉及复分解反应
4
C.HNO 的沸点比HSO 的低 D.制备使用的铁锅易损坏
3 2 4
【答案】A
【解析】A.据图可知FeSO 分解时生成SO 和SO ,部分S元素被还原,则Fe元素应被氧化,X为
4 2 3
Fe O,A错误;B.HSO 与KNO 在蒸馏条件下生成HNO 和KSO ,为复分解反应,B正确;C.
2 3 2 4 3 3 2 4
HSO 与KNO 混合后,蒸馏过程中生成HNO,说明HNO 的沸点比HSO 的低,C正确;D.硫酸、
2 4 3 3 3 2 4
硝酸均可以和铁反应,所以制备使用的铁锅易损坏,D正确;综上所述答案为A。
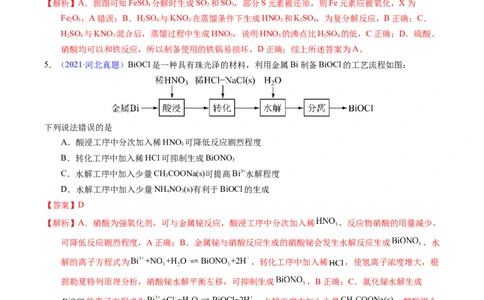
5.(2021·河北真题)BiOCl是一种具有珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:
下列说法错误的是
A.酸浸工序中分次加入稀HNO 可降低反应剧烈程度
3
B.转化工序中加入稀HCl可抑制生成BiONO
3
C.水解工序中加入少量CHCOONa(s)可提高Bi3+水解程度
3
D.水解工序中加入少量NH NO (s)有利于BiOCl的生成
4 3
【答案】D
【解析】A.硝酸为强氧化剂,可与金属铋反应,酸浸工序中分次加入稀 ,反应物硝酸的用量减少,
可降低反应剧烈程度,A正确;B.金属铋与硝酸反应生成的硝酸铋会发生水解反应生成 ,水
解的离子方程式为 ,转化工序中加入稀 ,使氢离子浓度增大,根
据勒夏特列原理分析,硝酸铋水解平衡左移,可抑制生成 ,B正确;C.氯化铋水解生成
的离子方程式为 ,水解工序中加入少量 ,醋酸根会
结合氢离子生成弱电解质醋酸,使氢离子浓度减小,根据勒夏特列原理分析,氯化铋水解平衡右移,
促进 水解,C正确;D.氯化铋水解生成 的离子方程式为 ,水
解工序中加入少量 ,铵根离子水解生成氢离子,使氢离子浓度增大,根据勒夏特列原理分
析,氯化铋水解平衡左移,不利于生成 ,且部分铋离子与硝酸根、水也会发生反应
,也不利于生成 ,综上所述,D错误;故选D。
6.(2018新课标Ⅰ卷)磷酸亚铁锂(LiFePO )电池是新能源汽车的动力电池之一。采用湿法冶金工艺回
4
收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是
A.合理处理废旧电池有利于保护环境和资源再利用
B.从“正极片”中可回收的金属元素有Al、Fe、Li
C.“沉淀”反应的金属离子为Fe3+
D.上述流程中可用硫酸钠代替碳酸钠
【答案】D
【解析】正极片碱溶时铝转化为偏铝酸钠,滤渣中含有磷酸亚铁锂,加入硫酸和硝酸酸溶,过滤后滤渣是
炭黑,得到含Li、P、Fe的滤液,加入碱液生成氢氧化铁沉淀,滤液中加入碳酸钠生成含锂的沉淀,
据此解答。A、废旧电池中含有重金属,随意排放容易污染环境,因此合理处理废旧电池有利于保护
环境和资源再利用,A正确;B、根据流程的转化可知从正极片中可回收的金属元素有Al、Fe、Li,B
正确;C、得到含Li、P、Fe的滤液,加入碱液生成氢氧化铁沉淀,因此“沉淀”反应的金属离子是
Fe3+,C正确;D、硫酸锂能溶于水,因此上述流程中不能用硫酸钠代替碳酸钠,D错误。答案选D。
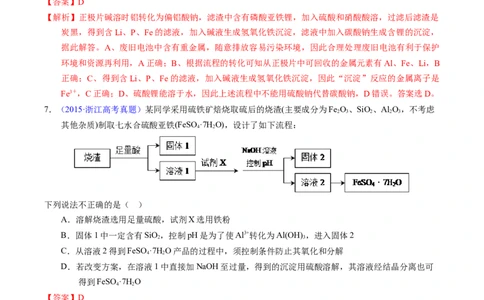
7.(2015·浙江高考真题)某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe O、SiO、Al O,不考虑
2 3 2 2 3
其他杂质)制取七水合硫酸亚铁(FeSO ·7H O),设计了如下流程:
4 2
下列说法不正确的是( )
A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定含有SiO,控制pH是为了使Al3+转化为Al(OH) ,进入固体2
2 3
C.从溶液2得到FeSO ·7H O产品的过程中,须控制条件防止其氧化和分解
4 2
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可
得到FeSO ·7H O
4 2
【答案】D
【解析】A、流程设计意图是用硫酸把Fe O、Al O,转化为硫酸盐,除去SiO,然后用铁粉还原Fe3+得到
2 3 2 3 2
硫酸亚铁,A正确;B、固体1为SiO,分离FeSO 和Al (SO ) 采用的是调控pH的方法,使Al3+转化
2 4 2 4 3
为Al(OH) 沉淀从而与FeSO 分离,B不正确;C、Fe2+容易被氧化,所以在得到FeSO ·7H O产品的过
3 4 4 2
程中,要防止其被氧化和分解,C正确;D、在溶液1中直接加过量的NaOH得到的是Fe(OH) 沉淀,
3
Fe(OH) 溶于硫酸后生成Fe (SO ),D不正确。答案选D。
3 2 4 3
8.(2016·全国高考真题)短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的
二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol·L-1r溶液的pH
为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )A.原子半径的大小W X>Y
C.Y的氢化物常温常压下为液态 D.X的最高价氧化物的水化物为强酸
【答案】C
【解析】由n是元素Z的单质,通常为黄绿色气体,可知Z元素为Cl,n为Cl,再根据q的水溶液具有漂
2
白性,可知q为HClO,由0.01 mol·L-1 r溶液的pH为2,可判断r为一元强酸,则r为HCl,然后根
据n和p的反应条件,以及s通常是难溶于水的混合物,可知p为烷烃,s为烷烃的氯代物;根据题意,
W、X、Y、Z是短周期原子序数依次增加的四种元素,可进一步推知W、X、Y、Z分别为H、C、
O、Cl。A、根据原子半径的变化规律,可知原子半径:H