文档内容
江苏省镇江第一中学 2021 级高三阶段学情检测
化学
命题人: 审核人:
可能用到的相对原子质量:C—12O—16S—32K—39Cr—52Fe—56Co—59
一、单项选择题:共 13题,每题 3分,共39分。每题只有一个选项最符合题意。
1.我国承诺在2060年前实现“碳中和”,碳中和是指CO 的排放总量和减少总量相当。下列措施中对促进“碳
2
中和”最直接有效的是
A.将重质油裂解为轻质油作为燃料 B.大规模开采可燃冰作为新能源
C.通过清洁煤技术减少煤燃烧污染 D.研发催化剂将CO 转化为甲醇
2
2.工业上制备保险粉的反应为HCOONaNaOH2SO Na S O CO H O 。下列有关说法正确的
2 2 2 4 2 2
是
A.Na的结构示意图为
B.NaOH的电子式为Na:O:H
C.HCOONa中含有键和键的数目之比为3:1
D.基态S原子的外围电子的轨道表达式为
3.下列有关氧化物的性质与用途具有对应关系的是
A.MgO的熔点高,可用于制造耐火材料
B.SO 具有漂白性,可使酸性KMnO 溶液褪色
2 4
C.SiO 的硬度大,可用于制作光导纤维
2
D.H O 具有还原性,可用于处理含CN的废水
2 2
4.水合肼 N H H O 是重要的氢能源稳定剂, N H 具有较强的还原性。其制备的反应原理为
2 4 2 2 4
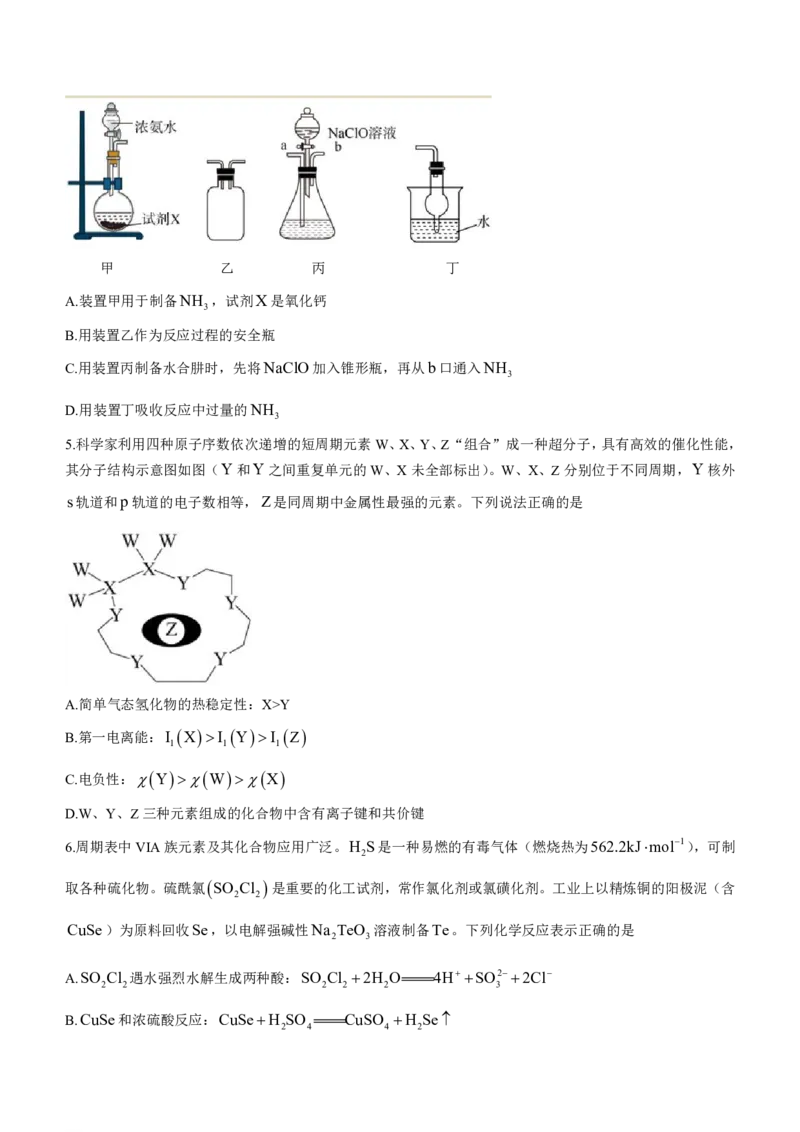
NaClO2NH N H H ONaCl 。下列装置和操作不能达到实验目的的是
3 2 4 2
学科网(北京)股份有限公司甲 乙 丙 丁
A.装置甲用于制备NH ,试剂X是氧化钙
3
B.用装置乙作为反应过程的安全瓶
C.用装置丙制备水合肼时,先将NaClO加入锥形瓶,再从b口通入NH
3
D.用装置丁吸收反应中过量的NH
3
5.科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,具有高效的催化性能,
其分子结构示意图如图(Y和Y之间重复单元的W、X未全部标出)。W、X、Z分别位于不同周期,Y核外
s轨道和p轨道的电子数相等,Z是同周期中金属性最强的元素。下列说法正确的是
A.简单气态氢化物的热稳定性:X>Y
B.第一电离能:I X I Y I Z
1 1 1
C.电负性:
Y
W
X
D.W、Y、Z三种元素组成的化合物中含有离子键和共价键
6.周期表中VIA族元素及其化合物应用广泛。H S是一种易燃的有毒气体(燃烧热为562.2kJmol1),可制
2
取各种硫化物。硫酰氯
SO Cl
是重要的化工试剂,常作氯化剂或氯磺化剂。工业上以精炼铜的阳极泥(含
2 2
CuSe)为原料回收Se,以电解强碱性Na TeO 溶液制备Te。下列化学反应表示正确的是
2 3
A.SO Cl 遇水强烈水解生成两种酸:SO Cl 2H O 4HSO22Cl
2 2 2 2 2 3
B.CuSe和浓硫酸反应:CuSeH SO CuSO H Se
2 4 4 2
学科网(北京)股份有限公司C.电解强碱性Na TeO 溶液的阴极反应:TeO2 4e 6H Te3H O
2 3 3 2
D.H S燃烧的热化学方程式:2H S g 3O g 2SO g 2H O l ΔH 1124.4kJmol1
2 2 2 2 2
7.利用惰性电极电解Na SO 和NaHSO 混合溶液分离得到两者的浓溶液,其电解装置如图所示,I室里加入
2 3 3
的是稀硫酸,II室和III室里加入的是Na SO 和NaHSO 的混合溶液。下列说法正确的是
2 3 3
A.阳极上发生的电极反应:2H 2e H
2
B.交换膜a 是阴离子交换膜
C.电解一段时间后,II室得到的NaHSO 溶液
3
D.电解时每转移1mol电子,理论上阴极区可获得11.2L气体
8.用软锰矿(主要成分是MnO )制备纯净MnO 的工艺流程如下:
2 2
下列说法不正确的是
A.“浸出”过程中参与反应的n FeSO :n MnO 为1:2
4 2
B.“沉锰”过程涉及:2HCO Mn2 MnCO H OCO
3 3 2 2
C.“沉锰”过程中产物过滤后所得滤液可制造化肥
D.“沉锰”和“热解、煅烧”过程生成的CO 可用来制备NH HCO
2 4 3
9.反应2SO g O g 2SO g ΔH 196.6kJmol1。在恒温恒压的密闭容器中进行时,下列
2 2 3
说法正确的是
A.反应中每充入2molSO 和1molO ,充分反应后转移电子数目为46.021023
2 2
B.该反应中,反应物的键能之和产物的键能之和
c2
SO
C.使用优质催化剂,体系中 3 的值增大
c2
SO
c
O
2 2
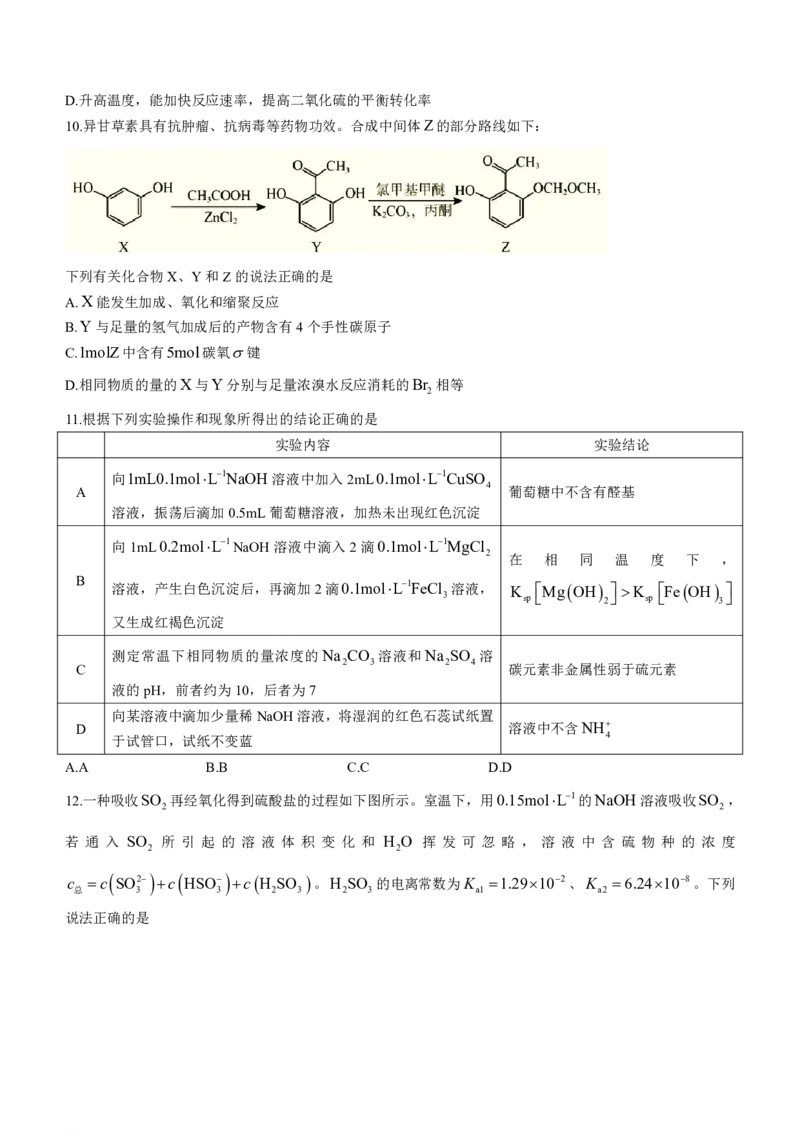
学科网(北京)股份有限公司D.升高温度,能加快反应速率,提高二氧化硫的平衡转化率
10.异甘草素具有抗肿瘤、抗病毒等药物功效。合成中间体Z的部分路线如下:
下列有关化合物X、Y和Z的说法正确的是
A.X能发生加成、氧化和缩聚反应
B.Y与足量的氢气加成后的产物含有4个手性碳原子
C.1molZ中含有5mol碳氧键
D.相同物质的量的X与Y分别与足量浓溴水反应消耗的Br 相等
2
11.根据下列实验操作和现象所得出的结论正确的是
实验内容 实验结论
向1mL0.1molL1NaOH溶液中加入2mL0.1molL1CuSO
A 4 葡萄糖中不含有醛基
溶液,振荡后滴加0.5mL葡萄糖溶液,加热未出现红色沉淀
向1mL0.2molL1NaOH 溶液中滴入 2滴0.1molL1MgCl
2 在 相 同 温 度 下 ,
B 溶液,产生白色沉淀后,再滴加2滴0.1molL1FeCl 溶液, K Mg OH K Fe OH
3 sp 2 sp 3
又生成红褐色沉淀
测定常温下相同物质的量浓度的Na CO 溶液和Na SO 溶
C 2 3 2 4 碳元素非金属性弱于硫元素
液的pH,前者约为10,后者为7
向某溶液中滴加少量稀NaOH溶液,将湿润的红色石蕊试纸置
D
溶液中不含NH
于试管口,试纸不变蓝 4
A.A B.B C.C D.D
12.一种吸收SO 再经氧化得到硫酸盐的过程如下图所示。室温下,用0.15molL1的NaOH溶液吸收SO ,
2 2
若 通 入 SO 所 引 起 的 溶 液 体 积 变 化 和 H O 挥 发 可 忽 略 , 溶 液 中 含 硫 物 种 的 浓 度
2 2
c c SO2 c HSO c H SO 。H SO 的电离常数为K 1.29102、K 6.24108。下列
总 3 3 2 3 2 3 a1 a2
说法正确的是
学科网(北京)股份有限公司A.c 0.1molL1的溶液中:3c Na 2c H SO 2c HSO 2c SO2
总 2 3 3 3
B.在NaHSO 溶液中:c H c SO2 c H SO c OH
3 3 2 3
C.NaOH完全转化为Na SO 时,溶液中:c H c HSO c SO2 c OH
2 3 3 3
D. 若 改 用 少 量 稀 的 Ba NO 溶 液 吸 收 SO , 则 发 生 反 应 的 离 子 方 程 式 :
3 2 2
Ba2 2NO 3SO 2H O BaSO 2NO4H 2SO2
3 2 2 4 4
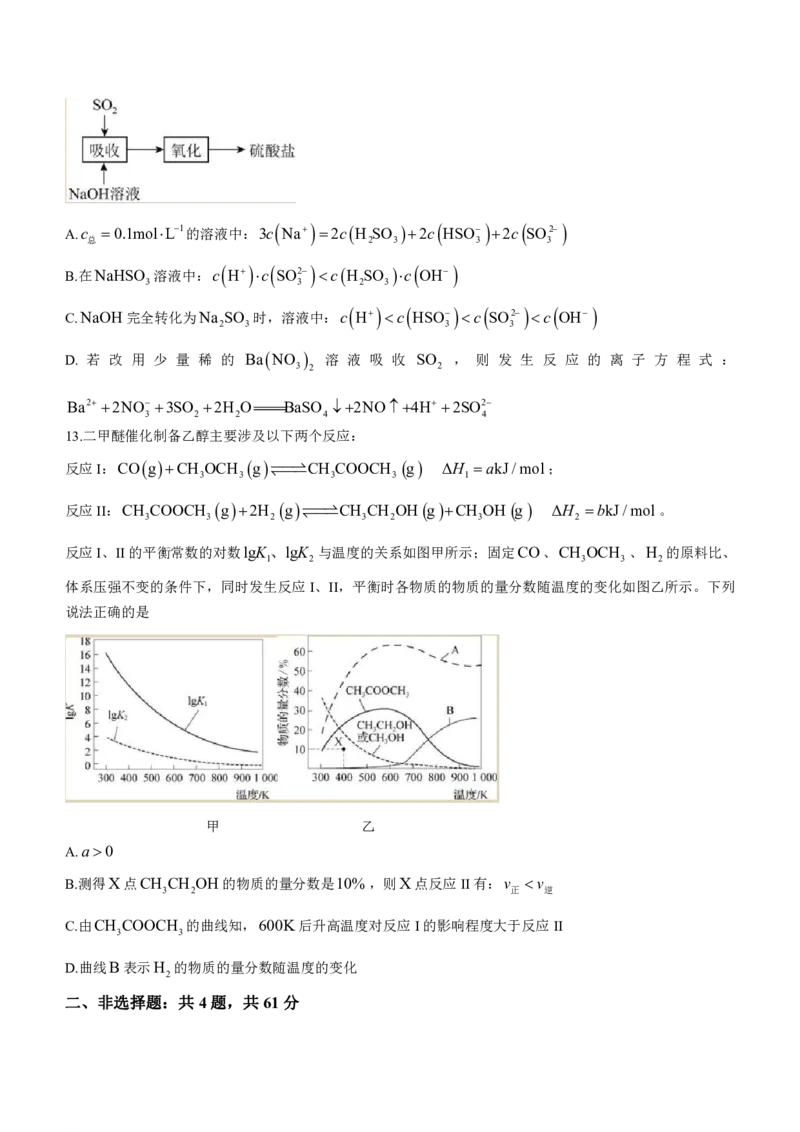
13.二甲醚催化制备乙醇主要涉及以下两个反应:
反应I:CO g CH OCH g CH COOCH g ΔH akJ/mol;
3 3 3 3 1
反应II:CH COOCH g 2H g CH CH OH g CH OH g ΔH bkJ/mol。
3 3 2 3 2 3 2
反应I、II的平衡常数的对数lgK、lgK 与温度的关系如图甲所示;固定CO、CH OCH 、H 的原料比、
1 2 3 3 2
体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图乙所示。下列
说法正确的是
甲 乙
A.a0
B.测得X点CH CH OH的物质的量分数是10%,则X点反应II有:v v
3 2 正 逆
C.由CH COOCH 的曲线知,600K后升高温度对反应I的影响程度大于反应II
3 3
D.曲线B表示H 的物质的量分数随温度的变化
2
二、非选择题:共 4题,共 61分
学科网(北京)股份有限公司14.(15分)Co O 在磁性材料、电化学领域应用广泛。以钴矿[主要成分是CoO、Co O 、Co(OH) ,还
3 4 2 3 3
含SiO 及少量Al O 、Fe O 、CuO及MnO 等]为原料可制取Co O 。步骤如下:
2 2 3 2 3 2 3 4
(1)浸取:用盐酸和Na SO 溶液浸取钴矿,浸取液中含有Al3、Fe2、Co2、Cu2、Mn2、Cl、SO2
2 3 4
等离子。写出Co O 发生反应的离子方程式:__________________。
2 3
(2)除杂:向浸取液中先加入足量NaClO 氧化Fe2,再加入NaOH调节pH除去Al3、Fe3、Cu2。有
3
关沉淀数据如表(“完全沉淀”时金属离子浓度1105molL1):
沉淀 Al OH Fe OH Co OH Cu OH Mn OH
3 3 2 2 2
恰好完全沉淀时的pH 5.2 2.8 9.4 6.7 10.1
若浸取液中c Co2 0.1molL1,则须调节溶液pH的范围是______(加入NaClO 和NaOH时,溶液的
3
体积变化忽略)。
( 3 ) 萃 取 、 反 萃 取 : 向 除 杂 后 的 溶 液 中 , 加 入 某 有 机 酸 萃 取 剂 HA , 发 生 反 应 :
2
Co2 n HA CoA n1 HA 2H 。实验测得:当溶液pH处于4.56.5范围内,Co2萃取
2 2 2
率随溶液pH的增大而增大(如图1所示),其原因是________________________。向萃取所得有机相中加入
H SO ,反萃取得到水相。该工艺中设计萃取、反萃取的目的是________________________。
2 4
图1 图2
(4)沉钴、热分解:向反萃取后得到的水相中加入NH HCO 溶液,过滤、洗涤、干燥,得到CoCO 固体,
4 3 3
加热CoCO 制备Co O 。1molCoCO 在空气中加热,反应温度对反应产物的影响如图 2 所示,请写出
3 3 4 3
5001000℃时,发生主要反应的化学方程式__________________。
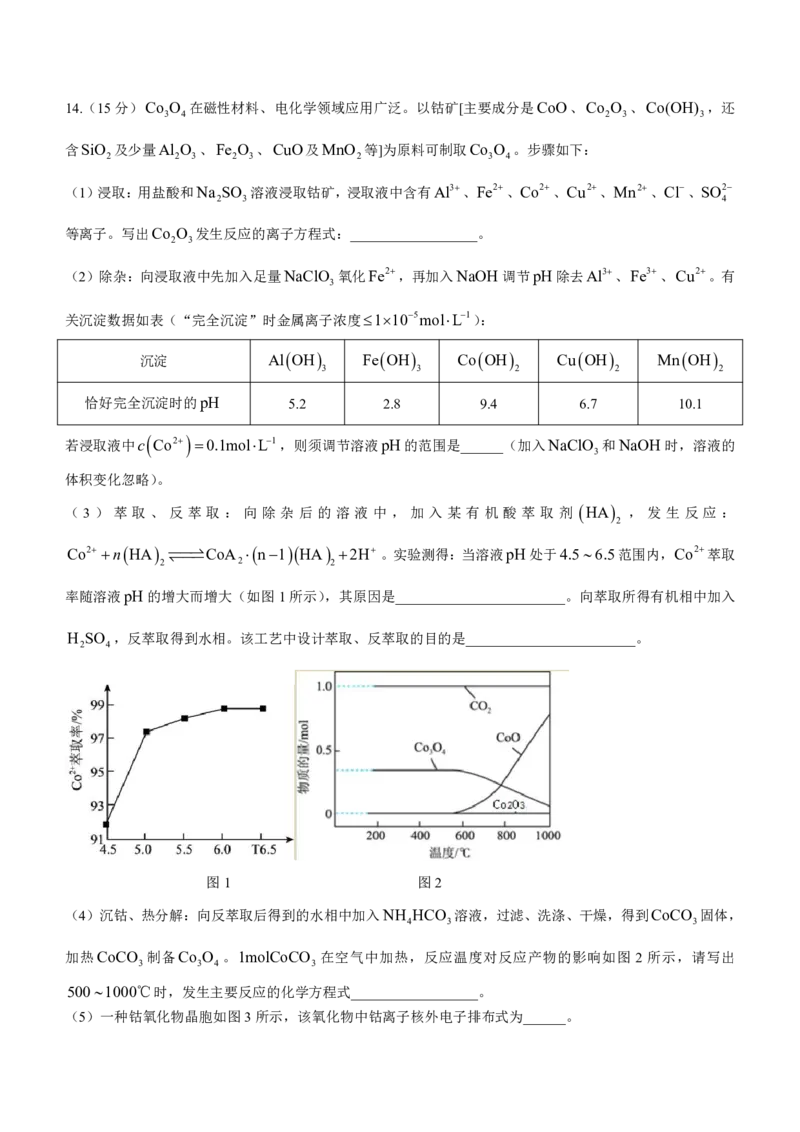
(5)一种钴氧化物晶胞如图3所示,该氧化物中钴离子核外电子排布式为______。
学科网(北京)股份有限公司图3
15.(15分)化合物F是合成心脏病治疗药法西多曲的中间体,其合成路线流程图如图:
(1)C中的含氧官能团名称为______和______。
(2)E中碳原子的杂化轨道类型有______。
(3)D的分子式为C H O ,写出D的结构简式:____________。
15 18 6
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:____________。
①能与FeCl 溶液发生显色反应,不能发生银镜反应;
3
②苯环上有4个取代基,分子中只有4种不同化学环境的氢。
( 5 ) 请 写 出 以 H CCH 、 H C COOC H 、 为 原 料 制 备
2 2 2 2 5 2
的合成路线流程图______(无机试剂和有机溶剂任用,合成路线流程图示例
见本题题干)。
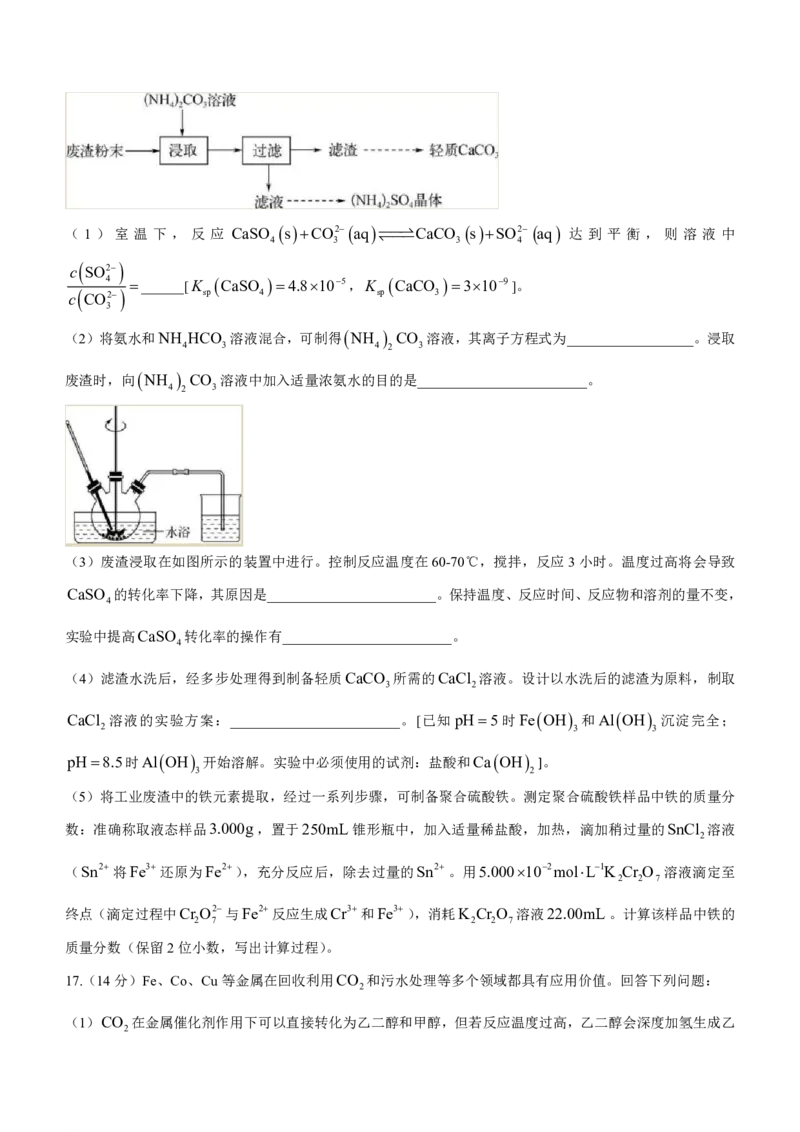
16(. 17分)实验室以工业废渣(主要含CaSO 2H O,还含少量SiO 、Al O 、Fe O )为原料制取轻CaCO
4 2 2 2 3 2 3 3
和 NH SO 晶体,其实验流程如下:
4 2 4
学科网(北京)股份有限公司( 1 ) 室 温 下 , 反 应 CaSO s CO2 aq CaCO s SO2 aq 达 到 平 衡 , 则 溶 液 中
4 3 3 4
c
SO2
4 ______[K CaSO 4.8105,K CaCO 3109]。
c
CO2 sp 4 sp 3
3
(2)将氨水和NH HCO 溶液混合,可制得 NH CO 溶液,其离子方程式为__________________。浸取
4 3 4 2 3
废渣时,向 NH CO 溶液中加入适量浓氨水的目的是________________________。
4 2 3
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60-70℃,搅拌,反应3小时。温度过高将会导致
CaSO 的转化率下降,其原因是________________________。保持温度、反应时间、反应物和溶剂的量不变,
4
实验中提高CaSO 转化率的操作有________________________。
4
(4)滤渣水洗后,经多步处理得到制备轻质CaCO 所需的CaCl 溶液。设计以水洗后的滤渣为原料,制取
3 2
CaCl 溶液的实验方案:________________________。[已知pH 5时Fe OH 和Al OH 沉淀完全;
2 3 3
pH 8.5时Al OH 开始溶解。实验中必须使用的试剂:盐酸和Ca OH ]。
3 2
(5)将工业废渣中的铁元素提取,经过一系列步骤,可制备聚合硫酸铁。测定聚合硫酸铁样品中铁的质量分
数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl 溶液
2
(Sn2将Fe3还原为Fe2),充分反应后,除去过量的Sn2。用5.000102molL1K Cr O 溶液滴定至
2 2 7
终点(滴定过程中Cr O2与Fe2反应生成Cr3和Fe3),消耗K Cr O 溶液22.00mL。计算该样品中铁的
2 7 2 2 7
质量分数(保留2位小数,写出计算过程)。
17.(14分)Fe、Co、Cu等金属在回收利用CO 和污水处理等多个领域都具有应用价值。回答下列问题:
2
(1)CO 在金属催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙
2
学科网(北京)股份有限公司醇。
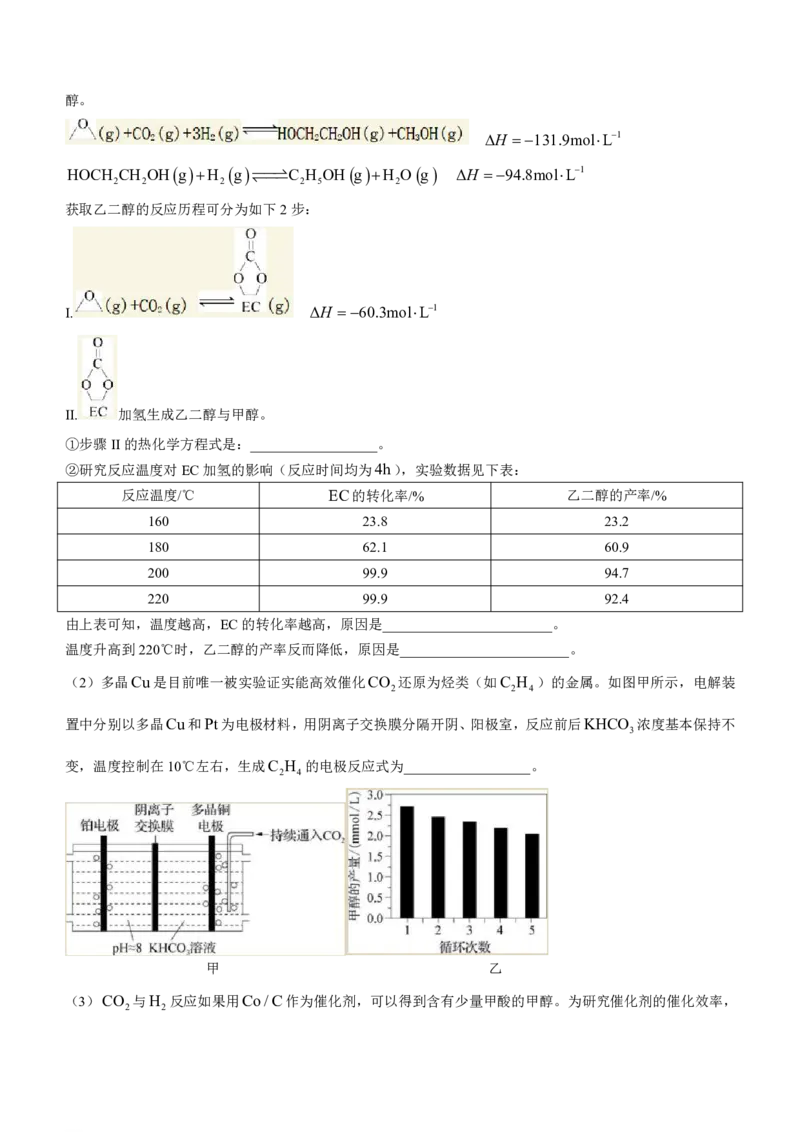
H 131.9molL1
HOCH CH OH g H g C H OH g H O g ΔH 94.8molL1
2 2 2 2 5 2
获取乙二醇的反应历程可分为如下2步:
I. ΔH 60.3molL1
II. 加氢生成乙二醇与甲醇。
①步骤II的热化学方程式是:__________________。
②研究反应温度对EC加氢的影响(反应时间均为4h),实验数据见下表:
反应温度/℃ EC的转化率/% 乙二醇的产率/%
160 23.8 23.2
180 62.1 60.9
200 99.9 94.7
220 99.9 92.4
由上表可知,温度越高,EC的转化率越高,原因是________________________。
温度升高到220℃时,乙二醇的产率反而降低,原因是________________________。
(2)多晶Cu是目前唯一被实验证实能高效催化CO 还原为烃类(如C H )的金属。如图甲所示,电解装
2 2 4
置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO 浓度基本保持不
3
变,温度控制在10℃左右,生成C H 的电极反应式为__________________。
2 4
甲 乙
(3)CO 与H 反应如果用Co/C作为催化剂,可以得到含有少量甲酸的甲醇。为研究催化剂的催化效率,
2 2
学科网(北京)股份有限公司将Co/C催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇产量如图乙所示,试推测甲醇产量
变化的原因:____________________。(Co的性质与Fe相似)
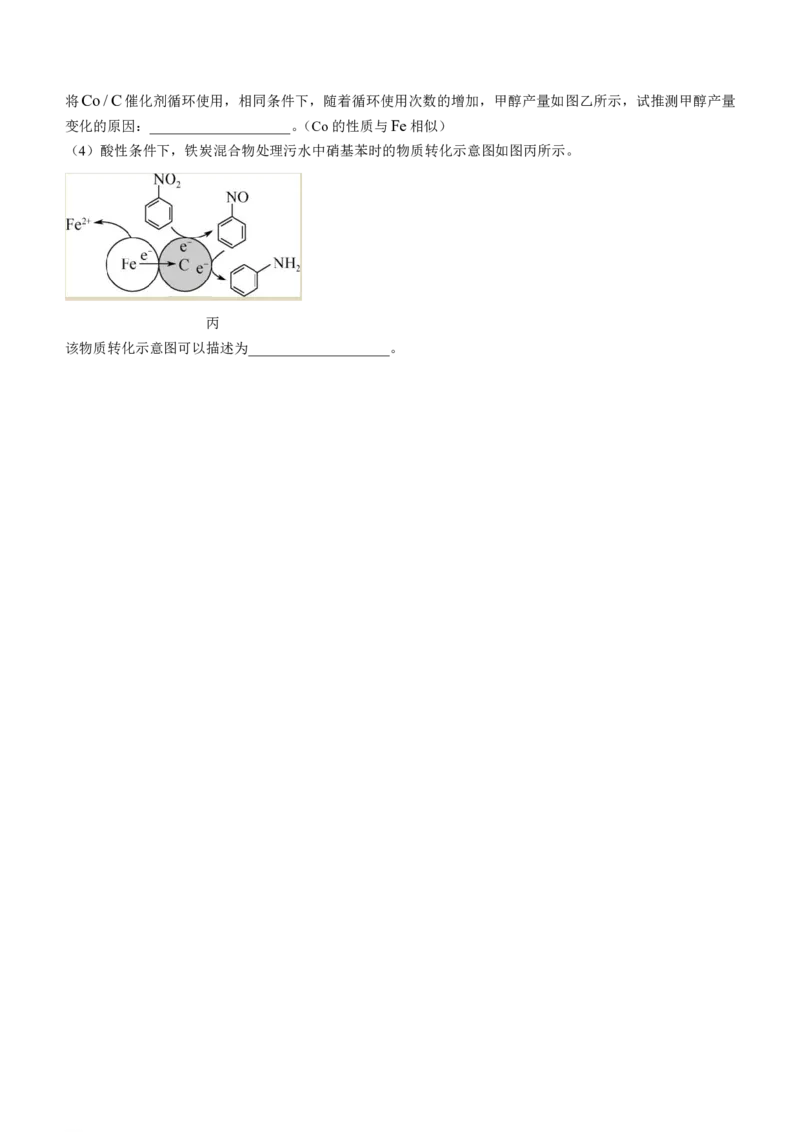
(4)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图丙所示。
丙
该物质转化示意图可以描述为____________________。
学科网(北京)股份有限公司