文档内容
2023 年湖北省高三 9 月起点考试
高三化学试卷
命题学校:应城一中 命题教师:邢泰宇 曹桂能 审题学校:孝昌一中
考试时间:2023年9月6日下午14:30-17:05 试卷满分:100分
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考证号条形码粘贴在
答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。写在试卷、草稿纸和
答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。写在试卷、草稿纸和答题卡上的非答
题区域均无效。
可能用到的相对原子质量:H-1 C-12 O-16 Al-27 Co-59
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学与生活密切相关。下列日常生活场景中,相关措施正确的是
选项 A B C D
场景 塑料的老化 食物氧化变质 金属的腐蚀 环境和物品消毒
措施 生产塑料时添加增塑剂 用生石灰作脱氧剂 被保护金属作原电池负极 用紫外线照射
2.我国古典文献中有丰富的化学知识。《格古要论》云:鍮石,自然铜之精也。今炉甘石(主要成分ZnCO )
3
炼成者,假鍮也。崔昉《外丹本草》云:铜一斤,炉甘石一斤,炼之成(假)鍮石。下列说法错误的是
A.假鍮石比鍮石更方便冲压成型 B.假鍮石的炼制过程会有气体产生
C.假鍮石的主要材质为合金 D.假鍮石的炼制过程涉及氧化还原反应
3.奥培米芬是一种雌激素受体调节剂,其结构简式如图,有关该化合物叙述正确的是
A.分子式为C H O Cl
24 23 2
B.所有碳原子一定共平面
C.1mol该物质最多消耗9molH
2
D.能发生消去反应,不能发生氧化反应
4.在无色透明溶液中能大量共存,且加入过量稀硫酸时,有气体生成的是
A.Na+、H+、SiO2-、Cl- B.K+、Mg2+、SO2-、Cl-
3 4
C.Na+、K+、CO2-、Cl- D.Na+、Fe3+、Cl-、HSO-
3 3
湖北省新高考联考协作体*化学试卷(共8页)第1页5.下列实验操作及现象与对应结论匹配的是
选项 实验操作及现象 结论
将Na S O 溶液和稀H SO 混合,得到沉淀,且生成的气体
2 2 3 2 4
A H SO 在反应中体现氧化性
2 4
可使品红溶液褪色
在导管口点燃纯净的H ,然后将导管伸入盛满Cl 的集气瓶
2 2
B 助燃物不一定是O
2
中,H 在Cl 中安静地燃烧,发出苍白色火焰
2 2
C 向苯酚浓溶液中滴加少量溴水、振荡,无白色沉淀产生 该条件下两者不反应
将银和AgNO 溶液、铁和NaCl溶液组成双液原电池,连通
3
D Ag是原电池的负极
后银表面有银白色金属沉积,铁电极的质量变轻
6.短周期主族元素X、Y、Z、W、M的原子序数依次增大,且位于三个不同周期。已知基态原子的最高能
级上的电子数W是X的4倍,Y与W同主族,Z是地壳中含量最高的金属元素。下列说法正确的是
A.非金属性:X>Y B.Z与Y、M形成的常见化合物熔点:Y<M
C.简单离子半径:Z>W D.X与W、M形成的常见化合物还原性:W>M
7.乙醚(微溶于水,熔点:-116.2℃,沸点:34.5℃,空气中遇明火易爆炸)在医学上可用作麻醉剂。实验室
浓硫酸
合成乙醚的原理如下:2CH
3
CH
2
OH―――――→ C
2
H
5
OC
2
H
5
+H
2
O。部分实验步骤如下:在干燥的三颈烧瓶
140℃
中先加入12mL无水乙醇,再缓缓加入12mL浓硫酸混匀。在恒压滴液漏斗中加入25mL无水乙醇,按
如图所示(夹持装置等略)连接好装置。用电热套加热,使反应温度迅
速升到140℃,再由恒压滴液漏斗慢慢滴加无水乙醇进行实验。下列
说法错误的是
A.仪器a可以更换为球形冷凝管
B.b中放置冰水,便于冷凝乙醚
C.用电热套而不用酒精灯加热,可避免乙醚蒸气燃烧或爆炸
D.实验开始后升温过慢会使乙醇来不及反应而挥发,乙醚产率降低
8.研究磷的卤化物发现:PCl +BBr =Cl PBBr 、固态PCl 和PBr 结构分别为[PCl ]+[PCl ]-和[PBr ]+Br-。
3 3 3 3 5 5 4 6 4
下列说法错误的是
A.化合物Cl PBBr 中含有配位键
3 3
B.PCl 和[PBr ]+的VSEPR模型是四面体形
3 4
C.Cl PBBr 和[PCl ]-中磷原子的杂化方式相同
3 3 6
D.PCl 和PBr 结构的差异是因为Br-半径较大,无法形成[PBr ]-
5 5 6
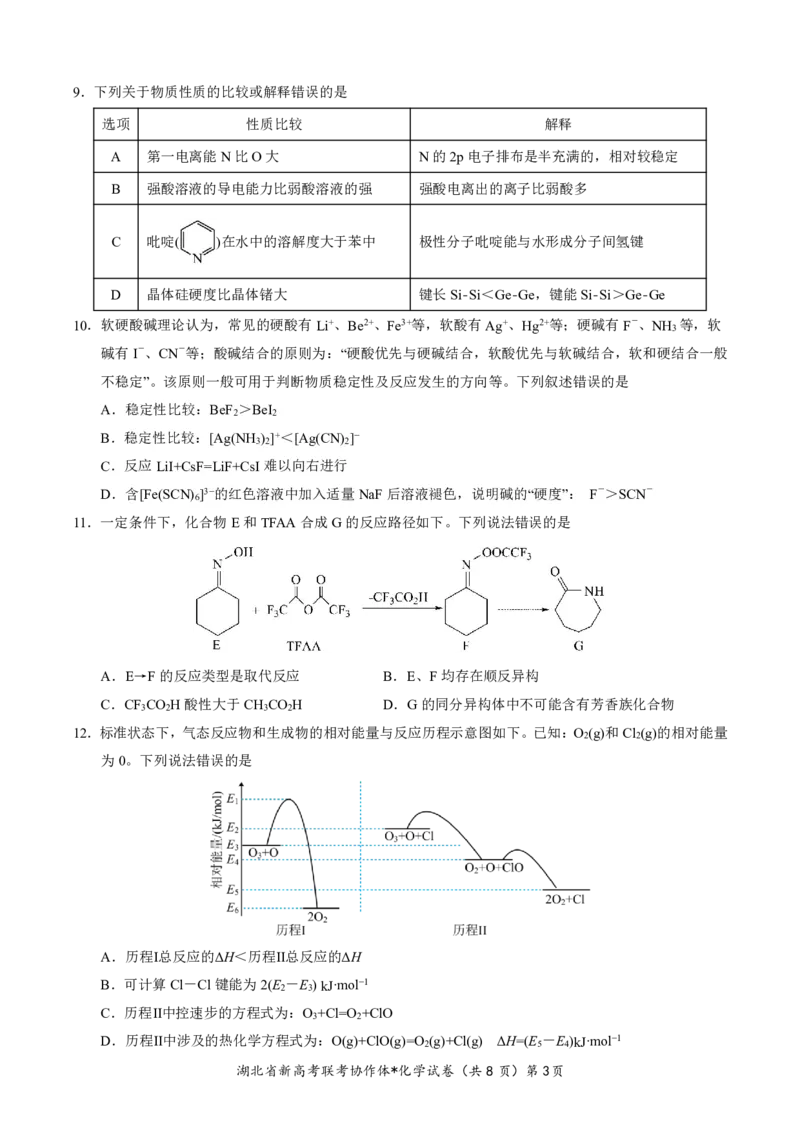
湖北省新高考联考协作体*化学试卷(共8页)第2页9.下列关于物质性质的比较或解释错误的是
选项 性质比较 解释
A 第一电离能N比O大 N的2p电子排布是半充满的,相对较稳定
B 强酸溶液的导电能力比弱酸溶液的强 强酸电离出的离子比弱酸多
C 吡啶( )在水中的溶解度大于苯中 极性分子吡啶能与水形成分子间氢键
D 晶体硅硬度比晶体锗大 键长Si-Si<Ge-Ge,键能Si-Si>Ge-Ge
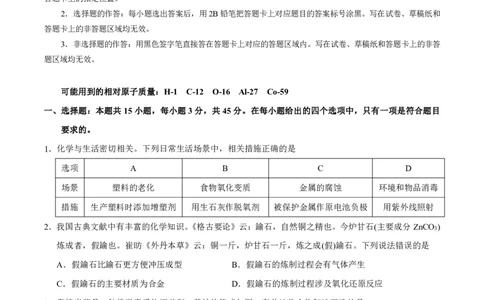
10.软硬酸碱理论认为,常见的硬酸有Li+、Be2+、Fe3+等,软酸有Ag+、Hg2+等;硬碱有F-、NH 等,软
3
碱有I-、CN-等;酸碱结合的原则为:“硬酸优先与硬碱结合,软酸优先与软碱结合,软和硬结合一般
不稳定”。该原则一般可用于判断物质稳定性及反应发生的方向等。下列叙述错误的是
A.稳定性比较:BeF >BeI
2 2
B.稳定性比较:[Ag(NH ) ]+<[Ag(CN) ]−
3 2 2
C.反应LiI+CsF=LiF+CsI难以向右进行
D.含[Fe(SCN) ]3−的红色溶液中加入适量NaF后溶液褪色,说明碱的“硬度”: F->SCN-
6
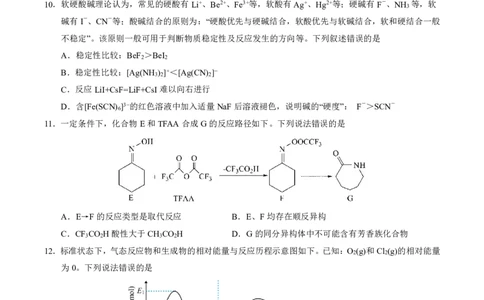
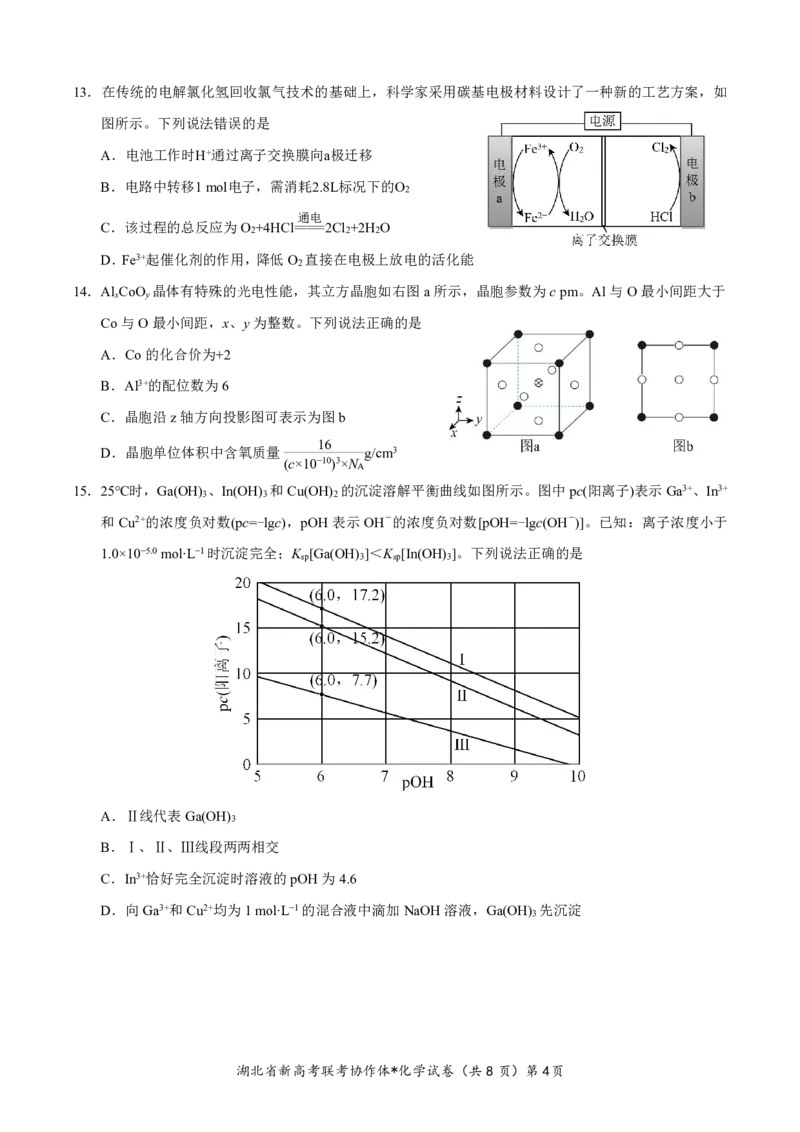
11.一定条件下,化合物E和TFAA合成G的反应路径如下。下列说法错误的是
A.E→F的反应类型是取代反应 B.E、F均存在顺反异构
C.CF CO H酸性大于CH CO H D.G的同分异构体中不可能含有芳香族化合物
3 2 3 2
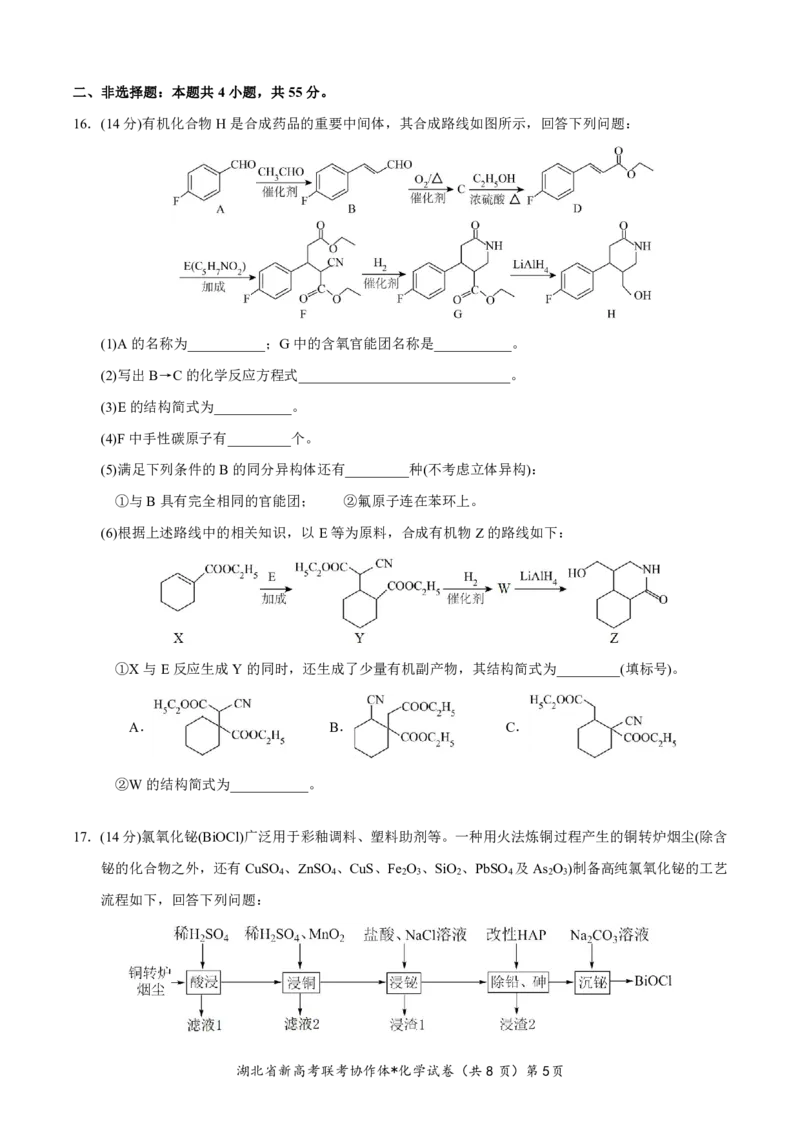
12.标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下。已知:O (g)和Cl (g)的相对能量
2 2
为0。下列说法错误的是
A.历程Ⅰ总反应的ΔH<历程Ⅱ总反应的ΔH
B.可计算Cl-Cl键能为2(E
2
-E
3
)kJ∙mol−1
C.历程Ⅱ中控速步的方程式为:O +Cl=O +ClO
3 2
D.历程Ⅱ中涉及的热化学方程式为:O(g)+ClO(g)=O
2
(g)+Cl(g) ΔH=(E
5
-E
4
)kJ∙mol−1
湖北省新高考联考协作体*化学试卷(共8页)第3页13.在传统的电解氯化氢回收氯气技术的基础上,科学家采用碳基电极材料设计了一种新的工艺方案,如
图所示。下列说法错误的是
A.电池工作时H+通过离子交换膜向a极迁移
B.电路中转移1mol电子,需消耗2.8L标况下的O
2
通电
C.该过程的总反应为O +4HCl=====2Cl +2H O
2 2 2
D.Fe3+起催化剂的作用,降低O 直接在电极上放电的活化能
2
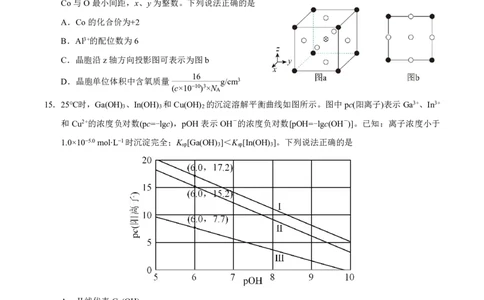
14.AlCoO 晶体有特殊的光电性能,其立方晶胞如右图a所示,晶胞参数为cpm。Al与O最小间距大于
x y
Co与O最小间距,x、y为整数。下列说法正确的是
A.Co的化合价为+2
B.Al3+的配位数为6
C.晶胞沿z轴方向投影图可表示为图b
16
D.晶胞单位体积中含氧质量 g/cm3
(c×10−10)3×N
A
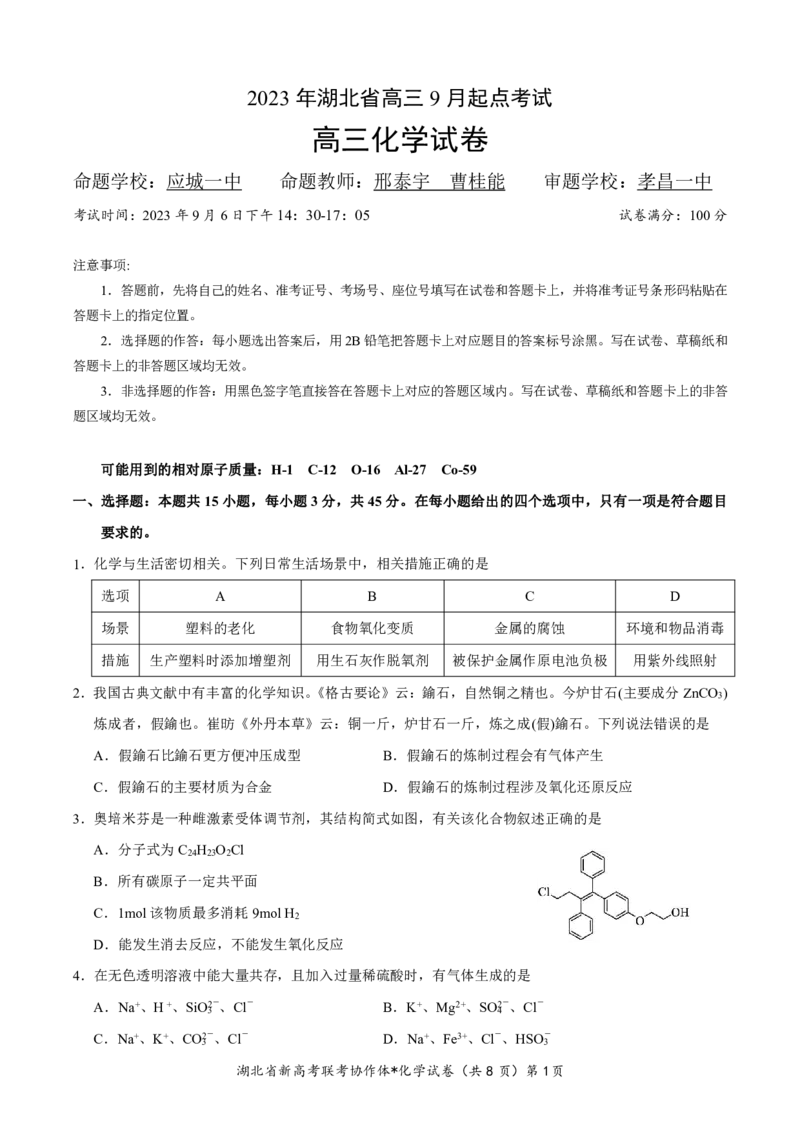
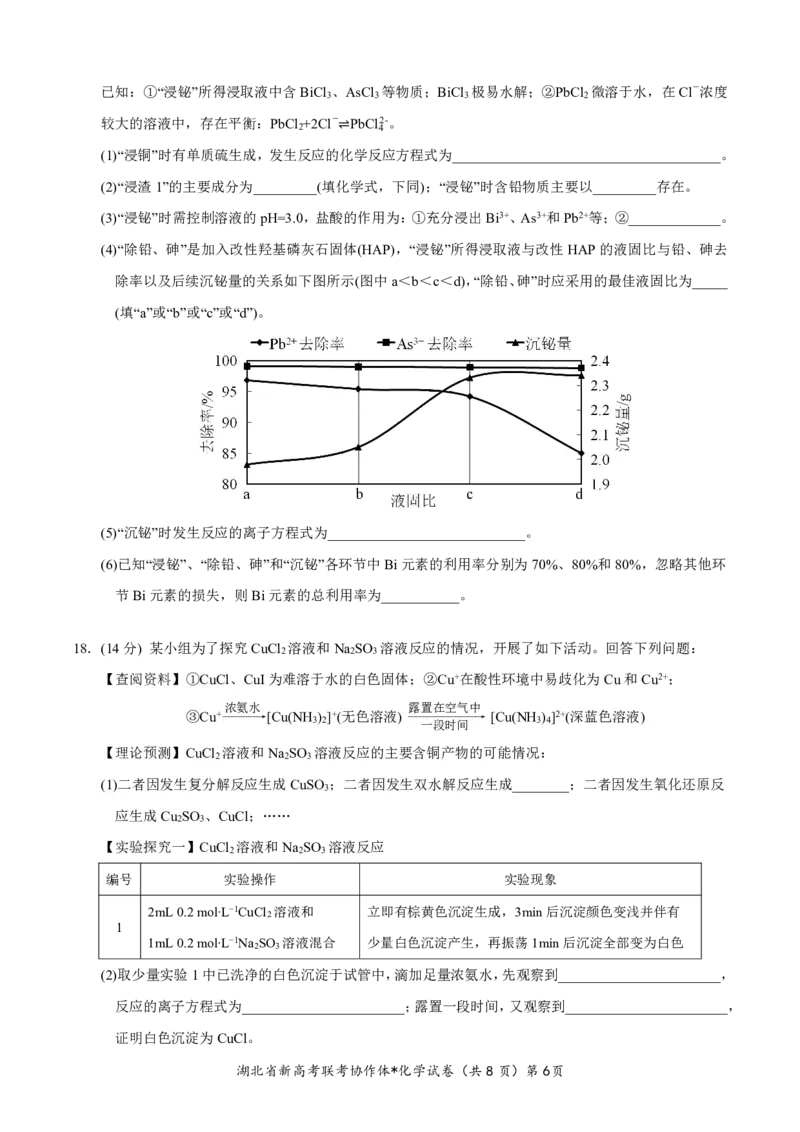
15.25℃时,Ga(OH) 、In(OH) 和Cu(OH) 的沉淀溶解平衡曲线如图所示。图中pc(阳离子)表示Ga3+、In3+
3 3 2
和Cu2+的浓度负对数(pc=-lgc),pOH表示OH-的浓度负对数[pOH=-lgc(OH-)]。已知:离子浓度小于
1.0×10−5.0mol∙L−1时沉淀完全;K [Ga(OH) ]<K [In(OH) ]。下列说法正确的是
sp 3 sp 3
A.Ⅱ线代表Ga(OH)
3
B.Ⅰ、Ⅱ、Ⅲ线段两两相交
C.In3+恰好完全沉淀时溶液的pOH为4.6
D.向Ga3+和Cu2+均为1mol∙L−1的混合液中滴加NaOH溶液,Ga(OH) 先沉淀
3
湖北省新高考联考协作体*化学试卷(共8页)第4页二、非选择题:本题共4小题,共55分。
16.(14分)有机化合物H是合成药品的重要中间体,其合成路线如图所示,回答下列问题:
(1)A的名称为___________;G中的含氧官能团名称是___________。
(2)写出B→C的化学反应方程式______________________________。
(3)E的结构简式为___________。
(4)F中手性碳原子有_________个。
(5)满足下列条件的B的同分异构体还有_________种(不考虑立体异构):
①与B具有完全相同的官能团; ②氟原子连在苯环上。
(6)根据上述路线中的相关知识,以E等为原料,合成有机物Z的路线如下:
①X与E反应生成Y的同时,还生成了少量有机副产物,其结构简式为_________(填标号)。
A. B. C.
②W的结构简式为___________。
17.(14分)氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂等。一种用火法炼铜过程产生的铜转炉烟尘(除含
铋的化合物之外,还有CuSO 、ZnSO 、CuS、Fe O 、SiO 、PbSO 及As O )制备高纯氯氧化铋的工艺
4 4 2 3 2 4 2 3
流程如下,回答下列问题:
湖北省新高考联考协作体*化学试卷(共8页)第5页已知:①“浸铋”所得浸取液中含BiCl 、AsCl 等物质;BiCl 极易水解;②PbCl 微溶于水,在Cl-浓度
3 3 3 2
较大的溶液中,存在平衡:PbCl +2Cl- PbCl2-。
2 4
(1)“浸铜”时有单质硫生成,发生反应的⇌化学反应方程式为______________________________________。
(2)“浸渣1”的主要成分为_________(填化学式,下同);“浸铋”时含铅物质主要以_________存在。
(3)“浸铋”时需控制溶液的pH=3.0,盐酸的作用为:①充分浸出Bi3+、As3+和Pb2+等;②_____________。
(4)“除铅、砷”是加入改性羟基磷灰石固体(HAP),“浸铋”所得浸取液与改性HAP的液固比与铅、砷去
除率以及后续沉铋量的关系如下图所示(图中a<b<c<d),“除铅、砷”时应采用的最佳液固比为_____
(填“a”或“b”或“c”或“d”)。
(5)“沉铋”时发生反应的离子方程式为____________________________。
(6)已知“浸铋”、“除铅、砷”和“沉铋”各环节中Bi元素的利用率分别为70%、80%和80%,忽略其他环
节Bi元素的损失,则Bi元素的总利用率为___________。
18.(14分) 某小组为了探究CuCl 溶液和Na SO 溶液反应的情况,开展了如下活动。回答下列问题:
2 2 3
【查阅资料】①CuCl、CuI为难溶于水的白色固体;②Cu+在酸性环境中易歧化为Cu和Cu2+;
浓氨水 露置在空气中
③Cu+――――→[Cu(NH ) ]+(无色溶液) ――――――――→ [Cu(NH ) ]2+(深蓝色溶液)
3 2 一段时间 3 4
【理论预测】CuCl 溶液和Na SO 溶液反应的主要含铜产物的可能情况:
2 2 3
(1)二者因发生复分解反应生成CuSO ;二者因发生双水解反应生成________;二者因发生氧化还原反
3
应生成Cu SO 、CuCl;……
2 3
【实验探究一】CuCl 溶液和Na SO 溶液反应
2 2 3
编号 实验操作 实验现象
2mL0.2mol∙L−1CuCl 溶液和 立即有棕黄色沉淀生成,3min后沉淀颜色变浅并伴有
2
1
1mL0.2mol∙L−1Na SO 溶液混合 少量白色沉淀产生,再振荡1min后沉淀全部变为白色
2 3
(2)取少量实验1中已洗净的白色沉淀于试管中,滴加足量浓氨水,先观察到_______________________,
反应的离子方程式为_______________________;露置一段时间,又观察到_______________________,
证明白色沉淀为CuCl。
湖北省新高考联考协作体*化学试卷(共8页)第6页【实验探究二】棕黄色沉淀的成分探究
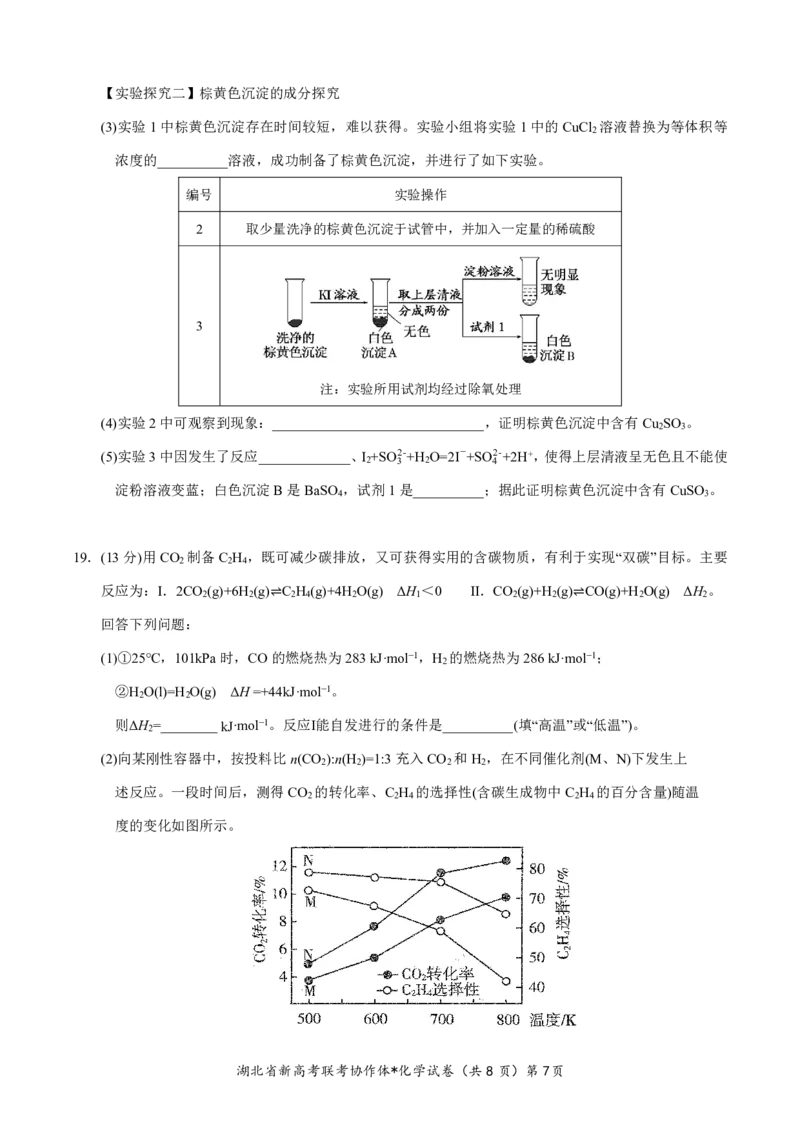
(3)实验1中棕黄色沉淀存在时间较短,难以获得。实验小组将实验1中的CuCl 溶液替换为等体积等
2
浓度的__________溶液,成功制备了棕黄色沉淀,并进行了如下实验。
编号 实验操作
2 取少量洗净的棕黄色沉淀于试管中,并加入一定量的稀硫酸
3
注:实验所用试剂均经过除氧处理
(4)实验2中可观察到现象:______________________________,证明棕黄色沉淀中含有Cu SO 。
2 3
(5)实验3中因发生了反应_____________、I +SO2-+H O=2I-+SO2-+2H+,使得上层清液呈无色且不能使
2 3 2 4
淀粉溶液变蓝;白色沉淀B是BaSO ,试剂1是__________;据此证明棕黄色沉淀中含有CuSO 。
4 3
19.(13分)用CO 制备C H ,既可减少碳排放,又可获得实用的含碳物质,有利于实现“双碳”目标。主要
2 2 4
反应为:Ⅰ.2CO (g)+6H (g) C H (g)+4H O(g) ΔH <0 Ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH 。
2 2 2 4 2 1 2 2 2 2
回答下列问题: ⇌ ⇌
(1)①25℃,101kPa时,CO的燃烧热为283kJ·mol−1,H 的燃烧热为286kJ·mol−1;
2
②H O(l)=H O(g) ΔH=+44kJ·mol−1。
2 2
则ΔH
2
=________kJ∙mol−1。反应Ⅰ能自发进行的条件是__________(填“高温”或“低温”)。
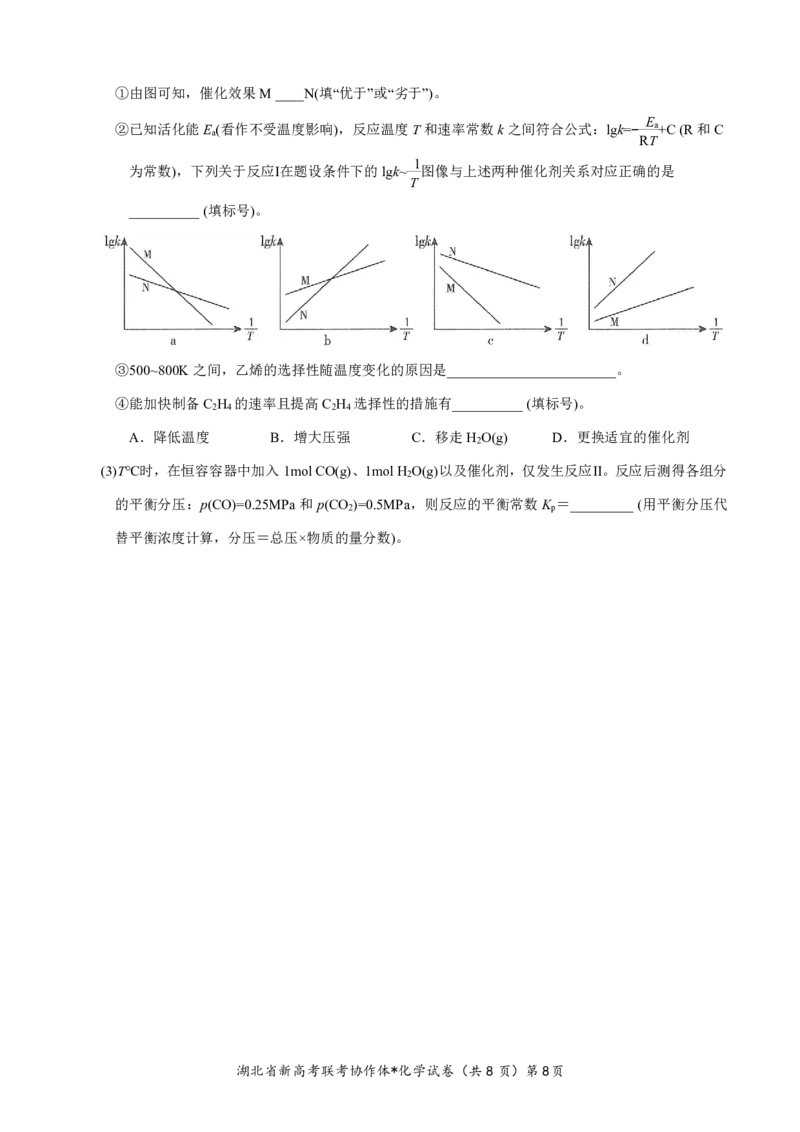
(2)向某刚性容器中,按投料比n(CO ):n(H )=1:3充入CO 和H ,在不同催化剂(M、N)下发生上
2 2 2 2
述反应。一段时间后,测得CO 的转化率、C H 的选择性(含碳生成物中C H 的百分含量)随温
2 2 4 2 4
度的变化如图所示。
湖北省新高考联考协作体*化学试卷(共8页)第7页①由图可知,催化效果M____N(填“优于”或“劣于”)。
E
②已知活化能E (看作不受温度影响),反应温度T和速率常数k之间符合公式:lgk=- a+C(R和C
a
RT
1
为常数),下列关于反应Ⅰ在题设条件下的lgk~ 图像与上述两种催化剂关系对应正确的是
T
__________(填标号)。
③500~800K之间,乙烯的选择性随温度变化的原因是________________________。
④能加快制备C H 的速率且提高C H 选择性的措施有__________(填标号)。
2 4 2 4
A.降低温度 B.增大压强 C.移走H O(g) D.更换适宜的催化剂
2
(3)T℃时,在恒容容器中加入1molCO(g)、1molH O(g)以及催化剂,仅发生反应Ⅱ。反应后测得各组分
2
的平衡分压:p(CO)=0.25MPa和p(CO )=0.5MPa,则反应的平衡常数K =_________(用平衡分压代
2 p
替平衡浓度计算,分压=总压×物质的量分数)。
湖北省新高考联考协作体*化学试卷(共8页)第8页