文档内容
绝密★启用前
2024 届高三入学摸底考试
化学
本试卷共6页。全卷满分100分,考试时间75分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答题卡上的
指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答题
区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作
答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
可能用到的相对原子质量:H 1 C 12 N 14 O16 Na23 S32 Cl 35.5 Cu 64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.化学与科技、生产、生活密切相关。下列说法正确的是
A.开发利用可燃冰有利于控制“温室效应”
B.聚乳酸等高分子材料在微生物的作用下可以降解为小分子,为消除“白色污染”带来了希望
C.用脱硫煤代替原煤作燃料有利于实现碳中和
D.利用纯碱可以处理泄漏的汽油
2.侯德榜联合制碱法的原理之一是NH +CO +H O+NaCl=NH C1+NaHCO ↓。下列说法正
3 2 2 4 3
确的是
A.基态N原子的轨道表示式为 .该轨道表示式违背了洪特规则.
B.p-pσ键电子云轮廓图为
C.氯化钠的电子式为
D. CO 、NH +、H O中心原子均为sp3杂化
2 4 2
3.设N 为阿伏加德罗常数的值,下列叙述中指定粒子数目--定大于N 的是
A A
A.常温常压下,质量为28g的N 和CO的混合气体中所含的分子数目
2
B.25 °C,1 L1mol. L-1的Na CO 溶液中含有的CO 2- 数目
2 3 3
C.足量锌与含2 mol H SO 的浓硫酸在加热条件下充分反应,所得混合气体的分子数目
2 4
D.25° C,1 LpH=14的Ba(OH) 溶液中含有的OH- 数目
2
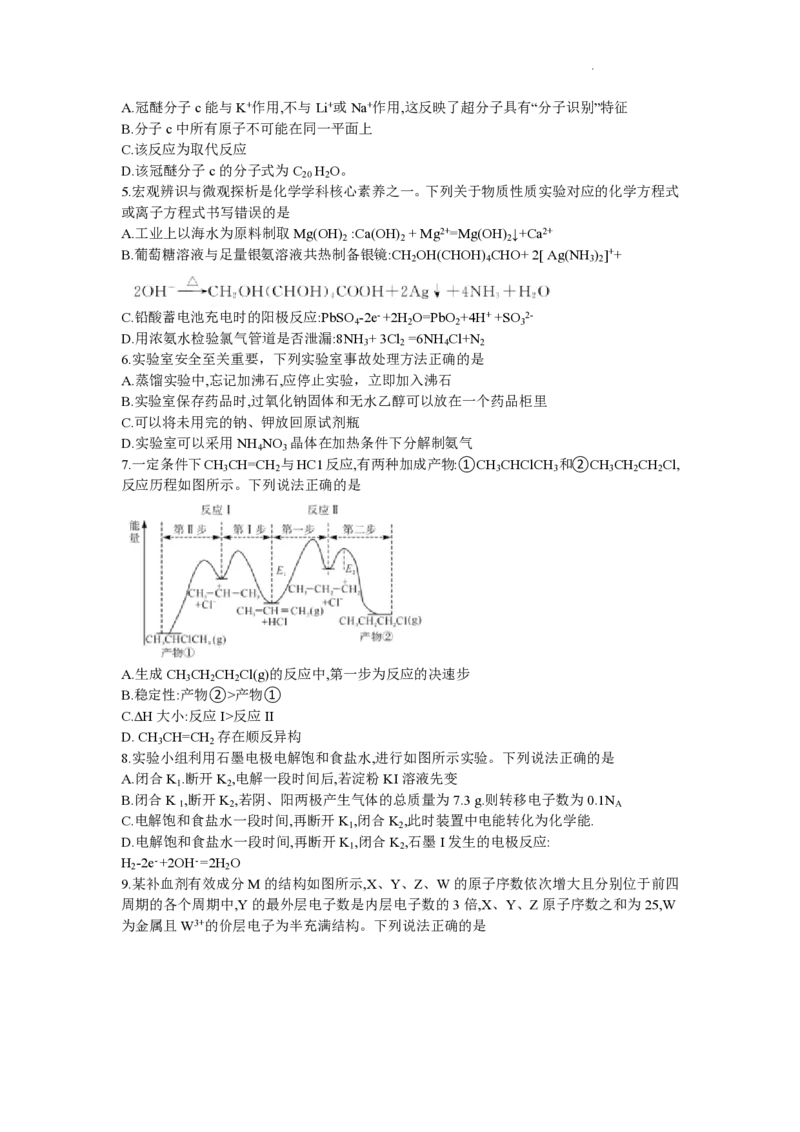
4.冠醚因分子结构形如皇冠而得名,某冠醚分子c(二苯并-18-冠- 6)可识别K+,其合成方法如
下。下列说法错误的是
学科网(北京)股份有限公司A.冠醚分子c能与K+作用,不与Li+或Na+作用,这反映了超分子具有“分子识别”特征
B.分子c中所有原子不可能在同一平面上
C.该反应为取代反应
D.该冠醚分子c的分子式为C H O。
20 2
5.宏观辨识与微观探析是化学学科核心素养之一。下列关于物质性质实验对应的化学方程式
或离子方程式书写错误的是
A.工业上以海水为原料制取Mg(OH) :Ca(OH) + Mg2+=Mg(OH) ↓+Ca2+
2 2 2
B.葡萄糖溶液与足量银氨溶液共热制备银镜:CH OH(CHOH) CHO+ 2[ Ag(NH ) ]++
2 4 3 2
C.铅酸蓄电池充电时的阳极反应:PbSO -2e- +2H O=PbO +4H+ +SO 2-
4 2 2 3
D.用浓氨水检验氯气管道是否泄漏:8NH + 3Cl =6NH Cl+N
3 2 4 2
6.实验室安全至关重要,下列实验室事故处理方法正确的是
A.蒸馏实验中,忘记加沸石,应停止实验,立即加入沸石
B.实验室保存药品时,过氧化钠固体和无水乙醇可以放在一个药品柜里
C.可以将未用完的钠、钾放回原试剂瓶
D.实验室可以采用NH NO 晶体在加热条件下分解制氨气
4 3
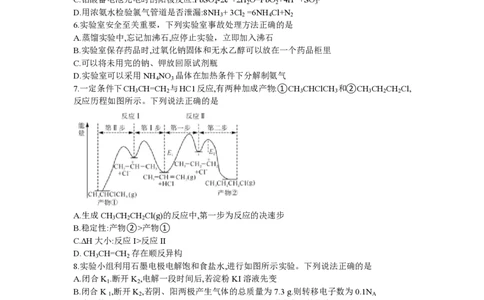
7.一定条件下CH CH=CH 与HC1反应,有两种加成产物:①CH CHClCH 和②CH CH CH Cl,
3 2 3 3 3 2 2
反应历程如图所示。下列说法正确的是
A.生成CH CH CH Cl(g)的反应中,第一步为反应的决速步
3 2 2
B.稳定性:产物②>产物①
C.∆H大小:反应I>反应II
D. CH CH=CH 存在顺反异构
3 2
8.实验小组利用石墨电极电解饱和食盐水,进行如图所示实验。下列说法正确的是
A.闭合K .断开K ,电解一段时间后,若淀粉KI溶液先变
1 2
B.闭合K ,断开K ,若阴、阳两极产生气体的总质量为7.3 g.则转移电子数为0.1N
1 2 A
C.电解饱和食盐水一段时间,再断开K ,闭合K ,此时装置中电能转化为化学能.
1 2
D.电解饱和食盐水一段时间,再断开K ,闭合K ,石墨I发生的电极反应:
1 2
H -2e- +2OH- =2H O
2 2
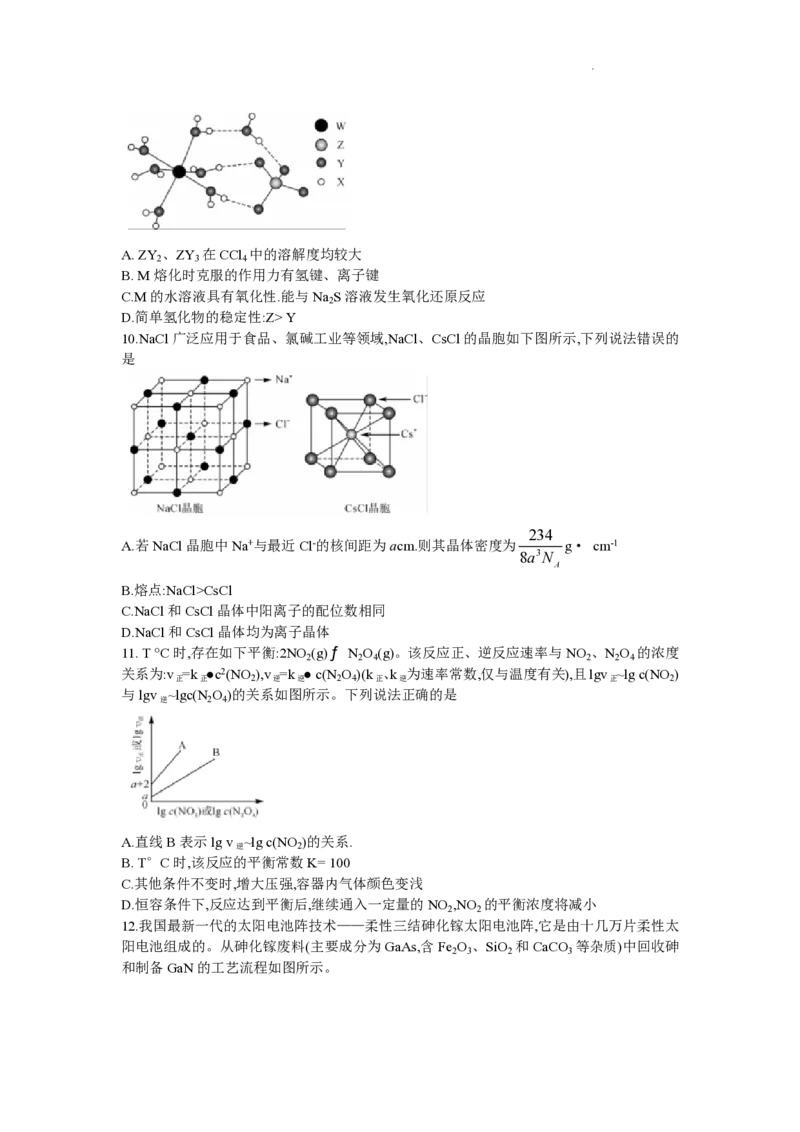
9.某补血剂有效成分M的结构如图所示,X、Y、Z、W的原子序数依次增大且分别位于前四
周期的各个周期中,Y的最外层电子数是内层电子数的3倍,X、Y、Z原子序数之和为25,W
为金属且W3+的价层电子为半充满结构。下列说法正确的是
学科网(北京)股份有限公司A. ZY 、ZY 在CCl 中的溶解度均较大
2 3 4
B. M熔化时克服的作用力有氢键、离子键
C.M的水溶液具有氧化性.能与Na S溶液发生氧化还原反应
2
D.简单氢化物的稳定性:Z> Y
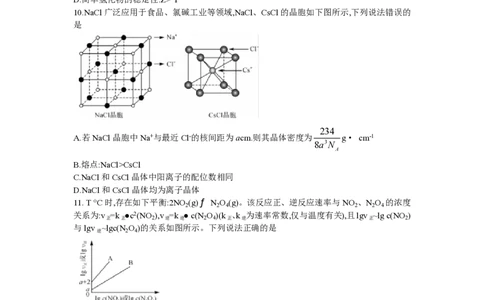
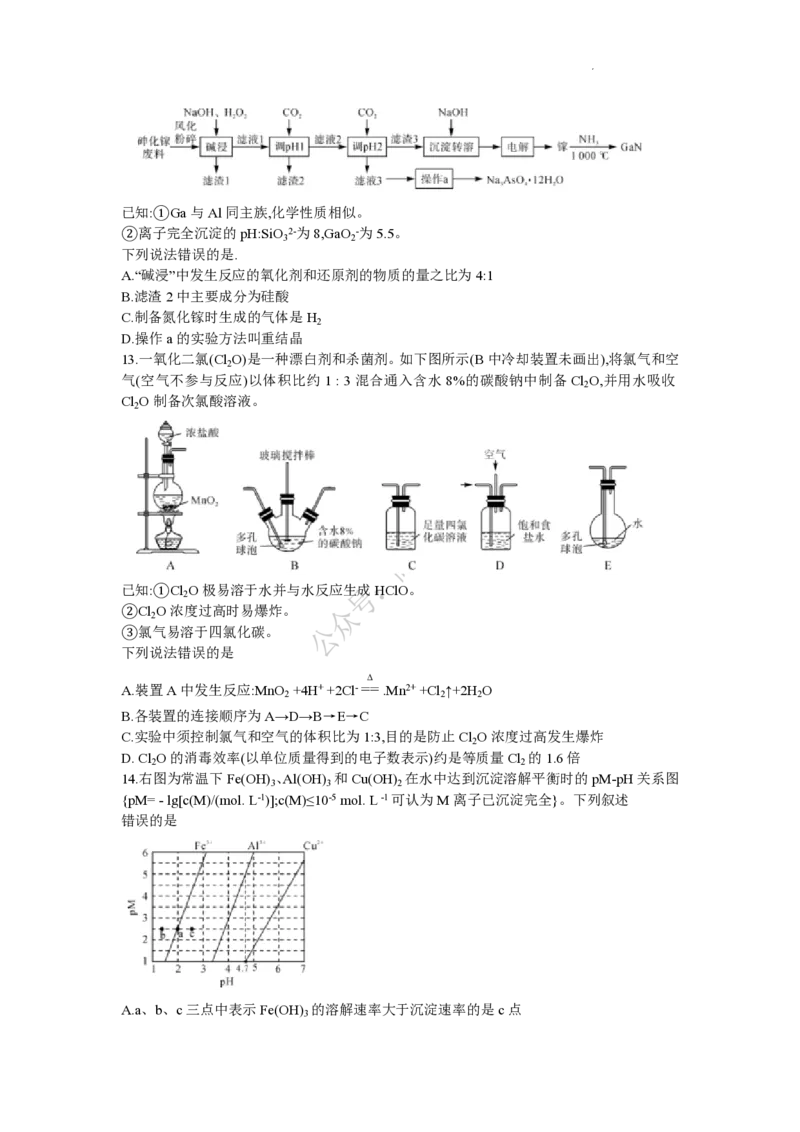
10.NaCl广泛应用于食品、氯碱工业等领域,NaCl、CsCl的晶胞如下图所示,下列说法错误的
是
234
A.若NaCl晶胞中Na+与最近Cl-的核间距为acm.则其晶体密度为 g· cm-1
8a3N
A
B.熔点:NaCl>CsCl
C.NaCl和CsCl晶体中阳离子的配位数相同
D.NaCl和CsCl晶体均为离子晶体
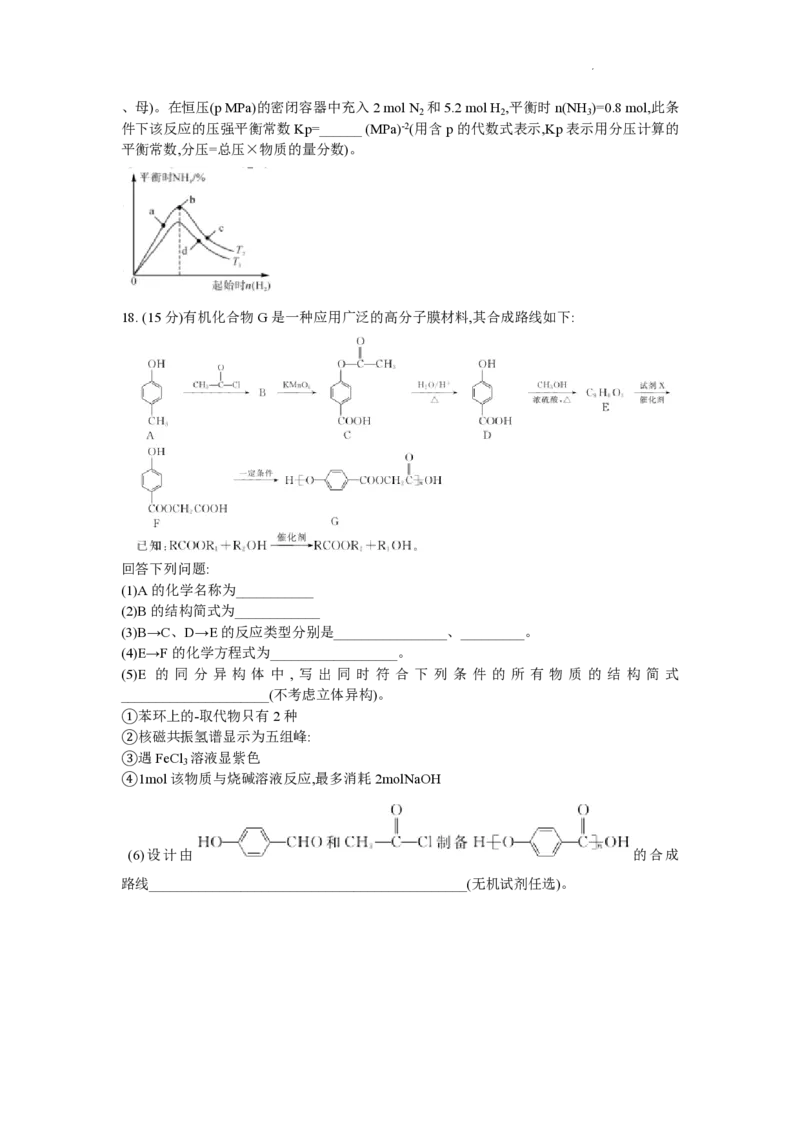
11. T °C时,存在如下平衡:2NO (g)ƒ N O (g)。该反应正、逆反应速率与NO 、N O 的浓度
2 2 4 2 2 4
关系为:v =k ●c2(NO ),v =k ● c(N O )(k 、k 为速率常数,仅与温度有关),且lgv ~lg c(NO )
正 正 2 逆 逆 2 4 正 逆 正 2
与lgv ~lgc(N O )的关系如图所示。下列说法正确的是
逆 2 4
A.直线B表示lg v ~lg c(NO )的关系.
逆 2
B. T°C时,该反应的平衡常数K= 100
C.其他条件不变时,增大压强,容器内气体颜色变浅
D.恒容条件下,反应达到平衡后,继续通入一定量的NO ,NO 的平衡浓度将减小
2 2
12.我国最新一代的太阳电池阵技术——柔性三结砷化镓太阳电池阵,它是由十几万片柔性太
阳电池组成的。从砷化镓废料(主要成分为GaAs,含Fe O 、SiO 和CaCO 等杂质)中回收砷
2 3 2 3
和制备GaN的工艺流程如图所示。
学科网(北京)股份有限公司已知:①Ga与Al同主族,化学性质相似。
②离子完全沉淀的pH:SiO 2-为8,GaO -为5.5。
3 2
下列说法错误的是.
A.“碱浸”中发生反应的氧化剂和还原剂的物质的量之比为4:1
B.滤渣2中主要成分为硅酸
C.制备氮化镓时生成的气体是H
2
D.操作a的实验方法叫重结晶
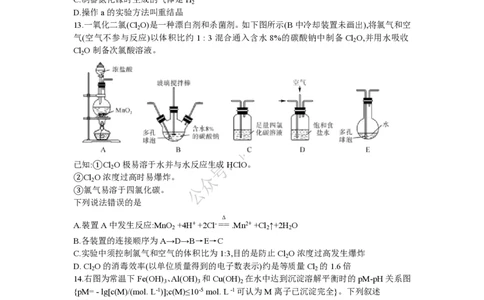
13.一氧化二氯(Cl O)是一种漂白剂和杀菌剂。如下图所示(B中冷却装置未画出),将氯气和空
2
气(空气不参与反应)以体积比约1 : 3混合通入含水8%的碳酸钠中制备Cl O,并用水吸收
2
Cl O制备次氯酸溶液。
2
已知:①Cl O极易溶于水并与水反应生成HClO。
2
②Cl O浓度过高时易爆炸。
2
③氯气易溶于四氯化碳。
下列说法错误的是
A.裝置A中发生反应:MnO +4H+ +2Cl-==.Mn2+ +Cl ↑+2H O
2 2 2
B.各装置的连接顺序为A→D→B→E→C
C.实验中须控制氯气和空气的体积比为1:3,目的是防止Cl O浓度过高发生爆炸
2
D. Cl O的消毒效率(以单位质量得到的电子数表示)约是等质量Cl 的1.6倍
2 2
14.右图为常温下Fe(OH) 、Al(OH) 和Cu(OH) 在水中达到沉淀溶解平衡时的pM-pH关系图
3 3 2
{pM= - lg[c(M)/(mol. L-1)];c(M)≤10-5 mol. L -1可认为M离子已沉淀完全}。下列叙述
错误的是
A.a、b、c三点中表示Fe(OH) 的溶解速率大于沉淀速率的是c点
3
学科网(北京)股份有限公司B.向三种沉淀中逐滴滴加盐酸.最先溶解的是Cu(OH)
2
C. K [Al(OH) ]≈10-23
sp 3
D. Al3+ .Cu2+混合溶液中,当c(Cu2+ )=0.01 mol. L-1时,二者不会同时沉淀
二、非选择题:本题共4小题,共58分。
15. (15分)过硫酸钾(K S O )可用作破胶剂、聚合促进剂、氧化剂、分析试剂等, 100°C时分
2 2 8
解。实验室模拟制备过硫酸钾并进行相关探究。回答下列问题:
I.利用电解法制备过硫酸钾,同时可制备H O 的方法如下:
2 2
(1)过硫酸钾(K S O )中硫元素处于最高正价。则1 mol K S O 中过氧键的数目为____ N 。
2 2 8 2 2 8 A
(2)“电解”时发生反应的离子方程式为______________________
(3)Y为____________________(填化学式)。
II.某同学预测过硫酸钾的分解产物有K S O 、SO 、SO 和O ,并用下图装置验证分解产物
2 2 8 3 2 2
中含有SO 和SO (夹持及加热仪器已省略)。
3 2
(4)实验时,通入He排尽装置中的空气后,应先加热装置_____(填“A"或“B")。
(5)装置 B 中石棉绒的作用为_________________________________,装置 D 中的试剂为
_______________。
(6)装置E和装置D是否可以调换顺序?__________(填“是”或“否”),原因是____________。
16. (14分)-种由含铜废催化剂(主要成分为Cu和少量Fe、Fe O 、CuO、SiO 等)为原料制备
2 3 2
CuCl的工艺流程如下:
已知:CuCl为白色粉末,微溶于水,易溶于Cl-浓度较大的体系{CuCl+Cl-ƒ [CuCl ]-},不溶
2
于乙醇,有水存在时易被O 氧化。
2
回答下列问题:
(1)实验室需450mL1.84 mol●L-1H SO 溶液,配制时需量取_______mL98%的硫酸溶液(密度为
2 4
1.84g. mL-1)。
(2)“浸取”时,H O 的实际用量远远超过理论用量,可能原因是__________________.
2 2
(3)“反应”时,CuSO 与Na SO 、NaCl在溶液中反应生成CuCl沉淀的离子方程式为_______。
4 2 3
当n(NaCl) : n(CuSO )比值逐渐增大时,CuCl产率先增大后减小,原因是_______________.
4
(4)为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品mg,
学科网(北京)股份有限公司将其置于过量的FeCl 溶液中完全溶解,加入适量稀硫酸,用a mol●L-1 K Cr O 溶液滴定到终
3 2 2 7
点,消耗K Cr O 溶液b mL,Cr O 2-被还原为Cr3+。 样品中CuCl的质量分数为_____%(已知
2 2 7 2 7
滴定过程发生的反应为Cr O 2- +6Fe2++ 14H+==2Cr3+ +6Fe3+ +7H O,不考虑Cr O 2-氧化C1 )。
2 7 2 2 7
(5)①已知:CuCl的熔点为326°C,能升华,熔化呈液态时不导电。则CuCl晶体属于____(填晶
体类型)。
1 1
②若晶胞中a、c原子的分数坐标分别为(0,0,0)、( ,,1),则b原子的分数坐标为______。
2 2
17.(14分)氨对人类的生存和发展有着重要意义.1909年德国化学家哈伯在实验室中首次利用
氮气与氢气反应合成氨,实现了人工固氮。回答下列问题:
1 3
(1)根据如图数据计算反应 N (g)+ H (g)=NH (g)的△H=_______.
2 2 3
2 2
(2)针对反应速率与平衡产率的矛盾.我国科学家提出了两种解决方案。
①方案一:使用Fe -TiO xH 双催化剂,通过光辐射产生温差(如体系温度为495 °C时,Fe
2- y
的
温度为547 °C,而TiO xH 的温度为415 °C),使N≡N在_____ (填“ 热Fe”或“冷Ti",下同)
2- y
表面断裂,氨气在______表面生成,有利于提高合成氨的反应速率和平衡产率。
②方案二:使用M-LiH复合催化剂。催化剂组成及反应温度对合成氨反应速率影响如图所示。
下列说法错误的是.______(填标号)。
A.催化剂能够改变反应路径,降低反应活化能
B.相同条件下,复合催化剂更有利于提高合成氨反应速率
C.高温下,使用复合催化剂更有利于提高氨的平衡产率
(3)在其他条件不变的情况下,改变起始时氢气的物质的量对工业合成氨反应[N2+3H2ƒ
2NH ]的影响如图所示(图中T表示温度)。
3
图像中T 和T 的关系是:T ______T (填“>”“<”或“=”)。a、b、c、d四点所处的平衡状态中,
2 1 1 2
反应物N 的转化率最高的是____点(填字
2
学科网(北京)股份有限公司、母)。在恒压(p MPa)的密闭容器中充入2 mol N 和5.2 mol H ,平衡时n(NH )=0.8 mol,此条
2 2 3
件下该反应的压强平衡常数Kp=______ (MPa)-2(用含p的代数式表示,Kp表示用分压计算的
平衡常数,分压=总压×物质的量分数)。
18. (15分)有机化合物G是一种应用广泛的高分子膜材料,其合成路线如下:
回答下列问题:
(1)A的化学名称为___________
(2)B的结构简式为____________
(3)B→C、D→E的反应类型分别是________________、_________。
(4)E→F的化学方程式为__________________。
(5)E 的 同 分 异 构 体 中 , 写 出 同 时 符 合 下 列 条 件 的 所 有 物 质 的 结 构 简 式
_____________________(不考虑立体异构)。
①苯环上的-取代物只有2种
②核磁共振氢谱显示为五组峰:
③遇FeCl 溶液显紫色
3
④1mol该物质与烧碱溶液反应,最多消耗2molNaOH
(6)设计由 的合成
路线_____________________________________________(无机试剂任选)。
学科网(北京)股份有限公司