文档内容
重庆市拔尖强基联盟 2023-2024 学年高三十月联合考试
化学试题
(满分100分,75分钟)
注意事项:
1.答卷前,请考生务必将自己的姓名、班级、考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改
动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上,写在
本试卷上无效。
3.考试结束后,请一定将答题卡上交。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Al 27 S 32 Fe 56 Co 59 Zn 65
Ga 70 Ba 137
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1. 8月29日,华为Mate60 Pro横空出世,国产麒麟9000s芯片闪耀登场。华为的坚毅不屈成就了中国芯,
不仅值得我们骄傲,更值得我们每个中国人学习!大国制造彰显中国实力,化学材料助力科技成果的转化
与应用。下列说法错误的是
A. 制造5G芯片的氮化铝晶圆属于无机非金属材料
B. 高纯度的二氧化硅被广泛用于制作计算机芯片
C. 华为首创的液冷散热技术所用的石墨烯材料是新型无机非金属材料
D. Mate60 Pro部分机型后盖采用“锦纤”材质与合金完美契合,其中合金属于金属材料
2. 下列说法正确的是
A. Fe分别与Cl、S反应,产物中Fe的化合价相同
2
B. Cu分别与浓硝酸、稀硝酸反应,生成的产物完全相同
.
C CO 分别与NaO、CaO反应,反应类型相同
2 2 2
D. Be分别与盐酸、氢氧化钠溶液反应,生成的气体相同
3. 下列离子方程式书写错误的是
A. SO 通入双氧水中:
2
第1页/共11页
学科网(北京)股份有限公司B. NaOH浓溶液与饱和NH Cl溶液:
4
C. Pb与Fe (SO ) 溶液:
2 4 3
D. Ca(HCO ) 与澄清石灰水:
3 2
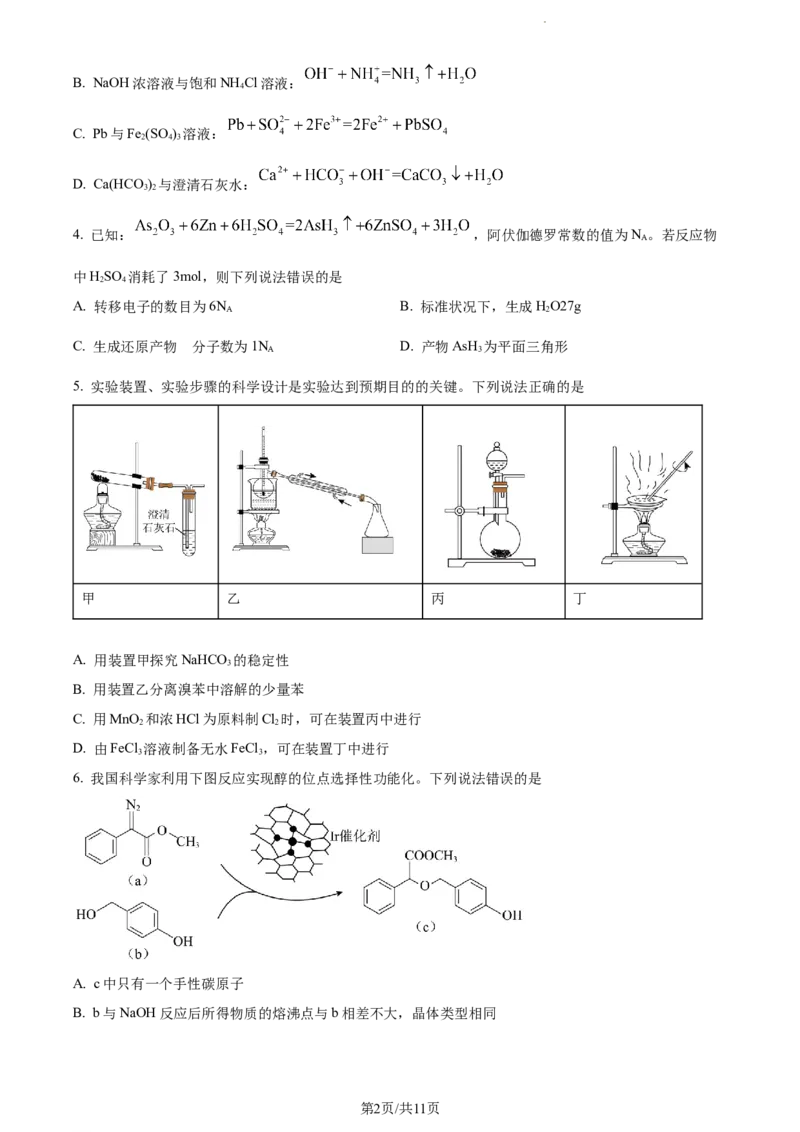
4. 已知: ,阿伏伽德罗常数的值为N 。若反应物
A
中HSO 消耗了3mol,则下列说法错误的是
2 4
A. 转移电子的数目为6N B. 标准状况下,生成HO27g
A 2
的
C. 生成还原产物 分子数为1N D. 产物AsH 为平面三角形
A 3
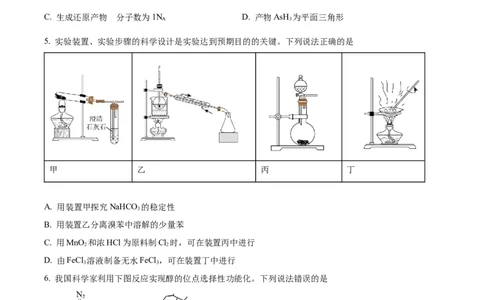
5. 实验装置、实验步骤的科学设计是实验达到预期目的的关键。下列说法正确的是
甲 乙 丙 丁
A. 用装置甲探究NaHCO 的稳定性
3
B. 用装置乙分离溴苯中溶解的少量苯
C. 用MnO 和浓HCl为原料制Cl 时,可在装置丙中进行
2 2
D. 由FeCl 溶液制备无水FeCl ,可在装置丁中进行
3 3
6. 我国科学家利用下图反应实现醇的位点选择性功能化。下列说法错误的是
A. c中只有一个手性碳原子
B. b与NaOH反应后所得物质的熔沸点与b相差不大,晶体类型相同
第2页/共11页
学科网(北京)股份有限公司C. a、b、c三种物质中,b在水中的溶解度最大
D. 已知基态铱(Ir)的价电子排布式为5d76s2,则Ir属于第Ⅷ族元素
7. 瓜环[n](n=5,6,7,8…)是一种具有大杯空腔、两端开口的化合物(结构如图),在分子开关、催化剂、
药物载体等方面有广泛应用。瓜环[n]可由 和HCHO在一定条件下合成。
瓜环[n]: 瓜环[7]:
下列说法错误的是
A. 的分子式为C HNO
4 7 4 2
B. 分子间可能存在不同类型的氢键
C. 生成瓜环[n]的反应中,有π键断裂
D. 合成1mol瓜环[7]时,有14mol水生成
8. 下列实验操作、现象和结论(或解释),均正确的是
选
操作 现象 结论(或解释)
项
向盛有2mL0.1mol·L-1NaCl溶液的试管中滴加2滴 先生成白色沉
A 0.1mol·L-1AgNO 溶液;振荡试管,然后再向其中滴加 淀,后沉淀由白 K (AgCl)>Ksp(AgI)
3 sp
4滴0.1mol·L-1KI溶液 色变为黄色
取2mL某溶液于试管中,滴加少量稀硝酸,再滴加几
B 有血红色出现 原溶液中一定含有Fe3+
滴KSCN溶液
溶液从蓝色变为 稳定性:[CuCl ]2-
C 向CuSO 溶液中加入NaCl固体 4
4 黄色 <[Cu(H O) ]2+
2 4
取少量某溶液于试管中,加入NaOH浓溶液并加热。 蓝色石蕊试纸变
D 原溶液中一定含有
用湿润的蓝色石蕊试纸检验产生的气体 红
第3页/共11页
学科网(北京)股份有限公司A. A B. B C. C D. D
的
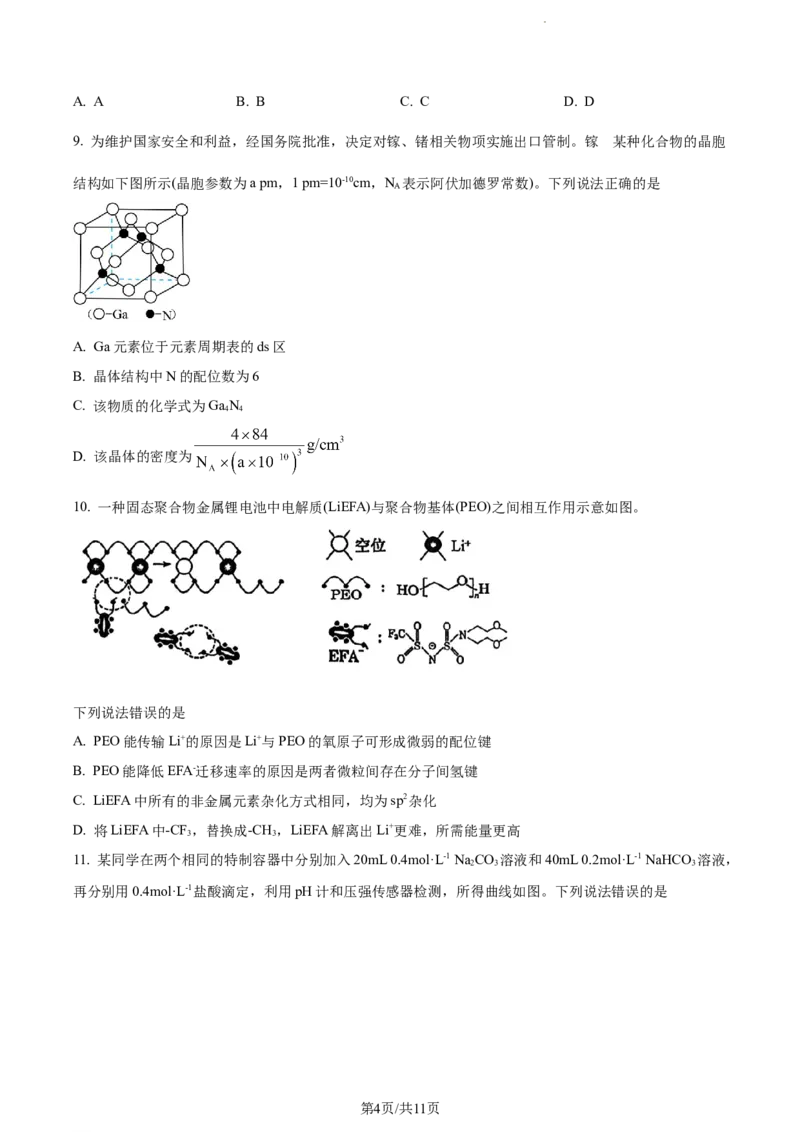
9. 为维护国家安全和利益,经国务院批准,决定对镓、锗相关物项实施出口管制。镓 某种化合物的晶胞
结构如下图所示(晶胞参数为a pm,1 pm=10-10cm,N 表示阿伏加德罗常数)。下列说法正确的是
A
A. Ga元素位于元素周期表的ds区
B. 晶体结构中N的配位数为6
C. 该物质的化学式为GaN
4 4
D. 该晶体的密度为
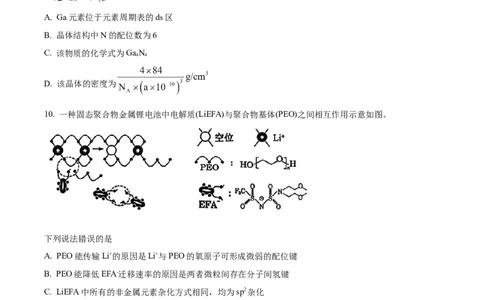
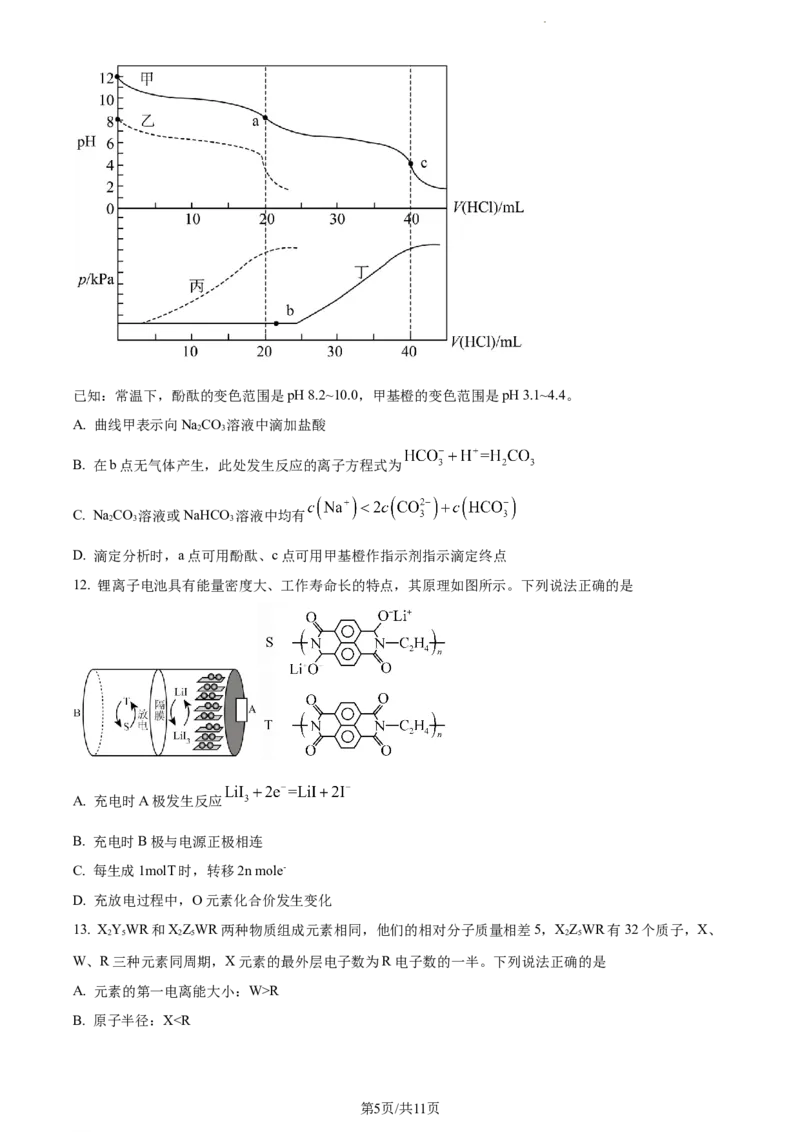
10. 一种固态聚合物金属锂电池中电解质(LiEFA)与聚合物基体(PEO)之间相互作用示意如图。
下列说法错误的是
A. PEO能传输Li+的原因是Li+与PEO的氧原子可形成微弱的配位键
B. PEO能降低EFA-迁移速率的原因是两者微粒间存在分子间氢键
C. LiEFA中所有的非金属元素杂化方式相同,均为sp2杂化
D. 将LiEFA中-CF,替换成-CH,LiEFA解离出Li+更难,所需能量更高
3 3
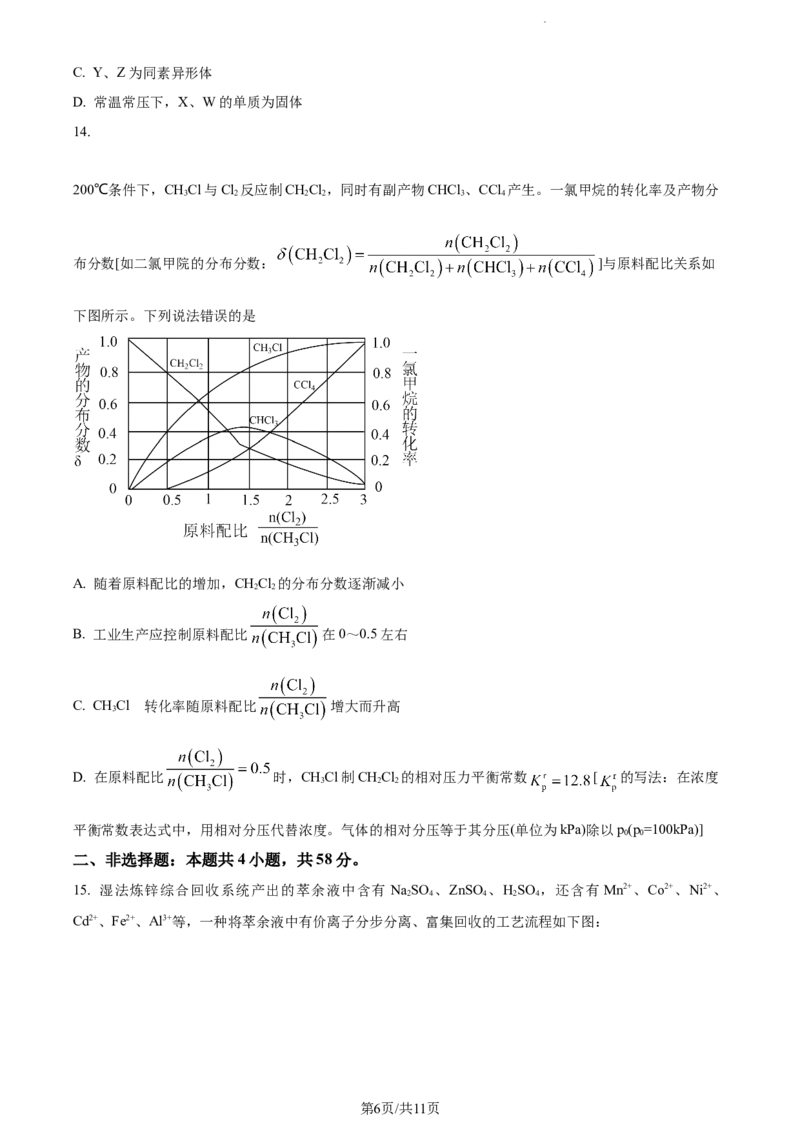
11. 某同学在两个相同的特制容器中分别加入20mL 0.4mol·L-1 NaCO 溶液和40mL 0.2mol·L-1 NaHCO 溶液,
2 3 3
再分别用0.4mol·L-1盐酸滴定,利用pH计和压强传感器检测,所得曲线如图。下列说法错误的是
第4页/共11页
学科网(北京)股份有限公司已知:常温下,酚酞的变色范围是pH 8.2~10.0,甲基橙的变色范围是pH 3.1~4.4。
A. 曲线甲表示向NaCO 溶液中滴加盐酸
2 3
B. 在b点无气体产生,此处发生反应的离子方程式为
C. NaCO 溶液或NaHCO 溶液中均有
2 3 3
D. 滴定分析时,a点可用酚酞、c点可用甲基橙作指示剂指示滴定终点
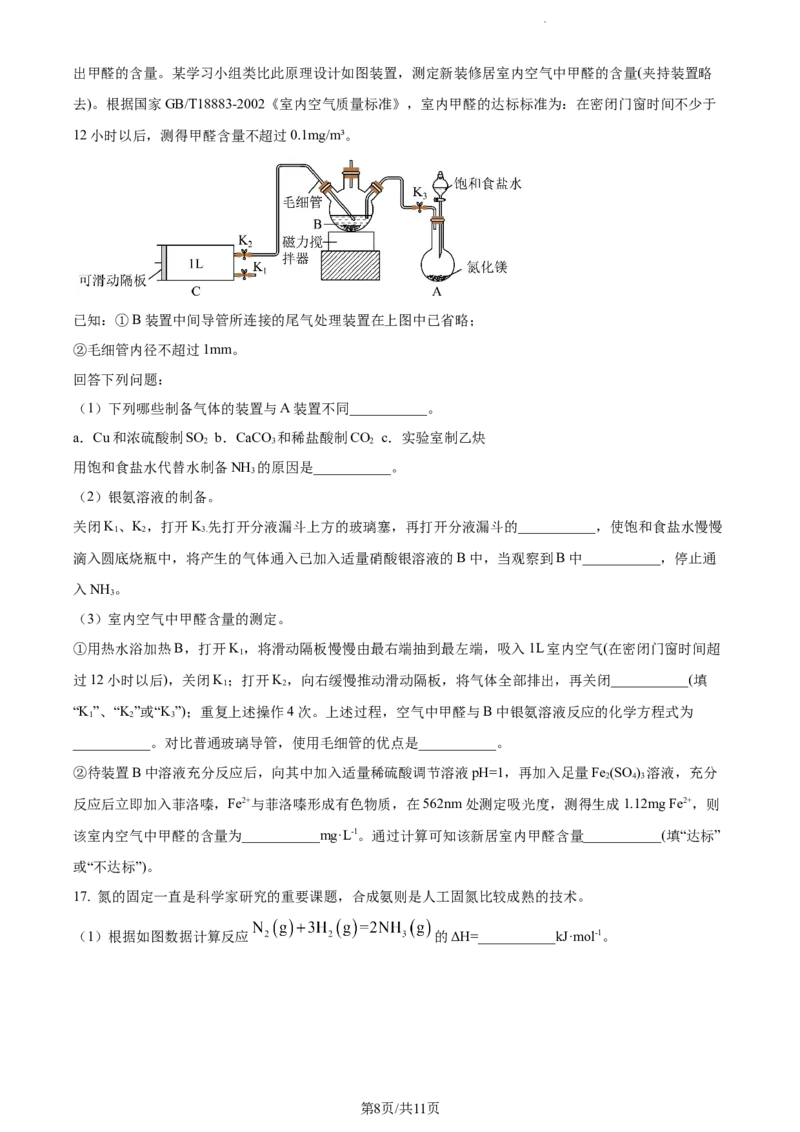
12. 锂离子电池具有能量密度大、工作寿命长的特点,其原理如图所示。下列说法正确的是
A. 充电时A极发生反应
B. 充电时B极与电源正极相连
C. 每生成1molT时,转移2n mole-
D. 充放电过程中,O元素化合价发生变化
13. XYWR和XZWR两种物质组成元素相同,他们的相对分子质量相差5,XZWR有32个质子,X、
2 5 2 5 2 5
W、R三种元素同周期,X元素的最外层电子数为R电子数的一半。下列说法正确的是
A. 元素的第一电离能大小:W>R
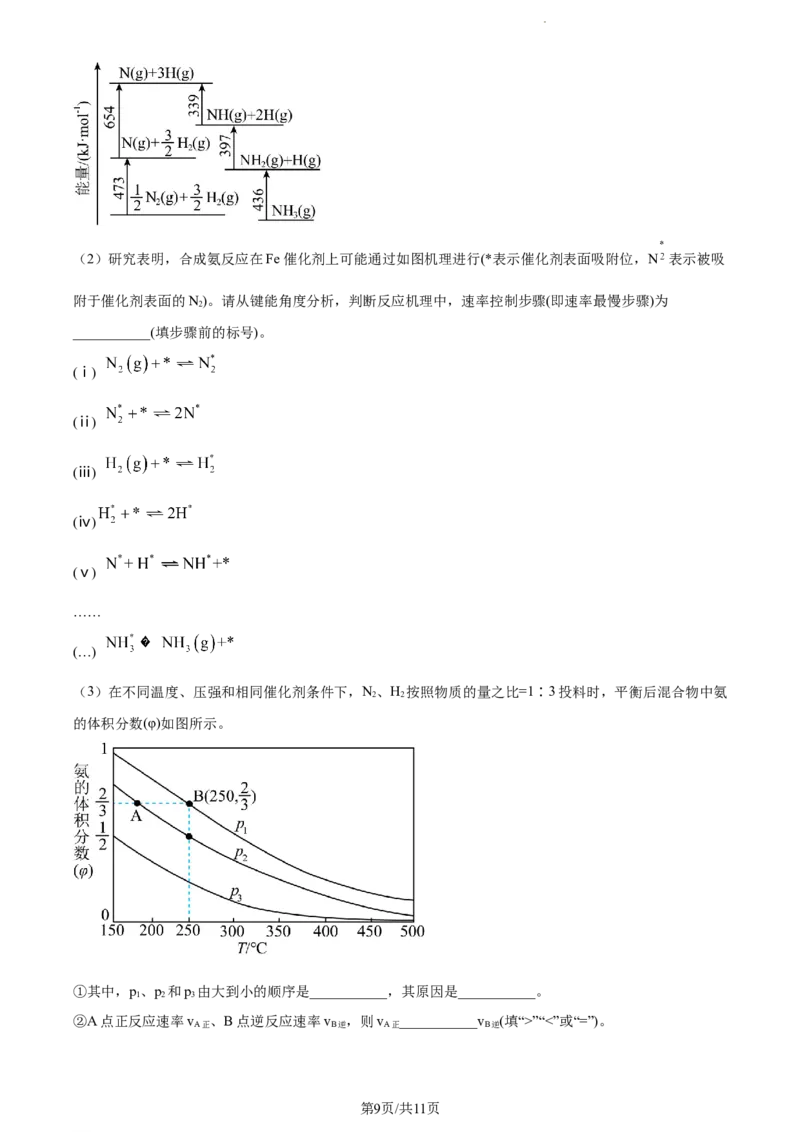
B. 原子半径:X”“<”或“=”)。
A正 B逆 A正 B逆
第9页/共11页
学科网(北京)股份有限公司③若在250℃、p 为105Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点平衡常数K 为
1 p
___________Pa-2(结果保留一位小数)。[K 的写法:在浓度平衡常数表达式中,用分压代替浓度;分压=总
p
压×该组分物质的量分数]
(4)纳米Fe O 在常压电化学法合成氨过程中起催化作用。该电解装置如下图所示。已知熔融NaOH—
2 3
KOH为电解液,Fe O 在电极上发生反应生成中间体Fe。
2 3
①惰性电极Ⅱ是电解池的___________(填“阳”或“阴”)极;
②惰性电极Ⅰ上生成中间体Fe的电极反应方程式为___________。
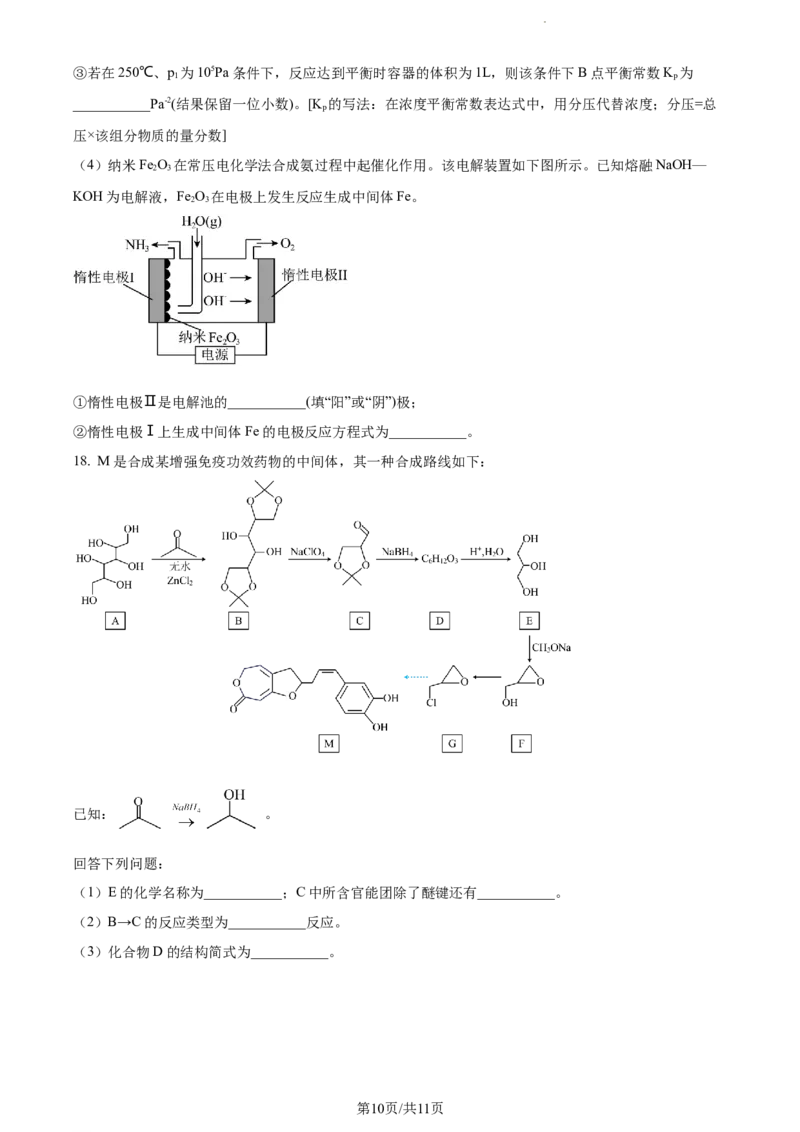
18. M是合成某增强免疫功效药物的中间体,其一种合成路线如下:
已知: 。
回答下列问题:
(1)E的化学名称为___________;C中所含官能团除了醚键还有___________。
(2)B→C的反应类型为___________反应。
(3)化合物D的结构简式为___________。
第10页/共11页
学科网(北京)股份有限公司(4)A→B反应的化学方程式为___________(方程式中用A代替 ;B代替 )。
(5)满足下列条件的C的同分异构体有___________种(不包含立体异构)。
①能与NaHCO 溶液反应生成CO;
3 2
②能发生银镜反应。
其中核磁共振氢谱显示有四组峰的结构简式为___________(任写一种)。
(6)参考以上合成路线及反应条件,写出以 为原料制备 的合成路线(其他无机试剂
任选):___________。
第11页/共11页
学科网(北京)股份有限公司