文档内容
哈师大附中 2021 级高三第二次调研考试化学试题
本卷可能用到的相对原子质量:H-1 C-12 O-16 V-51 Mn-55
一、选择题(本题包括15题,每题有一个正确答案,共45分)
1. 《新修本草》是我国古代中药学著作之一,其中关于“青矾”的描述为:“本来绿色,新出窟未见风者,
正如琉璃……,烧之赤色……”,则“青矾”的主要成分是
A. B.
C. D.
【答案】C
【解析】
【详解】本为绿色Fe2+为绿色,烧之转变为赤色即亚铁接触O 转变为+3铁,即该物质为FeSO ⋅7HO;
2 4 2
故选C。
2. 下列叙述正确的是
A. 物质按照组成可以分为单质和化合物
B. 氢氧化铁胶体带正电荷,土壤胶体带负电荷
C. 无机化合物主要包括:酸、碱、盐和氧化物
D. 按照树状分类法可将化学反应分为:氧化还原反应和离子反应
【答案】C
【解析】
【详解】A.纯净物按照元素组成可以分为单质和化合物,只有一种元素组成的纯净物为单质,由两种或
两种以上的元素组成的纯净物为化合物,故A错误;
B.胶体呈电中性,不带电,氢氧化铁胶体因吸附阳离子而带正电荷,土壤胶体因吸附阴离子而带负电荷,
故B错误;
C. 物质可以分为无机化合物和有机化合物,无机化合物主要包括:酸、碱、盐和氧化物,故C正确;
D.按照树状分类法可将化学反应分为:氧化还原反应和非氧化还原反应,故D错误;
故答案为:C。
3. 下列关于钠及其化合物的说法不正确的是
A. 钠通常保存在煤油中
B. 过氧化钠长期露置于空气中最终会变成氢氧化钠
C. 氢氧化钠固体称量时应放在烧杯或其他玻璃器皿中
D. 向饱和碳酸钠溶液中通入二氧化碳气体会产生细小晶体
第1页/共20页
学科网(北京)股份有限公司【答案】B
【解析】
【详解】A.钠属于活泼金属,易以空气中的氧气、水蒸气发生反应,密度比煤油大,保存在煤油中可隔
绝氧气、水蒸气等,A正确;
B.过氧化钠长期露置于空气中最终会变成碳酸钠,B错误;
C.氢氧化钠有腐蚀性,故氢氧化钠固体称量时应放在烧杯或其他玻璃器皿中,C正确;
D.向饱和碳酸钠溶液中通入二氧化碳气体会生成碳酸氢钠,碳酸氢钠的溶解度小于碳酸钠,故会产生细
小晶体,D正确;
故选B。
4. 化学与生活、生产、环境等密切相关。下列说法不正确的是
A. 乙醇、含氯消毒剂、过氧乙酸均可以有效灭活新型冠状病毒
B. 冬奥会短道速滑“战衣”含有聚氨基甲酸酯纤维材料,是一种合成有机高分子化合物
C. 二氧化碳、二氧化氮和二氧化硫是大气主要污染物,所以它们的含量是空气质量报告的主要项目
D. 天然气是一种清洁的燃料,它作为化工原料则主要用于合成氨和生产甲醇等
【答案】C
【解析】
【详解】A.乙醇、含氯消毒剂、过氧乙酸均能使蛋白质变性,均可以有效灭活新型冠状病毒,选项A正
确;
B.聚氨基甲酸酯材料,属于高分子有机化合物,是有机合成材料,选项B正确;
C. 二氧化碳的含量不是空气质量报告的主要项目,选项C错误;
D.天然气的燃烧产物为二氧化碳和水,是一种清洁的燃料,它作为化工原料则主要用于合成氨和生产甲
醇等,选项D正确;
答案选C。公众号:高中试卷君
5. 价类二维图是学习元素化合物的工具,a~g分别表示氮元素的不同价态所对应的物质,其关系如图所示。
下列说法正确的是
第2页/共20页
学科网(北京)股份有限公司A. f属于强碱 B. b能支持呼吸
C. e可用于实验室制H D. 可用湿润的红色石蕊试纸检验a
2
【答案】D
【解析】
【分析】a为氮的氢化物,氮的化合价为-3价,a为NH ,b为氮的单质,b为氮气,c为氮的氧化物,氮的
3
化合价为+2价,c为NO,d为氮的氧化物,氮的化合价为+4价,d为NO ,e为含氮酸,氮的化合价为+5
2
价,e为硝酸,f为碱,氮的化合价为-3价,f为一水合氨,g为盐,氮的化合价为-3价,g为铵盐。
【详解】A.根据分析可知,f为一水合氨,属于弱碱,A错误;
B.b为氮气,氮气不能支持呼吸,B错误;
C.e为硝酸,硝酸具有强氧化性,与金属反应生成NO或NO ,无法生成氢气,C错误;
2
D.a为NH ,可用湿润的红色石蕊试纸检验NH ,湿润的红色石蕊试纸变蓝即说明有氨气存在,D正确;
3 3
故答案选D。
6. 下列化学用语表达正确的是
A. 乙烯的实验式: B. 水分子间的氢键:
C. 的空间结构:平面三角形 D. 在元素周期表的位置:第四周期第ⅤB族
【答案】B
【解析】
【详解】A.乙烯的实验式:CH,故A错误;
2
B.水分子间的氢键可表示为 ,故B正确;
C. 中心原子价层电子对数为3+ =4,且含有1个孤电子对,空间结构:三角锥形,
故C错误;
第3页/共20页
学科网(北京)股份有限公司D. 在元素周期表的位置:第四周期第VIB族,故D错误;
故选B 。
7. 下列对应离子方程式书写正确的是
A. 向酸性高锰酸钾溶液中滴加双氧水:2MnO +H O+6H+=2Mn2++4H O+3O↑
2 2 2 2
B. 已知酸性强弱顺序:HCO>HCN>HCO ,则向NaCN溶液中通入少量CO:2CN-
2 3 2
+CO +H O=2HCN+CO
2 2
.
C 向Fe(NO ) 溶液中滴加盐酸,有气泡产生:3Fe2++NO +4H+=3Fe3++NO↑+2HO
3 2 2
D. 向淀粉KI溶液中滴加“84”消毒液,溶液变蓝:2I-+ClO-+2H+=I +Cl-+H O
2 2
【答案】C
【解析】
【详解】A.向酸性高锰酸钾溶液中滴加双氧水:2MnO +5H O+6H+=2Mn2++8H O+5O↑,A错误;
2 2 2 2
B.已知酸性强弱顺序:HCO>HCN>HCO ,则向NaCN溶液中通入少量CO:CN-
2 3 2
+CO +H O=HCN+HCO ,B错误;
2 2
C.向Fe(NO ) 溶液中滴加盐酸,硝酸根在氢离子的作用下氧化亚铁离子,硝酸根被还原为NO,所以有气
3 2
泡产生:3Fe2++NO +4H+=3Fe3++NO↑+2HO,C正确;
2
D.向淀粉KI溶液中滴加“84”消毒液,溶液变蓝,溶液显碱性:2I-+ClO-+ H O =I +Cl-+2OH-,D错误;
2 2
故选C 。
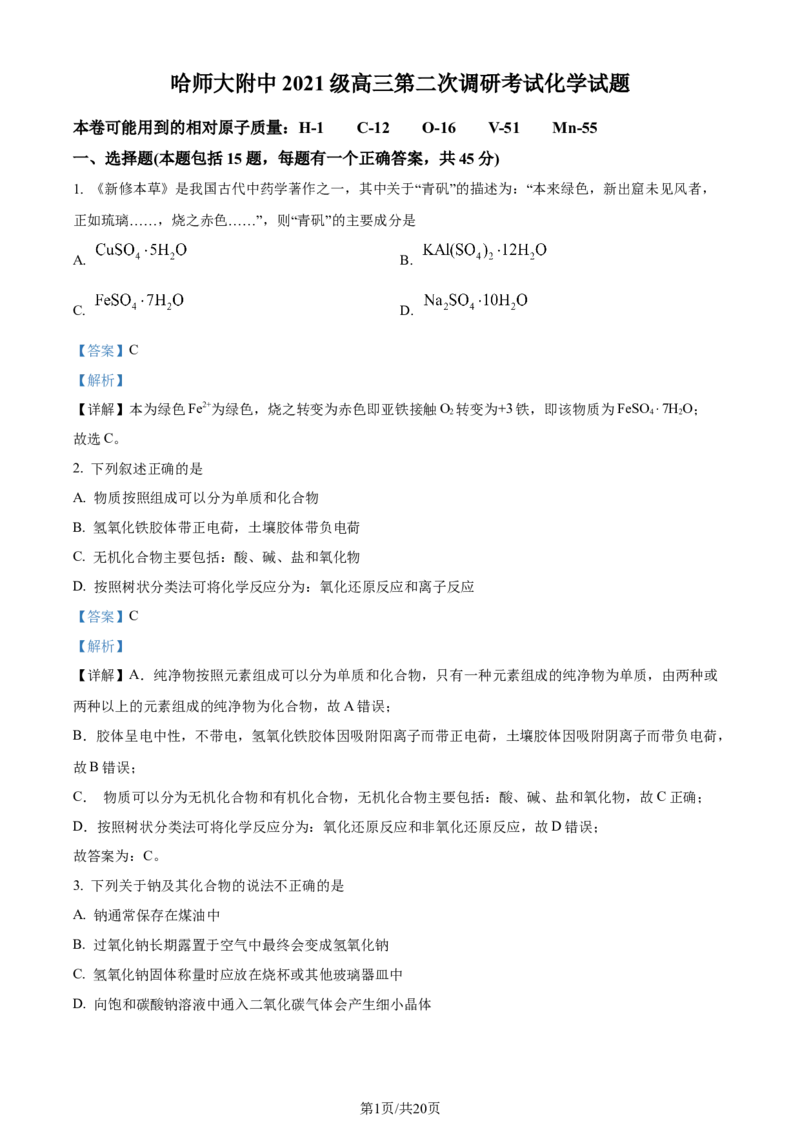
8. 中科院通过调控N-carbon的孔道结构和表面活性位构型,成功实现了电催化 生成甲酸和乙醇,合
成过程如图所示。用 表示阿伏加德罗常数的值,下列叙述正确的是
第4页/共20页
学科网(北京)股份有限公司A. 标准状况下, 中所含质子的数目为
B. 常温常压下, 分子中所含 键的数目为
C. 甲酸和乙醇的混合物所含氢原子的数目一定为
D. 电催化过程中,每生成 甲酸,转移电子的数目为
【答案】A
【解析】
【详解】A.每个CO中含质子数为6+8=14个,5.6LCO的物质的量为=
,含有质子为0.25mol×14=3.5mol=3.5N ,A项正确;
A
B.CO 中含有2个Π键,8.8gCO 物质的量为 ,含有Π键为0.2mol×2=0.4mol=0.4
2 2
N ,B项错误;
A
C.HCOOH和 C HOH摩尔质量均为46g/mol,计算得到总物质的量为0.5mol但二者H的贡献不同无法计
2 5
算氢原子数,C项错误;
D.CO 变为HCOOH化合价降低2,所以每生成1mol HCOOH转移2N 的电子,D项错误;
2 A
故答案为A。
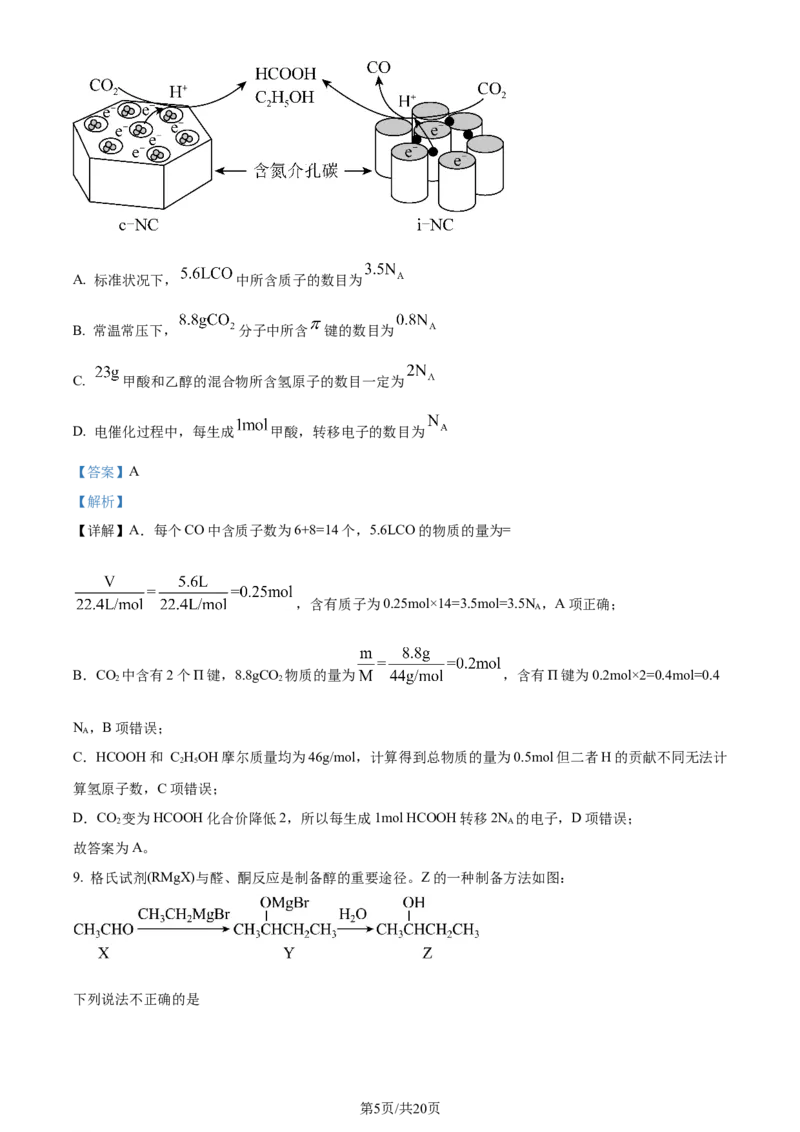
9. 格氏试剂(RMgX)与醛、酮反应是制备醇的重要途径。Z的一种制备方法如图:
下列说法不正确的是
第5页/共20页
学科网(北京)股份有限公司A. 以CHCOCH 、CHMgBr和水为原料也可制得Z
3 3 3
B. Y分子与Z分子中均含有手性碳原子
C. Z易溶于水是因为Z分子与水分子之间能形成氢键
D. X中碳原子的杂化轨道类型为sp3和sp2
【答案】A
【解析】
【详解】A.以CHCOCH 、CHMgBr和水为原料发生反应
3 3 3
,A错误;
B.Y分子与Z分子中均含有手性碳原子,B正确;
C.Z分子中含有羟基,与水分子之间能形成氢键,易溶于水,C正确;
D.X中甲基碳原子的杂化轨道类型为sp3,碳基碳原子的杂化轨道类型为sp2,D正确;
故选A。
10. 下列关于各种物质的工业制法的说法中正确的是
A. 工业制溴:利用氯气将海水中的溴离子氧化后,鼓入热空气或水蒸气将溴吹出
B. 工业制钠:电解饱和NaCl溶液,收集阴极产生的Na
C. 工业制铝:电解熔融的AlCl ,收集阴极产生的Al
3
D. 工业制硫酸:在沸腾炉中煅烧硫铁矿,吸收塔中浓硫酸充分吸收煅烧生成的SO 气体
3
【答案】A
【解析】
【详解】A.工业制溴:利用氯气将海水中的溴离子氧化后,鼓入热空气或水蒸气将溴吹出,A正确;
B.工业制钠:电解熔融的NaCl,收集阴极产生的Na,B错误;
C.工业制铝:电解熔融的Al O,收集阴极产生的Al,AlCl 为共价化合物,熔化状态下,不导电,C错
2 3 3
误;
D.工业制硫酸:在沸腾炉中煅烧硫铁矿生成SO ,经催化氧化后生成SO ,SO 为非极性分子,难溶于水,
2 3 3
故吸收塔中浓硫酸充分吸收煅烧生成的SO 气体,D错误;
3
故选A。
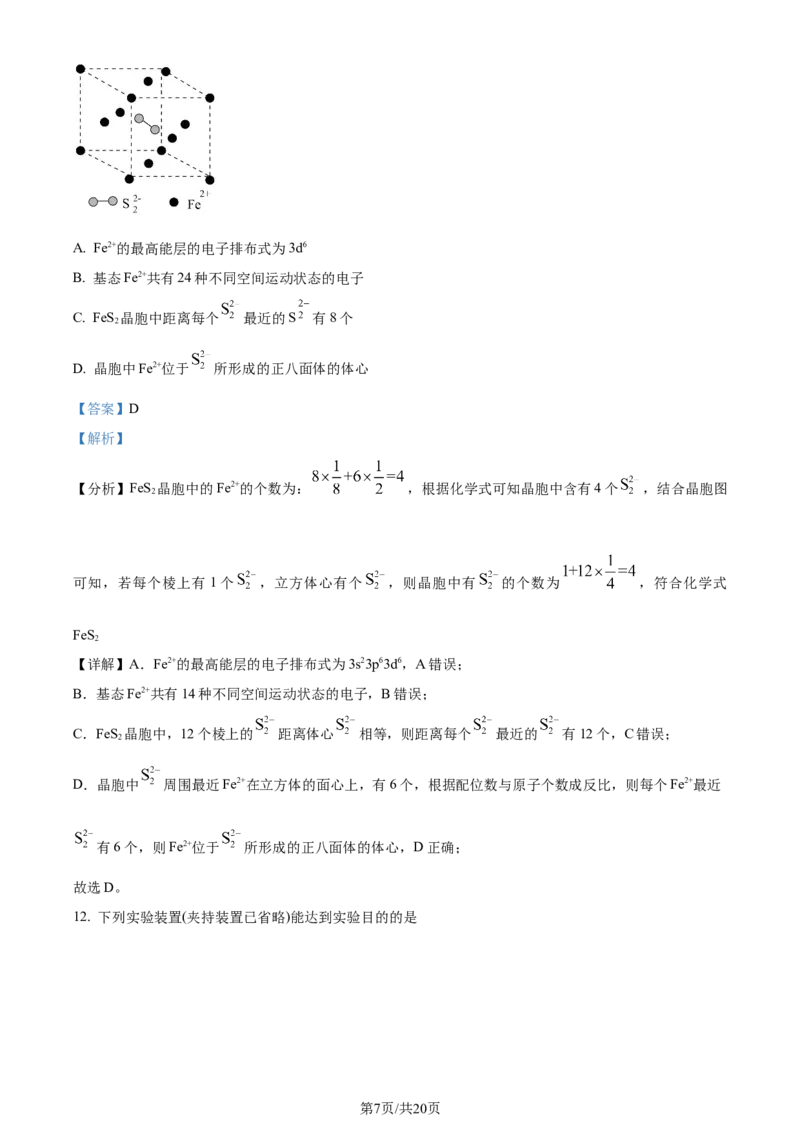
11. FeS 具有良好的半导体性能,如图给出了立方FeS 晶胞中的Fe2+和位于晶胞体心的 (晶胞中的其他
2 2
已省略)。下列叙述正确的是
第6页/共20页
学科网(北京)股份有限公司A. Fe2+的最高能层的电子排布式为3d6
B. 基态Fe2+共有24种不同空间运动状态的电子
C. FeS 晶胞中距离每个 最近的S 有8个
2
D. 晶胞中Fe2+位于 所形成的正八面体的体心
【答案】D
【解析】
【分析】FeS 晶胞中的Fe2+的个数为: ,根据化学式可知晶胞中含有4个 ,结合晶胞图
2
可知,若每个棱上有 1个 ,立方体心有个 ,则晶胞中有 的个数为 ,符合化学式
FeS
2
【详解】A.Fe2+的最高能层的电子排布式为3s23p63d6,A错误;
B.基态Fe2+共有14种不同空间运动状态的电子,B错误;
C.FeS 晶胞中,12个棱上的 距离体心 相等,则距离每个 最近的 有12个,C错误;
2
D.晶胞中 周围最近Fe2+在立方体的面心上,有6个,根据配位数与原子个数成反比,则每个Fe2+最近
有6个,则Fe2+位于 所形成的正八面体的体心,D正确;
故选D。
12. 下列实验装置(夹持装置已省略)能达到实验目的的是
第7页/共20页
学科网(北京)股份有限公司A. 利用A装置进行 的干燥、收集及尾气处理
B. 试管中可长时间观察到白色沉淀
C. 试管中充满溶液,说明通入氧气的体积为 体积的
D. 利用D装置比较 与 的热稳定性
【答案】C
【解析】
【详解】A. 为酸性气体,不能用碱石灰干燥,A错误;
B.试管中先观察到白色沉淀,随后转为灰绿色,最后变为红褐色,B错误;
C. 与HO反应生成硝酸和NO,NO又与O 反应生成 ,总反应可以表示为
2 2
4NO +O +2H O=4HNO ,即按物质的量之比n(NO ):n (O ) =4:1时,气体恰好被吸收完全说明通入氧气的体
2 2 2 3 2 2
积为 体积的 ,C正确;
D. 的热稳定性强于 ,故在大试管中的为 ,小试管中的为 ,D错误;
答案选C。
13. 足量铜与一定量浓硝酸反应,得到硝酸铜溶液和 、 、 的混合气体,这些气体与
(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入
氢氧化钠溶液至 恰好完全沉淀,则消耗 溶液的体积是
A. B. C. D.
第8页/共20页
学科网(北京)股份有限公司【答案】D
【解析】
【分析】
【详解】足量的 与一定量的浓 反应得到硝酸铜溶液和 、 、 的混合气体,混合气
体与 (标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸,则 提供的电子物质
的量等于氧气获得电子的物质的量,即 ,根据 和
的反应可得关系式: ,则
,则选项D符合题意。
答案选D。
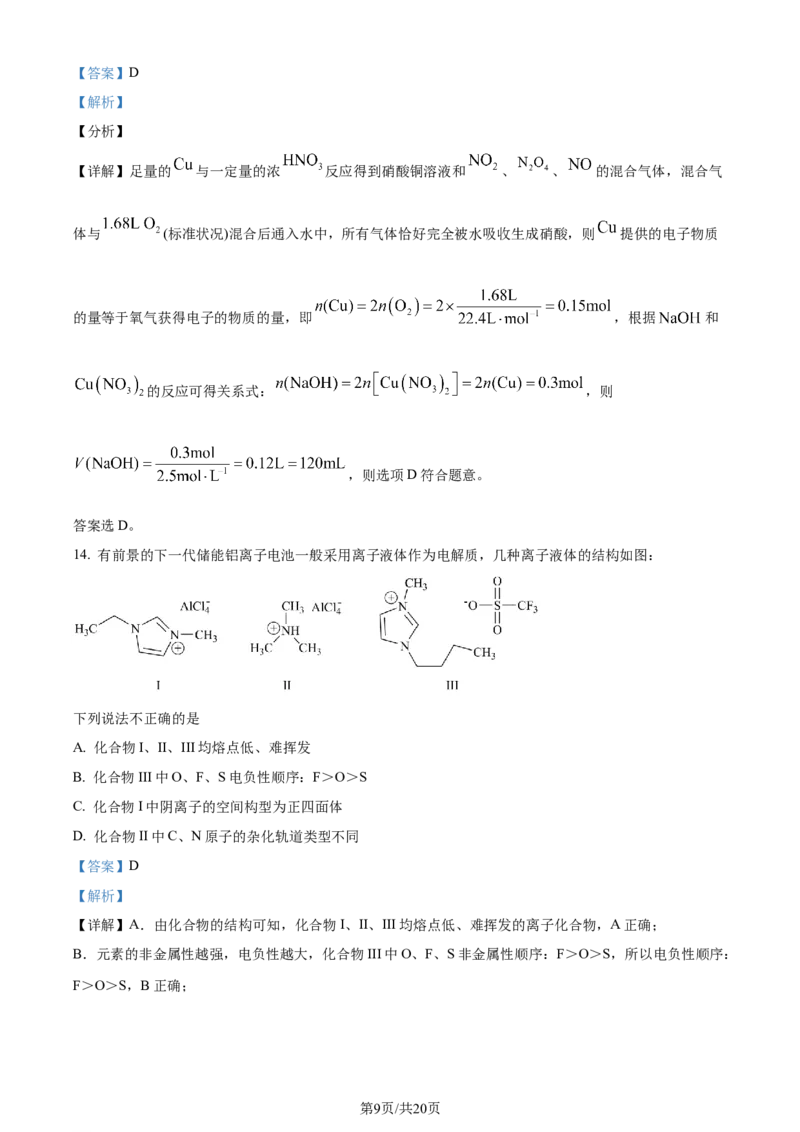
14. 有前景的下一代储能铝离子电池一般采用离子液体作为电解质,几种离子液体的结构如图:
下列说法不正确的是
A. 化合物I、II、III均熔点低、难挥发
B. 化合物III中O、F、S电负性顺序:F>O>S
C. 化合物I中阴离子的空间构型为正四面体
D. 化合物II中C、N原子的杂化轨道类型不同
【答案】D
【解析】
【详解】A.由化合物的结构可知,化合物I、II、III均熔点低、难挥发的离子化合物,A正确;
B.元素的非金属性越强,电负性越大,化合物III中O、F、S非金属性顺序:F>O>S,所以电负性顺序:
F>O>S,B正确;
第9页/共20页
学科网(北京)股份有限公司C.化合物I中阴离子为 ,中心原子杂化类型为sp3杂化,无孤电子对,空间构型为正四面体形,C
正确;
D.由化合物的结构可知,化合物II中的阴离子中C、N原子的价层电子对数为4,杂化轨道类型都是sp3
杂化,D错误;
故选D。
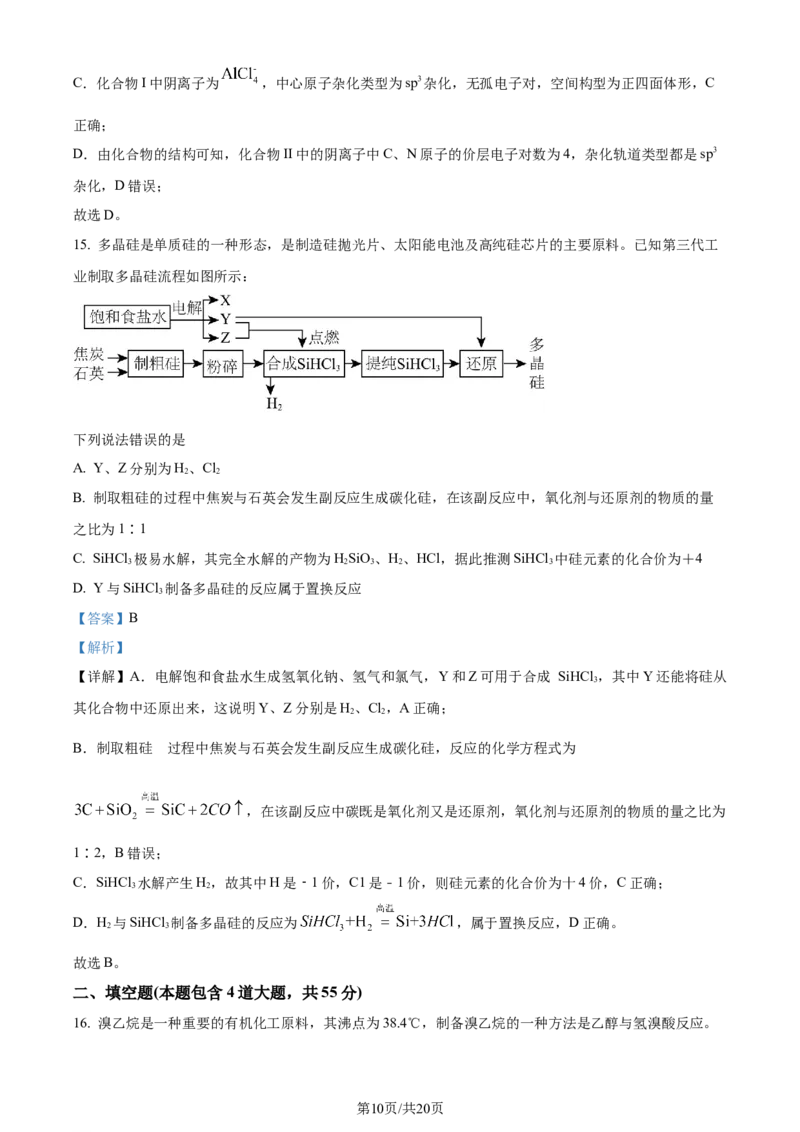
15. 多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅芯片的主要原料。已知第三代工
业制取多晶硅流程如图所示:
下列说法错误的是
A. Y、Z分别为H、Cl
2 2
B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量
之比为1∶1
C. SiHCl 极易水解,其完全水解的产物为HSiO、H、HCl,据此推测SiHCl 中硅元素的化合价为+4
3 2 3 2 3
D. Y与SiHCl 制备多晶硅的反应属于置换反应
3
【答案】B
【解析】
【详解】A.电解饱和食盐水生成氢氧化钠、氢气和氯气,Y和Z可用于合成 SiHCl ,其中Y还能将硅从
3
其化合物中还原出来,这说明Y、Z分别是H、Cl,A正确;
2 2
的
B.制取粗硅 过程中焦炭与石英会发生副反应生成碳化硅,反应的化学方程式为
,在该副反应中碳既是氧化剂又是还原剂,氧化剂与还原剂的物质的量之比为
1∶2,B错误;
C.SiHCl 水解产生H,故其中H是﹣1价,C1是﹣1价,则硅元素的化合价为十4价,C正确;
3 2
D.H 与SiHCl 制备多晶硅的反应为 ,属于置换反应,D正确。
2 3
故选B。
二、填空题(本题包含4道大题,共55分)
16. 溴乙烷是一种重要的有机化工原料,其沸点为38.4℃,制备溴乙烷的一种方法是乙醇与氢溴酸反应。
第10页/共20页
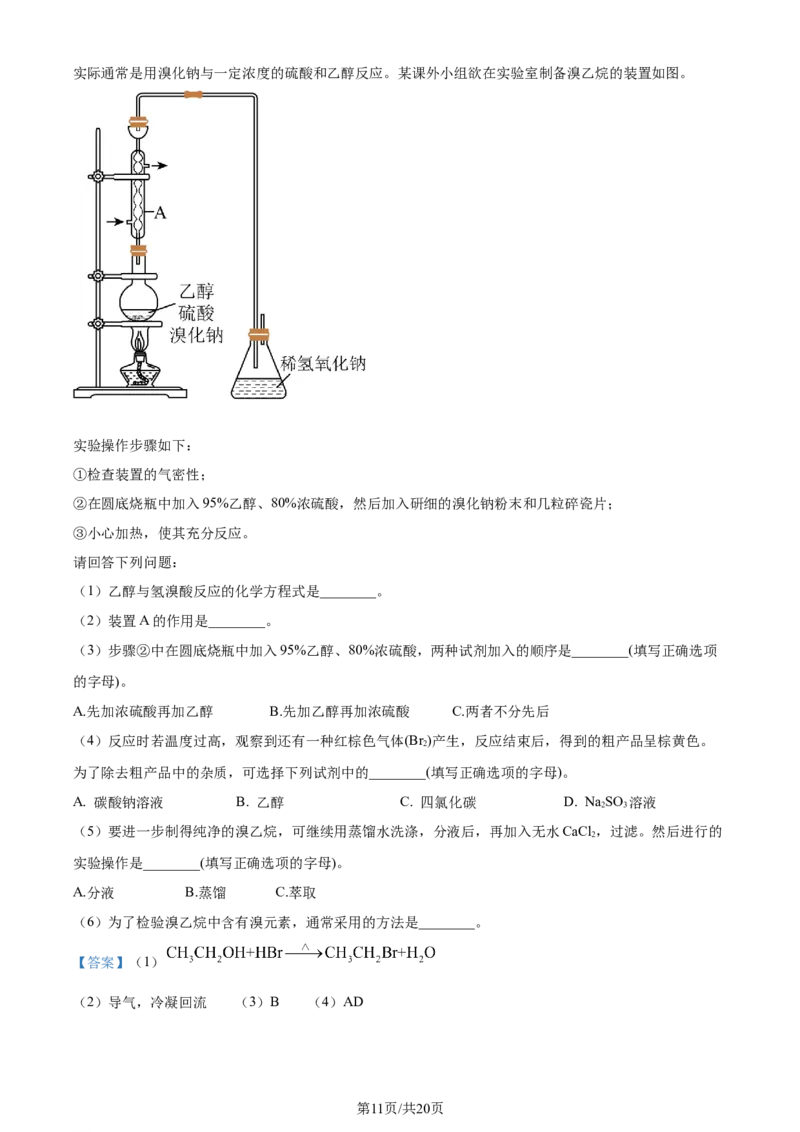
学科网(北京)股份有限公司实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图。
实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%浓硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请回答下列问题:
(1)乙醇与氢溴酸反应的化学方程式是________。
(2)装置A的作用是________。
(3)步骤②中在圆底烧瓶中加入95%乙醇、80%浓硫酸,两种试剂加入的顺序是________(填写正确选项
的字母)。
A.先加浓硫酸再加乙醇 B.先加乙醇再加浓硫酸 C.两者不分先后
(4)反应时若温度过高,观察到还有一种红棕色气体(Br)产生,反应结束后,得到的粗产品呈棕黄色。
2
为了除去粗产品中的杂质,可选择下列试剂中的________(填写正确选项的字母)。
A. 碳酸钠溶液 B. 乙醇 C. 四氯化碳 D. NaSO 溶液
2 3
(5)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水CaCl ,过滤。然后进行的
2
实验操作是________(填写正确选项的字母)。
A.分液 B.蒸馏 C.萃取
(6)为了检验溴乙烷中含有溴元素,通常采用的方法是________。
【答案】(1)
(2)导气,冷凝回流 (3)B (4)AD
第11页/共20页
学科网(北京)股份有限公司(5)B (6)加入氢氧化钠溶液,加热后,再加入硝酸酸化,再加硝酸银溶液,若有淡黄色沉淀生成,
则含有溴元素
【解析】
【分析】A装置中,硫酸和溴化钠利用不挥发性酸制备挥发性酸制备出溴化氢,在加热的条件下和乙醇发
生反应,生成溴乙烷,乙醇的沸点较低,经球形冷凝管冷凝回流,与溴乙烷分离,溴乙烷经导管进入锥形
瓶,氢氧化钠溶液可吸收产生溴化氢,防止逸散到空气中;
【小问1详解】
乙醇与氢溴酸发生取代反应,其化学方程式是: ;
【小问2详解】
装置A为球形冷凝管,其作用是导气,冷凝回流,提高乙醇的利用率;
【小问3详解】公众号:高中试卷君
步骤②中在圆底烧瓶中加入95%乙醇、80%浓硫酸,浓硫酸的密度大于乙醇,所以两种试剂的加入顺序是
先加95%乙醇,再加80%浓硫酸,故选B;
【小问4详解】
反应时若温度过高,观察到还有一种红棕色气体(Br )产生,反应结束后得到的粗产品呈棕黄色,为了除
2
去粗产品中的杂质,可选择稀氢氧化钠溶液或亚硫酸钠溶液,两者均可与溴单质反应,将其除去,故答案
为:AD;
【小问5详解】
无水氯化钙是一种干燥剂,具有吸水性,经蒸馏可将溴乙烷蒸出;
【小问6详解】
溴乙烷中不含有溴离子,为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液检验,通常
采用的方法是加入氢氧化钠溶液,加热后,再加入硝酸酸化,再加硝酸银溶液,若有淡黄色沉淀生成,则
含有溴元素。
17. 五氧化二钒( )广泛用于冶金、化工等行业,用作合金添加剂、生产硫酸或石油精炼用的催化剂等。
从废钒催化剂(含有 、 、 、 、 、 等)中回收钒,既能避免对环境的污染,
又能节约宝贵的资源,回收工艺流程如下:
第12页/共20页
学科网(北京)股份有限公司已知:
①“酸浸”时 和 与稀硫酸反应分别生成 和 。
②溶液中 与 可相互转化: ,且 为沉淀。
(1)“酸浸”前,需对废钒催化剂进行粉碎预处理,其目的是___________。
(2)“还原转化”中加入 的目的是将 转化为 ,写出反应的离子方程式:___________。
(3)加入 的目的是将过量的 转化为 。“氧化1”后,溶液中含有的金属阳离子主要有
、 、 ,调节 使离子沉淀,若溶液中 ,则调节溶液的 最小值
为___________可使 沉淀完全(离子浓度≤ 时沉淀完全),此时___________(填“有”
或“无”) 沉淀生成。{假设溶液体积不变, , ,
}
(4)“氧化2”过程中发生反应的离子方程式为___________。
(5)“沉钒”时,通入氨气的作用是___________。
(6)若该废钒催化剂中 的含量为10%(原料中所有的钒已换算成 )。取100g待处理样品,按照
上述流程进行实验。当加入 溶液时,溶液中的钒元素恰好完全反应,则该工艺
中钒的回收率是___________%(假设与 反应后的操作步骤中钒元素无损失)。
【答案】(1)增大接触面积,加快反应速率
第13页/共20页
学科网(北京)股份有限公司(2)
(3) ①. 2.8 ②. 无
(4)
(5)使 平衡正向移动,将 转化为 ,同时增大 的浓度
(6)81.9
【解析】
【分析】本题主要考查由废钒催化剂制备五氧化二钒的工艺流程,向废钒催化剂中加入稀硫酸进行酸浸,
将 和 与稀硫酸反应分别生成 和 ,Fe O 转化为Fe (SO ),NiO转化为NiSO ,过滤
2 3 2 4 3 4
后的滤渣1,主要成分为SiO,加入FeSO 是将 转化为 ,加入HO 是将过量的Fe2+全部转化为
2 4 2 2
Fe3+便于后续调pH步骤中除去,过滤得滤渣2,主要成分为Fe(OH) ,滤液2中加入萃取剂,萃取出含有
3
钒微粒,再进行反萃取后得到含钒的溶液,加入HSO 和KClO 的目的是将低价态的钒氧化为+5价的钒,
2 4 3
经过加入NH Cl和NH 后析出NH VO 沉淀,过滤洗涤最后灼烧沉淀得VO,据此分析解题。
4 3 4 3 2 5
【小问1详解】
“酸浸”前,需对废钒催化剂进行粉碎预处理,其目的是增大接触面积,加快反应速率,故答案为:增大
接触面积,加快反应速率;
【小问2详解】
“还原转化”中加入 的目的是将 转化为 ,根据氧化还原反应配平可知,该反应的离子
方程式为: ,故答案为: ;
【小问3详解】
当 时,根据 的公式可知,溶液中的
, ,计算可得
, ,因为 ,
第14页/共20页
学科网(北京)股份有限公司所以无 生成,故答案为:2.8;无;
【小问4详解】
将 氧化为 的过程中, 中氯元素得电子被还原为 ,根据氧化还原反应配平可得
其离子方程式为 ,故答案为:
;
【小问5详解】
溶液中存在平衡 ,通入氨气,溶液中 浓度增大,消耗了 ,该平衡正
向移动,从而使 尽可能都转化为 ,故答案为:使 平衡正向移动,
将 转化为 ,同时增大 的浓度;
【小问6详解】
“氧化2”过程中 将 氧化成 ,便于后续沉钒,进而实现钒的回收,相关的离子方程式
为 。100g待处理样品中, ,则
,即 ; ,
由于 ,故 ,则该工艺中钒的最大回收率为 ,故答
案为:81.9。
18. 碳酸锰(MnCO )是制造高性能磁性材料的主要原料。实验室以KMnO 为原料制备少量MnCO 并研究其
3 4 3
性
质,制备MnCO 的装置如图1所示。
3
已知: MnCO 难溶于水、乙醇,100°C开始分解 。 请回答下列问题:
3
第15页/共20页
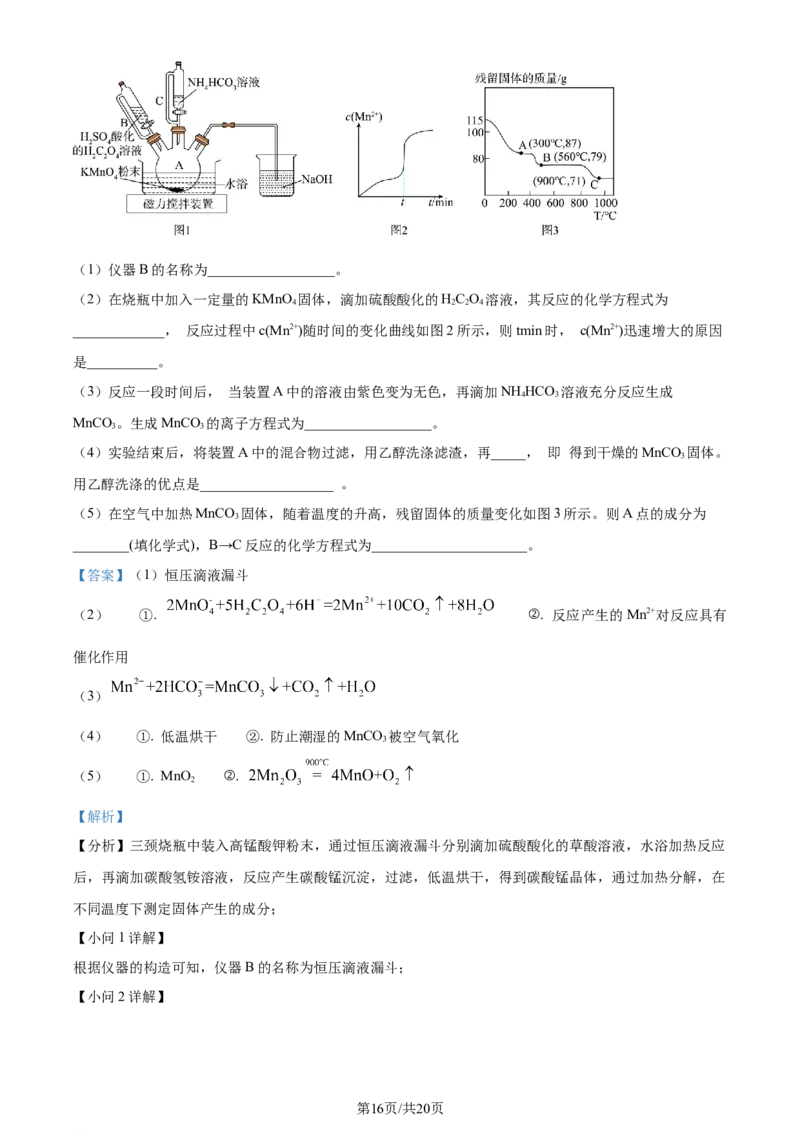
学科网(北京)股份有限公司(1)仪器B的名称为__________________。
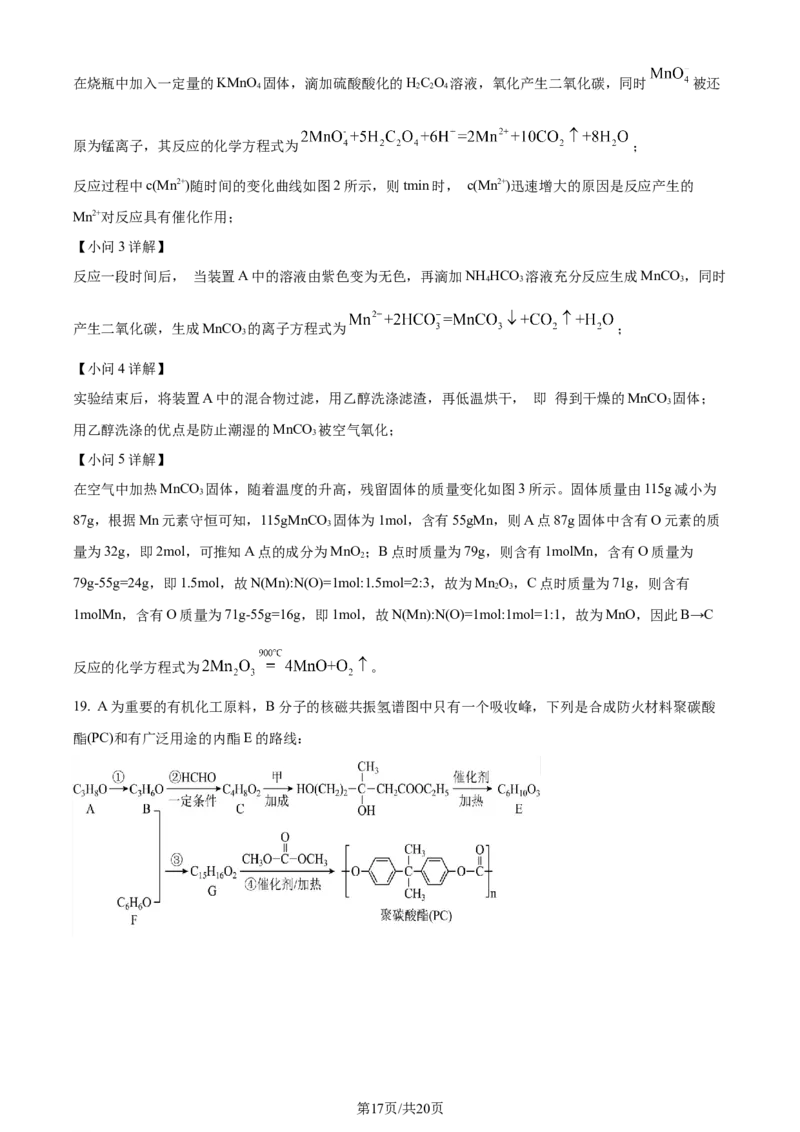
(2)在烧瓶中加入一定量的KMnO 固体,滴加硫酸酸化的HC O 溶液,其反应的化学方程式为
4 2 2 4
_____________, 反应过程中c(Mn2+)随时间的变化曲线如图2所示,则tmin时, c(Mn2+)迅速增大的原因
是__________。
(3)反应一段时间后, 当装置A中的溶液由紫色变为无色,再滴加NH HCO 溶液充分反应生成
4 3
MnCO 。生成MnCO 的离子方程式为__________________。
3 3
(4)实验结束后,将装置A中的混合物过滤,用乙醇洗涤滤渣,再_____, 即 得到干燥的MnCO 固体。
3
用乙醇洗涤的优点是___________________ 。
(5)在空气中加热MnCO 固体,随着温度的升高,残留固体的质量变化如图3所示。则A点的成分为
3
________(填化学式),B→C反应的化学方程式为______________________。
【答案】(1)恒压滴液漏斗
(2) ①. ②. 反应产生的Mn2+对反应具有
催化作用
(3)
(4) ①. 低温烘干 ②. 防止潮湿的MnCO 被空气氧化
3
(5) ①. MnO ②.
2
【解析】
【分析】三颈烧瓶中装入高锰酸钾粉末,通过恒压滴液漏斗分别滴加硫酸酸化的草酸溶液,水浴加热反应
后,再滴加碳酸氢铵溶液,反应产生碳酸锰沉淀,过滤,低温烘干,得到碳酸锰晶体,通过加热分解,在
不同温度下测定固体产生的成分;
【小问1详解】
根据仪器的构造可知,仪器B的名称为恒压滴液漏斗;
【小问2详解】
第16页/共20页
学科网(北京)股份有限公司在烧瓶中加入一定量的KMnO 固体,滴加硫酸酸化的HC O 溶液,氧化产生二氧化碳,同时 被还
4 2 2 4
原为锰离子,其反应的化学方程式为 ;
反应过程中c(Mn2+)随时间的变化曲线如图2所示,则tmin时, c(Mn2+)迅速增大的原因是反应产生的
Mn2+对反应具有催化作用;
【小问3详解】
反应一段时间后, 当装置A中的溶液由紫色变为无色,再滴加NH HCO 溶液充分反应生成MnCO ,同时
4 3 3
产生二氧化碳,生成MnCO 的离子方程式为 ;
3
【小问4详解】
实验结束后,将装置A中的混合物过滤,用乙醇洗涤滤渣,再低温烘干, 即 得到干燥的MnCO 固体;
3
用乙醇洗涤的优点是防止潮湿的MnCO 被空气氧化;
3
【小问5详解】
在空气中加热MnCO 固体,随着温度的升高,残留固体的质量变化如图3所示。固体质量由115g减小为
3
87g,根据Mn元素守恒可知,115gMnCO 固体为1mol,含有55gMn,则A点87g固体中含有O元素的质
3
量为32g,即2mol,可推知A点的成分为MnO ;B点时质量为79g,则含有1molMn,含有O质量为
2
79g-55g=24g,即1.5mol,故N(Mn):N(O)=1mol:1.5mol=2:3,故为MnO,C点时质量为71g,则含有
2 3
1molMn,含有O质量为71g-55g=16g,即1mol,故N(Mn):N(O)=1mol:1mol=1:1,故为MnO,因此B→C
反应的化学方程式为 。
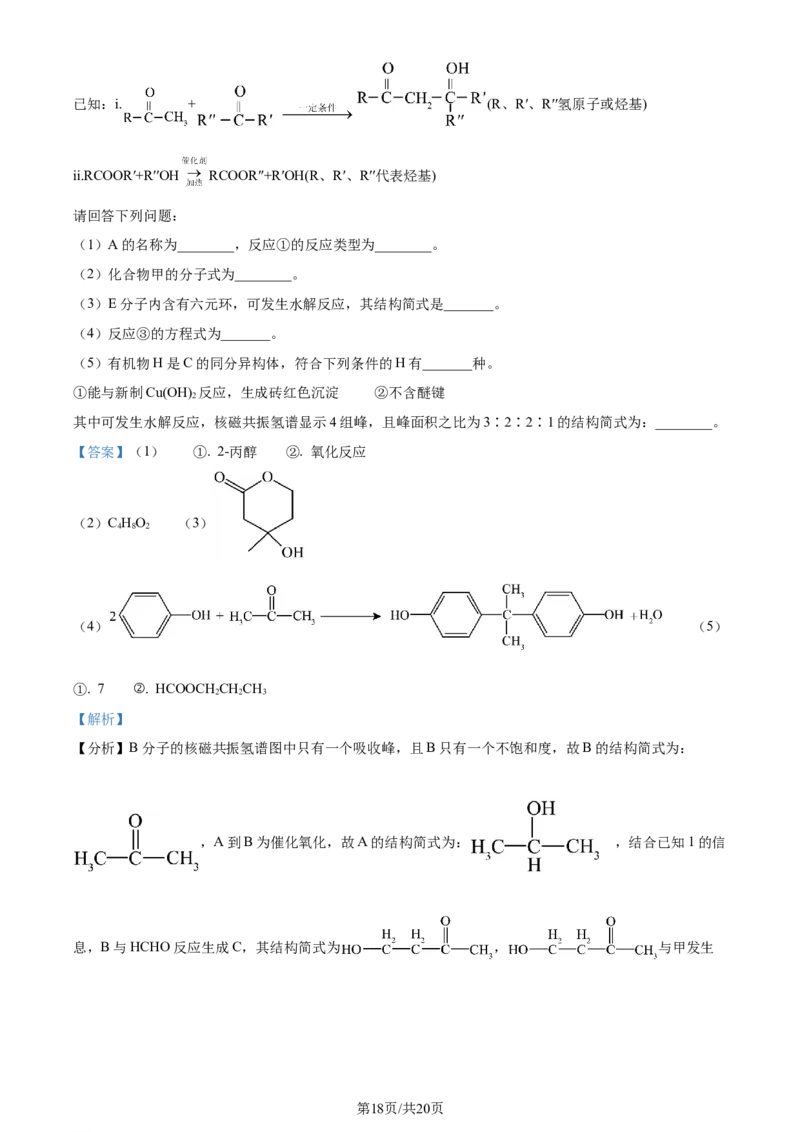
19. A为重要的有机化工原料,B分子的核磁共振氢谱图中只有一个吸收峰,下列是合成防火材料聚碳酸
酯(PC)和有广泛用途的内酯E的路线:
第17页/共20页
学科网(北京)股份有限公司已知:i. + (R、R′、R′′氢原子或烃基)
ii.RCOOR′+R′′OH RCOOR′′+R′OH(R、R′、R′′代表烃基)
请回答下列问题:
(1)A的名称为________,反应①的反应类型为________。
(2)化合物甲的分子式为________。
(3)E分子内含有六元环,可发生水解反应,其结构简式是_______。
(4)反应③的方程式为_______。
(5)有机物H是C的同分异构体,符合下列条件的H有_______种。
①能与新制Cu(OH) 反应,生成砖红色沉淀 ②不含醚键
2
其中可发生水解反应,核磁共振氢谱显示4组峰,且峰面积之比为3∶2∶2∶1的结构简式为:________。
【答案】(1) ①. 2-丙醇 ②. 氧化反应
(2)C HO (3)
4 8 2
(4) (5)
①. 7 ②. HCOOCH CHCH
2 2 3
【解析】
【分析】B分子的核磁共振氢谱图中只有一个吸收峰,且B只有一个不饱和度,故B的结构简式为:
,A到B为催化氧化,故A的结构简式为: ,结合已知1的信
息,B与HCHO反应生成C,其结构简式为 , 与甲发生
第18页/共20页
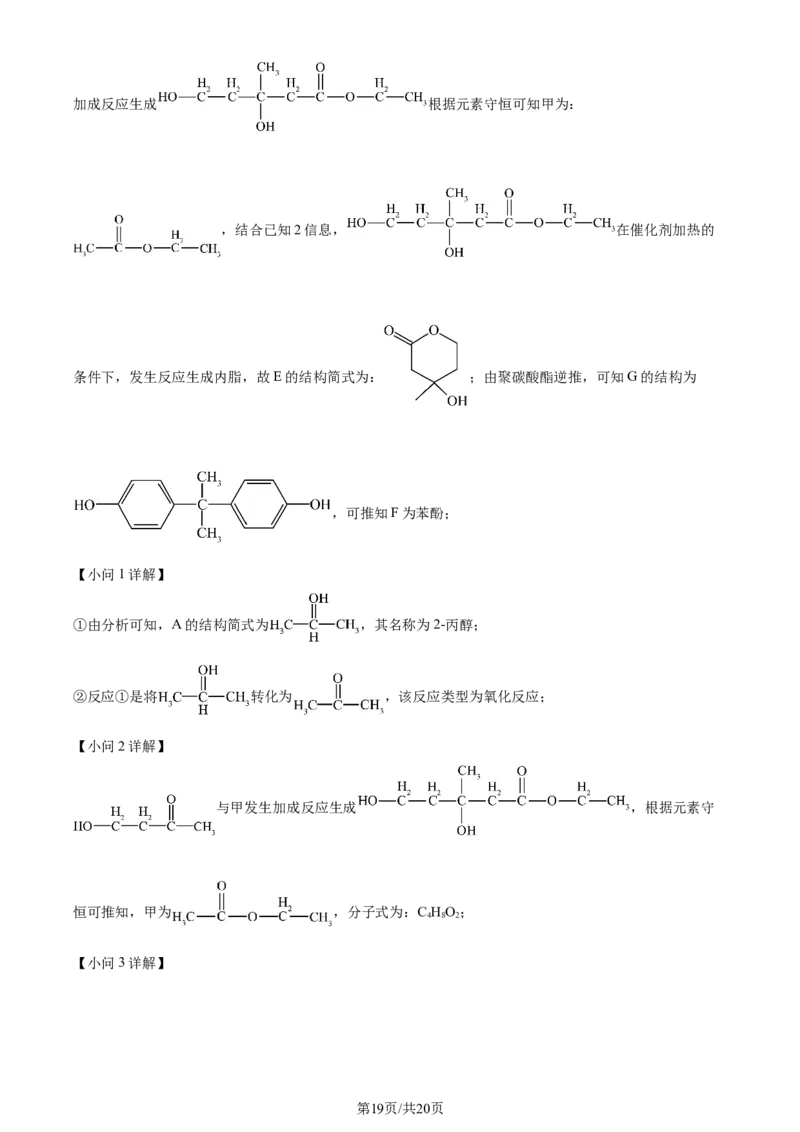
学科网(北京)股份有限公司加成反应生成 根据元素守恒可知甲为:
,结合已知2信息, 在催化剂加热的
条件下,发生反应生成内脂,故E的结构简式为: ;由聚碳酸酯逆推,可知G的结构为
,可推知F为苯酚;
【小问1详解】
①由分析可知,A的结构简式为 ,其名称为2-丙醇;
②反应①是将 转化为 ,该反应类型为氧化反应;
【小问2详解】
与甲发生加成反应生成 ,根据元素守
恒可推知,甲为 ,分子式为:C HO;
4 8 2
【小问3详解】
第19页/共20页
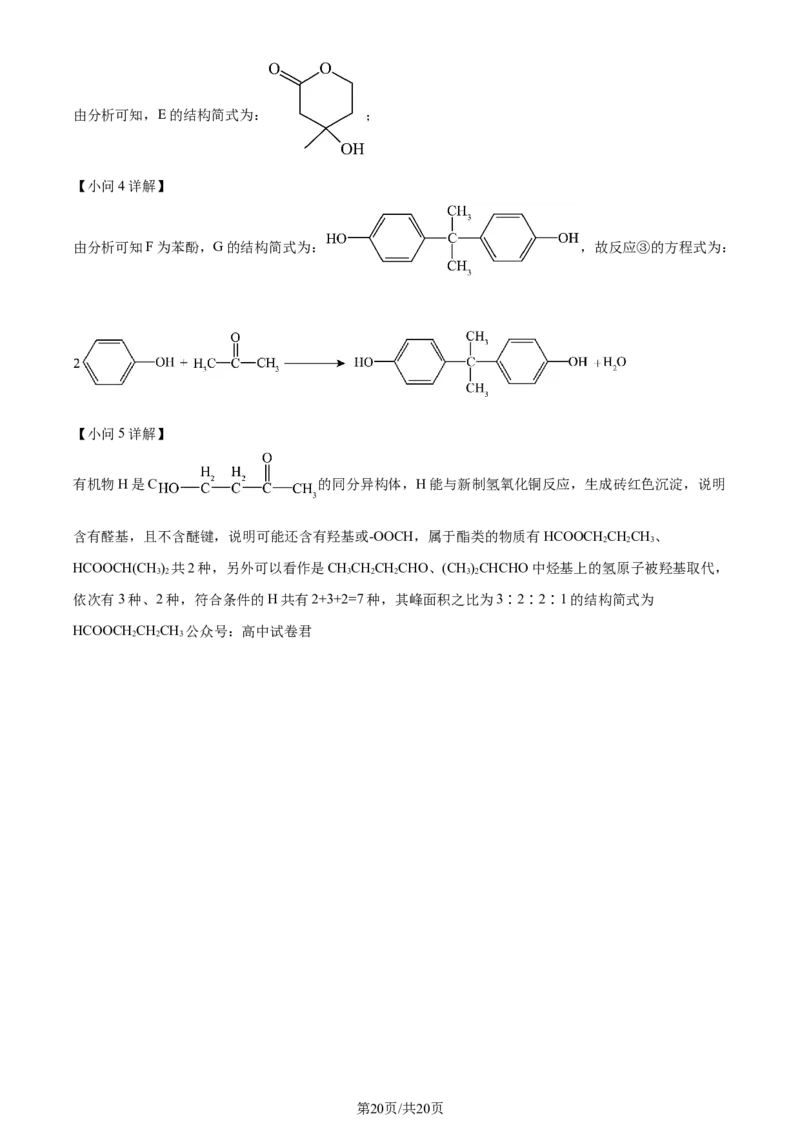
学科网(北京)股份有限公司由分析可知,E的结构简式为: ;
【小问4详解】
由分析可知F为苯酚,G的结构简式为: ,故反应③的方程式为:
【小问5详解】
有机物H是C 的同分异构体,H能与新制氢氧化铜反应,生成砖红色沉淀,说明
含有醛基,且不含醚键,说明可能还含有羟基或-OOCH,属于酯类的物质有HCOOCH CHCH、
2 2 3
HCOOCH(CH ) 共2种,另外可以看作是CHCHCHCHO、(CH)CHCHO中烃基上的氢原子被羟基取代,
3 2 3 2 2 3 2
依次有3种、2种,符合条件的H共有2+3+2=7种,其峰面积之比为3∶2∶2∶1的结构简式为
HCOOCH CHCH 公众号:高中试卷君
2 2 3
第20页/共20页
学科网(北京)股份有限公司