文档内容
第二章 第二节 分子的空间结构
1.下列有关 杂化轨道的说法错误的是( )
A.由同一能层上的s轨道与p轨道杂化而成
B.所形成的3个 杂化轨道的能量相同
C.每个 杂化轨道中s能级成分占三分之一
D. 杂化轨道最多可形成2个 键
2.利用价层电子对互斥模型可以预测许多分子或离子的空间结构,也可推测键角的大
小,下列判断正确的是( )
A. 是V形分子 B. 的键角大于120°
C. 是三角锥形分子 D. 的键角等于
3.下列有关 和 的说法正确的是( )
A. 和 的空间结构都是三角锥形
B. 中N原子上的孤电子对数为1, 中B原子上无孤电子对
C. 和 形成的化合物 中各原子最外层都达到8电子稳定结构
D. 和 的中心原子的价层电子对数均为4
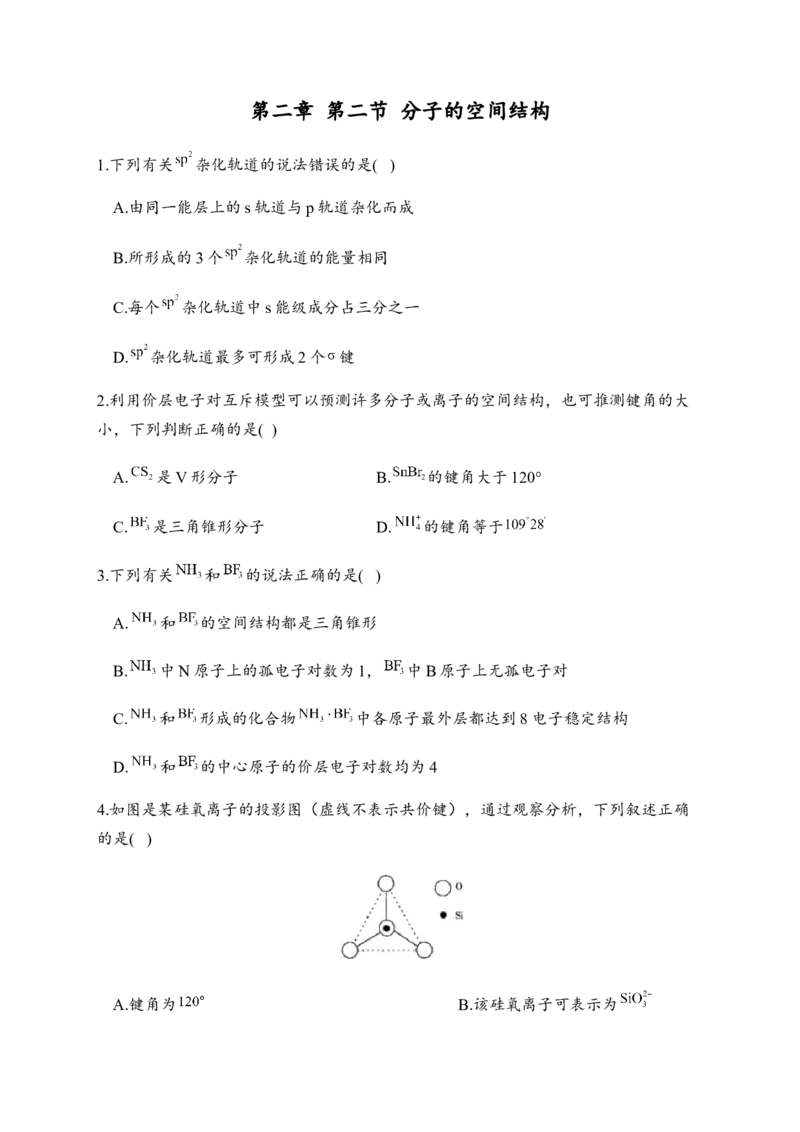
4.如图是某硅氧离子的投影图(虚线不表示共价键),通过观察分析,下列叙述正确
的是( )
A.键角为 B.该硅氧离子可表示为C. Si原子采用 杂化 D.该硅氧离子可表示为
5.杂化轨道理论是鲍林为了解释分子的空间结构提出的。下列关于 、 、sp杂化轨
道的夹角的比较正确的是( )
A.sp杂化轨道的夹角最大 B. 杂化轨道的夹角最大
C. 杂化轨道的夹角最大 D. 、 、sp杂化轨道的夹角相等
6.白磷是一种能自燃的单质,其分子的球棍模型如图所示: ,下列叙述错误
的是( )
A.每个磷原子形成3个 键,磷原子为 杂化
B.每个磷原子的价层电子对数为4,磷原子均为 杂化
C.1mol白磷中共含6mol非极性键
D.白磷分子的空间结构为正四面体形
7. 、 、 都是重要的有机反应中间体,下列说法不正确的是( )
A.碳原子均采取 杂化 B. 中所有原子共面
C. 的空间结构为三角锥形 D. 和 结合可得到
8.化合物A是一种新型锅炉水除氧剂,其结构式如图所示: ,下
列说法正确的是( )
A.碳、氮原子的杂化类型相同
B.氮原子与碳原子分别为 杂化与 杂化
C. 分子中所含 键为10molD.编号为a的氮原子和与其成键的另外三个原子在同一平面内
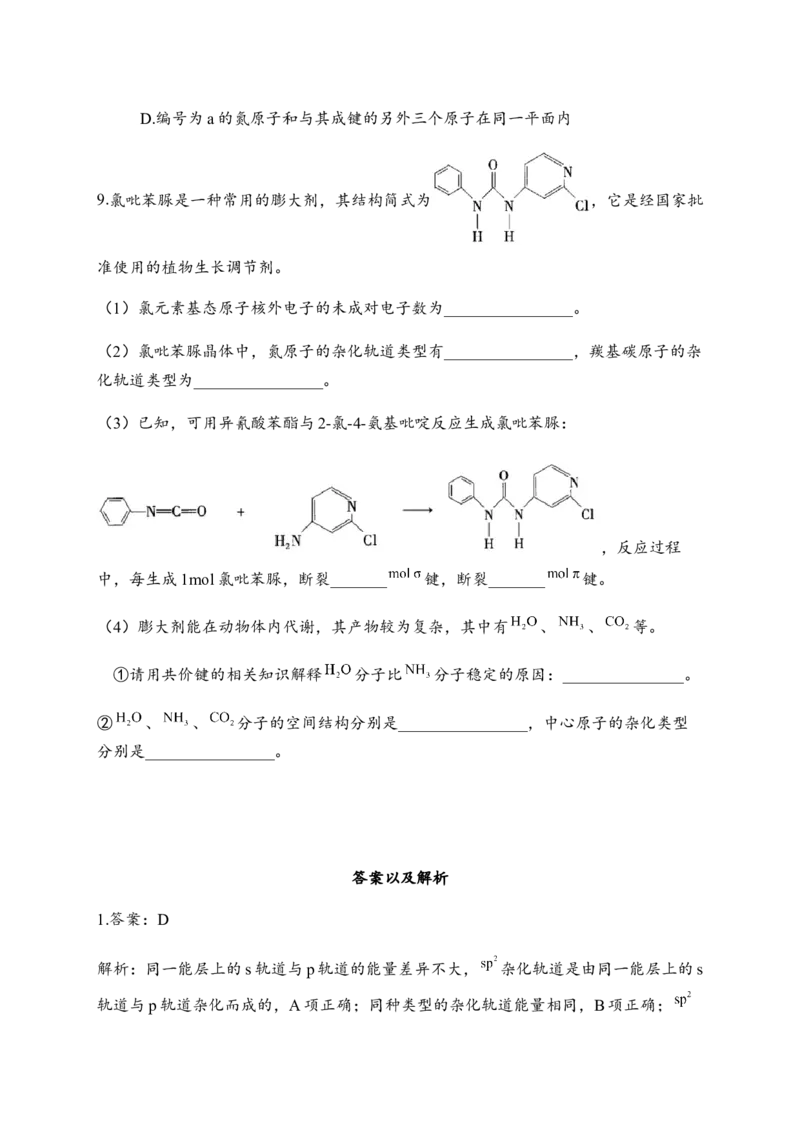
9.氯吡苯脲是一种常用的膨大剂,其结构简式为 ,它是经国家批
准使用的植物生长调节剂。
(1)氯元素基态原子核外电子的未成对电子数为________________。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型有________________,羰基碳原子的杂
化轨道类型为________________。
(3)已知,可用异氰酸苯酯与2-氯-4-氨基吡啶反应生成氯吡苯脲:
,反应过程
中,每生成1mol氯吡苯脲,断裂_______ 键,断裂_______ 键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有 、 、 等。
①请用共价键的相关知识解释 分子比 分子稳定的原因:_______________。
② 、 、 分子的空间结构分别是________________,中心原子的杂化类型
分别是________________。
答案以及解析
1.答案:D
解析:同一能层上的s轨道与p轨道的能量差异不大, 杂化轨道是由同一能层上的s
轨道与p轨道杂化而成的,A项正确;同种类型的杂化轨道能量相同,B项正确;杂化轨道是1个s轨道与2个p轨道杂化而成的,C项正确; 杂化轨道最多可形成3
个 键,D项错误。
2.答案:D
解析: 的中心原子的价层电子对数=2+(4-2×2)÷2=2,不含孤电子对, 为直线
形,A项错误; 的中心原子的价层电子对数=2+(4-2×1)÷2=3,孤电子对数为
1, 为V形,孤电子对与成键电子对之间的排斥力大于成键电子对之间的排斥
力,所以 的键角小于120°,B项错误; 的中心原子的价层电子对数=3+(3-
3×1)÷2=3,不含孤电子对, 为平面三角形,C项错误; 的中心原子的价层电
子对数=4+(5-1×4-1)÷2=4,不含孤电子对, 为正四面体形, 的键角等于
,D项正确。
3.答案:B
解析:A项, 的空间结构为平面三角形,错误;B项, 中N原子上的孤电子对
数= , 中B原子上的孤电子对数= ,正确;C项,
中氢原子形成2电子稳定结构,错误;D项, 中N原子的价层电子对数为
3+1=4, 中B原子的价层电子对数为3+0=3,错误。
4.答案:D
解析:该硅氧离子是以硅原子为中心的正四面体结构,硅氧离子中4个Si O键完全
相同,两个Si O键的夹角为 ,A项错误;根据该硅氧离子的空间结构的投影
图可知,其中含1个硅原子和4个氧原子,硅元素显+4价,氧元素显-2价,故该硅氧
离子可表小为 ,B项错误,D项正确;Si原子核外最外层为4个电子,与氧原子
形成4个 键,无孤电子对故Si原子采用 杂化,C项错误。
5.答案:A
解析: 、 、sp杂化轨道的夹角分别为 、120°、180°,故A项正确。
6.答案:A解析:由白磷分子的球棍模型图可知,每个磷原子均形成了3个 键,且每个磷原子
还有一对孤电子对,故价层电子对数为4,磷原子为 杂化,A项错误,B项正确;
由图可知C、D项正确。
7.答案:A
解析: 和 中碳原子采取 杂化,A项错误; 中碳原子采取 杂化,为平
面三角形,所有原子共面,B项正确; 中C采取 杂化,为三角锥形,C项正
确; 和 结合可得到 ,D项正确。
8.答案:B
解析:A分子中碳、氮原子各形成了3个 键,氮原子有一对孤电子对而碳原子没
有,故氮原子是 杂化而碳原子是 杂化,A项错误,B项正确;A分子中有一个碳
氧双键,故有12个共用电子对、11个 键,C项错误;由于氮原子为 杂化,故相应
的四个原子形成的是三角锥形结构,不可能共平面,D项错误。
9.答案:(1)1 (2) 、 (3)1 1 (4)①H—O键的键能
大于H—N键的键能 ②V形、三角锥形、直线形 、 、sp
解析:(1)氯元素基态原子核外电子排布式是 ,所以未成对电子数为1。
(2)根据氯吡苯脲的结构简式可知,有2个氮原子均形成3个单键,孤电子对数为
1,采取 杂化,剩余1个氮原子形成1个双键和1个单键,孤电子对数为1,采取
杂化;羰基碳原子形成2个单键和1个双键,采取 杂化。
(3)由于 键比 键稳定,根据反应方程式可知,断裂的化学键为异氰酸苯酯分子中
的N==C键中的 键和2-氯-4-氨基吡啶分子中的N—H键。
(4)①O、N属于同周期元素,O的原子半径小于N,H—O键的键能大于H—N键
的键能,所以 分子比 分子稳定。② 分子中O原子的价层电子对数= ,孤电子对数为2,所以其空间结
构为V形,O原子采取 杂化; 分子中N原子的价层电子对数= ,孤
电子对数为1,所以其空间结构为三角锥形,N原子采取 杂化; 分子中C原子
的价层电子对数= ,不含孤电子对,所以其空间结构为直线形,C原子采
取sp杂化。