文档内容
第一课时 盐类的水解基础练习题
1.下列关于盐类水解的叙述错误的是( )
A.盐类水解是中和反应的逆反应
B.盐类水解过程是吸热过程
C.含有弱酸根盐的水溶液一定显碱性
D.盐溶液的酸碱性主要取决于形成盐的酸和碱的相对强弱
2.下列说法中正确的是 ( )
A.HCO -在水溶液中只电离,不水解
3
B.硝酸钠溶液水解后呈中性
C.可溶性的铝盐都能发生水解反应
D.可溶性的钠盐都不发生水解反应
3.pH=4的醋酸和氯化铵溶液中,水的电离程度前者与后者比较 ( )
A.大于
B.小于
C.等于
D.无法比较
4.0.1mol·L-1 NaHCO 溶液的pH最接近于( )
3
A.5.6
B.7.0
C.8.4
D.13.0
5.下列离子组因发生水解反应不能大量共存的是( )
A.Ba2+、NH +、SO 2-、OH-
4 4
B.H+、Na+、NO -、I-
3
C.Al3+、K+、HCO -、NO -
3 3
D.H+、Ca2+、CO2-、Cl-
3
6.室温下,在 pH 都等于 9 的 NaOH 和 CH COONa 两种溶液中,设由水电离产生的 OH-浓度分别为 amol·L-1与
3
bmol·L-1,则a和b关系为 ( )
A.a>b
B.a=10-4b
C.b=10-4a
D. a=b
7.“84”消毒液在日常生活中被广泛使用。该消毒液无色,pH大于7,对某些有色物质有漂白作用。你认为它可能的有
效成分是 ( )
A. SO
2
B. NaCO
2 3
C.KMnO
4
D. NaClO
8.实验测定 NaHCO 溶液显碱性,下列说法中正确的是( )
3
A.在水溶液中,HCO -仅仅发生水解
3
B.在水溶液中,HCO -仅仅发生电离
3
C.在水溶液中,HCO -的水解程度要大于电离程度
3
D.在水溶液中,HCO -的电离程度要大于水解程度
3
9.相同物质的量浓度的NaCN和 NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HClO说法正确
的是 ( )
A.电离程度:HCN>HClO
B. pH: HClO>HCN
C.与NaOH溶液恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.酸根离子浓度:c(CN-)①=②>③
B.①>④>②>③
C.④>①>③>②
D.④>②>①>③
11.由一价离子组成的四种盐:AC、BD、AD、BC溶液的浓度为1mol·L-1,在室温下前两种溶液的pH=7,第三种溶液
pH>7,最后一种溶液pH<7,则 ( )
选项 A B C D
碱性 AOH> BOH AOH BOH AOHHD HC>HD HCb B.a=10-4b C.b=10-4a D. a=b
解析:NaOH抑制水的电离,所以由水电离出的c(OH-)等于溶液中的c(H+)等于10-9mol·L-1;CH COONa水解,促进了水
3
的电离,所以由水电离出的c(OH-)=10-14 / 10-9mol·L-1=10-5mol·L-1,故a/b=10-9 /10-5=10-4,即a=10-4b。答案:B
7.“84”消毒液在日常生活中被广泛使用。该消毒液无色,pH大于7,对某些有色物质有漂白作用。你认为它可能的有
效成分是 ( )
A. SO B. NaCO C.KMnO D. NaClO
2 2 3 4
解析:A项SO 的水溶液呈酸性,C项KMnO 溶液呈中性,NaCO 和 NaCIO溶液呈碱性,但B项没有漂白作用,D
2 4 2 3
项水解生成的HClO具有漂白性。答案:D
8.实验测定 NaHCO 溶液显碱性,下列说法中正确的是( )
3
A.在水溶液中,HCO -仅仅发生水解
3
B.在水溶液中,HCO -仅仅发生电离
3
C.在水溶液中,HCO -的水解程度要大于电离程度
3
D.在水溶液中,HCO -的电离程度要大于水解程度
3
解析:NaHCO 溶液中存在 HCO -的水解:HCO -+H O HCO+OH-, HCO -的电离:HCO - H++CO 2-,因
3 3 3 2 2 3 3 3 3
NaHCO 溶液呈碱性,故其水解程度大于电离程度。答案:C
3
9.相同物质的量浓度的NaCN和 NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HClO说法正确
的是 ( )A.电离程度:HCN>HClO
B. pH: HClO>HCN
C.与NaOH溶液恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.酸根离子浓度:c(CN-)①=②>③ B.①>④>②>③ C.④>①>③>②D.④>②>①>③
解析:本题主要考查对强弱电解质及电离与水解主次矛盾的掌握情况,由于电解质在水中以电离为主,水解是极其微
弱的,所以四种物质中NaCO 电离的阳离子数必为最多,HF为弱电解质,电离出的H+必为最少,先排除B、C项,
2 3
再观察KCl和FeCl ,如果只考虑电离,二者电离的阳离子数应相等,但Fe3+存在水解且一个Fe3+可水解生成三个H+,导
3
致其溶液中阳离子数增多,故D项正确。答案:D
11.由一价离子组成的四种盐:AC、BD、AD、BC溶液的浓度为1mol·L-1,在室温下前两种溶液的pH=7,第三种溶液
pH>7,最后一种溶液pH<7,则 ( )
选项 A B C D
碱性 AOH> BOH AOH BOH AOHHD HC>HD HC7,可知AOH的电离程度大于HD。由BC溶液的pH<7,可知BOH的电离程度小于HC。同理
由AC、BD溶液的pH=7,可知AOH与HC、BOH与HD的电离程度相同。故有电离程度:HC=AOH>HD=BOH,即HC
的酸性大于HD,AOH的碱性大于BOH。答案:A
12.有A、B、C、D四种无色溶液,它们分别是CHCOONa溶液、NH Cl溶液、NaHSO 溶液和BaCl 溶液中的一种。
3 4 4 2
已知:A、B溶液呈酸性,A、C溶液混合后溶液变浑浊。下列说法正确的是( )
A.D溶液的pH<7
B.C溶液是CHCOONa溶液
3
C.溶液A滴入到 NaHCO 溶液中产生气体
3
D.溶液B进行焰色反应呈黄色
解析:根据题意可知:A 为NaHSO 溶液,B为NH Cl溶液,C为BaCl 溶液,D为CHCOONa溶液。A项中D的溶
4 4 2 3
液水解显碱性,pH>7,故A错;B项中C为BaCl 溶液,故B错;C项中A滴入到 NaHCO 溶液中,发生反应:H++
2 3
HCO -=H O+CO↑,故C对;D项溶液B进行焰色反应没有颜色,故D错。答案:C
3 2 2
13.下列离子能促进水电离的是( )
解析:H+、OH-均抑制水的电离;F-水解:F-+H O HF+OH-,促进水的电离;Na+对水的电离无影响。 答案:C
2
14.下列有关盐类水解的说法不正确的是 ( )
A.盐类的水解过程破坏了纯水的电离平衡
B.盐类的水解是酸碱中和反应的逆过程
C.盐类水解的结果使溶液不一定呈中性
D.Na CO 水解的实质是Na 与HO电离出的OH-结合生成了NaOH
2 3 + 2
解析:NaCO 水解的实质是与HO电离出的H+结合成HCO -,使c(OH-)增大而显碱性。答案:D
2 3 2 3
15.下列物质的水溶液由于水解而呈碱性的是 ( )
A. NaHSO B. Na SO C. NaHCO D.NH
4 2 4 3 3
解析:A项,NaHSO 是强酸的酸式盐,不发生水解,错误;B项,NaSO 是强酸强碱盐,不水解,错误;C项是弱
4 2 4
酸的酸式盐,水解使溶液呈碱性,正确;D项NH 是非电解质,溶于水后生成弱碱,错误。答案:C
316.下列物质在常温下发生水解时,对应的离子方程式正确的 ( )
①NaCO:CO 2-+2H O HO+CO↑+2OH-
2 3 3 2 2 2
②NH Cl:NH ++ HO NH •HO+ H+
4 4 2 3 2
③CuSO : Cu2++2H O Cu(OH) +2H+
4 2 2
④NaF:F-+H O=HF+OH-
2
A.①④ B.②③ C.①③ D.②④
解析:①应为 CO2-+H O HCO -+OH-, HCO -+H O HCO+OH- (只写第一步也可);④应为 F-+H O HF+
3 2 3 3 2 2 3 2
OH-。答案:B
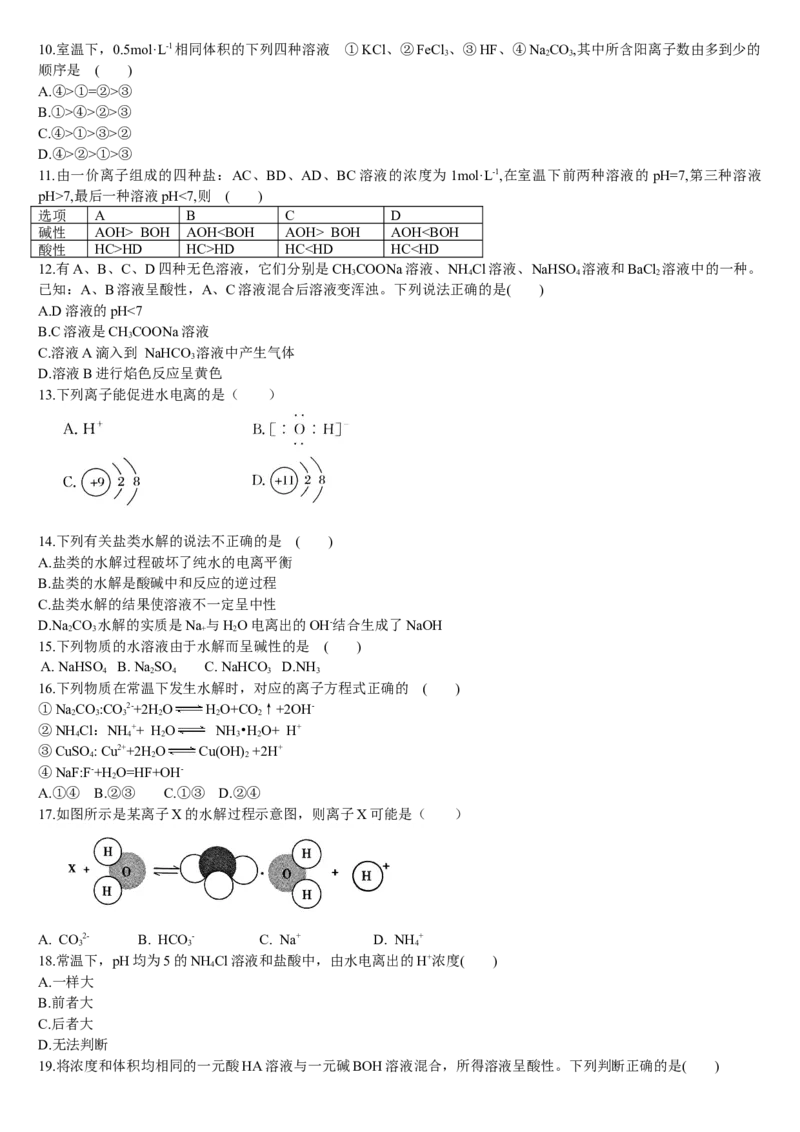
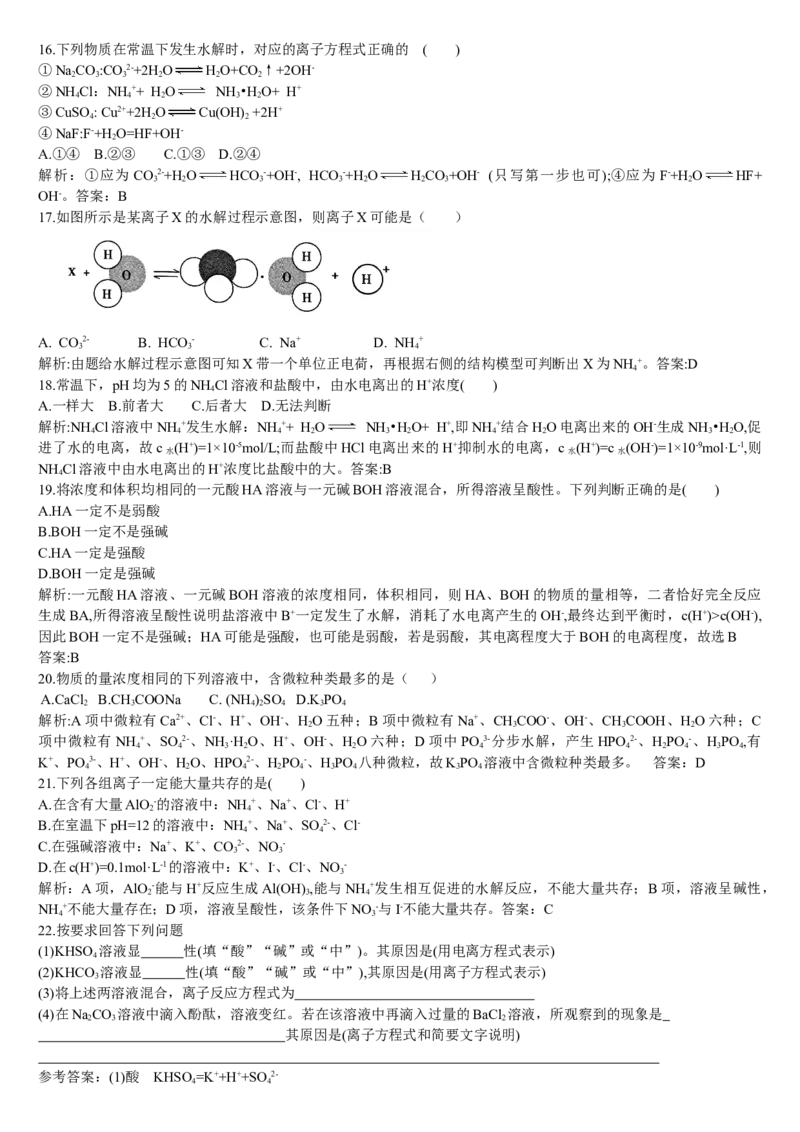
17.如图所示是某离子X的水解过程示意图,则离子X可能是( )
A. CO2- B. HCO - C. Na+ D. NH +
3 3 4
解析:由题给水解过程示意图可知X带一个单位正电荷,再根据右侧的结构模型可判断出X为NH +。答案:D
4
18.常温下,pH均为5的NH Cl溶液和盐酸中,由水电离出的H+浓度( )
4
A.一样大 B.前者大 C.后者大 D.无法判断
解析:NHCl溶液中NH +发生水解:NH ++ HO NH •HO+ H+,即NH +结合HO电离出来的OH-生成NH •HO,促
4 4 4 2 3 2 4 2 3 2
进了水的电离,故c (H+)=1×10-5mol/L;而盐酸中HCl电离出来的H+抑制水的电离,c (H+)=c (OH-)=1×10-9mol·L-1,则
水 水 水
NH Cl溶液中由水电离出的H+浓度比盐酸中的大。答案:B
4
19.将浓度和体积均相同的一元酸HA溶液与一元碱BOH溶液混合,所得溶液呈酸性。下列判断正确的是( )
A.HA一定不是弱酸
B.BOH一定不是强碱
C.HA一定是强酸
D.BOH一定是强碱
解析:一元酸HA溶液、一元碱BOH溶液的浓度相同,体积相同,则HA、BOH的物质的量相等,二者恰好完全反应
生成BA,所得溶液呈酸性说明盐溶液中B+一定发生了水解,消耗了水电离产生的OH-,最终达到平衡时,c(H+)>c(OH-),
因此BOH一定不是强碱;HA可能是强酸,也可能是弱酸,若是弱酸,其电离程度大于BOH的电离程度,故选B
答案:B
20.物质的量浓度相同的下列溶液中,含微粒种类最多的是( )
A.CaCl B.CH COONa C. (NH )SO D.K PO
2 3 4 2 4 3 4
解析:A项中微粒有Ca2+、Cl-、H+、OH-、HO五种;B项中微粒有Na+、CHCOO-、OH-、CHCOOH、HO六种;C
2 3 3 2
项中微粒有NH +、SO 2-、NH ·H O、H+、OH-、HO六种;D项中PO 3-分步水解,产生HPO 2-、HPO -、HPO ,有
4 4 3 2 2 4 4 2 4 3 4
K+、PO 3-、H+、OH-、HO、HPO 2-、HPO -、HPO 八种微粒,故KPO 溶液中含微粒种类最多。 答案:D
4 2 4 2 4 3 4 3 4
21.下列各组离子一定能大量共存的是( )
A.在含有大量AlO-的溶液中:NH +、Na+、Cl-、H+
2 4
B.在室温下pH=12的溶液中:NH +、Na+、SO 2-、Cl-
4 4
C.在强碱溶液中:Na+、K+、CO2-、NO -
3 3
D.在c(H+)=0.1mol·L-1的溶液中:K+、I-、Cl-、NO -
3
解析:A项,AlO-能与H+反应生成Al(OH) ,能与NH +发生相互促进的水解反应,不能大量共存;B项,溶液呈碱性,
2 3 4
NH +不能大量存在;D项,溶液呈酸性,该条件下NO -与I-不能大量共存。答案:C
4 3
22.按要求回答下列问题
(1)KHSO 溶液显 性(填“酸”“碱”或“中”)。其原因是(用电离方程式表示)
4
(2)KHCO 溶液显 性(填“酸”“碱”或“中”),其原因是(用离子方程式表示)
3
(3)将上述两溶液混合,离子反应方程式为
(4)在NaCO 溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的BaCl 溶液,所观察到的现象是
2 3 2
其原因是(离子方程式和简要文字说明)
参考答案:(1)酸 KHSO=K++H++SO2-
4 4(2)碱 HCO -+H O HCO+OH-
3 2 2 3
(3)H++HCO-=H O+CO↑
3 2 2
(4)产生白色沉淀,溶液红色变浅 CO2-+H O HCO -+ OH-,CO 2-+Ba2+=BaCO ↓,Ba2+消耗CO2-,使水解平衡逆移,
3 2 3 3 3 3
碱性减弱,红色变浅
解析(1)KHSO 在水溶液中能完全电离KHSO=K++H++SO2- 溶液显酸性。
4 4 4
(2)KHCO 溶液中HCO -水解:HCO -+H O HCO+OH-显碱性。
3 3 3 2 2 3
(3) H++HCO-=H O+CO↑
3 2 2
(4)Na CO 溶液中CO2-水解:CO2-+H O HCO -+ OH-, (主要)显碱性。加入BaCl , CO2-+Ba2+=BaCO ↓,水解平衡
2 3 3 3 2 3 2 3 3
逆移,碱性减弱,故红色变浅。