文档内容
更多全科试卷,请关注公众号:高中试卷君
2024 年 1 月“九省联考”考后提升卷(河南卷)
高三化学
(考试时间:50分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Mn 55 Ni 59 Ga 70
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
7.化学与科学、技术、社会、生活等密切相关。下列有关说法正确的是
A.用于清洗伤口、杀菌、消毒的医用酒精有强氧化性
B.我国“神舟十二号”飞船返回舱的舱体外壳部件材料是由金属复合材料——专业的铝合金材料制成的,
主要是利用了其硬度大的特性
C.食品袋中放置的CaO可直接防止食品氧化变质
D.客家围屋建造过程中用作黏稠剂的糯米和鸡蛋清都属于混合物
【答案】D
【解析】A.乙醇能够使蛋白质变性,医用酒精可用于清洗伤口、杀菌、消毒,但是乙醇不具有强的氧化
性,故A错误;B.铝合金是制造飞船返回舱的舱体外壳部件材料,这主要利用了它们具有的密度小、强
度好的性能,故B错误;C.食品袋中放置的CaO是干燥剂,不能直接防止食品氧化变质,故C错误;
D.糯米的成分是淀粉,鸡蛋清成分是蛋白质,都是高分子化合物,聚合度不确定,都属于混合物,故D
正确;故选D。
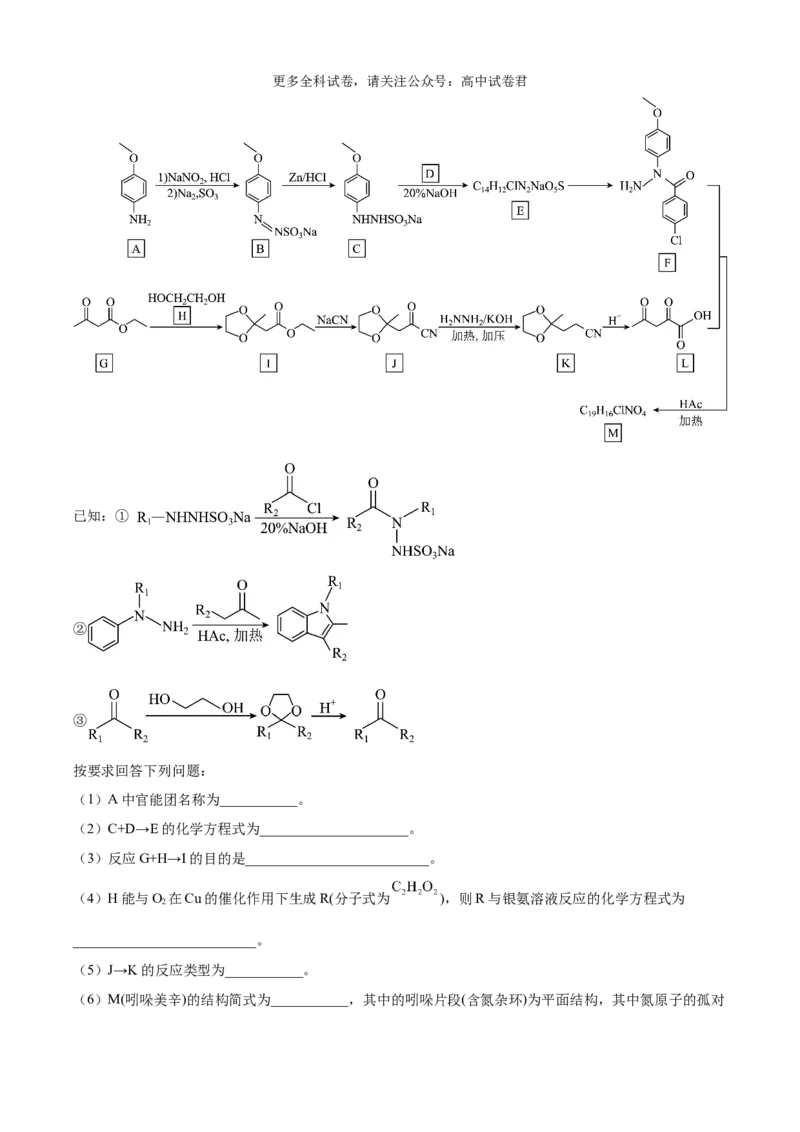
8.有机化合物Z具有镇痛、消炎等药理作用,其合成路线关键步骤如下:
有关有机物X、Y和Z的说法正确的是
A.1molZ最多只能与1molNaOH反应更多全科试卷,请关注公众号:高中试卷君
B.有机物Y含有3种含氧官能团
C.有机物X与丙烯酸互为同系物
D.有机物Z中含有手性碳原子
【答案】C
【分析】由有机物的转化关系可知,一定条件下, 与 发生取
代反应生成 和水,则Y为 。
【解析】A.由结构简式可知, 分子中含有的酚羟基和酰胺基能
与氢氧化钠溶液反应,则1molZ最多只能与2mol氢氧化钠反应,故A错误;
B.由结构简式可知, 分子的含氧官能团为醚键、酚羟基,共有2种,故B错误;
C.由结构简式可知, 与丙烯酸含有结构相似,分子组成上相差若干个CH
2
原子团,互为同系物,故C正确;
D.由结构简式可知, 分子中不含有连有4个不同原子或原子团
的手性碳原子,故D错误;
故选C。
9.钴(Co)在化学上称为铁系元素,其化合物在生产生活中应用广泛。以甲醇为溶剂,Co2+可与色胺酮分子
配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示),下列说法错误的是更多全科试卷,请关注公众号:高中试卷君
A.色胺酮分子中所含元素第一电离能由大到小的顺序为N>O>H>C
B.色胺酮分子中N原子均为sp3杂化
C.色胺酮钴配合物中钴的配位数为4
D.X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个CHOH分子,CHOH是通过氢键作用与色胺
3 3
酮钴配合物相结合
【答案】B
【解析】A.同周期元素,从左到右第一电离能呈增大趋势,氮原子的2p轨道为稳定的半充满结构,元素
的第一电离能大于O,则第一电离能由大到小的顺序为N>O>C,氢原子的原子半径小,核外电子受到原
子核的引力大于碳原子,失去1个电子消耗的能量大于碳,第一电离能大于大于碳,则元素第一电离能由
大到小的顺序为N>O>H>C,故A正确;
B.由结构简式可知,色胺酮分子中形成双键的氮原子的杂化方式为sp2杂化,故B错误;
C.由结构简式可知,色胺酮钴配合物中钴离子与2个氮原子和2个氧原子形成配位键,的配位数为4,故
C正确;
D.甲醇分子中的羟基可以形成氢键,则X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个甲醇分子
说明甲醇通过氢键作用与色胺酮钴配合物相结合,故D正确;
故选B。
10.微生物燃料电池碳氮联合去除的氮转化系统原理如图所示。下列说法错误的是
A.a极电势低于b极
B.离子交换膜是质子交换膜更多全科试卷,请关注公众号:高中试卷君
C.a、b两极生成 和 的物质的量之比为5∶4
D.好氧微生物反应器中反应的离子方程式为
【答案】C
【解析】从图分析,a电极上为乙酸根离子生成二氧化碳,失去电子,为负极反应,b为正极。据此解答。
A.a为负极,b为正极,正极电极比负极高,A正确;
B.a的电极反应为 ,b的电极反应为 ,
氢离子向正极移动,故使用质子交换膜膜,B正确;
C.根据ab电极反应分析,电子守恒,则二氧化碳和氮气的物质的量比为10:4=5:2,C错误;
D.从图分析,铵根离子和氧气进去反应生成硝酸根离子,故反应的离子方程式为:
,D正确;
故选C。
11.下列实验操作正确且能达到实验目的的是
A B C D
证明非金属性:
钠的燃烧反应 验证 制备
【答案】D
【解析】A.Na在空气中燃烧生成 , 吸收空气中的水蒸气生成NaOH,NaOH能和玻璃中的
反应,不能用玻璃表面器皿做钠的燃烧反应实验,A错误;
B.稀硫酸和硫化钠反应生成硫化氢气体,硫化氢与硝酸银溶液直接反应生成硫化银沉淀,不发生沉淀转
化,不能验证 ,B错误;更多全科试卷,请关注公众号:高中试卷君
C.制备 的原理是向饱和NaCl溶液中先后通入 和 ,通 的导气管应该伸入液面以下,
C错误;
D.最高价含氧酸的酸性越强,对应元素的非金属性越强,稀硫酸与碳酸钠反应,生成的 通入硅酸钠
溶液中,生成白色沉淀硅酸,即酸性:硫酸>碳酸>硅酸,D正确;
故选D。
12.甲烷可在铑/铈氧化物的催化下与过氧化氢反应,转化为甲醇和甲基过氧化氢 ,实现了天然
气的高效利用,其原理如图所示,下列说法错误的是
A.反应③有极性键的断裂与生成
B.反应⑤中,Ce的化合价升高
C.铑/铈氧化物改变了 和 的反应历程,降低了反应的活化能
D.若用 作反应物,一段时间后只有 、 中含有
【答案】D
【解析】A.反应③中CH 中断裂1条C-H键形成∙CH,∙OH与H形成HO中有O-H键生成,则有极性键
4 3 2
的断裂与生成,A正确;B.反应⑤中,HO→HO中O元素从-1降低至-2价,则Ce的化合价升高,B正
2 2 2
确;C.铑/铈氧化物是催化剂,可改变了CH 和HO 的反应历程,降低了反应的活化能,C正确;D.由
4 2 2
反应⑤可知O连接在Ce上,甲烷可在铑/铈氧化物的催化下与过氧化氢反应,转化为甲醇和甲基过氧化氢
(CHOOH),则若用Hl8O 作反应物,一段时间后CHOH、CHOOH和铑/铈氧化物中均含有18O,D错误;
3 2 2 3 3
故选D。
13.已知常温下水溶液中 、 、 、HB、 的分布分数δ[如更多全科试卷,请关注公众号:高中试卷君
]随pH变化曲线如图1;溶液中 和 关系如图2.用
溶液滴定20.00mL 溶液,下列说法错误的是
A.曲线d表示δ(HB)
B. 的水解平衡常数
C.滴定过程中溶液会变浑浊
D.滴定过程中始终存在:
【答案】D
【解析】A.由题中信息可知, 为二元弱酸, 、 ,用
溶液滴定20.00mL 溶液,发生反应: ,则
酸性: >HB,所以曲线a、b、c表示 的各微粒分布曲线,曲线a代表 ,曲线b代表 ,曲
线c代表 ,曲线d为HB,曲线e为 ,故A正确;
B. 的水解平衡常数 ,曲线d和e相交时 = , ,此时
pH=8.3, = ,则 ,故B正确;
C.根据图2可知,滴定过程中会生成CaA沉淀,溶液变浑浊,故C正确;
D.若滴定过程中不产生沉淀,则根据电荷守恒: ,根据更多全科试卷,请关注公众号:高中试卷君
物料守恒: = + ,则 ,但随着HA溶液的滴入,
2
Ca2+产生CaA沉淀而析出,溶液中 + ,则 ,
故错误;
故选:D。
二、非选择题:本题共4小题,共58分。
27.(14分)氰化钠 是一种重要的基本化工原料,同时也是一种剧毒物质,一旦泄漏需要及时处
理。一般可以用双氧水或硫代硫酸钠( )溶液来处理,以减轻环境污染。
(1) 易水解生成氰化氢(有剧毒,易在空气中均匀弥散)。 中C的化合价为___________;实
验室用 固体配制 溶液时,应先将其溶于氢氧化钠溶液中,再用蒸馏水稀释,其目的是
___________。 用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反
应的离子方程式是___________。
(2)工业制备硫代硫酸钠的反应原理: 。某化学小组利用该原
理在实验室制备硫代硫酸钠。
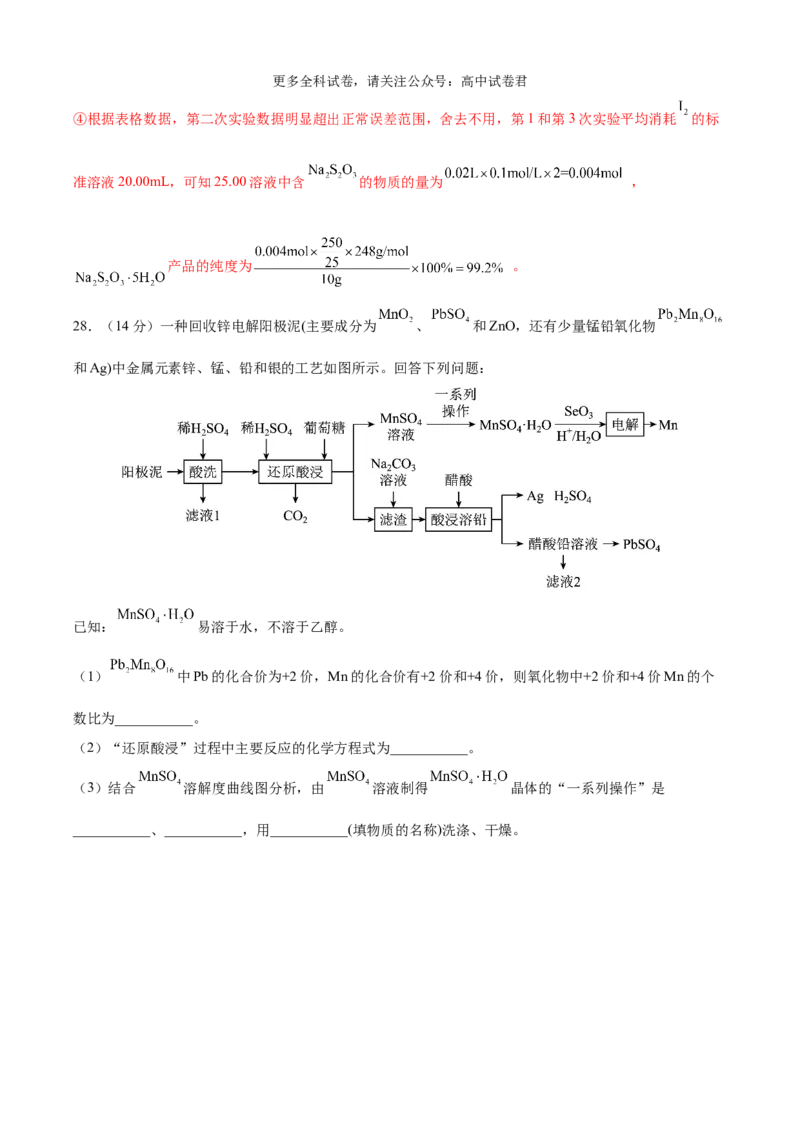
【实验一】制备硫代硫酸钠的装置如图所示。
①盛放 和 混合溶液的仪器名称是___________。
② 溶液的作用是___________。
【实验二】测定硫代硫酸钠产品的纯度。
制备的硫代硫酸钠产品一般为 ,可用 的标准溶液测定产品的纯度:取 产品配制成更多全科试卷,请关注公众号:高中试卷君
溶液,取 溶液,用 的标准溶液进行滴定(原理为
),相关数据记录如表:
实验编号 1 2 3
溶液体积 25.00 25.00 25.00
消耗 的标准溶液体积 20.05 18.00 19.95
③上述滴定操作中应该选用___________作为反应的指示剂。
④ 产品的纯度为___________。
【答案】(除标明外,每空2分)
(1)+2(1分) 防止 水解产生 污染环境
(2)①三颈烧瓶 ②尾气处理 ③淀粉溶液 ④99.2%(3分)
【解析】氧化还原反应中氧化剂得电子化合价降低,还原剂失电子化合价升高,根据得失电子守恒配平方
程式;
把二氧化硫通入盛放 和 混合溶液的三口烧瓶中发生
反应制备 ,用氢氧化钠溶液吸收剩余二氧化硫,防止污染。
(1) 中Na显+1价、N显-3价,根据化合价代数和等于0,C的化合价为+2; 易水解生成氰
化氢,溶液显碱性,为抑制 水解产生 污染环境,实验室用 固体配制 溶液时,应先将
其溶于氢氧化钠溶液中,再用蒸馏水稀释。 用双氧水处理后,产生一种酸式盐碳酸氢钠和一种能使
湿润红色石蕊试纸变蓝的气体氨气,反应中C元素化合价由+2升高为+4、双氧水中O元素化合价由-1降
低为-2,该反应的离子方程式是 ;
(2)①根据装置图,盛放 和 混合溶液的仪器名称是三口烧瓶。
②二氧化硫有毒,二氧化硫能被氢氧化钠吸收,所以 溶液的作用是吸收二氧化硫,防止污染,处理
尾气。
③碘能使淀粉溶液变蓝,上述滴定操作中应该选用淀粉溶液作为反应的指示剂。更多全科试卷,请关注公众号:高中试卷君
④根据表格数据,第二次实验数据明显超出正常误差范围,舍去不用,第1和第3次实验平均消耗 的标
准溶液20.00mL,可知25.00溶液中含 的物质的量为 ,
产品的纯度为 。
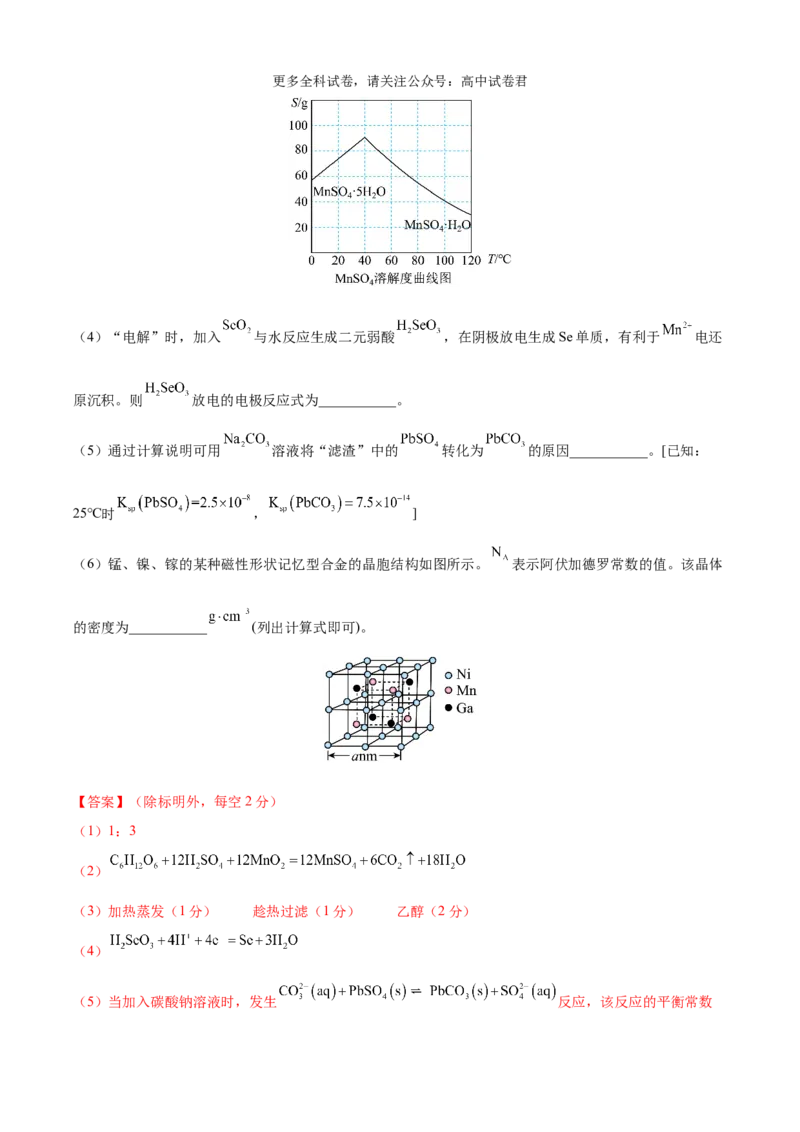
28.(14分)一种回收锌电解阳极泥(主要成分为 、 和ZnO,还有少量锰铅氧化物
和Ag)中金属元素锌、锰、铅和银的工艺如图所示。回答下列问题:
已知: 易溶于水,不溶于乙醇。
(1) 中Pb的化合价为+2价,Mn的化合价有+2价和+4价,则氧化物中+2价和+4价Mn的个
数比为___________。
(2)“还原酸浸”过程中主要反应的化学方程式为___________。
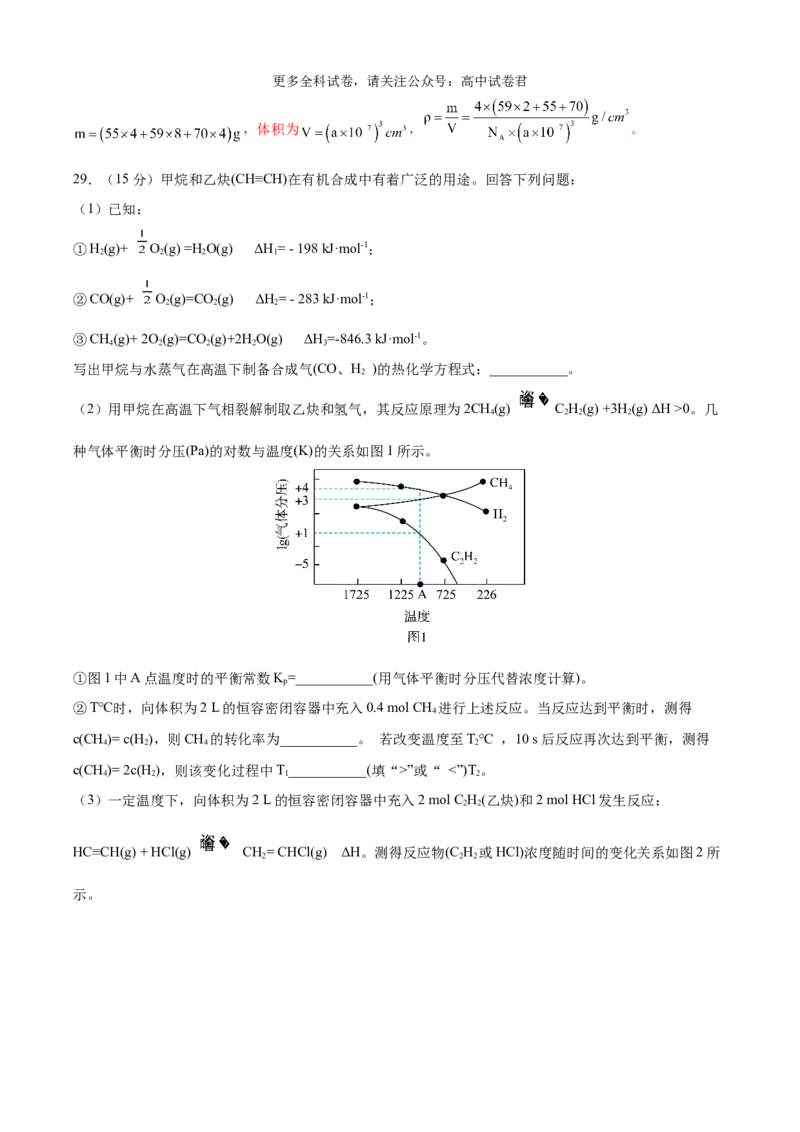
(3)结合 溶解度曲线图分析,由 溶液制得 晶体的“一系列操作”是
___________、___________,用___________(填物质的名称)洗涤、干燥。更多全科试卷,请关注公众号:高中试卷君
(4)“电解”时,加入 与水反应生成二元弱酸 ,在阴极放电生成Se单质,有利于 电还
原沉积。则 放电的电极反应式为___________。
(5)通过计算说明可用 溶液将“滤渣”中的 转化为 的原因___________。[已知:
25℃时 , ]
(6)锰、镍、镓的某种磁性形状记忆型合金的晶胞结构如图所示。 表示阿伏加德罗常数的值。该晶体
的密度为___________ (列出计算式即可)。
【答案】(除标明外,每空2分)
(1)1:3
(2)
(3)加热蒸发(1分) 趁热过滤(1分) 乙醇(2分)
(4)
(5)当加入碳酸钠溶液时,发生 反应,该反应的平衡常数更多全科试卷,请关注公众号:高中试卷君
,几乎可以完全转化
(6)
【分析】向阳极泥中加入稀硫酸将ZnO转成ZnSO,随滤液除去,向滤渣中加稀硫酸和葡萄糖酸浸还原+4
价Mn为+2价得滤渣1,过滤处理MnSO 滤液,获取 晶体,滤渣1中加入NaCO、溶液转化
4 2 3
PbSO ,为PbCO ,再向滤渣中加醋酸溶解Pb元素并分离出单质 Ag,醋酸铅溶液经酸化后获取硫酸铅,
4 3
据此可解答;
【解析】(1)设Pb MnO 中含a个+2价Mn,则+4价Mn有(8-a)个,据化合价代数和为0列式为
2 8 16
,解得a=2,则+2价和+4价Mn的个数比为1:3;
(2)还原酸浸过程中葡萄糖将+4价Mn还原为+2Mn,发生反应的方程式
;
(3)醋酸铅溶液经酸化后得到滤液主要成分是醋酸,因此醋酸可循环使用;当进行蒸发结晶出的晶体与
滤液分离操作时需进行趁热过滤,防止杂质从中因温度降低而析出混入;洗涤的操作采用过滤装置,品体
样品易溶于水,难溶于乙醇,可向漏斗中加入乙醇至浸没 品体,待乙醇自然流尽后重复2-3次;
(4)HSeO 中Se的化合价为+4价,生成0价的Se单质,则HSeO+4H++4e−=Se+3H O;
2 3 2 3 2
(5) 当加入碳酸钠溶液时,发生 反应,该反应的平衡常数
,几乎可以完全转化;
(6)根据图示,Ni原子处于的位置为顶点8个,面心6个,棱心12个,体心1个,则Ni的个数为
,Mn原子处于的位置为体内,则有4个原子,Ga原子位于体内,4个,则更多全科试卷,请关注公众号:高中试卷君
,体积为 , 。
29.(15分)甲烷和乙炔(CH≡CH)在有机合成中有着广泛的用途。回答下列问题:
(1)已知:
①H(g)+ O(g) =H O(g) ΔH= - 198 kJ·mol-1;
2 2 2 1
②CO(g)+ O(g)=CO (g) ΔH= - 283 kJ·mol-1;
2 2 2
③CH(g)+ 2O (g)=CO (g)+2HO(g) ΔH=-846.3 kJ·mol-1。
4 2 2 2 3
写出甲烷与水蒸气在高温下制备合成气(CO、H )的热化学方程式:___________。
2
(2)用甲烷在高温下气相裂解制取乙炔和氢气,其反应原理为2CH(g) C H(g) +3H (g) ΔH >0。几
4 2 2 2
种气体平衡时分压(Pa)的对数与温度(K)的关系如图1所示。
①图1中A点温度时的平衡常数K=___________(用气体平衡时分压代替浓度计算)。
p
②T℃时,向体积为2 L的恒容密闭容器中充入0.4 mol CH 进行上述反应。当反应达到平衡时,测得
4
c(CH)= c(H),则CH 的转化率为___________。 若改变温度至T℃ ,10 s后反应再次达到平衡,测得
4 2 4 2
c(CH)= 2c(H),则该变化过程中T___________(填“>”或“ <”)T。
4 2 1 2
(3)一定温度下,向体积为2 L的恒容密闭容器中充入2 mol C H(乙炔)和2 mol HCl发生反应:
2 2
HC≡CH(g) + HCl(g) CH= CHCl(g) ΔH。测得反应物(C H 或HCl)浓度随时间的变化关系如图2所
2 2 2
示。更多全科试卷,请关注公众号:高中试卷君
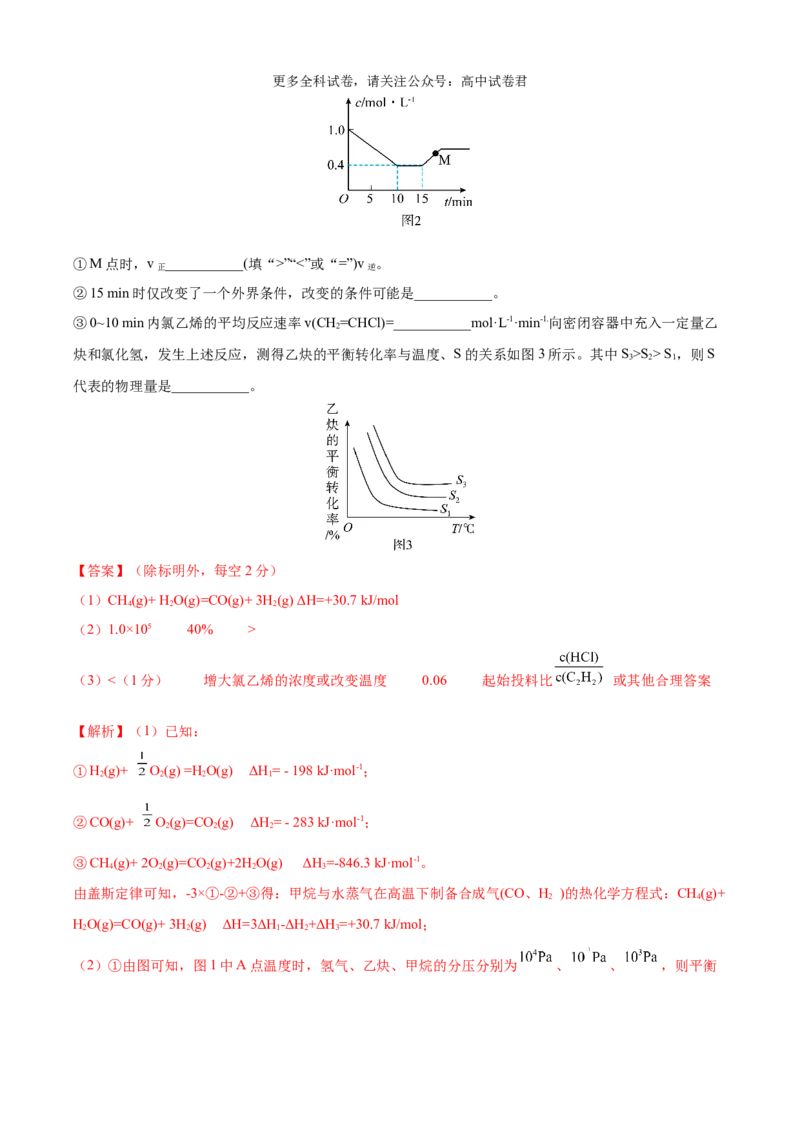
①M点时,v ___________(填“>”“<”或“=”)v 。
正 逆
②15 min时仅改变了一个外界条件,改变的条件可能是___________。
③0~10 min内氯乙烯的平均反应速率v(CH=CHCl)=___________mol·L-1·min-1.向密闭容器中充入一定量乙
2
炔和氯化氢,发生上述反应,测得乙炔的平衡转化率与温度、S的关系如图3所示。其中S>S > S ,则S
3 2 1
代表的物理量是___________。
【答案】(除标明外,每空2分)
(1)CH(g)+ H O(g)=CO(g)+ 3H (g) ΔH=+30.7 kJ/mol
4 2 2
(2)1.0×105 40% >
(3)<(1分) 增大氯乙烯的浓度或改变温度 0.06 起始投料比 或其他合理答案
【解析】(1)已知:
①H(g)+ O(g) =H O(g) ΔH= - 198 kJ·mol-1;
2 2 2 1
②CO(g)+ O(g)=CO (g) ΔH= - 283 kJ·mol-1;
2 2 2
③CH(g)+ 2O (g)=CO (g)+2HO(g) ΔH=-846.3 kJ·mol-1。
4 2 2 2 3
由盖斯定律可知,-3×①-②+③得:甲烷与水蒸气在高温下制备合成气(CO、H )的热化学方程式:CH(g)+
2 4
HO(g)=CO(g)+ 3H (g) ΔH=3ΔH-ΔH +ΔH =+30.7 kJ/mol;
2 2 1 2 3
(2)①由图可知,图1中A点温度时,氢气、乙炔、甲烷的分压分别为 、 、 ,则平衡更多全科试卷,请关注公众号:高中试卷君
常数K= 。
p
②T℃时,向体积为2 L的恒容密闭容器中充入0.4 mol CH 进行上述反应;
4
当反应达到平衡时,测得c(CH)= c(H),则0.4-2a=3a,a=0.8mol,则CH 的转化率为 。
4 2 4
若改变温度至T℃ ,10 s后反应再次达到平衡,测得c(CH)= 2c(H),则该变化过程中平衡逆向移动,甲
2 4 2
烷含量增大,由于反应ΔH >0,正反应为吸热反应,则说明为降温的过程,则T>T。
1 2
(3)①由图可知,M点后,反应物(C H 或HCl)浓度仍增大,说明M点时反应逆向进行,此时v