文档内容
高中化学人教版(2019)选择性必修1 第一章第一节 反应热
一、单选题
1.下列说法错误的是( )
A. 化学反应除了生成新物质外,还伴随着能量的变化
B. 放热反应不需要加热就可以发生
C. 反应条件是加热的反应不一定都是吸热反应
D. 化学反应放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量
www.21-cn-jy.com
2.下列反应过程中的能量变化与图一致的是( )
A. 2HO 2H↑ + O ↑ B. 在 加 热 条 件 下 氢 气 还 原 氧 化 铜 C. 胆 矾 受 热 分
2 2 2
解 D. 铝热反应
3.下列变化过程吸热的有多少个( )
①Ba(OH) ·8H O与NH Cl晶体混合搅拌;②盐酸和氢氧化钠溶液混合;③硫受热融化;④石灰石高温分解;
2 2 4
⑤碳和氧气反应生成一氧化碳;⑥生石灰和水反应生成熟石灰;⑦镁条在氮气中燃烧;⑧碳在高温下和水蒸
气反应生成水煤气;⑨水蒸气液化
21cnjy.com
A. 4个 B. 5个
C. 6个
D. 7个
4.下列属于吸热反应是( )
A. 金属钠与水的反应
B. 盐酸与氢氧化钠的反应
C. 铝与氧化铁的铝热反应
D. NH Cl晶体与Ba(OH) ·8H O晶体反应
4 2 2
5.已知甲烷的热值为56kJ/g,表示甲烷标准燃烧热的热化学方程式的是( )
A. CH(g)+2O (g)=CO (g)+2HO(g) △H=-56kJ·mol-1
4 2 2 2
B. CH(g)+2O(g)=CO (g)+2HO(g) △H=-896kJ·mol-1
4 2 2 2C. CH(g)+2O(g)=CO (g)+2HO(1) △H=-896kJ·mol-1
4 2 2 2
D. 2CH
4
(g)+4O
2
(g)=2CO
2
(g)+4H
2
O(1)△H=-112kJ·mol-1
2·1·c·n·j·y
6.N H 是一种高效清洁的火箭燃料。已知在25℃、101kPa下,8gNH(g)完全燃烧生成氮气和液态水时,放出
2 4 2 4
133.5 kJ热量。则下列热化学方程中正确的是( )
www-2-1-cnjy-com
A. NH(g)+O (g)=N (g)+2HO(g) △H=-534kJ·mol-1
2 4 2 2 2
B. NH(g)+O(g)=N(g)+2HO(l) △H=-133.5kJ·mol-1
2 4 2 2 2
C. NH(g)+O(g) =N (g)+2HO(l) △H=+534kJ·mol-1
2 4 2 2 2
D. N 2 H 4 (g)+O 2 (g) =N 2 (g)+2H 2 O(l) △H=-534kJ·mol-1 21教育名师原创作品
7.已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的( )
A. X的能量一定高于M B. Y的能量一定高于N
C. X和Y的总能量一定高于M和N的总能量 D. 因该反应为放热反应,故不必加热
就可发生反应
二、综合题
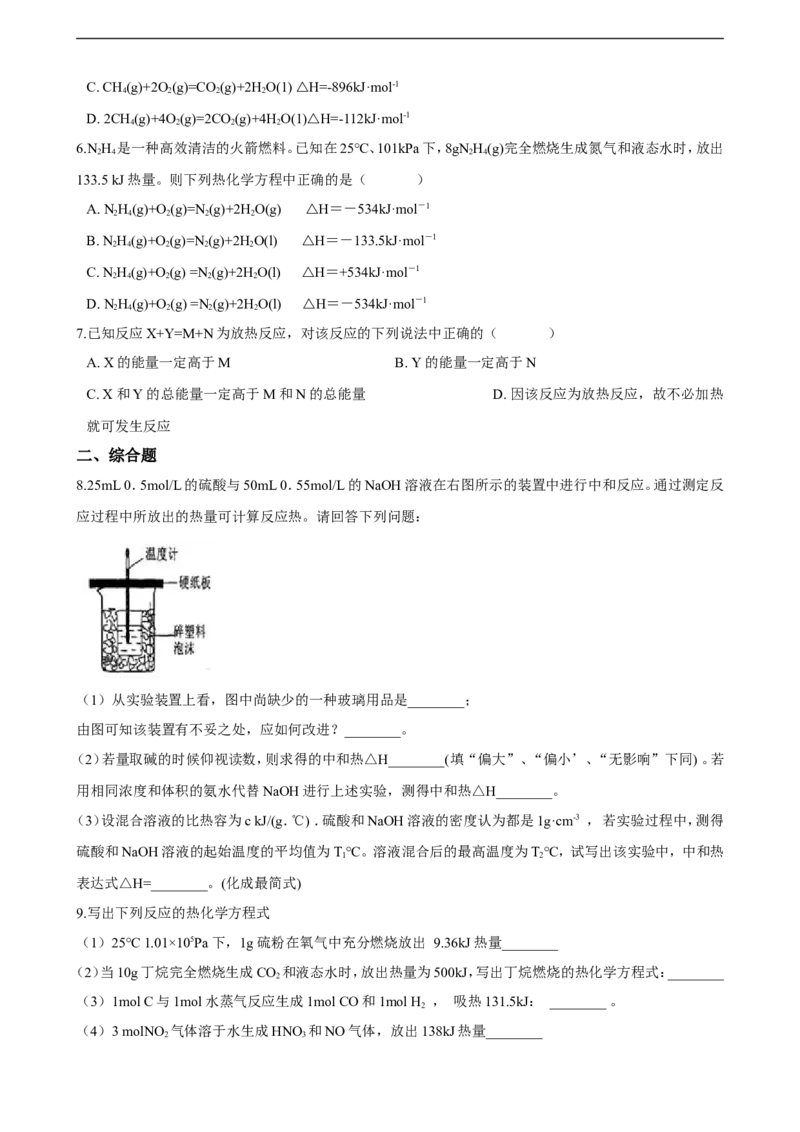
8.25mL 0.5mol/L的硫酸与50mL 0.55mol/L的NaOH溶液在右图所示的装置中进行中和反应。通过测定反
应过程中所放出的热量可计算反应热。请回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________;
由图可知该装置有不妥之处,应如何改进?________。
(2)若量取碱的时候仰视读数,则求得的中和热△H________(填“偏大”、“偏小’、“无影响”下同) 。若
用相同浓度和体积的氨水代替NaOH进行上述实验,测得中和热△H________。
(3)设混合溶液的比热容为c kJ/(g.℃) .硫酸和NaOH溶液的密度认为都是1g·cm-3 , 若实验过程中,测得
硫酸和NaOH溶液的起始温度的平均值为T℃。溶液混合后的最高温度为T℃,试写出该实验中,中和热
1 2
表达式△H=________。(化成最简式)
9.写出下列反应的热化学方程式
(1)25℃ 1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36kJ热量________
(2)当10g丁烷完全燃烧生成CO 和液态水时,放出热量为500kJ,写出丁烷燃烧的热化学方程式:________
2
(3)1mol C与1mol水蒸气反应生成1mol CO和1mol H , 吸热131.5kJ: ________ 。
2
(4)3 molNO 气体溶于水生成HNO 和NO气体,放出138kJ热量________
2 310.已知下列热化学方程式:
① H (g)+ O(g)=HO(l) ΔH =-285kJ/mol
2 2 2
② H(g)+ O(g)=HO(g) ΔH =-241.8kJ/mol
2 2 2
③ C(s)+ O(g)=CO(g) ΔH =-110.4 kJ/mol
2
④ C(s)+ O (g)=CO(g) ΔH =-393.5 kJ/mol
2 2
回答下列各问:
(1)上述反应中属于放热反应的是________。
(2)C的燃烧热为________。
(3)燃烧10g H 生成液态水,放出的热量为________。
2
(4)CO燃烧的热化学方程式为________。
(5)为了控制温室效应,各国科学家提出了不少设想。有人根据液态CO 密度大于海水密度的事实,设想将
2
CO 液化后,送入深海海底,以减少大气中的CO。为使CO 液化,可采取的措施________。
2 2 2
a 减压、升温 b 增压、降温
c 减压、降温 d 增压、升温答案解析部分
一、单选题
1. B
解析:A. 化学反应过程中断裂化学键吸收能量,形成化学键放出热量,反应过程中一定伴随能量变化,A不
符合题意;
B. 某些放热反应需要加热条件下才能发生反应,Al和Fe O 发生的铝热反应在引发剂作用下才能发生反应,
2 3
B符合题意;
C. 反应条件是加热的反应不一定都是吸热反应,Al和Fe O 发生的铝热反应在引发剂作用下才能发生反应,
2 3
但Al和Fe O 是放热反应,C不符合题意;
2 3
D. 化学反应放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量的相对高低,生成物能量高
是吸热反应,反之是放热反应,D不符合题意。
故答案为:B
分析:A. 化学反应过程中一定伴随能量变化;
B. 放热反应可能需要加热才能发生;
C. 需要加热的反应不一定是吸热反应;
D. 生成物具有的总能量大于反应物具有的总能量为放热反应,反之为吸热反应。
2. D
解析:A、电解时,电能转化为化学能,为吸热反应,故A不选;
B、在加热条件下氢气还原氧化铜为吸热反应,故B不选;
C、胆矾受热分解为吸热反应,故C不选;
D、铝热反应为放热反应,符合图像,故D选。
故答案为:D。
分析:由图可知,反应物能量大于生成物能量,因此该反应为放热反应,常见的放热反应有:所有的燃烧反
应,金属与酸或水的反应、酸碱中和反应、铝热反应、多数的化合反应等,其△H<0。常见的吸热反应:Ba
(OH)•8H O与NH Cl晶体混合反应、水解反应、大多数的分解反应、以C、CO、H 作为还原剂的反应等,以
2 2 4 2
此解答该题。
【来源:21·世纪·教育·网】
3. A
解析:①Ba(OH) ·8H O与NH Cl的反应为吸热反应,①符合题意;
2 2 4
②盐酸和NaOH溶液的反应为酸碱中和反应,属于放热反应,②不符合题意;
③硫受热融化需要吸收能量,因此过程中吸热,③符合题意;④石灰石高温分解为吸热反应,④符合题意;
⑤碳和氧气的反应生成CO,为燃烧反应,燃烧反应都是放热反应,⑤不符合题意;
⑥生石灰与水的反应为放热反应,⑥不符合题意;
⑦镁条在氮气中燃烧,燃烧反应属于放热反应,⑦不符合题意;
⑧碳在高温下和水蒸气反应生成水煤气,该反应为吸热反应,⑧符合题意;
⑨水蒸气液化过程放热,⑨不符合题意;
综上,上述变化过程中吸热的有①③④⑧,共4个,A符合题意;
21*cnjy*com
故答案为:A
分析:根据所给反应的热效应进行分析即可得出答案。
4. D
解析:A.金属钠与水的反应属于放热反应,故A不符合题意;
B.盐酸和氢氧化钠溶液反应为中和反应,是放热反应,故B不符合题意;
C.铝热反应属于放热反应,故C不符合题意;
D.氯化铵晶体与氢氧化钡晶体反应,属于吸热反应,故D符合题意;
故答案为:D。
分析:熟记 NH Cl晶体与Ba(OH) ·8H O晶体反应为吸热反应
4 2 2
5. C
解析:甲烷的热值为 56kJ/g,即表示 1gCH 完全燃烧,生成 CO(g)和 HO(l)时放出的热量为 56kJ/
4 2 2
g×16g=896kJ,所以甲烷的燃烧热ΔH=-896kJ/mol,所以表示甲烷标准燃烧热的热化学方程式为:CH(g)
4
+2O
2
(g)=CO
2
(g)+2H
2
O(1) △H=-896kJ·mol-1 , C符合题意;
21·cn·jy·com
故答案为:C
分析:此题是对燃烧热定义和热化学方程式书写的考查,燃烧热是指1mol纯物质完全燃烧生成稳定氧化物
时放出的热量;结合题干所给甲烷的热值计算甲烷的燃烧热,从而得出甲烷标准燃烧热的热化学方程式。
6. D
解析:8gNH(g)的物质的量 , 所以 1molN H(g)燃烧放出的热量为
2 4 2 4
, 因此该反应的热化学方程式为NH(g)+O(g)=N(g)+2HO(l) ΔH=-534kJ/mol,
2 4 2 2 2
D符合题意;
21世纪教育网版权所有
故答案为:D
分析:根据公式 计算8gNH(g)的物质的量,结合其燃烧放出的热量计算1molN H(g)燃烧放出的热
2 4 2 4
量,从而书写反应的热化学方程式。
2-1-c-n-j-y7. C
解析:A. 反应物的总能量大于生成物的总能量,X的能量与M的能量关系无法确定,A项不符合题意;
B. 反应物的总能量大于生成物的总能量,Y的能量与N的能量关系无法确定,B项不符合题意;
C. 该反应为放热反应,所以反应物的总能量大于生成物的总能量,即X和Y的总能量一定高于M和N的
总能量,C项符合题意;
21教育网
D. 反应的放热、吸热与反应条件(如加热)无关,某些放热反应也需要加热才能反应,如氢气和氧气的反应,
D项不符合题意;
【出处:21教育名师】
答案选C。
分析:放热反应的本质是反应物的总能量大于生成物的总能量,所以反应放热,以此解答。
二、综合题
8. (1)环形玻璃搅拌棒;①小烧杯上沿紧贴硬纸板②碎泡沫塑料填充满大烧杯
(2)偏大;偏大
(3)-3000c(T -T )kJ/mol或3000c(T-T )kJ/mol
2 1 1 2 【版权所有:21教育】
解析:(1)从实验装置看,该实验中缺少环形玻璃搅拌棒,用于搅拌溶液,使之混合均匀;同时,装置中大小
烧杯之间存在间隙,易导致热量散失,应将小烧杯上沿紧贴硬纸板,同时使用碎泡沫塑料填充满大烧杯。
( 2)若量取NaOH溶液时仰视读数,则所量取NaOH溶液的体积偏大,反应过程中放出的热量增大,求得中
和热ΔH偏小;
若用氨水代替NaOH,由于NH ·H O是弱碱,其电离过程需要吸热,导致反应过程中放出的热量减小,求得
3 2
中和热ΔH偏大;
( 3)反应生成0.025molHO时放出的热量为:c×(50+25)×1×(T -T )=75c(T-T )kJ,因此生成1molH O时的反
2 2 1 2 1 2
应热ΔH= 。
21*cnjy*com
分析:此题是对中和热测定实验的考查,解答此题时,应结合中和热的定义和实验测定过程进行分析。
9. (1)S(s)+O (g)=SO(g)△H=﹣299.52 kJ•mol﹣1
2 2
(2)C H (g)+13/2O (g)=4CO (g)+5HO(l) △H=﹣2900 kJ•mol﹣1
4 10 2 2 2
(3)C(s)+H O(g)=CO(g)+H (g)△H=+131.5kJ•mol-1
2 2
(4)3NO (g)+H O(l)=2HNO (aq)+NO(g)△H=-138kJ•mol-1
2 2 3
解析:(1)质量换算物质的量结合反应热计算得到生成1mol二氧化硫气体的焓变,1g 硫粉在氧气中充分燃
烧放出 9.36kJ热量,生成1molSO 的反应放出的热量=9.36kJ×32=299.52 kJ;依据热化学方程式书写方法,
2
标注物质聚集状态,和对应量的反应热,热化学方程式为:S(s)+O(g)=SO(g)△H=﹣299.52 kJ•mol﹣1;
2 2
( 2)质量换算物质的量结合反应热计算得到1mol丁烷完全燃烧的焓变,当10g丁烷完全燃烧生成CO 和液
2态水时,放热500kJ,则1mol丁烷(58g)完全燃烧时放热2900 kJ,由此可写出热化学方程式:C H (g)
4 10
+13/2O (g)=4CO (g)+5HO(l) △H=﹣2900 kJ•mol﹣1;
2 2 2
( 3)1molC与1mol水蒸气反应生成1mol CO和1mol H , 吸收131.5kJ的热量,则热化学方程式为:C(s)
2
+H O(g)=CO(g)+H (g)△H=+131.5kJ•mol-1;
2 2
( 4)3molNO 气体溶于水生成HNO 和NO气体,放出138kJ热量,其热化学方程式为:3NO(g)+H O(l)
2 3 2 2
=2HNO (aq)+NO(g)△H=-138kJ•mol-1。
3
分析:(1)根据1g硫充分燃烧放出的热量计算1mol硫完全燃烧放出的热量,然后书写热化学方程式;
(2)计算1mol丁烷完全燃烧放出的热量,然后书写热化学方程式;
(3)注意碳的状态,该反应是吸热反应;
(4)注意硝酸的状态时溶液。
10. (1)①②③④
(2)393.5 kJ/mol
(3)1425 kJ
(4)CO(g)+ O(g)=CO(g) ΔH =-283.1kJ/mol
2 2
(5)b
解析:(1)放热反应的ΔH<0,故①②③④都是放热反应;
( 2)1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量为燃烧热,则反应④中C完全燃烧,C的燃烧
热为393.5 kJ/mol;
(3)燃烧10g H 即5mol H 生成液态水,放出的热量为285kJ 5=1425 kJ;
2 2
( 4)由③C(s)+ O(g)=CO(g) ΔH =-110.4 kJ/mol,④C(s)+ O (g)=CO(g) ΔH =-393.5 kJ/mol,④-③可得
2 2 2
CO燃烧的热化学方程式为CO(g)+ O(g)=CO(g) ΔH =-283.1kJ/mol;
2 2
( 5)由物质的三态变化可知,在大气条件下,二氧化碳是无色无味的气体,而在温度低于31.2℃时,加压可
使CO 变为液态,即加压降温可减小分子之间的间隔,使二氧化碳由气体变为液体,则可将CO 液化后送入
2 2
深海海底,以减小大气中CO 的浓度,
2
故答案为:b。
分析:(1)燃烧反应是放热反应;
(2)根据燃烧热的定义进行判断;
(3)根据氢气燃烧生成液态水计算放出的热量;(4)根据燃烧热的定义书写热化学方程式;
(5)增压、降温可以液化二氧化碳。