文档内容
第三单元 金属材料
第一节 铁及其化合物(二)
一、基础巩固
1.某固体混合物X,可能含有BaCl 、NaHCO 、Fe O 、Cu、NaAlO 中的一种或几种,进行如下实验:
2 3 2 3 2
①取一定量样品溶于水中,得到固体A和溶液B;②向A中加入足量稀盐酸,得到澄清溶液C。下列说法
不正确的是( )
A.固体A可能溶于NaOH溶液
B.溶液C能与NaHCO 溶液反应产生沉淀
3
C.向溶液C中加入KSCN溶液,若不变色,则混合物X不含Fe O
2 3
D.向溶液B中加入NaOH溶液,若出现白色沉淀,则X中必定有BaCl 和NaHCO
2 3
2.不能和铁反应的溶液是( )
A.H S B.NaOH C.Fe (SO ) D.Cl
2 2 4 3 2
3.亚硝酸亚铁Fe(NO ) 易分解,若分解产物之一是红色粉末Fe O ,则另一分解产物可能是( )
2 2 2 3
A.NO B.N O C.NO D.N O
2 3 2 2 5
4.用KI溶液和FeCl 溶液进行如下实验。下列说法中错误的是( )
3
A.实验i发生的反应为:2Fe3++2I﹣ 2Fe2++I
2
B.黄色溶液中含有Fe2+、Fe3+、Cl﹣⇌、K+、I﹣离子
C.实验iii水溶液中c(Fe2+)小于i中c(Fe2+)
D.若向实验iii 所得液体中滴加KSCN溶液,水层红色比实验ii浅
5.可用于检验久置的FeSO 溶液是否变质的试剂( )
4
A.过氧化钠 B.铁粉 C.盐酸 D.KSCN溶液
6.某同学采用硫铁矿焙烧后的烧渣(主要成分为 Fe O 、SiO 、Al O )制取七水合硫酸亚铁
2 3 2 2 3
(FeSO •7H O),设计了如图流程:
4 2
下列说法不正确的是( )
A.溶液1中的阳离子可与NH +、I﹣、SO 2﹣在同一溶液中大量共存
4 4
B.固体1为SiO ,试剂X为Fe
2C.向固体2中加入足量NaOH溶液,发生反应的离子方程式:Al(OH) +OH﹣═AlO ﹣+2H O
3 2 2
D.从溶液2得到FeSO •7H O产品的过程中,须控制条件防止其氧化和分解
4 2
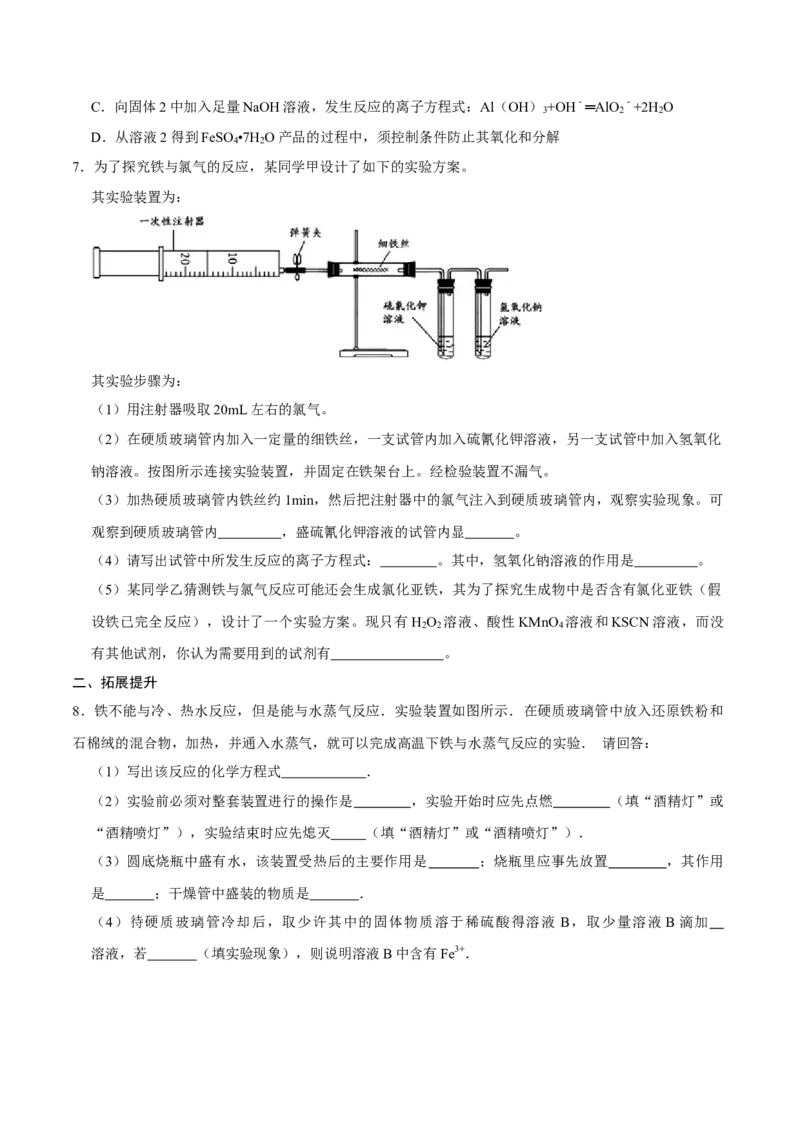
7.为了探究铁与氯气的反应,某同学甲设计了如下的实验方案。
其实验装置为:
其实验步骤为:
(1)用注射器吸取20mL左右的氯气。
(2)在硬质玻璃管内加入一定量的细铁丝,一支试管内加入硫氰化钾溶液,另一支试管中加入氢氧化
钠溶液。按图所示连接实验装置,并固定在铁架台上。经检验装置不漏气。
(3)加热硬质玻璃管内铁丝约1min,然后把注射器中的氯气注入到硬质玻璃管内,观察实验现象。可
观察到硬质玻璃管内 ,盛硫氰化钾溶液的试管内显 。
(4)请写出试管中所发生反应的离子方程式: 。其中,氢氧化钠溶液的作用是 。
(5)某同学乙猜测铁与氯气反应可能还会生成氯化亚铁,其为了探究生成物中是否含有氯化亚铁(假
设铁已完全反应),设计了一个实验方案。现只有H O 溶液、酸性KMnO 溶液和KSCN溶液,而没
2 2 4
有其他试剂,你认为需要用到的试剂有 。
二、拓展提升
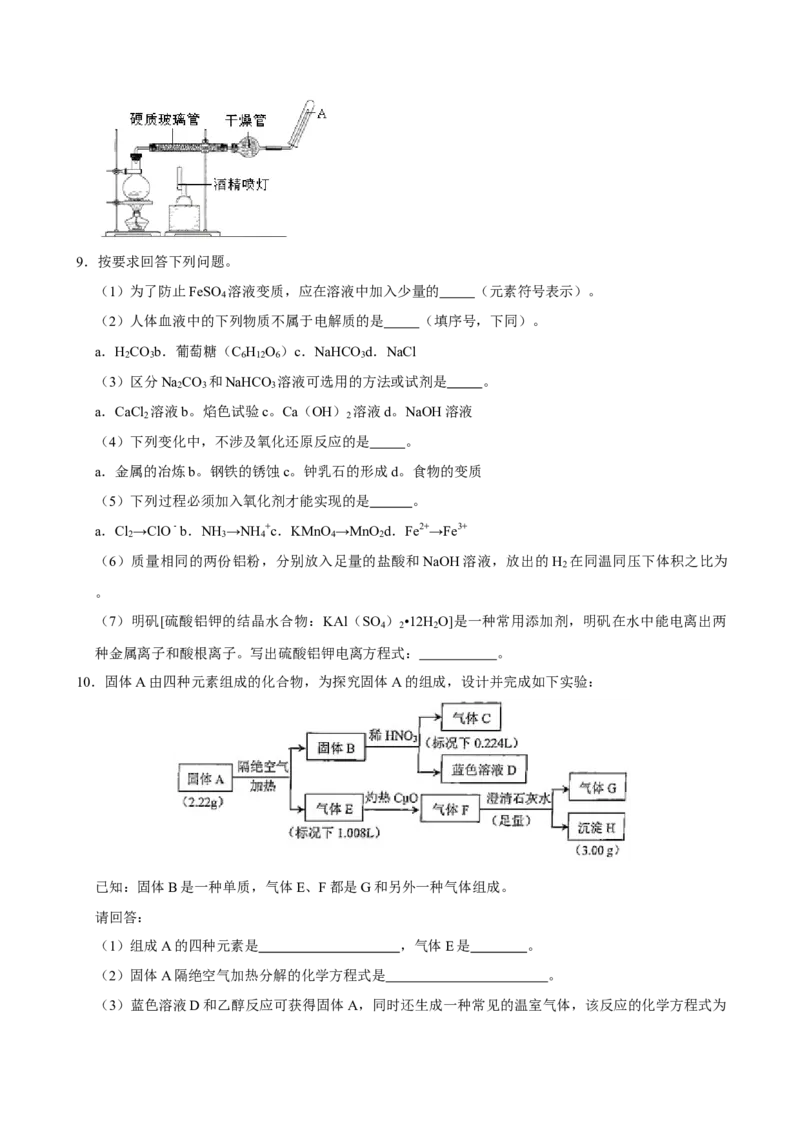
8.铁不能与冷、热水反应,但是能与水蒸气反应.实验装置如图所示.在硬质玻璃管中放入还原铁粉和
石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验. 请回答:
(1)写出该反应的化学方程式 .
(2)实验前必须对整套装置进行的操作是 ,实验开始时应先点燃 (填“酒精灯”或
“酒精喷灯”),实验结束时应先熄灭 (填“酒精灯”或“酒精喷灯”).
(3)圆底烧瓶中盛有水,该装置受热后的主要作用是 ;烧瓶里应事先放置 ,其作用
是 ;干燥管中盛装的物质是 .
(4)待硬质玻璃管冷却后,取少许其中的固体物质溶于稀硫酸得溶液 B,取少量溶液 B滴加
溶液,若 (填实验现象),则说明溶液B中含有Fe3+.9.按要求回答下列问题。
(1)为了防止FeSO 溶液变质,应在溶液中加入少量的 (元素符号表示)。
4
(2)人体血液中的下列物质不属于电解质的是 (填序号,下同)。
a.H CO b.葡萄糖(C H O )c.NaHCO d.NaCl
2 3 6 12 6 3
(3)区分Na CO 和NaHCO 溶液可选用的方法或试剂是 。
2 3 3
a.CaCl 溶液b。焰色试验c。Ca(OH) 溶液d。NaOH溶液
2 2
(4)下列变化中,不涉及氧化还原反应的是 。
a.金属的冶炼b。钢铁的锈蚀c。钟乳石的形成d。食物的变质
(5)下列过程必须加入氧化剂才能实现的是 。
a.Cl →ClO﹣b.NH →NH +c.KMnO →MnO d.Fe2+→Fe3+
2 3 4 4 2
(6)质量相同的两份铝粉,分别放入足量的盐酸和NaOH溶液,放出的H 在同温同压下体积之比为
2
。
(7)明矾[硫酸铝钾的结晶水合物:KAl(SO ) •12H O]是一种常用添加剂,明矾在水中能电离出两
4 2 2
种金属离子和酸根离子。写出硫酸铝钾电离方程式: 。
10.固体A由四种元素组成的化合物,为探究固体A的组成,设计并完成如下实验:
已知:固体B是一种单质,气体E、F都是G和另外一种气体组成。
请回答:
(1)组成A的四种元素是 ,气体E是 。
(2)固体A隔绝空气加热分解的化学方程式是 。
(3)蓝色溶液D和乙醇反应可获得固体A,同时还生成一种常见的温室气体,该反应的化学方程式为。