文档内容
人教版(2019)必修第二册第七章第一节 认识有机化合物
课时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.短周期主族元素X、Y、Z、W、R、Q原子序数依次增大。常温下,由这些元素组
成的化合物甲、乙、丙、丁的0.1 mol·L-1水溶液pH如下表,丙、丁为二元化合物。甲
溶液逐滴滴入丙溶液中,先产生白色沉淀,后沉淀消失;乙由Y、Z、W三种元素组成,
其水溶液常用于除油污。下列说法一定正确的是
0.1 mol·L-1水溶液 甲 乙 丙 丁
pH 13 11 5 1
A.W和Q形成的化合物只含有离子键
B.Y和Z的氢化物沸点:Y<Z
C.离子半径:r(Q)>r(R)>r(Z)
D.Y和Q的氧化物对应水化物的酸性:Q>Y
2.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.16gO、O 的混合气体所含的氧原子数目为2N
2 3 A
B.常温常压下,15g甲基(—CH)所含的电子数9N
3 A
C.标准状况下,2.24LSO 含有的氧原子数为0.3N
3 A
D.1molFe与1molCl 完全反应,转移的电子数为3N
2 A
3.下列说法不正确的是
A.12C和14C互为同位素 B.甲烷和丁烷互为同系物
C.正丁烷和异丁烷互为同分异构体 D.NaO和NaO 互为同素异形体
2 2 2
4.下列叙述正确的是
A.分子组成上相差一个或若干个CH 原子团的物质,一定互为同系物
2
B.CH=CH 和CH=CH—CH=CH 互为同系物
2 2 2 2
C. 和 互为同分异构体
D.同分异构体的化学性质可能相似
5.下列说法正确的是
A.O 和O 互为同位素 B.金刚石和石墨互为同素异形体
2 3C.CH 和HC≡CH互为同系物 D.乙醛和乙醇互为同分异构体
4
6.有关有机化合物中碳原子的成键特点,下列说法错误的是
A.碳原子最外层有4个电子,每个碳原子形成4个价键
B.碳原子间不仅能形成碳链,也能形成碳环
C.在CH 分子中,四个碳氢共价键的长度和强度均相同
4
D.在正丁烷分子中,4个碳原子形成的碳链为直线形
7.关于有机化合物中碳原子的成键特点,下列叙述不正确的是
A.碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键
B.碳原子性质活泼,可以跟多种元素原子形成共价键
C.碳原子之间既可以形成单键,又可以形成双键或三键
D.多个碳原子之间可以结合成碳链(可以带有支链),也可以结合成碳环,构成有机物
链状或环状的碳骨架
8.已知 是阿伏加德罗常数的值。下列说法不正确的是
A.标准状况下, 完全被过氧化钠固体吸收,转移的电子数目为
B.60g正戊烷和12g异戊烷的混合物中含有的共用电子对数目为
C.密闭容器中, 和 反应达到平衡状态时,容器内的分子数目为
D.标准状况下, 和 的混合气体中含有的H原子数目为
9.下列因素中不是有机化合物种类繁多的原因的是
A.一个碳原子可以形成四条共价键
B.碳可以与碳或其他原子形成单键、双键或三键
C.很多有机化合物存在同分异构现象
D.很多有机化合物可以燃烧
10.下列化学用语正确的是
A.中子数为19的硫离子: B.甲烷的球棍模型:
C.聚丙烯的结构简式: D.次氯酸钠的电子式:
11.下列说法正确的是
试卷第2页,共3页A.足球烯与金刚石互为同素异形体
B.氕、氘、氚互为同位素,中子数分别为1、2、3
C.乙二醇和丙三醇互为同系物
D.淀粉和纤维素互为同分异构体
12.下列说法正确的是
A.在光照下甲烷、乙烷和丙烷都能与氯水发生取代反应
B.等物质的量的甲烷和氯气发生取代反应的有机产物只有
C.正丁烷的沸点比异丁烷的沸点高
D. 和 互为同分异构体
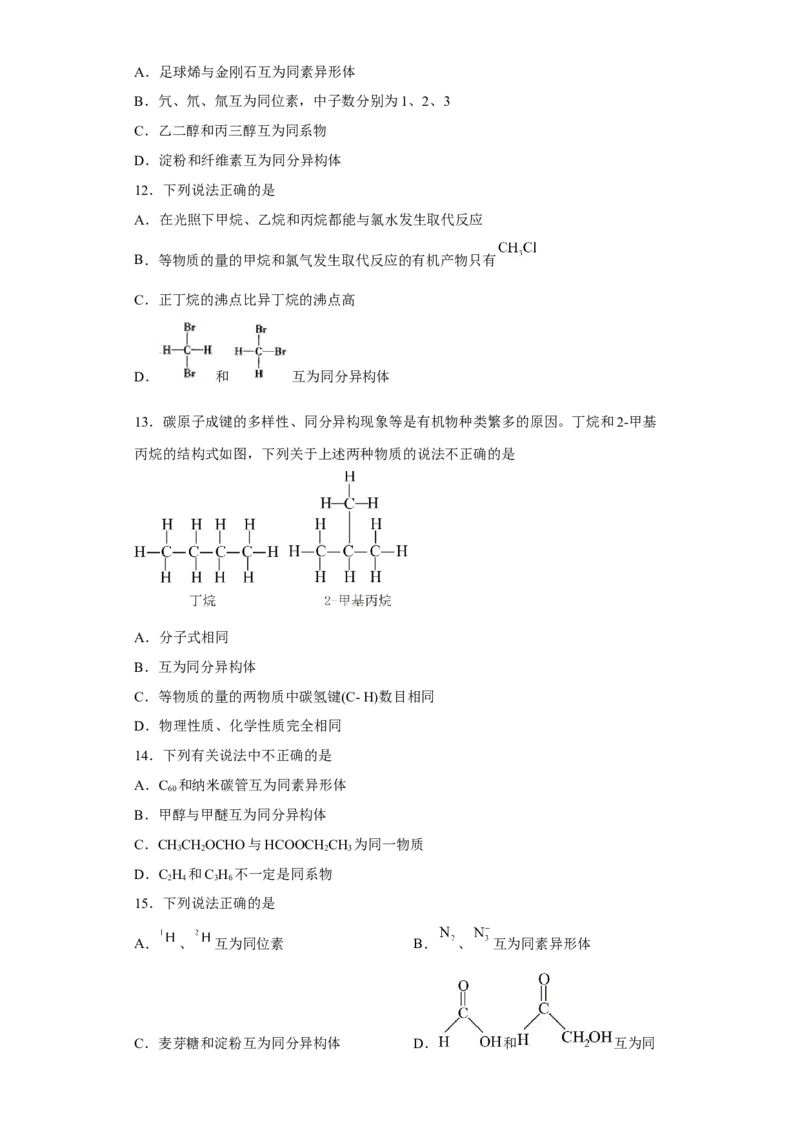
13.碳原子成键的多样性、同分异构现象等是有机物种类繁多的原因。丁烷和2-甲基
丙烷的结构式如图,下列关于上述两种物质的说法不正确的是
A.分子式相同
B.互为同分异构体
C.等物质的量的两物质中碳氢键(C- H)数目相同
D.物理性质、化学性质完全相同
14.下列有关说法中不正确的是
A.C 和纳米碳管互为同素异形体
60
B.甲醇与甲醚互为同分异构体
C.CHCHOCHO与HCOOCH CH 为同一物质
3 2 2 3
D.C H 和C H 不一定是同系物
2 4 3 6
15.下列说法正确的是
A. 、 互为同位素 B. 、 互为同素异形体
C.麦芽糖和淀粉互为同分异构体 D. 和 互为同系物
二、填空题
16.下列反应属于取代反应的是___________(填序号)。
①CH C+2H
4 2
②CuSO +Fe=FeSO +Cu
4 4
③CH Cl+Cl CHCl+HCl
3 2 2 2
④2NaBr+Cl=2NaCl+Br
2 2
⑤CHOH+HCl CHCl+HO
3 3 2
⑥CH CHBr+HO CHCHOH+HBr
3 2 2 3 2
⑦CH +2O CO+2HO
4 2 2 2
17.将下列物质进行分类(填序号):
①O 与O; ② C与 C;③HO 和DO;④冰与干冰 ;⑤H、D、T;⑥乙醇
2 3 2 2 2 2 2
与乙醚(CH-O-CH ) ;⑦CHCHCHCHCH 和CHCHCHCHCH
3 3 3 2 2 2 3 3 2 2 2 3
(1)互为同位素的是_______;
(2)互为同素异形体的是_______;
(3)互为同分异构体的是_______;
(4)属于同一化合物的是_______。
(5)下列各图均能表示甲烷的分子结构,按要求回答下列问题。
①甲烷的球棍模型是_______,甲烷的电子式是_______(填序号)。
②写出甲烷在氧气中燃烧的化学方程式:_______
③相对分子质量为 30 的烷烃的分子式是_______。
④甲烷与丙烷互为_________
A.同位素 B.同素异形体 C.同系物 D.同分异构体
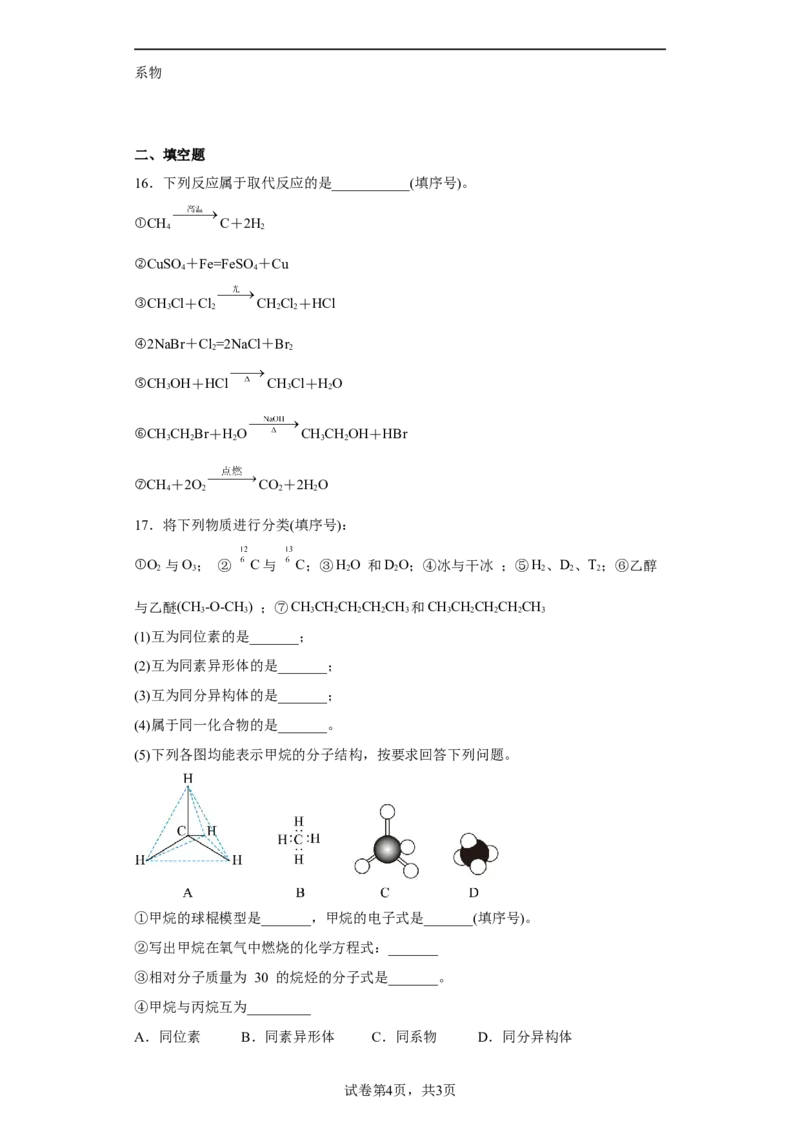
试卷第4页,共3页18.按照组成元素可将有机物分为烃和烃的衍生物。
I.某些烃分子的模型如图所示:
回答下列问题:
(1)乙的分子式为_______,用习惯命名法命名,戊的名称是_______。
(2)写出丁完全燃烧的化学方程式_______。
(3)甲与O 的反应可将化学能转化为电能,其工作原理如下图所示,图中甲从
2
_______(填A或B)通入,a极附近溶液pH将_______(填升高,降低或不变),b极的电
极反应式是_______
II.烃可以通过化学反应制得烃的衍生物,例如由丙烯可以制得丙烯酸
(CH CHCOOH)、乳酸 等。
2=
(4)乳酸中官能团的名称是_______。
(5)丙烯酸可以使酸性高锰酸钾溶液褪色,该反应类型为_______。
(6)3.6g乳酸与足量钠反应,能生成标准状况下H 的体积为_______L。
2
(7)如下图所示的物质含有_______个碳原子。19.甲烷的综合利用是各国科学家研究的重要课题。回答下列问题:
(1)天然气的主要成分是甲烷,甲烷的结构式为_______,甲烷的空间构型为_______。
(2)验证甲烷和氯气发生取代反应的条件,实验装置如图所示:
①装置A、B中的实验现象分别为_______、_______
②写出甲烷与氯气反应生成一氯甲烷的化学方程式:_______
③若将2mol 与一定量的 反应,得到等物质的量的4种取代物,则消耗 的物
质的量为_______。
20.下列各图均能表示甲烷的分子结构,按要求回答下列问题。
(1)甲烷的球棍模型是_______,甲烷的电子式是_______(填序号)。
(2)写出甲烷与氯气反应的化学方程式:_______(只写第一步),该反应的反应类型是
_______。
(3)甲烷与丙烷互为_______(填序号)。
a.同位素 b.同素异形体 c.同系物 d.同分异构体
(4)相对分子质量为72的烷烃的分子式是_______。
(5)甲烷的分子形状为_______。
三、实验题
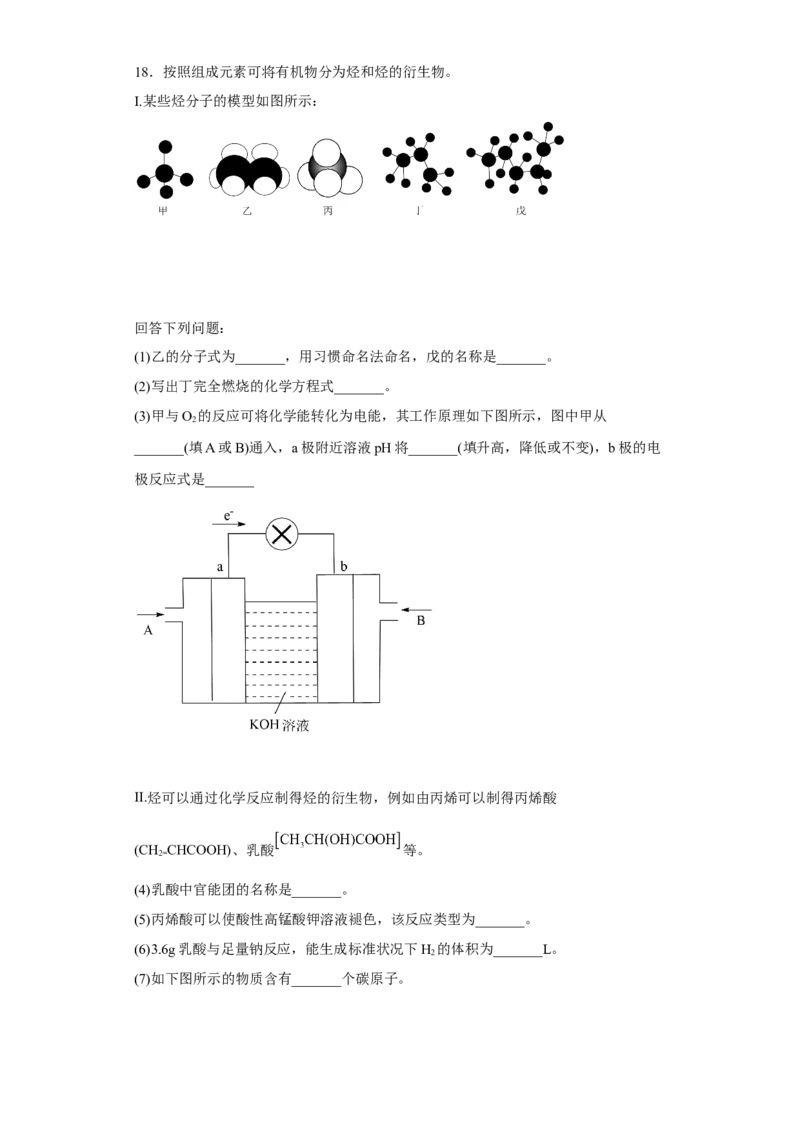
21.利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某
化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如图所示:
试卷第6页,共3页(1)A中制取Cl 的反应的化学方程式是____。
2
(2)B装置的作用:①____;②____;③____。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是____。
(4)E装置的作用是____(填序号)。
A.收集气体 B.吸收氯气 C.吸收氯化氢
(5)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是____。
(6)将1molCH 与Cl 发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的
4 2
氯气的物质的量是____。
(7)E中发生反应的化学方程式是____。
(8)C中发生反应的化学方程式是____。
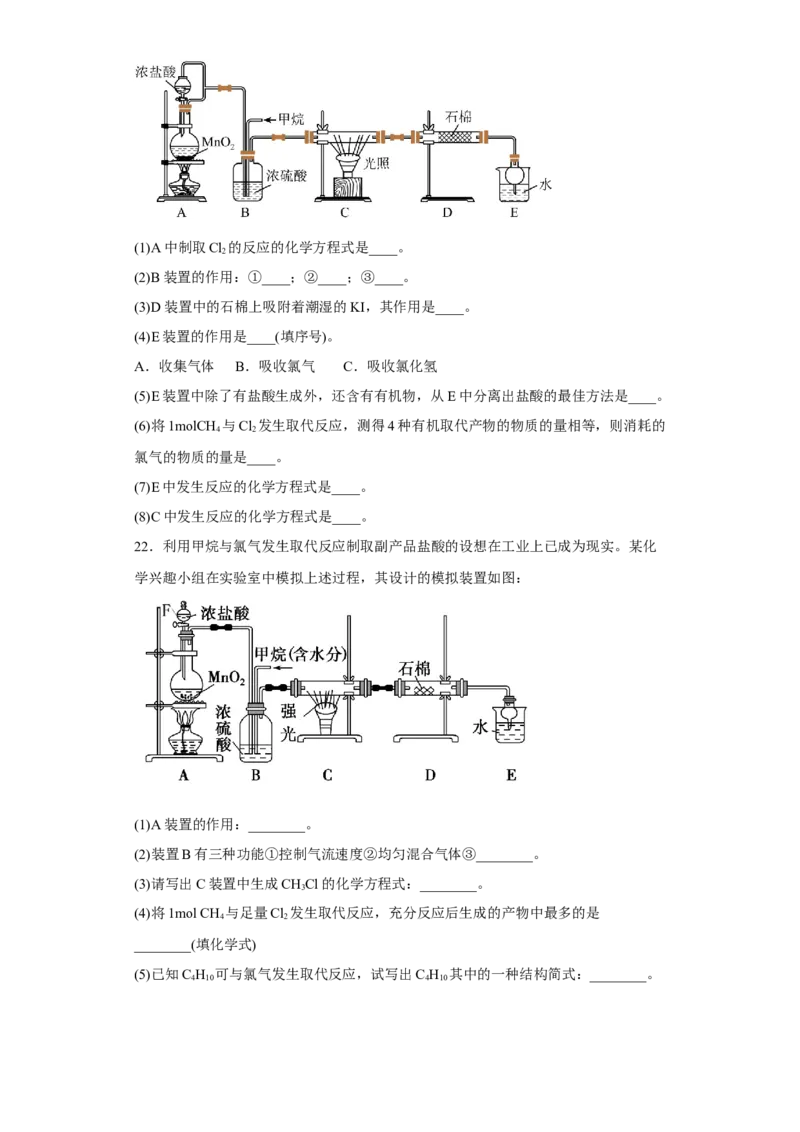
22.利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化
学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:
(1)A装置的作用:________。
(2)装置B有三种功能①控制气流速度②均匀混合气体③________。
(3)请写出C装置中生成CHCl的化学方程式:________。
3
(4)将1mol CH 与足量Cl 发生取代反应,充分反应后生成的产物中最多的是
4 2
________(填化学式)
(5)已知C H 可与氯气发生取代反应,试写出C H 其中的一种结构简式:________。
4 10 4 10参考答案:
1.A
【分析】常温下,0.1 mol·L-1甲溶液pH为13,说明甲为一元强碱,则甲为NaOH;0.1
mol·L-1丁溶液pH为1,且丁为二元化合物,说明丁为一元强酸,则丁为HCl;乙、丙的
0.1 mol·L-1水溶液pH分别为11、5,则乙为弱碱性溶液,丙为弱酸性溶液;甲溶液逐滴滴
入丙溶液中,先产生白色沉淀,后沉淀消失,则丙溶液中含有铝离子,且丙为二元化合物,
则丙为AlCl ;乙由Y、Z、W三种元素组成,其水溶液常用于除油污,可能为NaCO 溶液。
3 2 3
根据上述分析,甲为NaOH,丁为HCl,丙为AlCl ,乙为NaCO 溶液,6种元素,则X为
3 2 3
H,Y为C,Z为O,W为Na,R为Al,Q为Cl。
【详解】A.W和Q形成的化合物为氯化钠,只含有离子键,A正确;
B.Y为C,Z为O,C的氢化物有很多种,其氢化物沸点可能高于水也可能低于水,B错
误;
C.离子的电子层数越多,离子半径越大,电子层结构相同的离子,核电荷数越大,离子
半径越小,因此离子半径:r(Q)>r(Z)>r(R),C错误;
D.Y和Q的氧化物对应的水化物可能分别为碳酸和次氯酸,此时酸性:HCO>HClO,D
2 3
错误;
故选A。
2.B
【详解】A.氧气和臭氧的最简式都为O,16gO含有的氧原子个数为 ×1×N mol—
A
1=N ,故A错误;
A
B.甲基的电子数为9,常温常压下,15g甲基含有的电子数 ×9×N mol—1=9N ,故B
A A
正确;
C.标准状况下,三氧化硫为固态,无法计算2.24L三氧化硫含有的氧原子数,故C错误;
D.铁在氯气中燃烧生成氯化铁,1mol铁与1mol氯气完全反应时铁过量,转移的电子数为
1mol×2×N mol—1=2N ,故D错误;
A A
故选B。
3.D
【详解】A.12C和14C的质子数相同、中子数不同,互为同位素,A正确;
B.甲烷和丁烷的结构相似,分子组成相差3个CH 原子团,互为同系物,B正确;
2
C.正丁烷和异丁烷的分子式都为C H ,二者结构不同,互为同分异构体,C正确;
4 10D.NaO和NaO 是钠的不同氧化物,为化合物,二者不是同素异形体,同素异形体是指
2 2 2
由同一元素组成,而结构形态却不相同的单质,D错误;
故本题选D。
4.D
【详解】A.结构相似,分子组成上相差一个或若干个CH 原子团的有机物,互为同系物,
2
故A错误;
B.CH=CH 和CH=CH—CH=CH 所含碳碳双键的个数不同,不是互为同系物,故B错误;
2 2 2 2
C.分子式相同,结构不同的物质互为同分异构体, 和
的分子式不同,结构不同,不是互为同分异构体,故C错误;
D.互为同分异构体的两种有机物的物理性质有差别,化学性质可能相似,如正丙烷和异
烷;也可能不同,如乙酸与甲酸甲酯性质不同,故D正确;
故选:D。
5.B
【详解】A.同位素为质子数相同而中子数不同的同种元素的不同种核素;O 和O 均为单
2 3
质,故A错误;
B.同素异形体为同种元素所组成的不同单质,金刚石和石墨为C元素所组成的两种不同
单质,故B正确;
C.同系物为结构相似,分子组成相差一个或多个CH 原子团的有机化合物;CH 和
2 4
HC≡CH结构不相似,故不属于同系物,故C错误;
D.同分异构体为分子式相同而结构式不同的有机化合物,乙醛和乙醇的分子式分别为
CHCHO、CHCHOH,其分子式不相同,故D错误;
3 3 2
答案选B。
6.D
【详解】A.碳原子最外层有4个电子,每个碳原子形成4个价键,达到8电子稳定结构,
故A正确;
B.碳原子间不仅能形成碳链,也能形成碳环,如各种烷烃和苯,故B正确;
C.在CH 分子中,四个碳氢共价键的长度和强度均相同,构成正四面体结构,故C正确;
4
答案第2页,共2页D.在正丁烷分子中,4个碳原子形成的碳链为锯齿状,故D错误;
故选:D。
7.B
【详解】A.碳原子最外层有4个电子,碳原子与碳原子、其他原子(如氢原子)形成4个共
价键达到稳定结构,故A正确;
B.常温下碳原子性质不活泼,故B错误;
C.碳原子之间成键方式具有多样性,碳原子与碳原子之间不仅可以形成共价单键,还可
以形成双键、三键,故C正确;
D.碳原子最外层有四个电子,碳原子之间可以形成稳定的单键,又可以形成稳定的双键
和三键,不仅可以形成碳链,还可以形成碳环,且多个碳原子可以形成长度不同的链、支
链及环,且链、环之间又可以相互结合,故D正确;
答案选B。
8.A
【详解】A. 的物质的量为 ,根据反应 中氧元素
的化合价变化可知, 反应生成 ,转移的电子数目为 ,A项错误;
B.正戊烷和异戊烷是同分异构体,分子式均为 ,摩尔质量均为 ,故60g
正戊烷和12g异戊烷的混合物的总物质的量为 ,虽然正戊烷和异戊烷中碳原子的连接
方式不同,但二者含有的共用电子对数是相同的, 中含有 共用电子对,数
目为 ,B项正确;
C. ,反应前后气体分子数目不变,故 和 反应达
到平衡状态时,容器内的分子总数为 ,C项正确;
D.标准状况下, 和 的混合气体的物质的量为 ,H原子的物质的量
为 ,H原子数目为 ,D项正确;故选A。
9.D
【详解】A.碳原子最外层有4个电子,能与碳原子或其他原子形成4个共价键,是有机物
种类繁多的原因之一,A不符合题意;
B.碳原子之间也能相互成键,可以是双键,可以是单键,可以是三键,是有机物种类繁
多的原因之一,B不符合题意;
C.碳原子的成键方式的多样性使得有机化合物普遍存在着同分异构现象,常见的同分异
构,有碳链异构、官能团位置异构和官能团类型异构等,C不符合题意;
D.有机物燃烧不是有机物的种类繁多的原因,D符合题意;
故选D。
10.B
【详解】A.S是16号元素,S原子核外有16个电子,原子核内有16个质子。S2-是S原子
获得2个电子形成的,中子数为19的硫离子质量数为16+19=35,可表示为 ,A错误;
B.原子半径:C>H,CH 为正四面体结构,故甲烷的球棍模型为 ,B正确;
4
C.聚丙烯是丙烯CH=CH-CH 通过加聚反应产生的,其结构简式为 ,C错误;
2 3
D.次氯酸钠NaClO是离子化合物,Na+与ClO-之间以离子键结合,在阴离子ClO-中Cl原
子与O原子之间以共价单键结合,故NaClO的电子式为: ,D错误;
故合理选项是B。
11.A
【详解】A.足球烯与金刚石是两种同碳单质,互为同素异形体,A正确;
B. 、 、 中子数分别为0,1,2,B错误;
C乙二醇中含有2个 和丙三醇3个 含有的官能团数目不同,不能互为同系物,C
错误;
答案第4页,共2页D.淀粉和纤维素分子式为: ,因为n不同,不能互为同分异构体,D错误;
故选A。
12.C
【详解】A.在光照下甲烷、乙烷和丙烷都能与氯气发生取代反应,不能与氯水发生取代
反应,A项错误;
B.甲烷分子中的4个氢原子都可以被氯原子取代,等物质的量的甲烷和氯气发生取代反应
的有机产物有CHCl、CHCl、CHCl 、CCl ,B项错误;
3 2 2 3 4
C.正丁烷和异丁烷是互为同分异构体的烷烃,正丁烷的主链有4个碳原子,异丁烷的主链
只有3个碳原子,正丁烷的分子间作用力强于异丁烷,正丁烷的沸点比异丁烷的沸点高,C
项正确;
D.CHBr 为四面体构型, 和 为同一物质,D项错误;
2 2
答案选C。
13.D
【详解】A.分子式相同,均是C H ,A正确;
4 10
B.二者分子式相同,结构不同,互为同分异构体,B正确;
C.每个分子中碳氢键(C-H)数目相同,均含有10个,C正确;
D.二者互为同分异构体,物理性质不同,均是烷烃,化学性质相似,D错误;
故选D。
14.B
【详解】A.C 和纳米碳管为碳元素的不同单质互为同素异形体,故A正确;
60
B.分子式相同而结构不同的化合物互为同分异构体,而甲醇的分子式为CHO,甲醚的分
4
子式为C HO,故两者分子式不同,不是同分异构体,故B错误;
2 6
C.CHCHOCHO与HCOOCH CH 都表示甲酸乙酯,是一种物质,故C正确;
3 2 2 3
D.C H 属于烯烃,C H 可以是烯烃可以是环烷烃,C H 和C H 不一定是同系物,故D正
2 4 3 6 2 4 3 6
确;
故选:B。
15.A
【详解】A.质子数相同而中子数不同的核素互为同位素, 和 的质子数都是1,中子数分别为0和1,二者互为同位素,A正确;
B.同素异形体是由同种元素形成的不同单质, 是离子,B错误;
C.同分异构体是分子式相同、结构不同的化合物,麦芽糖的分子式为 ,淀粉的
分子式为 ,分子式不相同,C错误;
D.同系物是指结构相似、分子组成相差一个或若干个 原子团的化合物,HCOOH的官
能团是羧基(—COOH), 的官能团是醛基( )和羟基(—OH),结构不
相似,D错误;
故选A。
16.③⑤⑥
【解析】略
17.(1)②
(2)①
(3)⑥
(4)③⑦
(5) C B C H C
2 6
【解析】(1)
①O 与O 都是由氧元素组成的不同单质,互为同素异形体;
2 3
②12C与13C的质子数相同、中子数不同,都是碳元素的不同核素,互为同位素;
6 6
③HO和DO为相同的分子,相同的化学性质,是同一物质且是化合物;
2 2
④冰与干冰分子式不同,冰的分子式HO,干冰分子式CO,是不同物质;
2 2
⑤H、D 和T 都是氢气分子,属于同一种物质;
2 2 2
⑥乙醇与乙醚(CH-O-CH ),分子式都是C HOH,乙醇的结构简式是CHCHOH,互为同
3 3 2 5 3 2
分异构体;
⑦CH CHCHCHCH 和CHCHCHCHCH,名称都是正戊烷,分子式都是C H ,是同一
3 2 2 2 3 3 2 2 2 3 4 10
答案第6页,共2页种物质且是化合物;同位素:质子数相同,中子数不同的同一元素的不同核素;故答案为:
②;①;⑥;③⑦;
(2)
同素异形体:由相同元素组成的形态不同的单质;O 与O 互为同素异形体,故答案为:①;
2 3
(3)
同分异构体:分子式相同,结构不同的化合物;乙醇与乙醚(CH-O-CH ),分子式都是
3 3
C HOH,乙醇的结构简式是CHCHOH,互为同分异构体,故答案为:⑥
2 5 3 2
(4)
同一化合物:分子式相同,结构也相同,还要是化合物;③HO和DO、
2 2
⑦CHCHCHCHCH 和CHCHCHCHCH 都是同一物质,故答案为:③⑦;
3 2 2 2 3 3 2 2 2 3
(5)
①A为甲烷空间构型、B为甲烷电子式、C为甲烷球棍模型、D为甲烷比例模型,则甲烷的
球棍模型是C、甲烷的电子式是B,故答案为:C;B;
②甲烷气体在氧气中燃烧生成二氧化碳和水,反应的化学方程式为:
;
③设该烷烃的分子式为C H ,其相对分子质量=14n+2=30,n=2,所以其分子式为C H;
n 2n+2 2 6
④结构相似,在分子组成上相差1个或n个-CH 原子团的有机物互为同系物,甲烷和丙烷
2
结构相似,在分子组成上相差2个-CH 原子团,互为同系物,故答案为:C。
2
18.(1) C H 正戊烷
2 6
(2)C H+5O 3CO+4H O
3 8 2 2 2
(3) A 降低
(4)羟基、羧基
(5)氧化反应
(6)0.896
(7)59
【分析】根据烃分子的模型图可知,甲为甲烷的球棍模型,乙为乙烷的比例模型,丙为甲
烷的比例模型,丁为丙烷的球棍模型,戊为正戊烷的球棍模型,据此分析解答;丙烯酸
(CH=CHCOOH)中含有碳碳双键和羧基,乳酸[CHCH(OH)COOH]中含有羟基和羧基,结
2 3合官能团的性质分析解答。
(1)由分析可知,乙为乙烷,其分子式为:C H;戊为正戊烷,其习惯命名法的名称为:
2 6
正戊烷;
(2)由分析可知丁为丙烷,分子式为C H 完全燃烧的化学方程式为:C H+5O
3 8 3 8 2
3CO+4H O;
2 2
(3)由图可知,电子从电极a流出,为负极,物质甲为甲烷,发生氧化反应,参与负极反
应,应该从A通入,电极反应为: ,反应消耗氢氧根离子,a
极附近pH降低,b极通入的是氧气,发生还原反应,电极方程式为: ;
(4)乳酸的结构简式为 ,则其官能团的名称是:羟基、羧基;
(5)丙烯酸中的碳碳双键可以被酸性高锰酸钾氧化,而使其褪色,反应类型为氧化反应;
(6)3.6g乳酸的物质的量为 =0.04mol,羟基和羧基都能与与钠反应,则1mol乳酸
与足量钠反应放出1mol氢气,因此0.04mol乳酸与足量钠反应放出0.04mol氢气,标准状
况下H 的体积为0.04mol×22.4L/mol=0.896L,故答案为:0.896;
2
(7)根据该物质的结构简式可知,其中含有的碳原子为:9+5×10=59。
19.(1) 正四面体
(2) A试管内气体颜色逐渐变浅,试管壁上有油状液产生,液面上有少量白雾出
现 B试管中没有明显现象 CH+Cl CHCl+HCl 5mol
4 2 3
【解析】(1)
甲烷的结构式为 ;甲烷的空间构型为正四面体。
(2)
答案第8页,共2页①装置A 内CH 与Cl 在漫射日光作用下发生取代反应,生成CHCl、CHCl、CHCl 、
4 2 3 2 2 3
CCl 等难溶于水的物质,A试管内气体颜色逐渐变浅,试管壁上有油状液产生,液面上有
4
少量白雾出现;B中试管被黑色纸套包裹,CH 与Cl 不会反应,B试管中没有明显现象;
4 2
②甲烷与氯气反应生成一氯甲烷的化学方程式:CH+Cl CHCl+HCl;
4 2 3
③若将2mol 与一定量的 反应,得到等物质的量的4种取代物,则CHCl、CHCl、
3 2 2
CHCl 、CCl 分别为0.5mol,根据CHCl~Cl 、CHCl~2Cl 、CHCl ~3Cl 、CCl ~4Cl 则消耗
3 4 3 2 2 2 2 3 2 4 2
的物质的量为0.5+0.5×2+0.5×3+0.5×4=5mol。
20.(1) C B
(2) CH+Cl CHCl+HCl 取代反应
4 2 3
(3)c
(4)C H
5 12
(5)正四面体
【解析】(1)
A为甲烷的结构式,B为甲烷的电子式,C为甲烷球棍模型,D为甲烷空间填充模型,故答
案为C;B;
(2)
甲烷和氯气发生取代反应,其第一步反应方程式为CH+Cl CHCl+HCl;故答案为
4 2 3
CH+Cl CHCl+HCl;取代反应;
4 2 3
(3)
A.同位素研究范围是原子,甲烷和丙烷为化合物,甲烷和丙烷不属于同位素研究范围,
故A不符合题意;
B.同素异形体研究范围是单质,甲烷和丙烷为化合物,甲烷和丙烷不属于同素异形体研
究范围,故B不符合题意;
C.同系物研究的范围是化合物,甲烷结构简式为CH,丙烷的结构简式为CHCHCH,
4 3 2 3
它们结构相似,组成相差2个“CH”,它们互为同系物,故C符合题意;
2D.甲烷分子式为CH,丙烷的分子式为C H,分子式不同,它们不互为同分异构体,故
4 3 8
D不符合题意;
故答案为C;
(4)
烷烃的通式为C H ,相对分子质量为72,则n=5,该烷烃分子式为C H ;故答案为
n 2n+2 5 12
C H ;
5 12
(5)
甲烷空间构型为正四面体形;故答案为正四面体。
21.(1)MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
(2) 控制流速 均匀混合 干燥气体
(3)湿润的KI可除去过量的Cl
2
(4)C
(5)分液
(6)2.5mol
(7)Cl +H O HCl+HClO
2 2
(8)CH +Cl CHCl+HCl
4 2 3
【分析】A中MnO 和浓盐酸加热制备氯气,B中浓硫酸干燥氯气、使甲烷和氯气均匀混合、
2
控制气体流速,C中甲烷和氯气在光照条件下发生取代反应生成氯代甲烷和氯化氢,D中
氯气和KI反应除去过量的氯气,E装置用水吸收氯化氢制备盐酸。
【详解】(1)A中MnO 和浓盐酸加热生成氯气、氯化锰、水,反应的化学方程式是
2
MnO +4HCl(浓) MnCl +Cl↑+2H O;
2 2 2 2
(2)B装置中盛有浓硫酸,B的作用:①根据气泡可知气体流速;②使甲烷和氯气均匀混
合;③浓硫酸能干燥氯气和甲烷;
(3)D装置中的石棉上吸附着潮湿的KI,发生反应2KI+Cl =KCl+I ,其作用是除去过量
2 2
的Cl;
2
答案第10页,共2页(4)氯化氢易溶于水得到盐酸,E装置的作用是吸收氯化氢,选C;
(5)E装置中除了有盐酸生成外,还含有氯代甲烷等有机物,有机物难溶于水,从E中分
离出盐酸的最佳方法是分液;
(6)将1molCH 与Cl 发生取代反应,测得4种有机取代产物的物质的量相等,则生成
4 2
CHCl、CHCl、CHCl 、CCl 的物质的量各为0.25mol,则消耗的氯气的物质的量是
3 2 2 3 4
。
(7)E中氯气和水反应生成盐酸和次氯酸,发生反应的化学方程式是Cl+H O
2 2
HCl+HClO;
(8)C中甲烷和氯气发生取代反应生成氯代甲烷和氯化氢,发生反应的化学方程式是
CH+Cl CHCl+HCl、CHCl+Cl CHCl+HCl、CHCl+Cl
4 2 3 3 2 2 2 2 2 2
CHCl +HCl、CHCl +Cl CCl +HCl。
3 3 2 4
22.(1)制备Cl
2
(2)干燥混合气体
(3)CH +Cl CHCl+HCl
4 2 3
(4)HCl
(5)CH CHCHCH 或CHCHCH(CH )
3 2 2 3 3 2 3 2
【分析】由实验装置图可知,装置A中二氧化锰与浓盐酸共热反应制备氯气,装置B中盛
有浓硫酸用于控制气流速度、均匀混合气体、干燥混合气体,装置C中氯气和甲烷在光照
条件发生取代反应生成氯代甲烷和氯化氢,装置D中的石棉网上可均匀附着碘化钾粉末除
去未反应的氯气,装置E中盛有水吸收反应生成的氯化氢气体。
(1)
由分析可知,装置A中二氧化锰与浓盐酸共热反应制备氯气,故答案为:制备Cl;
2
(2)
装置B盛有浓硫酸,具有吸水性,所以装置B的第③个作用为干燥混合气体,故答案为:
干燥混合气体;
(3)CH 与Cl 在光照条件下反应生成CHCl和HCl,反应的化学方程式为:CH+Cl
4 2 3 4 2
CHCl+HCl,故答案为:CH+Cl CHCl+HCl;
3 4 2 3
(4)
光照条件下,1mol CH 与足量Cl 发生取代反应生成氯代甲烷和氯化氢,充分反应后生成
4 2
的产物中最多的是氯化氢,化学式为HCl,故答案为:HCl;
(5)
C H 符合烷烃的通式,是可与氯气发生取代反应的丁烷,丁烷的同分异构体有2种,分别
4 10
为正丁烷和异丁烷,结构简式分别为CHCHCHCH 或CHCHCH(CH ),故答案为:
3 2 2 3 3 2 3 2
CHCHCHCH 或CHCHCH(CH )。
3 2 2 3 3 2 3 2
答案第12页,共2页