文档内容
2025年12月高一化学月考试题
一、单选题(每题3分,共48分)
1.椰树牌天然矿泉水的成分:含钠46.31g/L、含钙35.11g/L、含碘0.051g/L,这里所标成
分钠、钙、碘指的是
A.元素 B.单质 C.原子 D.氧化物
2.下列离子方程式书写正确的是
A.用FeCl 溶液腐蚀印刷电路板上铜箔:2Fe3++Cu=2Fe2++Cu2+
3
B.Fe与稀盐酸反应:2Fe+6H+=2Fe3++3H ↑
2
C.氢氧化钡溶液与硫酸反应:Ba2++ +OH-+H+=H O+BaSO↓
2 4
D.向小苏打溶液中滴入醋酸: +2CH COOH=CO↑+H O+2CHCOO-
3 2 2 3
3.在元素周期表中,从左到右共有18个纵行。第1纵行(除氢以外)为碱金属元素,稀有气
体元素是第18纵行。下列说法正确的是( )
A.铝元素位于第3纵行
B.过渡元素在周期表中占10个纵行
C.第18纵行所有元素的最外层均有8个电子
D.第16纵行元素都是非金属元素
4.下列化学用语书写正确的是
A. 俗称:纯碱
B. 在熔融状态下的电离方程式:
C.Na与 溶液反应的离子方程式:
D.用双线桥表示电子转移方向:
5.节日焰火绚烂多彩,这与高中化学中“焰色试验”知识相关。下列说法中正确的是
A.焰色试验是化学变化
B.用稀盐酸清洗做焰色试验的铂丝
C.利用焰色试验可区分NaOH与NaCO 固体
2 3D.焰色试验均应透过蓝色钴玻璃观察
6.用N 表示阿伏加 德罗常数的值,下列叙述正确的是( )
A
A.1mol氩气在标准状况下的体积约为11.2L
B.20℃、101MPa状态下,32gO 和O 的混合气体所含原子数为2.5N
2 3 A
C.标准状况下,11.2LCCl 含有的原子数为3N
4 A
D.常温常压下,44gCO 含有的原子数为3N
2 A
7.下列关于钠及其化合物的叙述正确的是
A.金属钠保存在煤油里,说明金属钠的密度比煤油的小
B.金属钠与水反应时会熔化,说明钠的熔点低且反应放热
C.分别加热 和 固体,试管内壁均有水珠,说明两种物质均受热分解
D.钠燃烧或氯化钠固体于酒精灯火焰上加热时,透过蓝色钴玻璃均可观察到黄色火焰
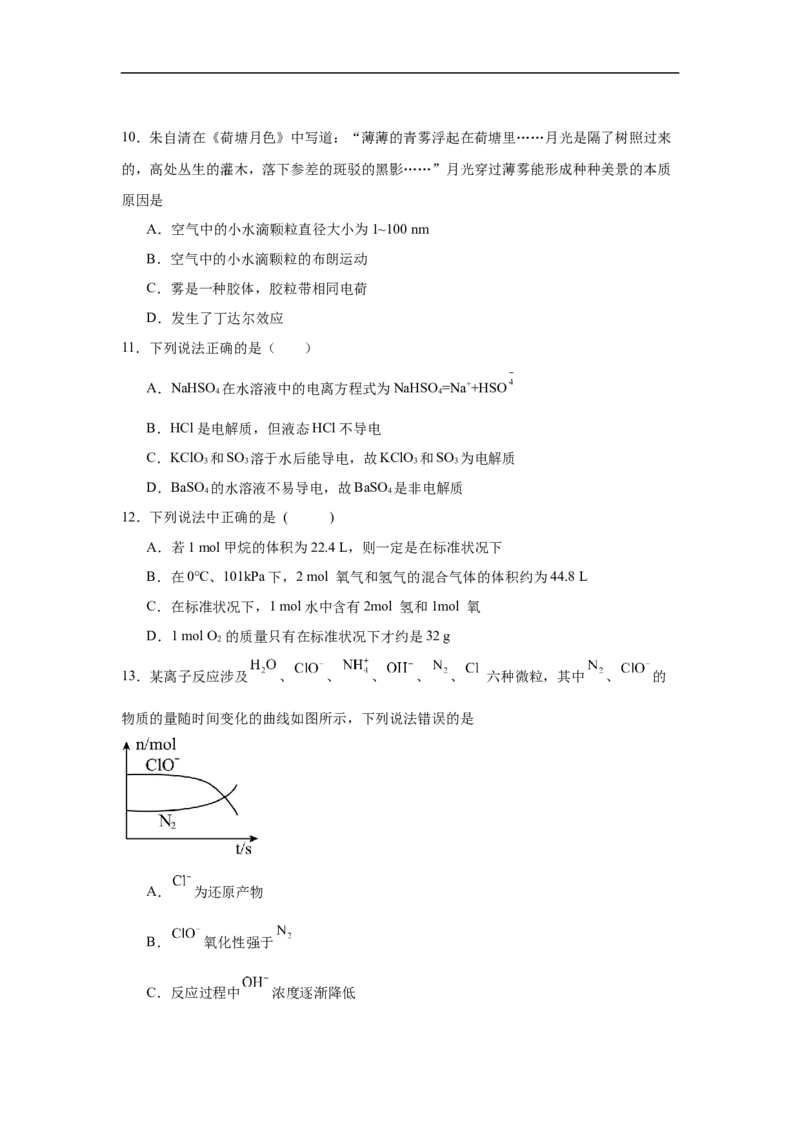
8.X、Y、Z、M、Q、R为短周期元素,其原子半径和最外层电子数之间的关系如图所示。
下列说法错误的是
A.R不能把Q从其盐溶液中置换出来
B.X、R、Q三种元素可以构成离子化合物
C.热稳定性:ZX<YX
3 4
D.XM的水溶液露置于空气中易变质
2
9.下列反应既属于离子反应,又属于氧化还原反应的是
A.CaO+HO= Ca(OH) B.2KClO 2KCl+3O ↑
2 2 2
C. D.
试卷第2页,共3页10.朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来
的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾能形成种种美景的本质
原因是
A.空气中的小水滴颗粒直径大小为1~100 nm
B.空气中的小水滴颗粒的布朗运动
C.雾是一种胶体,胶粒带相同电荷
D.发生了丁达尔效应
11.下列说法正确的是( )
A.NaHSO 在水溶液中的电离方程式为NaHSO=Na++HSO
4 4
B.HCl是电解质,但液态HCl不导电
C.KClO 和SO 溶于水后能导电,故KClO 和SO 为电解质
3 3 3 3
D.BaSO 的水溶液不易导电,故BaSO 是非电解质
4 4
12.下列说法中正确的是 ( )
A.若1 mol甲烷的体积为22.4 L,则一定是在标准状况下
B.在0℃、101kPa下,2 mol 氧气和氢气的混合气体的体积约为44.8 L
C.在标准状况下,1 mol水中含有2mol 氢和1mol 氧
D.1 mol O 的质量只有在标准状况下才约是32 g
2
13.某离子反应涉及 、 、 、 、 、 六种微粒,其中 、 的
物质的量随时间变化的曲线如图所示,下列说法错误的是
A. 为还原产物
B. 氧化性强于
C.反应过程中 浓度逐渐降低D.氧化剂与还原剂的物质的量之比为
14.配制250 mL 0.1 mol·L−1的盐酸时,下列实验操作使所配溶液浓度偏大的是( )
A.用量筒量取所需的浓盐酸时俯视刻度线
B.定容时仰视刻度线
C.定容后倒转容量瓶几次,发现凹液面最低点低于刻度线,再补几滴蒸馏水
D.用量筒量取所需浓盐酸倒入烧杯后,用水洗涤量筒2~3次,洗涤液倒入烧杯中
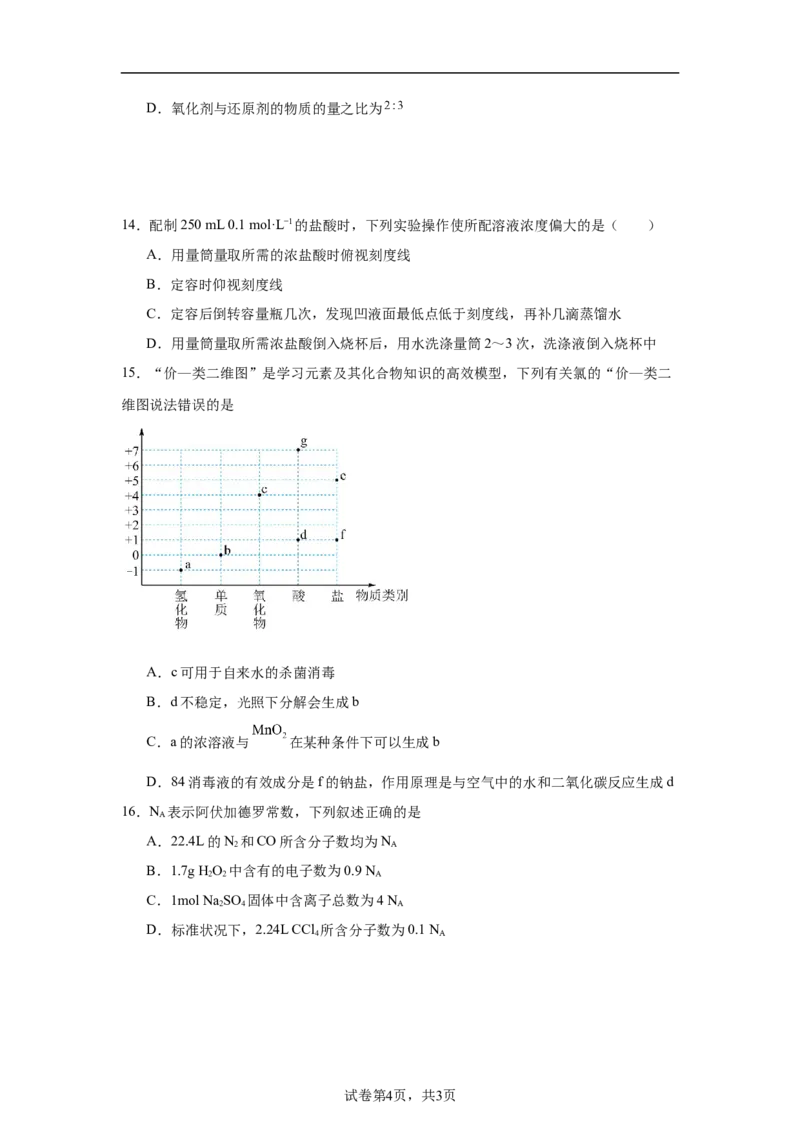
15.“价—类二维图”是学习元素及其化合物知识的高效模型,下列有关氯的“价—类二
维图说法错误的是
A.c可用于自来水的杀菌消毒
B.d不稳定,光照下分解会生成b
C.a的浓溶液与 在某种条件下可以生成b
D.84消毒液的有效成分是f的钠盐,作用原理是与空气中的水和二氧化碳反应生成d
16.N 表示阿伏加德罗常数,下列叙述正确的是
A
A.22.4L的N 和CO所含分子数均为N
2 A
B.1.7g HO 中含有的电子数为0.9 N
2 2 A
C.1mol Na SO 固体中含离子总数为4 N
2 4 A
D.标准状况下,2.24L CCl 所含分子数为0.1 N
4 A
试卷第4页,共3页二、填空题(共24分)
17.(本题12分)回答下列问题:
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,
爆炸时的反应为: ;在该反应中还原剂是(填化学式,下
同): ;还原产物是: 和 ;发生氧化反应是: 。
(2)配平如下反应方程式:
① 。
② 。
(3)在硫酸溶液中, 和 能按粒子个数比1:2完全反应,生成一种棕黄色气体
X,同时 被氧化为 ,则X为_______。(填选项序号)
A. B. C. D.
(4)在 的反应中,则生成1分子NO转移电子数为
;56 g Fe参加反应时,被还原的 为 g。
18.(本题12分)按要求填空
(1)向CuCl 溶液中滴加NaOH溶液,现象: ,离子方程式:
2
(2)向NaHCO 溶液中滴加稀硫酸,现象: ,离子方程式: ;
3
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂 ,离子方程式: 。
(4)FeSO (CuSO ):除杂,括号内为杂质,所加试剂 ,离子方程式 。
4 4
(5)NaHSO 和Ba(OH) 两溶液混合,反应后溶液成中性时的离子方程式为: 。
4 2三、解答题(共28分)
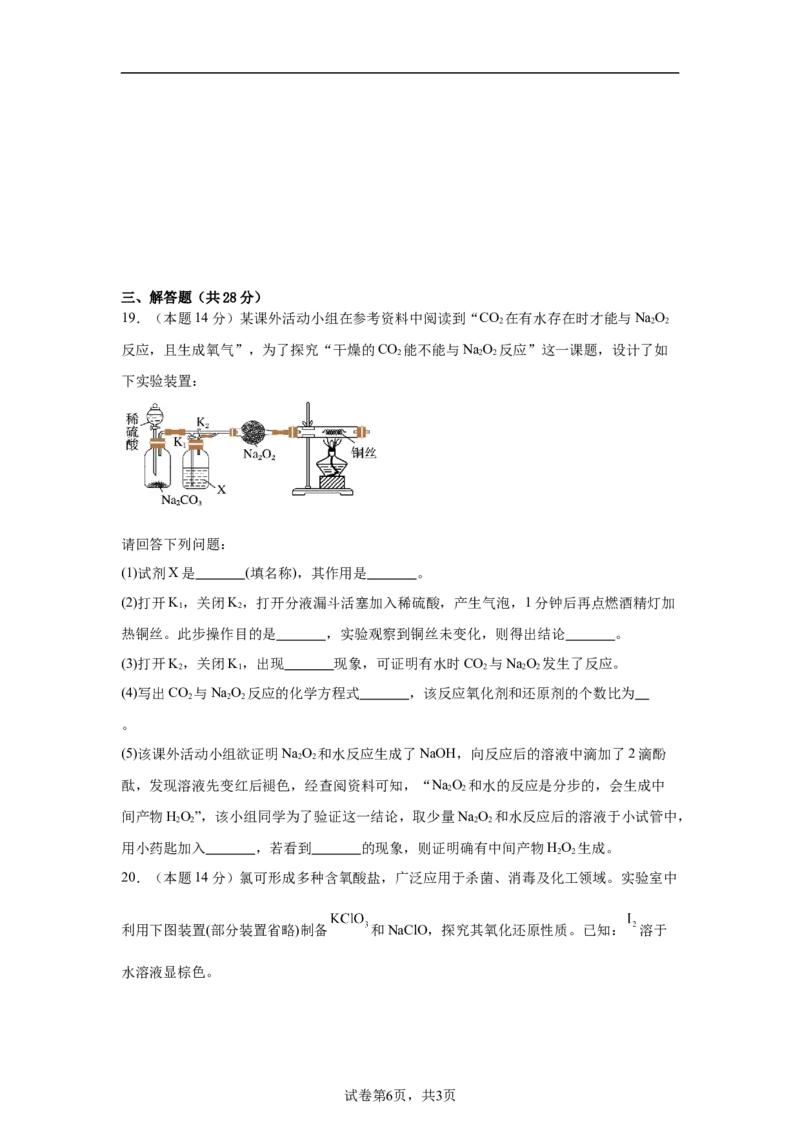
19.(本题14分)某课外活动小组在参考资料中阅读到“CO 在有水存在时才能与NaO
2 2 2
反应,且生成氧气”,为了探究“干燥的CO 能不能与NaO 反应”这一课题,设计了如
2 2 2
下实验装置:
请回答下列问题:
(1)试剂X是 (填名称),其作用是 。
(2)打开K,关闭K,打开分液漏斗活塞加入稀硫酸,产生气泡,1分钟后再点燃酒精灯加
1 2
热铜丝。此步操作目的是 ,实验观察到铜丝未变化,则得出结论 。
(3)打开K,关闭K,出现 现象,可证明有水时CO 与NaO 发生了反应。
2 1 2 2 2
(4)写出CO 与NaO 反应的化学方程式 ,该反应氧化剂和还原剂的个数比为
2 2 2
。
(5)该课外活动小组欲证明NaO 和水反应生成了NaOH,向反应后的溶液中滴加了2滴酚
2 2
酞,发现溶液先变红后褪色,经查阅资料可知,“NaO 和水的反应是分步的,会生成中
2 2
间产物HO”,该小组同学为了验证这一结论,取少量NaO 和水反应后的溶液于小试管中,
2 2 2 2
用小药匙加入 ,若看到 的现象,则证明确有中间产物HO 生成。
2 2
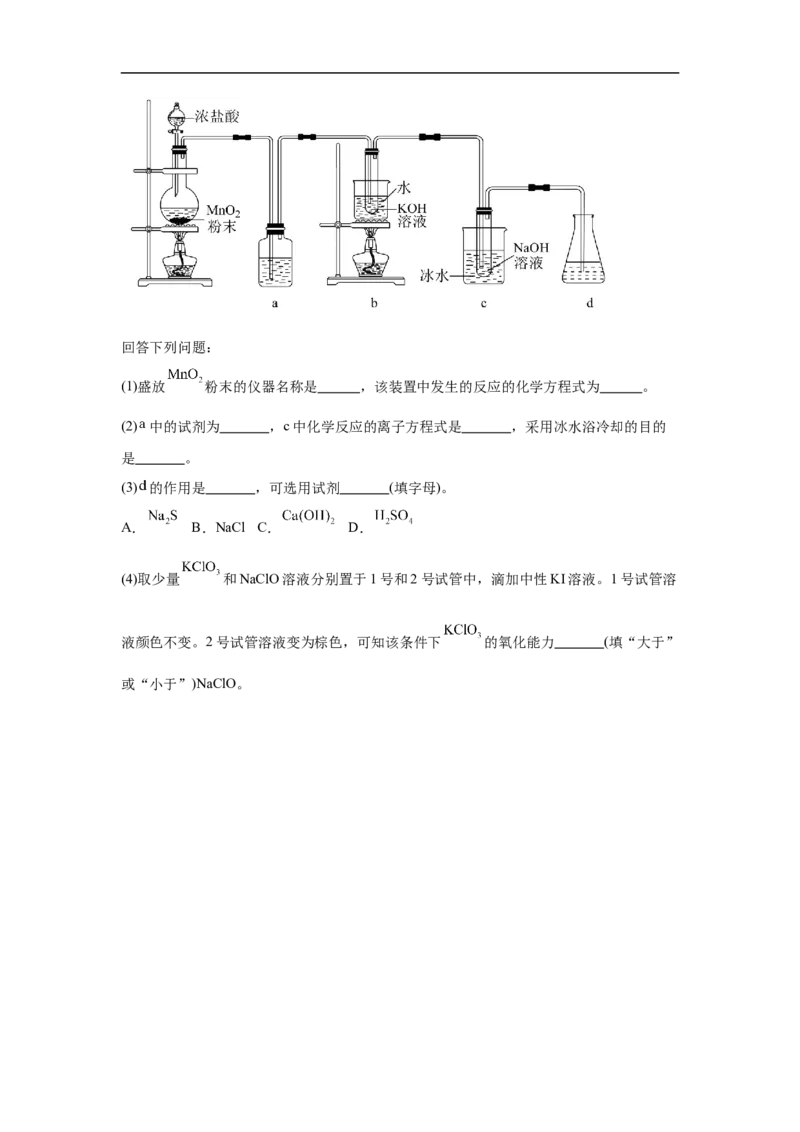
20.(本题14分)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中
利用下图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。已知: 溶于
水溶液显棕色。
试卷第6页,共3页回答下列问题:
(1)盛放 粉末的仪器名称是 ,该装置中发生的反应的化学方程式为 。
(2) 中的试剂为 ,c中化学反应的离子方程式是 ,采用冰水浴冷却的目的
是 。
(3) 的作用是 ,可选用试剂 (填字母)。
A. B.NaCl C. D.
(4)取少量 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶
液颜色不变。2号试管溶液变为棕色,可知该条件下 的氧化能力 (填“大于”
或“小于”)NaClO。参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 A A B D B D B C D A
题号 11 12 13 14 15 16
答案 B B D D B B
17.(1) C K S N C
2 2
(2)
(3)C
(4) 3 63
18.(1) 有蓝色沉淀生成 Cu2++2OH-=Cu(OH) ↓
2
(2) 生成无色无味的气体 +H+=CO ↑+H O
2 2
(3) 盐酸(或硫酸、或硫酸铜溶液) Fe+2H+=Fe2++H ↑(或Fe+Cu2+=Fe2++Cu)
2
(4) 铁粉 Fe+Cu2+=Fe2++Cu
(5)2H++SO +Ba2++2OH-=BaSO ↓+2H O
4 2
19.(1) 浓硫酸 除去CO 气体中混入的水蒸气,防止干扰后续实验
2
(2) 用CO 排尽装置内的空气,防止空气中的氧气干扰实验 无水时,CO 与
2 2
NaO 不发生反应
2 2
(3)红色铜丝变黑色
(4) 2Na O+2CO =2Na CO+O 1:1
2 2 2 2 3 2
(5) MnO 有气泡逸出
2
20.(1) 圆底烧瓶
(2) 饱和食盐水 Cl+2OH−=ClO−+Cl−+H O 避免生成NaClO
2 2 3
(3) 吸收尾气(Cl ) AC
2
(4)小于