文档内容
班级 姓名 学号 分数
第三章 水溶液中的离子反应与平衡(A卷·知识通关练)
核心知识1 弱电解质的电离平衡
1.(2021·前郭尔罗斯蒙古族自治县蒙古族中学高二期末)下列有关强、弱电解质的叙述正确的是
A.强电解质溶液的导电性不一定比弱电解质溶液的导电性强
B.强电解质的水溶液中不存在分子
C.强电解质都是离子化合物,而弱电解质都是共价化合物
D.不同的弱电解质只要物质的量浓度相同,电离程度也相同
【答案】A
【详解】A.溶液导电能力取决于溶液中离子浓度大小,强电解质溶液的导电性不一定比弱电解质溶液的
导电性强,A项正确;
B.强电解质的水溶液中含有水分子,B项错误;
C.离子化合物都是强电解质,但强电解质不一定是离子化合物;弱电解质都是共价化合物,但共价化合
物不一定是弱电解质,C项错误;
D.不同弱电解质电离程度由本性决定,浓度相同的弱电解质溶液中电离程度不一定相同,D项错误;
答案选A。
2.食用白醋是生活中重要的调味品,其中含3% ~5%的醋酸。以下实验能证明醋酸为弱电解质的是( )
A.用食用白醋做导电实验,灯泡很暗
B.将水垢浸泡在白醋中,有CO 气体放出
2
C.向白醋中滴入紫色石蕊试液,溶液呈红色
D.中和等pH、等体积的盐酸和白醋,白醋消耗NaOH多
【答案】D
【解析】强弱电解质的根本区别是电离程度,部分电离的电解质是弱电解质,只要证明醋酸部分电离就能
证明醋酸是弱电解质,据此分析解答。
A.溶液的导电性与离子的浓度有关,弱电解质的浓度大时导电实验中灯泡也很亮,没有对比实验,无法
说明醋酸是弱电解质,故A不符合题意;
B.水垢浸泡在白醋中有CO 气体放出,说明醋酸酸性大于碳酸,但不能证明醋酸部分电离,所以不能证
2
明醋酸是弱电解质,故B不符合题意;
C.白醋中滴入石蕊试液变红色,说明白醋属于酸,不能证明其部分电离,所以不能证明醋酸是弱酸,故
1 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司C不符合题意;
D.等体积等pH的醋酸和盐酸溶液中,醋酸溶液浓度大于盐酸,醋酸存在电离平衡,随反应进行,促进电
离正向移动,醋酸消耗NaOH多,故D符合题意;
答案选D。
3.与0.1mol/L的氨水溶液中c(OH-)最接近的数值是
A.0.1mol/L B.1.0×10-3mol/L C.1.0×10-7mol/L D.1.0×10-13mol/L
【答案】B
【详解】
一水合氨为弱电解质,电离微弱,所以c(OH-)远小于0.1mol/L,而氨水显碱性,所以溶液中c(OH-)>
1.0×10-7mol/L;
综上所述最接近的数值应为1.0×10-3mol/L,故答案为B。
4.下列属于电离方程式且书写正确的一项是
A.HCO3
-
+H
OHCO+OH-
2 2 3
B.HCO
2H++CO3 2-
2 3
C.CHCOOH+OH-CHCOO-+H
O
3 3 2
D.CHCOOHCHCOO-+H+
3 3
【答案】D
【详解】
HCO HCO H CO2
A. 3 部分电离,其电离方程式为 3 3 ,故A错误;
B.碳酸是二元弱酸,应分步电离,故B错误;
CH COOH CH COOH CH COOH
C. 3 是弱酸,部分电离,电离方程式为 3 3 ,故C错误;
CH COOH CH COOH CH COOH
D. 3 是弱酸,部分电离,电离方程式为 3 3 ,故D正确;
故答案选D。
5.已知醋酸溶液达到电离平衡后,改变某一条件使电离平衡向正反应方向移动,则下列说法正确的是
A.醋酸的电离程度一定变大 B.溶液的导电能力一定变强
C.溶液的pH一定减小 D.发生电离的分子总数增多
2 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司【答案】D
【详解】
A.增大醋酸的浓度,电离平衡正向移动,但醋酸的电离程度变小,A错误;
B.加水稀释,醋酸的电离平衡正向移动,由于CHCOO-和H+浓度均减小,故溶液的导电能力变弱,B错
3
误;
C.加水稀释,醋酸的电离平衡正向移动,由于CHCOO-和H+浓度均减小,溶液的pH增大,C错误;
3
D.醋酸电离平衡正向移动,一定有更多的醋酸分子发生电离,D正确;
故答案为:D。
6.用水稀释 0.1mol/L 氨水时,溶液中随着水量的增加而减小的是( )
A.c(OH﹣)/ c(NH .H O) B.c(NH .H O)/ c(OH﹣)
3 2 3 2
C.c(H+)和 c(OH﹣)的乘积 D.OH﹣的物质的量
【答案】B
【解析】A.由NH .HO OH-+NH+可知,加水促进电离,则n(NH .HO)减少,n(OH-)增大,c(OH﹣)/
3 2 4 3 2
c(NH .H O),上下同时乘以体积,c(OH﹣)/ c(NH .H O)= n(OH-)/ n(NH .HO),二者的比值增大,A项不符
3 2 3 2 3 2
合题意;
B. 由NH .HO OH-+NH+可知,加水促进电离,则n(NH .HO)减少,n(OH-)增大,c(OH﹣)/
3 2 4 3 2
c(NH .H O),上下同时乘以体积, c(NH .H O)/ c(OH﹣) = n(NH .HO)/ n(OH-),二者的比值减小,B项符
3 2 3 2 3 2
合题意;
C.因加水稀释时,温度不变,则c(H+)和c(OH-)的乘积不变,C项不符合题意;
D.由NH ·HO OH-+NH+可知,加水促进电离,OH-的物质的量增大,D项不符合题意;
3 2 4
故选B。
7.在体积都为1 L、c(H+)102molL1的盐酸和醋酸溶液中,投入0.65 g锌粒,则下图所示比较符合客
观事实的是
A. B.
3 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司C. D.
【答案】C
【详解】
体积都为1L氢离子浓度均为10—2mol/L盐酸和醋酸溶液中,氢离子浓度相等,反应速率相等,但醋酸是弱
酸,溶液中存在电离平衡,醋酸的浓度大于盐酸浓度,向两种酸溶液中加入0.65g锌粒时,盐酸溶液中锌
过量,醋酸溶液中锌不足,则醋酸溶液中与锌反应生成的氢气的物质的量大于盐酸,由于醋酸中电离平衡
向电离方向移动,溶液中氢离子浓度变化小,生成氢气的反应速率大于盐酸,醋酸先完全反应,故选C。
核心知识2 电离平衡常数
8.1 mol·L-1 HA溶液中有1%的HA电离,则HA的电离平衡常数K 为
a
A.1.0×10-4 B.1.0×10-5 C.1.0×10-2 D.1.0×10-6
【答案】A
【详解】
1 mol·L-1 HA溶液中有1%的HA电离,则电离的HA的物质的量浓度为0.01 mol·L-1,可建立以下三段式:
HA H A
起始量mol/L 1 0 0
变化量mol/L 0.01 0.01 0.01
平衡量mol/L 0.99 0.01 0.01
0.010.01
K= ≈1.0×10-4,故选A。
a 0.99
9.现有浓度均为0.1mol•L-1某二元酸HA和某一元酸HB,已知HA的电离方程式为:HA=H++HA-,HA-
2 2 2
噲垐��
H++A2-。则下列有关说法不正确的是
A.若KHA溶液显酸性,说明HA-的电离程度大于水解程度
B.中和相同体积的两种溶液,需要相同浓度的NaOH溶液体积比为V(H A):V(HB)=2:1
2
C.常温下,若两溶液有pH(H A)1×10-7mol/L,说明促进水的电离,
A.NaOH是强碱,电离出的OH-抑制了水的电离,故A错误;
B.NaHSO 溶液中溶质完全电离,溶液显酸性,抑制水的电离,故B错误;
4
C.HNO 是强酸,完全电离,电离出的H+抑制了水的电离,故C错误;
3
D.CHCOONa属于强碱弱酸盐,电离出的CHCOO-发生水解,促进水的电离,故D正确。
3 3
故选D。
19.(2021·江苏省镇江第一中学高二月考)在相同温度下,0.01 mol·L-1 NaOH溶液和0.01 mol·L-1的盐酸
相比,下列说法正确的是
A.两溶液中由水电离的c(H+)都是1.0×10-12 mol·L-1
B.NaOH溶液和盐酸由水电离出c(OH-)分别为1.0×10-2 mol·L-1、1.0×10-12 mol·L-1
C.两溶液中由水电离出的c(H+)相等
D.两者都促进了水的电离
【答案】C
【详解】
K
w
酸和碱的电离都会抑制水的电离,温度相同则K 相同,0.01mol/L NaOH溶液中水电离出的c(H+) =
w 水 0.01
K
w
mol/L,0.01mol/L的盐酸溶液中水电离出的c(H+) =c(OH-) = mol/L,所以由水电离出的c(H+)相等,但
水 水 0.01
由于温度未知,所以无法确定具体值;
综上所述答案为C。
20.温度为t℃时,某NaOH稀溶液中c(H+)=10 -amol·L -1,c(OH -)=10 -bmol·L -1;已知:a+b=13,请回答下
列问题:
10 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(1)该温度下水的离子积常数K =_______,t_______(填“<”、“>”或“=”)25。
w
(2)该NaOH溶液中NaOH的物质的量浓度为_______,该NaOH溶液中由水电离出的c(OH-)为_______。
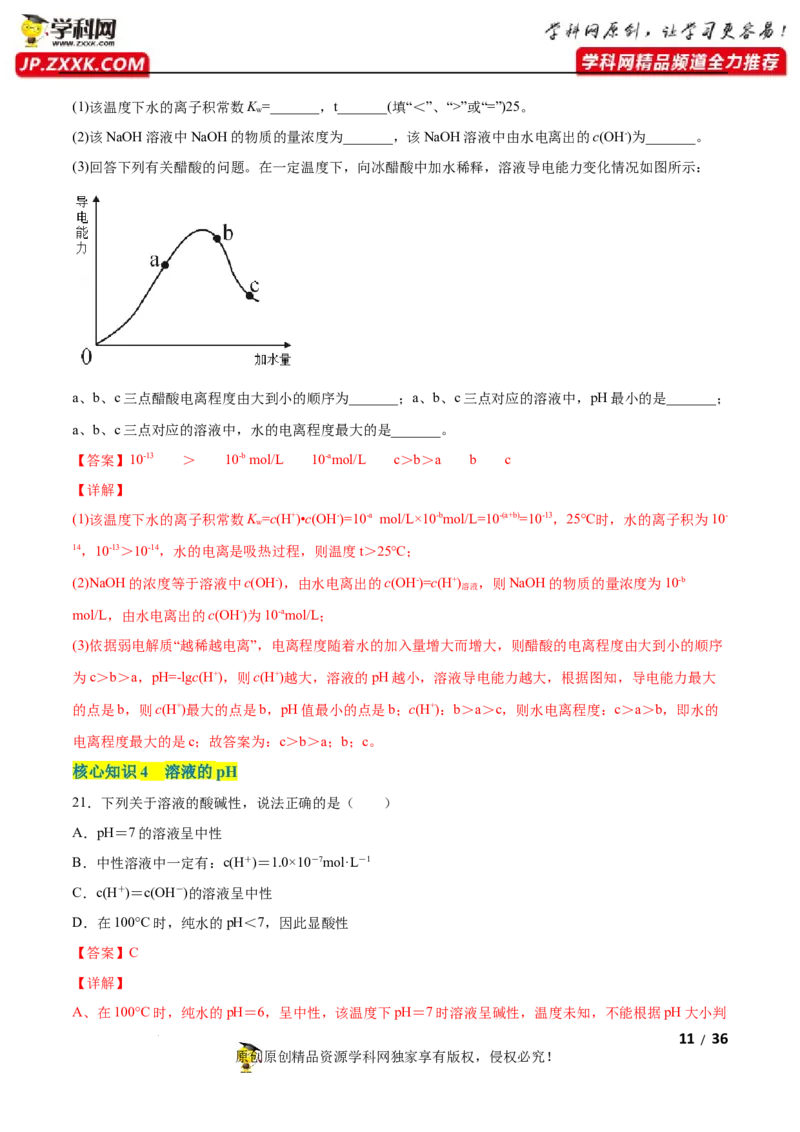
(3)回答下列有关醋酸的问题。在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示:
a、b、c三点醋酸电离程度由大到小的顺序为_______;a、b、c三点对应的溶液中,pH最小的是_______;
a、b、c三点对应的溶液中,水的电离程度最大的是_______。
【答案】10-13 > 10-b mol/L 10-amol/L c>b>a b c
【详解】
(1)该温度下水的离子积常数K =c(H+)•c(OH-)=10-a mol/L×10-bmol/L=10-(a+b)=10-13,25℃时,水的离子积为10-
w
14,10-13>10-14,水的电离是吸热过程,则温度t>25℃;
(2)NaOH的浓度等于溶液中c(OH-),由水电离出的c(OH-)=c(H+) ,则NaOH的物质的量浓度为10-b
溶液
mol/L,由水电离出的c(OH-)为10-amol/L;
(3)依据弱电解质“越稀越电离”,电离程度随着水的加入量增大而增大,则醋酸的电离程度由大到小的顺序
为c>b>a,pH=-lgc(H+),则c(H+)越大,溶液的pH越小,溶液导电能力越大,根据图知,导电能力最大
的点是b,则c(H+)最大的点是b,pH值最小的点是b;c(H+):b>a>c,则水电离程度:c>a>b,即水的
电离程度最大的是c;故答案为:c>b>a;b;c。
核心知识4 溶液的pH
21.下列关于溶液的酸碱性,说法正确的是( )
A.pH=7的溶液呈中性
B.中性溶液中一定有:c(H+)=1.0×10-7mol·L-1
C.c(H+)=c(OH-)的溶液呈中性
D.在100°C时,纯水的pH<7,因此显酸性
【答案】C
【详解】
A、在100°C时,纯水的pH=6,呈中性,该温度下pH=7时溶液呈碱性,温度未知,不能根据pH大小判
11 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司断溶液酸碱性,故A错误;
B、常温下中性溶液中c(H+)=1.0×10-7 mol·L-1,温度未知,中性溶液中不一定有c(H+)=1.0×10-7 mol·L
-1,故B错误;
C、c(H+)=c(OH-)的溶液呈中性,与溶液温度高低无关,故C正确;
D、在100°C时,纯水的pH=6,呈中性,故D错误;
答案为C。
【点睛】
温度未知,不能根据pH大小判断溶液酸碱性,也不能根据氢离子或氢氧根浓度来判断溶液酸碱性,只能
根据c(H+)、c(OH-)相对大小来判断。
c(OH-)
22.常温下,pH=11的氢氧化钡溶液中,由水电离出的 为
1.0107molL1 1.01011molL1
A. B.
2.0103molL1 5.01012molL1
C. D.
【答案】B
【详解】
在碱溶液中有:c(OH-) =c(OH-) +c(OH-) ,c(H+) =c(H+) ,c(OH-) = c(H+) ,故有常温下,pH=11的氢
(aq) 碱 水 (aq) 水 水 水
c(OH-)
氧化钡溶液中,由水电离出的 等于水电离出的c(H+),也等于溶液中的H+浓度,故等于
1.01011molL1
,故B正确。
故答案为:B。
pH
23.室温下,对于等体积、 均为2的醋酸和盐酸两种溶液,下列叙述不正确的是
A.分别加足量的锌充分反应后,醋酸溶液产生的氢气多
pH
B.分别加水稀释10倍数后,两溶液的 均为3
C.若HA表示 HCl 或 CH 3 COOH ,两溶液中都有
c2 H
c
H
c
A
K w
pH
D.温度都升高20℃后,两溶液的 不再相等
【答案】B
12 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司【详解】
A.醋酸为弱酸,pH相同、体积相同的醋酸和盐酸,醋酸的浓度大,分别加足量的锌充分反应后,醋酸溶
液产生的氢气多,故A正确;
B.pH相同、体积相同的醋酸和盐酸两种溶液分别加水稀释10倍后,溶液中氢离子浓度都减小,醋酸为
弱电解质,加水稀释要继续电离出氢离子,所以pH<3,盐酸为强电解质,所以稀释后pH=3,故B错误;
c
H
c
OH
c
A
c
H
C.溶液存在电荷守恒: ,两边同乘以 ,
c2 H
c
OH
·c
H
c
A
·c
H
c
A
·c
H
K
w,故C正确;
D.盐酸是强酸,不存在电离平衡,升高温度,盐酸的pH几乎不变,醋酸是弱酸,其水溶液中存在电离平
衡,升高温度,促进醋酸电离,导致醋酸溶液中氢离子浓度增大,所以醋酸的pH减小,故D正确;
故答案为B。
24.下列关于常温下,体积均为10mL,pH均为4的HCl溶液a和CHCOOH溶液b的有关说法不正确的
3
是
A.对水的电离的抑制程度相同
B.稀释至相同pH后,V;升温促进水的电离,K 增大;
w
K 110-12
w
(2) 根据第(1)问可知,该温度下,c(H+)=1×10-7 mol/L的溶液,c(OH−)=c H+ 110-7 =1×10−5
mol·L−1,c(H+)< c(OH−),溶液显碱性;该溶液中只存在NaOH溶质,则由HO电离出来的c(OH−) =c(H+)
2 水 水
= c(H+)=10−7molL−1
(3) Zn和稀硫酸⋅反应,使溶液酸性减弱,对水的电离抑制程度减弱,即水的电离平衡向右移动;在新制氯
水中加入少量NaCl固体,水中的Cl-浓度增大,则平衡Cl+H OH++Cl-+HClO向逆反应方向移动,即向
2 2
生成Cl 分子的方向移动,氯水中的H+浓度降低,对水的电离抑制程度降低,水的电离向右移动,故答案
2
为:向右;向右;
K
(4) ①HCl,0.1mol/L的HCl,氢离子浓度为0.1mol/L,溶液中氢氧根离子浓度为
w =10-13mol/L,溶
0.1mol/L
液中氢氧根离子完全来源于水的电离,水电离的氢离子浓度和氢氧根离子浓度相等,故水电离的氢离子浓
14 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司度为10-13mol/L;
K
②HSO ,0.1mol/L的HSO ,氢离子浓度为0.2mol/L,溶液中氢氧根离子浓度为
w =510-14mol/L,
2 4 2 4 0.2mol/L
溶液中氢氧根离子完全来源于水的电离,水电离的氢离子浓度和氢氧根离子浓度相等,故水电离的氢离子
浓度为510-14mol/L;
= K c 1.7106 1.3103mol/L
③CHCOOH(K=1.7×10-5),0.1mol/L的CHCOOH,氢离子浓度为 a ,
3 a 3
K
溶液中氢氧根离子浓度为
w =7.610-12mol/L,溶液中氢氧根离子完全来源于水的电离,水电离
1.310-3mol/L
的氢离子浓度和氢氧根离子浓度相等,故水电离的氢离子浓度为7.610-12mol/L;
= K c 1.7106 1.3103mol/L
④NH ·H O(K =1.7×10-5),0.1mol/L的NH ·H O,氢氧根离子浓度为 b ,
3 2 b 3 2
K
氢离子浓度为
w =7.610-12mol/L,溶液中,溶液中氢离子完全来源于水的电离,故水电离的氢
1.310-3mol/L
离子浓度为7.610-12mol/L;
K
⑤NaOH,0.1mol/L的NaOH,氢氧根离子浓度为0.1mol/L,溶液中氢离子浓度为
w =10-13mol/L,
0.1mol/L
溶液中氢离子完全来源于水的电离,故水电离的氢离子浓度为10-13mol/L;
⑥Ba(OH) ,0.1mol/L的Ba(OH) ,氢氧根离子浓度为0.2mol/L,溶液中氢离子浓度为
2 2
K
w =510-14mol/L,溶液中氢离子完全来源于水的电离,故水电离的氢离子浓度为
;
0.2mol/L 510-14mol/L
故水电离出的c(H+)由大到小的关系是③=④>①=⑤>②=⑥;
K 110-14
W
(5) 25 ℃时,pH=4的盐酸中c(H+)=1×10-4mol/L,c(OH-)=c H+ 110-4 =1×10-10mol/L=c(OH-) = c(H+) ,
水 水
pH=10的Ba(OH) 溶液中c(H+)=1×10-10mol/L= c(H+) = c(OH-) ,由此可知,两溶液中水的电离程度相同。
2 水 水
核心知识5 酸碱中和滴定
26.实验室现有3种酸碱指示剂。其pH变色范围如下
甲基橙:3.1~4.4 石蕊:`5.0~8.0 酚酞:8.2~10.0
用0.1000 mol/L NaOH溶液滴定未知浓度的CHCOOH溶液,反应恰好完全时。下列叙述正确的是
3
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
15 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司C.溶液呈酸性,可选用甲基橙作指示剂
D.溶液星碱性,只能选用酚酞作指示剂
【答案】D
【详解】
NaOH与CHCOOH恰好完全反应生成CHCOONa,CHCOONa为强碱弱酸盐,水解后溶液呈碱性,为了
3 3 3
减少滴定误差,应选择指示剂的pH范围与CHCOONa溶液的pH接近,所以指示剂选择酚酞,D正确;
3
故选D
27.酸碱滴定实验必须要用到的仪器是
①烧杯 ②玻璃棒 ③锥形瓶 ④坩埚 ⑤滴定管 ⑥ 胶头滴管
A.①②③ B.②③④⑥ C.③⑤ D.②③⑤
【答案】C
【详解】
酸碱滴定需要用到的仪器有铁架台、滴定管、滴定管夹、锥形瓶、烧杯等,必须要用到的仪器是锥形瓶和
滴定管,答案选C。
28.下列关于中和滴定实验的说法中正确的是
A.应用碱式滴定管盛放稀盐酸标准溶液
B.锥形瓶一定要用蒸馏水洗净并烘干
C.接近终点时应控制滴速,使溶液一滴一滴地缓慢滴下
D.滴定终点时俯视读数,会使测定结果偏大
【答案】C
【详解】
A.稀盐酸为酸性溶液,应该用酸性滴定管盛放稀盐酸标准液,故A错误;
B.锥形瓶中的水不影响待测定物质的物质的量,消耗的标准液不变,故锥形瓶用蒸馏水洗净后不用烘干,
故B错误;
C.接近终点应控制滴速,防止过量使滴定终点有误,故C正确;
D.滴定终点时俯视读数,测得标准液的体积偏小,待测液浓度偏小,故D错误;
故选C。
29.(2021·吉林白城市·白城一中高二月考)NaOH标准溶液的配制和标定,需经过NaOH溶液配制、基
准物质HC O•2H O的称量以及用NaOH溶液滴定等操作。下列有关说法正确的是
2 2 4 2
16 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A.图甲:转移NaOH溶液到250mL容量瓶中
B.图乙:准确称得0.1575gH C O·2H O固体
2 2 4 2
C.用图丙所示操作排除碱式滴定管中的气泡
D.用图丁所示装置以NaOH待测液滴定HC O 溶液
2 2 4
【答案】C
【详解】
A.向容量瓶中转移溶液时需要用玻璃棒引流,故A错误;
B.托盘天平的精度值为0.1g,故B错误;
C.碱式滴定管中气泡排出操作:把橡皮管向上弯曲,出口上斜,挤捏玻璃珠,使溶液从尖嘴快速喷出,
气泡即可随之排掉,故C正确;
D.NaOH溶液应装在碱式滴定管中,故D错误;
故答案为C。
30.按要求回答下列问题
(1)一定温度下,现有a.盐酸,b.硫酸,c.醋酸三种酸
①当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需NaOH的物质的量由大到小的顺序是
_______(用a、b、c表示)
②当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是
_______(用a、b、c表示)
③当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H(相同状况),
2
则开始时反应速率的大小关系为 _______(用a、b、c表示)
(2)现用中和滴定法测定某烧碱溶液的浓度,有关数据记录如表:
所消耗盐酸标准液的体积/mL
滴定序 待测液体积
号 /mL
滴定前 滴定后 消耗的体积
1 25.00 0.50 26.80 26.30
17 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司2 25.00 - - -
3 25.00 5.00 31.34 26.34
0.2500mol·L1
①用_______式滴定管盛装 盐酸标准液。如图表示第二次滴定前后50mL滴定管中液面的位置。
该次滴定所用标准盐酸体积为_______mL。
②现实验室中有石蕊和酚酞两种指示剂,该实验应选用_______作指示剂。
③根据所给数据,该烧碱样品的物质的量浓度为_______。
④若操作过程中滴加盐酸速度过快,未充分振荡,刚看到溶液变色,就立刻停止滴定,则会造成测定结果
_______(填“偏低”“偏高”或“无影响”)。
【答案】(1)b>a=c c>a=b a=b=c
(2)酸 24.60 酚酞 0.2632mol/L 偏低
【分析】
(1)①三种酸体积相同、物质的量浓度也相同即物质的量相同,盐酸和醋酸都是一元酸,和NaOH完全
中和时,需要的NaOH的物质的量和一元酸的物质的量相等,所以盐酸和醋酸消耗的氢氧化钠的物质的量
相等;硫酸是二元酸,和NaOH完全中和时,需要的NaOH的物质的量是硫酸的物质的量的2倍,所以三
种酸和NaOH恰好完全中和所需NaOH的物质的量由大到小的顺序是b>a=c;
②三者c(H+)相同时 ,由于醋酸是弱酸,醋酸的浓度要大于盐酸的浓度,所以当盐酸和醋酸体积相同时,
醋酸的物质的量大于盐酸的物质的量,和足量的锌反应时,醋酸生成氢气的物质的量大于盐酸生成氢气的
物质的量。盐酸和硫酸都是强酸,完全电离,H+的物质的量相等,和足量的锌反应,生成氢气的物质的量
相等。相同状况下,气体体积和气体的物质的量成正比,所以相同状况下产生气体的体积由大到小的顺序
是c>a=b;③形状、密度、质量完全相同的锌和三种酸反应,反应的实质是锌和H+反应,反应速率由
c(H+)决定,所以三种酸溶液中c(H+)相同时,开始时反应速率相等,即a=b=c;
(2)①盐酸要用酸式滴定管盛装。从滴定管液面可以看出,滴定前液面在0.30mL处,滴定后液面在
24.90mL处,所以该次滴定所用标准盐酸体积为用24.60mL;②石蕊颜色变化不明显,通常不用做酸碱中
18 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司和滴定的指示剂,应选用酚酞作指示剂;③分析三组数据,消耗盐酸的体积的第二组数据和其他两组差别
较大,舍去,第一组和第三组消耗盐酸的体积的平均值为26.32mL,盐酸和NaOH等物质的量反应,所以
有0.2500mol/L×0.02632L=c(NaOH)×0.02500L,可计算出c(NaOH)=0.2632mol/L;④滴定操作开始时滴加盐
酸的速度可以快一些,当快达到滴定终点时,一定要逐滴滴入,直到指示剂颜色改变且摇动半分钟颜色不
恢复,才可以停止滴定,等液面稳定之后再读数。若操作过程中滴加盐酸速度过快,未充分振荡,刚看到
溶液变色,就立刻停止滴定,则滴入的盐酸的体积偏小,会造成测定结果偏低。
核心知识6 盐溶液的酸碱性及其原因
31.常温下,测得0.5mol·L-1的CHCOONa溶液的pH=9。下列说法正确的是
3
A.该溶液中由水电离出的c(OH-)=1×10-9mol·L-1
B.该溶液中存在:c(Na+)>c(CH COOH)>c(CH COO-)>c(H+)
3 3
C.该溶液中存在:c(H+)+c(CH COOH)>c(OH-)
3
cCH COOH
3
D.向溶液中加入少量水, c
CH
COO-
增大
3
【答案】D
【详解】
A.CHCOONa溶液水解呈碱性,氢氧根完全来自水的电离,c(H+)=1×10-9 mol·L-1,则由水电离出的
3
c(OH-)=1×10-5 mol·L-1,A错误;
B.该溶液中微粒浓度大小:c(Na+)> c(CHCOO-) > c(OH-)>c(CH COOH)>c(H+),B错误;
3 3
C.该溶液中存在质子守恒:c(H+)+c(CH COOH)=c(OH-),C错误;
3
c CH COO- c H+ cCH COOH c H+
Ka 3 3
D.由 cCH COOH 知, c CH COO- cK 向溶液中加入少量水,溶液的碱性减小,氢离
3 3 a
cCH COOH
3
子浓度增大,所以, c
CH
COO-
增大,D正确
3
故选D。
32.某温度下,0.1 mol·L-1NaHCO 溶液pH=10,下列判断正确的是
3
A.c(OH-)=10-4 mol·L-1
B.加入少量NaOH固体,c(Na+)和c(HCO3)均增大
19 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司
C.c(Na+)+c(H+)=c(HCO3)+c(OH-)
2
D.c(Na+)=c(HCO3)+c(CO3 )+c(H CO)
2 3
【答案】D
【详解】
A.溶液pH=10,则c(H+)=10-10 mol/L,由于温度不一定是室温,温度未知,因此不能确定K 的大小,也
w
就不能计算出溶液中c(OH-)大小,A错误;
B.加入少量NaOH固体,c(Na+)增大,c(OH-)增大,对HCO3的水解平衡起抑制作用,导致溶液中c(HCO
3)减小,B错误;
CO2
C.在溶液中存在HCO3电离产生的 3 ,根据电荷守恒可得:c(Na+)+c(H+)=c(HCO3)+c(OH-)+2c(CO
2
3 ),C错误;
2
D.根据物料守恒可得:c(Na+)=c(HCO3)+c(CO3 )+c(H CO),D正确;
2 3
故合理选项是D。
33.下列离子方程式的书写正确的是
A.硫化钠水解:S2-+2H O HS↑+2OH-
2 2
HSO⇌- SO2-
B.亚硫酸氢钠水解: 3+H O HO++ 3
2 3
⇌
C.硫化钾水解:S2-+H O=HS-+OH-
2
AlO-
D.硫酸铝溶液跟偏铝酸钠溶液反应:Al3++3 2+6H O=4Al(OH) ↓
2 3
【答案】D
【详解】
A. S2- 水解要分两步,且不产生 H 2 S 气体,为: S2-+H 2 O HS-+OH- ; HS-+H 2 O H 2 S+OH- ,故A错误;
B.硫氢根离子水解生成硫化氢和氢氧根离子,离子方程式:HS-+H O HS+OH-,故B错误;
2 2
C.硫化钾水解: S2- 水解要分两步,为: S2-+H 2 O HS-+OH- ; HS-+H⇌ 2 O H 2 S+OH- ,故C错误;
20 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司D.
Al3+
与
AlO-
2水解相互促进而彻底反应生成
AlOH
3沉淀,故离子反应方程式为:
Al3++3AlO-+6H O=4Al(OH)
2 2 3 ,故D正确;
故答案为D。
核心知识7 影响盐类水解的主要因素
34.下列关于盐类水解的说法错误的是
A.在纯水中加入能水解的盐一定促进水的电离
pH7
B.常温下,醋酸分子不可能存在于 的碱性溶液中
NH Cl NH
C.在 4 溶液中加入稀盐酸能抑制 4水解
c
CH
COO
3
D.加热 CH COONa 溶液,溶液中 c Na 的值将减小
3
【答案】AB
【详解】
A.不一定如硫酸氢铵溶液,铵根离子能够发生水解反应,但本身电离产生的氢离子对水的电离起抑制作
用,故A错误;
CH COONa CH COO CH COOH
B.常温下, 3 溶液呈碱性,溶液中 3 水解能生成 3 ,B错误;
NH NH
C.溶液中 4水解使溶液显酸性,加入稀盐酸能抑制 4的水解,C正确;
CH COONa CH COO c
CH
COO
c
Na+
D.加热 3 溶液, 3 的水解程度增大, 3 减小, 不变,则
c
CH
COO
3
c Na 的值变小,D正确;
正确答案选AB。
Al3 3H O Al(OH) 3H
35.在反应 2 3 的平衡体系中,要使平衡向水解方向移动,且使溶液的pH增大,
应采取的措施是
21 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司HCl NaOH AlCl
A.加热 B.通入 气体 C.加入适量的 溶液 D.加入固体 3
【答案】C
【详解】
A.盐的水解是酸碱中和反应的逆反应,是吸热的,加热可以使平衡正向移动,溶液的pH减小,故A不
选;
B.通入HCl气体,增大氢离子浓度,平衡逆向移动,故B不选;
C.加入NaOH溶液,中和H+,降低了氢离子浓度,平衡正向移动,pH增大,故C选;
D.加入AlCl 固体,Al3+浓度增大,平衡正向移动,使H+浓度增大,pH减小,故D不选;
3
故选C。
c
Na
36.为使
Na S
溶液中
c
S2 的值减小,可加入的物质是( )
2
①HCl ②适量的NaOH固体 ③适量的KOH固体 ④适量的KHS固体
A.①② B.②③ C.③④ D.①④
【答案】C
【分析】
在硫化钠溶液中存在水解平衡:
S2 H
2
O HS OH
,
HS H
2
O H
2
SOH
,且以第一步水解
c
Na
为主, 为使
Na S
溶液中
c
S2 的值减小,平衡逆移。
2
【详解】
在硫化钠溶液中存在水解平衡:
S2 H
2
O HS OH
,
HS H
2
O H
2
SOH
,且以第一步水解
c
Na
为主。①通入 ,硫离子水解平衡正向移动, c S2减小, c Na不变, c S2 的值增大,错误;②
HCl
c
OH
c
S2
c
Na
加入适量的NaOH固体, 增大,硫离子水解平衡逆向移动, 增大,但 也增大,且钠
22 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司c
Na
离子浓度增大得更多, c S2 的值增大,错误;③加入适量的 固体, c OH增大,硫离子水解平
KOH
c
Na
衡逆向移动, c S2增大, c Na不变, c S2 的值减小,正确;④加入适量的 固体, 浓度不
KHS Na
c
Na
变, HS 浓度增大, S2 H
2
O HS OH水解平衡逆向移动, c S2增大, c S2 值减小,正确,
故答案选:C。
37.某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
探究浓度对醋酸电离程度的影响:用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度(mol/L) 0.0010 0.0100 0.0200 0.1000 0.2000
pH 3.88 3.38 3.23 2.88 2.73
回答下列问题:
(1)若用pH试纸测醋酸的pH,实验操作为:_______。
(2)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:_______。
(3)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度_______(填增大、减小
或不变)
Na CO CO2 K =210-4
(4) 2 3俗称纯碱,因 3 水解而使其水溶液呈碱性(忽略第二步水解),已知25℃时, h ,
c
HCO
:c
CO2
2:1
则当溶液中 3 3 时,溶液的pH=_______。
【答案】(1)将一小片pH试纸放在表面皿上,用玻璃棒或胶头滴管将待测液滴在试纸上,再将变色的试
纸与标准比色卡对照读出数值;
(2)当醋酸溶液的浓度为10-3 mol/L时,pH = 3.88,c(H+) =10-3.88 mol/L <10-3 mol/L
(3)增大
(4)10
【解析】(1)pH试纸测定pH的方法是:将一小片pH试纸放在表面皿上,用玻璃棒或胶头滴管将待测液
滴在试纸上,再将变色的试纸与标准比色卡对照读出数值
23 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(2)当醋酸溶液的浓度为10-3 mol/L时,pH = 3.88,c(H+) =10-3.88 mol/L <10-3 mol/L,说明醋酸在溶液中
不能完全电离,可证明醋酸时弱电解质,故依据是:当醋酸溶液的浓度为10-3 mol/L时,pH = 3.88,c(H+)
=10-3.88 mol/L <10-3 mol/L;
(3)当醋酸溶液的浓度为10-3 mol/L时,pH =3.88,c(H+) =10-3.88 mol/L,当醋酸溶液浓度为10-2mol·L—1
1 1
时,pH=3.38,c(H+) =10-3.38 mol/L,综合以上数据,溶液浓度减小为原来的 ,c(H+)大于原来的 ,由
10 10
此可知,随醋酸浓度的减小,醋酸的电离程度增大。
c(HCO)c(OH-)
K = 3 =210-4mol/L
(4)K= 2×10-4mol/L,则当溶液中c HCO :c CO2 2:1时, h c(CO2-) ,
3 3 3
c(OH-)=110-4mol/L c(H+)=110-10mol/L
,
所以溶液的pH =10,故答案为:10;
核心知识8 盐类水解的应用
38.下列说法不正确的是
Mg(OH) FeCl
A.向 2悬浊液中滴加 3溶液,生成红褐色沉淀
B.碳酸氢钠药片,该药是抗酸药,服用时喝些醋能提高药效
C.配制氯化铁溶液时需加入适量盐酸抑制水解
CaSO Na CO
D.水垢中的 4,可先用 2 3溶液处理,而后用酸除去
【答案】B
【详解】
Mg(OH) FeCl Mg(OH) Fe(OH)
A.向 2悬浊液中滴加 3溶液,可使 2转化为红褐色沉淀 3,A正确;
NaHCO
B.碳酸氢钠属于抗酸药,醋酸会与 3反应,从而降低药效,B错误;
C.氯化铁为强酸弱碱盐,溶于水后易发生水解,为抑制水解,配制氯化铁溶液时需加入适量盐酸,C正
确;
D.水垢中的
CaSO
4,可先用
Na
2
CO
3溶液处理,发生反应
CaSO
4
+Na
2
CO 3 CaCO
3
Na
2
SO
4,将
CaSO CaCO CaCO
4 3 3
24 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司CaSO CaCO CaCO
4转化为溶解度更小的 3,而后用酸除去 3,D正确。
故选B。
39.实验室在配制氯化铁溶液时,先把氯化铁晶体溶解在稀盐酸中,再加水稀释所需浓度,如此操作的目
的是
A.防止氯化铁电离 B.抑制氯化铁水解
C.提高溶液的pH D.提高氯化铁的溶解度
【答案】B
【详解】
实验室在配制氯化铁溶液时,由于铁离子要发生水解,配制时容易变浑浊,因此先把氯化铁晶体溶解在稀
盐酸中,再加水稀释所需浓度,如此操作的目的是防止铁离子水解,故B正确。
综上所述,答案为B。
40.根据下列实验操作所得的现象及结论不正确的是
选项 实验操作 现象及结论
A 将MgCl 溶液加热蒸干并灼烧 得到的白色固体为MgO
2
向体积均为20mL的冷水和沸水中分别滴入3滴
前者为黄色,后者为红褐色,说明温度升高,
B
FeCl 饱和溶液 Fe3+的水解程度增大
3
取CH COONa溶液于试管中并加入几滴酚酞试 溶液颜色变深,说明CH COONa溶液中存在水
3. 3.
C
剂,再给试管加热 解平衡
室温下,用pH试纸测0.1molL1的NaHSO 溶
3
D 说明HSO的水解大于电离
3
液的pH约为5
【答案】D
【详解】
A.加热促进MgCl 水解平衡正向移动,生成氢氧化镁沉淀,灼烧氢氧化镁分解为氧化镁,故A正确;
2
B.向体积均为20mL的冷水和沸水中分别滴入3滴FeCl 饱和溶液,前者为黄色溶液,后者为红褐色胶体,
3
说明温度升高,Fe3+的水解程度增大,故B正确;
C.CHCOONa为强碱弱酸盐,其溶液显碱性,给试管加热,水解程度增大,溶液颜色变深,故C正确;
3
D.亚硫酸氢根离子电离呈酸性,水解呈碱性,0.1mol/L的NaHSO 溶液的pH约为5,电离程度大于水解
3
程度,结论错误,D错误;
故选D。
核心知识9 溶液中粒子浓度的关系
25 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司0.1molL1 NH HSO
4 4
41.在 的 溶液中,下列关于微粒物质的量浓度的关系式不正确的是( )
c
H
c
SO2
c
NH
A. 4 4
c
NH
c
H
2c
SO2
c
OH
B. 4 4
c H c NH cNH H Oc OH
C. 4 3 2
c
Na
c
SO2
c
NH
c
OH
c
H
D.常温下向该溶液中滴加 NaOH 溶液至中性后: 4 4
【答案】C
【详解】
c
H
c
SO2
c
NH
A.H+包括NH HSO 和HO电离出的H+,NH +发生水解,所以 4 4 ,A正确;
4 4 2 4
B.符合电荷守恒,B正确;
NH HSO NH H SO2
C. 4 4 4 4 ,NH H O NH H OH,由物料守恒
4 2 3 2
c NH cNH H Oc SO2 c NH c H 2c SO2 c OH
4 3 2 4 ,由电荷守恒得, 4 4 ,所以
c H c NH 2cNH H Oc OH
4 3 2 ,C错误;
NaOH NH HSO
4 4
D.当 溶液和 溶液等浓度、等体积混合后,所得溶液显酸性,所以若使题中所得溶液呈中
NaOH NaOH NH HSO NH HSO
4 4 4 4
性,则加入的 溶液中 的物质的量应大于 溶液中 的物质的量,D正确;
正确答案选C。
42.下列说法正确的是
2- -
A.常温下pH= 10的NaC O 溶液中:2c(Na+) = c(C O4 ) + c(HC O4) + c(H C O)
2 2 4 2 2 2 2 4
B.向醋酸溶液中加入醋酸钠晶体使溶液呈中性,此时混合液中c(Na+) < c(CHCOO-)
3
+
C.0.2 mol/L NH Cl溶液和0.1 mol/L (NH )SO 溶液中,c(NH4)前者较大
4 4 2 3
D.浓度均为0.1 mol/L的NaCl溶液和NaF溶液中,离子总浓度后者较大
26 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司【答案】C
【详解】
2- -
A.任何电解质溶液中都存在物料守恒,根据物料守恒得c(Na+) = 2c(C O4 ) + 2c(HC O4) + 2c(H C O),A
2 2 2 2 4
错误;
B.c(Na+)+c(H+)= c(OH-)+c(CH COO-),溶液呈中性c(H+)= c(OH-),此时混合液中c(Na+) =c(CHCOO-),B
3 3
错误;
C.0.2 mol/L NH Cl溶液中铵根无水解影响, 0.1 mol/L (NH )SO 溶液中亚硫酸根水解生成氢氧根,氢氧
4 4 2 3
+
根与铵根离子反应,故c(NH4)前者较大,C正确;
D.NaCl中离子不会水解,氟离子水解为HF,所以NaF溶液中,离子总浓度降低,离子总浓度前者较大,
D错误;
答案选C。
43.常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:
实验编号 c(HA)/mol·L-1 c(NaOH)/mol·L-1 反应后溶液pH
甲 0.1 0.1 pH=9
乙 c 0.2 pH=7
1
下列判断不正确的是
A.c 一定大于0.2
1
噲垐��
B.HA的电离方程式是HA H++A-
C.乙反应后溶液中:c(Na+)=c(HA)+c(A-)
D.甲反应后溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
【答案】C
【分析】
由甲实验数据可知,等浓度等体积的一元酸HA和NaOH溶液混合后溶液恰好生成NaA,反应后的溶液
pH=9,可知NaA为强碱弱酸盐,所以HA为一元弱酸,据此分析选择。
【详解】
A.HA是弱酸,与等体积、等浓度的NaOH溶液混合反应后恰好生成NaA,溶液应显碱性,要溶液显中
性,HA应过量,故c 一定大于0.2,A正确;
1
27 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司噲垐��
B.根据上述分析可知HA为一元弱酸,电离方程式为:HA H++A-,B正确;
C.乙反应后溶液的pH为7,c(OH-)=c(H+),根据电荷守恒可知c(Na+)=c(A-),C错误;
D.甲反应后溶液恰好生成NaA,溶液显碱性,所以NaA溶液中离子浓度的大小顺序为c(Na+)>c(A-)>
c(OH-)>c(H+),D正确;
答案为:C。
44.在水质检验中,测定水的硬度时,用到氨和氯化铵(NH ·HO~ NH Cl)缓冲溶液,控制溶液在pH=9.1左
3 2 4
右。则关于该缓冲溶液的说法正确的是
+
A.在缓冲溶液中,不可能有c(Cl- )>c(NH4 )>c(H+) >c(OH-)
+
B.在缓冲溶液中,一定有c(NH4) +c(NH ) =2c(Cl-)
3
C.在有效缓冲范围内,将缓冲溶液加水稀释时,pH基本不变
D.在缓冲溶液中,水的电离可能受到促进也可能受到抑制
【答案】AC
45.某二元酸(化学式用HA表示)在水中的电离方程式是:HA==H++HA-、HA-
H++A2-
2 2
回答下列问题:
(1)Na A溶液显____________(填“酸性”“中性”或“碱性”)。理由是____________(用离子方程式表示)。
2
(2)在0.1mol·L-1的NaA溶液中,下列粒子浓度关系式正确的是____________。
2
A.c(A2-)+c(HA-)+c(H A)=0.1mol·L-1 B.c(Na+)+c(OH-)=c(H+)+c(HA-)
2
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)已知0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1HA溶液中氢离子的物质的量浓度可能是
2
____________0.11mol·L-1(填“<”“>”或“=”),理由是____________。
(4)0.1mol·L-1NaHA溶液中各种离子浓度由大到小的顺序是____________。
【答案】碱性 A-+H
O
HA+OH- CD < HA发生完全电离生成的H+,对HA-的电离起
2 2
抑制作用 c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
【分析】
在电解质溶液中,电解质电离或水解产生的离子浓度(不包含水电离出的离子)间满足物料守恒关系;在电
解质溶液中,所有离子间满足电荷守恒关系。
【详解】
28 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(1)因为HA-在水溶液中发生部分电离,所以NaA在溶液中发生水解,溶液显碱性。理由是A-+H
O
2 2
HA+OH-。答案为:碱性;A-+H
O
HA+OH-;
2
(2)A.因为在溶液中HA发生完全电离,所以溶液中不存在HA,A不正确;
2 2
B.在溶液中存在A2-+H
O HA-+OH-和HOH++OH-,所以c(OH-)=c(H+)+c(HA-),B不正确;
2 2
C.依据电荷守恒,溶液中存在c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),C正确;
D.依据物料守恒,溶液中存在c(Na+)=2c(A2-)+2c(HA-),D正确;
故选CD;
(3)已知0.1mol·L-1NaHA溶液的pH=2,在酸性溶液中,HA-的电离程度减小,则0.1mol·L-1HA溶液中氢离
2
子的物质的量浓度可能是<0.11mol·L-1,理由是HA发生完全电离生成的H+,对HA-的电离起抑制作用。
2
答案为:<;HA发生完全电离生成的H+,对HA-的电离起抑制作用;
2
(4)0.1mol·L-1NaHA溶液中,发生如下电离:NaHA==Na++HA-,HA-H++A2-,HOH++OH-,所以
2
各种离子浓度由大到小的顺序是c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)。答案为:c(Na+)>c(HA-)>c(H+)>
c(A2-)>c(OH-)。
【点睛】
因为HA-在水溶液中发生部分电离,所以我们易错误地认为溶液中存在HA-的水解平衡
核心知识10 沉淀溶解平衡
46.常温下,将足量的AgCl固体分别放入下列液体中,AgCl溶解的量最小的是
A.20 ml蒸馏水 B.30mL 0.03mol/L HCl溶液
C.40mL 0.05mol/L AgNO 溶液 D.50mL 0.02mol/L CaCl 溶液
3 2
【答案】C
【分析】
AgCl饱和溶液中存在AgCl(aq) Ag+(aq)+Cl-(aq),AgCl的溶解度大小取决于溶液中c(Ag+)或c(Cl-),从平衡
移动的角度分析。 ⇌
【解析】
根据c(Ag+)或c(Cl-)大小比较AgCl的溶解度,c(Ag+)或c(Cl-)越大,AgCl的溶解度越小,
A.20mL蒸馏水,c(Ag+)或c(Cl-)为0;
B.30mL 0.03mol·L-1 HCl溶液中c(Cl-)= 0.03mol·L-1;
29 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司C.40mL 0.05mol·L-1 AgNO 溶液中c(Ag+)=0.05mol·L-1;
3
D.50mL 0.02mol·L-1 CaCl 溶液中c(Cl-)= 0.04mol·L-1。
2
则AgCl的溶解度最小是C;
故选:C。
噲垐��
47.常温下,某PbI 悬浊液中存在平衡PbI (s) Pb2+(aq)+2I-(aq),加入少量KI固体并完全溶解。下列
2 2
说法错误的是
A.溶度积常数K (PbI )减小 B.溶液中c(I-)增大
sp 2
C.沉淀溶解平衡向左移动 D.悬浊液中固体质量增大
【答案】A
【解析】
A.溶度积常数K (PbI )只与温度有关,温度不变,则K (PbI )不变,故A错误;
sp 2 sp 2
B.加入少量KI固体并完全溶解,平衡逆向移动,但移动减少的量远小于加入的量,所以溶液中c(I-)增大,
故B正确;
噲垐��
C.含有大量PbI 的饱和溶液中存在着平衡PbI (s) Pb2+(aq)+2I-(aq),加入KI溶液,c(I-)增大,沉淀
2 2
溶解平衡左移,故C正确;
D.溶液中c(I-)增大,沉淀溶解平衡向左移动,生成沉淀,所以悬浊液中固体质量增大,故D正确;
综上所述,答案为A。
48.下列说法不正确的是
Mg(OH) FeCl
A.向 2悬浊液中滴加 3溶液,生成红褐色沉淀
B.碳酸氢钠药片,该药是抗酸药,服用时喝些醋能提高药效
C.配制氯化铁溶液时需加入适量盐酸抑制水解
CaSO Na CO
D.水垢中的 4,可先用 2 3溶液处理,而后用酸除去
【答案】B
【详解】
Mg(OH) FeCl Mg(OH) Fe(OH)
A.向 2悬浊液中滴加 3溶液,可使 2转化为红褐色沉淀 3,A正确;
30 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司NaHCO
3
B.碳酸氢钠属于抗酸药,醋酸会与 反应,从而降低药效,B错误;
C.氯化铁为强酸弱碱盐,溶于水后易发生水解,为抑制水解,配制氯化铁溶液时需加入适量盐酸,C正
确;
D.水垢中的
CaSO
4,可先用
Na
2
CO
3溶液处理,发生反应
CaSO
4
+Na
2
CO 3 CaCO
3
Na
2
SO
4,将
CaSO CaCO CaCO
4转化为溶解度更小的 3,而后用酸除去 3,D正确。
故选B。
49.已知25℃时,RSO (s)+CO2-(aq) RCO(s)+SO 2-(aq)的平衡常数K=1.75×104,K (RCO)=2.80×10-9,下
4 3 3 4 sp 3
列叙述中正确的是 ⇌
A.25℃ 时,RSO 的K 约为4.9×10-5
4 sp
B.将浓度均为6×10-5mol/L的RCl 、NaCO 溶液等体积混合后可得到RCO 沉淀
2 2 3 3
C.向c(CO2-)=c(SO 2-)的混合液中滴加RCl 溶液,首先析出RSO 沉淀
3 4 2 4
D.相同温度下,RCO 在水中的K 大于在NaCO 溶液中的K
3 sp 2 3 sp
【答案】A
【解析】25℃时,RSO (s)+CO2-(aq) RCO(s)+SO 2-(aq)的平衡常数K=
4 3 3 4
⇌
c
SO2-
c
R2+
c
SO2-
K RSO
c CO 4 2- = c R2+ c CO 4 2 = K sp RCO 4 =1.75×104, K RSO =
3 3 sp 3 sp 4
1.75104K RCO =1.751042.80109=4.9105
sp 3 。
A. 根据上述计算分析,25℃ 时,RSO 的K 约为4.9×10-5,故A正确;
4 sp
B. 将浓度均为6×10-5mol/L的RCl 、NaCO 溶液等体积混合,则浓度变为原来的一半,混合后溶液中
2 2 3
c(R2+)=3×10-5mol/L,c(CO2-)=3×10-5mol/L,Q(RCO)= c(R2+)∙ c(CO2-)=3×10-5mol/L×3×10-5mol/L=9×10-10<
3 c 3 3
K (RCO)=2.80×10-9,不会产生RCO 沉淀,故B错误;
sp 3 3
C. RSO 、RCO 属于同类型且K (RSO ) > K (RCO),向c(CO2-)=c(SO 2-)的混合液中滴加RCl 溶液,首先
4 3 sp 4 sp 3 3 4 2
析出RCO 沉淀,故C错误;
3
D. K 只与温度有关,与浓度无关,相同温度下RCO 在水中的K 等于在NaCO 溶液中的K ,故D错误;
sp 3 sp 2 3 sp
答案选A。
【点睛】本题易错点在于D选项,K 也属于平衡常数,只与温度有关,与溶液中离子浓度大小无关。
sp
31 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司50.25℃时,
MnCO
3和
CaCO
3的沉淀溶解平衡曲线如图(
M2
代表
Mn2
或
Ca2
)所示。下列说法不正确的
是
CaCO
A.a点可表示 3的饱和溶液
CaCO
B.c点可表示 3的过饱和溶液,达新平衡时可到达b点
c(Mn2)c(CO2)1.61011
C.d点时溶液中存在 3 (忽略单位)
0.10molL1CaCl MnCO MnCO CaCO
D.用 2溶液浸泡足量 3,会有部分 3转化为 3
【答案】B
【详解】A.a点在CaCO 沉淀溶解平衡曲线上,可表示CaCO 的饱和溶液,A正确;
3 3
B.c点表示的是
CaCO
3的过饱和溶液,溶液中存在
CaCO
3
s Ca2aqCO
3
2aq
,平衡逆向移动,
c Ca2 c CO2
、 3 同时减小,达到新平衡后,无法到达b点,B错误;
CO2
C.d点在MnCO 的沉淀溶解平衡曲线上,根据图可知,c(Mn2+)·c( 3 )=4×10-6×4×10-6=1.6×10-11,C正确;
3
Ca2MnCO CaCO Mn2
D.虽然MnCO 的溶度积常数小于CaCO ,但是仍会发生反应 3 3 ,用
3 3
0.10molL−1CaCl 溶液浸泡足量MnCO ,相当于增大反应物浓度,平衡正向移动,会有部分碳酸锰转化为
2 3
碳酸钙,⋅ D正确;
故答案选B。
51.根据题目提供的溶度积数据进行计算并回答下列问题:
(1)已知25℃时,K [Mg(OH) ]=5.6×10﹣12;酸碱指示剂百里酚蓝变色的pH范围如下:
sp 2
pH <8.0 8.0~9.6 >9.6
32 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司颜色 黄色 绿色 蓝色
25℃时,在Mg(OH) 饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为___________。
2
(2)向50mL0.018mol•L﹣1的AgNO 溶液中加入50mL0.020mol•L﹣1的盐酸,生成沉淀。已知该温度下AgCl
3
的K =1.0×10﹣10,忽略溶液的体积变化,请计算:
sp
①完全沉淀后,溶液中c(Ag+)=___________。
②完全沉淀后,溶液的pH=___________。
③如果向完全沉淀后的溶液中继续加入50mL0.001mol•L﹣1的盐酸,是否有白色沉淀生成?___________(填
“是”或“否”)。
(3)在某温度下,K (FeS)=6.25×10﹣18,FeS饱和溶液中c(H+)与c(S2﹣)之间存在关系:c2(H+)•c(S2﹣)=1.0×10﹣
sp
22,为了使溶液里c(Fe2+)达到1mol•L﹣1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为
___________。
【答案】蓝色 1.0×10﹣7mol•L﹣1 2 否 4×10﹣3mol/L
【解析】
(1)25℃时,Mg(OH) 的溶度积K =5.6×10﹣12,根据Mg(OH) (s) Mg2+(aq)+2OH﹣(aq)可得:c(Mg2+)×c2(OH
2 sp 2
﹣)=5.6×10﹣12,设c(OH﹣)=2c(Mg2+)=xmol/L,则:0.5x×x2=5.6×1⇌0﹣12,解得:x=2.24×10﹣4mol/L,c(H+)=
1014
mol/L=4.5×10﹣11mol/L,溶液的pH=10.4>9.6,所以溶液呈蓝色,故答案为:蓝色;
2.24104
(2)①反应前,n(Ag+)=0.018mol•L﹣1×0.05L=0.9×10﹣3mol,n(Cl﹣)=0.020mol•L﹣1×0.05L=1×10﹣3mol;反应后
K
spAgCl
剩余的Cl﹣为0.1×10﹣3mol,则混合溶液中c(Cl﹣)=1.0×10﹣3mol•L﹣1,c(Ag+)= c Cl =1.0×10﹣7mol•L﹣1,故
答案为:1.0×10﹣7mol•L﹣1;
②H+没有参与反应,完全沉淀后,c(H+)=0.010mol•L﹣1,溶液的pH=2,故答案为:2;
2
③再向反应后的溶液中加入50mL0.001mol•L﹣1盐酸,不发生反应时c(Ag+)= ×1.0×10﹣7mol•L﹣1=0.67×10﹣
3
2
7mol•L﹣1、c(Cl﹣)= ×[(0.001+1.0×10﹣7+0.001]mol•L﹣1≈0.001mol•L﹣1,而离子浓度积Q=0.001×0.67×10﹣
3 c
7=0.67×10﹣10<K (AgCl)=1.0×10﹣10,所以没有沉淀产生,故答案为:否;
sp
K (FeS) 6.251018
sp =
(3)溶液中c(S2﹣)= c(Fe2+) 1 mol/L=6.25×10﹣18mol/L,c2(H+)•c(S2﹣)=1.0×10﹣22,则c(H+)=
33 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司11022
6.25101811022
6.251018 mol/L=4×10﹣3mol/L,故答案为:4×10﹣3mol/L。
52.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理
含砷废水,相关数据如表。
K
表1 几种砷酸盐的 sp
难溶物 K
sp
Ca AsO 6.81019
3 4 2
AlAsO 1.61016
4
FeAsO 5.71021
4
表2 工厂污染物排放浓度及允许排放标准
污染物 H SO As
2 4
浓度 28.42gL1 1.6gL1
排放标准 pH6~9 0.5mgL1
回答以下问题:
H SO molL1
2 4
(1)该工厂排放的废水中 的物质的量浓度为_______ 。
(2)若处理后的工厂废水中Al3 、 Fe3 的浓度均为1.0104molL1 ,则此时废水中 c AsO3 4 最大是_______
molL1。
H AsO MnO
3 3 2
(3)工厂排放出的酸性废水中的三价砷( ,弱酸)不易沉降,可投入 先将其氧化成五价砷(
H AsO
3 4,弱酸),写出该反应的离子方程式:_______。
(4)在处理含砷废水时采用分段式,先向废水中投入适量生石灰调节pH为2,再投入适量生石灰将pH调节
Ca AsO
为8左右,使五价砷以 3 4 2形式沉降。
①将pH调节为2时废水中有大量沉淀产生,沉淀主要成分的化学式为_______。
34 / 36
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司Ca AsO
②在pH调节为8左右才出现大量 3 4 2沉淀的原因为_______。
【答案】(1)0.29
5.71017
(2)
2H++MnO +H AsO =H AsO +Mn2++H O
(3) 2 3 3 3 4 2
CaSO H AsO pH AsO3- Ca AsO
(4) 4 3 4是弱酸,当溶液中 调节为8左右时 4 浓度增大, 3 4 2大量沉淀
28.42
【解析】(1)由题表2可知,该工厂排放的废水中
cH SO molL10.29molL1
;
2 4 98
(2)若处理后的工厂废水中 Al3 、 Fe3 的浓度均为 1.0104molL1 , K sp FeAsO 4