文档内容
高中化学人教版(2019)选择性必修1 第三章第四节 沉淀溶解平衡
一、单选题
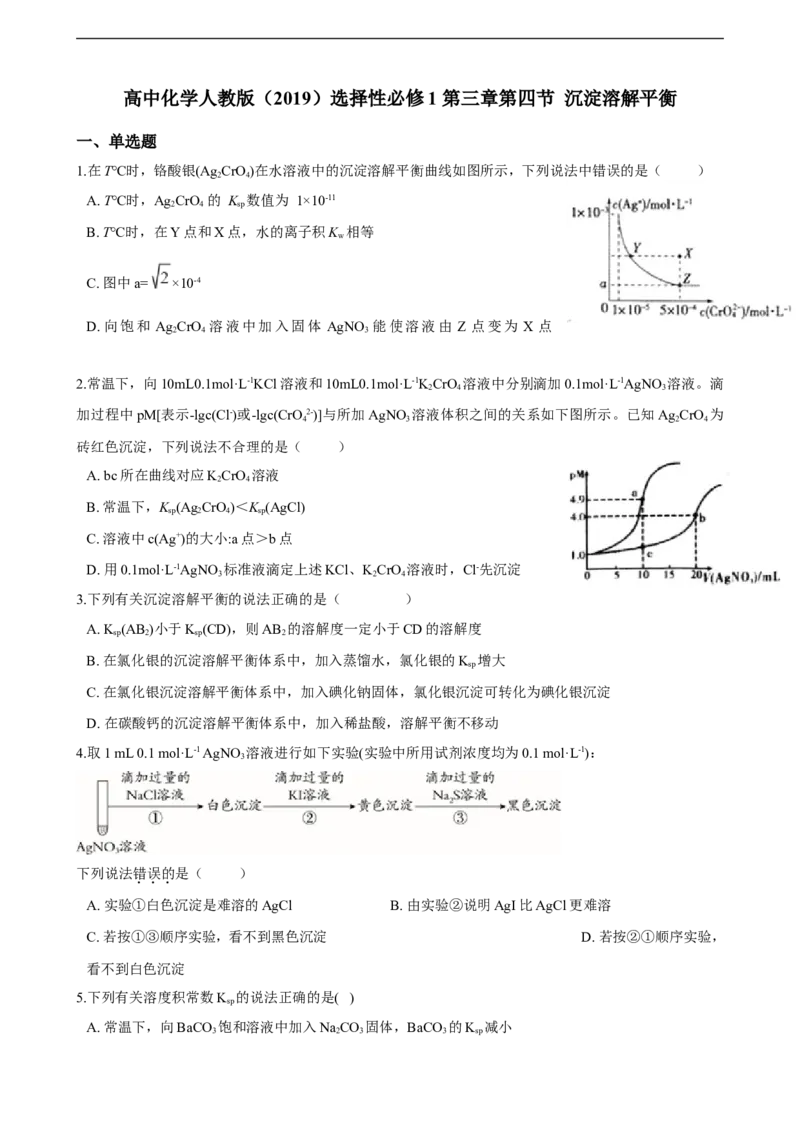
1.在T℃时,铬酸银(Ag CrO)在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中错误的是( )
2 4
A. T℃时,Ag CrO 的 K 数值为 1×10-11
2 4 sp
B. T℃时,在Y点和X点,水的离子积K 相等
w
C. 图中a= ×10-4
D. 向饱和 Ag CrO 溶液中加入固体 AgNO 能使溶液由 Z 点变为 X 点
2 4 3
21·cn·jy·com
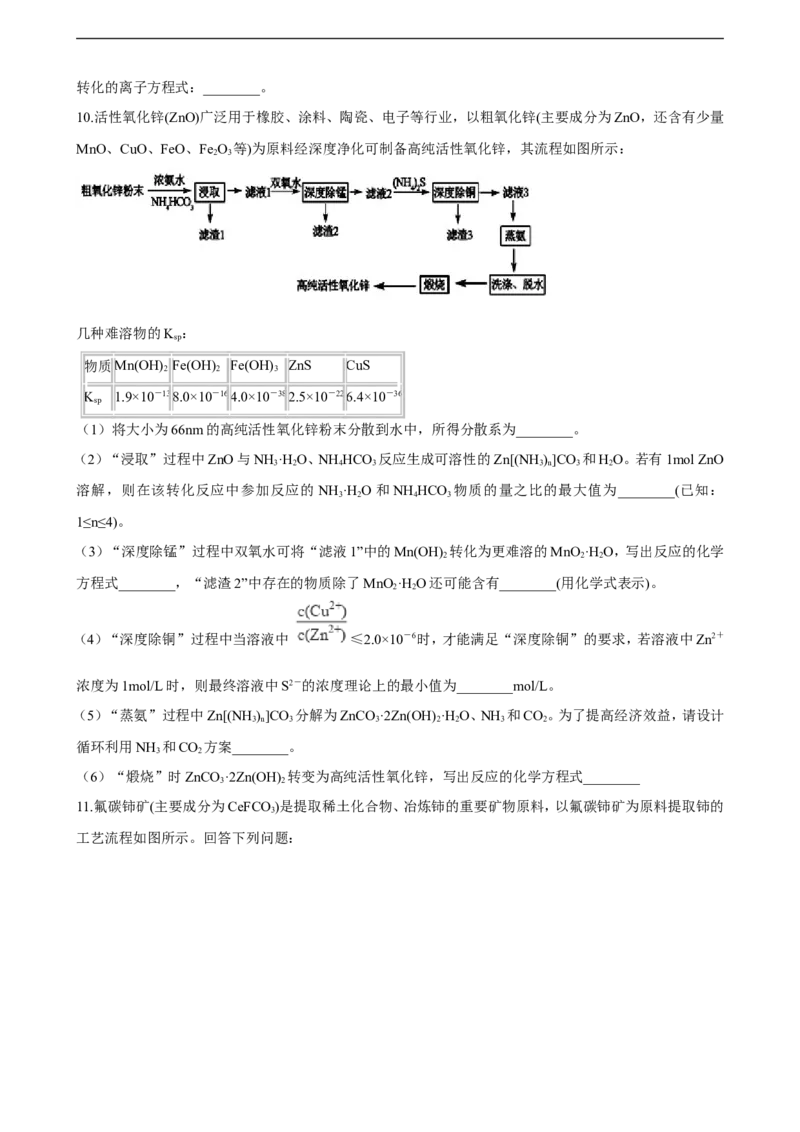
2.常温下,向10mL0.1mol·L-1KCl溶液和10mL0.1mol·L-1KCrO 溶液中分别滴加0.1mol·L-1AgNO 溶液。滴
2 4 3
加过程中pM[表示-lgc(Cl-)或-lgc(CrO 2-)]与所加AgNO 溶液体积之间的关系如下图所示。已知Ag CrO 为
4 3 2 4
砖红色沉淀,下列说法不合理的是( )
21*cnjy*com
A. bc所在曲线对应KCrO 溶液
2 4
B. 常温下,K (Ag CrO)<K (AgCl)
sp 2 4 sp
C. 溶液中c(Ag+)的大小:a点>b点
D. 用0.1mol·L-1AgNO 标准液滴定上述KCl、KCrO 溶液时,Cl-先沉淀
3 2 4
3.下列有关沉淀溶解平衡的说法正确的是( )
A. K (AB )小于K (CD),则AB 的溶解度一定小于CD的溶解度
sp 2 sp 2
B. 在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的K 增大
sp
C. 在氯化银沉淀溶解平衡体系中,加入碘化钠固体,氯化银沉淀可转化为碘化银沉淀
D. 在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动
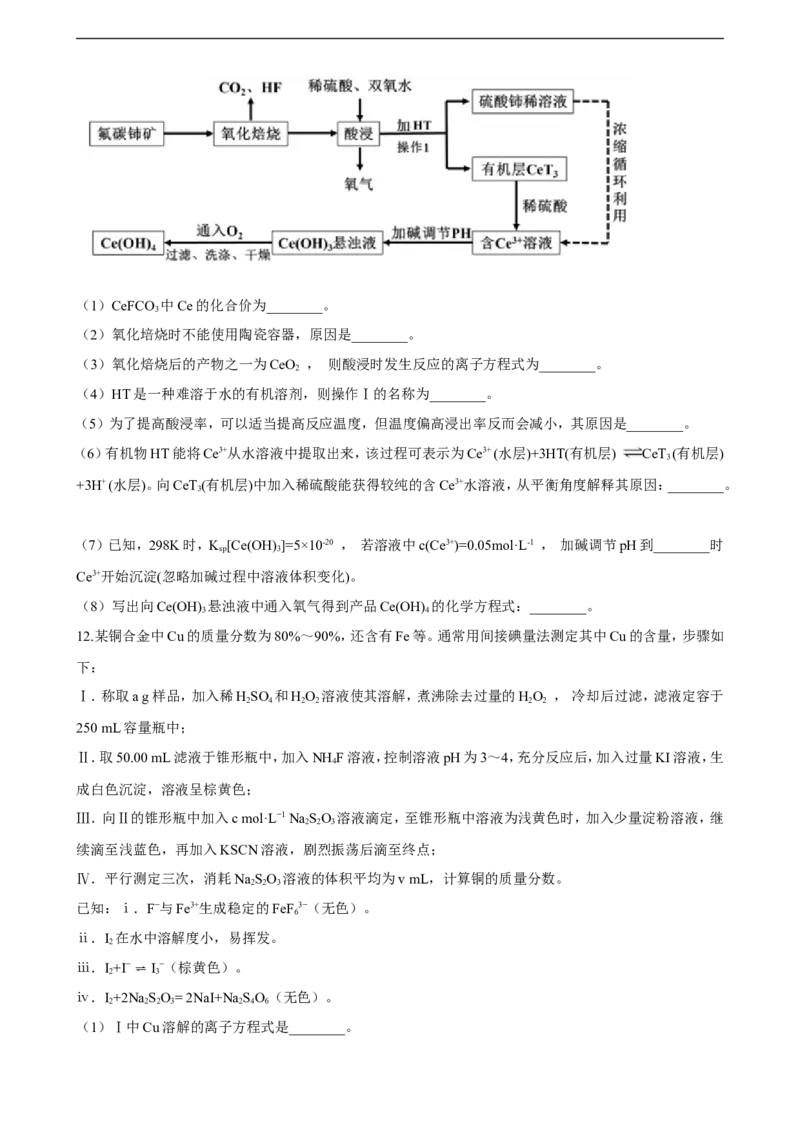
4.取1 mL 0.1 mol·L-1 AgNO 溶液进行如下实验(实验中所用试剂浓度均为0.1 mol·L-1):
3
下列说法错误的是( )
A. 实验①白色沉淀是难溶的AgCl B. 由实验②说明AgI比AgCl更难溶
C. 若按①③顺序实验,看不到黑色沉淀 D. 若按②①顺序实验,
看不到白色沉淀
5.下列有关溶度积常数K 的说法正确的是( )
sp
A. 常温下,向BaCO 饱和溶液中加入NaCO 固体,BaCO 的K 减小
3 2 3 3 spB. 溶度积常数K 只受温度影响,温度升高K 减小
sp sp
C. 溶度积常数K 只受温度影响,温度升高K 增大
sp sp
D. 常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的K 不变
2 2 sp
6.25℃时,在含有大量PbI 的饱和溶液中存在着平衡:PbI (s) Pb2+(aq)+2I-(aq),加入KI溶液,下列说法
2 2
正确的是( )
A. 溶液中Pb2+和I-浓度都增大 B.
溶度积常数K 增大
SP
C. 沉淀溶解平衡向左移动
D. 溶液中Pb2+浓度增大
7.已知K (AgCl)=1.8×10-10 , K (AgI)=1.5×10-16 , K (Ag CrO)=2.0×10-12 , 则下列难溶盐的饱和溶
sp sp sp 2 4
液中,Ag+浓度大小顺序正确的是( )
A. AgCl>AgI>Ag CrO B. AgCl>Ag CrO>AgI
2 4 2 4
C. Ag CrO>AgCl>AgI D. Ag CrO>AgI>AgCl
2 4 2 4
8.下列化学方程式中,不能正确表达反应颜色变化的是( )
A. 向 溶液中加入足量Zn粉,溶液蓝色消失:
B. 澄清的石灰水久置后出现白色固体:
C. 在空气中放置后由淡黄色变为白色:
D. 向 悬 浊 液 中 滴 加 足 量 溶 液 出 现 红 褐 色 沉 淀 :
二、综合题
9.某温度时,Ag SO 在水溶液中的沉淀溶解平衡曲线如图所示。请回答下列问题:
2 4
(1)A 点表示Ag SO 是________( 填“过饱和”“饱和”或“不饱和”)溶液。
2 4
(2)该温度下Ag SO 的溶度积常数 Ksp=________。(列式带入数据并计算出结果)
2 4
(3)现将足量的Ag SO 固体分别加入:
2 4
a.40mL0.01mol·L-1KSO 溶液
2 4
b.10 mL 蒸馏水
c.10mL0.02mol·L-1HSO 溶液。
2 4
则Ag SO 的溶解程度由大到小的顺序为________(填字母)。
2 4
(4)向Ag SO 悬浊液中加入足量NaCrO 固体,可观察到有砖红色沉淀生成(Ag CrO 为砖红色),写出沉淀
2 4 2 4 2 4转化的离子方程式:________。
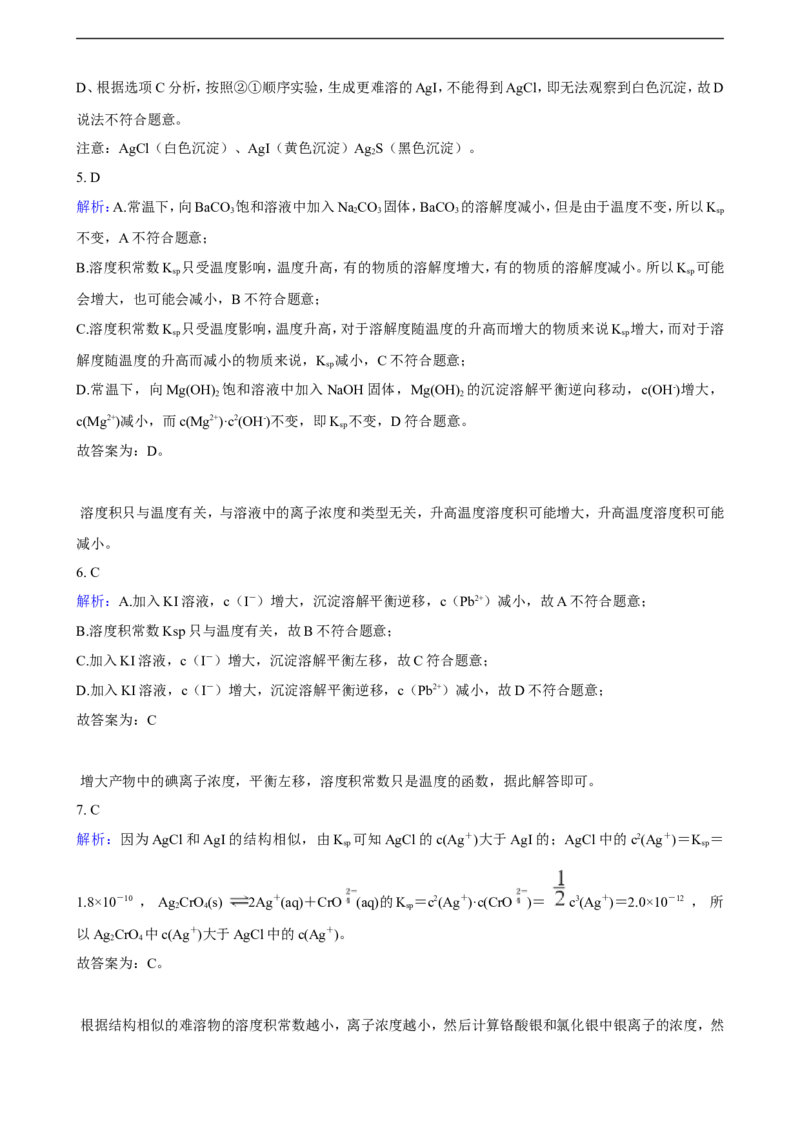
10.活性氧化锌(ZnO)广泛用于橡胶、涂料、陶瓷、电子等行业,以粗氧化锌(主要成分为ZnO,还含有少量
MnO、CuO、FeO、Fe O 等)为原料经深度净化可制备高纯活性氧化锌,其流程如图所示:
2 3
几种难溶物的K :
sp
物质Mn(OH) Fe(OH) Fe(OH) ZnS CuS
2 2 3
K 1.9×10-138.0×10-164.0×10-382.5×10-226.4×10-36
sp
(1)将大小为66nm的高纯活性氧化锌粉末分散到水中,所得分散系为________。
(2)“浸取”过程中ZnO与NH·H O、NH HCO 反应生成可溶性的Zn[(NH )]CO 和HO。若有1mol ZnO
3 2 4 3 3 n 3 2
溶解,则在该转化反应中参加反应的 NH ·H O和NH HCO 物质的量之比的最大值为________(已知:
3 2 4 3
1≤n≤4)。
2-1-c-n-j-y
(3)“深度除锰”过程中双氧水可将“滤液1”中的Mn(OH) 转化为更难溶的MnO ·H O,写出反应的化学
2 2 2
方程式________,“滤渣2”中存在的物质除了MnO ·H O还可能含有________(用化学式表示)。
2 2
(4)“深度除铜”过程中当溶液中 ≤2.0×10-6时,才能满足“深度除铜”的要求,若溶液中Zn2+
浓度为1mol/L时,则最终溶液中S2-的浓度理论上的最小值为________mol/L。
【来源:21cnj*y.co*m】
(5)“蒸氨”过程中Zn[(NH )]CO 分解为ZnCO ·2Zn(OH) ·H O、NH 和CO。为了提高经济效益,请设计
3 n 3 3 2 2 3 2
循环利用NH 和CO 方案________。
3 2
(6)“煅烧”时ZnCO ·2Zn(OH) 转变为高纯活性氧化锌,写出反应的化学方程式________
3 2
11.氟碳铈矿(主要成分为CeFCO)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的
3
工艺流程如图所示。回答下列问题:(1)CeFCO 中Ce的化合价为________。
3
(2)氧化培烧时不能使用陶瓷容器,原因是________。
(3)氧化焙烧后的产物之一为CeO , 则酸浸时发生反应的离子方程式为________。
2
(4)HT是一种难溶于水的有机溶剂,则操作Ⅰ的名称为________。
(5)为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是________。
(6)有机物HT能将Ce3+从水溶液中提取出来,该过程可表示为Ce3+ (水层)+3HT(有机层) CeT (有机层)
3
+3H+ (水层)。向CeT (有机层)中加入稀硫酸能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:________。
3
(7)已知,298K时,K [Ce(OH) ]=5×10-20 , 若溶液中c(Ce3+)=0.05mol·L-1 , 加碱调节pH到________时
sp 3
Ce3+开始沉淀(忽略加碱过程中溶液体积变化)。
(8)写出向Ce(OH) 悬浊液中通入氧气得到产品Ce(OH) 的化学方程式:________。
3 4
12.某铜合金中Cu的质量分数为80%~90%,还含有Fe等。通常用间接碘量法测定其中Cu的含量,步骤如
下:
Ⅰ.称取a g样品,加入稀HSO 和HO 溶液使其溶解,煮沸除去过量的HO , 冷却后过滤,滤液定容于
2 4 2 2 2 2
250 mL容量瓶中;
Ⅱ.取50.00 mL滤液于锥形瓶中,加入NH F溶液,控制溶液pH为3~4,充分反应后,加入过量KI溶液,生
4
成白色沉淀,溶液呈棕黄色;
Ⅲ.向Ⅱ的锥形瓶中加入c mol·L−1 Na SO 溶液滴定,至锥形瓶中溶液为浅黄色时,加入少量淀粉溶液,继
2 2 3
续滴至浅蓝色,再加入KSCN溶液,剧烈振荡后滴至终点;
Ⅳ.平行测定三次,消耗NaSO 溶液的体积平均为v mL,计算铜的质量分数。
2 2 3
已知:ⅰ.F−与Fe3+生成稳定的FeF3−(无色)。
6
ⅱ.I 在水中溶解度小,易挥发。
2
ⅲ.I 2 +I− ⇌ I 3 −(棕黄色)。
ⅳ.I+2Na SO= 2NaI+Na SO(无色)。
2 2 2 3 2 4 6
(1)Ⅰ中Cu溶解的离子方程式是________。(2)Ⅱ中Cu2+和I−反应生成CuI白色沉淀和I。
2
①加入NH F溶液的目的是________。
4
②Cu2+和I−反应的离子方程式是________。
③加入过量KI溶液的作用是________。
(3)室温时,CuSCN的溶解度比CuI小。CuI沉淀表面易吸附I 和I− , 使测定结果不准确。Ⅲ中,在滴定至
2 3
终点前加入KSCN溶液的原因是________。
21世纪教育网版权所有
(4)样品中Cu的质量分数为________(列出表达式)。
三、解答题
13.已知Cu(OH) 的K =2×10-20:某溶液中c(Cu2+)=0.02 mol·L-1 , 如要生成Cu(OH) 沉淀,应调整溶液
2 sp 2
的pH大于?(写步骤)
21·世纪*教育网答案解析部分
一、单选题
1. D
解析:A.依据图象数据,曲线上的点是沉淀溶解平衡的点,Ag
2
CrO
4
的沉淀溶解平衡为:Ag
2
CrO
4
(s)⇌2Ag+
+CrO ,K =c2(Ag+)•c(CrO )=(10-3)2×10-5=10-11 , 故A不符合题意;
sp
B.一定温度下水的离子积K 是常数,只随温度变化,不随浓度变化,所以T℃时,Y点和X点时水的离子积
w
K 相等,故B不符合题意;
w www.21-cn-jy.com
C.依据溶度积常数计算 K (Ag CrO)=c2(Ag+)•c(CrO )=1×10-11 , Z 点时 c(CrO )=5×10-4 , 则
sp 2 4
c(Ag+)2=2×10-8 , 所以a= ×10-4 , 故C不符合题意;
21教育名师原创作品
D.在饱和Ag
2
CrO
4
溶液中加入AgNO
3
固体,Ag
2
CrO
4
(s)⇌2Ag++CrO 平衡逆向移动,移动后,仍存在
Ag
2
CrO
4
(s)⇌2Ag++CrO ,点仍在曲线上,所以在饱和Ag
2
CrO
4
溶液中加入AgNO
3
固体不能使溶液由Z点
变为X点,故D符合题意;
故答案为:D。
铬酸银(Ag
2
CrO
4
)在水溶液中的沉淀溶解平衡方程式为Ag
2
CrO
4
(s)⇌2Ag++CrO ,结合K
sp
=c2(Ag+)•c(CrO )
分析解答。
2. C
解析:A.常温下,向10mL0.1mol•L-1KCl溶液和10mL0.1mol•L-1KCrO 溶液中分别滴加0.1mol•L-1AgNO 溶
2 4 3
液,当加入10mLAgNO 溶液时,KCl恰好完全反应,加入20mLAgNO 溶液时KCrO 恰好完全反应,因此a
3 3 2 4
点所在曲线表示KCl溶液中变化的曲线,b、c点所在曲线表示KCrO 溶液中的变化曲线,故A符合题意;
2 4
2·1·c·n·j·y
B.a点时恰好反应生成AgCl,由题图可知,此时-lgc(Cl-)=4.9,则溶液中c(Cl-)=1×10-4.9mol•L-1 , c(Ag+)=
,该温度下,K (AgCl)=c(Cl-)×c(Ag+)=1×10-9.8 , b点时恰好反应生成Ag (CrO ),由题图
sp 2 4
可知,此时-lgc(CrO 2-)=4.0,则溶液中c(CrO 2-)=1×10-4 mol•L-1 , c(Ag+)=2×10-4 mol•L-1 , 该温度下,
4 4
K (Ag CrO)=c(CrO 2-)×c2(Ag+)=4×10-12 , K (Ag CrO)<K (AgCl),故B符合题意;
sp 2 4 4 sp 2 4 sp
C.溶液中a点c(Ag+)=1×10-4.9mol•L-1 , b点c(Ag+)=2×10-4 mol•L-1 , 则a点<b点,故C不符合题意;D.用0.1mol·L-1AgNO 标准液滴定上述KCl、KCrO 溶液时,对于KCl溶液c(Ag+)= =
3 2 4
=1×10-8.8 mol•L-1 , 对于KCrO 溶液c(Ag+)= = =6.33×10-6 mol•L-1 , 则Cl-沉淀所需
2 4
Ag+浓度小,Cl-先沉淀,故D符合题意;
21cnjy.com
故答案为:C。
由反应Cl-+Ag+=AgCl↓和CrO2-+2Ag+=Ag CrO↓分析,10mL0.1mol•L-1KCl溶液和10mL 0.1mol•L-1KCrO 溶
4 2 4 2 4
液中分别滴加等浓度的AgNO 溶液,当加入AgNO10mL时Cl-恰好完全沉淀,当加入AgNO 20mL时,
3 3 3
CrO2-沉淀完全,据此分析反应对应曲线。
4
3. C
解析:A、因为Ksp(AB )=c(A2+)c2(B-)、Ksp(CD)=c(C+)c(D-),物质的组成和结构不相似,所以Ksp(AB )小于
2 2
Ksp(CD),AB 的溶解度不一定小于CD的溶解度,A不符合题意;
2
B、在氯化银的沉淀溶解平衡体系中,加入蒸馏水,减小了溶液中的Ag+、Cl-的浓度,溶解平衡正向移动,直
至达到新的条件下的溶解平衡状态。由于温度不变,所以氯化银的Ksp不变,B不符合题意;
C、在氯化银沉淀溶解平衡体系中,加入碘化钠固体,Ag+与加入的碘化钠电离产生的I-发生沉淀反应,生成
溶解度比AgCl沉淀更小的AgI沉淀,破坏了AgCl的沉淀溶解平衡,AgCl继续溶解电离,产生的Ag+再与I-
反应产生AgI沉淀,最终导致AgCl沉淀转化为碘化银沉淀,颜色由白色转化为黄色,C符合题意;
D、在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,发生反应:CO2-+2H+=CO ↑+H O,破坏了CaCO 的沉淀
3 2 2 3
溶解平衡,使它不断溶解,溶解产生的碳酸根离子继续与盐酸电离产生的H+发生反应,最终导致CaCO 完
3
全溶解,D不符合题意。
故答案为:C
A、溶解度还与各物质的相对分子质量有关;
B、溶度积常数在温度不变时为定值;
C、Ksp(AgBr)大于Ksp(Agl),两者之间可以实现转化;
D、在碳酸钙沉淀中存在如下溶解平衡:CaCO Ca2++CO 2- , 加入稀盐酸,平衡右移。
3 3
4. C
解析:A、AgNO 溶液中加入NaCl溶液,发生Ag++Cl-=AgCl↓,即实验①中白色沉淀是AgCl,故A说法不
3
符合题意;
B、实验②中加入过量KI溶液,出现黄色沉淀,说明产生AgI,即发生AgCl(s)+I-(aq)=AgI(s)+Cl-(aq),推
出AgI比AgCl更难溶,故B说法不符合题意;
C、实验③得到黑色沉淀,该黑色沉淀为AgS,推出Ag S比AgI更难溶,溶解度由大到小的顺序是
2 2
AgCl>AgI>Ag S,按①③顺序实验,能观察黑色沉淀,故C说法符合题意;
2D、根据选项C分析,按照②①顺序实验,生成更难溶的AgI,不能得到AgCl,即无法观察到白色沉淀,故D
说法不符合题意。
注意:AgCl(白色沉淀)、AgI(黄色沉淀)Ag S(黑色沉淀)。
2
5. D
解析:A.常温下,向BaCO 饱和溶液中加入NaCO 固体,BaCO 的溶解度减小,但是由于温度不变,所以K
3 2 3 3 sp
不变,A不符合题意;
B.溶度积常数K 只受温度影响,温度升高,有的物质的溶解度增大,有的物质的溶解度减小。所以K 可能
sp sp
会增大,也可能会减小,B不符合题意;
C.溶度积常数K 只受温度影响,温度升高,对于溶解度随温度的升高而增大的物质来说K 增大,而对于溶
sp sp
解度随温度的升高而减小的物质来说,K 减小,C不符合题意;
sp
D.常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的沉淀溶解平衡逆向移动,c(OH-)增大,
2 2
c(Mg2+)减小,而c(Mg2+)·c2(OH-)不变,即K 不变,D符合题意。
sp
故答案为:D。
溶度积只与温度有关,与溶液中的离子浓度和类型无关,升高温度溶度积可能增大,升高温度溶度积可能
减小。
6. C
解析:A.加入KI溶液,c(I-)增大,沉淀溶解平衡逆移,c(Pb2+)减小,故A不符合题意;
B.溶度积常数Ksp只与温度有关,故B不符合题意;
C.加入KI溶液,c(I-)增大,沉淀溶解平衡左移,故C符合题意;
D.加入KI溶液,c(I-)增大,沉淀溶解平衡逆移,c(Pb2+)减小,故D不符合题意;
故答案为:C
增大产物中的碘离子浓度,平衡左移,溶度积常数只是温度的函数,据此解答即可。
7. C
解析:因为AgCl和AgI的结构相似,由K 可知AgCl的c(Ag+)大于AgI的;AgCl中的c2(Ag+)=K =
sp sp
1.8×10-10 , Ag CrO(s) 2Ag+(aq)+CrO (aq)的K =c2(Ag+)·c(CrO )= c3(Ag+)=2.0×10-12 , 所
2 4 sp
以Ag CrO 中c(Ag+)大于AgCl中的c(Ag+)。
2 4 www-2-1-cnjy-com
故答案为:C。
根据结构相似的难溶物的溶度积常数越小,离子浓度越小,然后计算铬酸银和氯化银中银离子的浓度,然后进行比较即可。
8. C
解析:A.CuSO 溶液显蓝色,加入锌粉后,发生反应Zn+CuSO =ZnSO +Cu,反应后形成ZnSO 溶液,为无
4 4 4 4
色溶液,选项正确,A不符合题意;
【来源:21·世纪·教育·网】
B.空气中含有CO , 能与Ca(OH) 反应生成CaCO 沉淀,其反应的化学方程式为:Ca(OH) +CO=H O+
2 2 3 2 2 2
CaCO ↓,因此久置的澄清石灰水变浑浊,选项正确,B不符合题意;
3
C.空气中含有HO和CO , NaO 放置在空气中,易发生反应2NaO+2CO=2Na CO+O , NaO 为淡
2 2 2 2 2 2 2 2 3 2 2 2
黄色固体,NaCO 为白色,因此可观察到固体由淡黄色变为白色,选项错误,C符合题意;
2 3
D.由于Fe(OH) 的溶度积小于Mg(OH) 的溶度积,因此向Mg(OH) 悬浊液中加入FeCl 溶液,可发生反应
3 2 2 3
3Mg(OH) +2FeCl =2Fe(OH) +3MgCl , 因此可观察到有红褐色沉淀产生,选项正确,D不符合题意;
2 3 3 2
故答案为:C
根据物质发生的反应的化学方程式,分析其颜色变化。
二、综合题
9. (1)不饱和
(2)1.6×10-5(mol/L)3
(3)b>a>c
(4)Ag SO (s)+ =Ag CrO(s)+
2 4 2 4
解析:(1)A 点时,c(Ag+)=1×10-2mol/L,c( )=4×10-2mol/L,与A点c(Ag+)相同的曲线上的点相比,4×10-
2mol/L<16×10-2mol/L,所以A点未达沉淀溶解平衡,表示Ag SO 是不饱和溶液。答案为:不饱和;(2)该温度
2 4
下Ag SO 的溶度积常数 Ksp=c2(Ag+)∙c( )=(1×10-2mol/L)2×16×10-2mol/L =1.6×10-5(mol/L)3。答案为:
2 4
1.6×10-5(mol/L)3;(3)在饱和Ag SO 溶液中,c2(Ag+)∙c( )是一个定值,溶液中c( )越大,c(Ag+)越小,
2 4
a.40mL0.01mol·L-1KSO 溶液,c( )=0.01mol·L-1;
2 4
b.10 mL 蒸馏水,c( )=0;
c.10mL0.02mol·L-1HSO 溶液中,c( )=0.02mol·L-1;
2 4
在溶液中,c( ):c>a>b,则溶液中 c(Ag+):b>a>c,从而得出Ag SO 的溶解程度由大到小的顺序为
2 4
b>a>c。答案为:b>a>c;(4)向Ag SO 悬浊液中加入足量NaCrO 固体,生成Ag CrO 和NaSO , 沉淀转化
2 4 2 4 2 4 2 4的离子方程式:Ag SO (s)+ =Ag CrO(s)+ 。答案为:Ag SO (s)+ =Ag CrO(s)+ 。
2 4 2 4 2 4 2 4
某温度时,在Ag SO 沉淀溶解平衡曲线上每一点,都是该温度下的平衡点,所以利用浓度幂与沉淀溶解平
2 4
衡常数进行比较,可确定曲线外的某一点是否达到沉淀溶解平衡;利用沉淀溶解平衡常数,可由一种离子浓
度计算另一种离子的浓度。
10. (1)胶体
(2)3:1
(3)Mn(OH) +HO=MnO ·H O↓+HO;Fe(OH)
2 2 2 2 2 2 3
(4)3.2×10-30
(5)用水吸收NH 和CO 使之转化为NH HCO
3 2 4 3
(6)ZnCO ·2Zn(OH) 3ZnO+CO↑+2HO
3 2 2 2
解析:(1)分散质粒子高纯活性氧化锌粉末大小为66nm,在1 nm到100nm 之间,所得分散系为胶体;答案为:
胶体; (2) 按信息,“浸取”过程中反应:ZnO+(n-1)NH ·H O+NH HCO =Zn[(NH)]CO+nH O,在该转化反
3 2 4 3 3 n 3 2
应中,若有1mol ZnO溶解,则参加反应的NH ·H O和NH HCO 物质的量之比为(n-1):1,当n=4时,比值达最
3 2 4 3
大值;答案为:3:1; (3)按提供的反应物和生成物信息,“深度除锰”过程中双氧水把Mn(OH) 氧化得到
2
MnO ·H O沉淀,双氧水是绿色氧化剂,故该化学方程式为Mn(OH) +HO=MnO ·H O↓+HO;答案为:
2 2 2 2 2 2 2 2
Mn(OH) +HO=MnO ·H O↓+HO;从流程看,滤液1中含有亚铁,也被双氧水氧化为Fe(OH) 沉淀,故滤
2 2 2 2 2 2 3
渣中也含有氢氧化铁沉淀; 答案为:Fe(OH) ; (4)根据 ≤2.0×10-6、溶液中Zn2+浓度为1mol/L,则
3
c(Cu2+)≤2.0×10-6 , CuS的溶度积常数为6.4×10-36 , 则 ,
故S2-的浓度的最小值为3.2×10-30 mol/L ;
答案为:3.2×10-30 ; (5)要循环利用NH 和CO , 结合流程图中可知把它们转变为碳酸氢铵,故循环利用
3 2
NH 和CO 的方案为用水吸收NH 和CO 使之转化为NH HCO ;
3 2 3 2 4 3
答案为:用水吸收NH 和CO 使之转化为NH HCO ; (6)“煅烧”时ZnCO ·2Zn(OH) 转变为高纯活性氧化
3 2 4 3 3 2
锌,因为碳酸盐和不溶性碱或碱式盐受热分解生成金属氧化物、二氧化碳和水,则该反应方程式为
ZnCO ·2Zn(OH) 3ZnO+CO↑+2HO;
3 2 2 2 【版权所有:21教育】答案为:ZnCO ·2Zn(OH) 3ZnO+CO↑+2HO。
3 2 2 2
(1) 按分散质粒子高纯活性氧化锌粉末大小为66nm判断所得分散系类型;(2) 按“浸取”过程中提供的反
应物和生成物信息,书写方程式,据此判断在该转化反应中参加反应的NH ·H O和NH HCO 物质的量之比
3 2 4 3
的最大值; (3)按提供的反应物和生成物信息书写“深度除锰”过程中双氧水与 Mn(OH) 反应的化学方程
2
式,从流程和题给信息判断“滤渣2”其它的沉淀;(4)根据 ≤2.0×10-6、溶液中Zn2+浓度为1mol/L
以及溶度积常数,可求的最终溶液中S2-的浓度的最小值;(5)循环利用NH 和CO , 主要考虑氨水吸收二
3 2
氧化碳时生成什么物质,结合流程图中相关物质回答;(6)“煅烧”时ZnCO ·2Zn(OH) 转变为高纯活性氧化
3 2
锌,参考碳酸盐和不溶性碱或碱式盐受热分解的产物书写该反应的化学方程式;
11. (1)+3
(2)陶瓷会与生成的HF反应
(3)2CeO+H O+6H+ = 2Ce3++O ↑+4H O
2 2 2 2 2
(4)分液
(5)温度升高,双氧水发生分解,造成浸出率偏小
(6)向混合液中加入稀硫酸,使c(H+)增大,平衡向形成Ce3+水溶液方向移动
(7)8
(8)4Ce(OH) +O +2H O = 4Ce(OH)
3 2 2 4 21教育网
解析:(1)CeFCO 中CO2-整体显-2价,F显-1价,整个化合价代数和为0,推出Ce的价态为+3价;(2)
3 3
陶瓷容器中含有SiO , SiO 与HF发生反应:SiO+4HF=SiF↑+2HO,因此钙流程氧化焙烧时不能使用
2 2 2 4 2
陶瓷容器;(3)有机层中CeF , Ce显+3价,CeO 中Ce显+4价,即在酸浸时,Ce的价态降低,CeO 为氧
3 2 2
化剂,HO 为还原剂,离子方程式为2CeO+HO+6H+=2Ce3++O↑+4HO;(4)操作I得到溶液和有机相,
2 2 2 2 2 2 2
因此操作I的名称为分液;(5)根据流程,酸浸时加入HO , HO 在高温下发生分解,HO 与CeO 发生反
2 2 2 2 2 2 2
应时HO 的量减少,造成浸出率降低;(6)该过程中存在Ce3+ (水层)+3HT(有机层) CeT (有机层)+3H+
2 2 3
(水层),加入稀硫酸,c(H+)增大,平衡向逆反应方向进行,生成Ce3+的水溶液,能获得较纯含Ce3+水溶液;
( 7 ) Ce3 + 开 始 出 现 沉 淀 , c(Ce3 + )×c3(OH - )=K [Ce(OH) ] , 则 有 c(OH - )=
sp 3
mol·L-1=1×10-6mol·L-1 , 即当pH=8时Ce3+开始出现沉淀;(8)利用氧气将Ce(OH) 氧化成Ce(OH) , 其反应的方程式为4Ce(OH) +O+2HO=4Ce(OH) 。
3 4 3 2 2 4
(1)F为-1价,碳酸根为-2价;
(2)二氧化硅能与氢氟酸反应;
( 3)结合核心产物,根据氧化还原反应原理,方程式为 2CeO+H O+6H+ = 2Ce3++O ↑+4H O( 4)难溶于水
2 2 2 2 2
的有机溶剂,分离方法为分液;
(5)根据物质性质,高温下双氧水容易发生分解;
(6)增大氢离子浓度,平衡逆向移动;
(7)根据溶度积含义进行计算得出氢氧根离子浓度,进而计算pH值;
(8)结合核心产物,根据氧化还原反应原理,方程式为 4Ce(OH) +O +2H O = 4Ce(OH) 。
3 2 2 4
12. (1)Cu+H O+2H+=Cu2++2H O
2 2 2
(2)将溶液中的Fe3+转化为FeF3− , 防止其氧化I−;2Cu2++4I−=2CuI↓+I ;将Cu2+充分还原为CuI;I−与I 结合
6 2 2
生成I− , 减少I 的挥发
3 2
(3)将CuI沉淀转化为溶解度更小的CuSCN沉淀,释放出吸附的I 和I− , 提高测定结果的准确程度
2 3
(4)(63.5×5×cv×10−3× )×100%
解析:(1)Ⅰ中Cu在酸性条件下被双氧水氧化生成铜离子和水,离子反应方程式为:Cu+H O+2H+=Cu2+
2 2
+2H O; (2)①由于样品中含有少量铁单质,在酸性条件下被溶解为铁离子,铁离子具有氧化性也可与I−反
2
应,导致消耗I−的含量最大,使Cu含量测定不准确,根据题意,F−与Fe3+生成稳定的FeF3−(无色),加入NH F
6 4
溶液的目的是将溶液中的Fe3+转化为FeF3− , 防止其氧化I− , 确保Cu含量测定的准确性;②根据题意,
6
Cu2+和I−反应CuI白色沉淀和I , 离子方程式为:2Cu2++4I−=2CuI↓+I ;③加入过量KI溶液可确保将Cu2+充
2 2
分还原为CuI,同时过量的KI溶液可发生I 2 +I− ⇌ I 3 − , I−与I 2 结合生成I 3 − , 减少I 2 的挥发,提高Cu含量
测定的准确性;(3)因室温时,CuSCN的溶解度比CuI小,加入KSCN溶液,将CuI沉淀转化为溶解度更小的
CuSCN沉淀,转化过程中释放出吸附的I 和I− , I 充分被滴定,提高测定结果的准确程度;(4)根据2Cu2+
2 3 2
+4I−=2CuI↓+I 、I+2Na SO=2NaI+Na SO 可得:2Cu2+~ I ~ NaSO , 滴定50.00mL滤液过程中消耗
2 2 2 2 3 2 4 6 2 2 2 3
n(Na SO)=cmol·L−1×v×10-3L=cv×10-3mol,则n(Cu)= n(Cu2+)= 2n(Na SO)=2cv×10-3mol,则样品中Cu的质量
2 2 3 2 2 3
分数为= =(63.5×5×cv×10−3× )×100%。
(1)Ⅰ中Cu在酸性条件下被双氧水氧化生成铜离子和水; (2)①由于样品中含有少量铁单质,在酸性条件下
被溶解为铁离子,铁离子具有氧化性也可与I−反应,影响Cu含量测定的准确性;②根据题意,Cu2+和I−反应
CuI白色沉淀和I;③加入过量KI溶液可确保将Cu2+充分还原为CuI,提高Cu含量测定的准确性;(3)室温
2时,CuSCN的溶解度比CuI小,加入KSCN溶液可使沉淀发生转化,释放沉淀表面易吸附I 和I−;(4)根据
2 3
2Cu2++4I−=2CuI↓+I 、I+2Na SO= 2NaI+Na SO 可得:2Cu2+~ I ~ NaSO , 根据滴定消耗NaSO 计算
2 2 2 2 3 2 4 6 2 2 2 3 2 2 3
Cu2+的物质的量,再计算样品中Cu的质量分数。
三、解答题
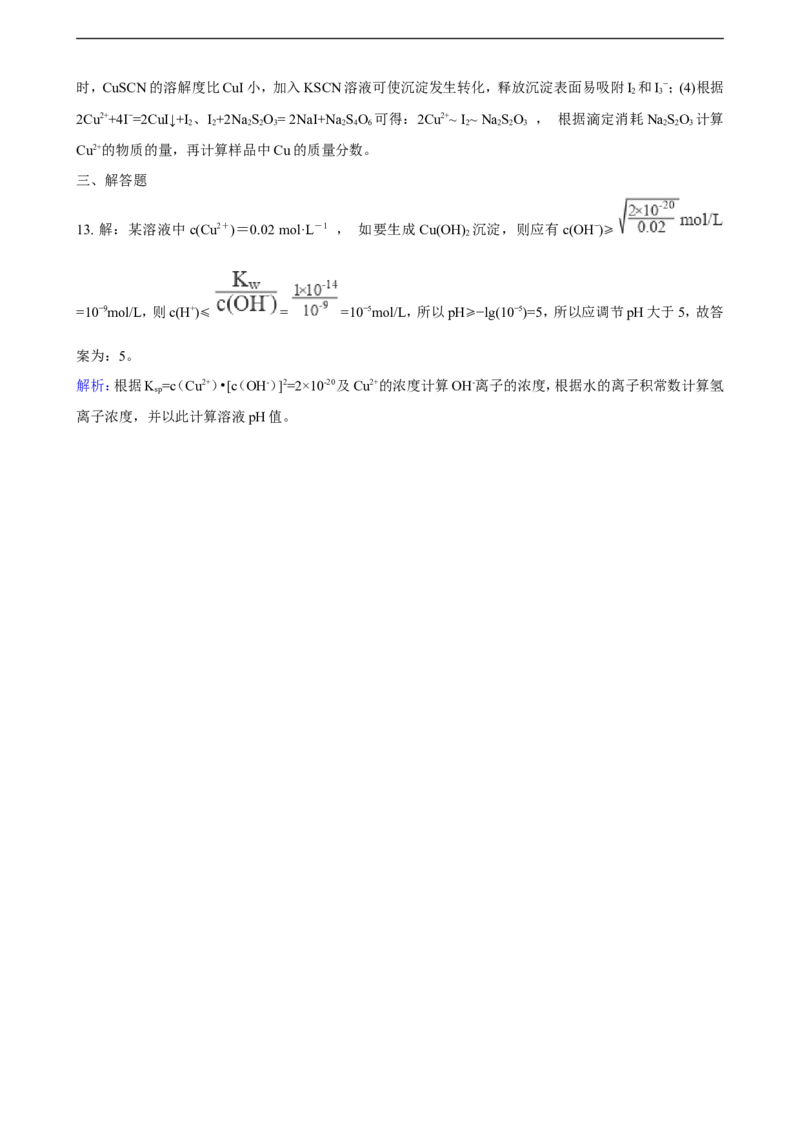
13. 解:某溶液中c(Cu2+)=0.02 mol·L-1 , 如要生成Cu(OH) 沉淀,则应有c(OH−)⩾
2
=10−9mol/L,则c(H+)⩽ = =10−5mol/L,所以pH⩾−lg(10−5)=5,所以应调节pH大于5,故答
案为:5。
【出处:21教育名师】
解析:根据K =c(Cu2+)•[c(OH-)]2=2×10-20及Cu2+的浓度计算OH-离子的浓度,根据水的离子积常数计算氢
sp
离子浓度,并以此计算溶液pH值。