文档内容
兰州一中 2024-2025-1 学期 10 月月考试题
高一化学
命题人:杨小敏 审题人:戴雅倩
说明:本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100分,考试时间75分钟。答案写
在答题卡上,交卷时只交答题卡。
第Ⅰ卷(选择题,42分)
一、单选题(每小题只有一个选项符合题意,每题3分,共42分)
1.下列说法不正确的是( )
A.侯德榜发明联合制碱法,为我国化学工业发展做出重要贡献
B.我国合成结晶牛胰岛素和核糖核酸,为人类揭开生命奥秘作出了贡献
C.英国科学家道尔顿提出分子学说,为近代化学的发展奠定了坚实的基础
D.俄国化学家门捷列夫发现了元素周期律,使化学的研究变得有规律可循
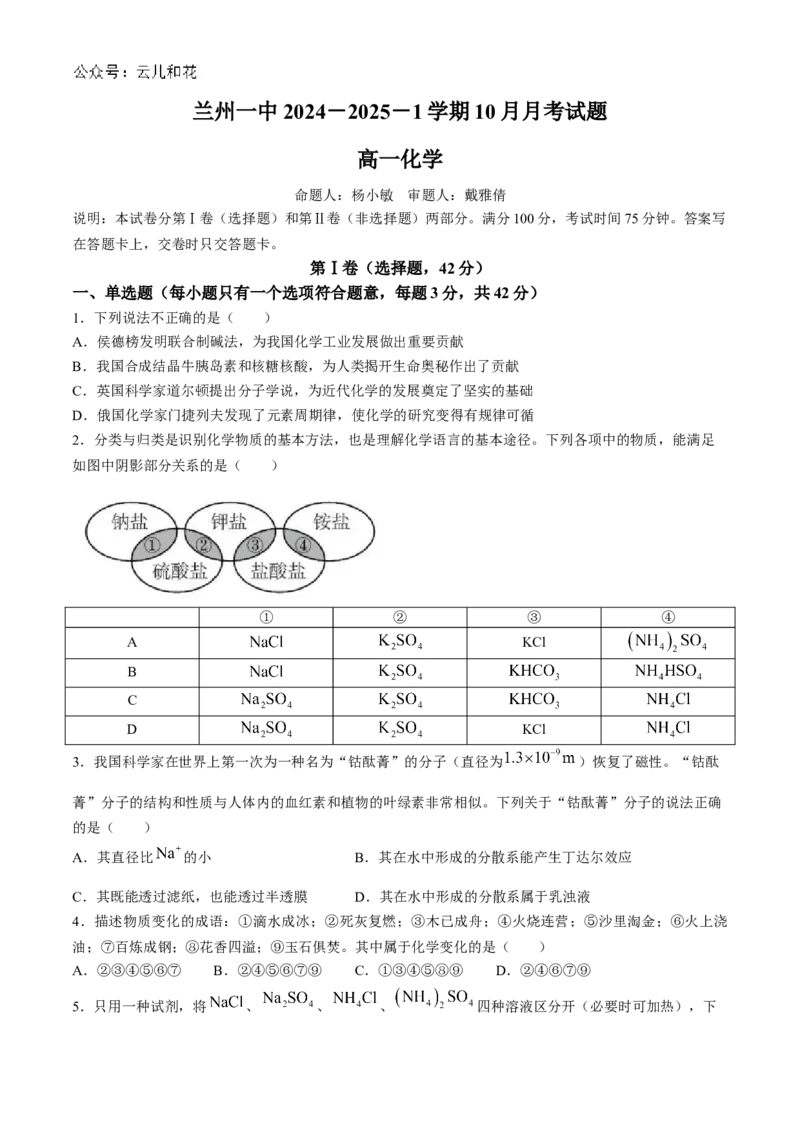
2.分类与归类是识别化学物质的基本方法,也是理解化学语言的基本途径。下列各项中的物质,能满足
如图中阴影部分关系的是( )
① ② ③ ④
A KCl
B
C
D KCl
3.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为 )恢复了磁性。“钴酞
菁”分子的结构和性质与人体内的血红素和植物的叶绿素非常相似。下列关于“钴酞菁”分子的说法正确
的是( )
A.其直径比 的小 B.其在水中形成的分散系能产生丁达尔效应
C.其既能透过滤纸,也能透过半透膜 D.其在水中形成的分散系属于乳浊液
4.描述物质变化的成语:①滴水成冰;②死灰复燃;③木已成舟;④火烧连营;⑤沙里淘金;⑥火上浇
油;⑦百炼成钢;⑧花香四溢;⑨玉石俱焚。其中属于化学变化的是( )
A.②③④⑤⑥⑦ B.②④⑤⑥⑦⑨ C.①③④⑤⑧⑨ D.②④⑥⑦⑨
5.只用一种试剂,将 、 、 、 四种溶液区分开(必要时可加热),下列试剂中可选用的是( )
A. 溶液 B. 溶液 C. 溶液 D.NaOH溶液
6. 作为一种广谱型的消毒剂,将逐渐取代 成为自来水的消毒剂。可用氯酸钠和双氧水在酸性条
件下制备,反应方程式为: ,下列说法
不正确的是( )
A. 的还原性强于
B. 在反应中被还原
C.1个 参加反应,转移2个电子
D.该反应的离子方程式为:
7.现有某无色透明溶液,可能含有 、 、 、 、 、 、 中的几种,每种离
子的个数相等,依次进行下列实验,且每步所加试剂均过量:
①取少量溶液滴加 溶液,有沉淀产生,加入足量盐酸后沉淀全部溶解;
②取①中的溶液再滴加 溶液,有白色沉淀生成
③加入足量NaOH溶液加热有气体放出(查资料可知, )
下列结论正确的是( )
A.可能含有的离子是 、 B.可能含有 、
C.肯定含有的离子是 、 、 D.一定含有的离子是 、
8.下列各组离子不能大量共存的是( )
A.使石蕊变红的溶液中: 、 、 、 B.酸性溶液中: 、 、 、
C.澄清透明的溶液中: 、 、 、 D.含有 的溶液中: 、 、 、9.下列说法中正确的是( )
①酸性氧化物在一定条件下均能与碱发生反应;
②金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物;
③氯化钠溶液在电流作用下电离成钠离子和氯离子;
④硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
⑤因为胶粒比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来;
⑥使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固(利用胶体的性质)而减少失血
A.3个 B.4个 C.5个 D.6个
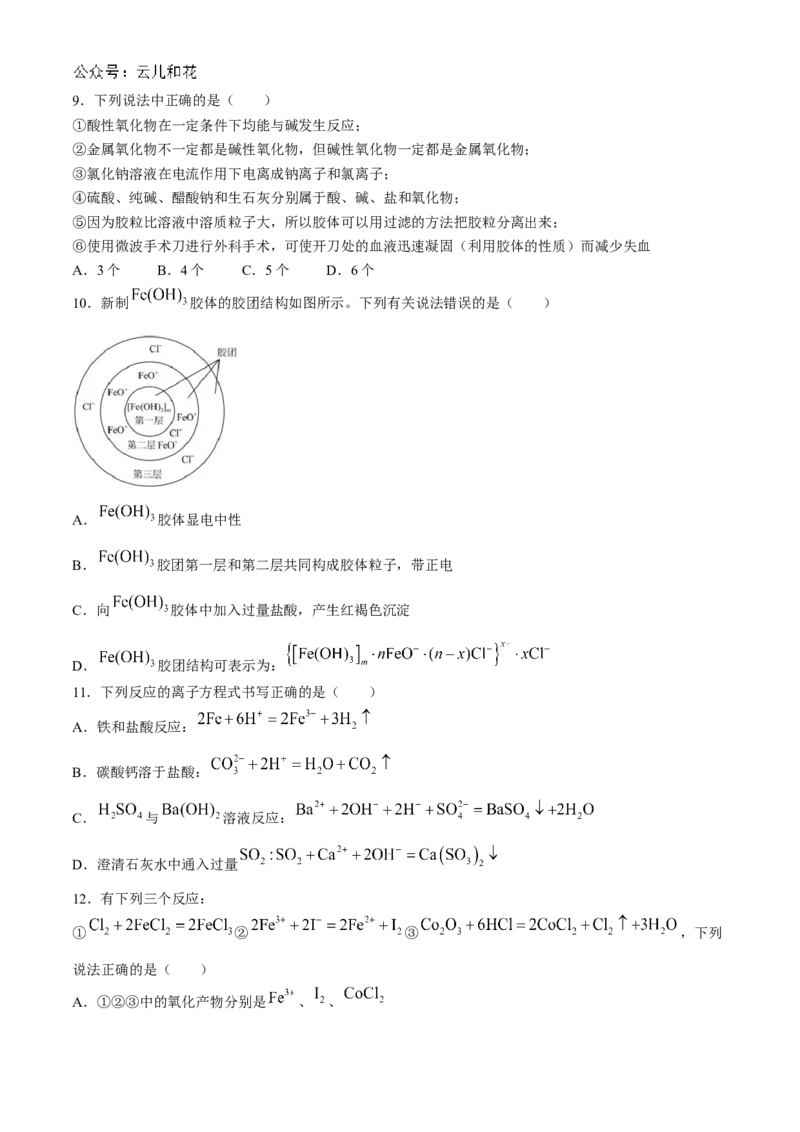
10.新制 胶体的胶团结构如图所示。下列有关说法错误的是( )
A. 胶体显电中性
B. 胶团第一层和第二层共同构成胶体粒子,带正电
C.向 胶体中加入过量盐酸,产生红褐色沉淀
D. 胶团结构可表示为:
11.下列反应的离子方程式书写正确的是( )
A.铁和盐酸反应:
B.碳酸钙溶于盐酸:
C. 与 溶液反应:
D.澄清石灰水中通入过量
12.有下列三个反应:
① ② ③ ,下列
说法正确的是( )
A.①②③中的氧化产物分别是 、 、B.氧化性
C.根据反应①②可以推测反应: 不能发生
D.在反应③中当HCl做还原剂,在反应过程中全部被氧化
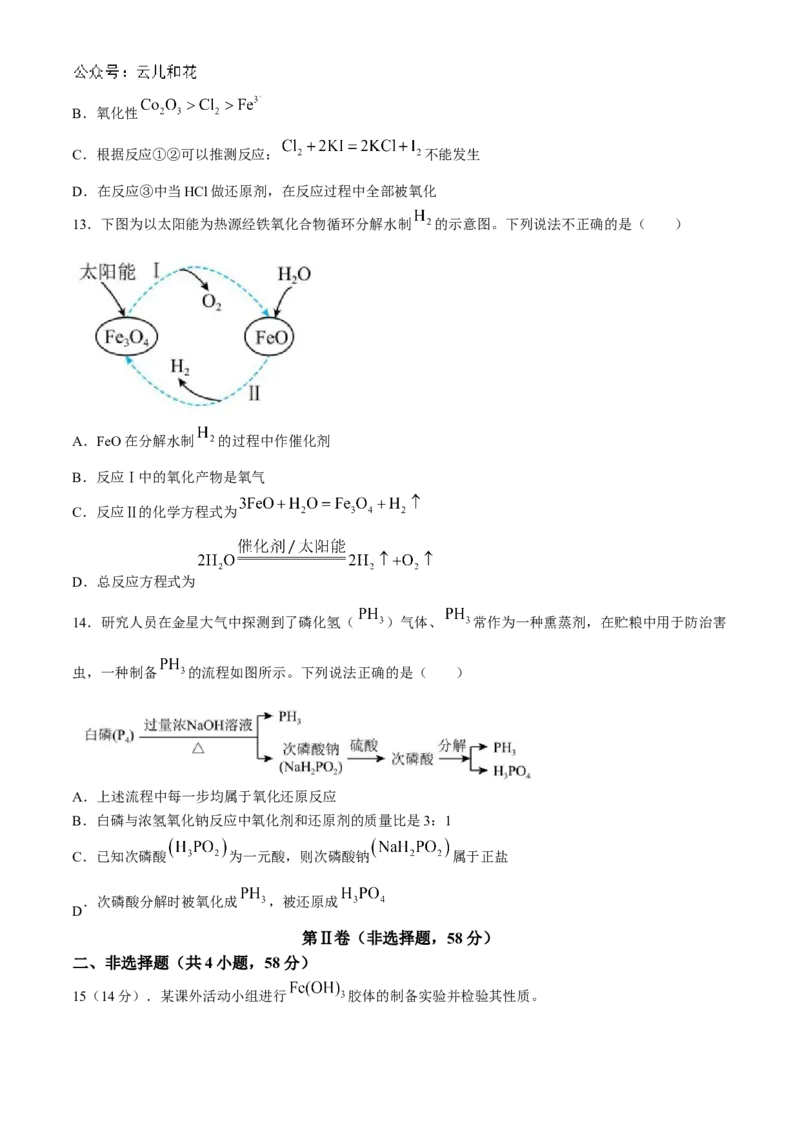
13.下图为以太阳能为热源经铁氧化合物循环分解水制 的示意图。下列说法不正确的是( )
A.FeO在分解水制 的过程中作催化剂
B.反应Ⅰ中的氧化产物是氧气
C.反应Ⅱ的化学方程式为
D.总反应方程式为
14.研究人员在金星大气中探测到了磷化氢( )气体、 常作为一种熏蒸剂,在贮粮中用于防治害
虫,一种制备 的流程如图所示。下列说法正确的是( )
A.上述流程中每一步均属于氧化还原反应
B.白磷与浓氢氧化钠反应中氧化剂和还原剂的质量比是3:1
C.已知次磷酸 为一元酸,则次磷酸钠 属于正盐
.次磷酸分解时被氧化成 ,被还原成
D
第Ⅱ卷(非选择题,58分)
二、非选择题(共4小题,58分)
15(14分).某课外活动小组进行 胶体的制备实验并检验其性质。(1)现有甲、乙、丙三名同学进行 胶体的制备。
①甲同学的操作是:直接加热饱和 溶液。
②乙同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入 饱和溶
液,继续煮沸至混合液呈红褐色,停止加热。
③丙同学的操作是:向沸水中滴加饱和 溶液,为了使反应进行充分,煮沸30min。
你认为______同学的制备方法更合理,制备时证明有 胶体生成的方法是______。上述制备
胶体时发生反应的化学方程式为______。
(2) 胶体区别于 溶液最本质的特征是______(填字母)。
A. 胶体为红褐色 B. 胶体粒子的直径在
C. 胶体是均一的分散系 D. 胶体的分散质能透过滤纸
(3)提纯所制 胶体常用的方法是______。
(4)将制得的胶体放入半透膜制成的袋内,如图所示,放置 后,取少量半透膜外的烧杯内液体于试
管中,置于暗处,用一束强光从侧面照射,观察到______(填“有”或“无”)光亮的“通路”;再向试
管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为______,发生反应的离子方程式为______。
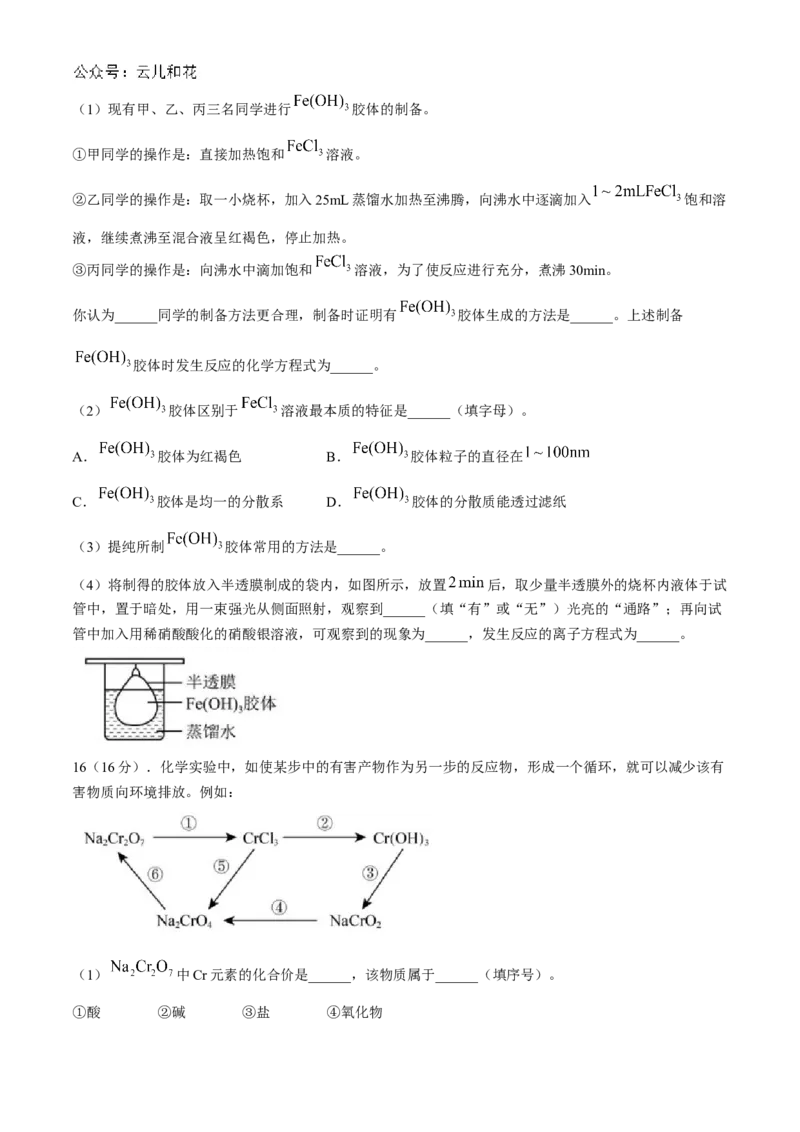
16(16分).化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可以减少该有
害物质向环境排放。例如:
(1) 中Cr元素的化合价是______,该物质属于______(填序号)。
①酸 ②碱 ③盐 ④氧化物(2)在上述转化中,Cr元素化合价不变的步骤是______(填序号)。
(3)反应①为: (未配平)。其中还原剂为______,还
原产物为______。 与 的反应系数比为______。
(4)完成反应④的配平,并用单线桥标出电子转移的方向和数目。(系数若为1也请写出)
④为:______ ______ ______ =______ ______ ______
反应
17(14分).有下列物质:① 固体;②熔融的 ;③ ;④稀硫酸;⑤ ;⑥铜;
⑦氨水;⑧蔗糖晶体;⑨ 固体;⑩ 。
(1)上述状态下的物质可导电的是______(填序号,下同)。
(2)属于电解质的是______,属于非电解质的是______。
(3)写出 在水溶液中的电离方程式:______。
(4)写出①的溶液与②的溶液恰好中和时的离子方程式:______。
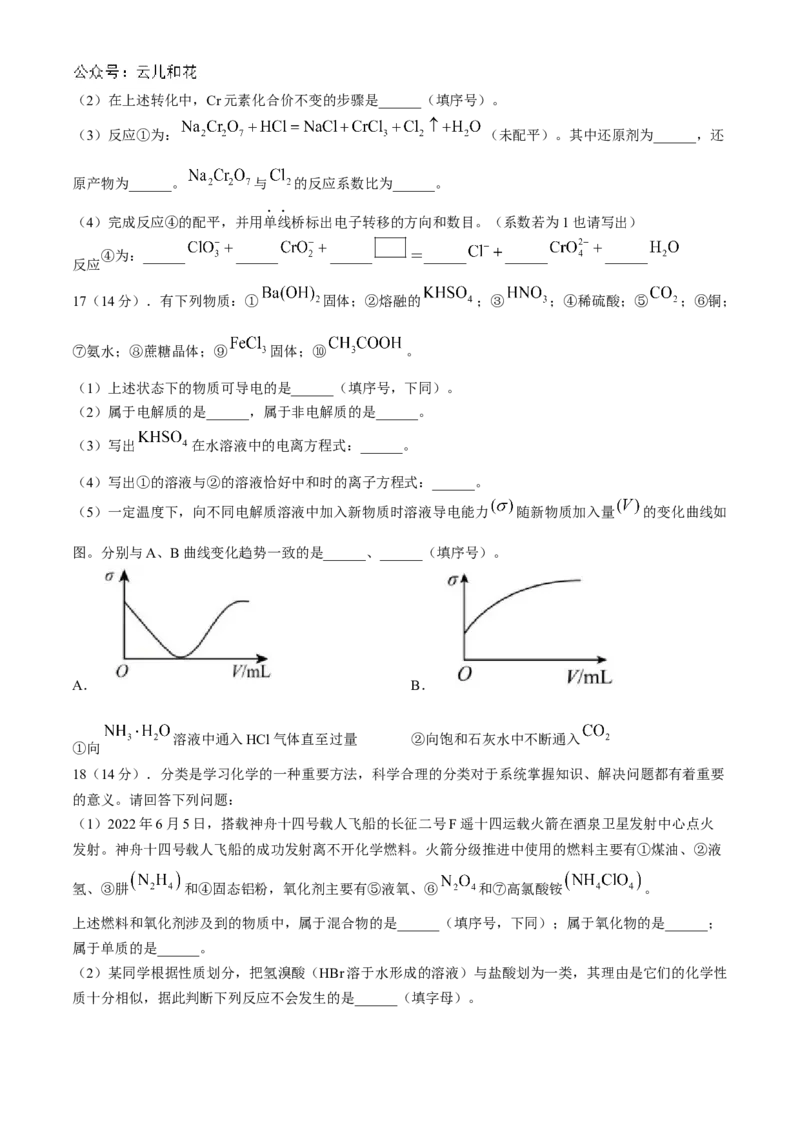
(5)一定温度下,向不同电解质溶液中加入新物质时溶液导电能力 随新物质加入量 的变化曲线如
图。分别与A、B曲线变化趋势一致的是______、______(填序号)。
A. B.
溶液中通入HCl气体直至过量 ②向饱和石灰水中不断通入
①向
18(14分).分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、解决问题都有着重要
的意义。请回答下列问题:
(1)2022年6月5日,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭在酒泉卫星发射中心点火
发射。神舟十四号载人飞船的成功发射离不开化学燃料。火箭分级推进中使用的燃料主要有①煤油、②液
氢、③肼 和④固态铝粉,氧化剂主要有⑤液氧、⑥ 和⑦高氯酸铵 。
上述燃料和氧化剂涉及到的物质中,属于混合物的是______(填序号,下同);属于氧化物的是______;
属于单质的是______。
(2)某同学根据性质划分,把氢溴酸(HBr溶于水形成的溶液)与盐酸划为一类,其理由是它们的化学性
质十分相似,据此判断下列反应不会发生的是______(填字母)。A. B.
C. D.
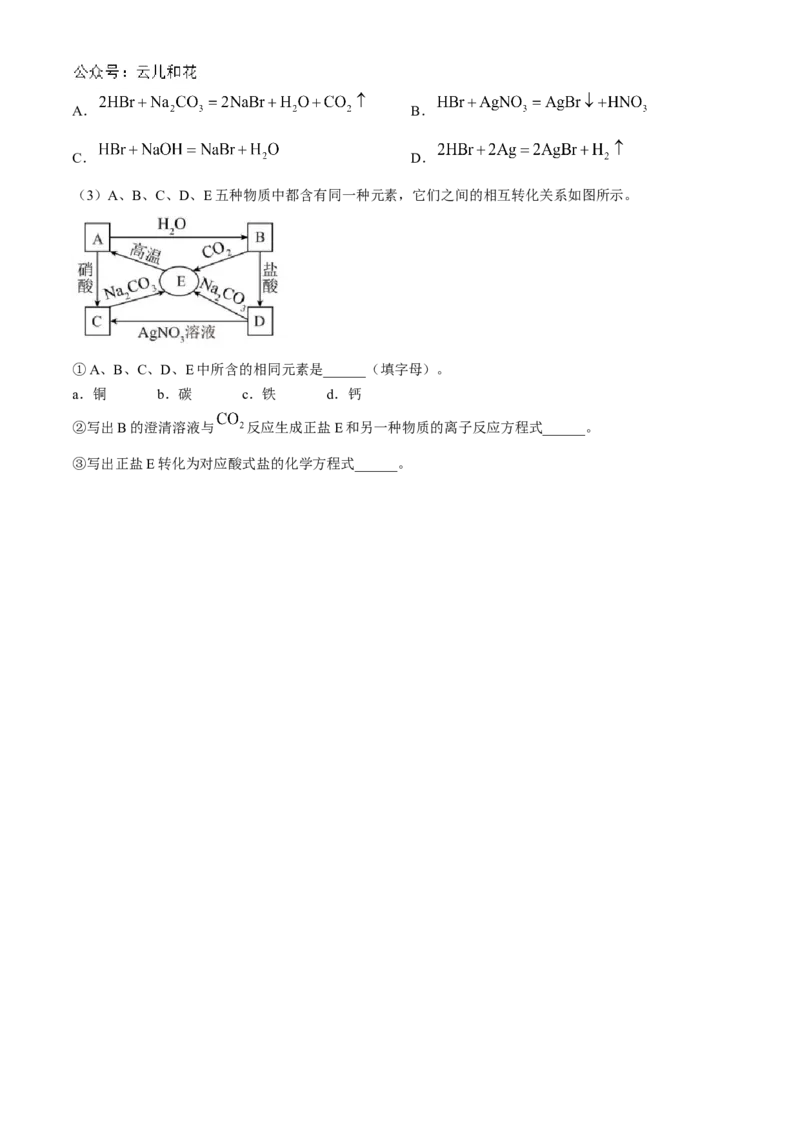
(3)A、B、C、D、E五种物质中都含有同一种元素,它们之间的相互转化关系如图所示。
①A、B、C、D、E中所含的相同元素是______(填字母)。
a.铜 b.碳 c.铁 d.钙
②写出B的澄清溶液与 反应生成正盐E和另一种物质的离子反应方程式______。
③写出正盐E转化为对应酸式盐的化学方程式______。兰州一中 2024-2025-1 学期 10 月月考答案
高一化学
一、选择题(每小题3分,共14小题,42分)
题号 1 2 3 4 5 6 7 8 9 10
答案 C D B D A C C B A C
题号 11 12 13 14
答案 C B A C
二、非选择题(共4小题,58分)
15(除标记外,每空2分,共14分)
(1)乙(1分) 丁达尔效应(1分)
(2)B (3)渗析
4)无 有白色沉淀生成
(
16(除标记外,每空2分,共16分)
(1)+6 ③
(2)②③⑥(多写不给分,少写扣一分)
(3)
(4) (4分,配平2分,单线桥2分,题目要求系数若为1也请写出。)
17(每空2分,共14分)
(1)②④⑥⑦(多写不给分,少写扣一分)
(2)①②③⑨⑩(多写不给分,少写扣一分) ⑤⑧(多写不给分,少写扣一分)
(3)
(4)
(5)② ①
18(每空2分,共14分)
(1)① ⑥ ②④⑤(多写不给分,少写扣一分) (2)D
3)d
(