文档内容
人教版(2019)高一必修第一册 第三章 铁 金属材料 第二
节 金属材料
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.关于合金的说法不正确的是
A.青铜是我国使用最早的合金 B.钢是用量最大、用途最广的合金
C.古代常用金属铁铸造货币 D.焊锡中加入铅是为了降低熔点
2.下列金属用途和有关性质的对应关系错误的是
金属用途 金属的有关性质
A 金可以制成比纸还薄的金箔 延展性
B 生活用铁锅 导热性
C 用铁回收照相定影废液中的银 氧化性
D 用铜制作印刷电路 导电性
A.A B.B C.C D.D
3.铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应
关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应的离子
方程式书写正确的是
A.OH−+HCl=H O+Cl− B.Ca(OH) +Cu2+=Ca2++Cu(OH)
2 2 2
C.Fe+Cu2+=Cu+Fe2+ D.Fe+2H+=Fe3++H ↑
2
4.2021年11月7日,王亚平身着我国新一代“飞天”舱外航天服成功出舱,下列
“飞天”舱外航天服使用的材料中,不属于有机物的是
A.棉布 B.橡胶 C.涤纶 D.铝合金
5.合金材料在生活中有广泛用途,下列属于合金的是
A.钢铁 B.石墨 C.水银 D.金刚石
6.广东文物资源丰富,文物是承载中华文化的血脉。广东博物馆内以下文物主要是由
合金制成的是选
A B C D
项
文
物
名 五代岳州窑青釉 清象牙雕空雕八仙福
北宋木雕罗汉像 西周信宜铜蚕
称 莲瓣纹小口瓶 寿提梁盒
A.A B.B C.C D.D
7.下列叙述错误的是
A.碳酸氢钠可用于治疗胃酸过多的药物
B.明矾溶于水形成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化
3
C.二氧化硫有漂白性,可以用来漂白食物
D.常温下,用铁、铝制容器来盛装浓硝酸
8.下列关于金属的叙述中正确的是
A.金属元素的原子只有还原性,离子只有氧化性
B.含金属元素的离子不一定都是阳离子
C.“真金不怕火炼”是指金的熔点高
D.金属元素单质在常温下均为固体
9.固体单质A和气体单质B在容积一定的密闭容器中恰好完全反应生成气体C,同温
下测得容器内压强不变,且反应后气体C的密度是原气体密度的4倍。则下列判断正
确的是( )
A.B,C两种气体的摩尔质量之比为4:1
B.生成物C中A元素的质量分数为75%
C.生成物C中A、B的原子个数之比为3∶1
D.反应前后气体分子数之比为1∶4
10.铝分别与足量的稀硫酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况
体积相等时,反应中消耗的HSO 和NaOH物质的量之比为( )
2 4
A.1:4 B.2:3 C.3:2 D.4:1
11.120℃时,将2LHO、1LCO、1LO 和2LCO 组成的混合气体依次缓慢通过分别装
2 2 2
有过量炽热铜粉、过量过氧化钠的两个反应管并充分反应,恢复到原来的温度和压强
试卷第2页,共3页后得到的气体是( )
A.O B.O 和CO C.H、O 和CO D.H 和O
2 2 2 2 2 2
12.下列反应的离子方程式书写正确的是
A.稀硫酸滴在铜片上:Cu+2H+=Cu2++H ↑
2
B.氧化镁溶于盐酸:MgO + 2H+ = Mg2+ + H O
2
C.稀硝酸滴在大理石上:CO + 2H+ = H O + CO↑
2 2
D.氢氧化钡溶液与硫酸铜溶液混合:Ba2+ + SO = BaSO↓
4
13.下列离子方程式中正确的是
A.用氯气作为水的消毒剂:Cl+H O=2H++Cl-+ClO-
2 2
B.用Cl 除去FeCl 溶液中的FeCl :Cl+2Fe2+=2Fe3++2Cl-
2 3 2 2
C.用小苏打治疗胃酸过多:CO +2H+=CO ↑+H O
2 2
D.胃药里含氢氧化铝能降低胃酸:OH-+H+=H O
2
14.下列说法错误的是
A.铝合金大量用于高铁建设
B.“玉兔二号”钛合金筛网轮的主要成分是非金属材料
C.制饭勺、饭盒,高压锅等的不锈钢是合金
D.商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎属于铜合金制品
15.下列物质中,不属于铁合金的是( )
A.球墨铸铁 B.不锈钢 C.锰钢 D.氧化铁
16.科技改变生活。下列说法不正确的是
A.国产大飞机C919机壳采用的铝锂合金,具备耐腐蚀性
B.“天宫课堂”实验乙酸钠过饱和溶液结晶形成温热“冰球”,该过程发生吸热反应
C.“嫦娥五号”使用的锂离子电池组,可将化学能转变成电能
D.国家速滑馆“冰丝带”采用 超临界制冰,比氟利昂制冰更加环保
17.下列实验与物质微粒大小无直接关系的是
A.丁达尔效应 B.渗析C.萃取 D.过滤
18.下列试剂中,能用来分离 和 的是
A. 溶液 B. 溶液 C.氨水 D.食盐水
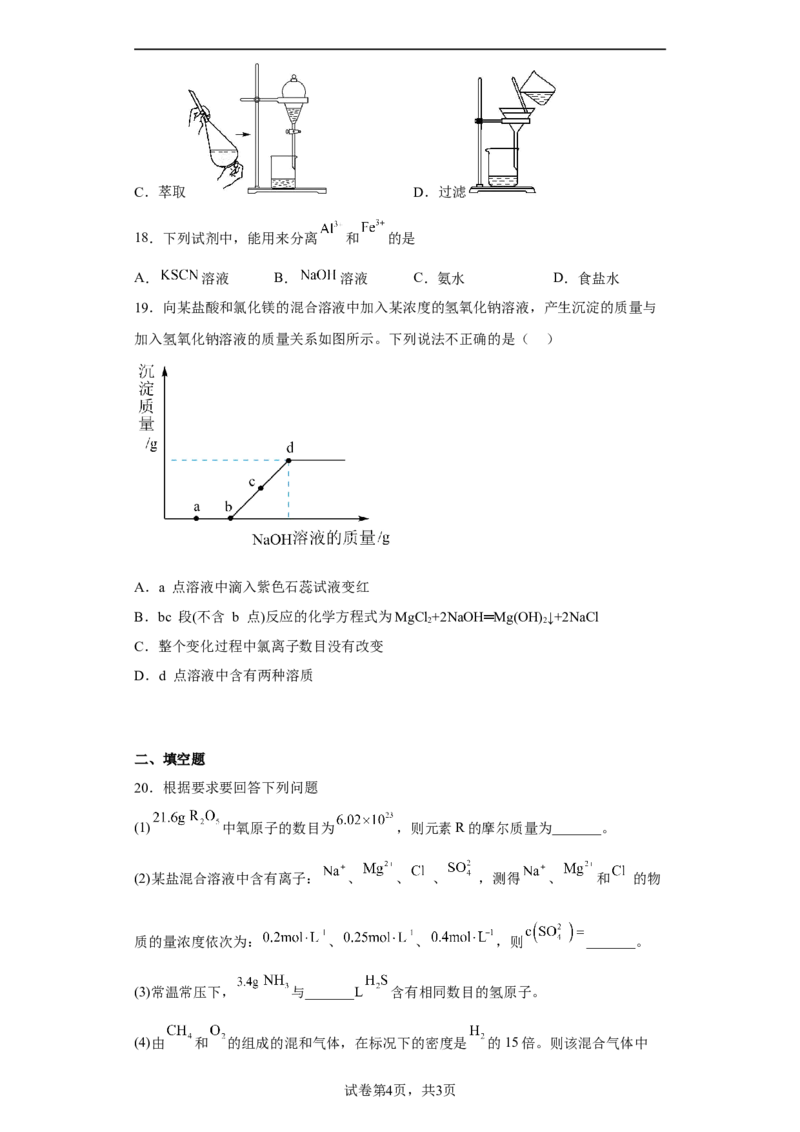
19.向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与
加入氢氧化钠溶液的质量关系如图所示。下列说法不正确的是( )
A.a 点溶液中滴入紫色石蕊试液变红
B.bc 段(不含 b 点)反应的化学方程式为MgCl +2NaOH═Mg(OH) ↓+2NaCl
2 2
C.整个变化过程中氯离子数目没有改变
D.d 点溶液中含有两种溶质
二、填空题
20.根据要求要回答下列问题
(1) 中氧原子的数目为 ,则元素R的摩尔质量为_______。
(2)某盐混合溶液中含有离子: 、 、 、 ,测得 、 和 的物
质的量浓度依次为: 、 、 ,则 _______。
(3)常温常压下, 与_______L 含有相同数目的氢原子。
(4)由 和 的组成的混和气体,在标况下的密度是 的15倍。则该混合气体中
试卷第4页,共3页的体积分数为_______。
三、计算题
21.按要求填空。
(1) 固体与水完全反应时的化学方程式为_______,该反应转移的电子数为
_______。
(2)工业上由辉铜矿生产铜的主要反应为: ,该反应中被还原
的元素是_______(填元素符号)。该反应中产生的 尾气可用NaOH溶液吸收,若用
1L1mol/L的NaOH溶液恰好吸收标准状况下 ,反应的离子方程式为_______。
22.将0.46g金属钠加入足量水中充分反应,测得反应后溶液的体积为200mL。试计
算:
(1)反应生成的氢气在标准状况下的体积为多少毫升? ____________
(2)反应所得NaOH溶液的物质的量浓度是多少?______________
23.将一定量的 Na2CO3和NaHCO3的混合物,跟足量盐酸反应共消耗0.8 mol HCl,
生成0.5mol二氧化碳。求原混合物中NaHCO3的质量分数为多少?参考答案:
1.C
【详解】A. 青铜是我国使用最早的合金,A正确;B. 钢是用量最大、用途最广的合金,B
正确;C. 铁是活泼的金属,不易冶炼,古代常用金属铜铸造货币,C错误;D. 焊锡中加
入铅是为了降低熔点,D正确,答案选C。
2.C
【详解】A.金做成金箔,说明有延展性,故正确;
B.生活用铁锅,利用其导热性,故正确;
C.铁回收银,利用其还原性,不是氧化性,故错误;
D.铜能做印刷电路,说明其有导电性,故正确。
故选C。
【点睛】
3.C
【详解】A. 稀盐酸和石灰水发生中和反应,反应的离子方程式应为H++OH−=H O,A项错
2
误;
B. 氯化铜和石灰水反应生成氢氧化铜沉淀,反应的离子方程式为Cu2++2OH−=Cu(OH) ↓,B
2
项错误;
C. 铁与氯化铜溶液发生置换反应,生成氯化亚铁和铜,反应的离子方程式为Fe+Cu2+=Fe2+
+Cu,C项正确;
D. 铁为活泼金属,与稀盐酸发生置换反应生成氢气,离子方程式为Fe+2H+=Fe2++H ↑,D
2
项错误;
答案选C。
4.D
【详解】A.棉布属于天然高分子化合物,属于有机物,A不符合题意;
B.橡胶为高分子材料,属于有机物,B不符合题意;
C.涤纶为高分子材料,属于有机物,C不符合题意;
D.铝合金属于金属材料,不属于有机物,D符合题意;
故选D。
故答案选D。
5.A
【详解】A.钢铁是含碳量0.03%~2%的铁合金,故A选;B.石墨是碳元素的一种单质,是纯净物,不是合金,故B不选;
C.水银是金属汞,为纯净物,不是合金,故C不选;
D.金刚石是碳元素的一种单质,是纯净物,不是合金,故D不选;
答案选A。
6.D
【详解】A.五代岳州窑青釉莲瓣纹小口瓶,主要成分为硅酸盐,不是合金,A错误;
B.木雕罗汉像,木材的主要成分为纤维素,不是合金,B错误;
C.清象牙雕,主要成分为蛋白质,不是合金,C错误;
D.信宜铜蚕,主要成分为铜合金,D正确;
答案选D。
7.C
【详解】A. 碳酸氢钠碱性减弱,能与盐酸反应,可用于治疗胃酸过多的药物,A正确;
B. 明矾溶于水铝离子水解形成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化,B正
3
确;
C. 二氧化硫有漂白性,但二氧化硫有毒,不能用来漂白食物,C错误;
D. 常温下铁和铝在浓硝酸中钝化,因此可用铁、铝制容器来盛装浓硝酸,D正确;
答案选C。
8.B
【详解】A.因金属原子的化合价只能升高,只有还原性,有些金属阳离子如Fe2+既有氧化
性又有还原性,故A错误;B.含金属元素的离子不一定都是阳离子,如MnO -、AlO-等,
4 2
故B正确;C.“真金不怕火炼”指金的化学性质稳定,故C错误;D.常温下金属单质汞
为液体,故D错误;答案为B。
9.B
【详解】固体单质A和气体单质B在容积一定的密闭容器中恰好完全反应生成气体C,同
温下测得容器内压强不变,说明气体B、C的化学计量数相同,所以方程式可以写成mA
(s)+nB(g)=nC(g)。
A. 反应后气体C的密度是原气体密度的4倍,说明C的质量是B的质量的4倍,因为二者
的物质的量相同,所以B、C的摩尔质量的比为1:4,故错误;
B. C的质量是B的质量的4倍,且C的质量等于B和A的质量和,所以C中A元素的质量
分数为75%,故正确;
C. 生成物C中A、B的元素的质量比为3:1,但是不能确定原子个数之比,故错误;
答案第2页,共2页D. 同温下测得容器内压强不变,说明气体B、C的化学计量数相同,即B和C的分子数相
同,故错误。
故选B。
【点睛】掌握化学反应中的质量守恒定律,和同温同体积条件下,压强比等于物质的量比。
10.C
【详解】令生成的氢气的物质的量为3mol,根据2Al+3H SO =Al(SO )+3H ↑和
2 4 2 4 3 2
2Al+2NaOH+2H O=2NaAlO +3H ↑,需要硫酸和氢氧化钠的物质的量分别为3mol、2mol,
2 2 2
物质的量的之比为3mol∶2mol=3∶2,故选C。
11.A
【分析】气体先通过炽热铜粉,分别发生2Cu+O 2CuO,CuO+CO Cu+CO,相当于
2 2
O+2CO=2CO,混合气体中1LCO、1LO 可以生成CO 为1L,剩余氧气与铜反应,即通
2 2 2 2
过过量的热铜粉出来的气体是HO和CO;出来气体通过过量过氧化钠,水、二氧化碳完
2 2
全反应,生成氧气,以此解答该题。
【详解】气体先通过炽热铜粉,分别发生2Cu+O 2CuO,CuO+CO Cu+CO,相当于
2 2
O+2CO=2CO,混合气体中1LCO、1LO 可以生成CO 为1L,剩余氧气与铜反应,即通
2 2 2 2
过过量的热铜粉出来的气体是2LHO和3LCO ;出来气体通过过量过氧化钠,发生反应
2 2
2HO+2NaO=4NaOH+O,2CO+2NaO=2NaCO+O,水、二氧化碳完全反应,由
2 2 2 2 2 2 2 2 3 2
化学方程式可知,生成氧气V(O )= V(CO)+ V(H O)= ×3L+ ×2L=2.5L,恢复到
2 2 2
原来的温度和压强后得到的气体是O,故答案选A。
2
【点睛】应用化学反应守恒的思想把化学方程式合并,可以简化计算步骤,注意在该温度
下HO是气体。
2
12.B
【详解】A.Cu与稀硫酸不反应,故A项错误;
B.氧化镁与盐酸反应生成氯化镁和水,反应离子方程式为MgO+2H+=Mg2++H O,故B项
2
正确;
C.大理石主要成分为碳酸钙,碳酸钙为难溶物,离子方程式中不能拆分,故C项错误;D.氢氧化钡溶液与硫酸铜溶液混合,OH-与Cu2+反应生成难溶物Cu(OH) ,Ba2+与 反
2
应生成难溶物BaSO,反应离子方程式为 ,
4
故D项错误;
答案选B。
13.B
【详解】A.氯气和水反应生成盐酸和次氯酸,次氯酸为弱酸,不能拆成离子形式,正确
的离子方程式为:Cl+H O=H++Cl-+HClO,故A错误;
2 2
B.氯气具有强氧化性,能够把Fe2+氧化为Fe3+,离子方程式符合电荷、原子守恒,故B正
确;
C.小苏打为碳酸氢钠,与盐酸反应生成氯化钠、二氧化碳和水,正确的离子方程式为:
HCO +H+=CO ↑+H O,故C错误;
2 2
D.氢氧化铝属于弱电解质,保留分子式,正确的离子方程式为:Al(OH) +3H+=Al3+
3
+3H O,故D错误;
2
故选B。
14.B
【详解】A.铝合金具有质地轻、强度高、抗腐蚀能力强等特点,可用于制造高铁车厢等,
故A正确;
B.钛合金是金属材料,故B错误;
C.不锈钢是铁与镍、铬等形成的合金,故C正确;
D.后(司)母戊鼎为商代后期的青铜器,属于铜合金制品,故D正确;
答案选B。
15.D
【分析】根据题中铁合金可知,本题考查铁合金的概念,运用铁与一种或几种元素组成的
中间合金称为铁合金分析。
【详解】A.球墨铸铁是铁、碳、硅、锰形成的合金,故A不符合题意;
B.不锈钢是铁、铬、镍形成的合金,故B不符合题意;
C.锰钢是铁、锰、碳形成的合金,故C不符合题意;
D.氧化铁是金属氧化物,不属于合金,故D符合题意;
答案第4页,共2页答案选D。
16.B
【详解】A.国产大飞机C919机壳采用的铝锂合金,具有密度小、硬度大、耐腐蚀的优良
性质,A正确;
B.乙酸钠在温度较高的水中的溶解度非常大,很容易形成过饱和溶液,暂时处于亚稳态;
这种溶液里只要有一丁点的结晶和颗粒,就能打破它的亚稳态,迅速结晶的同时释放出大
量热量,B错误;
C.“嫦娥五号”使用的锂离子电池组属于原电池装置,可将化学能转化为电能,C正确;
D.国家速滑馆“冰丝带”采用CO2超临界制冰,将CO 利用起来,减少了CO 的排放,
2 2
比氟利昂制冰更加环保,D正确;
故选B。
17.C
【详解】A.丁达尔效应在胶体中发生,形成胶体的分散质粒径在1-100nm之间,故丁达
尔效应与物质微粒大小有直接关系,A不符合题意;
B.渗析指微粒直径小于1nm的可以通过,而大于1nm的不可以通过,即溶液可通过,胶
体、浊液不能通过,从而达到分离的目的,与物质微粒大小有直接关系,B不符合题意;
C.萃取是利用溶质在两种互不相溶溶剂中的溶解度差异,达到分离提纯目的,与物质微
粒大小无直接关系,C符合题意;
D.过滤指微粒直径小于100nm的可以通过,而大于100nm的不可以通过,即溶液、胶体
可通过,浊液不能通过,从而达到分离的目的,与物质微粒大小有直接关系,D不符合题
意;
故选C。
18.B
【详解】 与过量的 溶液生成可溶的偏铝酸钠溶液, 生成氢氧化铁沉淀,过
滤,滤液中加入足量的盐酸得到铝离子,滤渣中加入足量的盐酸,得到铁离子,将两种离
子分开,故答案为:B。
19.D
【详解】A.a点溶液中含有的溶质有没有反应的盐酸、反应生成的硫酸钠和没有反应的氯
化镁三种物质,盐酸呈酸性,能使紫色石蕊试液变红,故A正确;
B.bc段发生的反应是氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,化学方程式为MgCl +2NaOH═Mg(OH) ↓+2NaCl,故B正确;
2 2
C.整个变化过程中氯离子没有生成沉淀或气体,也没有加入氯离子,所以整个变化过程
中氯离子数目没有改变,故C正确;
D.d点时,氢氧化钠和盐酸、氯化镁恰好完全反应,溶液中的溶质只有氯化钠一种,故D
错误;
答案选D。
20.(1)14g/mol
(2)0.15mol/L
(3)6.72L
(4)
【详解】(1)21.6gR O 中氧原子的数目为 ,则氧原子的物质的量=
2 5
=1mol,则n(R O)=0.2mol,R O 的摩尔质量=21.6g÷0.2mol=108g/mol,元
2 5 2 5
素R的相对原子质量为 =14,所以M(R)=14g/mol;
(2)由电荷守恒:c(Na+)+ 2c(Mg2+)= c(Cl﹣)+ 2c(SO 2﹣)代入数值得0.2mol•L﹣1+
4
2 0.25mol•L﹣1= 0.4mol•L﹣1+ 2c(SO 2﹣),则c(SO 2﹣)=0.15mol/L;
4 4
(3)3.4gNH 的物质的量为: =0.2mol;含有氢原子的物质的量为0.6mol,与氨气
3
所含H原子数相同的HS的物质的量为0.3mol,则其体积为0.3mol×22.4L/mol=6.72L。
2
(4)由 CH 和 O 的组成的混和气体,在标况下的密度是H 的 15倍,则其平均相对分
4 2 2
子质量为30,设该混合气体中 CH 和 O 的物质的量分别为a、b,则 ,
4 2
a:b=1:7,根据阿伏伽德罗定律可知,则该混合气体中CH 的体积分数= ;
4
21.(1) 2NaO+2H O=4Na++4OH—+O ↑ N
2 2 2 2 A
答案第6页,共2页(2) Cu、O SO +OH—=HSO
2
【解析】(1)
过氧化钠与水反应生成氢氧化钠和氧气,反应的离子方程式为2NaO+2H O=4Na++4OH—
2 2 2
+O ↑,反应中2mol过氧化钠反应转移电子的物质的量为2mol,则1mol过氧化钠与水完全
2
反应时,反应转移的电子数为N ,故答案为:2NaO+2H O=4Na++4OH—+O ↑;N ;
A 2 2 2 2 A
(2)
由方程式可知,反应中铜元素和氧元素的化合价降低被还原;由题意可知,氢氧化钠溶液
中氢氧化钠的物质的量为1L×1mol/L=1mol,二氧化硫的物质的量为 =1mol,由
氢氧化钠和二氧化硫的物质的量比为1:1可知氢氧化钠溶液与二氧化硫反应生成亚硫酸氢
钠,反应的离子方程式为SO +OH—=HSO ,故答案为:Cu、O;SO +OH—=HSO 。
2 2
22. 224mL 0.1mol/L
【详解】(1)根据2Na+2HO=2NaOH+H ↑,0.46g金属钠即0.02mol,与足量的水可生成
2 2
0.01mol氢气,标况下,V(H)=0.01mol×22.4L/mol=0.224L,即224mL;
2
(2)0.02molNa与水反应可生成0.02molNaOH,c(NaOH)= =0.1mol/L。
23.34.6%
【分析】根据NaCO 和NaHCO 都能与盐酸反应放出二氧化碳,设与NaCO 和NaHCO 反
2 3 3 2 3 3
应的盐酸分别为xmol,ymol,建立方程组,求出x、y,然后求出NaCO、NaHCO 的质量,最后
2 3 3
得出NaHCO 的质量分数。
3
【详解】设与NaCO 和NaHCO 的盐酸分别为,xmol,ymol,则
2 3 3
NaCO+2HCl=2NaCl+H O+CO↑;关系式为NaCO--2HCl--CO ↑;
2 3 2 2 2 3 2
NaHCO +HCl=NaCl+H O+CO↑;关系式为NaHCO --HCl--CO ↑;所以
3 2 2 3 2
x+y=0.8,0.5x+y=0.5,计算得出:x=0.6,y=0.2;则NaHCO 的物质的量为0.2mol, NaHCO 的
3 3
质量为0.2×84=16.8g;NaCO 的物质的量为0.3mol,NaCO 的质量为0.3×106=31.8g;所
2 3 2 3
以NaHCO 的质量分数16.8/(16.8+31.8)×100%=34.6%;
3
答:原混合物中NaHCO 的质量分数为34.6%。
3答案第8页,共2页