文档内容
2022--2023学年人教版(2019)高一必修第一册 第二章 海
水中的重要元素 第一节 钠及其化合物
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.学好化学让生活更美好。下列相关说法错误的是
A.节日燃放的五彩缤纷的烟花,与金属元素的焰色有关
B.小苏打是碳酸氢钠的俗称,可用作发酵粉,也可用于治疗胃酸过多症
C.为防止中秋月饼等富脂食品被氧化变质,常在包装袋中放入生石灰
D.葡萄酒中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒
2.下列离子方程式正确的是
A.浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H ↑
2
B.钠与水反应:2Na+2H+=2Na++H ↑
2
C.NH HCO 与足量烧碱反应:HCO +OH﹣=CO +H O
4 3 2
D.NaCO 与足量盐酸反应:CO +2H+=CO ↑+H O
2 3 2 2
3.下列关于金属钠的说法不正确的是( )
A.金属钠在空气中燃烧,生成淡黄色过氧化钠固体
B.用小刀切下一小块金属钠备用,剩余的金属钠不应放回原试剂瓶中
C.少量的金属钠保存在煤油中,多量的金属钠一般用石蜡油封存
D.钠和钾的合金可用作原子反应堆的导热剂
4.下列有关钠的物理性质的叙述正确的有( )
①银白色金属 ②质软,可以用小刀切 ③熔点低于100℃ ④密度比水小 ⑤热和
电的良导体
A.仅①②④⑤ B.仅①②③④
C.仅①③④⑤ D.①②③④⑤
5.下列表述中,Ⅰ、Ⅱ两者间不具有因果关系的是
选项 表述Ⅰ 表述Ⅱ
A 常温下铝在浓硫酸中发生钝化 可用铝槽车密封运送浓硫酸
B SO 有漂白性 SO 通入品红溶液中,溶液褪色
2 2
C 热稳定性:NaCO>NaHCO 同浓度溶液碱性:NaCO>NaHCO
2 3 3 2 3 3
D 非金属性:F>Cl 氢化物的稳定性:HF>HClA.A B.B C.C D.D
6.下列关于焰色试验的说法中,正确的是
A.焰色试验是化学变化
B.在做焰色试验的实验时,应用玻璃棒蘸取待测液,放在酒精灯外焰上灼烧
C.Na、NaCl、NaCO 灼烧时火焰颜色相同
2 3
D.若某物质的焰色反应呈黄色,说明该物质只含钠元素,不含钾元素
7.下列关于钠及其化合物的叙述正确的是( )
①Na O与NaO 都能和水反应生成碱,它们都是碱性氧化物
2 2 2
②Na CO 溶液和NaHCO 溶液都能跟CaCl 稀溶液反应得到白色沉淀
2 3 3 2
③钠在常温下不容易被氧化
④Na O 可作供氧剂,而NaO不能
2 2 2
⑤向酚酞溶液中加入NaO 粉末,溶液先变红后褪色,并有气泡生成
2 2
⑥钠与浓NH Cl溶液反应,放出的气体中含有H 和NH
4 2 3
A.①④⑥ B.②③④⑤
C.②⑤⑥ D.④⑤⑥
8.下列叙述正确的是
①Na O与NaO 都能和水反应生成碱,它们都是碱性氧化物
2 2 2
②Na O与CO 发生化合生成NaCO,NaO 与CO 发生置换生成O
2 2 2 3 2 2 2 2
③Na O是淡黄色物质,NaO 是白色物质
2 2 2
④Na O 可作供氧剂,而NaO不行
2 2 2
⑤Na O 和NaO焰色反应均为黄色
2 2 2
A.都正确 B.②③④⑤ C.②③⑤ D.④⑤
9.甲、乙两烧杯各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液,向烧杯分别加入等
质量的铝粉,反应结束后测得生成的气体体积比为甲∶乙=3∶4,则加入铝粉的质量为
A.1.8 g B.2.7 g C.3.6 g D.5.4 g
10.观察是化学学习的重要方法。金属钠放置于空气中观察到下列现象,下列推证正
确的是
A.若将钠放置于坩埚中加热,观察到的现象与①、②相同
B.取①得到的产物,滴加适量水和 溶液,可观察到蓝色沉淀生成
试卷第2页,共3页C.取③后液滴的稀溶液滴加酚酞溶液,可观察到酚酞先变红后褪色
D.加热④的白色晶体,通入水中有气泡则可证明白色晶体是
11.下列关于钠的说法中,正确的是( )
A.钠的化学性质很活泼,所以它在自然界中不能以游离态存在
B.钠可以把钛、锆、铌等金属从它们的氯化物的水溶液中置换出来
C.实验后剩余的钠不可放回原试剂瓶中
D.钠在空气中燃烧生成氧化钠,发出黄色火焰
12.下列有关钠、铝、铁单质及其化合物的性质的说法中正确的是
A.钠表面自然形成的氧化层能够保护内层金属不被空气氧化
B.可用氢氧化钙溶液鉴别 溶液和 溶液
C. 、 、 均能通过化合反应制得
D.Al、 、 、 均能与NaOH溶液发生反应
13.下列各组中两种物质反应时,反应条件或反应物用量改变,对生成物没有影响的
是( )
A.Na与O B.NaO 与CO
2 2 2 2
C.NaCO 溶液与盐酸 D.NaAlO 溶液与盐酸
2 3 2
二、实验题
14.某化学实验需要450 mL 0.10 mol·L-1 NaCO 溶液,某同学选用NaCO·10H O晶
2 3 2 3 2
体进行配制,简要回答下列问题:
(1)该实验应选择__________mL容量瓶。
(2)需称取NaCO·10H O的质量为__________g。
2 3 2
(3)该实验的正确操作顺序是_______________(填字母代号)。
A.用托盘天平称取NaCO·10H O晶体
2 3 2
B.上下颠倒摇匀
C.用胶头滴管加水至刻度线
D.洗涤所用仪器并将洗涤液转移进容量瓶
E.将所称取的晶体溶于蒸馏水并冷却至室温
F.将溶液转入容量瓶
(4)另需配制一定浓度的NaOH溶液,称量时若将NaOH固体置于滤纸上称量,则所配溶液浓度______;若容量瓶中有检漏时残留的少量蒸馏水,会使所配溶液浓度
______;NaOH溶解后未经______;立即注入容量瓶至刻度线,会使浓度______;定
容时必须使凹液面最低处与刻度线相切,若仰视会使所配溶液浓度______(凡涉及浓
度变化填“偏高”、“偏低”或“无影响”)。
(5)向200 mL所配的 0.10 mol·L-1NaCO 溶液中逐滴加入10 mL 12.25%稀HSO
2 3 2 4
(ρ=1.0 g/cm3),理论上能收集到标准状况下的气体__________mL。
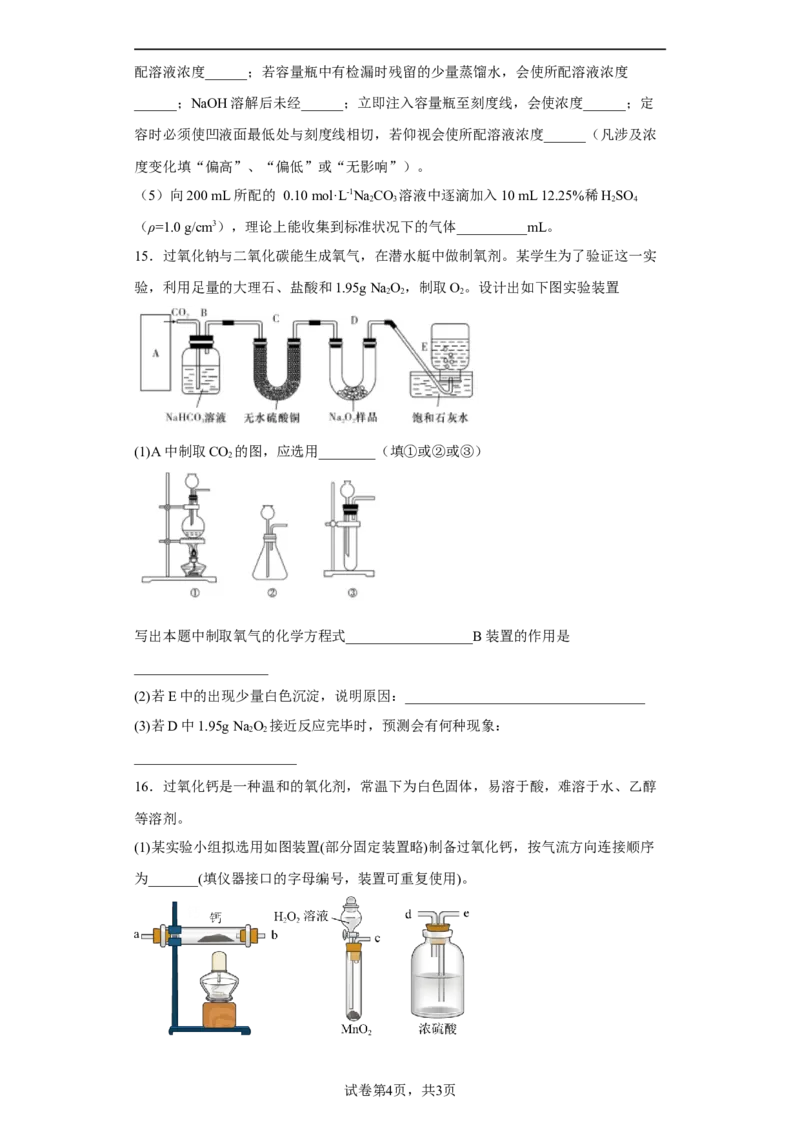
15.过氧化钠与二氧化碳能生成氧气,在潜水艇中做制氧剂。某学生为了验证这一实
验,利用足量的大理石、盐酸和1.95g NaO,制取O。设计出如下图实验装置
2 2 2
(1)A中制取CO 的图,应选用________(填①或②或③)
2
写出本题中制取氧气的化学方程式__________________B装置的作用是
___________________
(2)若E中的出现少量白色沉淀,说明原因:__________________________________
(3)若D中1.95g NaO 接近反应完毕时,预测会有何种现象:
2 2
_______________________
16.过氧化钙是一种温和的氧化剂,常温下为白色固体,易溶于酸,难溶于水、乙醇
等溶剂。
(1)某实验小组拟选用如图装置(部分固定装置略)制备过氧化钙,按气流方向连接顺序
为_______(填仪器接口的字母编号,装置可重复使用)。
试卷第4页,共3页实验步骤如下:
①检验装置的气密性后,装入药品;
②打开分液漏斗活塞,通入一段时间气体,加热药品;
③反应结束后,先熄灭酒精灯,待反应管冷却至室温后,停止通入气体;
④拆除装置,取出产物。
实验步骤③的操作目的是_______。
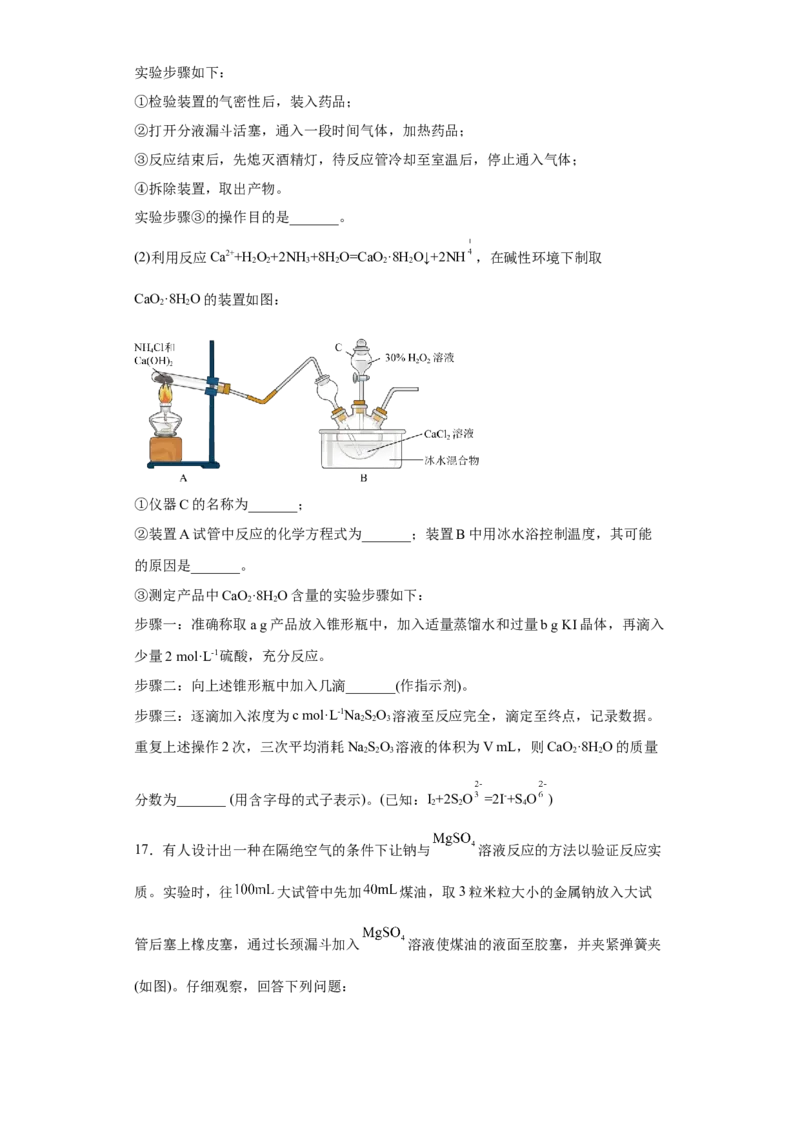
(2)利用反应Ca2++H O+2NH+8H O=CaO ·8H O↓+2NH ,在碱性环境下制取
2 2 3 2 2 2
CaO·8H O的装置如图:
2 2
①仪器C的名称为_______;
②装置A试管中反应的化学方程式为_______;装置B中用冰水浴控制温度,其可能
的原因是_______。
③测定产品中CaO·8H O含量的实验步骤如下:
2 2
步骤一:准确称取a g产品放入锥形瓶中,加入适量蒸馏水和过量b g KI晶体,再滴入
少量2 mol·L-1硫酸,充分反应。
步骤二:向上述锥形瓶中加入几滴_______(作指示剂)。
步骤三:逐滴加入浓度为c mol·L-1NaSO 溶液至反应完全,滴定至终点,记录数据。
2 2 3
重复上述操作2次,三次平均消耗NaSO 溶液的体积为V mL,则CaO·8H O的质量
2 2 3 2 2
分数为_______ (用含字母的式子表示)。(已知:I+2S O =2I-+S O )
2 2 4
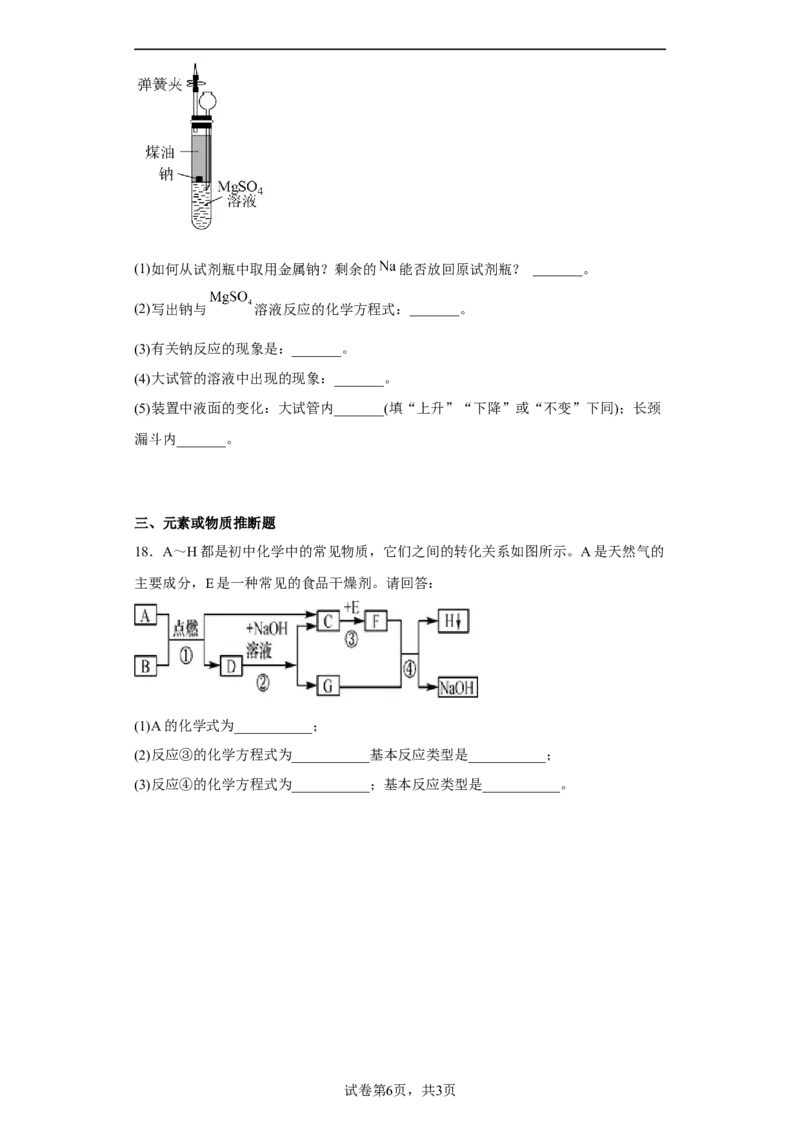
17.有人设计出一种在隔绝空气的条件下让钠与 溶液反应的方法以验证反应实
质。实验时,往 大试管中先加 煤油,取3粒米粒大小的金属钠放入大试
管后塞上橡皮塞,通过长颈漏斗加入 溶液使煤油的液面至胶塞,并夹紧弹簧夹
(如图)。仔细观察,回答下列问题:(1)如何从试剂瓶中取用金属钠?剩余的 能否放回原试剂瓶? _______。
(2)写出钠与 溶液反应的化学方程式:_______。
(3)有关钠反应的现象是:_______。
(4)大试管的溶液中出现的现象:_______。
(5)装置中液面的变化:大试管内_______(填“上升”“下降”或“不变”下同);长颈
漏斗内_______。
三、元素或物质推断题
18.A~H都是初中化学中的常见物质,它们之间的转化关系如图所示。A是天然气的
主要成分,E是一种常见的食品干燥剂。请回答:
(1)A的化学式为___________;
(2)反应③的化学方程式为___________基本反应类型是___________;
(3)反应④的化学方程式为___________;基本反应类型是___________。
试卷第6页,共3页参考答案:
1.C
【详解】A.节日燃放的五彩缤纷的烟花,与金属元素的焰色有关,属物理变化,A项正
确;
B.碳酸氢钠俗称小苏打,可做发酵粉,可治疗胃酸过多,B项正确;
C.生石灰有吸水性,做干燥剂,不能做防氧化剂,C项错误;
D.食用苏打粉主要成分是碳酸氢钠,其溶液显弱碱性,D项正确;
故答案选C。
2.D
【详解】A.浓盐酸与铁屑反应: ,A错误;
B.钠与水反应: ,B错误;
C.NH HCO 与足量烧碱反应: ,C错误;
4 3
D.NaCO 与足量盐酸反应: ,D正确;
2 3
故选D。
3.B
【详解】A. 金属钠在常温下与氧气反应生成白色固体氧化钠,在空气中燃烧生成淡黄色固
体过氧化钠,A项正确,不符合题意;
B. 取用金属钠后,剩余的金属钠放回原试剂瓶,B项错误,符合题意;
C. 少量的金属钠保存在煤油中,多量的金属钠一般用石蜡油封存,C项正确,不符合题意;
D. 钠和钾的合金可用作原子反应堆的导热剂,D项正确,不符合题意;
答案选B。
【点睛】解答本题时要注意特殊试剂的取用:
试剂 取用方法
用镊子取出一些金属钠或钾后,用滤纸吸干表面的煤油,放在玻
金属钠、钾等活泼金属
璃片或白瓷板上用小刀切割一小块,余下的立即放回原瓶
白磷 用镊子夹持住白磷,用小刀在水下切割
(在通风橱中)先捏瘪滴管胶头,再伸入下层吸取(上层为水溶液
液溴
层),因液溴有很强的腐蚀性,要注意防止其沾在皮肤上4.D
【详解】①钠是I A族元素,为银白色金属单质,有金属光泽;②质地较软,可以用小刀
切割;③将钠放入水中,钠会立即熔成小球,说明熔点较低;④钠能浮于水面上,说明钠
的密度比水的小;⑤钠是金属,含有自由移动的电子,所以是热和电的良导体;故选D。
5.C
【详解】A.因为常温下铝和浓硫酸发生钝化反应,因此可用铝槽车密封运送浓硫酸,Ⅰ、
Ⅱ两者间具有因果关系,故A不符题意;
B.SO 具有漂白性,能使品红溶液褪色,Ⅰ、Ⅱ两者间具有因果关系,故B不符题意;
2
C.NaCO 的热稳定性高于NaHCO ,但与溶液碱性强弱无关,Ⅰ、Ⅱ两者间不具有因果
2 3 3
关系,故C符题意;
D.非金属性越强,其氢化物越稳定,Ⅰ、Ⅱ两者间具有因果关系,故D不符题意;
答案选C。
6.C
【详解】A.焰色试验是一种元素的物理性质,而不是化学性质,焰色试验是物理变化,
故A错误;
B.在做焰色试验的实验时,应用铂丝蘸取待测液,放在酒精灯外焰上灼烧,故B错误;
C.Na、NaCl、NaCO 均含钠元素,焰色试验均为黄色,故C正确;
2 3
D.若某物质的焰色试验呈黄色,说明该物质一定含钠元素,没有透过蓝色钴玻璃观察,
因此不能说明不含钾元素,故D错误;
故选C。
7.D
【详解】①NaO 属于过氧化物,不是碱性氧化物,故①错误;
2 2
②NaHCO 溶液不与CaCl 稀溶液反应,故②错误;
3 2
③钠在常温下易被氧化成氧化钠,故③错误;
④Na O 能和水蒸气或二氧化碳反应放出氧气,可用作供氧剂,而NaO不能,故④正确;
2 2 2
⑤向酚酞溶液中加入NaO 粉末,生成氢氧化钠和氧气,溶液先变红,由于反应中有HO
2 2 2 2
生成,且HO 具有强氧化性,所以溶液会褪色,故⑤正确;
2 2
⑥钠与浓NH Cl溶液反应,生成NaCl、H 和NH ,故⑥正确;
4 2 3
正确的是④⑤⑥,答案选D。
8.D
【详解】①NaO 能和水反应生成氢氧化钠和氧气,为过氧化物,不是碱性氧化物,故①
2 2
答案第2页,共2页错误;
②Na O与CO 发生化合生成NaCO,NaO 与CO 发生氧化还原反应生成O,不是置换反
2 2 2 3 2 2 2 2
应,故②错误;
③Na O是白色物质,NaO 是淡黄色物质,故③错误;
2 2 2
④Na O 可与水、二氧化碳反应生成氧气,可作供氧剂,而NaO不行,故④正确;
2 2 2
⑤Na O 和NaO均含有钠元素,则焰色反应均为黄色,故⑤正确。
2 2 2
故答案选D。
9.C
【分析】本题主要考查铝的化学性质以及化学方程式的有关计算。根据铝的质量相同,盐
酸和氢氧化钠溶液中溶质的物质的量相同,反应结束后测得生成的气体体积比为甲:乙
=3:4,由化学反应方程式可知,酸与金属反应时酸不足,碱与金属反应时碱过量来计算解
答。
【详解】盐酸和氢氧化钠溶液中溶质的物质的量均为0.1L×3mol/L=0.3mol,又两烧杯中分
别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=3:4,
设铝与酸反应时,酸完全反应,生成的氢气的物质的量为x,
则 2Al+6HCl═2AlCl +3H ↑
3 2
6 3
0.3mol x
,解得x=0.15mol,一定条件下,气体的物质的量之比等于体积之比,则碱与金
属铝反应生成的氢气的物质的量为0.15mol× =0.2mol,
碱与金属铝反应时,铝完全反应,设与碱反应的铝的物质的量为y,
则 2Al+2NaOH+2H O═2NaAlO+3H ↑
2 2 2
2 3
y 0.2mol
,解得y= mol,其质量为 mol×27g/mol=3.6g。
10.B
【分析】金属钠露置于空气中发生的变化中,①是钠被氧化为氧化钠为灰暗色;②是氧化
钠和水反应生成氢氧化钠为白色;③氢氧化钠潮解形成氢氧化钠溶液;④是二氧化碳和氢氧化钠反应生成碳酸钠晶体,
【详解】A.钠放置于坩埚中加热,钠首先融化成小球,继而剧烈燃烧产生黄色火焰,燃
烧产物为淡黄色的固体过氧化钠,A错误;
B.①是钠被氧化为氧化钠,水与氧化钠反应生成NaOH,加入 溶液生成Cu(OH) 沉
2
淀,可观察到蓝色沉淀生成,B正确;
C.③氢氧化钠潮解形成氢氧化钠溶液,滴加酚酞溶液,溶液只变红不褪色,C错误;
D.加热④的白色晶体,即加热NaCO·10H O,对其加热通入水中无明显现象,D错误;
2 3 2
故选:B。
11.A
【详解】A.钠性质活泼,可与水、氧气等发生反应,在自然界中不能以游离态存在,故
A正确;
B.钠和钛锆等金属盐溶液的反应是先和其中的水反应置换出氢气,不会置换出金属,故B
错误;
C.因钠活泼,易与水、氧气反应,如在实验室随意丢弃,可引起火灾,实验时剩余的钠
粒可放回原试剂瓶中,故C错误;
D.钠在空气中燃烧生成过氧化钠,故D错误;
故答案为A。
12.C
【详解】A.钠表面自然形成的氧化层为NaO,能与空气中的水和 反应,然后继续与
2
空气中 、 、 反应,A项错误;
B. 溶液和 溶液均能与氢氧化钙溶液反应生成白色沉淀,现象相同,不能
鉴别,B项错误;
C.Fe在氧气中燃烧生成 ,发生化合反应; 、O 与HO化合生成 ;
2 2
Fe与 化合生成 ,C项正确;
D.Al、 、 均能与NaOH溶液发生反应,但 与NaOH不反应,D项
答案第4页,共2页错误;
答案选C。
13.B
【详解】A.Na与O 反应,温度不同,产物不同,常温下生成氧化钠,加热条件下反应生
2
成过氧化钠,反应条件不同,生成物不同,A不合题意;
B.过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应条件或反应物用量改变,对生成物没
有影响,B符合题意;
C.Na CO 溶液与盐酸反应,盐酸不足可生成碳酸氢钠,盐酸过量,可生成二氧化碳气体,
2 3
则反应物用量不同,产物不同,C不合题意;
D.NaAlO 溶液与盐酸反应,盐酸不足,可生成氢氧化铝,盐酸过量可生成氯化铝,反应物
2
用量不同,产物不同,D不合题意。
故选B。
14. 500 14.3 A E F D C B 偏低 无影响 冷
却 偏高 偏低 112
【详解】(1)由于没有450mL容量瓶,则该实验应选择500mL容量瓶。
(2)需称取NaCO·10H O的质量为0.5L×0.1mol/L×286g/mol=14.3g。
2 3 2
(3)配制一定物质的量浓度溶液的基本操作步骤是计算、称量、溶解、冷却、转移、洗涤、
定容、摇匀等,则该实验的正确操作顺序是A、E、F、D、C、B。
(4)另需配制一定浓度的NaOH溶液,称量时若将NaOH固体置于滤纸上称量,由于氢氧
化钠易吸水,则氢氧化钠的质量减少,因此所配溶液浓度偏低;若容量瓶中有检漏时残留
的少量蒸馏水,由于不会影响溶质和溶液体积,则会使所配溶液浓度无影响;氢氧化钠溶
于水放热,则NaOH溶解后未经冷却,立即注入容量瓶至刻度线,冷却后溶液体积减少,
则会使浓度偏高;定容时必须使凹液面最低处与刻度线相切,若仰视会使溶液体积增加,
所配溶液浓度偏低。
(5)200mL溶液中碳酸钠的物质的量是0.2L×0.1mol/L=0.02mol。10 mL 12.25%稀HSO
2 4
(ρ=1.0 g/cm3)的物质的量是 ,其中氢离子的物质的量
是0.025mol。由于与碳酸钠反应时分步进行,即首先转化为碳酸氢钠,消耗氢离子是
0.02mol,剩余的氢离子再与碳酸氢钠反应放出二氧化碳,此时氢离子不足,则根据HCO -
3+H+=CO↑+H O可知生成的二氧化碳是0.025mol-0.02mol=0.005mol,在标准状况下的体
2 2
积是0.005mol×22.4L/mol=0.112L=112mL。
15. ② 2NaO+2CO =2Na CO+ O 除去CO 中混有的HCl气
2 2 2 2 3 2 2
体 CO 并未全部与NaO 反应,少许溢出使石灰水变浑浊,E中石灰水变浑浊明显
2 2 2
增加 集气瓶内液面不再下降
【分析】(1)A中制取CO 的图,制取二氧化碳是用大理石和盐酸反应,不需要加热,该反
2
应是放热反应,应该用比较大的容器反应;用过氧化钠和二氧化碳的反应,用饱和碳酸氢
钠溶液吸收二氧化碳中的氯化氢气体。
(2)二氧化碳未完全反应则可能会使澄清石灰水变浑浊。
(3)当过氧化钠接近反应完,则集气瓶内液面不再下降。
【详解】(1)A中制取CO 的图,制取二氧化碳是用大理石和盐酸反应,不需要加热,该反
2
应是放热反应,应该用比较大的容器反应,应选用②,制取氧气主要是二氧化碳和过氧化
钠反应,其化学方程式2NaO+2CO =2Na CO+ O ,B装置的作用是主要是除掉二氧化碳
2 2 2 2 3 2
中的氯化氢,故答案为②;2NaO+2CO =2Na CO+ O ;除掉二氧化碳中的氯化氢。
2 2 2 2 3 2
(2)若E中的出现少量白色沉淀,说明原因CO 并未全部与NaO 反应,少许溢出使石灰水
2 2 2
变浑浊,故答案为CO 并未全部与NaO 反应,少许溢出使石灰水变浑浊。
2 2 2
(3)若D中1.95g NaO 接近反应完毕时,不再生成氧气,出来的二氧化碳和澄清石灰水反应,
2 2
因此出现集气瓶内液面不再下降,溶液变浑浊,故答案为集气瓶内液面不再下降。
16.(1) cedabe或cedbae 防止倒吸
(2) 分液漏斗 Ca(OH) +2NHCl CaCl +2NH↑+2H O 温度低可减少过氧化氢
2 4 2 3 2
分解,提高过氧化氢的利用率 淀粉溶液 ×100%
【分析】本题是一道常见的无机物的制备类实验题,首先通过过氧化氢在二氧化锰的催化
作用下制备氧气,随后用浓硫酸干燥氧气后,在加热的情况下和钙反应制备过氧化钙,以
此解题。
(1)
制备过氧化钙时,用双氧水制备氧气,钙属于极活泼的金属,极易与水反应生成氢氧化钙
和氢气,而制备的氧气中会混有水蒸气,所以在与钙化合之前需要干燥,选用试剂是浓硫
答案第6页,共2页酸;同时为防止空气中水蒸气进入,最后还需要连接浓硫酸的洗气瓶,所以正确的顺序为:
cedabe或cedbac;实验结束时为防止空气进入装置,还要继续通氧气直到装置冷却,所以
实验步骤③的操作目的是防止倒吸;
(2)
①根据图中仪器可知,仪器C的名称为分液漏斗;
②装置A中利用熟石灰与氯化铵共热制取氨气,发生反应的化学方程式为Ca(OH) +2NHCl
2 4
CaCl +2NH↑+2H O;反应过程中使用了过氧化氢,过氧化氢受热分解,装置B中用冰水
2 3 2
浴控制温度,其可能原因是温度低可减少过氧化氢分解,提高过氧化氢的利用率;
③利用淀粉遇碘变蓝,故选择的指示剂为淀粉溶液;
CaO 和碘化钾反应的方程式为: 2KI+CaO+2H SO =CaSO +K SO +O +I ,则根据电子转
2 2 2 4 4 2 4 2 2
移守恒关系可知:
CaO·8H O ~ I ~ 2SO
2 2 2 2
216 2
am c×V×10-3mol
因此 。
17.(1)用镊子从试剂瓶中取一块金属钠,用滤纸吸干表面上的煤油,用小刀在玻璃片上切
米粒大小的钠做实验用,剩余的钠要放回原试剂瓶,不要随意丢弃
(2)
(3)有气泡生成,钠熔化成小球且在煤油和 溶液界面处上下跳动,最终完全溶解
(4)下层溶液出现白色沉淀
(5) 下降 上升
【详解】(1)金属钠保存在煤油中,用镊子从试剂瓶中取一块金属钠,用滤纸吸干表面上的
煤油,用小刀在玻璃片上切米粒大小的钠做实验用,由于钠容易和空气中的水蒸气反应生
成易燃性的氢气和强碱NaOH,且剩余的钠不污染原试剂瓶中的钠,所以剩余的钠要放回
原试剂瓶,不要随意丢弃。
(2)钠与硫酸镁溶液反应,钠先跟水反应生成氢氧化钠和氢气,生成的氢氧化钠再和硫酸镁反应生成氢氧化镁沉淀,化学方程式为:
MgSO +2NaOH=Mg(OH)↓+Na SO 。
4 2 2 4
(3)金属钠在重力的作用下,逐渐下落至煤油与 溶液的交界面,金属 与水反应,
有气泡生成,钠和水反应放热,所以钠熔化成小球,生成的氢气将钠托举上升,氢气逸出
后钠又回落,所以钠在煤油和 溶液界面处上下跳动,最终完全溶解。
(4)因反应生成的 又与 反应生成氢氧化镁沉淀,因此下层溶液出现白色沉淀。
(5)因钠与水反应消耗了 溶液中的水,且产生了 ,使装置内压强增大,将大试管
中的溶液压至长颈漏斗中,故大试管内液面下降,长颈漏斗内液面上升。
18.(1)CH
4
(2) CaO+H O=Ca(OH) 化合反应
2 2
(3) NaCO+Ca(OH) =CaCO +2NaOH 复分解反应
2 3 2 3
【分析】A是天然气的主要成分,A是CH,甲烷燃烧生成水和CO,A和B点燃生成C
4 2
和D,D和NaOH溶液反应生成C和G,C是水,D是CO,G是NaCO,E是一种常见的
2 2 3
食品干燥剂,C和E生成F,水和CaO反应生成Ca(OH) ,E是CaO,F是Ca(OH) ,F和G
2 2
生成H是沉淀和NaOH,NaCO 和Ca(OH) 反应生成CaCO 沉淀和NaOH,H是CaCO 。
2 3 2 3 3
(1)
根据分析,A为甲烷,分子式是CH;
4
(2)
根据分析,反应③是水和CaO反应生成Ca(OH) 的反应,方程式为CaO+H O=Ca(OH) ,属
2 2 2
于化合反应;
(3)
根据分析,反应④是NaCO 和Ca(OH) 反应生成CaCO 沉淀和NaOH的反应,方程式为
2 3 2 3
NaCO+Ca(OH) =CaCO +2NaOH,属于复分解反应。
2 3 2 3
答案第8页,共2页