文档内容
第五章化工生产中的重要非金属元素
第一节 硫及其化合物
第1课时 硫和二氧化硫
学校:___________姓名:___________班级:___________考号:___________
一、单选题
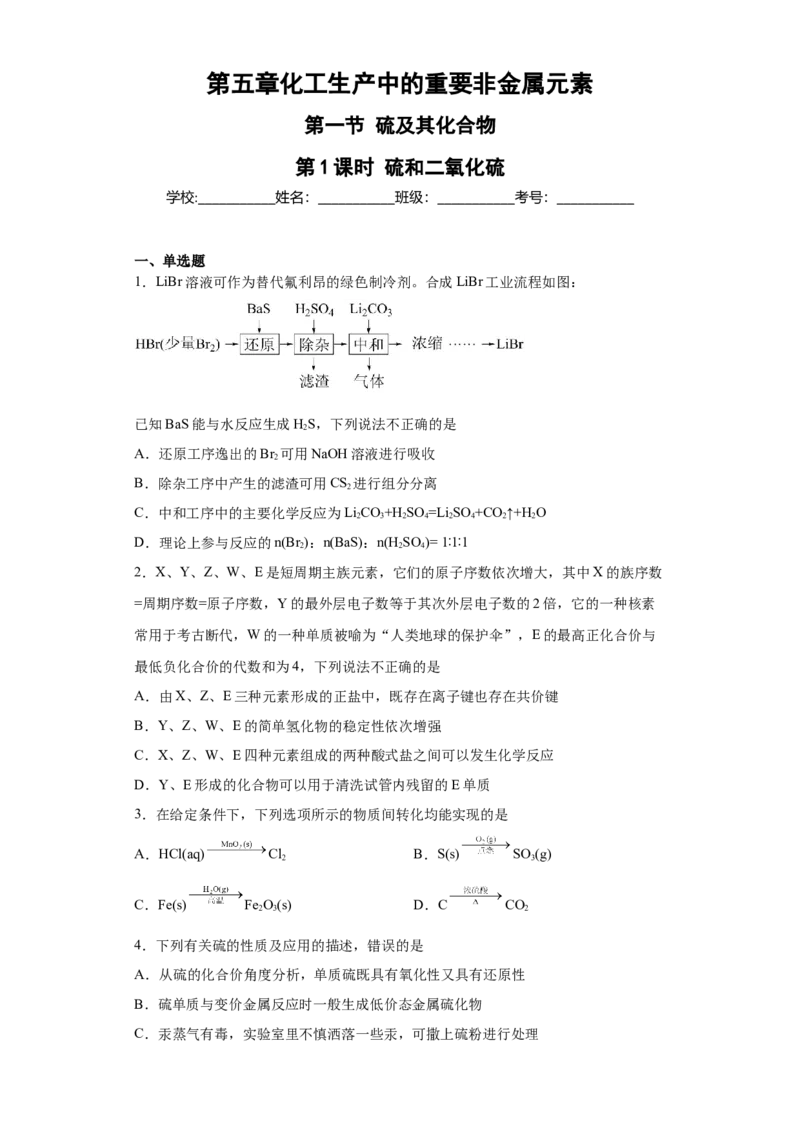
1.LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工业流程如图:
已知BaS能与水反应生成HS,下列说法不正确的是
2
A.还原工序逸出的Br 可用NaOH溶液进行吸收
2
B.除杂工序中产生的滤渣可用CS 进行组分分离
2
C.中和工序中的主要化学反应为LiCO+H SO =Li SO +CO ↑+H O
2 3 2 4 2 4 2 2
D.理论上参与反应的n(Br):n(BaS):n(H SO )= 1∶1∶1
2 2 4
2.X、Y、Z、W、E是短周期主族元素,它们的原子序数依次增大,其中X的族序数
=周期序数=原子序数,Y的最外层电子数等于其次外层电子数的2倍,它的一种核素
常用于考古断代,W的一种单质被喻为“人类地球的保护伞”,E的最高正化合价与
最低负化合价的代数和为4,下列说法不正确的是
A.由X、Z、E三种元素形成的正盐中,既存在离子键也存在共价键
B.Y、Z、W、E的简单氢化物的稳定性依次增强
C.X、Z、W、E四种元素组成的两种酸式盐之间可以发生化学反应
D.Y、E形成的化合物可以用于清洗试管内残留的E单质
3.在给定条件下,下列选项所示的物质间转化均能实现的是
A.HCl(aq) Cl B.S(s) SO (g)
2 3
C.Fe(s) Fe O(s) D.C CO
2 3 2
4.下列有关硫的性质及应用的描述,错误的是
A.从硫的化合价角度分析,单质硫既具有氧化性又具有还原性
B.硫单质与变价金属反应时一般生成低价态金属硫化物
C.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理D.单质硫燃烧时,氧气少量可生成SO ,氧气足量时可生成SO
2 3
5.学会识图能发展科学思维。下列图像与反应过程的变化趋势对应正确的有
序
① ② ③ ④
号
图
像
反 向含等质量HCl
向NaOH溶液中逐
应 的稀盐酸中分别 硫在充满 的
受热分解 滴加入稀盐酸至过
过 加入Zn和Fe至 集气瓶中燃烧
量
程 过量
A.1个 B.2个 C.3个 D.4个
6.中医中药的博大精深,其用药讲究十八反和十八畏,其中有“硫黄原是火中精,朴
硝一见便相争”,硫黄即硫单质。下列说法中正确的是
A.根据化合价可知,S在化学反应中只能作还原剂
B.硫是重要的非金属元素,其单质有多种同素异形体
C.过量的硫与铜反应生成CuS,表现了硫单质的氧化性
D.S+O SO ,S被氧化,作氧化剂
2 2
7.科学家发现微量硫化氢可以调节心血管功能。有关硫化氢的叙述正确的是
A.硫化氢很稳定,受热难分解
B.将硫化氢通入氯水中,氯水褪色并产生浑浊
C.硫化氢在足量氧气中燃烧生成淡黄色固体
D.硫化氢是弱电解质,其电离方程式是H 2 S ⇋ 2H+ + S2-
8.为探究铁和硫反应产物中铁的化合价,某同学设计了如下实验过程:
Fe、S混合粉末 黑色固体 滤渣 溶液A ……
已知:①铁和硫反应产物不溶于碱,能溶于硫酸;
试卷第2页,共3页②硫可溶于热碱溶液,发生类似Cl 和NaOH溶液的化学反应。
2
下列说法不正确的是
A.混合粉末应在N 氛围中进行加热,所用HSO 溶液应先煮沸
2 2 4
B.取溶液A,滴加KSCN溶液,未出现红色,可证明铁和硫反应只有+2价铁生成
C.滤渣用稀HSO 溶解时应在通风橱中进行
2 4
D.硫溶于热碱溶液可能发生的离子反应是3S+6OH- 2S2-+ +3H O
2
9.下列有关单质硫的说法中,不正确的是
A.硫单质与变价金属反应时一般生成低价态的金属硫化物
B.单质硫燃烧时,氧气少量时生成SO ,氧气足量时可通过一步反应生成SO
2 3
C.残留在试管内壁上的硫可用CS 溶解除去,也可用热的NaOH溶液除去
2
D.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理
10.下列有关物质的性质与用途具有对应关系的是
A.硫酸钡难溶于盐酸,可用作检查肠胃的内服药剂
B. 具有氧化性,可用于漂白纸浆
C.硫磺为淡黄色固体,可用作制硫磺皂
D. 易溶于水,可用于净水
11.古代四大发明之一黑火药的配方“一硫二硝三木炭”,爆炸时产生N、CO 气体
2 2
和大量的烟。下列说法正确的是
A.配方中“硝”是指硝酸,作氧化剂 B.着火时只因产生气体而爆炸
C.硫是指硫黄,作还原剂 D.大量的烟是KS
2
12.某兴趣小组为了探究SO 气体还原Fe3+的反应,他们使用的药品和装置如下图所
2
示,下列说法不合理的是
A.能表明I-的还原性弱于SO 的现象是B中蓝色溶液褪色
2
B.装置C的作用是吸收SO 尾气,防止污染空气
2
C.为了验证A中发生了氧化还原反应,加入酸性KMnO 溶液,紫色褪去
4D.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl 溶液,产生白色沉
2
淀
二、非选择题
13.氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水
是一种高效、无污染的制氢方法。其反应过程如图所示:
(1)反应I的化学方程式是_____。
(2)反应I得到的产物用I 进行分离。该产物的溶液在过量I 的存在下会分成两层——
2 2
含低浓度I 的HSO 层和高浓度的I 的HI层。
2 2 4 2
①根据上述事实,下列说法不正确的是_____(选填序号)。
a.两层溶液的密度存在差异
b.加I 前,HSO 溶液和HI溶液不互溶
2 2 4
c.I 在HI溶液中比在HSO 溶液中易溶
2 2 4
②经检测,HSO 层中c(H+):c(SO )=2.06:1。其比值大于2的原因是_____。
2 4
14.在无氧的条件下以干燥的钠汞齐(以Na-Hg表示)和干燥的二氧化硫一起振荡,得
固态化合物A。已知:A中钠元素的质量分数为26.44%,氧元素的质量分数为
36.78%,其余为S元素。1mol A暴露在潮湿空气中易吸收氧气而氧化,其氧化产物需
2 mol NaOH反应生成正盐。
(1)试确定A的化学式_______。
(2)若将A加热到402K时能产生一种刺激性气味的气体,固体质量减轻了18.39%。分
析得到的固体残渣,发现是与A含有相同元素的两种物质(记为B和C)。试写出A分
解的化学方程式_______。
15.阅读短文,回答问题。
燃放烟花爆竹是我国的传统习俗,烟花爆竹的主要成分有黑火药、特效药剂等。
试卷第4页,共3页黑火药由硝酸钾(KNO)、硫黄(S)和木炭组成,
3
燃烧时,瞬间产生大量气体,同时释放大量热,在有限的空间里,气体受热迅速膨胀
引起爆炸。特效药剂常含一些金属元素,燃烧时会产生五彩缤纷的火焰。(如右图所
示)
下表为几种金属元素的化合物燃烧时的火焰颜色:
所含金属元素 钠 钙 钡 铯
火焰颜色 黄 砖红色 黄绿 蓝
然而,传统的烟花爆竹不仅会污染环境,也会造成各种伤残及火灾事故。为了改善传
统烟花爆竹的不足,又能为人们的佳节祝兴,电子鞭炮应运而生。目前,常见的电子
鞭炮有三种形式。
第一,雷电式仿真电子鞭炮,不仅能发出普通鞭炮的模拟声,而且还能发出闪光,以
假乱真。无火药、无污染,不会发生伤残及火灾事故。能重复使用,大大减少经济支
出。其局限性是需要使用家用电源,不方便移动。
第二,电子鞭炮机,是一种使用煤气和氧气混合气体作为燃料的设备,声响大,与火
药鞭炮无异,但缺陷是点燃混合气体时存在一定的安全隐患。
第三,录音鞭炮,通过音频解码播放存储于芯片中的鞭炮录音,声音与功率大小有关。
这种鞭炮的优点是纯电能、可移动、造价低廉。缺点是仿真和氛围感度稍差。
新型电子鞭炮正在不断地被研发出来,更好地促进民俗与科技的融合。
依据上文,回答问题:
(1)若燃放烟花的火焰呈现黄绿色,则烟花中可能含有______元素。
(2)雷电式仿真电子鞭炮的优点有______(填序号)。
A.无火药、无污染
B.不会发生伤残及火灾事故
C.能重复使用,减少经济支出
(3)判断下列说法是否正确(填“对”或“错”)。
①燃放烟花爆竹时产生不同颜色的火焰,是因为药剂中含有不同的金属元素。______
②燃放烟花爆竹后会闻到刺激性的气味,是因为生成了二氧化碳。______
③电子鞭炮机在点燃混合气体时存在一定的安全隐患。______
④录音鞭炮的声音大小与功率无关。______
16.火山喷发是一种地质现象,是地壳运动的一种表现形式,喷发出的火山气体中
占 ,此外还含有 等。火山喷发可引起环境污染,也可使某些地区的土壤增加营养成分。
(1) 是黄铁矿的主要成分,其中S的化合价是_______。
(2)火山气体中的 与 发生反应生成S,冷却后沉积在火山口附近,该反应中的氧
化剂是_______。
(3)火山气体中的 与 在粉尘的催化下反应生成 的化学方程式是_______。
(4)火山喷发造成酸雨的原因是_______(用化学方程式表示),随时间的增长,酸雨的
_______(填“增大”“减小”或“不变”)。
(5)火山灰中富含植物生长所需要的营养元素,可作为化肥使土地更肥沃。请写出一种
钾肥的化学式_______。
试卷第6页,共3页参考答案:
1.C
【分析】HBr(Br )中加入BaS,将Br 还原为Br-,同时BaS转化为BaBr 和S;BaBr 与
2 2 2 2
HSO 反应生成BaSO 沉淀和HBr;过滤出滤渣BaSO 和S,滤液中的主要成分为HBr;加
2 4 4 4
入LiCO,与HBr反应生成LiBr、CO 等,得到的LiBr溶液经浓缩等操作后得到产品
2 3 2
LiBr。
【详解】A.还原工序逸出的Br 用NaOH溶液吸收,可以减小环境污染,A正确;
2
B.除杂工序中产生的滤渣为硫酸钡和硫,硫易溶于CS,而硫酸钡不溶于CS,因此可用
2 2
CS 进行组分分离,B正确;
2
C.由于溶液中存在大量的 ,故中和工序中发生的化学反应主要为:
,而用硫酸会引入新的杂质离子,C错误;
D.根据得失电子守恒可知, 和 反应时物质的量之比为 ,根据硫酸钡的化学组
成及钡元素守恒可知, 为 ,故参与反应的
,D正确;
故选C。
2.B
【分析】X、Y、Z、W、E是短周期主族元素,它们的原子序数依次增大,其中X的族序
数=周期序数=原子序数,X是H;Y的最外层电子数等于其次外层电子数的2倍,它的一
种核素常用于考古断代,Y是C;W的一种单质被喻为“人类地球的保护伞”,W是O,
则Z是N;E的最高正化合价与最低负化合价的代数和为4,E是S,据此解答。
【详解】A.由H、N、S三种元素形成的正盐如硫酸铵,既存在离子键也存在共价键,A
正确;
B.非金属性越强,简单氢化物越稳定,非金属性O>N>S>C,则简单氢化物的稳定性是
O>N>S>C,B错误;
C.H、N、O、S四种元素组成的两种酸式盐,硫酸氢铵和亚硫酸氢铵之间可以发生化学反
应,C正确;
D.硫单质易溶于二硫化碳,Y、E形成的化合物二硫化碳,可以用于清洗试管内残留的硫单质,D正确;
故选B。
3.D
【详解】A.浓盐酸只有在加热条件下才能与MnO 反应制取Cl,常温下,即便是浓盐酸,
2 2
也不能与MnO 发生反应,A不正确;
2
B.S(s)与O 在点燃条件下反应,只能生成SO (g),B不正确;
2 2
C.Fe(s)与水蒸气在高温下发生反应,生成Fe O(s)和H,C不正确;
3 4 2
D.C与浓硫酸在加热条件下反应,生成CO、SO 等,D正确;
2 2
故选D。
4.D
【详解】A.硫单质中硫元素为0价,位于中间价态,既有还原性又有氧化性,A项正确;
B.硫单质的氧化性较弱,与变价金属反应时一般生成低价态金属硫化物,如S与Fe、Cu
反应分别生成FeS、Cu S,B项正确;
2
C.汞可与S发生反应Hg+S=HgS,所以可用硫粉处理Hg,C项正确;
D.单质硫燃烧时,产物只有SO ,无论O 的量是否充足,均不会生成SO ,D项错误:
2 2 3
故选D。
5.C
【详解】①高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,氧气是气体,逸出,根据质
量守恒定律,反应前后物质的总质量相等,故随着反应的进行,固体逐渐减小,但不会为
0,故①错误;
②锌、铁与盐酸反应都生成氢气,Zn+2HCl═ZnCl +H ↑;Fe+2HCl=FeCl +H ↑,由于锌、铁
2 2 2 2
过量,盐酸完全反应,根据质量守恒定律,反应前后元素的质量不变,氯化氢质量相等,
最终生成氢气质量相等,横坐标是金属的质量,等量盐酸消耗锌的质量大,故②正确;
③向一定量的氢氧化钠溶液中逐滴加入稀盐酸至过量,溶液的pH从大于7逐渐的减小到
7,稀盐酸过量后,溶液的pH小于7,故③正确;
④硫在氧气中燃烧,放热,故温度升高,但反应结束,冷却降温,温度减小,最终恢复原
来温度,故④正确;
故选:C。
6.B
【详解】A.S单质的化合价为0,是S的中间价态,故S既可作氧化剂,又可作还原剂,
A错误;
答案第2页,共2页B.硫是重要的非金属元素,其单质有多种同素异形体,有斜方硫、单斜硫和弹性硫等,B
正确;
C.硫的氧化性较弱,与变价金属化合时,只能生成低价态金属硫化物,如S与Fe、Cu反
应,生成FeS、Cu S,C错误;
2
D.反应中S被氧化,化合价升高,作还原剂,D错误;
故选B。
7.B
【详解】A、硫的非金属性比氯弱,故其氢化物易分解,故A错误;
B、氯气具有强氧化性,硫化氢具有还原性,发生反应生成HCl和S,故褪色和产生浑浊,
故B正确;
C、在足量的氧气中燃烧生成SO ,故C错误;
2
D、多元弱酸分步电离,故D错误;
答案选B。
8.B
【分析】Fe、S混合粉末加热,得到黑色固体,加入足量热的KOH溶液,S溶于热碱液,
铁和硫反应的产物不溶,过滤得到的滤渣中含铁和硫反应的产物,滤渣中加入稀硫酸,铁
和硫反应的产物溶解,然后加试剂检验阳离子从而判断铁和硫反应产物中铁的化合价。
【详解】A.铁和硫都能和空气中的氧气反应,所以铁和硫的混合粉末应在氮气氛围中加
热,所用硫酸溶液应先煮沸,除去溶于其中的氧气,故A正确;
B.铁和硫反应的产物溶于稀硫酸中,若铁和硫反应的产物中含有三价铁的同时还有剩余
的铁单质,当加入稀硫酸后,三价铁会被铁还原为正二价,向溶液A中滴加KSCN溶液,
未出现红色,不能证明铁和硫反应只有+2价铁生成,故B错误;
C.滤渣中可能含有FeS,FeS可以和稀硫酸反应生成有毒气体HS,所以滤渣用稀HSO
2 2 4
溶解时应在通风橱中进行,故C正确;
D.硫可溶于热碱溶液,发生类似Cl 和NaOH溶液的化学反应,即发生歧化反应,生成
2
NaS、NaSO 和水,选项中的离子方程式正确;
2 2 3
故选B。
9.B
【详解】A.硫单质的氧化能力较弱,与变价金属反应时,一般生成低价态的金属硫化物,
如Fe与S反应生成FeS,Cu与S反应生成Cu S,A正确;
2
B.单质硫燃烧时,不管氧气的用量如何,都只能生成SO ,B不正确;
2C.硫易溶于CS,所以可用CS 洗涤试管内壁的硫,也可用热的NaOH溶液洗涤,因为S
2 2
与NaOH反应可生成NaS、NaSO 等,C正确;
2 2 3
D.汞在常温下能与硫反应,生成不挥发的HgS,从而避免汞蒸气的挥发,D正确;
故选B。
10.A
【详解】A.胃酸的主要成分是盐酸,利用硫酸钡难溶于盐酸的性质,决定BaSO 可用作
4
检查肠胃的内服药剂,A符合题意;
B.SO 的漂白不是氧化性漂白,故SO 漂白纸浆不是因为SO 具有氧化性,而是因为SO
2 2 2 2
具有漂白性,B不合题意;
C.硫磺用于制硫磺皂是利用硫磺有毒性,可使蛋白质发生变性,故能够杀菌消毒,与硫
磺为淡黄色固体无关,C不合题意;
D.明矾 用于净水是由于其电离出的Al3+能够发生水解生成氢氧化铝胶
体,具有很强的吸附性,与其易溶于水无关,D不合题意;
故答案为:A。
11.D
【分析】黑火药爆炸反应方程式为S+2KNO +3C=K S+3CO+N 。
3 2 2 2
【详解】A.黑火药由硫磺、木炭、硝酸钾混合而成,配方中“硝”是指硝酸钾,故A错
误;
B.着火时,除了因放出气体而爆炸外,还因为放出大量的热使产生气体膨胀而爆炸,故B
错误;
C.硫是指硫黄,S元素化合价降低生成KS,硫作氧化剂,故C错误;
2
D.爆炸时生成KS、CO、N,CO、N 是无色气体,大量的烟是KS,故D正确;
2 2 2 2 2 2
选D。
12.C
【分析】 先后通入 溶液、含淀粉的碘水中,根据溶液颜色的变化来探究 与
反应的情况,多余的 最后通入 溶液进行吸收,防止染污空气。
【详解】A.向含有淀粉的碘水中通入 气体,会发生反应 ,
答案第4页,共2页被消耗,B中蓝色溶液褪色,证明物质的还原性强弱为 ,A正确;
B. 是大气污染物,且是酸性气体,可以与 反应而被吸收,装置C可吸收 尾
气,防止污染空气,B正确;
C.若A中 与 不发生反应,加入酸性 溶液时, 被 还原,溶液
紫色褪去;若A中 与 发生反应,生成的 可使加入的 被还原,溶液紫
色也褪去,因此不能验证A中是否发生了氧化还原反应,C错误;
D.若A中发生了氧化还原反应 ,溶液中含有硫酸,
当加入用稀盐酸酸化的 溶液时,会发生反应 ,产生白
色沉淀;若没有发生氧化还原反应,由于 酸性强于 ,当向溶液中加入用稀盐酸
酸化的 溶液时,不产生白色沉淀,D正确;
故选C。
13.(1)SO +2H O+I =H SO +2HI
2 2 2 2 4
(2) b 硫酸层中含少量的HI,且HI电离出氢离子
【详解】(1)根据反应过程,反应Ⅰ中的反应物是SO 、HO、I,产物是HSO 和HI,
2 2 2 2 4
其反应方程式为SO +2H O+I =H SO +2HI;故答案为SO +2H O+I =H SO +2HI;
2 2 2 2 4 2 2 2 2 4
(2)①a.根据信息可知,产物中存在分层,说明两层溶液的密度存在差异,故a说法正
确;
b.加碘单质前,硫酸溶液和HI溶液互溶,故b说法错误;
c.碘单质与I-反应:I+I- I ,增加了碘单质的溶解度,碘单质在HI溶液中比在HSO
2 2 4
溶液中易溶,故c说法正确;
答案为b;②H SO 溶液中c(H+)与c(SO )的比值为2∶1,但硫酸层中含有HI,HI为强酸,HI电离出
2 4
H+,使得中c(H+)与c(SO )的比值大于2∶1,故答案为硫酸层中含少量的HI,且HI电离出
氢离子。
14.(1)Na SO
2 2 4
(2) ↑
【解析】(1)
A中钠元素的质量分数为26.41%,氧元素的质量分数为36.76%,其余为S元素,则S元素
质量分数为1-26.41%-36.76%=36.83%,则Na、S、O原子数目之比为
,故A为NaSO;
2 2 4
(2)
若将A加热到402K时,质量减轻了18.39% ,1molA分解时减少的质量为( 46+64+64 )
g×18.39%=32g,则剩余固体质量为174g-32g=142g ,1mol硫的含氧酸盐均含有2mol钠离
子,故剩余固体为1mol,平均相对分子质量为142,而硫酸钠的相对分子质量为142,由
于为混合物,故含有NaSO ,NaSO 中S元素的化合价为+3,故另一固体中S元素化合价
2 3 2 2 4
应小于3,可能为NaSO,生成的氧化物为SO 时符合关系,故反应方程式为
2 2 3 2
↑ 。
15. 钡 A、B、C 对 错 对 错
【分析】(1)钡元素的焰色反应为黄绿色;
(2)雷电式仿真电子鞭炮,不仅能发出普通鞭炮的模拟声,且能随着响声并发出闪光,以
假乱真,无火药、无污染,不会发生伤残及火灾事故,又能重复使用,还能大大减少经济
支出;
(3)①燃放时,烟花中某些金属元素发生焰色反应而呈现绚丽缤纷的颜色;
②燃放烟花爆竹后会闻到刺激性的气味,是因为生成了二氧化硫;
③电子鞭炮机是一种使用煤气和氧气混合的设备;
④录音鞭炮通过音频解码播放存储于芯片中的鞭炮录音。
答案第6页,共2页【详解】(1)节日施放的焰火五彩缤纷,是因为火药当中加入了一些金属元素,火焰呈现
黄绿色时,烟花中放入了含钡离子的化合物,故答案为钡;
(2)雷电式仿真电子鞭炮,不仅能发出普通鞭炮的模拟声,且能随着响声并发出闪光,以
假乱真,无火药、无污染,不会发生伤残及火灾事故,又能重复使用,还能大大减少经济
支出,故答案为A、B、C;
(3)①烟花中添加含钾、钠、钙、铜等某些金属元素的化合物,燃放时发生焰色反应而呈
现绚丽缤纷的颜色,①正确,故答案为对;
②燃放烟花爆竹时,会产生一种刺激性气味的气体,是因为烟花爆竹中的硫燃烧生成二氧
化硫,②错误,故答案为错;
③电子鞭炮机是一种使用煤气和氧气混合的设备,声响大,与火药鞭炮无异,但缺陷是混
合气体点燃存在一定的安全隐患,③正确,故答案为对;
④录音鞭炮通过音频解码播放存储于芯片中的鞭炮录音,声音与功率大小有关,④错误,
故答案为错。
【点睛】本题考查环境污染及治理,侧重于化学与生活、环保的考查,把握焰色反应及相
关物质的污染性以及治理方法是解答关键。
16.(1)-1
(2)
(3)2 + 2
(4) SO +H O═H SO 、2HSO +O ═2H SO 减小
2 2 2 3 2 3 2 2 4
(5)KCl
【解析】(1)
中Fe元素是+2价,则S的化合价是-1;
(2)
与 发生反应生成S, 中S化合价从+4降至0价,该反应中的氧化剂是 ;
(3)
与 在粉尘的催化下反应生成 的化学方程式是2 + 2 ;
(4)火山爆发产生的二氧化硫和水反应生成亚硫酸,亚硫酸再被氧气氧化生成硫酸,则形成酸
雨的化学方程式为SO +H O═H SO 、2HSO +O ═2H SO ;随时间的增长,亚硫酸能与氧
2 2 2 3 2 3 2 2 4
气反应生成硫酸,酸性增强,则酸雨的 减小;
(5)
一种钾肥的化学式为KCl。
答案第8页,共2页