文档内容
2022--2023学年必修第二册RJ第5章第二节 氮及其化合物
硝酸 酸雨及其防治专题三
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.关于硝酸的说法中正确的是
A.硝酸电离出的H+,能被Zn还原成H
2
B.常温下,向浓HNO 中投入Fe片,会产生大量的红棕色气体
3
C.王水是浓硝酸和浓盐酸体积比为3∶1的混合物,能溶解金和铂
D.浓硝酸和稀硝酸都是强氧化剂
2.下列说法正确的是
A.浓硝酸保存在棕色瓶内仅是因为硝酸易挥发
B.与金属反应时,稀HNO 可能被还原为更低价态,说明稀HNO 氧化性强于浓
3 3
HNO
3
C.SO 、漂白粉、活性炭、NaO 都能使品红溶液褪色,其褪色原理有两种物质相同
2 2 2
D.N 分子的结构稳定,因此氮气不能支持任何物质的燃烧
2
3.化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是
选
操作或做法 目的
项
A 将铜丝插入浓硝酸中 制备NO
B 工业酒精中加生石灰,蒸馏 工业酒精制备无水乙醇
C 将溴水滴入KI 溶液中,加入乙醇并振荡 萃取溶液中生成的碘
D 实验结束,将剩余NaCl固体放回原试剂瓶 节约试剂
A.A B.B C.C D.D
4.在如图所示的蓝色石蕊试纸上,X、Y、Z三处分别滴加浓硝酸、浓硫酸和新制的
氯水,三处最后呈现的颜色分别是
A.白、黑、白 B.红、黑、红 C.红、红、白 D.红、黑、白
5.下列反应既是吸热反应,又是氧化还原反应的是A. B.
C. D.
6.下列单质或化合物性质的描述正确的是
A.NaHSO 水溶液显中性
4
B.NO 溶于水时发生氧化还原反应
2
C.SiO 与酸、碱均不反应
2
D.Fe在足量Cl 中燃烧生成FeCl 和FeCl
2 2 3
7.酸性条件下,可发生如下反应:2XO +16H++10Cl-=2X2++5Cl↑+8H O,XO 中X
2 2
的化合价是
A.+4 B.+5 C.+6 D.+7
8.2021年5月9日,我国第一所培养“碳中和”领域专门人才的新型研究型学院——
西北大学榆林碳中和学院成立。下列措施或方法无助于实现“碳中和”的是
A.可用碳酸钠溶液捕捉(吸收)
B.煤中添加石灰石,以减少二氧化硫对环境的污染
C.开发新型光伏电池材料,提高太阳能电池的光电转换效率
D.开发新型催化剂直接利用太阳能和水制备氢气,制造氢能汽车
9.下列气体排放到空气中,会导致酸雨的是
A. B. C. D.
10.下列过程不涉及氧化还原反应的是
A.黑火药的爆炸
B.丹砂( )烧之成水银,积变又成丹砂
C.利用明矾溶液清除铜绿
D.湿法炼铜
11.下列有关物质的性质与用途具有对应关系的是
A.SO 具有氧化性,可用于漂白纸浆
2
B.CaO能与水反应,可用作食品干燥剂
C.硅晶体熔点高,可用于制造半导体芯片
D.浓硝酸具有酸性,可用于洗涤附有银镜的试管
试卷第2页,共3页12.类推的思维方法可以预测许多物质的性质。但类比是相对的,不能违背客观事实。
下列类比正确的是
A. 与浓 加热可制 ,则 与浓 加热可制
B. 与S加热直接化合生成 ,则 与S加热也能直接化合生成
C.适量 通入 溶液中可生成 和 ,则适量 通入
溶液中也可生成 和
D. 通入 溶液不产生沉淀,则 通入 溶液也不产生沉淀
13.下列说法错误的是
A.蒸发结晶时,将溶液蒸干后才停止加热 B.配制溶液定容时,应使溶液的凹液面
与容量瓶的刻度线相切
C.酒精着火时可用湿的抹布盖灭 D.试管内壁的银镜可用稀硝酸洗涤
14.HS是无色有恶臭味的有毒气体,下列说法不正确的是
2
A.硫化氢能被氧气、氯气、碘、溴等单质氧化成硫单质
B.将HS通入足量的氢氧化钠溶液,可得到含NaS的溶液
2 2
C.将HS气体通入CuSO 溶液中得到CuS沉淀,通入FeSO 溶液会产生FeS沉淀
2 4 4
D.HS通入到FeCl 溶液中,溶液酸性增强
2 3
二、计算题
15.钠是活泼金属,受热后与氧气剧烈反应,发出黄色火焰,生成一种淡黄色固体
——过氧化钠,由于空气中还有其它成分,因此可能还有一些同时发生的其它反应”。
某校化学兴趣小组同学据此进行了有关探究。
【猜想】钠在空气中燃烧,生成过氧化钠、氧化钠,还有氮化钠。
【查阅资料】氮化钠与水反应能生成氢氧化钠和氨气。
【实验】①取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸
性气体的空气),用酒精灯加热薄铁皮,钠燃烧;
②将燃烧产物投入水中,得到0.224L(折算成标准状态)气体和1000mL溶液;
③经检验,该气体为纯净的氧气;
④从1000mL溶液中取出25.00mL溶液,加入1.00mol·L-1HCl溶液至13.50mL时恰好完
全反应。【结论】
(1)通过计算确定钠的燃烧产物中是否含有氮化钠___________。
(2)计算钠在空气中燃烧产物中各成分的物质的量之比___________。
三、实验题
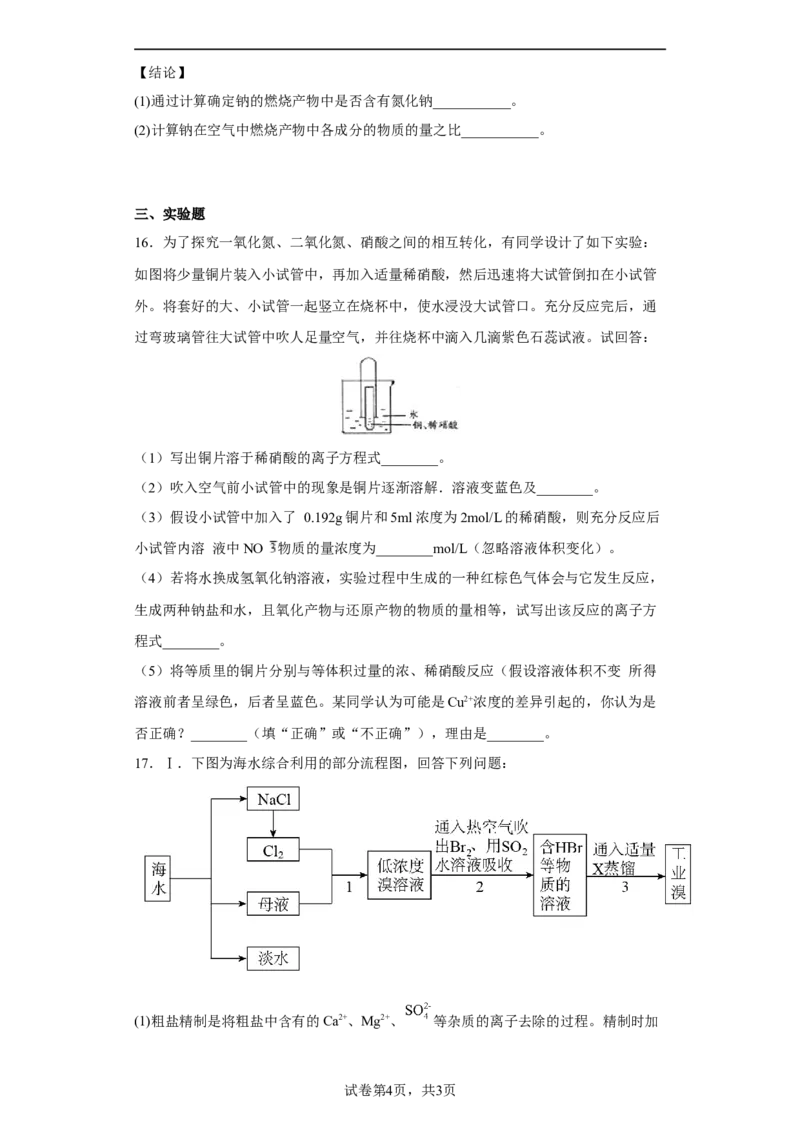
16.为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:
如图将少量铜片装入小试管中,再加入适量稀硝酸,然后迅速将大试管倒扣在小试管
外。将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口。充分反应完后,通
过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴入几滴紫色石蕊试液。试回答:
(1)写出铜片溶于稀硝酸的离子方程式________。
(2)吹入空气前小试管中的现象是铜片逐渐溶解.溶液变蓝色及________。
(3)假设小试管中加入了 0.192g铜片和5ml浓度为2mol/L的稀硝酸,则充分反应后
小试管内溶 液中NO 物质的量浓度为________mol/L(忽略溶液体积变化)。
(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,
生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,试写出该反应的离子方
程式________。
(5)将等质里的铜片分别与等体积过量的浓、稀硝酸反应(假设溶液体积不变 所得
溶液前者呈绿色,后者呈蓝色。某同学认为可能是Cu2+浓度的差异引起的,你认为是
否正确?________(填“正确”或“不正确”),理由是________。
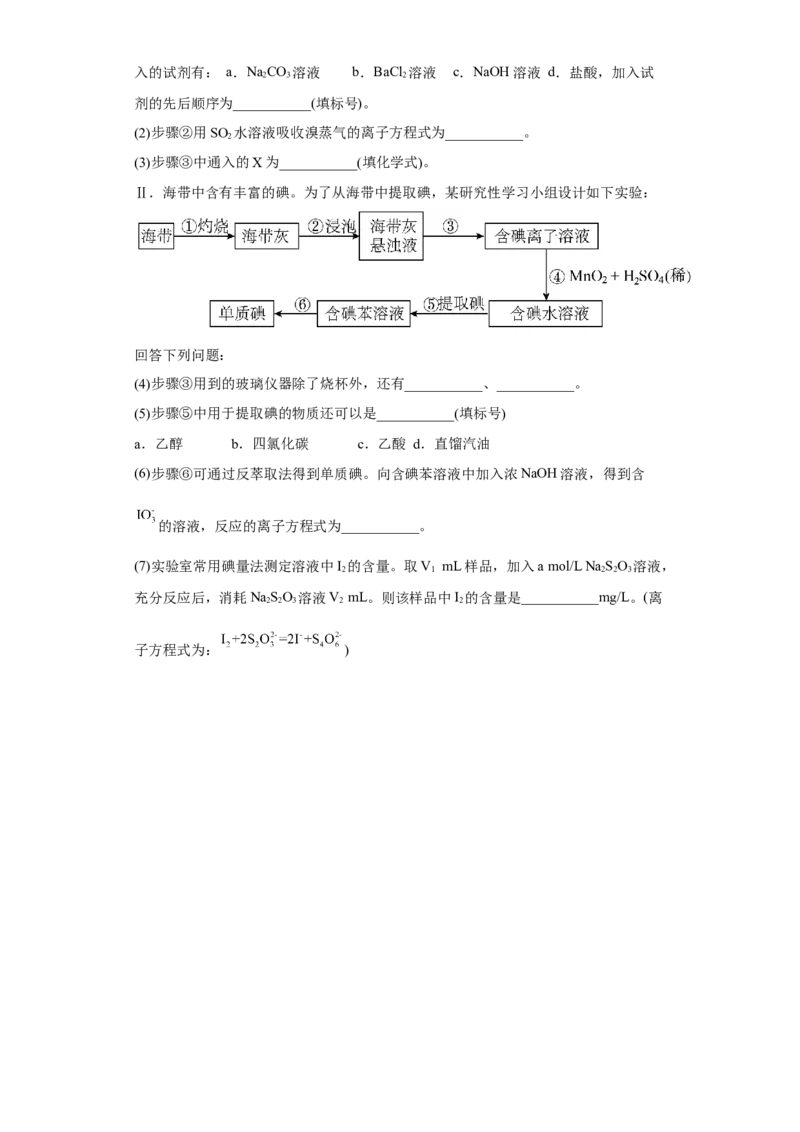
17.Ⅰ.下图为海水综合利用的部分流程图,回答下列问题:
(1)粗盐精制是将粗盐中含有的Ca2+、Mg2+、 等杂质的离子去除的过程。精制时加
试卷第4页,共3页入的试剂有: a.NaCO 溶液 b.BaCl 溶液 c.NaOH溶液 d.盐酸,加入试
2 3 2
剂的先后顺序为___________(填标号)。
(2)步骤②用SO 水溶液吸收溴蒸气的离子方程式为___________。
2
(3)步骤③中通入的X为___________(填化学式)。
Ⅱ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:
回答下列问题:
(4)步骤③用到的玻璃仪器除了烧杯外,还有___________、___________。
(5)步骤⑤中用于提取碘的物质还可以是___________(填标号)
a.乙醇 b.四氯化碳 c.乙酸 d.直馏汽油
(6)步骤⑥可通过反萃取法得到单质碘。向含碘苯溶液中加入浓NaOH溶液,得到含
的溶液,反应的离子方程式为___________。
(7)实验室常用碘量法测定溶液中I 的含量。取V mL样品,加入a mol/L Na SO 溶液,
2 1 2 2 3
充分反应后,消耗NaSO 溶液V mL。则该样品中I 的含量是___________mg/L。(离
2 2 3 2 2
子方程式为: )参考答案:
1.D
【详解】A.硝酸电离出的H+,其氧化能力比 弱,所以 能优先被Zn还原成氮的
氧化物等,A不正确;
B.常温下,向浓HNO 中投入Fe片,Fe片发生钝化,不会产生大量的红棕色气体,B不
3
正确;
C.王水是浓硝酸和浓盐酸按体积比为1∶3组成的混合物,它具有很强的氧化性,能溶解金
和铂,C不正确;
D.浓硝酸和稀硝酸都是强氧化剂,与金属反应,通常都生成氮的氧化物,不生成氢气,D
正确;
故选D。
2.C
【详解】A. 浓硝酸保存在棕色瓶内主要是因为硝酸见光易分解,A不正确;B. 与金属反
应时,稀HNO 可能被还原为更低价态,不能说明稀HNO 氧化性强于浓HNO,物质的氧
3 3 3
化性的强弱与得到电子的多少无关,只与得到电子的难易有关,B不正确;C. SO 、漂白
2
粉、活性炭、NaO 都能使品红溶液褪色, SO 可与品红化合成无色物质,活性炭可吸附
2 2 2
品红,漂白粉和NaO 可以把品红氧化为无色物质,C正确;D. 虽然N 分子的结构稳定,
2 2 2
通常不支持燃烧,但是氮气可以支持镁条燃烧,D不正确。本题选C。
3.B
【详解】A.铜与浓硝酸反应生成NO ,故A不选;
2
B.生石灰中含有CaO,能与HO反应生成Ca(OH) ,可向工业酒精中加生石灰,再蒸馏制
2 2
备无水乙醇,故B选;
C.乙醇能与水混溶,不满足从水中萃取I 的萃取剂选择要求,故C不选;
2
D.固体试剂取出后不能放回原试剂瓶,避免试剂污染,故D不选;
综上所述,答案为B。
4.A
【详解】因硝酸具有强氧化性,能使试纸褪色,则滴加浓硝酸,先变红后褪色,最后为白
色;浓硫酸具有脱水性,则能使蓝色石蕊试纸最后变为黑色;因氯水中含有盐酸和次氯酸,
新制氯水具有漂白性,则在试纸上滴加氯水,先变红后褪色,最后为白色。
故选A。5.A
【详解】A.C与CO 反应生成CO是吸热反应,其中C元素的化合价由0价、+4价变成
2
+2价,是氧化还原反应,A符合题意;
B.CaCO 反应生成CaO和CO,属于分解反应,是吸热反应,反应中没有化合价的改变,
3 2
不是氧化还原反应,B不符合题意;
C.H 和O 反应生成HO,燃烧是放热反应,H元素化合价由0价变成+1价,O元素化合
2 2 2
价由0价变成-2价,是氧化还原反应,C不符合题意;
D.HCl与NaOH反应生成NaCl和HO,中和反应是放热反应,反应中没有化合价的改变,
2
不是氧化还原反应,D不符合题意;
故选A。
6.B
【详解】A.NaHSO 在水中的电离方程式为:NaHSO=Na++H++SO2﹣溶液呈酸性,故A错
4 4 4
误;
B.NO 与水反应为3NO +H O═2HNO +NO,反应中氮元素的化合价发生变化,由NO 中
2 2 2 3 2
+4价升高为HNO 中+5价,由NO 中+4价降低为NO中+2价,NO 既是氧化剂也是还原剂,
3 2 2
故B正确;
C.氢氟酸能和二氧化硅发生SiO+4HF═SiF ↑+2H O,玻璃中含有二氧化硅,常用此反应
2 4 2
在玻璃上刻字;氢氧化钠能和二氧化硅发生2NaOH+SiO ═Na SiO+H O,实验室盛放氢氧
2 2 3 2
化钠溶液的试剂瓶不能用玻璃塞,其原因是玻璃中的SiO 与NaOH反应,生成具有粘性的
2
NaSiO,会粘住瓶塞,故C错误;
2 3
D.氯气具有强氧化性,金属铁具有较强的还原性,氯气和金属反应生成高价金属,能将
铁氧化成+3价的铁,氯气和金属铁反应的产物是氯化铁,Cl 与铁粉加热时发生反应的化
2
学方程式为2Fe+3Cl FeCl ,故D错误;
2 3
故选B.
【点评】本题主要考查了元素化合物的知识,考查角度广,要求学生具有分析和解决问题
的能力,平时注意相关知识的积累,题目难度中等.
7.D
【分析】根据离子方程式的电荷守恒以及化合价规则计算判断。
【详解】离子方程式前后遵循电荷守恒,所以2×(-n) +16×(+1)+10×(-1) =2×(+2),解得:
答案第2页,共2页n=1,根据化合价规则,XO 中为-2价,所以X元素的化合价为+7价,故选D。
8.B
【详解】A.可用碳酸钠溶液捕捉(吸收) ,利于实现碳中和,A不符合;
B.煤中添加石灰石,以减少二氧化硫对环境的污染,但不能减少二氧化碳排放,不利于
实现碳中和,B符合;
C.开发新型光伏电池材料,提高太阳能电池的光电转换效率,减少CO 的排放,利于实
2
现碳中和,C不符合;
D.开发新型催化剂直接利用太阳能和水制备氢气,制造氢能汽车,减少CO 的排放,利
2
于实现碳中和,D不符合。
故答案选B。
9.D
【详解】A.NH 溶于水形成碱性溶液,不可能形成酸雨,选项A不合题意;
3
B.CO 与雨水反应生成碳酸,浓度不同时,其pH不同,但pH≥5.6,不属于酸雨,选项B
2
不合题意;
C.N 难溶于水,雨水呈中性,选项C不合题意;
2
D. 与雨水反应生成HSO ,继续氧化生成硫酸,使雨水的pH<5.6,选项D符合题意;
2 3
答案选D。
10.C
【分析】
【详解】
A.黑火药由木炭、硫磺粉、硝酸钾按照一定比例混合而成,爆炸时的化学反应为2KNO
3
+3C+S KS+N↑+3CO↑,有化合价的变化,涉及氧化还原反应,A不选;
2 2 2
B.其中涉及的反应有HgS Hg+S,Hg+S=HgS,有化合价的变化,涉及氧化还原反应,
B不选;C.明矾中的Al3+在水溶液中能够水解,Al3++3HO Al(OH) +3H+,使得溶液呈酸性;
2 3
铜绿的主要成分是Cu (OH) CO,能溶于酸,整个过程中化合价不变,不涉及氧化还原反
2 2 3
应,C符合题意;
D.湿法炼铜涉及的反应为CuSO +Fe=FeSO +Cu,有化合价的变化,涉及氧化还原反应,
4 4
D不选;
答案选C。
11.B
【详解】A.SO 是化合漂白,不具有强氧化性,可用于漂白纸浆,故A错误;
2
B.氧化钙具有吸水性,可以用作食品干燥剂,故B正确;
C.晶体硅位于金属与非金属的交界处,则用于制作半导体材料,与熔点、硬度无关,故C
错误;
D.稀硝酸有强氧化性,能将银氧化,与酸性无关,故D错误。
答案选B。
12.B
【详解】A.NaCl与浓 加热可制HCl,原理为难挥发性酸制易挥发性酸,同理NaBr
与浓 加热时浓硫酸会将NaBr氧化而得不到HBr,A错误;
B.硫单质的氧化性较弱,与金属单质反应时都生成低价态的金属硫化物,故 与S加热
直接化合生成 ,则 与S加热也能直接化合生成 ,B正确;
C. 通入 溶液中可生成 和 ,是因为强酸制弱酸,但是 具有
氧化性,会将 氧化为硫酸钙,C错误;
D.SO 通入BaCl 溶液不产生沉淀,是因为弱酸不能制取强酸,但SO 通入Ba(NO ) 溶液
2 2 2 3 2
中,SO 溶于水,生成亚硫酸使溶液呈现酸性,溶液中存在硝酸根离子,将SO 氧化成
2
SO ,会生成硫酸钡沉淀,D错误;
答案第4页,共2页答案为B。
13.A
【详解】A.蒸发结晶时,将溶液蒸发到有大量晶体析出时就停止加热,利用余热继续蒸
干,防止余热让晶体分解或者失去结晶水,造成产品不纯,A错误;
B.配制溶液定容时,应使溶液的凹液面与容量瓶的刻度线相切,B正确;
C.酒精着火时不可用水浇灭,可用湿的抹布或者沙土盖灭,C正确;
D.由于3Ag+4HNO (稀)=3AgNO +NO+2HO,试管内壁的银镜可用稀硝酸洗,D正确;
3 3 2
故答案为:A。
14.C
【详解】A.氧气、氯气、碘、溴等单质的氧化性强于硫单质,故硫化氢能被氧气、氯气、
碘、溴等单质氧化成硫单质,A正确;
B.少量硫化氢与过量氢氧化钠溶液反应生成NaS,B正确;
2
C.FeS相对于CuS溶解度较大,会溶于稀硫酸,所以将HS气体通入FeSO 溶液中得不
2 4
FeS沉淀,C错误;
D.HS通入到FeCl 溶液中,Fe3+将S2-氧化,发生反应:H S+2Fe3+=S↓+2Fe2++2H+,氢离子
2 3 2
浓度增大,酸性增强,D正确;
故选C。
15.(1)有
(2)2:17:4
【解析】(1)
由题意可知,过氧化钠、氧化钠、氮化钠都能与水反应生成氢氧化钠,由钠原子个数守恒
可知,25.00mL溶液中氢氧化钠的物质的量为 × =0.0125mol,反应消耗盐酸的
物质的量为1.00mol/L×0.0 135L=0.0135mol,消耗盐酸的物质的量大于溶液中氢氧化钠的物
质的量,说明溶液中含有一水合氨的物质的量为(0.0135mol—0.0125mol)=0.001mol,所以
钠的燃烧产物中含有氮化钠,故答案为:有;
(2)由钠原子的原子个数守恒可知,溶液中氢氧化钠的物质的量为 =0.5mol,过氧化
钠与水反应生成氢氧化钠和氧气,反应的化学方程式为2NaO+2H O=4NaOH+O ↑,反应
2 2 2 2
生成0.224L氧气,则过氧化钠和反应生成氢氧化钠的物质的量分别为
×2=0.02mol和 ×4=0.04mol;氮化钠与水反应生成氢氧化钠和一水合氨,反应的
化学方程式为NaN+3HO=3NaOH+NH ·H O,由反应消耗盐酸的物质的量可知,由25ml
3 2 3 2
溶液中一水合氨的物质的量为0.001mol可知,氮化钠和反应生成氢氧化钠的物质的量分别
为0.001mol×40=0.04mol和0.001mol×3×40=0.12mol,则燃烧生成氧化钠的物质的量为
=0.17mol,则燃烧产物中过氧化钠、氧化钠、氮化钠的物质的量
比为0.02mol:0.17mol:0.04mol =2:17:4,故答案为:2:17:4。
16. 3Cu+8H++2NO—=3Cu2++2NO↑+4HO 有红棕色气体生成 1.6
3 2
2NO +2OH﹣=NO—+NO—+H O 不正确 等质量的铜与等体积的浓、稀硝酸反应
2 2 3 2
后,所得溶液中Cu2+的浓度相等
【分析】(1)铜和稀硝酸反应生成硝酸铜、一氧化氮和水;(2)稀硝酸和铜反应生成硝
酸铜、一氧化氮和水,一氧化氮和空气中氧气反应生成二氧化氮;(3)依据铜的物质的量
和稀硝酸提供氢离子物质的量,结合离子方程式定量关系分析计算硝酸根离子浓度;(4)
二氧化氮和氢氧化钠溶液反应生成硝酸钠、亚硝酸钠和水;(5)等质量的铜片与等体积过
量的浓、稀硝酸反应,Cu完全反应,铜离子浓度相同。
【详解】(1)铜和稀硝酸反应的离子方程式为:3Cu+8H++2 NO —=3Cu2++2NO↑+4HO,故
3 2
答案为3Cu+8H++2NO﹣=3Cu2++2NO↑+4HO;(2)吹入空气前小试管中的现象是铜片逐渐
3 2
溶解,铜和稀硝酸反应生成硝酸铜溶液为蓝色溶液,生成一氧化氮气体和大试管中远期反
应生成二氧化氮红棕色气体,故答案为有红棕色气体生成;(3)铜和稀硝酸反应的离子方
程式为:3Cu+8H++2NO—=3Cu2++2NO↑+4HO,0.192g铜片物质的量=
3 2
=0.003mol,5ml浓度为2mol/L的稀硝酸溶液中硝酸物质的量=0.005L×2mol/L=0.01mol,反
应的硝酸根离子物质的量为0.002mol,剩余硝酸根离子物质的量=0.01mol﹣
答案第6页,共2页0.002mol=0.008mol,则溶液中硝酸根离子浓度= =1.6mol/L,故答案为1.6;(4)
若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种
钠盐和水,且氧化产物与还原产物的物质的量相等,是二氧化氮自身氧化还原反应生成硝
酸钠、亚硝酸钠和水,反应的离子方程式为:2NO +2OH﹣=NO—+NO—+H O,故答案为
2 2 3 2
2NO +2OH﹣=NO—+NO—+H O;(5)等质量的铜片与等体积过量的浓、稀硝酸反应,硝
2 2 3 2
酸足量,则Cu完全反应,铜离子浓度相同,所以颜色不同与Cu2+浓度的差异引起的说法不
正确,故答案为不正确;等质量的铜与等体积的浓、稀硝酸反应后,所得溶液中Cu2+的浓
度相等。
【点睛】本题考查了物质性质、化学反应的离子方程式书写和定量计算应用,主要是反应
现象等知识点的理解应用,掌握基础是解题关键,题目较简单。
17. bacd或cbad或bcad SO +Br +2H O=4H++ +2Br- Cl 漏
2 2 2 2
斗 玻璃棒 bd
【详解】(1)粗盐精制是将粗盐中含有的Ca2+、Mg2+、 等杂质的离子去除的过程。精制
时可以先加入过量BaCl 溶液除去 ;再加入NaCO 溶液除去Ca2+及过量的Ba2+;然后
2 2 3
加入过量NaOH溶液除去Mg2+,然后过滤分离除去沉淀,最后向滤液中加入稍过量的盐酸,
除去过量OH-及 就得到纯净NaCl溶液,故加入试剂的先后顺序为bacd;或先加入过
量BaCl 溶液除去 ;然后加入过量NaOH溶液除去Mg2+;再加入过量的NaCO 溶液除
2 2 3
去Ca2+及过量的Ba2+,然后过滤分离除去沉淀,向滤液中加入稍过量的盐酸,除去过量
OH-及 ,就得到纯净NaCl溶液,故加入试剂的先后顺序为bcad;或先加入过量NaOH
溶液除去Mg2+,再加入过量的BaCl 溶液除去 ;再加入过量的NaCO 溶液除去Ca2+及
2 2 3过量的Ba2+,然后过滤分离除去沉淀,向滤液中过量的稀盐酸,除去过量OH-及 就
得到纯净NaCl溶液,故加入试剂的先后顺序为cbad;
(2)SO 气体具有还原性,Br 具有氧化性,二者在溶液中发生氧化还原反应:
2 2
SO +Br +2H O=4H++ +2Br-;
2 2 2
(3)向含有HBr的溶液中通入氧化性的物质如Cl,可以将Br-氧化为Br ,发生反应的化学方
2 2
程式为:2HBr+Cl =2HCl+Br;
2 2
(4)步骤③是分离难溶性固体与可溶性液体混合物的操作,名称为过滤,用到的玻璃仪器除
了烧杯外,还有漏斗、玻璃棒;
(5)I 在水中溶解度不大而易溶于苯中,苯与水互不相溶,且I 不能与苯反应,因此从碘水
2 2
中分离出碘的操作为萃取,使用的萃取剂除苯外,还可以使用四氯化碳、直馏汽油,但由
于乙醇与水混溶不分层,因此不能作萃取剂;乙酸易溶于水,也不能作萃取剂,故合理选
项是bd;
(6)I 与NaOH浓溶液混合,发生歧化反应产生NaI、NaIO 、HO,根据电子守恒、电荷守
2 3 2
恒、原子守恒,可得该反应的离子方程式为: ;
(7)V mL含I 的苯溶液反应消耗NaSO 的物质的量n(Na SO)=aV ×10-3 mol,根据方程式
1 2 2 2 3 2 2 3 2
可知该样品溶液中I 的物质的量为n(I)= ,
2 2
则该样品中I 的含量是 。
2
答案第8页,共2页