文档内容
选择性必修1 第四章 第一节 原电池 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
1. 下列选项中能将化学能转化为电能的装置是( )
A. 天然气燃烧 B. 硅太阳能电池 C. 锂离子电池 D. 太阳能集热器
2. 化学电源在日常生活和高科技领域中都有广泛应用。
下列说法不正确的是( )
A.甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.乙:正极的电极反应式为Ag O+2e-+HO===2Ag+2OH-
2 2
C.丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
3. 我国科学家发明了一种“可固氮”的镁—氮二次电池,其装置如图所示,下列说法不正确的是
( )
A.固氮时,电池的总反应为3Mg+N===Mg N
2 3 2
B.脱氮时,钌复合电极的电极反应式为MgN-6e-===3Mg2++N↑
3 2 2
C.固氮时,外电路中电子由钌复合电极流向镁电极
D.当无水LiClMgCl 混合物受热熔融后电池才能工作
2
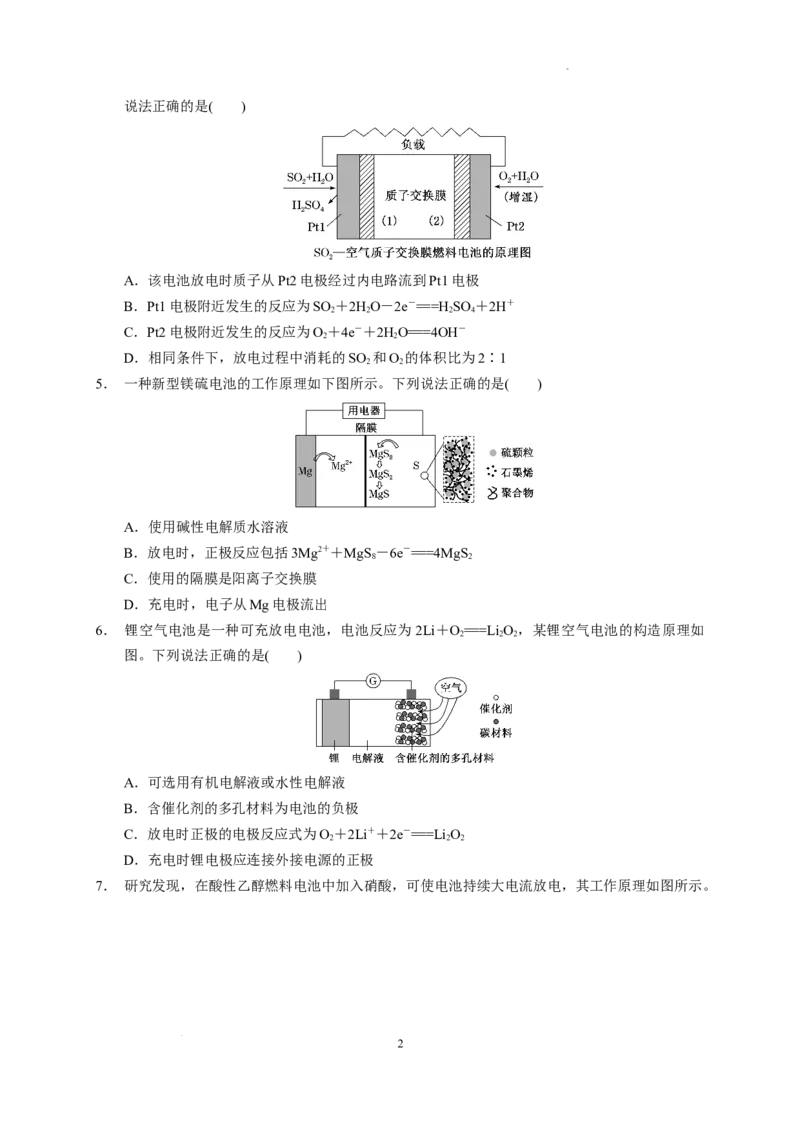
4. 十九大报告中提出要“打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。二氧化硫
—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。下列
1
学科网(北京)股份有限公司说法正确的是( )
A.该电池放电时质子从Pt2电极经过内电路流到Pt1电极
B.Pt1电极附近发生的反应为SO +2HO-2e-===H SO +2H+
2 2 2 4
C.Pt2电极附近发生的反应为O+4e-+2HO===4OH-
2 2
D.相同条件下,放电过程中消耗的SO 和O 的体积比为2∶1
2 2
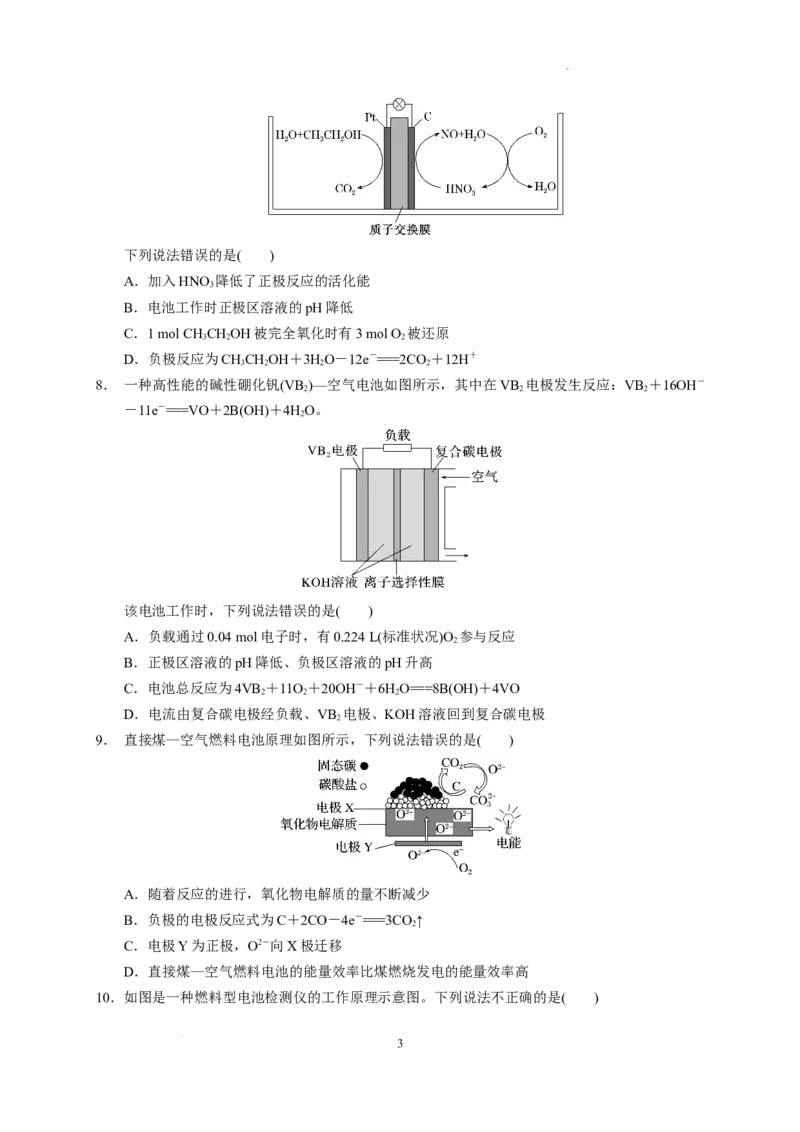
5. 一种新型镁硫电池的工作原理如下图所示。下列说法正确的是( )
A.使用碱性电解质水溶液
B.放电时,正极反应包括3Mg2++MgS -6e-===4MgS
8 2
C.使用的隔膜是阳离子交换膜
D.充电时,电子从Mg电极流出
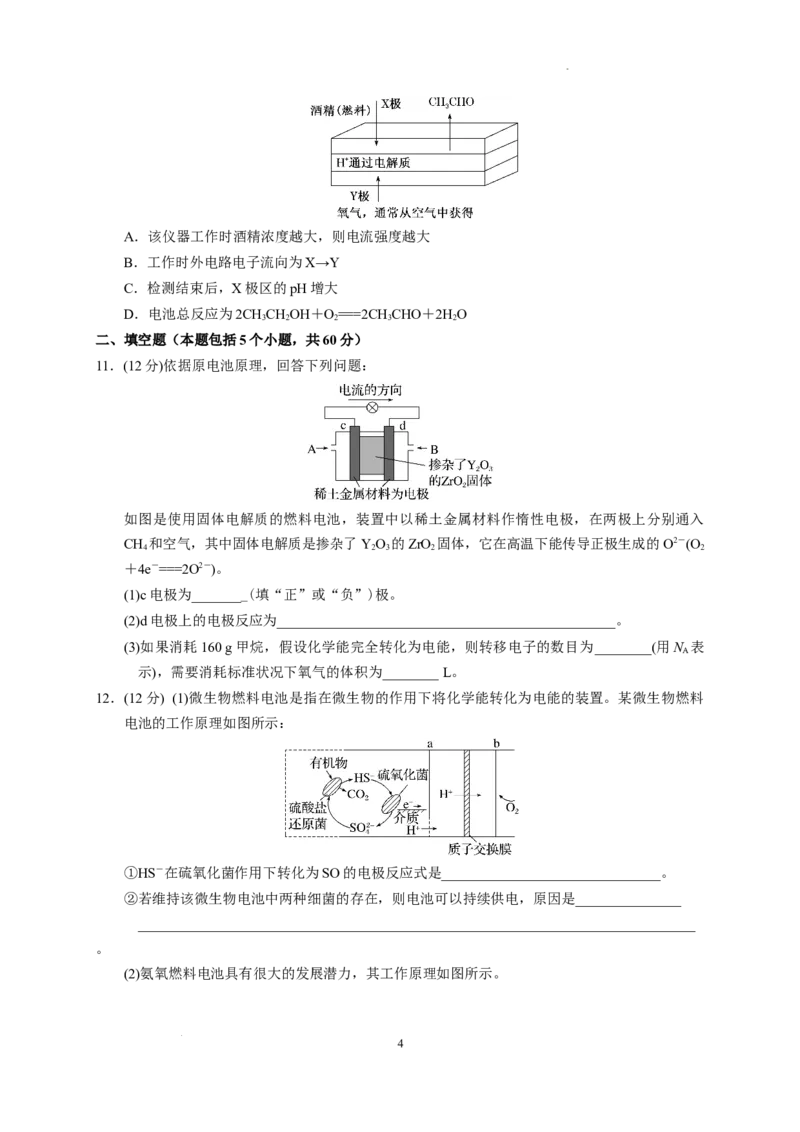
6. 锂空气电池是一种可充放电电池,电池反应为2Li+O===Li O ,某锂空气电池的构造原理如
2 2 2
图。下列说法正确的是( )
A.可选用有机电解液或水性电解液
B.含催化剂的多孔材料为电池的负极
C.放电时正极的电极反应式为O+2Li++2e-===Li O
2 2 2
D.充电时锂电极应连接外接电源的正极
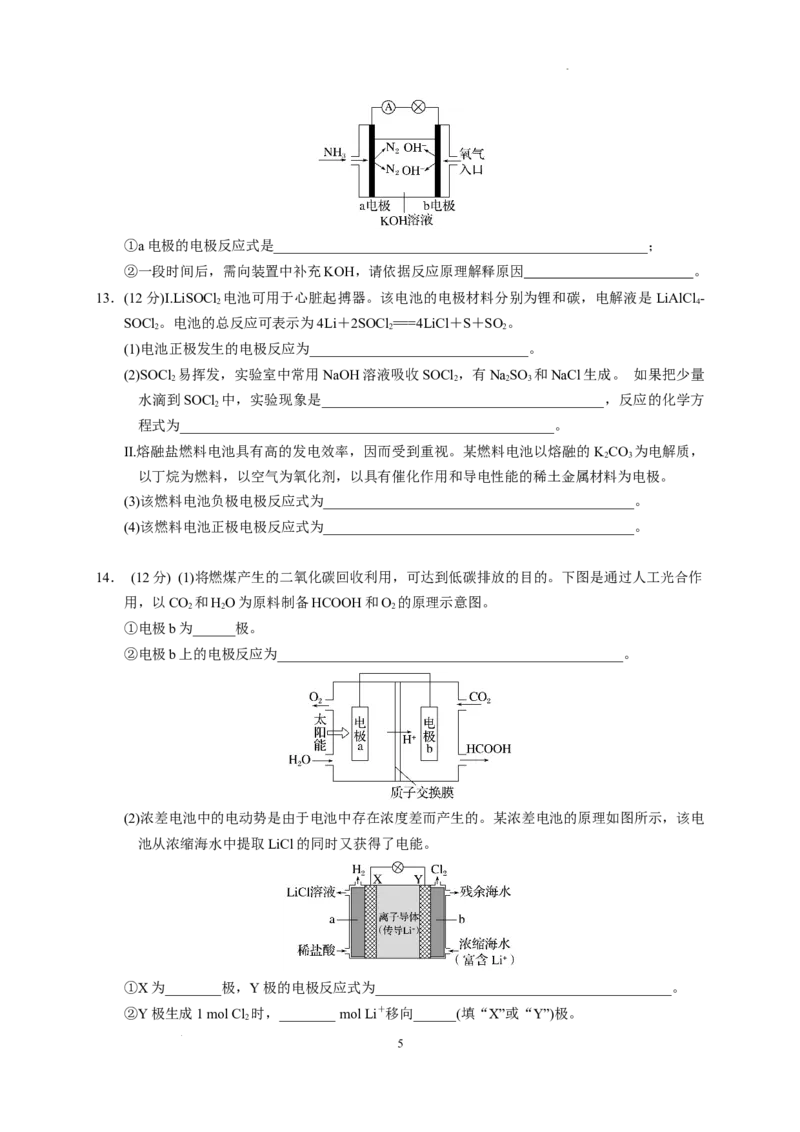
7. 研究发现,在酸性乙醇燃料电池中加入硝酸,可使电池持续大电流放电,其工作原理如图所示。
2
学科网(北京)股份有限公司下列说法错误的是( )
A.加入HNO 降低了正极反应的活化能
3
B.电池工作时正极区溶液的pH降低
C.1 mol CH CHOH被完全氧化时有3 mol O 被还原
3 2 2
D.负极反应为CHCHOH+3HO-12e-===2CO +12H+
3 2 2 2
8. 一种高性能的碱性硼化钒(VB )—空气电池如图所示,其中在VB 电极发生反应:VB +16OH-
2 2 2
-11e-===VO+2B(OH)+4HO。
2
该电池工作时,下列说法错误的是( )
A.负载通过0.04 mol电子时,有0.224 L(标准状况)O 参与反应
2
B.正极区溶液的pH降低、负极区溶液的pH升高
C.电池总反应为4VB +11O+20OH-+6HO===8B(OH)+4VO
2 2 2
D.电流由复合碳电极经负载、VB 电极、KOH溶液回到复合碳电极
2
9. 直接煤—空气燃料电池原理如图所示,下列说法错误的是( )
A.随着反应的进行,氧化物电解质的量不断减少
B.负极的电极反应式为C+2CO-4e-===3CO ↑
2
C.电极Y为正极,O2-向X极迁移
D.直接煤—空气燃料电池的能量效率比煤燃烧发电的能量效率高
10.如图是一种燃料型电池检测仪的工作原理示意图。下列说法不正确的是( )
3
学科网(北京)股份有限公司A.该仪器工作时酒精浓度越大,则电流强度越大
B.工作时外电路电子流向为X→Y
C.检测结束后,X极区的pH增大
D.电池总反应为2CHCHOH+O===2CH CHO+2HO
3 2 2 3 2
二、填空题(本题包括5个小题,共60分)
11.(12分)依据原电池原理,回答下列问题:
如图是使用固体电解质的燃料电池,装置中以稀土金属材料作惰性电极,在两极上分别通入
CH 和空气,其中固体电解质是掺杂了YO 的ZrO 固体,它在高温下能传导正极生成的O2-(O
4 2 3 2 2
+4e-===2O2-)。
(1)c电极为________(填“正”或“负”)极。
(2)d电极上的电极反应为________________________________________________。
(3)如果消耗160 g甲烷,假设化学能完全转化为电能,则转移电子的数目为________(用N 表
A
示),需要消耗标准状况下氧气的体积为________ L。
12.(12分) (1)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料
电池的工作原理如图所示:
①HS-在硫氧化菌作用下转化为SO的电极反应式是_______________________________。
②若维持该微生物电池中两种细菌的存在,则电池可以持续供电,原因是_______________
_______________________________________________________________________________
。
(2)氨氧燃料电池具有很大的发展潜力,其工作原理如图所示。
4
学科网(北京)股份有限公司①a电极的电极反应式是_____________________________________________________;
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因 。
13.(12分)Ⅰ.LiSOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是 LiAlCl -
2 4
SOCl 。电池的总反应可表示为4Li+2SOCl ===4LiCl+S+SO 。
2 2 2
(1)电池正极发生的电极反应为_______________________________。
(2)SOCl 易挥发,实验室中常用NaOH溶液吸收SOCl ,有NaSO 和NaCl生成。 如果把少量
2 2 2 3
水滴到SOCl 中,实验现象是________________________________________,反应的化学方
2
程式为_____________________________________________________。
Ⅱ.熔融盐燃料电池具有高的发电效率,因而受到重视。某燃料电池以熔融的 KCO 为电解质,
2 3
以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。
(3)该燃料电池负极电极反应式为____________________________________________。
(4)该燃料电池正极电极反应式为____________________________________________。
14. (12分) (1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作
用,以CO 和HO为原料制备HCOOH和O 的原理示意图。
2 2 2
①电极b为______极。
②电极b上的电极反应为_________________________________________________。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电
池从浓缩海水中提取LiCl的同时又获得了电能。
①X为________极,Y极的电极反应式为__________________________________________。
②Y极生成1 mol Cl 时,________ mol Li+移向______(填“X”或“Y”)极。
2
5
学科网(北京)股份有限公司(3)微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃
料电池中,电解质溶液为酸性,示意图如下:
①该电池中外电路电子的流动方向为______________(填“从A到B”或“从B到A”)。
②A电极附近甲醇发生的电极反应为___________________________________________。
15.(12分)(1)高铁酸钾(K FeO)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如
2 4
图1是高铁电池的模拟实验装置:
①该电池放电时正极的电极反应式为__________________________________________。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向________(填“左”或“右”)移动;若用阳离
子交换膜代替盐桥,则钾离子向________(填“左”或“右”)移动。
③图 2 为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
____________________________________________________________________。
(2)有人设想以N 和H 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,
2 2
又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是_______________,A
是________。
(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固
6
学科网(北京)股份有限公司体介质NASICON (固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或
“从b到a”),负极发生的电极反应式为__________________________。
1.答案 C
解析:天然气燃烧是化学能转化成热能;硅太阳能电池是太阳能转化成电能;锂离子电池是化学能
转化成电能;太阳能集器是太阳能转化成热能。
2. 答案 A
解析:Zn较Cu活泼,作负极,Zn失电子变Zn2+,Zn2+和H+迁移至铜电极,H+得电子变为H ,
2
因而c(H+)减小,A项错误;Ag O作正极,得到来自Zn失去的电子,被还原成Ag,结合KOH溶
2
液作电解液,故电极反应式为Ag O+2e-+HO===2Ag+2OH-,B项正确;Zn为较活泼电极,作
2 2
负极,发生氧化反应,锌溶解,因而锌筒会变薄,C项正确;铅蓄电池总反应式为PbO (s)+Pb(s)
2
+2HSO (aq)2PbSO (s)+2HO(l),放电一段时间后,HSO 不断被消耗,因而电解质溶液的
2 4 4 2 2 4
酸性减弱,导电能力下降,D项正确。
3. 答案 C
解析:固氮时该装置为原电池装置,镁为活泼金属,作负极,被氧化成 Mg2+,钌复合电极为正极,
氮气在电极上发生还原反应生成N3-,与熔融电解质中镁离子生成MgN ,所以总反应为3Mg+
3 2
N===Mg N ,故A正确;脱氮时,-3价的氮要被氧化,钌复合电极应发生氧化反应,MgN 失电
2 3 2 3 2
子发生氧化反应生成氮气,电极反应式为 MgN -6e-===3Mg2++N↑,故B正确;固氮时,镁电
3 2 2
极为负极,外电路中电子由负极镁电极流向钌复合电极,故C错误;无水LiClMgCl 混合物常温下
2
为固体,无自由移动的离子,不能导电,受热熔融后产生自由移动的离子能导电,电池才能工作,
故D正确。
4. 答案 D
解析:放电时为原电池,质子向正极移动,Pt1电极为负极,则该电池放电时质子从 Pt1电极移向
Pt2电极,A错误;Pt1电极为负极,发生氧化反应,SO 被氧化为硫酸,电极反应式为SO +2HO
2 2 2
-2e-===SO+4H+,硫酸应当拆写成离子形式,B错误;酸性条件下,氧气得电子生成水, C错
误;相同条件下,放电过程中:负极发生氧化反应:2SO +4HO-4e-===2SO+8H+,正极发生还
2 2
原反应:O +4e-+4H+===2H O,根据转移电子数相等可知,放电过程中消耗的 SO 和O 的体积
2 2 2 2
比为2∶1,D正确。
5. 答案 C
解析:碱性电解质水溶液中负极生成的Mg2+会生成Mg(OH) 沉淀,降低电池效率,A错误;放电
2
时为原电池,原电池正极发生得电子的还原反应,包括3Mg2++MgS +6e-===4MgS ,B错误;据
8 2
7
学科网(北京)股份有限公司图可知Mg2+通过隔膜移向正极参与电极反应,所以使用的隔膜是阳离子交换膜,C正确;放电时
Mg电极发生氧化反应,充电时Mg电极得电子发生还原反应,即电子流入Mg电极,D错误。
6. 答案 C
解析:在锂空气电池中,锂失电子作负极,反应式为Li-e-===Li+,以空气中的氧气作为正极反应
物,氧气得电子生成LiO ,正极反应为O +2Li++2e-===Li O ,总反应为2Li+O===Li O 。选
2 2 2 2 2 2 2 2
项A,可选用有机电解液,水性电解液会与Li直接反应,错误;选项B,含催化剂的多孔材料为电
池的正极,错误;选项C,放电时正极的电极反应式为O +2Li++2e-===Li O ,正确;选项D,
2 2 2
充电时锂电极应连接外接电源的负极,电极反应式为Li++e-===Li,错误。
7. 答案 B
解析:乙醇燃料电池中,通入乙醇的一极为负极,电极反应式为CHCHOH+3HO-12e-===2CO
3 2 2 2
+12H+,通入氧气的一极为正极,由工作原理图可知,正极发生反应HNO +3e-+3H+===NO↑+
3
2HO,4NO+3O +2HO===4HNO ,二者加合可得O +4e-+4H+===2H O,则HNO 在正极起催化
2 2 2 3 2 2 3
作用,据此分析解答。HNO 在正极起催化作用,作催化剂,则加入HNO 降低了正极反应的活化
3 3
能,故A正确;电池工作时正极区的总反应为O +4e-+4H+===2H O,则溶液中氢离子浓度减小,
2 2
pH增大,故B错误;根据得失电子守恒可知,1 mol CH CHOH被完全氧化时,转移12 mol电子,
3 2
则有3 mol O 被还原,故C正确;由分析知,负极反应为CHCHOH+3HO-12e-===2CO +12H
2 3 2 2 2
+,故D正确。
8. 答案 B
解析: 根据VB 电极发生的反应:VB +16OH--11e-===VO+2B(OH)+4HO,判断得出VB 电
2 2 2 2
极为负极,复合碳电极为正极,电极反应式为O +4e-+2HO===4OH-,所以电池总反应为4VB
2 2 2
+11O +20OH-+6HO===8B(OH)+4VO,C正确;负载通过0.04 mol电子时,有0.01 mol氧气参
2 2
与反应,即标准状况下有0.224 L氧气参与反应,A正确;负极区消耗OH-,溶液的pH降低,正
极区生成OH-,溶液的pH升高,B错误。
9. 答案 A
解析: A项,由题图可知,电极X反应消耗O2-,电极Y上O 得电子生成O2-不断补充,氧化物
2
电解质的量不会减少,错误;D项,该燃料电池是把化学能直接转化为电能,而煤燃烧发电是把化
学能转化为热能,再转化为电能,正确。
10. 答案 C
解析:该燃料电池为酒精燃料电池,该仪器工作时酒精浓度越大,则单位时间内转移电子数越多,
电流强度越大,故A正确;燃料电池中通入燃料的一极发生氧化反应作原电池的负极,所以 X是
负极,Y是正极,电子从外电路的负极流向正极,故B正确;酒精发生氧化反应生成乙醛和氢离子,
所以X极区的氢离子浓度增大,pH减小,故C错误;燃料电池的反应实质就是乙醇与氧气反应生
成乙醛和水,所以电池总反应为2CHCHOH+O===2CH CHO+2HO,故D正确。
3 2 2 3 2
11.答案 (1)正 (2)CH +4O2--8e-===CO +2HO (3)80N 448
4 2 2 A
解析: (1)根据图中电流方向可知,c电极是正极。(3)160 g CH 的物质的量为10 mol,根据电极反
4
应式可知,反应中转移 80 mol 电子,则正极消耗 O 应为 20 mol,在标准状况下的体积为 20
2
mol×22.4 L·mol-1=448 L。
8
学科网(北京)股份有限公司12.答案 (1)①HS-+4HO-8e-===SO+9H+
2
②HS-、SO的浓度不会发生变化,只要有两种细菌存在,就会循环地把有机物氧化成
CO 放出电子
2
(2)①2NH -6e-+6OH-===N +6HO
3 2 2
②发生反应:4NH +3O===2N +6HO,有水生成,使溶液逐渐变稀,为了保持碱溶液
3 2 2 2
的浓度不变,所以要补充KOH
解析: (1)①酸性环境中反应物为HS-,产物为SO,利用质量守恒和电荷守恒进行配平,电极反应
式为HS-+4HO-8e-===SO+9H+。
2
(2)①a电极是通入NH 的电极,失去电子,发生氧化反应,所以该电极作负极,电极反应式是
3
2NH -6e-+6OH-===N +6HO。
3 2 2
13.答案:(1)2SOCl +4e-===4Cl-+S+SO
2 2
(2)出现白雾,有刺激性气味的气体生成 SOCl +HO===SO↑+2HCl↑
2 2 2
(3)C H +13CO-26e-===17CO +5HO
4 10 2 2
(4)O +2CO+4e-===2CO
2 2
解析:Ⅰ.(1)原电池的负极发生氧化反应,电极反应式为 4Li-4e-+4Cl-===4LiCl,则正极的电极
反应式用总反应式减去负极反应式得 2SOCl +4e-===4Cl-+S+SO 。(2)用 NaOH 溶液吸收
2 2
SOCl ,有NaSO 和NaCl生成,说明反应过程中S元素的化合价仍是+4价,未发生氧化还原反应,
2 2 3
所以SOCl 与水反应的产物是二氧化硫与氯化氢,氯化氢与水结合形成白雾,则实验现象是出现白
2
雾,有刺激性气味的气体生成;反应的化学方程式为SOCl +HO===SO↑+2HCl↑。Ⅱ.(3)燃料电池
2 2 2
的负极发生氧化反应,所以丁烷在负极发生氧化反应,失去电子,因为熔融KCO 为电解质,所以
2 3
生成二氧化碳和水,电极反应式为C H +13CO-26e-===17CO +5HO。(4)正极是氧气发生还原
4 10 2 2
反应,与二氧化碳结合生成碳酸根离子,电极反应式为O+2CO+4e-===2CO。
2 2
14.答案 (1)①正 ②CO+2e-+2H+===HCOOH
2
(2)①正 2Cl--2e-===Cl↑ ②2 X
2
(3)①从A到B ②CHOH+HO-6e-===6H++CO↑
3 2 2
解析: (1)从图示可以看出,右侧通入的CO 转变成HCOOH,C元素被还原,电极b为正极,电极
2
反应式为CO +2e-+2H+===HCOOH。(2)根据装置可知生成H 的电极为正极,生成Cl 的电极为
2 2 2
负极。(3)①甲醇失去电子,作为电池的负极,所以该电池外电路电子的流动方向为从 A到B。
②CHOH失电子生成CO 和H+,根据化合价变化和元素守恒可得电极反应式:CHOH+HO-6e
3 2 3 2
-===6H++CO↑。
2
15.答案:(1)①FeO+4HO+3e-===Fe(OH) ↓+5OH- ②右 左 ③使用时间长、工作电压稳定
2 3
(2)N +8H++6e-===2NH 氯化铵
2
(3)从b到a CO+O2--2e-===CO
2
解析:(1)①放电时石墨为正极,高铁酸钾在正极上发生还原反应,电极反应式为 FeO+4HO+3e-
2
===Fe(OH) ↓+5OH-。
3
②电池工作时,阴离子移向负极,阳离子移向正极,所以盐桥中氯离子向右移动;若用阳离子
9
学科网(北京)股份有限公司交换膜代替盐桥,则钾离子向左移动。
③由题图中高铁电池和常用的高能碱性电池的放电曲线,可知高铁电池的优点有使用时间长、
工作电压稳定。
(2)该电池的本质反应是合成氨反应,电池中氢气失电子在负极发生氧化反应,氮气得电子在正
极发生还原反应,则正极反应式为N+8H++6e-===2NH,氨气与HCl反应生成氯化铵,则电解质
2
溶液为氯化铵溶液。
(3)该装置是原电池,工作时电极b作正极,O2-由电极b移向电极a,通入一氧化碳的电极a是
负极,负极上一氧化碳失去电子发生氧化反应,电极反应式为CO+O2--2e-===CO 。
2
10
学科网(北京)股份有限公司11
学科网(北京)股份有限公司