文档内容
绝密★启用前|考 下学期期中测试卷 03 4.(本题3分)已知:稀硝酸能与SO 2 发生氧化还原反应:3SO 2 +2HNO 3 +2H 2 O=3H 2 SO 4 +2NO。下列过程中最
终的白色沉淀不一定是BaSO 的是( )
4
高一化学
A.Fe(NO ) 溶液→通入SO +过量盐酸→加BaCl 溶液→白色沉淀
3 2 2 2
B.Ba(NO ) 溶液→加过量盐酸→加NaSO 溶液→白色沉淀
3 2 2 3
(考试时间:90分钟 试卷满分:100分)
C.无色溶液→加稀HNO→加BaCl 溶液→白色沉淀
3 2
测试范围:人教版2019必修第二册:第五章、第六章
D.无色溶液→加过量盐酸→无色溶液→加BaCl 溶液→白色溶液
2
第Ⅰ卷(选择题 共 48 分)
5.(本题3分)下列离子能大量共存的是
A.含有大量Ba(NO ) 的溶液中:Mg2+、 、 、Cl-
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题目要求的。 3 2
1.(本题3分)下列有关SO 2 的性质说法正确的是( ) B.含 的溶液中:H+、K+、I-、Fe2+
A.因为SO 具有漂白性,所以它能使酸性KMnO 溶液褪色
2 4
C.使无色酚酞溶液呈红色的溶液中:Na+、K+、 、
B.SO 具有还原性,能被浓硫酸氧化
2
C.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同 D.酸性溶液: 、Fe3+、CHCOO-、
2 2 2 3
D.SO 能与HS反应生成S,说明SO 具有氧化性
2 2 2 6.(本题3分)下列变化的实质相似的是
A.浓硫酸和浓硝酸在空气中敞口放置时浓度均减小
2.(本题3分)已知反应2FeSO Fe O+SO↑+SO↑,设N 为阿伏加德罗常数的值。下列说法正确的是(
4 2 3 2 3 A
B.SO 和Cl 均能能使品红溶液褪色
2 2
C.HS和HI气体均不能用浓硫酸干燥
) 2
D.浓HSO 和稀HSO 与金属反应时均有气体放出
A.上述反应的还原产物为SO 和SO 2 4 2 4
2 3
7.(本题3分)下列实验操作、现象与结论对应关系正确的是
B.每生成16g SO,该反应转移的电子数为0.8N
3 A
选项 实验操作 实验现象与结论
C.2mol/L FeSO 溶液中,SO 的数目为2N
4 A
D.若将生成的气体通入氯化钡溶液中,得到的沉淀物是BaSO 4 A 将SO 2 通入酸性KMnO 4 溶液中 酸性KMnO 4 溶液褪色,证明SO 2 具有漂白性
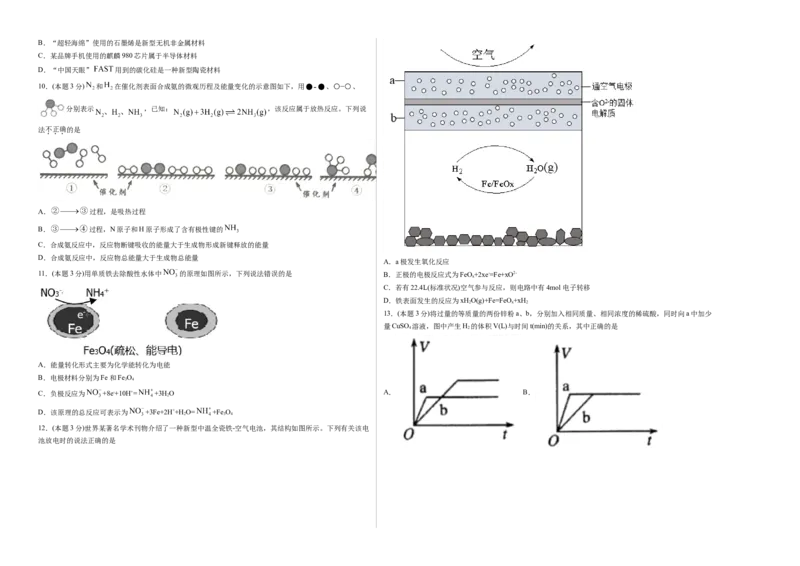
3.(本题3分)X、Y、Z、W为原子序数依次增大的四种短周期元素。甲、乙、丙是由这些元素组成的二元
滴加稀硝酸无现象,滴加BaCl 后出现白色沉
化合物,A、B、C、D是四种元素形成的非金属单质,甲是10电子微粒,丙是18电子微粒,B是密度最小 向样品溶液中先滴加过量的稀硝 2
B
的气体,C为淡黄色固体。上述物质的转化关系如图所示。下列说法正确的是( ) 酸,再滴加BaCl 2 溶液 淀。说明样品溶液中一定含有SO
某溶液中加入足量浓NaOH溶
C 液,加热,在试管口放一片湿润 湿润的红色石蕊试纸变蓝,则样品中含有NH
的红色石蕊试纸
某溶液中加入盐酸,并将产生的
D 澄清石灰水变浑浊,说明溶液中一定含有CO
气体通入澄清石灰水
8.(本题3分)下列说法正确的是
A.浓硫酸有强腐蚀性,可用浓硫酸刻蚀石英制成艺术品
B.食品袋中放入盛有硅胶和铁粉的透气小袋目的是防止食物受潮、氧化
C.晶体硅具有特殊的光学性能,可制成光导纤维
A.W的原子半径是这些元素中最大的
D.SiO 能与NaOH溶液和HF溶液反应,故SiO 是两性氧化物
B.甲、乙、丙溶于水后溶液呈酸性 2 2
9.(本题3分)现代社会的发展与进步离不开材料,下列有关材料的说法不正确的是
C.Z、W的氧化物对应水化物的酸性:
A.“辽宁舰”上用于舰载机降落的阻拦索是一种特种钢缆,属于纯金属材料
D.稳定性:丙>乙B.“超轻海绵”使用的石墨烯是新型无机非金属材料
C.某品牌手机使用的麒麟980芯片属于半导体材料
D.“中国天眼” 用到的碳化硅是一种新型陶瓷材料
10.(本题3分) 和 在催化剂表面合成氨的微观历程及能量变化的示意图如下,用 、 、
分别表示 ,已知: ,该反应属于放热反应。下列说
法不正确的是
A. 过程,是吸热过程
B. 过程,N原子和H原子形成了含有极性键的
C.合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
D.合成氨反应中,反应物总能量大于生成物总能量
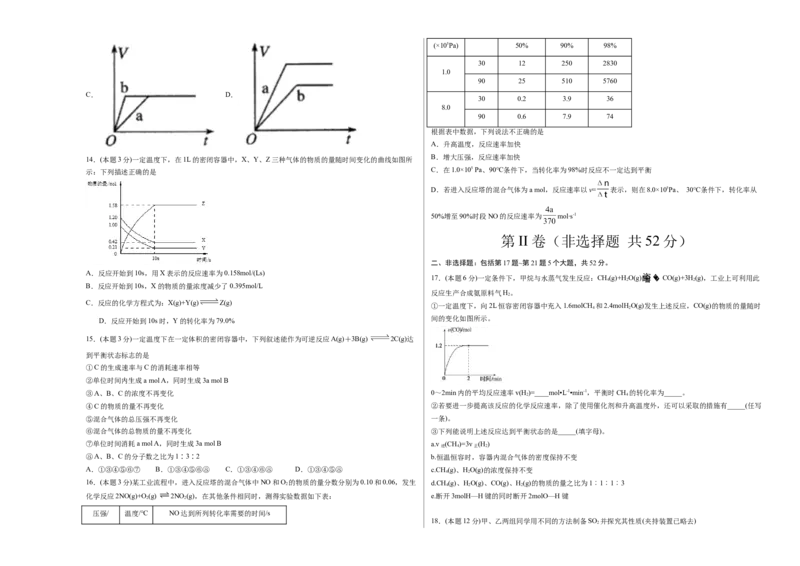
A.a极发生氧化反应
11.(本题3分)用单质铁去除酸性水体中 的原理如图所示,下列说法错误的是 B.正极的电极反应式为FeO+2xe-=Fe+xO2-
x
C.若有22.4L(标准状况)空气参与反应,则电路中有4mol电子转移
D.铁表面发生的反应为xHO(g)+Fe=FeO +xH
2 x 2
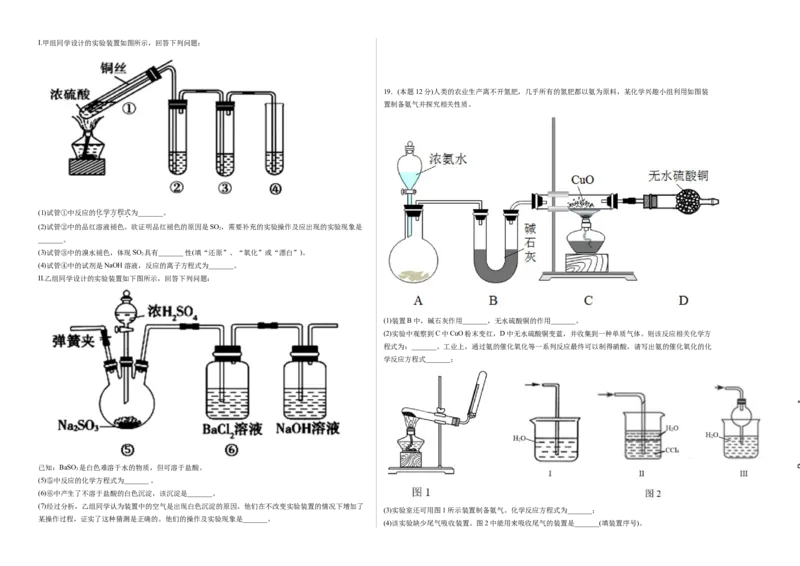
13.(本题3分)将过量的等质量的两份锌粉a、b,分别加入相同质量、相同浓度的稀硫酸,同时向a中加少
量CuSO 溶液,图中产生H 的体积V(L)与时间t(min)的关系,其中正确的是
4 2
A.能量转化形式主要为化学能转化为电能
B.电极材料分别为Fe和Fe O
3 4
C.负极反应为 +8e-+10H+= +3H O A. B.
2
D.该原理的总反应可表示为 +3Fe+2H++H O= +Fe O
2 3 4
12.(本题3分)世界某著名学术刊物介绍了一种新型中温全瓷铁-空气电池,其结构如图所示。下列有关该电
池放电时的说法正确的是(×105Pa) 50% 90% 98%
30 12 250 2830
1.0
90 25 510 5760
C. D.
30 0.2 3.9 36
8.0
90 0.6 7.9 74
根据表中数据,下列说法不正确的是
A.升高温度,反应速率加快
B.增大压强,反应速率加快
14.(本题3分)一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所
C.在1.0×105 Pa、90℃条件下,当转化率为98%时反应不一定达到平衡
示:下列描述正确的是
D.若进入反应塔的混合气体为a mol,反应速率以v= 表示,则在8.0×105Pa、 30℃条件下,转化率从
50%增至90%时段NO的反应速率为 mol∙s-1
第 II 卷(非选择题 共 52 分)
二、非选择题:包括第17题~第21题5个大题,共52分。
A.反应开始到10s,用X表示的反应速率为0.158mol/(Ls)
17.(本题6分)一定条件下,甲烷与水蒸气发生反应:CH(g)+HO(g) CO(g)+3H(g),工业上可利用此
4 2 2
B.反应开始到10s,X的物质的量浓度减少了0.395mol/L
反应生产合成氨原料气H。
2
C.反应的化学方程式为:X(g)+Y(g) Z(g)
①一定温度下,向2L恒容密闭容器中充入1.6molCH 和2.4molHO(g)发生上述反应,CO(g)的物质的量随时
4 2
间的变化如图所示。
D.反应开始到10s时,Y的转化率为79.0%
15.(本题3分)一定温度下在一定体积的密闭容器中,下列叙述能作为可逆反应A(g)+3B(g) 2C(g)达
到平衡状态标志的是
①C的生成速率与C的消耗速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化 0~2min内的平均反应速率v(H )=____mol•L-1•min-1,平衡时CH 的转化率为_____。
2 4
④C的物质的量不再变化 ②若要进一步提高该反应的化学反应速率,除了使用催化剂和升高温度外,还可以采取的措施有_____(任写
⑤混合气体的总压强不再变化 一条)。
⑥混合气体的总物质的量不再变化 ③下列能说明上述反应达到平衡状态的是_____(填字母)。
⑦单位时间消耗a mol A,同时生成3a mol B a.v (CH)=3v (H )
逆 4 正 2
⑧A、B、C的分子数之比为1∶3∶2 b.恒温恒容时,容器内混合气体的密度保持不变
A.①③④⑤⑥⑦ B.①③④⑤⑥⑧ C.①③④⑥⑧ D.①③④⑤⑧ c.CH (g)、HO(g)的浓度保持不变
4 2
16.(本题3分)某工业流程中,进入反应塔的混合气体中NO和O 的物质的量分数分别为0.10和0.06,发生 d.CH (g)、HO(g)、CO(g)、H(g)的物质的量之比为1︰1︰1︰3
2 4 2 2
化学反应2NO(g)+O (g) 2NO (g),在其他条件相同时,测得实验数据如下表: e.断开3molH—H键的同时断开2molO—H键
2 2
压强/ 温度/℃ NO达到所列转化率需要的时间/s
18.(本题12分)甲、乙两组同学用不同的方法制备SO 并探究其性质(夹持装置已略去)
2I.甲组同学设计的实验装置如图所示,回答下列问题:
19.(本题12分)人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用如图装
置制备氨气并探究相关性质。
(1)试管①中反应的化学方程式为_______。
(2)试管②中的品红溶液褪色。欲证明品红褪色的原因是SO ,需要补充的实验操作及应出现的实验现象是
2
_______。
(3)试管③中的溴水褪色,体现SO 具有_______ 性(填“还原”、“氧化”或“漂白”)。
2
(4)试管④中的试剂是NaOH溶液,反应的离子方程式为_______。
II.乙组同学设计的实验装置如下图所示,回答下列问题:
(1)装置B中,碱石灰作用_______,无水硫酸铜的作用_______。
(2)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体。则该反应相关化学方
程式为:_______。工业上,通过氨的催化氧化等一系列反应最终可以制得硝酸,请写出氨的催化氧化的化
学反应方程式_______;
已知:BaSO 是白色难溶于水的物质,但可溶于盐酸。
3
(5)⑤中反应的化学方程式为_______ 。
(6)⑥中产生了不溶于盐酸的白色沉淀,该沉淀是_______。
(7)经过分析,乙组同学认为装置中的空气是出现白色沉淀的原因。他们在不改变实验装置的情况下增加了
(3)实验室还可用图1所示装置制备氨气。化学反应方程式为_______;
某操作过程,证实了这种猜测是正确的。他们的操作及实验现象是_______。
(4)该实验缺少尾气吸收装置。图2中能用来吸收尾气的装置是_______(填装置序号)。(5)图3装置中,a表示胶头滴管和烧杯中的液体,b表示烧瓶中的气体,不能形成喷泉实验现象的a中液体
和b中气体的组合是_______
A.a-NaOH溶液、b-HC1气体 B.a-NaOH溶液、b-CO 气体
2
C.a-HCl溶液、b-NH 气体 D.a-水、b-CO
3 2
20.(本题11分)X、Y、Z、W、R是短周期元素,原子序数依次增大。非金属X原子核外各层电子数之比
为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均
能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为___________;元素Z的离子结构示意图为___________。
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为___________。
(3)元素W位于周期表的第___________族,其非金属性比R弱,用原子结构的知识解释原因:___________。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收
剂与足量该氧化物反应的离子方程式:___________。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制
备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为___________。
21.(本题11分)某化学兴趣小组利用NaI溶液中通入少量Cl 得到含碘废液,再利用含碘废液获取NaI固体,
2
实验流程如图:
已知反应②:2I-+2Cu2++SO +H O=2CuI↓+SO +2H+
2
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_______,所缺玻璃仪器的作用是_______。
(2)反应③中CuI被氧化,还原产物只有NO ,该反应的化学方程式为_______。
2
(3)化合物B中含两种元素,铁元素原子与另一种元素原子的物质的量之比为3:8,则化合物B的化学式为
_______。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为_______。
(5)将足量的Cl 通入含12g NaI的溶液中,一段时间后把溶液蒸干、灼烧,得到的固体是_______,其质量为
2
_______g。