文档内容
江西师大附中高三下学期三模化学试卷
命题人:李桥生 审题人:颜标峰 2024.5
可能用到的相对原子质量:H1 C12 N14 O16 Cl35.5 K39 Pb207
一、选择题:本题共14小题,每题3分,共42分。在每小题给出的四个选项中,只有一项最
符合题目要求。
1.江西省进贤县李渡镇拥有中国时代最早、遗址最全、遗物最多、时间跨度最长且最富有地方特色
的大型古代烧酒作坊遗址。李渡高粱酒酿制过程中,下列说法不正确的是
A.“蒸粮”时可适当鼓风加快燃烧速率 B.“拌曲”加入的酒曲在酿酒时起到催化作用
C.“堆酵”时升温是因为此过程ΔH>0 D.“馏酒”的原理即实验操作中的“蒸馏”
2. 化学学科的学习有助于我们实现“德智体美劳”的全面发展目标。下列实践项目相关的化学知
识描述不正确的是
选项 实践项目 化学知识
A 德:废书废纸不随意丢弃,整理后进行回收处理 纸张的原料中含纤维素高分子
B 体:剧烈运动大量出汗后,喝淡盐水补充体力 淡盐水属于电解质
C 美:美术课上用铅笔勾勒出写意山水画 铅笔芯的石墨属于混合型晶体
D 劳:制作豆腐时可用石膏、氯化镁进行点卤 石膏、氯化镁作凝固剂可使豆浆聚沉
3.下列示意图或图示正确的是
A.基态铍原子价电
B.NH的结构式 C.丙氨酸的手性异构体 D.HF分子间的氢键
子云图 4
4.Fe、HCN与K CO 在一定条件下发生如下反应:
2 3
Fe+6HCN+2K CO =K Fe(CN) +H ↑+2CO ↑+2H O,下列说法正确的是
2 3 4 6 2 2 2
A.依据反应方程式可知:K HCNK H CO
a a1 2 3
B.键角:CO CO2 H O
2 3 2
C.
1mol HCN
分子中含有π键的数目为6.021023
D.配合物K FeCN 的中心离子的价层电子中有5个未成对电子
4 6
高三化学试卷 第1页,共10页
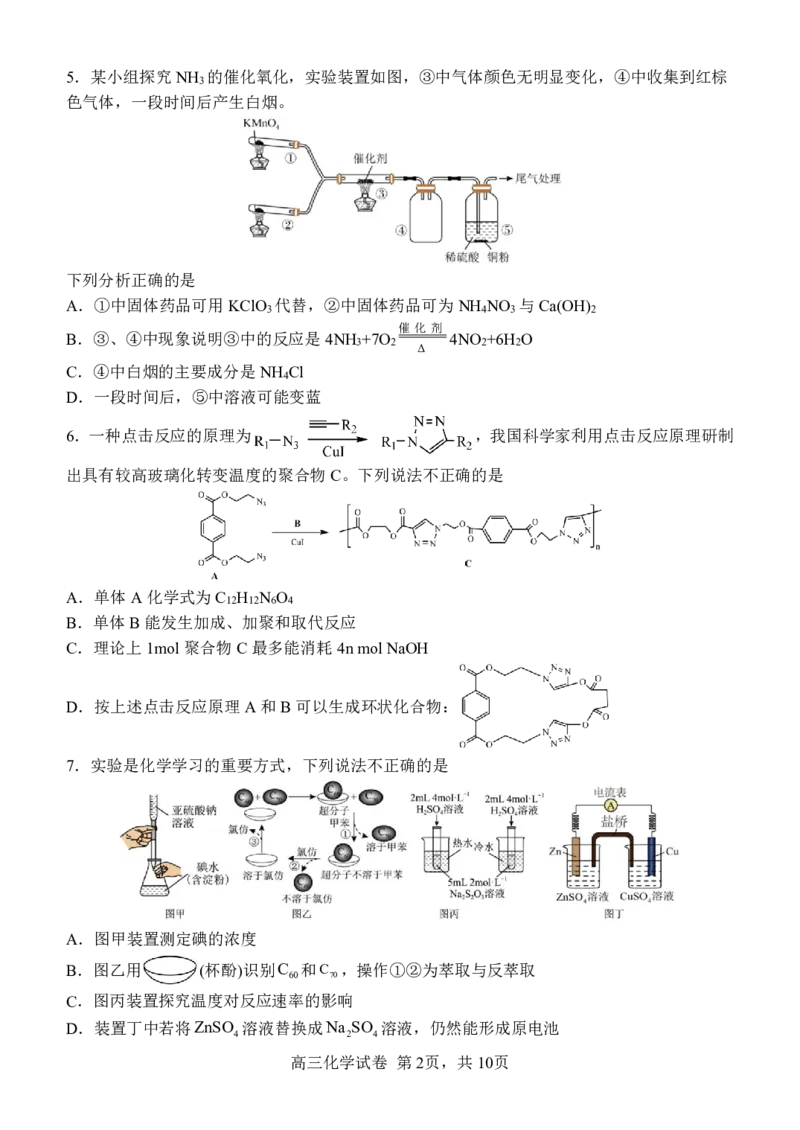
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}5.某小组探究NH 的催化氧化,实验装置如图,③中气体颜色无明显变化,④中收集到红棕
3
色气体,一段时间后产生白烟。
下列分析正确的是
A.①中固体药品可用KClO 代替,②中固体药品可为NH NO 与Ca(OH)
3 4 3 2
催化剂
B.③、④中现象说明③中的反应是4NH +7O 4NO +6H O
3 2 2 2
Δ
C.④中白烟的主要成分是NH Cl
4
D.一段时间后,⑤中溶液可能变蓝
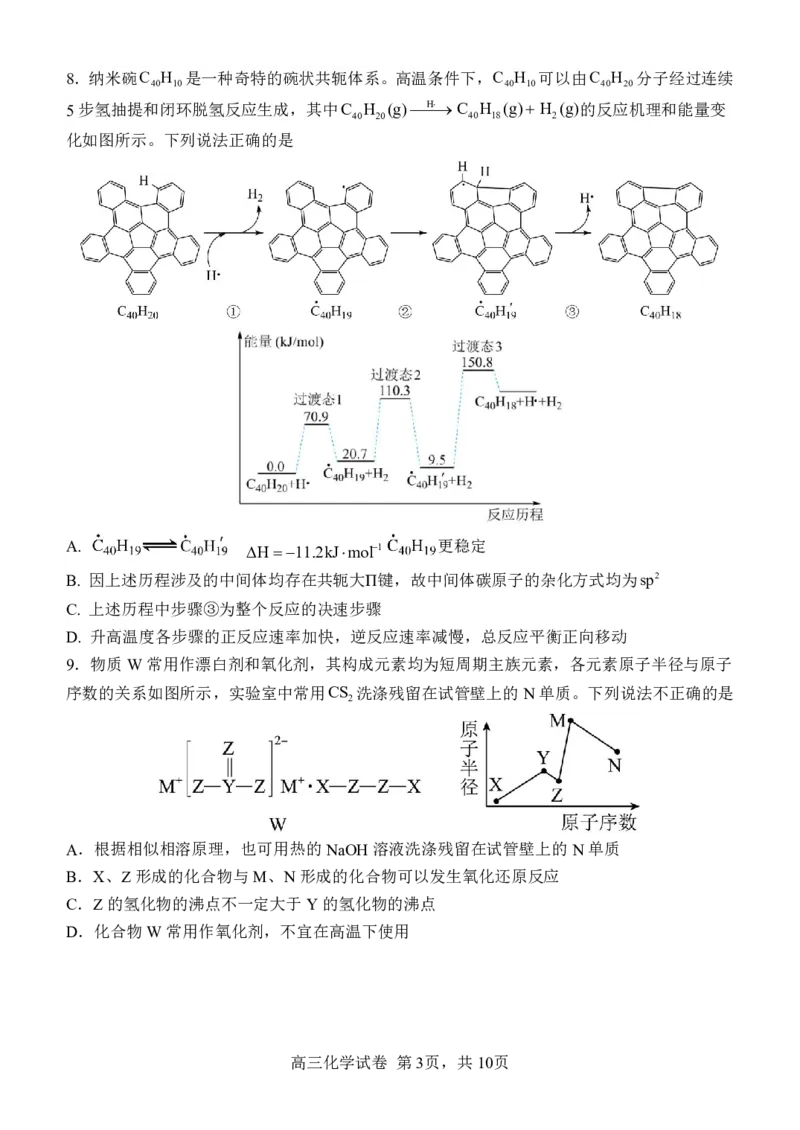
6.一种点击反应的原理为 ,我国科学家利用点击反应原理研制
出具有较高玻璃化转变温度的聚合物C。下列说法不正确的是
A.单体A化学式为C H N O
12 12 6 4
B.单体B能发生加成、加聚和取代反应
C.理论上1mol聚合物C最多能消耗4nmolNaOH
D.按上述点击反应原理A和B可以生成环状化合物:
7.实验是化学学习的重要方式,下列说法不正确的是
A.图甲装置测定碘的浓度
B.图乙用 (杯酚)识别C 和C ,操作①②为萃取与反萃取
60 70
C.图丙装置探究温度对反应速率的影响
D.装置丁中若将ZnSO 溶液替换成Na SO 溶液,仍然能形成原电池
4 2 4
高三化学试卷 第2页,共10页
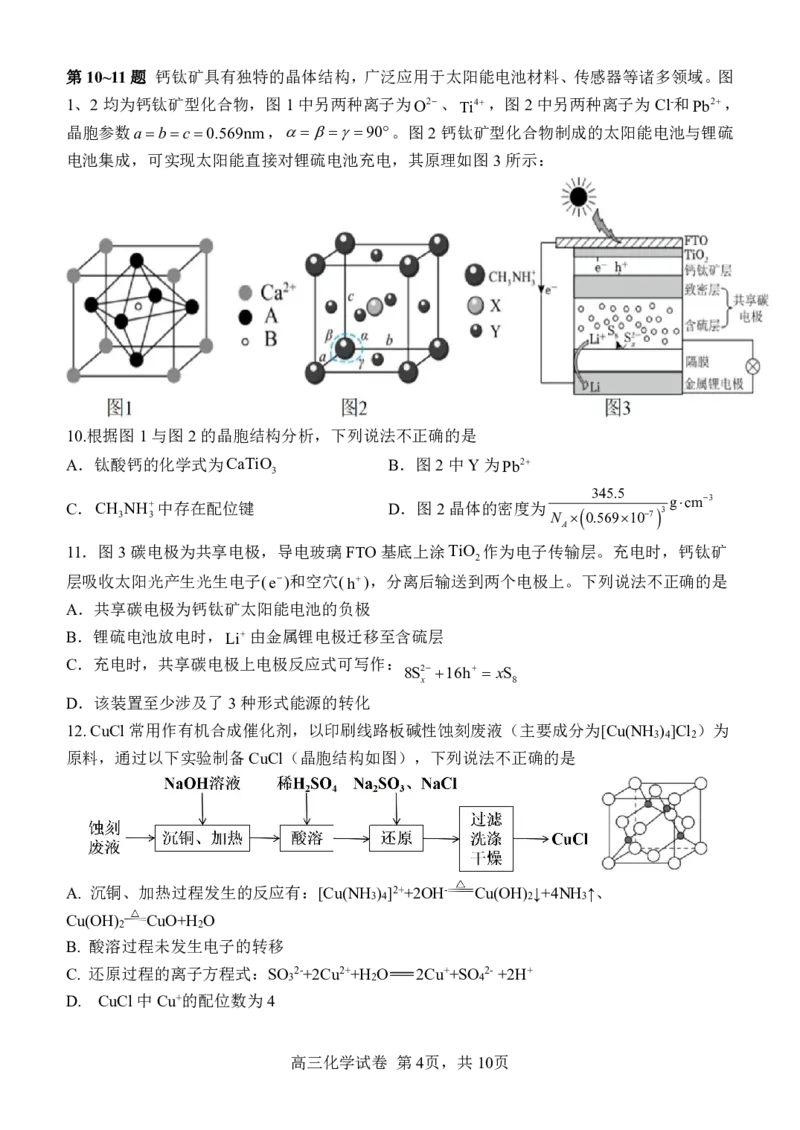
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}8.纳米碗C H 是一种奇特的碗状共轭体系。高温条件下,C H 可以由C H 分子经过连续
40 10 40 10 40 20
5步氢抽提和闭环脱氢反应生成,其中C H (g)HC H (g) H (g)的反应机理和能量变
40 20 40 18 2
化如图所示。下列说法正确的是
A. H11.2kJmol1 更稳定
B. 因上述历程涉及的中间体均存在共轭大Π键,故中间体碳原子的杂化方式均为sp2
C. 上述历程中步骤③为整个反应的决速步骤
D. 升高温度各步骤的正反应速率加快,逆反应速率减慢,总反应平衡正向移动
9.物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子
序数的关系如图所示,实验室中常用CS 洗涤残留在试管壁上的N单质。下列说法不正确的是
2
A.根据相似相溶原理,也可用热的NaOH溶液洗涤残留在试管壁上的N单质
B.X、Z形成的化合物与M、N形成的化合物可以发生氧化还原反应
C.Z的氢化物的沸点不一定大于Y的氢化物的沸点
D.化合物W常用作氧化剂,不宜在高温下使用
高三化学试卷 第3页,共10页
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}第10~11题 钙钛矿具有独特的晶体结构,广泛应用于太阳能电池材料、传感器等诸多领域。图
1、2均为钙钛矿型化合物,图1中另两种离子为O2、Ti4,图2中另两种离子为Cl-和Pb2,
晶胞参数abc0.569nm,90。图2钙钛矿型化合物制成的太阳能电池与锂硫
电池集成,可实现太阳能直接对锂硫电池充电,其原理如图3所示:
10.根据图1与图2的晶胞结构分析,下列说法不正确的是
A.钛酸钙的化学式为CaTiO B.图2中Y为Pb2
3
345.5
C.CH 3 NH 3 中存在配位键 D.图2晶体的密度为 N 0.5691073
gcm3
A
11.图3碳电极为共享电极,导电玻璃FTO基底上涂TiO 作为电子传输层。充电时,钙钛矿
2
层吸收太阳光产生光生电子(e)和空穴(h),分离后输送到两个电极上。下列说法不正确的是
A.共享碳电极为钙钛矿太阳能电池的负极
B.锂硫电池放电时,Li由金属锂电极迁移至含硫层
C.充电时,共享碳电极上电极反应式可写作:
8S216h xS
x 8
D.该装置至少涉及了3种形式能源的转化
12.CuCl常用作有机合成催化剂,以印刷线路板碱性蚀刻废液(主要成分为[Cu(NH ) ]Cl )为
3 4 2
原料,通过以下实验制备CuCl(晶胞结构如图),下列说法不正确的是
A. 沉铜、加热过程发生的反应有:[Cu(NH ) ]2++2OH- Cu(OH) ↓+4NH ↑、
3 4 2 3
Cu(OH) CuO+H O
2 2
B. 酸溶过程未发生电子的转移
C. 还原过程的离子方程式:SO 2-+2Cu2++H O 2Cu++SO 2-+2H+
3 2 4
D. CuCl中Cu+的配位数为4
高三化学试卷 第4页,共10页
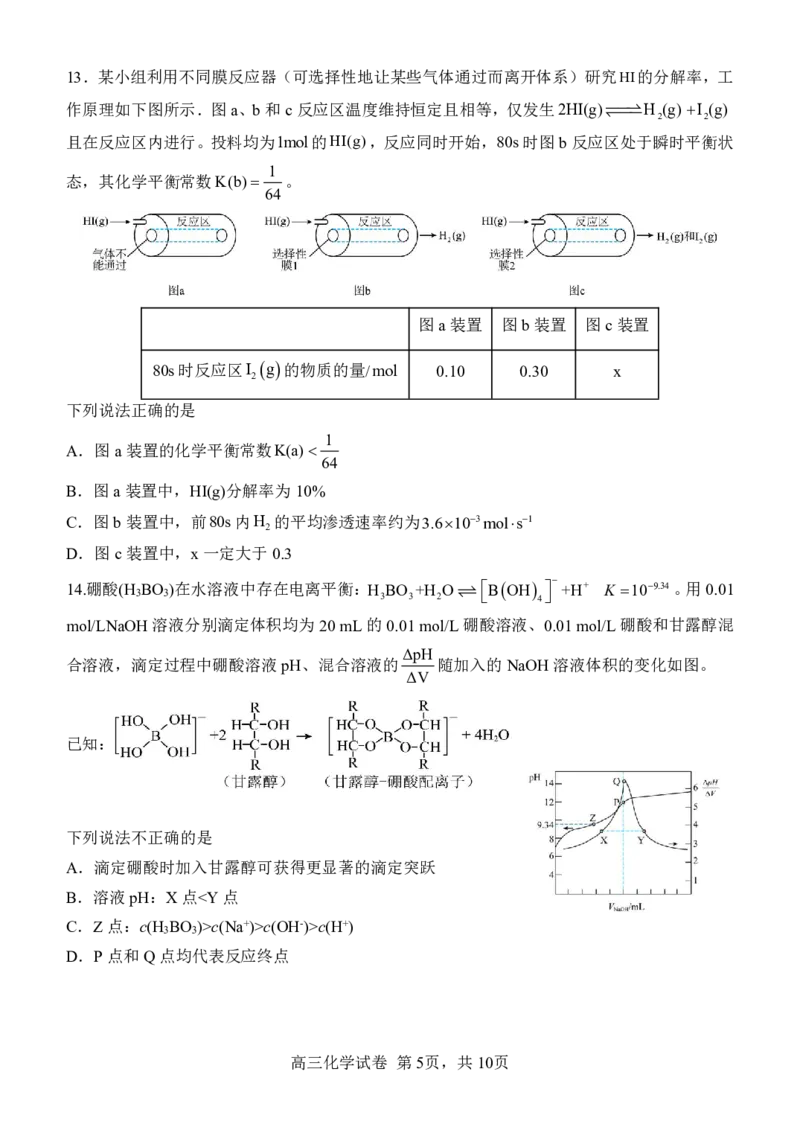
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}13.某小组利用不同膜反应器(可选择性地让某些气体通过而离开体系)研究HI的分解率,工
作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生2HI(g)H (g) I (g)
2 2
且在反应区内进行。投料均为1mol的HI(g),反应同时开始,80s时图b反应区处于瞬时平衡状
1
态,其化学平衡常数K(b) 。
64
图a装置 图b装置 图c装置
80s时反应区I g的物质的量/mol 0.10 0.30 x
2
下列说法正确的是
1
A.图a装置的化学平衡常数K(a)
64
B.图a装置中,HI(g)分解率为10%
C.图b装置中,前80s内H 的平均渗透速率约为3.6103mols1
2
D.图c装置中,x一定大于0.3
14.硼酸(H 3 BO 3 )在水溶液中存在电离平衡:H 3 BO 3 +H 2 O BOH 4 +H+ K 109.34。用0.01
mol/LNaOH溶液分别滴定体积均为20mL的0.01mol/L硼酸溶液、0.01mol/L硼酸和甘露醇混
ΔpH
合溶液,滴定过程中硼酸溶液pH、混合溶液的 随加入的NaOH溶液体积的变化如图。
ΔV
已知:
下列说法不正确的是
A.滴定硼酸时加入甘露醇可获得更显著的滴定突跃
B.溶液pH:X点c(Na+)>c(OH-)>c(H+)
3 3
D.P点和Q点均代表反应终点
高三化学试卷 第5页,共10页
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}二、非选择题:本题共 4小题,共 58分。
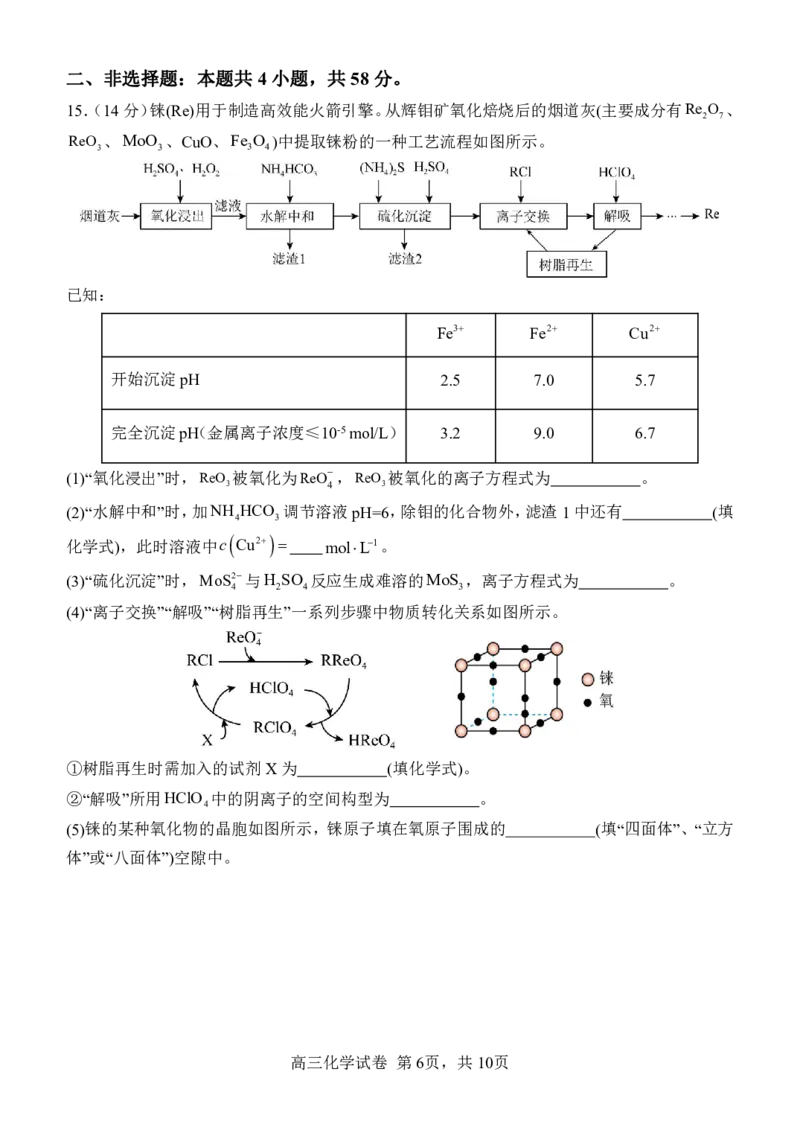
15.(14分)铼(Re)用于制造高效能火箭引擎。从辉钼矿氧化焙烧后的烟道灰(主要成分有Re O 、
2 7
ReO 、MoO 、CuO、Fe O )中提取铼粉的一种工艺流程如图所示。
3 3 3 4
已知:
Fe3 Fe2 Cu2
开始沉淀pH 2.5 7.0 5.7
完全沉淀pH(金属离子浓度≤10-5mol/L) 3.2 9.0 6.7
(1)“氧化浸出”时,ReO 被氧化为ReO ,ReO 被氧化的离子方程式为 。
3 4 3
(2)“水解中和”时,加NH HCO 调节溶液pH=6,除钼的化合物外,滤渣1中还有 (填
4 3
化学式),此时溶液中c
Cu2
molL1。
(3)“硫化沉淀”时,MoS2与H SO 反应生成难溶的MoS ,离子方程式为 。
4 2 4 3
(4)“离子交换”“解吸”“树脂再生”一系列步骤中物质转化关系如图所示。
①树脂再生时需加入的试剂X为 (填化学式)。
②“解吸”所用HClO 中的阴离子的空间构型为 。
4
(5)铼的某种氧化物的晶胞如图所示,铼原子填在氧原子围成的 (填“四面体”、“立方
体”或“八面体”)空隙中。
高三化学试卷 第6页,共10页
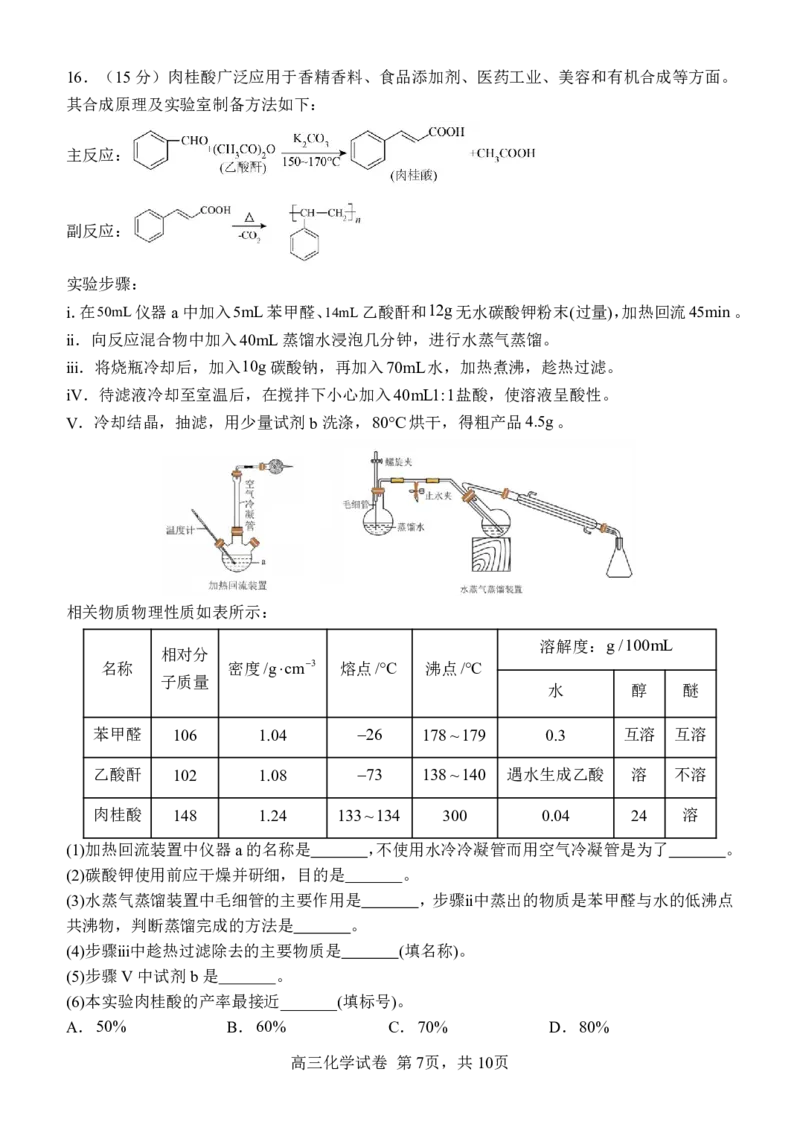
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}16.(15分)肉桂酸广泛应用于香精香料、食品添加剂、医药工业、美容和有机合成等方面。
其合成原理及实验室制备方法如下:
主反应:
副反应:
实验步骤:
i.在50mL仪器a中加入5mL苯甲醛、14mL乙酸酐和12g无水碳酸钾粉末(过量),加热回流45min。
ⅱ.向反应混合物中加入40mL蒸馏水浸泡几分钟,进行水蒸气蒸馏。
ⅲ.将烧瓶冷却后,加入10g碳酸钠,再加入70mL水,加热煮沸,趁热过滤。
iV.待滤液冷却至室温后,在搅拌下小心加入40mL1:1盐酸,使溶液呈酸性。
V.冷却结晶,抽滤,用少量试剂b洗涤,80C烘干,得粗产品4.5g。
相关物质物理性质如表所示:
溶解度:g/100mL
相对分
名称 密度/gcm3 熔点/C 沸点/C
子质量
水 醇 醚
苯甲醛 106 1.04 26 178~179 0.3 互溶 互溶
乙酸酐 102 1.08 73 138~140 遇水生成乙酸 溶 不溶
肉桂酸 148 1.24 133~134 300 0.04 24 溶
(1)加热回流装置中仪器a的名称是 ,不使用水冷冷凝管而用空气冷凝管是为了 。
(2)碳酸钾使用前应干燥并研细,目的是 。
(3)水蒸气蒸馏装置中毛细管的主要作用是 ,步骤ⅱ中蒸出的物质是苯甲醛与水的低沸点
共沸物,判断蒸馏完成的方法是 。
(4)步骤ⅲ中趁热过滤除去的主要物质是 (填名称)。
(5)步骤V中试剂b是 。
(6)本实验肉桂酸的产率最接近_______(填标号)。
A.50% B.60% C.70% D.80%
高三化学试卷 第7页,共10页
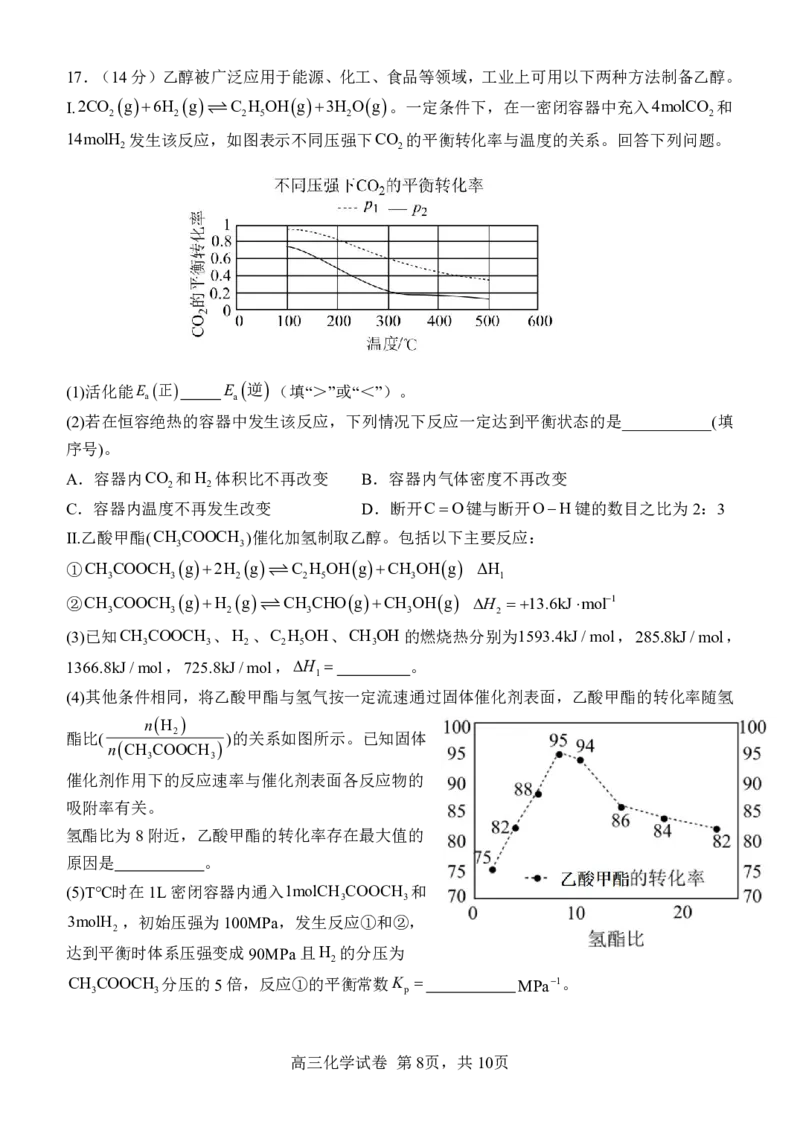
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}17.(14分)乙醇被广泛应用于能源、化工、食品等领域,工业上可用以下两种方法制备乙醇。
Ⅰ.2CO g6H g C H OHg3H Og。一定条件下,在一密闭容器中充入4molCO 和
2 2 2 5 2 2
14molH 发生该反应,如图表示不同压强下CO 的平衡转化率与温度的关系。回答下列问题。
2 2
(1)活化能E 正 E 逆(填“>”或“<”)。
a a
(2)若在恒容绝热的容器中发生该反应,下列情况下反应一定达到平衡状态的是___________(填
序号)。
A.容器内CO 和H 体积比不再改变 B.容器内气体密度不再改变
2 2
C.容器内温度不再发生改变 D.断开CO键与断开OH键的数目之比为2:3
Ⅱ.乙酸甲酯(CH COOCH )催化加氢制取乙醇。包括以下主要反应:
3 3
①CH COOCH g2H g C H OHgCH OHg ΔH
3 3 2 2 5 3 1
②CH COOCH gH g CH CHOgCH OHg H 13.6kJmol1
3 3 2 3 3 2
(3)已知CH COOCH 、H 、C H OH、CH OH的燃烧热分别为1593.4kJ/mol,285.8kJ/mol,
3 3 2 2 5 3
1366.8kJ/mol,725.8kJ/mol,H 。
1
(4)其他条件相同,将乙酸甲酯与氢气按一定流速通过固体催化剂表面,乙酸甲酯的转化率随氢
nH
酯比( 2 )的关系如图所示。已知固体
nCH COOCH
3 3
催化剂作用下的反应速率与催化剂表面各反应物的
吸附率有关。
氢酯比为8附近,乙酸甲酯的转化率存在最大值的
原因是 。
(5)T℃时在1L密闭容器内通入1molCH COOCH 和
3 3
3molH ,初始压强为100MPa,发生反应①和②,
2
达到平衡时体系压强变成90MPa且H 的分压为
2
CH COOCH 分压的5倍,反应①的平衡常数K MPa1。
3 3 p
高三化学试卷 第8页,共10页
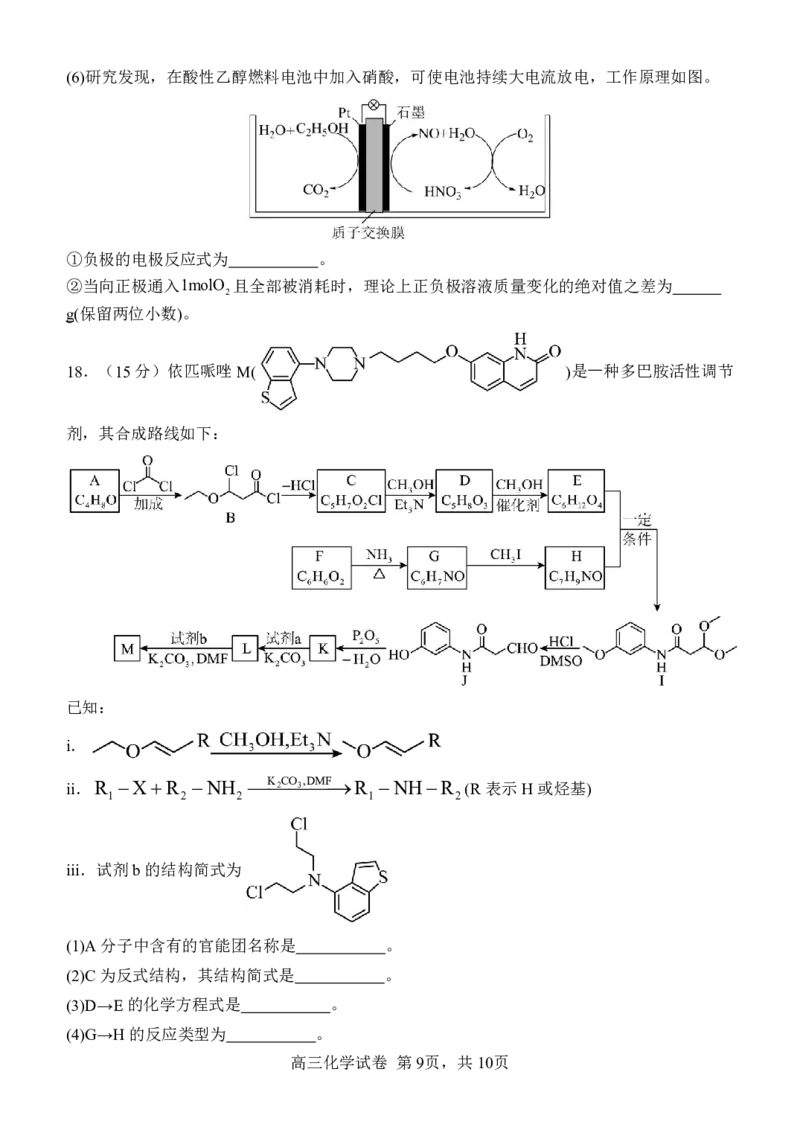
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}(6)研究发现,在酸性乙醇燃料电池中加入硝酸,可使电池持续大电流放电,工作原理如图。
①负极的电极反应式为 。
②当向正极通入1molO 且全部被消耗时,理论上正负极溶液质量变化的绝对值之差为
2
g(保留两位小数)。
18.(15分)依匹哌唑M( )是⼀种多巴胺活性调节
剂,其合成路线如下:
已知:
i.
ii.R XR NH K2 CO3 ,DMFR NHR (R表示H或烃基)
1 2 2 1 2
iii.试剂b的结构简式为
(1)A分子中含有的官能团名称是 。
(2)C为反式结构,其结构简式是 。
(3)D→E的化学方程式是 。
(4)G→H的反应类型为 。
高三化学试卷 第9页,共10页
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}(5)K转化为L的过程中,K CO 可吸收生成的HBr,则试剂a的结构简式是 。
2 3
(6)X是E的同分异构体,写出满足下列条件的X的结构简式 。
a.1molX与足量的Na反应可产生2mol H b.核磁共振氢谱显示有3组峰
2
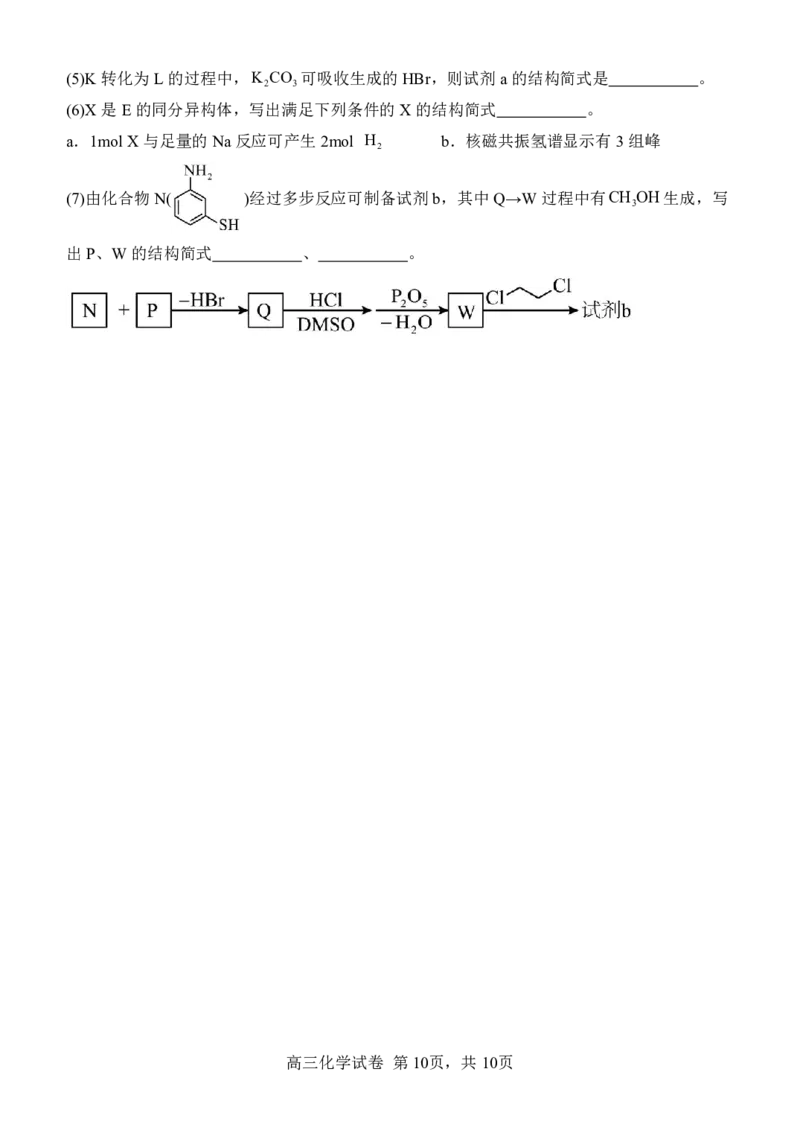
(7)由化合物N( )经过多步反应可制备试剂b,其中Q→W过程中有CH OH生成,写
3
出P、W的结构简式 、 。
高三化学试卷 第10页,共10页
{#{QQABBYAQggCIAIJAARgCEwEQCkEQkBACACoOQAAMsAIAyBFABAA=}#}