文档内容
2023—2024 学年度下学期 2021 级
3 月月考化学试卷
时间:75分钟 满分:100分
命题人:金双娇 审题人:蔡艳
考试时间:2024年3月2日
可能用到的相对原子质量:H-1 O-16 Na-23 S-32 Fe-56 Zr-91 Pb-207
一、选择题(本题包括15个小题,每小3分,共45分,每小题只有1个选项符合题意)
1.“十四五”生态环保工作强调要落实“减污降碳”的总要求。下列说法不正确的是
A.推广使用煤液化技术,可减少二氧化碳的排放
B.采用化学链燃烧技术,对二氧化碳进行捕集和再利用
C.开发太阳能、风能、生物质能等新能源是践行低碳生活的有效途径
D.人工合成淀粉技术的应用,有助于实现“碳达峰”和“碳中和”
2.劳动有利于“知行合一”。下列劳动项目与所述的化学知识没有关联的是
选
劳动项目 化学知识
项
A 帮厨活动:帮食堂师傅煎鸡蛋准备午餐 加热使蛋白质变性
B 环保行动:宣传使用聚乳酸制造的包装材料 聚乳酸在自然界可生物降解
C 家务劳动:擦干已洗净的铁锅,以防生锈 铁丝在 中燃烧生成
D 学农活动:利用秸秆、厨余垃圾等生产沼气 沼气中含有的 可作燃料
3.下列化学用语表示正确的是
A.顺-2-丁烯的球棍模型:
B.碳的基态原子轨道表示式:
C. 的空间结构: (平面三角形)
1
学科网(北京)股份有限公司D. 的形成过程:
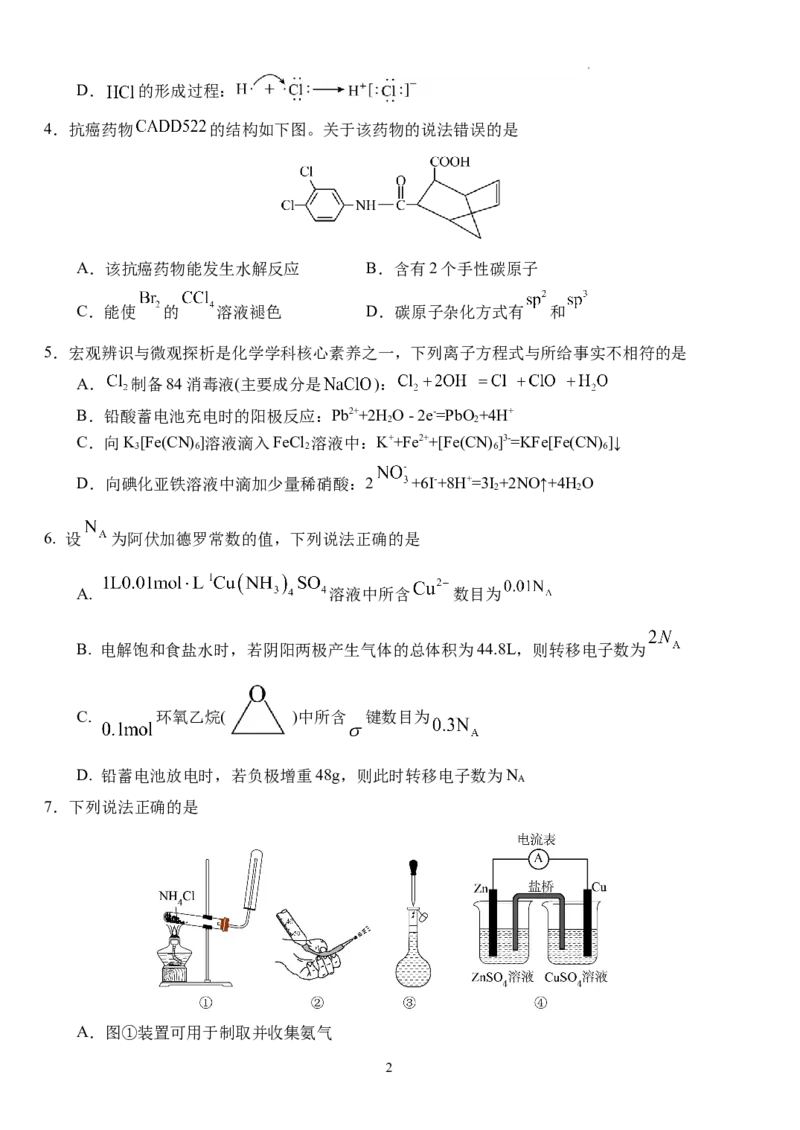
4.抗癌药物 的结构如下图。关于该药物的说法错误的是
A.该抗癌药物能发生水解反应 B.含有2个手性碳原子
C.能使 的 溶液褪色 D.碳原子杂化方式有 和
5.宏观辨识与微观探析是化学学科核心素养之一,下列离子方程式与所给事实不相符的是
A. 制备84消毒液(主要成分是 ):
B.铅酸蓄电池充电时的阳极反应:Pb2++2H O - 2e-=PbO+4H+
2 2
C.向K[Fe(CN) ]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN)]3-=KFe[Fe(CN) ]↓
3 6 2 6 6
D.向碘化亚铁溶液中滴加少量稀硝酸:2 +6I-+8H+=3I +2NO↑+4HO
2 2
6. 设 为阿伏加德罗常数的值,下列说法正确的是
A. 溶液中所含 数目为
B. 电解饱和食盐水时,若阴阳两极产生气体的总体积为44.8L,则转移电子数为
C. 环氧乙烷( )中所含 键数目为
D. 铅蓄电池放电时,若负极增重48g,则此时转移电子数为N
A
7.下列说法正确的是
A.图①装置可用于制取并收集氨气
2
学科网(北京)股份有限公司B.图②操作可排出盛有 溶液滴定管尖嘴内的气泡
C.图③操作俯视刻度线定容会导致所配溶液浓度偏大
D.图④装置盐桥中阳离子向 溶液中迁移
8.探究卤族元素单质及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 现象 结论
分层,下层由紫红色
往碘的 溶液中加入等体 碘在浓 溶液中的溶解能力大于
A 变为浅粉红色,上层
积的浓 溶液,振荡 在 中的溶解能力
呈棕黄色
用玻璃棒蘸取次氯酸钠溶液点
B 试纸变白 次氯酸钠溶液呈中性
在 试纸上
向 溶
液中先滴加4滴0.1mol∙L-1
先产生白色沉淀,再 转化为 , 溶解度小
C KCl溶液,观察现象,振荡试
产生黄色沉淀 于 溶解度
管,再滴加4滴
溶液
将CHCHX(卤代烃)与NaOH
3 2
证明CHCHX中的卤素原子的种
3 2
D 溶液共热,冷却后取上层水溶 观察沉淀颜色
类
液,加入AgNO 溶液
3
9.石墨与F 在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具润滑性,其
2
单层局部结构如图所示。下列关于该化合物的说法正确的
是
A.与石墨相比,(CF)x导电性增强
B.与石墨相比,(CF)x抗氧化性增强
C.(CF)x中 的键长比 短
D.1mol(CF)x中含有2xmol共价单键
10.某种镁盐具有良好的电化学性能,其阴离子结构如右图所示。W、X、
Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和
等于Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的
是
3
学科网(北京)股份有限公司A.W与X的化合物为极性分子 B.第一电离能
C.Q的氧化物是两性氧化物 D.该阴离子中含有配位键
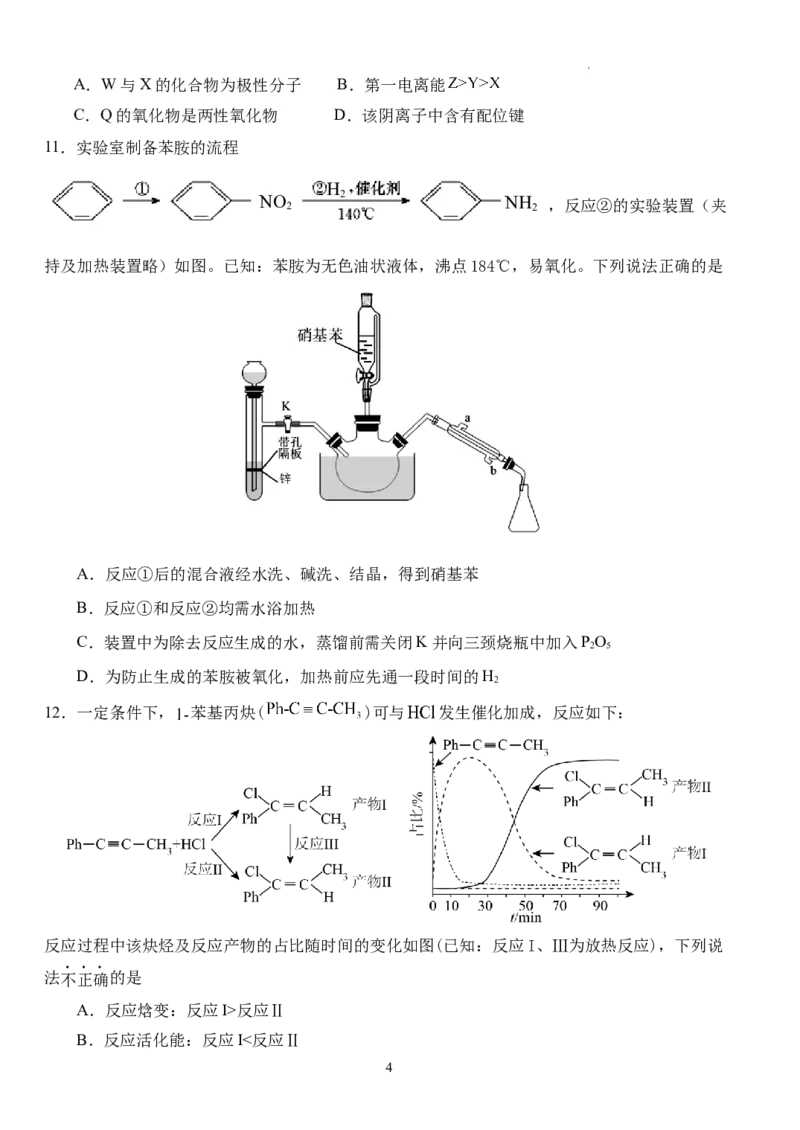
11.实验室制备苯胺的流程
H
NO 2 2 N H 2 ,反应②的实验装置(夹
持及加热装置略)如图。已知:苯胺为无色油状液体,沸点184℃,易氧化。下列说法正确的是
A.反应①后的混合液经水洗、碱洗、结晶,得到硝基苯
B.反应①和反应②均需水浴加热
C.装置中为除去反应生成的水,蒸馏前需关闭K并向三颈烧瓶中加入PO
2 5
D.为防止生成的苯胺被氧化,加热前应先通一段时间的H
2
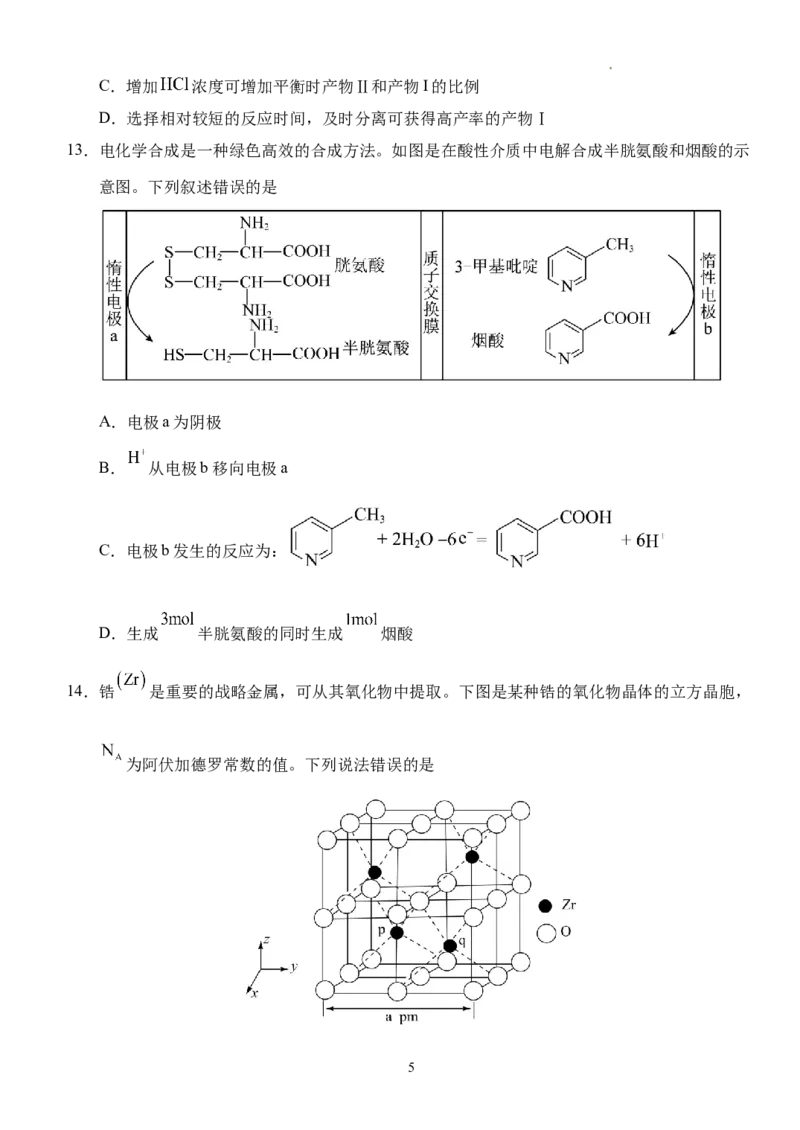
12.一定条件下, 苯基丙炔( )可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说
法不正确的是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
4
学科网(北京)股份有限公司C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
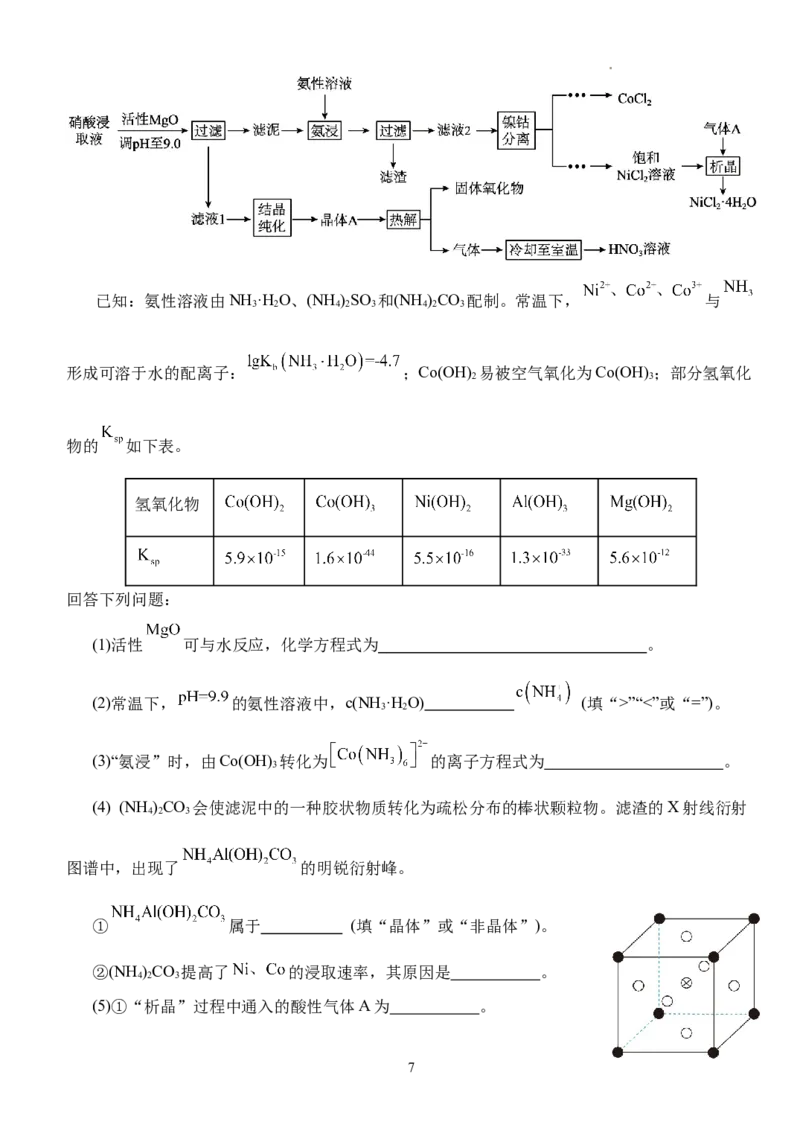
13.电化学合成是一种绿色高效的合成方法。如图是在酸性介质中电解合成半胱氨酸和烟酸的示
意图。下列叙述错误的是
A.电极a为阴极
B. 从电极b移向电极a
C.电极b发生的反应为:
D.生成 半胱氨酸的同时生成 烟酸
14.锆 是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方晶胞,
为阿伏加德罗常数的值。下列说法错误的是
5
学科网(北京)股份有限公司A.该氧化物的化学式为
B.该氧化物的密度为
C. 原子之间的最短距离为
D.若坐标取向不变,将p点 原子平移至原点,则q点 原子位于晶胞 面的面心
15.甘氨酸 是人体必需氨基酸之一、在 时, 、
和 的分布分数【如 】与溶液
关系如图。下列说法错误的是
A.甘氨酸具有两性 B.曲线c代表
C.NH +CHCOO-+H O NH +CHCOOH+OH—的平衡常数
3 2 2 3
D.
二、非选择题(本题包括4个小题,共55分)
16.(14分) 均是重要的战略性金属。从处理后的矿石硝酸浸取液(
)中,利用氨浸工艺可提取 ,并获得高附加值化工产品。工
艺流程如下:
6
学科网(北京)股份有限公司已知:氨性溶液由NH ·H O、(NH )SO 和(NH )CO 配制。常温下, 与
3 2 4 2 3 4 2 3
形成可溶于水的配离子: ;Co(OH) 易被空气氧化为Co(OH) ;部分氢氧化
2 3
物的 如下表。
氢氧化物
回答下列问题:
(1)活性 可与水反应,化学方程式为 。
(2)常温下, 的氨性溶液中,c(NH ·H O) (填“>”“<”或“=”)。
3 2
(3)“氨浸”时,由Co(OH) 转化为 的离子方程式为 。
3
(4) (NH )CO 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射
4 2 3
图谱中,出现了 的明锐衍射峰。
① 属于 (填“晶体”或“非晶体”)。
②(NH )CO 提高了 的浸取速率,其原因是 。
4 2 3
(5)①“析晶”过程中通入的酸性气体A为 。
7
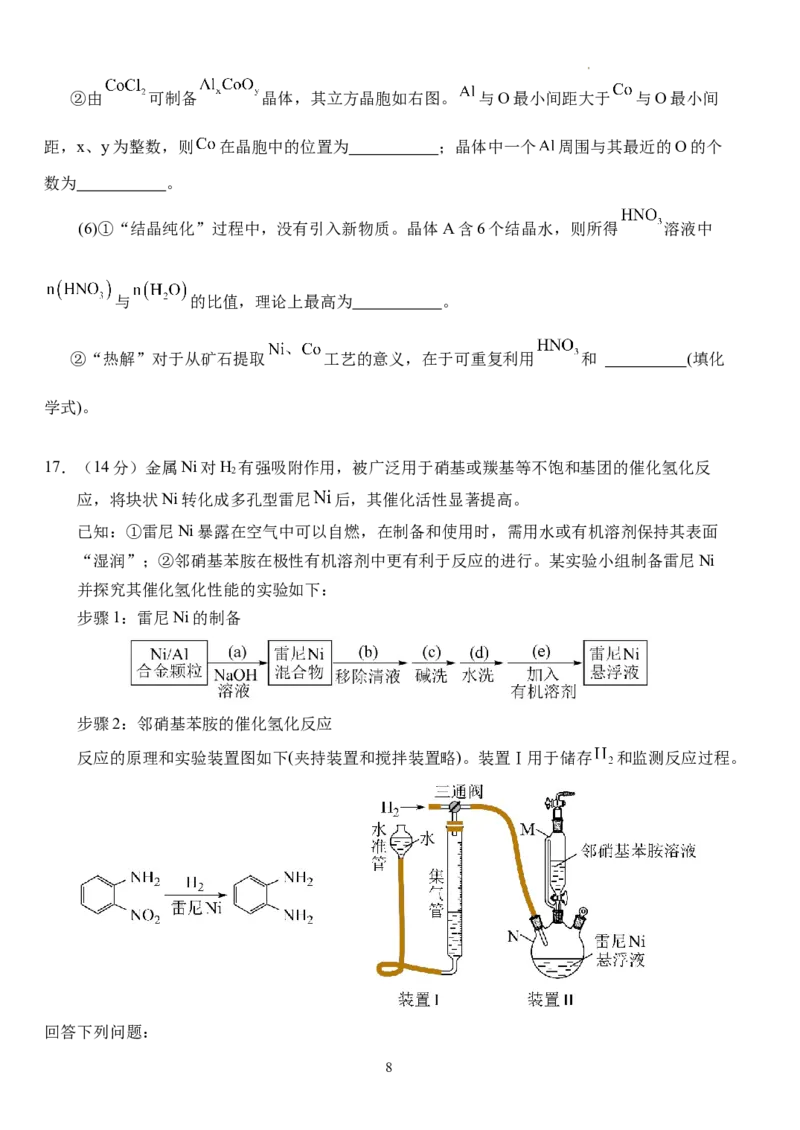
学科网(北京)股份有限公司②由 可制备 晶体,其立方晶胞如右图。 与O最小间距大于 与O最小间
距,x、y为整数,则 在晶胞中的位置为 ;晶体中一个 周围与其最近的O的个
数为 。
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得 溶液中
与 的比值,理论上最高为 。
②“热解”对于从矿石提取 工艺的意义,在于可重复利用 和 (填化
学式)。
17.(14分)金属Ni对H 有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反
2
应,将块状Ni转化成多孔型雷尼 后,其催化活性显著提高。
已知:①雷尼Ni暴露在空气中可以自燃,在制备和使用时,需用水或有机溶剂保持其表面
“湿润”;②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。某实验小组制备雷尼Ni
并探究其催化氢化性能的实验如下:
步骤1:雷尼Ni的制备
步骤2:邻硝基苯胺的催化氢化反应
反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置Ⅰ用于储存 和监测反应过程。
回答下列问题:
8
学科网(北京)股份有限公司(1)操作(a)中,反应的离子方程式是_______;
(2)操作(d)中,判断雷尼 被水洗净的方法是_______;
(3)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是_______;
A.丙酮 B.四氯化碳 C.乙醇 D.正己烷
(4)向集气管中充入 时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置Ⅱ
供气,此时孔路位置需调节为_______;
(5)仪器M的名称是________________;
(6)反应前应向装置Ⅱ中通入 一段时间,目的是__________________________;
(7)如果将三颈瓶N中的导气管口插入液面以下,可能导致的后果是_____________;
(8)判断氢化反应完全的现象是_____________________________________________。
18.(13分)聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①C HC H(g) + 21/2 O (g) = 8CO(g)+5HO(g) △H=-4386.9 kJ.mo1-1
6 5 2 5 2 2 2 1
②C HCH=CH(g) + 10 O (g) = 8CO(g)+4HO(g) △H =-4263.l kJ.mol-1
6 5 2 2 2 2 2
③H(g)+1/2 O(g) = HO(g) = △H=-241.8 kJ.mo1-l
2 2 2 3
计算反应④C HC H(g) C HCH=CH(g)+H(g) 的 _______kJ.mol-1;
6 5 2 5 6 5 2 2
(2)在某温度、 下,向反应器中充入 气态乙苯发生反应④,其平衡转化率为50%,
欲将平衡转化率提高至75%,需要向反应器中充入_______ 水蒸气作为稀释气(计算时忽略副
反应);
9
学科网(北京)股份有限公司(3)在 、 下,以水蒸气作稀释气。Fe O 作催
2 3
化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反
应:
⑤ C HC H(g) C H(g)+CH =CH (g)
6 5 2 5 6 6 2 2
⑥ C HC H(g)+H(g) C HCH(g)+CH (g)
6 5 2 5 2 6 5 3 4
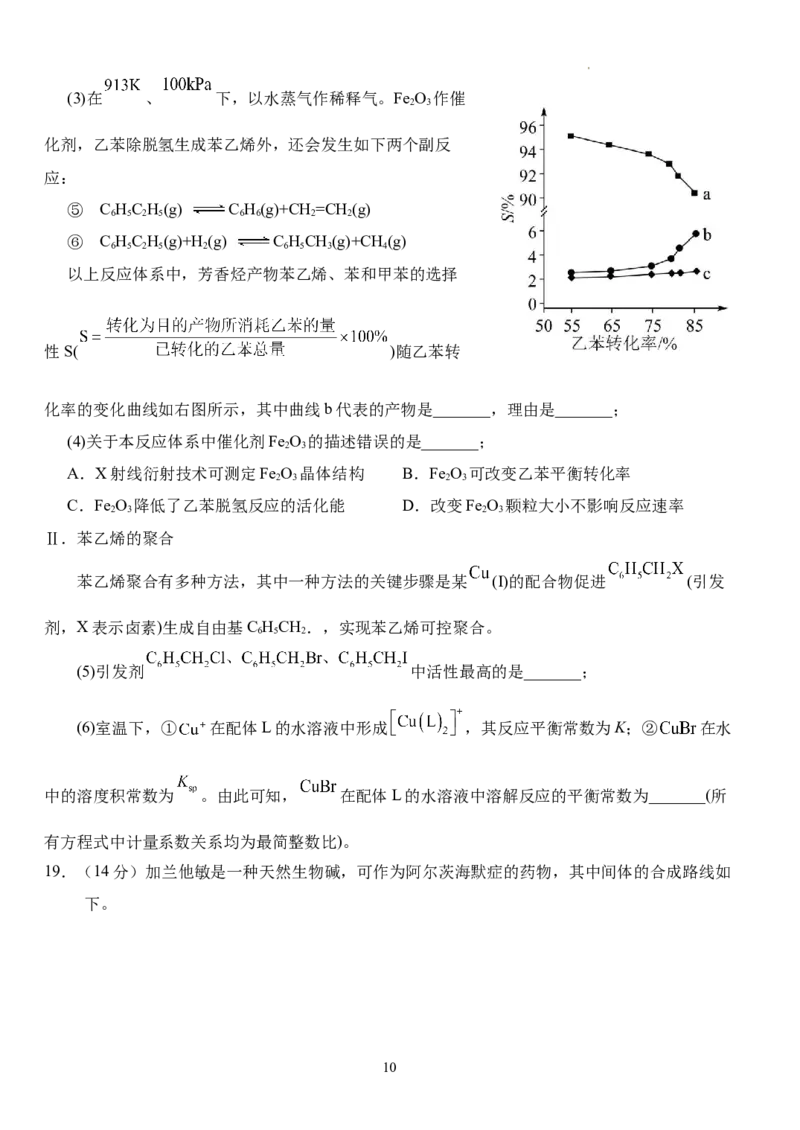
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择
性S( )随乙苯转
化率的变化曲线如右图所示,其中曲线b代表的产物是_______,理由是_______;
(4)关于本反应体系中催化剂Fe O 的描述错误的是_______;
2 3
A.X射线衍射技术可测定Fe O 晶体结构 B.Fe O 可改变乙苯平衡转化率
2 3 2 3
C.Fe O 降低了乙苯脱氢反应的活化能 D.改变Fe O 颗粒大小不影响反应速率
2 3 2 3
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某 (Ⅰ)的配合物促进 (引发
剂,X表示卤素)生成自由基C HCH.,实现苯乙烯可控聚合。
6 5 2
(5)引发剂 中活性最高的是_______;
(6)室温下,① 在配体L的水溶液中形成 ,其反应平衡常数为K;② 在水
中的溶度积常数为 。由此可知, 在配体L的水溶液中溶解反应的平衡常数为_______(所
有方程式中计量系数关系均为最简整数比)。
19.(14分)加兰他敏是一种天然生物碱,可作为阿尔茨海默症的药物,其中间体的合成路线如
下。
10
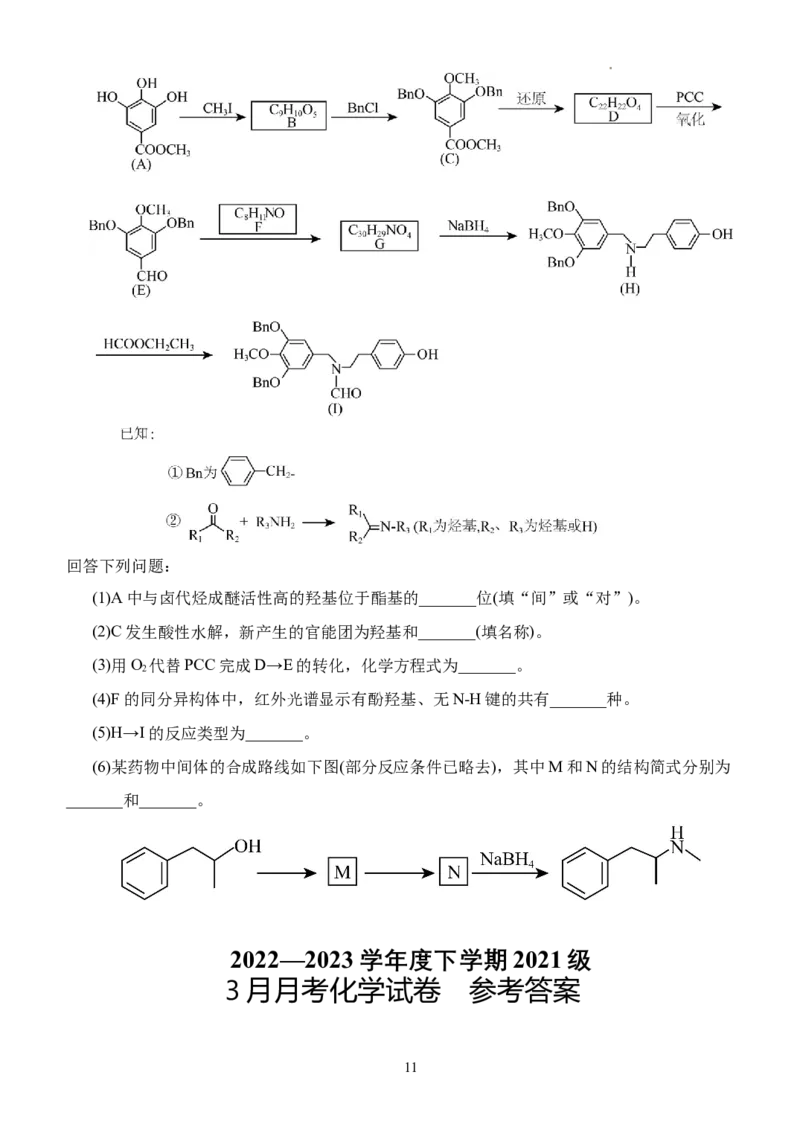
学科网(北京)股份有限公司回答下列问题:
(1)A中与卤代烃成醚活性高的羟基位于酯基的_______位(填“间”或“对”)。
(2)C发生酸性水解,新产生的官能团为羟基和_______(填名称)。
(3)用O 代替PCC完成D→E的转化,化学方程式为_______。
2
(4)F的同分异构体中,红外光谱显示有酚羟基、无N-H键的共有_______种。
(5)H→I的反应类型为_______。
(6)某药物中间体的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别为
_______和_______。
2022—2023 学年度下学期 2021 级
3 月月考化学试卷 参考答案
11
学科网(北京)股份有限公司1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
A C C B B D C A B A D C D B D
16.(14分,除标注外每空2分)
(1) (2分)
(2)>(1分)
(3) 或
(2分)
(4)晶体(1分)
减少胶状物质对镍钴氢氧化物的包裹,增加了滤泥与氨性溶液的接触面积(2分)
(5) (1分) 体心(1分) 12(1分)
(6)0.4或 (2分) (1分)
17.(14分,除标注外每空2分)
(1)2Al+2OH-+2H O=2AlO +3H ↑(2分)
2 2
(2)取最后一次洗涤液于试管中,滴加几滴酚酞,如果溶液不变粉红色,则证明洗涤干净,否
则没有洗涤干净(2分)
(3)C(2分) (4)B(2分)
(5)恒压滴液漏斗(1分) (6)排除装置中的空气,防止雷尼 自燃(2分)
(7)管道中气流不稳,不利于监测反应过程(2分)(8)集气管中液面不再改变(1分)
12
学科网(北京)股份有限公司18.(13分,除标注外每空2分)
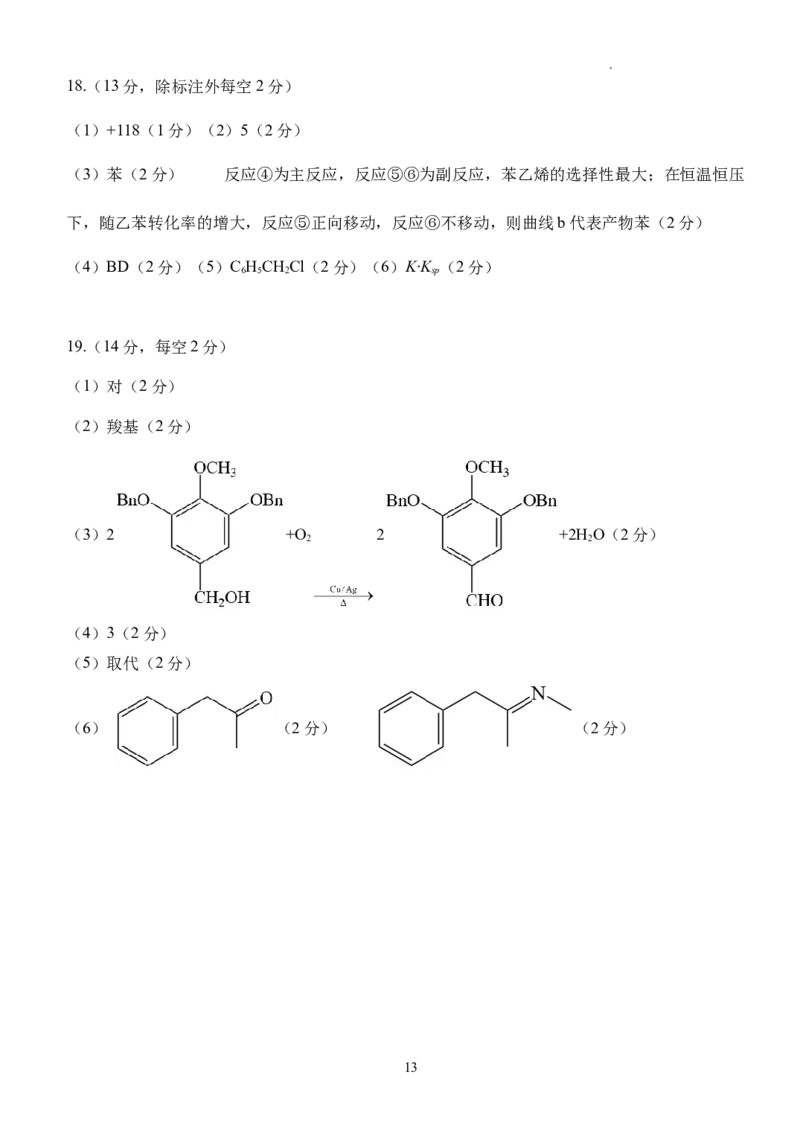
(1)+118(1分)(2)5(2分)
(3)苯(2分) 反应④为主反应,反应⑤⑥为副反应,苯乙烯的选择性最大;在恒温恒压
下,随乙苯转化率的增大,反应⑤正向移动,反应⑥不移动,则曲线b代表产物苯(2分)
(4)BD(2分)(5)C HCHCl(2分)(6)K∙K (2分)
6 5 2 sp
19.(14分,每空2分)
(1)对(2分)
(2)羧基(2分)
(3)2 +O 2 +2H O(2分)
2 2
(4)3(2分)
(5)取代(2分)
(6) (2分) (2分)
13
学科网(北京)股份有限公司