文档内容
济宁市第一中学 2024-2025 学年度阶段性学业检测
高二化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3. 考试结束后将本试卷和答题卡一并收回。
4. 本试卷考试时间为90分钟,满分为100分。
可能用到的相对原子质量:H1 C12 N14 O16 F19 P31 Cl35.5 Br80
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.下列有关化学用语的表达正确的是( )
A. 基态Cl原子的核外电子排布式:3s23p5
B. 甲基的电子式:
C. S2 的结构示意图:
D. 基态Sc原子的价层电子轨道表示式:
2. 下列各项中正确的是( )
A. 中所有碳原子可能在同一平面上
B.CH CH(CH )C≡CCH 的命名为2-甲基-3-戊炔
3 3 3
C. 聚丙炔、聚氯乙烯和苯分子中均不含有碳碳双键
D.C H 属于烯烃的同分异构体共有4种(含顺反异构)
4 8
3. 在光照的条件下,将1molCH 与一定量的氯气充分混合,经过一段时间,甲烷和氯气均无剩余,生成CH Cl、
4 3
CH Cl 、CHCl 、CCl 和HCl,若已知生成的二氯甲烷、三氯甲烷、四氯化碳的物质的量分别为Xmol,Ymol,Zmol,
2 2 3 4
该反应中生成HCl的物质的量是( )
A.(1+X+2Y+3Z)mol B.(X+Y+Z)mol
C.(2X+3Y+4Z)mol D.(1-X-Y-Z)mol
4.某有机物的结构如图所示,则下列说法中正确的是( )
A.该有机物中有4种官能团
B. 该有机物的分子式为C H O
11 14 3
C.1mol该有机物能与足量Na反应可生成2molH
2
化学试题 第1页,共8页
{#{QQABaY284gAYgAYACQ7LA00ACEiQsJERJQouxQAYqARCwAFABAA=}#}D.该有机物分子最多可实现22个原子共平面
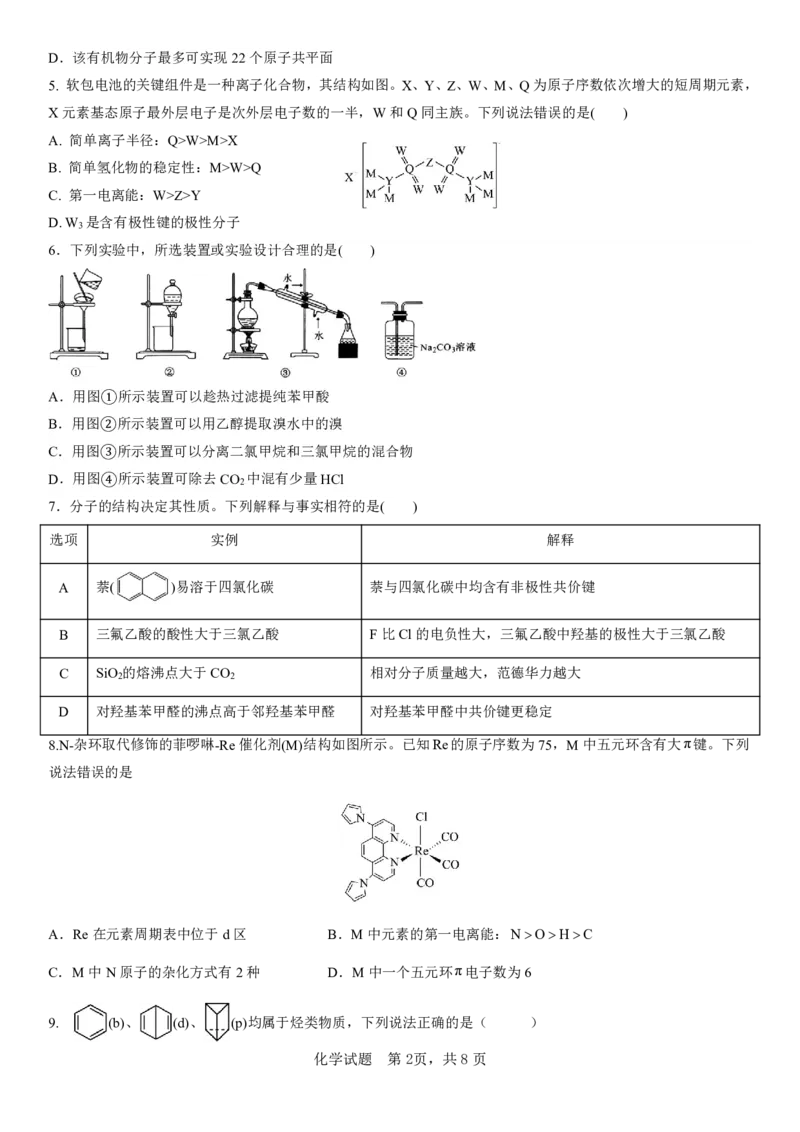
5. 软包电池的关键组件是一种离子化合物,其结构如图。X、Y、Z、W、M、Q为原子序数依次增大的短周期元素,
X元素基态原子最外层电子是次外层电子数的一半,W和Q同主族。下列说法错误的是( )
A. 简单离子半径:Q>W>M>X
B. 简单氢化物的稳定性:M>W>Q
C. 第一电离能:W>Z>Y
D.W 是含有极性键的极性分子
3
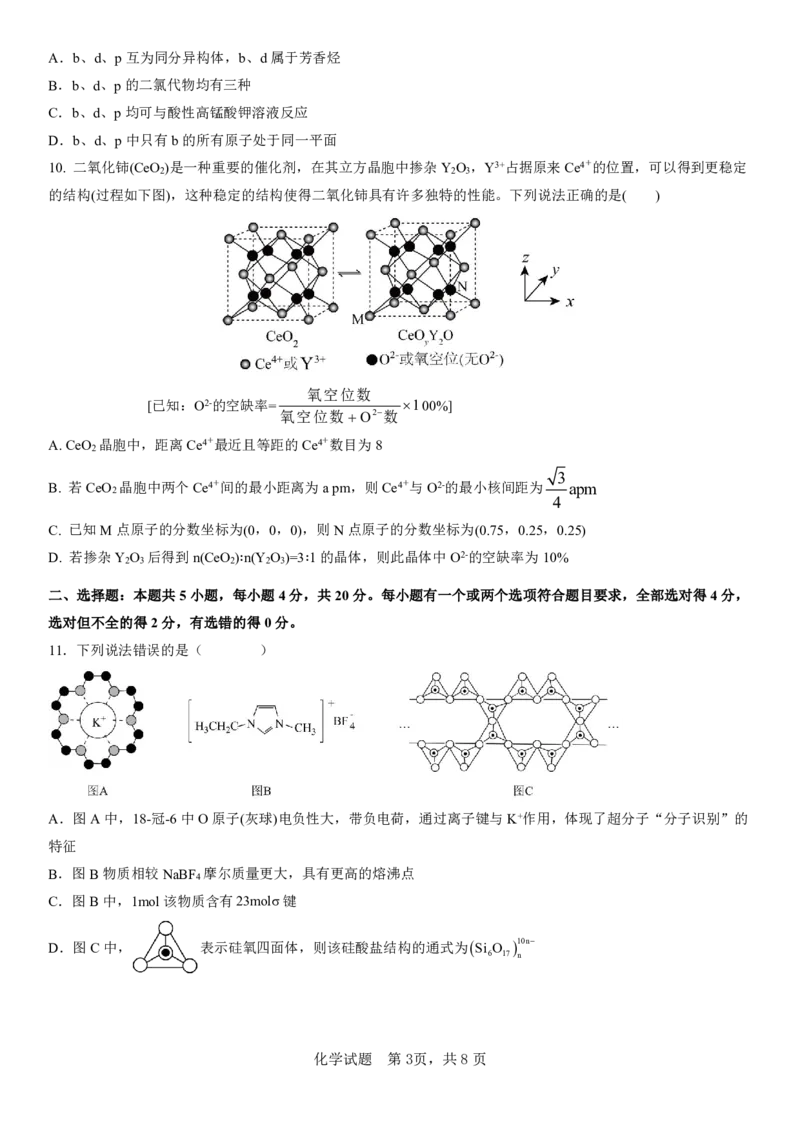
6.下列实验中,所选装置或实验设计合理的是( )
A.用图 所示装置可以趁热过滤提纯苯甲酸
B.用图
①
所示装置可以用乙醇提取溴水中的溴
C.用图
②
所示装置可以分离二氯甲烷和三氯甲烷的混合物
D.用图
③
所示装置可除去CO
2
中混有少量HCl
7.分子的 ④ 结构决定其性质。下列解释与事实相符的是( )
选项 实例 解释
A 萘( )易溶于四氯化碳 萘与四氯化碳中均含有非极性共价键
B 三氟乙酸的酸性大于三氯乙酸 F比Cl的电负性大,三氟乙酸中羟基的极性大于三氯乙酸
C SiO 2 的熔沸点大于CO 2 相对分子质量越大,范德华力越大
D 对羟基苯甲醛的沸点高于邻羟基苯甲醛 对羟基苯甲醛中共价键更稳定
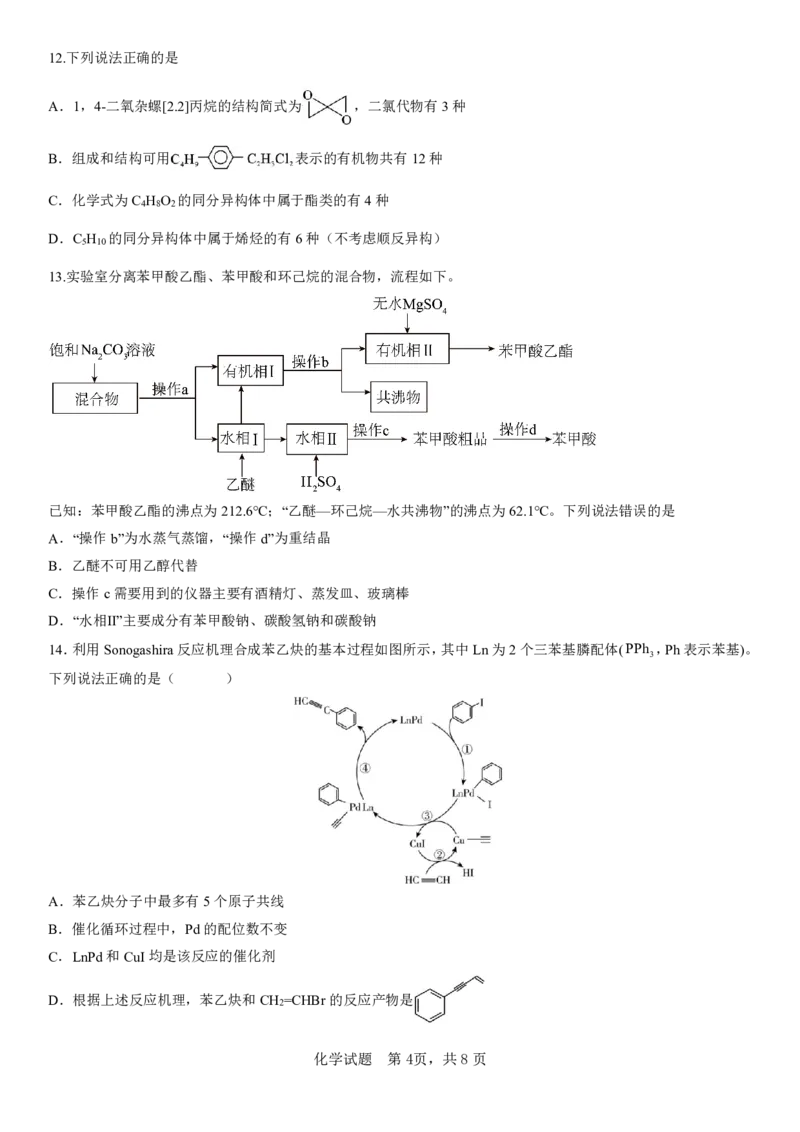
8.N-杂环取代修饰的菲啰啉-Re催化剂(M)结构如图所示。已知Re的原子序数为75,M中五元环含有大π键。下列
说法错误的是
A.Re在元素周期表中位于d区 B.M中元素的第一电离能:NOHC
C.M中N原子的杂化方式有2种 D.M中一个五元环π电子数为6
9. (b)、 (d)、 (p)均属于烃类物质,下列说法正确的是( )
化学试题 第2页,共8页
{#{QQABaY284gAYgAYACQ7LA00ACEiQsJERJQouxQAYqARCwAFABAA=}#}A.b、d、p互为同分异构体,b、d属于芳香烃
B.b、d、p的二氯代物均有三种
C.b、d、p均可与酸性高锰酸钾溶液反应
D.b、d、p中只有b的所有原子处于同一平面
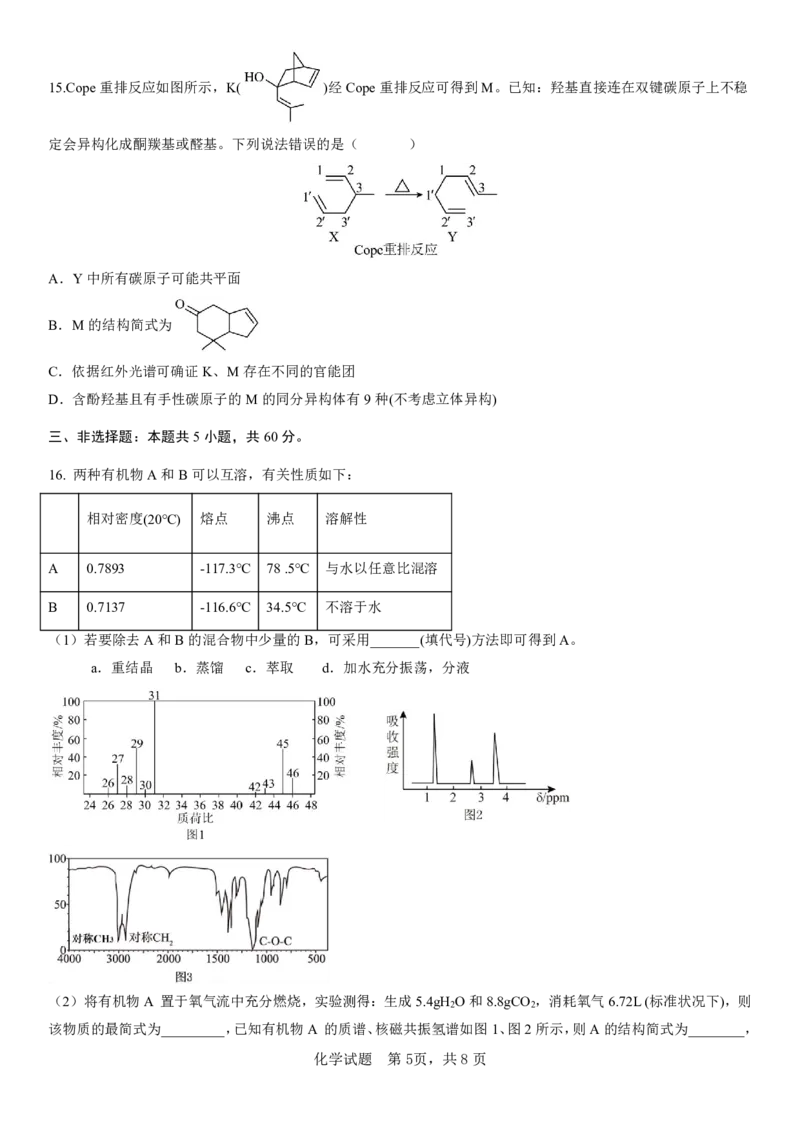
10. 二氧化铈(CeO )是一种重要的催化剂,在其立方晶胞中掺杂Y O ,Y3+占据原来Ce4+的位置,可以得到更稳定
2 2 3
的结构(过程如下图),这种稳定的结构使得二氧化铈具有许多独特的性能。下列说法正确的是( )
氧空位数
[已知:O2-的空缺率= 100%]
氧空位数 O2数
A.CeO 晶胞中,距离Ce4+最近且等距的Ce4+数目为8
2
3
B. 若CeO 晶胞中两个Ce4+间的最小距离为apm,则Ce4+与O2-的最小核间距为 apm
2
4
C. 已知M点原子的分数坐标为(0,0,0),则N点原子的分数坐标为(0.75,0.25,0.25)
D. 若掺杂Y O 后得到n(CeO ) n(Y O )=3 1的晶体,则此晶体中O2-的空缺率为10%
2 3 2 2 3
∶ ∶
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,
选对但不全的得2分,有选错的得0分。
11.下列说法错误的是( )
A.图A中,18-冠-6中O原子(灰球)电负性大,带负电荷,通过离子键与K+作用,体现了超分子“分子识别”的
特征
B.图B物质相较NaBF 摩尔质量更大,具有更高的熔沸点
4
C.图B中,1mol该物质含有23molσ键
D.图C中, 表示硅氧四面体,则该硅酸盐结构的通式为Si O 10n
6 17 n
化学试题 第3页,共8页
{#{QQABaY284gAYgAYACQ7LA00ACEiQsJERJQouxQAYqARCwAFABAA=}#}12.下列说法正确的是
A.1,4-二氧杂螺[2.2]丙烷的结构简式为 ,二氯代物有3种
B.组成和结构可用 表示的有机物共有12种
C.化学式为C H O 的同分异构体中属于酯类的有4种
4 8 2
D.C H 的同分异构体中属于烯烃的有6种(不考虑顺反异构)
5 10
13.实验室分离苯甲酸乙酯、苯甲酸和环己烷的混合物,流程如下。
已知:苯甲酸乙酯的沸点为212.6℃;“乙醚—环己烷—水共沸物”的沸点为62.1℃。下列说法错误的是
A.“操作b”为水蒸气蒸馏,“操作d”为重结晶
B.乙醚不可用乙醇代替
C.操作c需要用到的仪器主要有酒精灯、蒸发皿、玻璃棒
D.“水相Ⅱ”主要成分有苯甲酸钠、碳酸氢钠和碳酸钠
14.利用Sonogashira反应机理合成苯乙炔的基本过程如图所示,其中Ln为2个三苯基膦配体(PPh ,Ph表示苯基)。
3
下列说法正确的是( )
A.苯乙炔分子中最多有5个原子共线
B.催化循环过程中,Pd的配位数不变
C.LnPd和CuI均是该反应的催化剂
D.根据上述反应机理,苯乙炔和CH =CHBr的反应产物是
2
化学试题 第4页,共8页
{#{QQABaY284gAYgAYACQ7LA00ACEiQsJERJQouxQAYqARCwAFABAA=}#}15.Cope重排反应如图所示,K( )经Cope重排反应可得到M。已知:羟基直接连在双键碳原子上不稳
定会异构化成酮羰基或醛基。下列说法错误的是( )
A.Y中所有碳原子可能共平面
B.M的结构简式为
C.依据红外光谱可确证K、M存在不同的官能团
D.含酚羟基且有手性碳原子的M的同分异构体有9种(不考虑立体异构)
三、非选择题:本题共5小题,共60分。
16. 两种有机物A和B可以互溶,有关性质如下:
相对密度(20℃) 熔点 沸点 溶解性
A 0.7893 -117.3℃ 78.5℃ 与水以任意比混溶
B 0.7137 -116.6℃ 34.5℃ 不溶于水
(1)若要除去A和B的混合物中少量的B,可采用_______(填代号)方法即可得到A。
a.重结晶 b.蒸馏 c.萃取 d.加水充分振荡,分液
(2)将有机物A 置于氧气流中充分燃烧,实验测得:生成5.4gH O和8.8gCO ,消耗氧气6.72L(标准状况下),则
2 2
该物质的最简式为_________,已知有机物A 的质谱、核磁共振氢谱如图1、图2所示,则A的结构简式为________,
化学试题 第5页,共8页
{#{QQABaY284gAYgAYACQ7LA00ACEiQsJERJQouxQAYqARCwAFABAA=}#}其官能团的名称为_________。
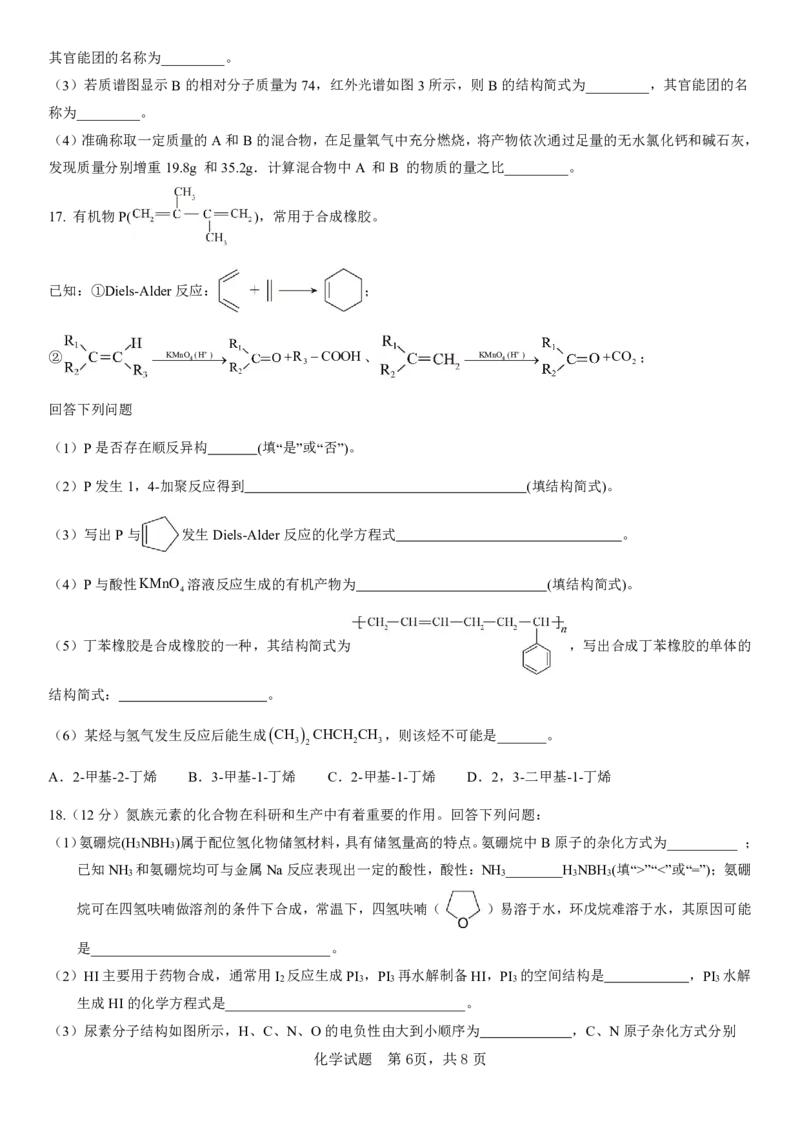
(3)若质谱图显示B的相对分子质量为74,红外光谱如图3所示,则B的结构简式为_________,其官能团的名
称为_________。
(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,
发现质量分别增重19.8g 和35.2g.计算混合物中A 和B 的物质的量之比_________。
17. 有机物P( ),常用于合成橡胶。
已知:①Diels-Alder反应: ;
② KMnO4(H) R
3
COOH、 KMnO4(H) CO
2
;
回答下列问题
(1)P是否存在顺反异构 (填“是”或“否”)。
(2)P发生1,4-加聚反应得到 (填结构简式)。
(3)写出P与 发生Diels-Alder反应的化学方程式 。
(4)P与酸性KMnO 溶液反应生成的有机产物为 (填结构简式)。
4
(5)丁苯橡胶是合成橡胶的一种,其结构简式为 ,写出合成丁苯橡胶的单体的
结构简式: 。
(6)某烃与氢气发生反应后能生成CH CHCH CH ,则该烃不可能是_______。
3 2 2 3
A.2-甲基-2-丁烯 B.3-甲基-1-丁烯 C.2-甲基-1-丁烯 D.2,3-二甲基-1-丁烯
18.(12分)氮族元素的化合物在科研和生产中有着重要的作用。回答下列问题:
(1)氨硼烷(H NBH )属于配位氢化物储氢材料,具有储氢量高的特点。氨硼烷中B原子的杂化方式为__________ ;
3 3
已知NH 和氨硼烷均可与金属Na反应表现出一定的酸性,酸性:NH ________H NBH (填“>”“<”或“=”);氨硼
3 3 3 3
烷可在四氢呋喃做溶剂的条件下合成,常温下,四氢呋喃( )易溶于水,环戊烷难溶于水,其原因可能
是__________________________________。
(2)HI主要用于药物合成,通常用I 反应生成PI ,PI 再水解制备HI,PI 的空间结构是 ,PI 水解
2 3 3 3 3
生成HI的化学方程式是__________________________________。
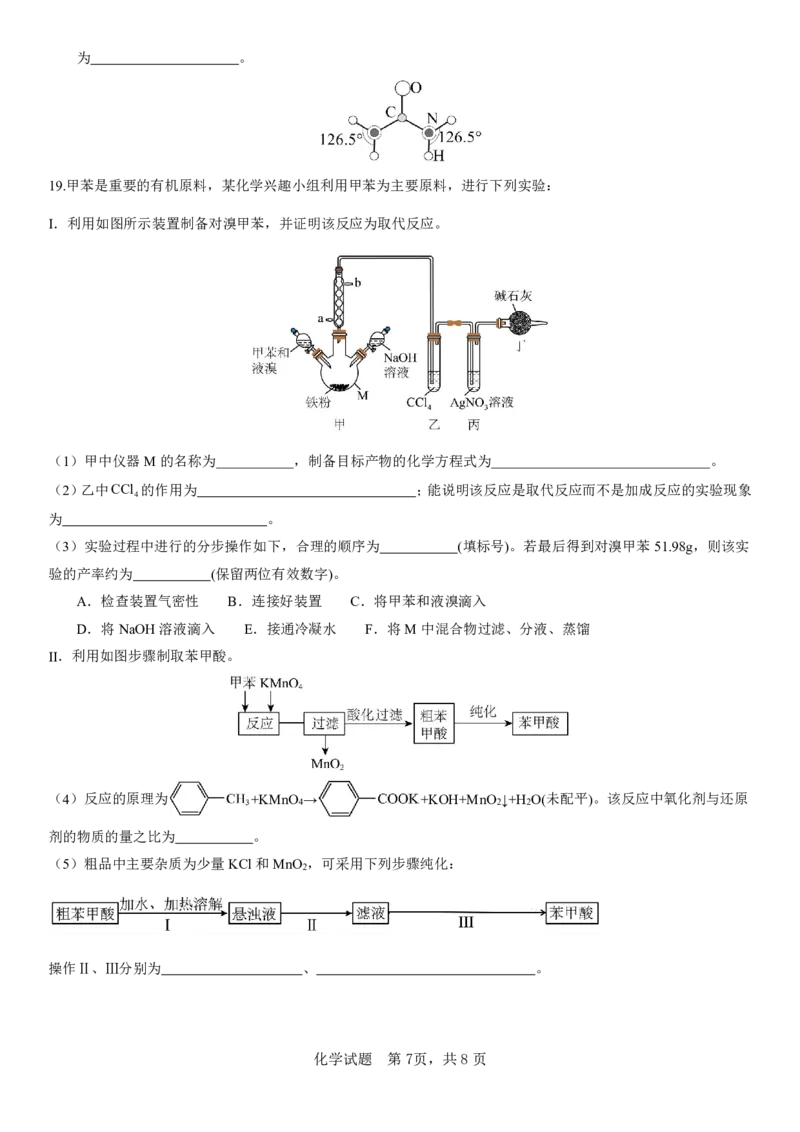
(3)尿素分子结构如图所示,H、C、N、O的电负性由大到小顺序为 ,C、N原子杂化方式分别
化学试题 第6页,共8页
{#{QQABaY284gAYgAYACQ7LA00ACEiQsJERJQouxQAYqARCwAFABAA=}#}为 。
19.甲苯是重要的有机原料,某化学兴趣小组利用甲苯为主要原料,进行下列实验:
Ⅰ.利用如图所示装置制备对溴甲苯,并证明该反应为取代反应。
(1)甲中仪器M的名称为 ,制备目标产物的化学方程式为 。
(2)乙中CCl 的作用为 ;能说明该反应是取代反应而不是加成反应的实验现象
4
为 。
(3)实验过程中进行的分步操作如下,合理的顺序为 (填标号)。若最后得到对溴甲苯51.98g,则该实
验的产率约为 (保留两位有效数字)。
A.检查装置气密性 B.连接好装置 C.将甲苯和液溴滴入
D.将NaOH溶液滴入 E.接通冷凝水 F.将M中混合物过滤、分液、蒸馏
Ⅱ.利用如图步骤制取苯甲酸。
(4)反应的原理为 +KMnO → +KOH+MnO ↓+H O(未配平)。该反应中氧化剂与还原
4 2 2
剂的物质的量之比为 。
(5)粗品中主要杂质为少量KCl和MnO ,可采用下列步骤纯化:
2
操作Ⅱ、Ⅲ分别为 、 。
化学试题 第7页,共8页
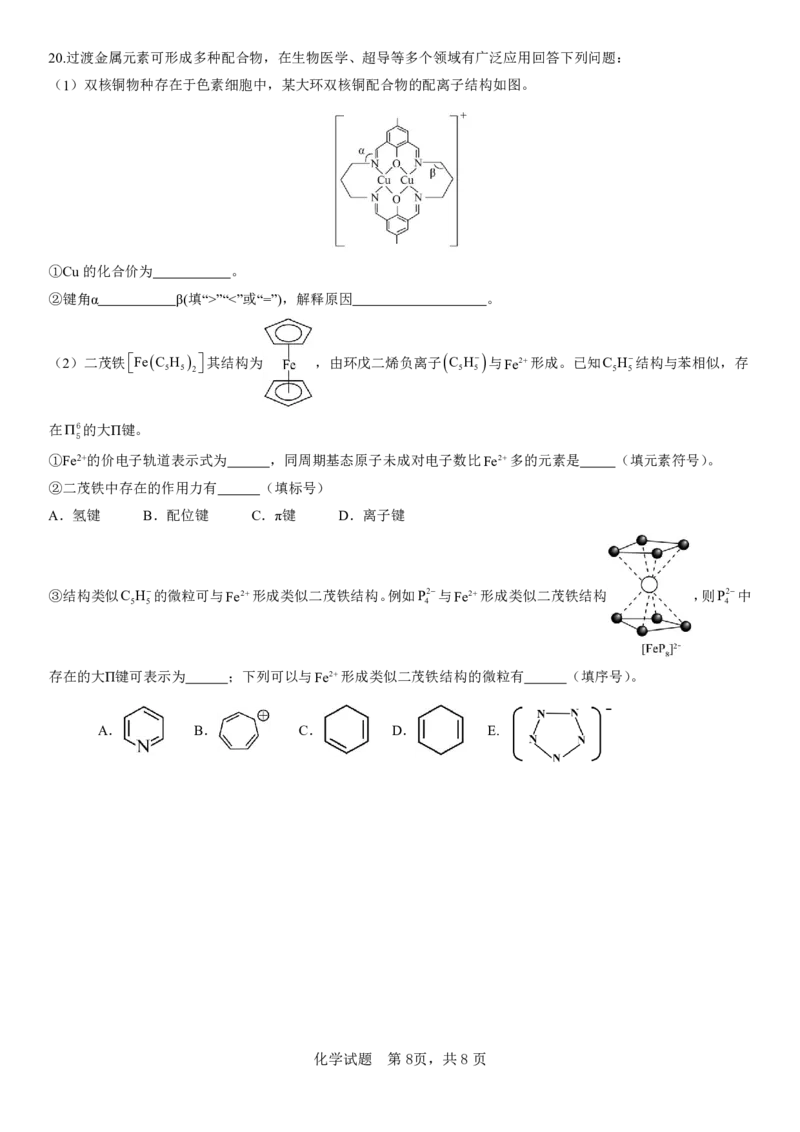
{#{QQABaY284gAYgAYACQ7LA00ACEiQsJERJQouxQAYqARCwAFABAA=}#}20.过渡金属元素可形成多种配合物,在生物医学、超导等多个领域有广泛应用回答下列问题:
(1)双核铜物种存在于色素细胞中,某大环双核铜配合物的配离子结构如图。
①Cu的化合价为 。
②键角α β(填“>”“<”或“=”),解释原因 。
(2)二茂铁
FeC
5
H
5
2
其结构为 ,由环戊二烯负离子 C
5
H
5
与Fe2形成。已知C
5
H
5
结构与苯相似,存
在6的大Π键。
5
①Fe2+的价电子轨道表示式为 ,同周期基态原子未成对电子数比Fe2多的元素是 (填元素符号)。
②二茂铁中存在的作用力有 (填标号)
A.氢键 B.配位键 C.π键 D.离子键
③结构类似C H的微粒可与Fe2形成类似二茂铁结构。例如P2与Fe2形成类似二茂铁结构 ,则P2中
5 5 4 4
存在的大П键可表示为 ;下列可以与Fe2形成类似二茂铁结构的微粒有 (填序号)。
A. B. C. D. E.
化学试题 第8页,共8页
{#{QQABaY284gAYgAYACQ7LA00ACEiQsJERJQouxQAYqARCwAFABAA=}#}