文档内容
2024 年湖北云学名校联盟高三年级 12 月联考
化学试卷
命题学校:云学研究院 审题人:云学研究院
考试时间:2024年12月13日14:30-17:05 时长:75分钟 总分:100分
可能用到的相对原子质量:H 1 B11 C12 N14 O16 S 32 Ba 137
一、选择题:本题共 15 小题,每小题3 分,共 45分。在每小题给出的四个选项中,
只有一项是符合题目要求的。
1.化学物质与生活密切相关。下列说法错误的是
A.味精的主要成分为谷氨酸钠
B.水溶液中的葡萄糖绝大部分为环状结构
C.酶是生物体内具有高效催化作用的蛋白质
D.ATP 分子中的磷酸与核糖之间通过磷酯键连接
2.化学促进了科学进步和社会发展。下列叙述中没有涉及化学变化的是
A.采用高温高压合成法将石墨转化为金刚石
B.我国首次在月壤样品中发现了天然石墨烯,石墨烯具有导电性
C.汽车排气管加装“催化转化器”可减少尾气中有害气体的排放
D.使用稀土催化剂活化CO 形成聚碳酸酯能有效缓解温室效应
2
3.下列化学用语书写错误的是
A.聚乙炔的结构简式:
B.CH CH C(CH )=CH 的名称:2-甲基-1-丁烯
3 2 3 2
C.用电子式表示溴化钠的形成过程:
D.次磷酸(H PO )为一元酸,次磷酸根的结构式:
3 2
4.布洛芬具有抗炎、镇痛、解热作用,为避免口服该药对胃、肠道产生刺激,可以
对其进行成酯修饰。下列说法错误的是
A.成酯修饰后使得布洛芬水溶性减弱
B.布洛芬分子中有 9种化学环境不同的氢原子
C.1mol 布洛芬最多消耗3molH
2
D.该修饰过程中原子利用率小于100%
湖北云学名校联盟高三年级12月联考化学试卷 第 1 页 共 8 页5.下列化学反应表示错误的是
A.镁条在CO 中燃烧:2Mg+CO 2MgO+C
2 2
B.胆矾溶液向地壳深层浸透时遇到方铅矿:Cu2++SO2+PbS CuS+PbSO
4 4
C.NaHCO 溶液中通入少量Cl :2HCO+Cl 2CO +Cl+ClO+H O
3 2 3 2 2 2
D.少量Ba(OH) 溶液和KHSO 反应:Ba2++2OH+2HSO BaSO ↓+SO2+2H O
2 3 3 3 3 2
6.下列装置能达到相应目的的是
A.制取明矾晶体 B.验证析氢腐蚀 C.观察气体扩散 D.测定反应速率
7.某物质可用于检测污水中是否含 Ni2+,该物质的结构简式如图所示,X、Y、Z、
W为原子序数依次增大的前两周期元素。下列说法错误的是
A.最简单氢化物的稳定性:W>Z
B.元素电负性由大到小的顺序:W>Z>Y>X
C.基态W原子的核外电子的空间运动状态有5种
D.该物质中只有W 原子可以与金属离子形成配位键
8.在给定条件下,下列制备过程涉及的物质转化均可实现的是
电解 点燃
A.HCl 制备:NaCl 溶液 H 和Cl HCl
2 2
盐酸 电解
B.金属Mg 制备:Mg(OH��)�2� MgC�l 2� 溶 �� 液 Mg
C.纯碱工业:NaCl 溶液 NaHCO Na CO
���� 3 2 �3���
CO2 ∆
水
D.硫酸工业:FeS 2 SO�2��H 2 SO 4 �
9.下列有关物质的性质及O2对应解释均正确是
�� ��
性质 解释原因
中心原子电负性Cl>Br>I,使氧氢键
A. 酸性:HClO >HBrO >HIO
3 3 3 的极性减弱,则对应酸的酸性增强
O 是极性分子,水是极性溶剂而CCl
B. O 在CCl 中的溶解度比在水中小 3 4
3 4 是非极性溶剂
顺丁橡胶链节中的碳碳双键可打开与
C. 顺丁橡胶可以硫化处理来改善性能
S原子形成二硫键
D. 碳酸氢钠在水中的溶解度比碳酸钠小 碳酸氢根不与水分子形成氢键
湖北云学名校联盟高三年级12月联考化学试卷 第 2 页 共 8 页10.C 在材料学、医学等领域用途广泛。世界上第一辆单分子“纳米小车”的四个轮
60
子是C ,其运行情况如右图所示。下列说法错误
60
的是
A.C 是由非极性键构成的非极性分子
60
B.轴中碳原子通过键与C 相连,能绕键轴旋转
60
C.纳米小车可作运输载体,将药物送到病变部位
D.纳米小车通过共价键与药物分子形成超分子
11.根据下列实验操作和现象,所得到的结论正确的是
选项 实验操作和现象 结论
向氯水中加入一定量铁粉,充分振荡后滴加
A. 该氯水为久置氯水
几滴KSCN溶液,溶液呈浅绿色
将浓硫酸和灼热木炭反应产生的气体依次通
浓硫酸和木炭反应产生
B. 过品红溶液、饱和NaHCO 溶液、澄清石灰
3 SO 和CO 气体
水,发现品红溶液褪色,澄清石灰水变浑浊 2 2
向少量 FeS 悬浊液中加入足量饱和MnCl 溶
C. 2 K (FeS)>K (MnS)
液,沉淀颜色变为浅红色(MnS) sp sp
向0.1 mol/L 的NaHA 溶液中滴加酚酞溶液,
D. K >K (H A)·K (H A)
溶液变为浅红色 w a1 2 a2 2
12.中氢气体有限公司通过电解水制高纯氢,工作原理
如图所示。通过控制开关连接K 或K ,可交替得
1 2
到H 和O 。下列说法正确的是
2 2
A.Ni 位于元素周期表的ds 区
B.连接K ,电极1附近产生O
1 2
C.连接K ,产生H 的电极方程式是
2 2
2H O+2e H ↑+2OH-
2 2
D.电极3制氢气时消耗电极1产生的OH-,制氧气
时补充电极2消耗的OH-
13.将Ta O 和KHF 按一定的比例混合
2 5 2
能在一定条件下获得晶体P,P的晶
胞结构如图所示,晶胞参数a=b≠c nm
α=β=γ=90。,晶胞中Ta-O键键长为x
nm。已知晶胞化学式对应的相对分子
质量为M,下列说法错误的是
湖北云学名校联盟高三年级12月联考化学试卷 第 3 页 共 8 页A.晶体P 在熔融状态下能导电,推知其是离子晶体
B.晶体P的密度为 g/cm3
−21
2 ×10
C.R 点氧原子的分数 坐 标2 为( , , )
1 1 c−2x
D.制备晶体 P 的化学方程式:
2 2 2c
14.血红蛋白能准确、快速地吸收和释放氧气,保证生命活动的正常进行,同时血红
蛋白也能与CO等结合。根据图示下列说法正确的是
A.碳原子比氧原子的半径大,故CO是
以C 原子与血红蛋白中的 Fe 结合
B.蛋白质中的血红素比自由的血红素更
容易与CO结合从而导致CO中毒
C. 在血红蛋白中,O 分子仅有一个O
2
原子与Fe 相连,形成的Fe-O-O 键角
大约为120°
D. 在血红蛋白中,O 中未键合的O 以配位键与组氨酸相连,使血红蛋白能快速
2
的释放O
2
15.常温下,起始浓度均为 0.1mol/L的CH COOH和C H COOH(后者酸性略强)
3 6 5
的两种溶液中,两种酸(简写为HM)与两种酸根离子(简写为M-)的分布系数
c
CH
COO
δ与pH的变化关系如图所示。已知[ CH COO 3 ],lg2=0.3。
3 cCH COOHc CH COO
3 3
下列叙述正确的是
A.a、c点所在曲线表示 CH COOH ~pH的变化关系
3
B.b点时,两溶液中 =1.85
−
CH3COO
C.常温下,若将这两种溶液等− 体积混合,则C H COOH 的电离度增大
C6H5COO 6 5
D.若要将d点溶液pH调至4,则溶液不可能存在:c(H+)-c(OH)=c(M)
湖北云学名校联盟高三年级12月联考化学试卷 第 4 页 共 8 页二、非选择题:本题共4小题,共55分。
16.(13分)
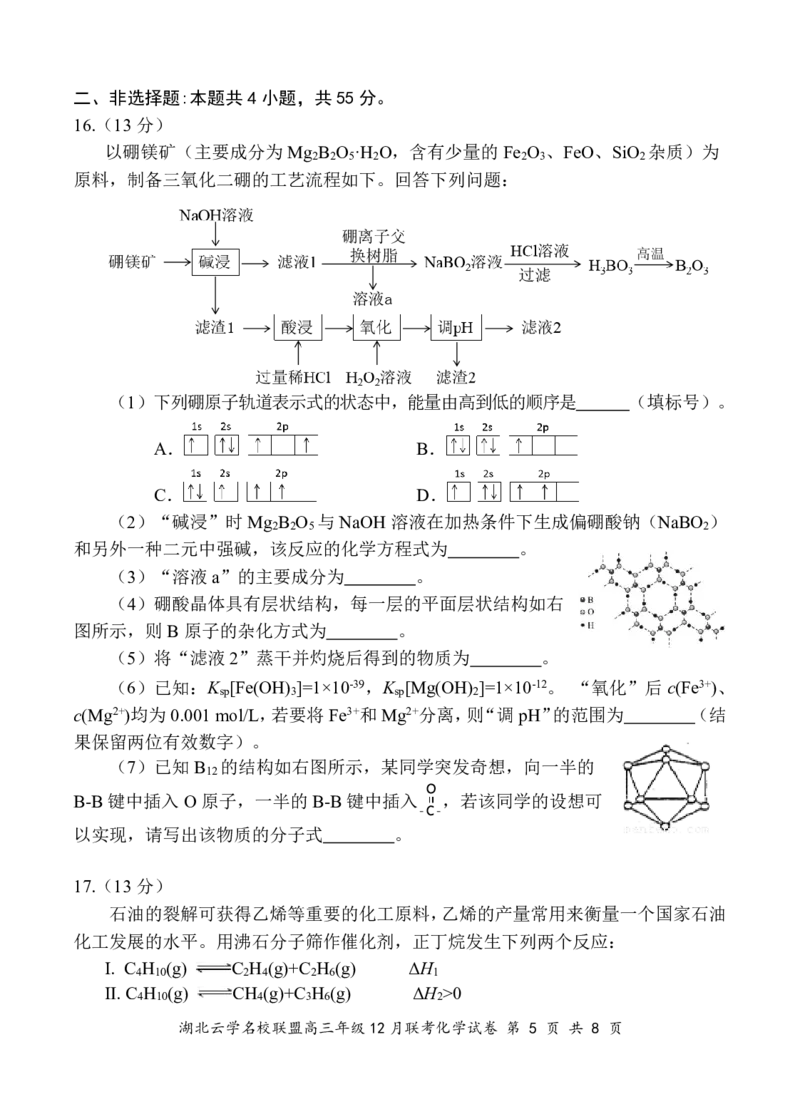
以硼镁矿(主要成分为Mg B O ·H O,含有少量的Fe O 、FeO、SiO 杂质)为
2 2 5 2 2 3 2
原料,制备三氧化二硼的工艺流程如下。回答下列问题:
(1)下列硼原子轨道表示式的状态中,能量由高到低的顺序是 (填标号)。
A. B.
C. D.
(2)“碱浸”时Mg B O 与NaOH 溶液在加热条件下生成偏硼酸钠(NaBO )
2 2 5 2
和另外一种二元中强碱,该反应的化学方程式为 。
(3)“溶液a”的主要成分为 。
(4)硼酸晶体具有层状结构,每一层的平面层状结构如右
图所示,则 B 原子的杂化方式为 。
(5)将“滤液2”蒸干并灼烧后得到的物质为 。
(6)已知:K [Fe(OH) ]=1×10-39,K [Mg(OH) ]=1×10-12。 “氧化”后c(Fe3+)、
sp 3 sp 2
c(Mg2+)均为0.001mol/L,若要将Fe3+和Mg2+分离,则“调pH”的范围为 (结
果保留两位有效数字)。
(7)已知B 的结构如右图所示,某同学突发奇想,向一半的
12
B-B 键中插入O原子,一半的B-B 键中插入 ,若该同学的设想可
以实现,请写出该物质的分子式 。
17.(13分)
石油的裂解可获得乙烯等重要的化工原料,乙烯的产量常用来衡量一个国家石油
化工发展的水平。用沸石分子筛作催化剂,正丁烷发生下列两个反应:
Ⅰ. C H (g) C H (g)+C H (g) ΔH
4 10 2 4 2 6 1
Ⅱ.C H (g) CH (g)+C H (g) ΔH >0
4 10 4 3 6 2
湖北云学名校联盟高三年级12月联考化学试卷 第 5 页 共 8 页回答下列问题:
(1)已知:
化学键 C-H C-C C=C
键能 /kJmol1 413 348 615
则ΔH = kJ/mol
1
(2)煤的综合利用也能获得多种化工原料,其主要途径有 (填一种)。
(3)在恒温恒容容器中,同时发生反应Ⅰ和Ⅱ,不能判断反应Ⅰ达到平衡状态的
是 。
A.混合气体的密度不再变化 B.混合气体的平均摩尔质量不再变化
C.容器中甲烷的浓度不再变化 D.甲烷消耗速率等于乙烯的生成速率
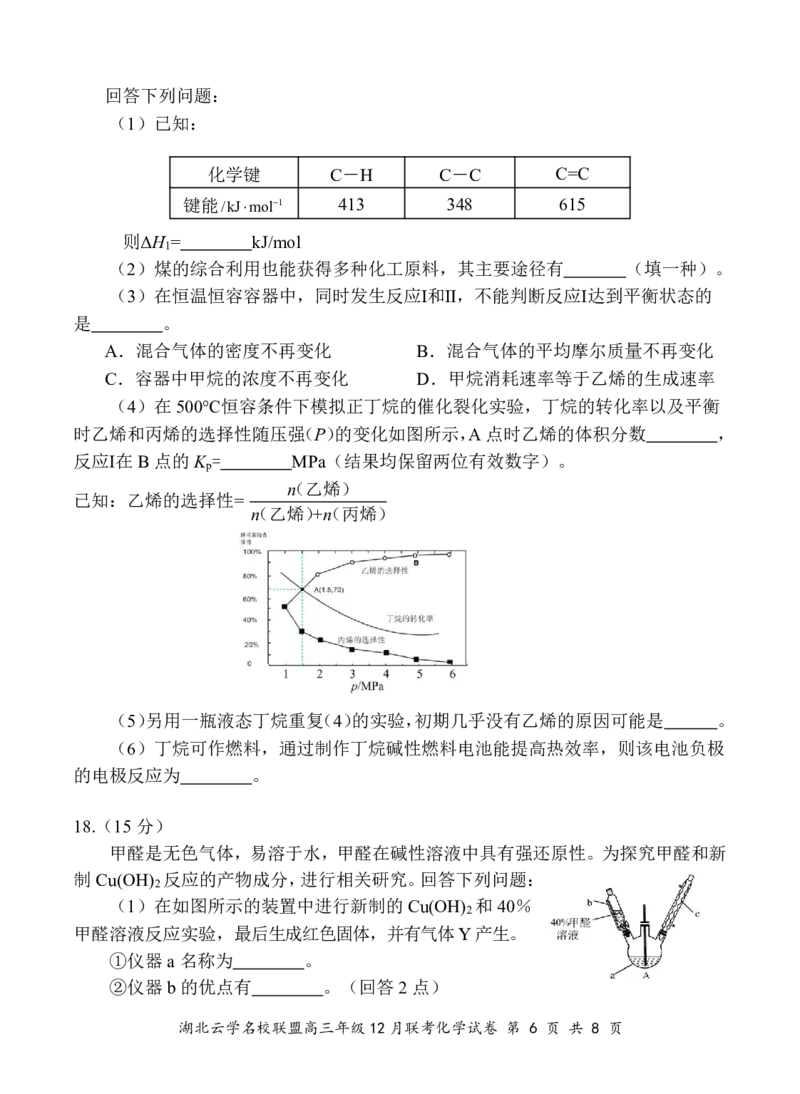
(4)在500℃恒容条件下模拟正丁烷的催化裂化实验,丁烷的转化率以及平衡
时乙烯和丙烯的选择性随压强(P)的变化如图所示,A 点时乙烯的体积分数 ,
反应Ⅰ在B 点的K = MPa(结果均保留两位有效数字)。
p
(n 乙烯)
已知:乙烯的选择性=
(n 乙烯)+n(丙烯)
(5)另用一瓶液态丁烷重复(4)的实验,初期几乎没有乙烯的原因可能是 。
(6)丁烷可作燃料,通过制作丁烷碱性燃料电池能提高热效率,则该电池负极
的电极反应为 。
18.(15分)
甲醛是无色气体,易溶于水,甲醛在碱性溶液中具有强还原性。为探究甲醛和新
制 Cu(OH) 反应的产物成分,进行相关研究。回答下列问题:
2
(1)在如图所示的装置中进行新制的Cu(OH) 和40%
2
甲醛溶液反应实验,最后生成红色固体,并有气体Y产生。
①仪器a名称为 。
②仪器b的优点有 。(回答2点)
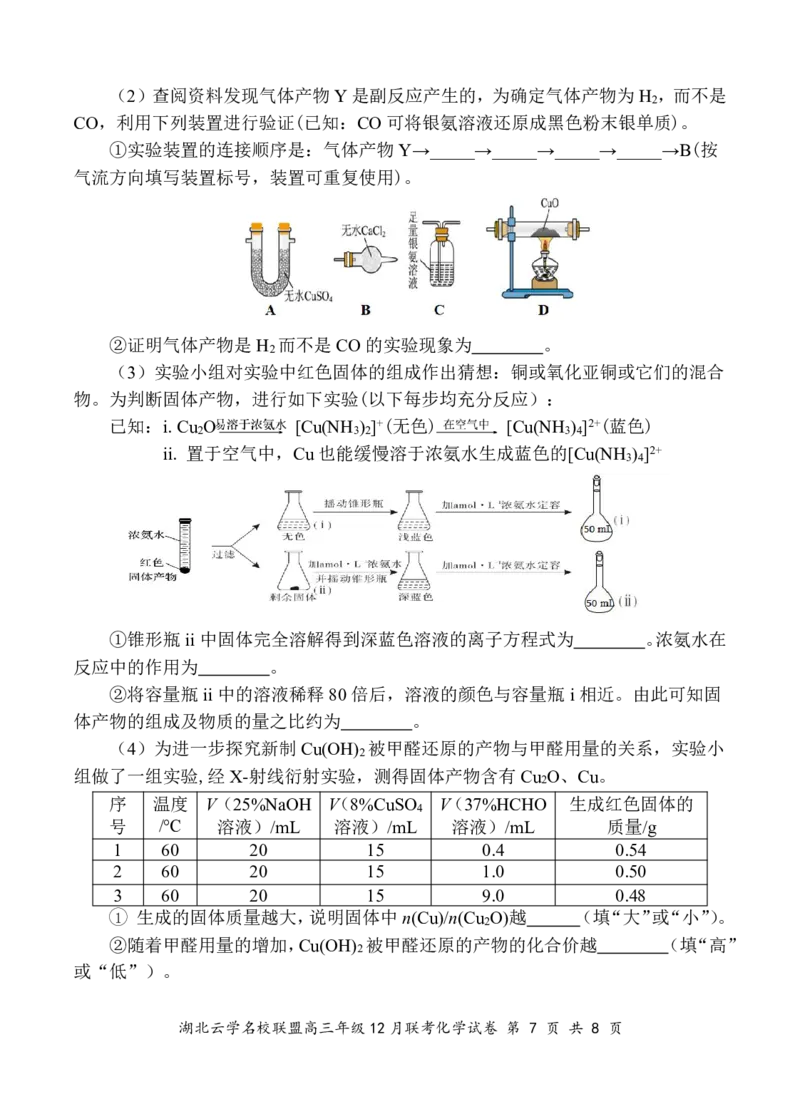
湖北云学名校联盟高三年级12月联考化学试卷 第 6 页 共 8 页(2)查阅资料发现气体产物Y是副反应产生的,为确定气体产物为H ,而不是
2
CO,利用下列装置进行验证(已知:CO可将银氨溶液还原成黑色粉末银单质)。
①实验装置的连接顺序是:气体产物Y→_____→_____→_____→_____→B(按
气流方向填写装置标号,装置可重复使用)。
②证明气体产物是H 而不是CO的实验现象为 。
2
(3)实验小组对实验中红色固体的组成作出猜想:铜或氧化亚铜或它们的混合
物。为判断固体产物,进行如下实验(以下每步均充分反应):
已知:i. Cu O [Cu(NH ) ]+(无色) [Cu(NH ) ]2+(蓝色)
2 3 2 3 4
ii. 置于空气中,Cu也能缓慢溶于浓氨水生成蓝色的[Cu(NH ) ]2+
3 4
①锥形瓶ii 中固体完全溶解得到深蓝色溶液的离子方程式为 。浓氨水在
反应中的作用为 。
②将容量瓶ii 中的溶液稀释80倍后,溶液的颜色与容量瓶i 相近。由此可知固
体产物的组成及物质的量之比约为 。
(4)为进一步探究新制Cu(OH) 被甲醛还原的产物与甲醛用量的关系,实验小
2
组做了一组实验,经X-射线衍射实验,测得固体产物含有Cu O、Cu。
2
序 温度 V(25%NaOH V(8%CuSO V(37%HCHO 生成红色固体的
4
号 /℃ 溶液)/mL 溶液)/mL 溶液)/mL 质量/g
1 60 20 15 0.4 0.54
2 60 20 15 1.0 0.50
3 60 20 15 9.0 0.48
1 生成的固体质量越大,说明固体中n(Cu)/n(Cu O)越 (填“大”或“小”)。
2
②随着甲醛用量的增加,Cu(OH) 被甲醛还原的产物的化合价越 (填“高”
2
或“低”)。
湖北云学名校联盟高三年级12月联考化学试卷 第 7 页 共 8 页19.(14分)
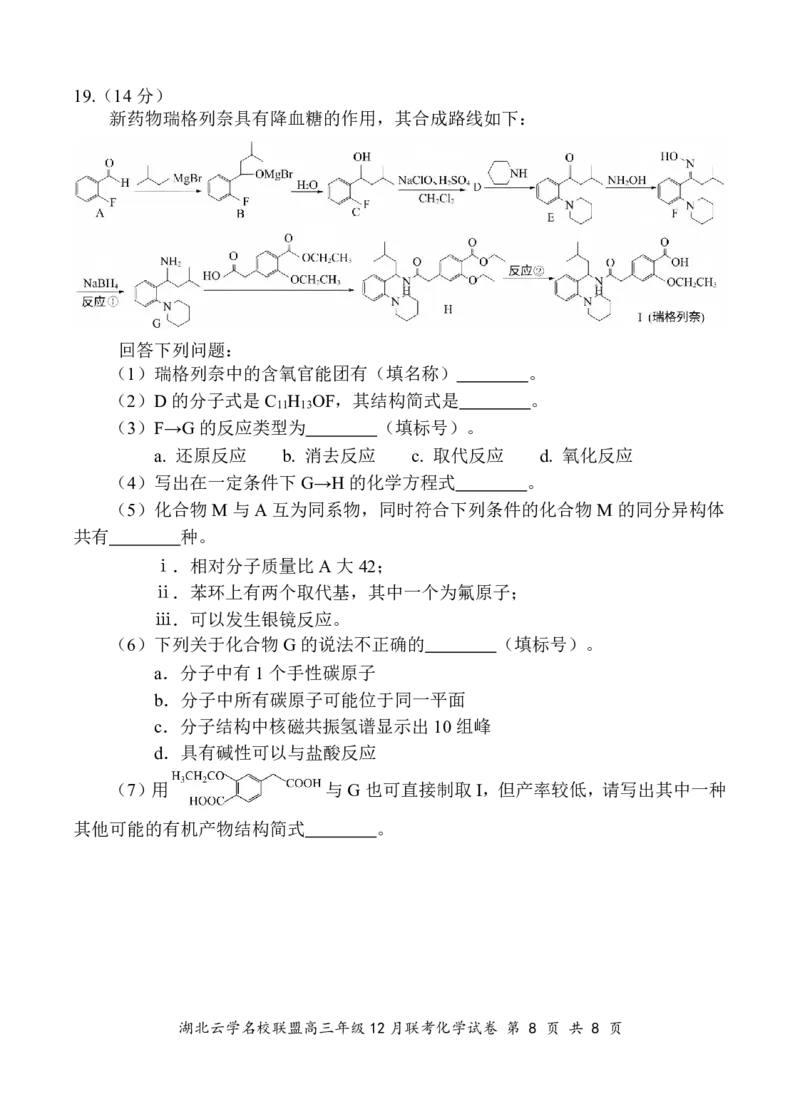
新药物瑞格列奈具有降血糖的作用,其合成路线如下:
回答下列问题:
(1)瑞格列奈中的含氧官能团有(填名称) 。
(2)D的分子式是C H OF,其结构简式是 。
11 13
(3)F→G的反应类型为 (填标号)。
a. 还原反应 b. 消去反应 c. 取代反应 d. 氧化反应
(4)写出在一定条件下G→H的化学方程式 。
(5)化合物M 与A互为同系物,同时符合下列条件的化合物M 的同分异构体
共有 种。
ⅰ.相对分子质量比A大42;
ⅱ.苯环上有两个取代基,其中一个为氟原子;
ⅲ.可以发生银镜反应。
(6)下列关于化合物G的说法不正确的 (填标号)。
a.分子中有1个手性碳原子
b.分子中所有碳原子可能位于同一平面
c.分子结构中核磁共振氢谱显示出10组峰
d.具有碱性可以与盐酸反应
(7)用 与G 也可直接制取I,但产率较低,请写出其中一种
其他可能的有机产物结构简式 。
湖北云学名校联盟高三年级12月联考化学试卷 第 8 页 共 8 页