文档内容
2025~2026 学年度上期高 2027届半期考试
化学试卷
(考试时间:75分钟;满分:100分)
可能用到的相对原子质量: H-1 C-12 O-16 Cl-35.5 Fe-56
第Ⅰ卷 选择题(共 45分)
一、选择题(本题共15个小题,每小题3分,共45分,每小题只有一个选项符合题意)
1.下列事实不
.
能
.
用勒夏特列原理解释的是
A.打开可乐瓶盖立刻产生大量泡沫
B.氯水中加入CaCO 粉末可以提高氯水中HClO的浓度
3
C.常温下将注射器中的NO 气体压缩后颜色变深
2
D.配制FeCl 溶液时将FeCl 晶体溶于较浓的盐酸中,再加水稀释到所需浓度
3 3
2.下列滴定反应中,指示剂使用错误的是
A.用FeCl 标准溶液滴定KI溶液,选择KSCN溶液作指示剂
3
B.用NaOH标准溶液滴定醋酸溶液,选择酚酞作指示剂
C.用酸性KMnO 标准溶液滴定H C O 溶液,不需要另加指示剂
4 2 2 4
D.用H O 标准溶液滴定KI溶液,选择淀粉溶液作指示剂
2 2
3.已知如下热化学方程式:
①NH (g)+HClO (l)=NH ClO (s) ΔH =-akJ·mol-1; ②N (g)+3H (g) 2NH (g) ΔH =-bkJ·mol-1
3 4 4 4 1 2 2 3 2
③4HClO (l)=2Cl (g)+7O (g)+2H O(g) ΔH =+ckJ·mol-1;④2H (g)+O (g)=2H O(g) ΔH =-dkJ·mol-1
4 2 2 2 3 2 2 2 4
高氯酸铵是发射火箭的固体能源,发生如下反应:
2NH ClO (s)=N (g)+Cl (g)+2O (g)+4H O(g) ΔH,ΔH可表示为
4 4 2 2 2 2
(4a2bc3d)
A.
kJmol1
B.
(4a2bc3d)kJmol1
2
(4a2bc3d) (4a2bc3d)
C.
kJmol1
D.
kJmol1
2 2
4.对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
选项 粒子组 判断和分析
A K+、Fe3+、Al3+、Cl-、SO 2- 常温下能大量共存,且溶液pH=7
4
不能大量共存,因Al(OH) -和HCO -之间会发生反应生
B Na+、K+、Al(OH) -、HCO - 4 3
4 3 成Al(OH) 沉淀和CO 气体
3 2
C Na+、Fe3+、SO 2-、H O 能大量共存,粒子间不反应
4 2 2
不能大量共存,因发生反应:
D K+、H+、MnO -、SO 2-、H C O
4 4 2 2 4 2MnO -+5H C O +6H+=2Mn2++10CO ↑+8H O
4 2 2 4 2 2
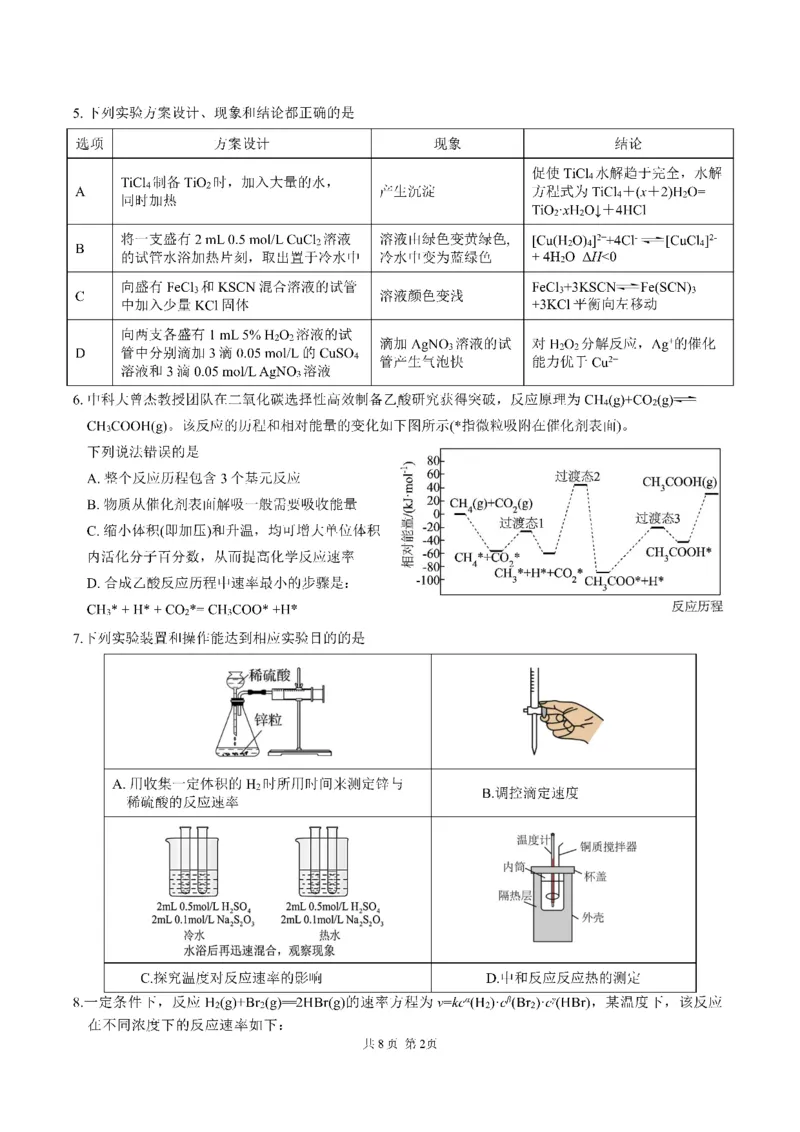
共8页 第1页c(H )/(mol·L-1) c(Br )/(mol·L-1) c(HBr)/(mol·L-1) 反应速率
2 2
0.1 0.1 2 v
0.1 0.4 2 8v
0.2 0.4 2 16v
0.4 0.1 4 2v
0.2 0.1 c 4v
根据表中的测定结果,下列结论错误的是
A.表中c的值为1 B.α、β、γ的值分别为1、2、-1
C.反应体系的三种物质中,Br (g)的浓度对反应速率影响最大
2
D.在反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率降低
9.下图是工业合成氨的流程图,下列说法错误的是
A.步骤①中“净化”可以防止催化剂中毒
B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C.步骤③、④、⑤均有利于提高原料的平衡转化率
D.为保持足够高的原料转化率,在反应达到一定时间时将氨从混合气中分离出去
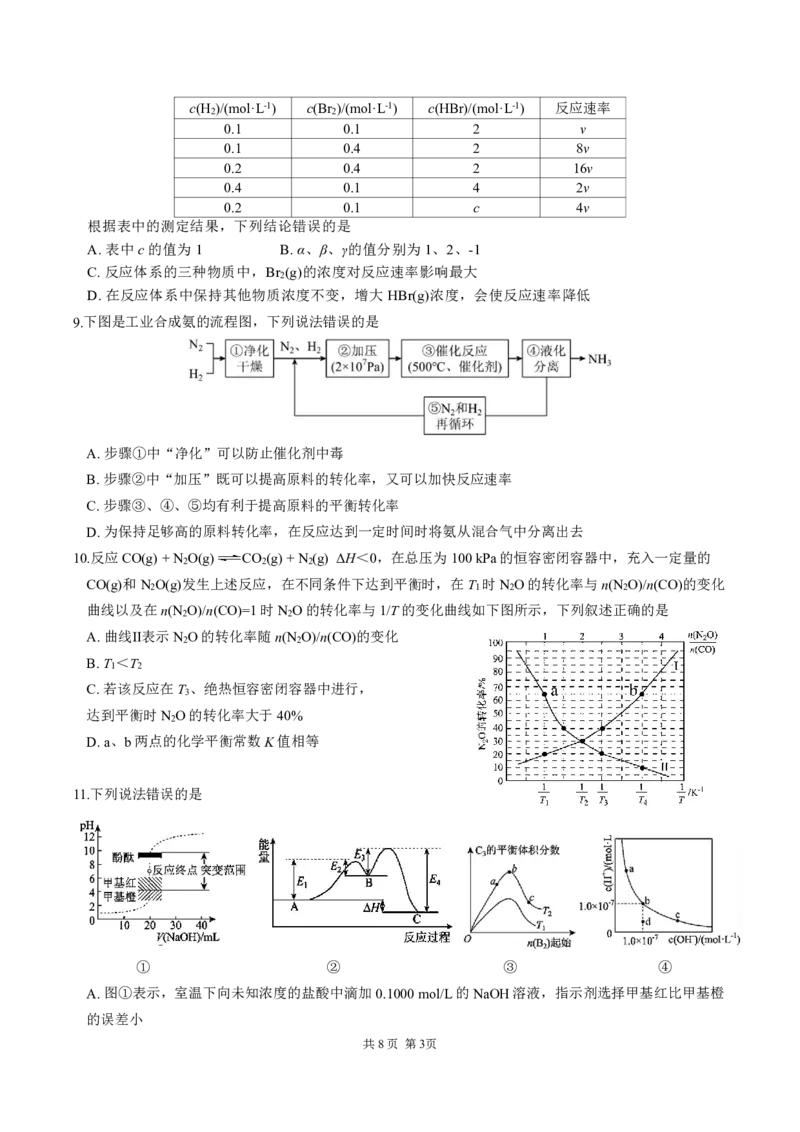
10.反应CO(g)+N O(g) CO (g)+N (g) ΔH<0,在总压为100kPa的恒容密闭容器中,充入一定量的
2 2 2
CO(g)和N O(g)发生上述反应,在不同条件下达到平衡时,在T 时N O的转化率与n(N O)/n(CO)的变化
2 1 2 2
曲线以及在n(N O)/n(CO)=1时N O的转化率与1/T的变化曲线如下图所示,下列叙述正确的是
2 2
A.曲线Ⅱ表示N O的转化率随n(N O)/n(CO)的变化
2 2
B.T <T
1 2
C.若该反应在T 、绝热恒容密闭容器中进行,
3
达到平衡时N O的转化率大于40%
2
D.a、b两点的化学平衡常数K值相等
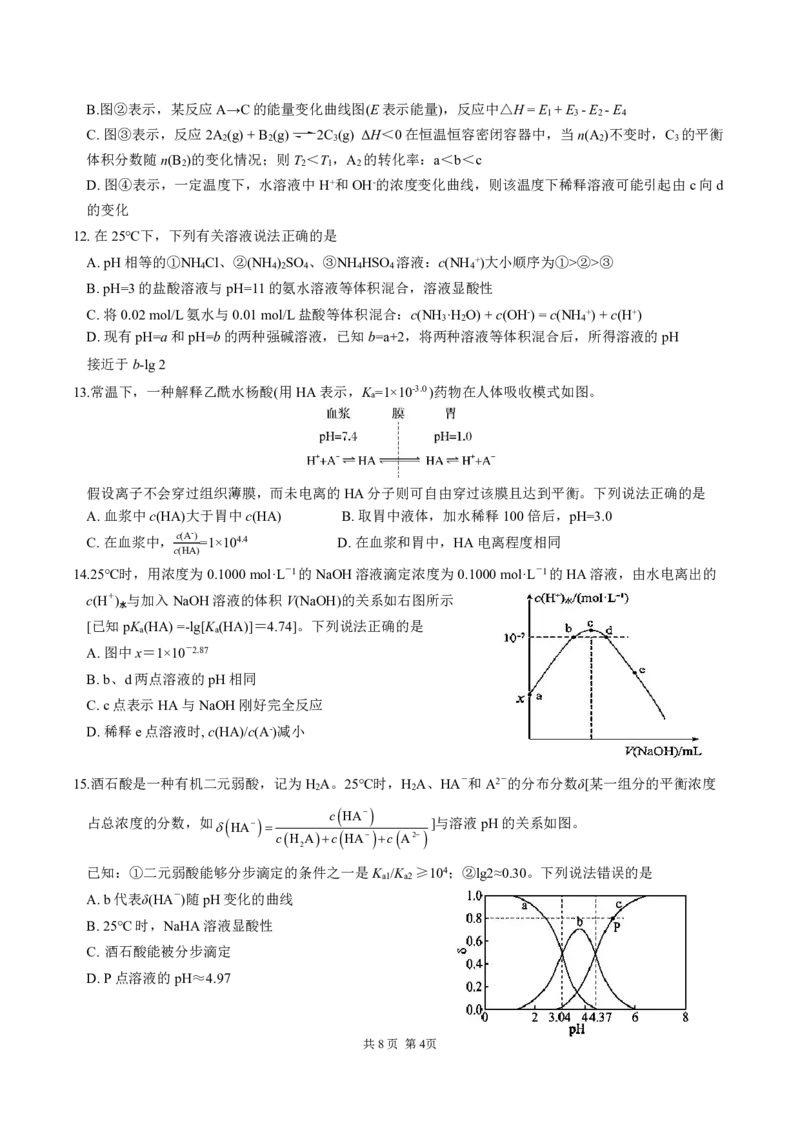
11.下列说法错误的是
① ② ③ ④
A.图①表示,室温下向未知浓度的盐酸中滴加0.1000mol/L的NaOH溶液,指示剂选择甲基红比甲基橙
的误差小
共8页 第3页B.图②表示,某反应A→C的能量变化曲线图(E表示能量),反应中△H=E +E -E -E
1 3 2 4
C.图③表示,反应2A (g)+B (g) 2C (g) ΔH<0在恒温恒容密闭容器中,当n(A )不变时,C 的平衡
2 2 3 2 3
体积分数随n(B )的变化情况;则T <T ,A 的转化率:a<b<c
2 2 1 2
D.图④表示,一定温度下,水溶液中H+和OH-的浓度变化曲线,则该温度下稀释溶液可能引起由c向d
的变化
12.在25℃下,下列有关溶液说法正确的是
A.pH相等的①NH Cl、②(NH ) SO 、③NH HSO 溶液:c(NH +)大小顺序为①>②>③
4 4 2 4 4 4 4
B.pH=3的盐酸溶液与pH=11的氨水溶液等体积混合,溶液显酸性
C.将0.02mol/L氨水与0.01mol/L盐酸等体积混合:c(NH ·H O)+c(OH-)=c(NH +)+c(H+)
3 2 4
D.现有pH=a和pH=b的两种强碱溶液,已知b=a+2,将两种溶液等体积混合后,所得溶液的pH
接近于b-lg2
13.常温下,一种解释乙酰水杨酸(用HA表示,K =1×10-3.0)药物在人体吸收模式如图。
a
假设离子不会穿过组织薄膜,而未电离的HA分子则可自由穿过该膜且达到平衡。下列说法正确的是
A.血浆中c(HA)大于胃中c(HA) B.取胃中液体,加水稀释100倍后,pH=3.0
C.在血浆中,c(A-)
=1×104.4 D.在血浆和胃中,HA电离程度相同
c(HA)
14.25℃时,用浓度为0.1000mol·L-1的NaOH溶液滴定浓度为0.1000mol·L-1的HA溶液,由水电离出的
c(H+) 与加入NaOH溶液的体积V(NaOH)的关系如右图所示
水
[已知pK (HA)=-lg[K (HA)]=4.74]。下列说法正确的是
a a
A.图中x=1×10-2.87
B.b、d两点溶液的pH相同
C.c点表示HA与NaOH刚好完全反应
D.稀释e点溶液时,c(HA)/c(A-)减小
15.酒石酸是一种有机二元弱酸,记为H A。25℃时,H A、HA-和A2-的分布分数δ[某一组分的平衡浓度
2 2
c
HA
占总浓度的分数,如
HA
]与溶液pH的关系如图。
cH Ac HA c A2
2
已知:①二元弱酸能够分步滴定的条件之一是K /K ≥104;②lg2≈0.30。下列说法错误的是
a1 a2
A.b代表δ(HA-)随pH变化的曲线
B.25℃时,NaHA溶液显酸性
C. 酒石酸能被分步滴定
D.P点溶液的pH≈4.97
共8页 第4页第Ⅱ卷 非选择题(共 55分)
二、填空题(本题共4道题,共55分)
16.(16分)
氯化铁是重要的化工原料,实验室用废铁屑(表面有油污)制取无水氯化铁并测其纯度。方案如下:
I.FeCl ·6H O制备
3 2
①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)控制温度在40~50℃之间的原因是 。
Ⅱ.无水FeCl 制备
3
已知:SOCl 沸点为77℃,易水解生成SO 和HCl。
2 2
(2)将FeCl ·6H O与液体SOCl 置于圆底烧瓶中混合并水浴加
3 2 2
热,制得无水FeCl 。装置如图所示(夹持和加热装置略)。圆底烧
3
瓶中生成无水FeCl 的总化学方程式为 ;
3
仪器A的作用是 。
Ⅲ.产品纯度测定
已知:I (aq)+I—(aq) I —(aq),I 和I —在水溶液中均为棕黄色。
2 3 2 3
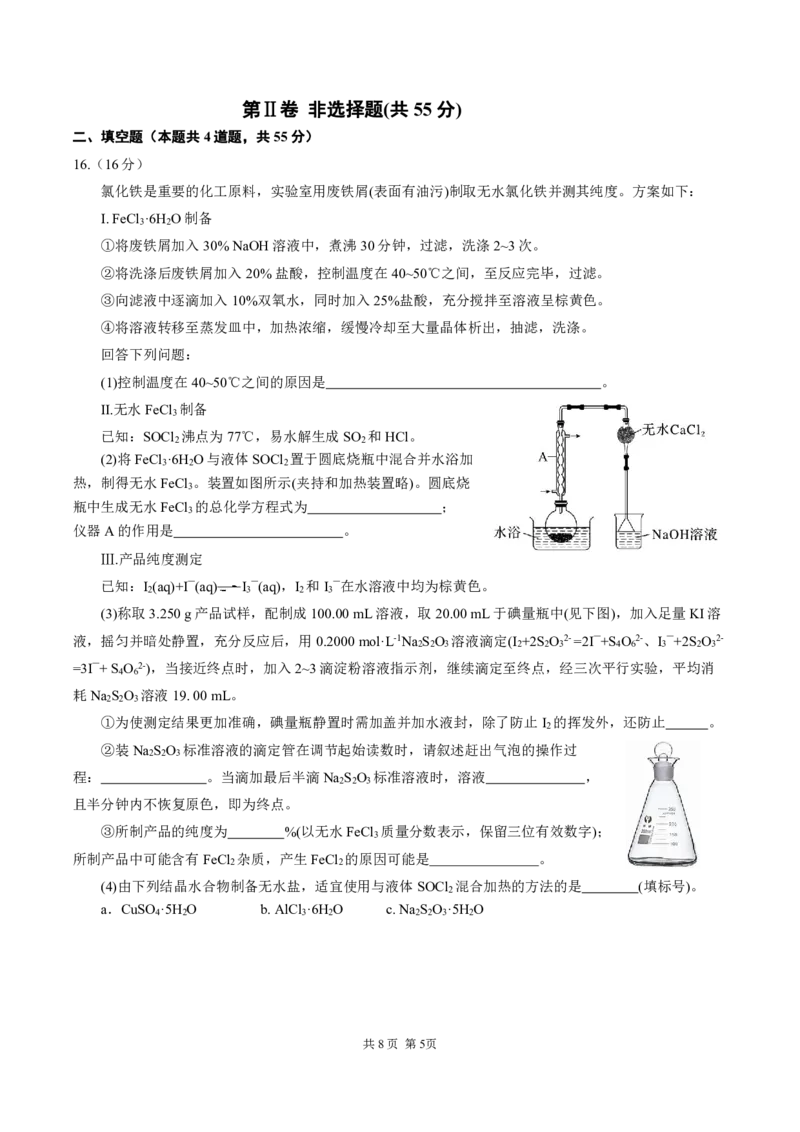
(3)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于碘量瓶中(见下图),加入足量KI溶
液,摇匀并暗处静置,充分反应后,用0.2000mol·L-1Na S O 溶液滴定(I +2S O 2-=2I—+S O 2-、I —+2S O 2-
2 2 3 2 2 3 4 6 3 2 3
=3I—+S O 2-),当接近终点时,加入2~3滴淀粉溶液指示剂,继续滴定至终点,经三次平行实验,平均消
4 6
耗Na S O 溶液19.00mL。
2 2 3
①为使测定结果更加准确,碘量瓶静置时需加盖并加水液封,除了防止I 的挥发外,还防止 。
2
②装Na S O 标准溶液的滴定管在调节起始读数时,请叙述赶出气泡的操作过
2 2 3
程: 。当滴加最后半滴Na S O 标准溶液时,溶液 ,
2 2 3
且半分钟内不恢复原色,即为终点。
③所制产品的纯度为 %(以无水FeCl 质量分数表示,保留三位有效数字);
3
所制产品中可能含有FeCl 杂质,产生FeCl 的原因可能是 。
2 2
(4)由下列结晶水合物制备无水盐,适宜使用与液体SOCl 混合加热的方法的是 (填标号)。
2
a.CuSO ·5H O b.AlCl ·6H O c.Na S O ·5H O
4 2 3 2 2 2 3 2
共8页 第5页17.(13分)
CO和H 称之为合成气,两种气体分别通过下列方法制备。回答下列问题。
2
Ⅰ.通过甲酸分解可获得超高纯度的CO。甲酸有两种可能的分解反应:
①HCOOH(g)=CO(g)+H O(g) ΔH =+26.3kJ·mol-1;②HCOOH(g)=CO (g)+H (g) ΔH =-14.9kJ·mol-1
2 1 2 2 2
(1)一定温度下,向恒容密闭容器中通入一定量的HCOOH(g),发生上述两个分解反应,下列说法中能
表明反应达到平衡状态的是 (填标号)。
a.气体密度不变 b.混合气体的平均相对分子质量不变 c.v (HCOOH)=v (CO)
正 逆
d.H O(g)的浓度不变 e.CO和CO 的物质的量相等
2 2
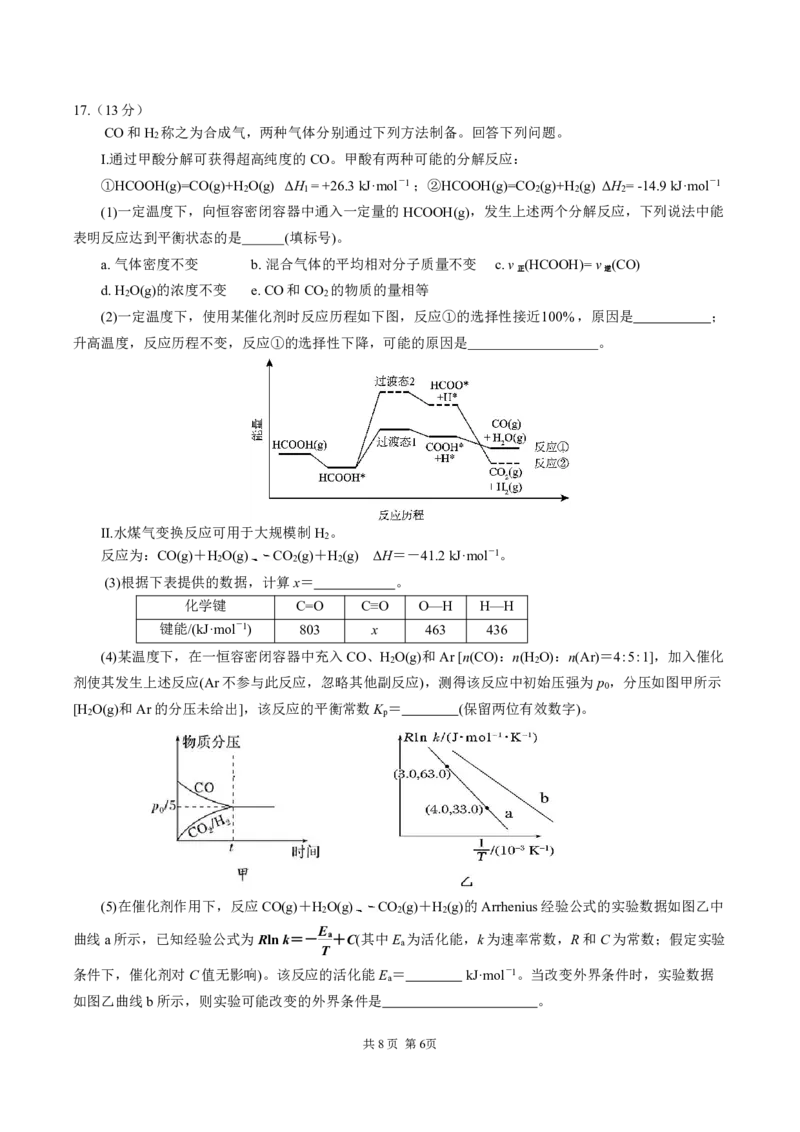
(2)一定温度下,使用某催化剂时反应历程如下图,反应①的选择性接近100%,原因是 ;
升高温度,反应历程不变,反应①的选择性下降,可能的原因是 。
Ⅱ.水煤气变换反应可用于大规模制H 。
2
反应为:CO(g)+H O(g) CO (g)+H (g) ΔH=-41.2kJ·mol-1。
2 2 2
(3)根据下表提供的数据,计算x= 。
化学键 C=O C≡O O—H H—H
键能/(kJ·mol-1) 803 x 463 436
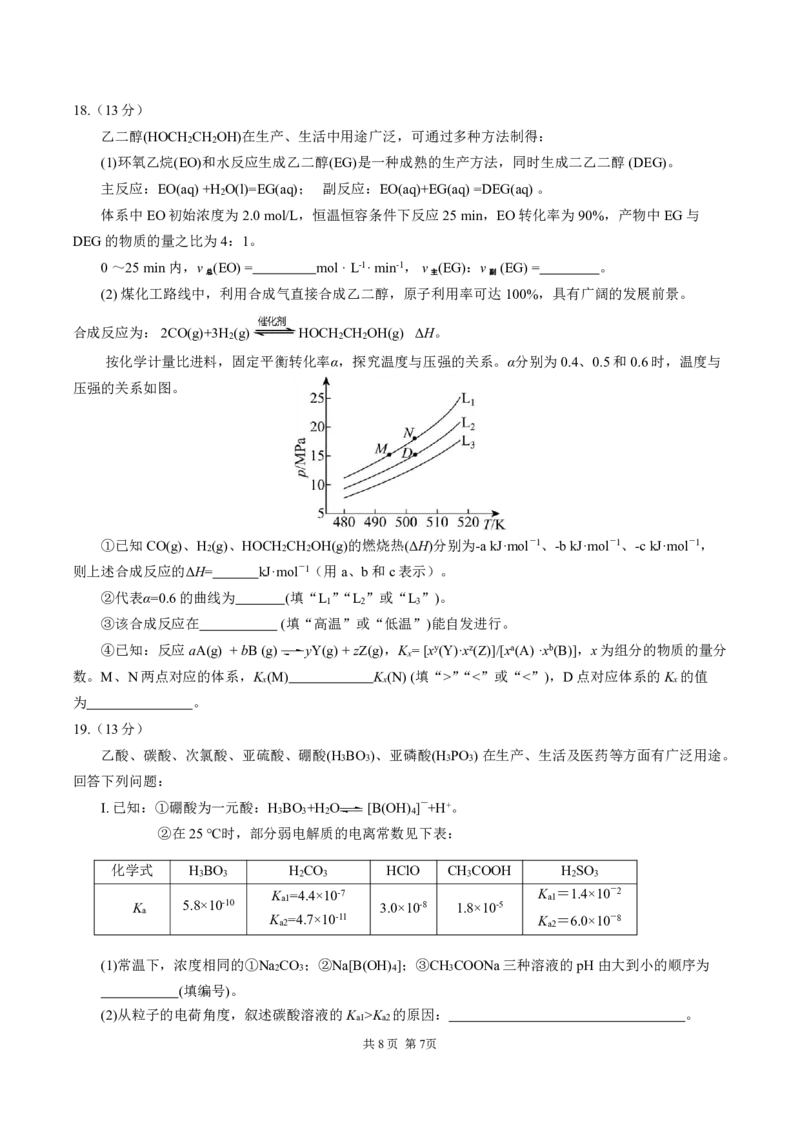
(4)某温度下,在一恒容密闭容器中充入CO、H O(g)和Ar[n(CO):n(H O):n(Ar)=4:5:1],加入催化
2 2
剂使其发生上述反应(Ar不参与此反应,忽略其他副反应),测得该反应中初始压强为p ,分压如图甲所示
0
[H O(g)和Ar的分压未给出],该反应的平衡常数K = (保留两位有效数字)。
2 p
(5)在催化剂作用下,反应CO(g)+H O(g) CO (g)+H (g)的Arrhenius经验公式的实验数据如图乙中
2 2 2
E
曲线a所示,已知经验公式为Rlnk=- a+C(其中E 为活化能,k为速率常数,R和C为常数;假定实验
a
T
条件下,催化剂对C值无影响)。该反应的活化能E= kJ·mol-1。当改变外界条件时,实验数据
a
如图乙曲线b所示,则实验可能改变的外界条件是 。
共8页 第6页18.(13分)
乙二醇(HOCH CH OH)在生产、生活中用途广泛,可通过多种方法制得:
2 2
(1)环氧乙烷(EO)和水反应生成乙二醇(EG)是一种成熟的生产方法,同时生成二乙二醇(DEG)。
主反应:EO(aq)+H O(l)=EG(aq); 副反应:EO(aq)+EG(aq)=DEG(aq)。
2
体系中EO初始浓度为2.0mol/L,恒温恒容条件下反应25min,EO转化率为90%,产物中EG与
DEG的物质的量之比为4:1。
0~25min内,v (EO)= mol·L-1·min-1,v (EG):v (EG)= 。
总 主 副
(2)煤化工路线中,利用合成气直接合成乙二醇,原子利用率可达100%,具有广阔的发展前景。
合成反应为:2CO(g)+3H (g) HOCH CH OH(g) ΔH。
2 2 2
按化学计量比进料,固定平衡转化率α,探究温度与压强的关系。α分别为0.4、0.5和0.6时,温度与
压强的关系如图。
①已知CO(g)、H (g)、HOCH CH OH(g)的燃烧热(ΔH)分别为-akJ·mol-1、-bkJ·mol-1、-ckJ·mol-1,
2 2 2
则上述合成反应的ΔH= kJ·mol-1(用a、b和c表示)。
②代表α=0.6的曲线为 (填“L ”“L ”或“L ”)。
1 2 3
③该合成反应在 (填“高温”或“低温”)能自发进行。
④已知:反应aA(g) +bB(g) yY(g)+zZ(g),K =[xy(Y)·xz(Z)]/[xa(A)·xb(B)],x为组分的物质的量分
x
数。M、N两点对应的体系,K (M) K (N)(填“>”“<”或“<”),D点对应体系的K 的值
x x x
为 。
19.(13分)
乙酸、碳酸、次氯酸、亚硫酸、硼酸(H BO )、亚磷酸(H PO )在生产、生活及医药等方面有广泛用途。
3 3 3 3
回答下列问题:
I.已知:①硼酸为一元酸:H BO +H O [B(OH) ]—+H+。
3 3 2 4
②在25℃时,部分弱电解质的电离常数见下表:
化学式 H BO H CO HClO CH COOH H SO
3 3 2 3 3 2 3
K a1 =4.4×10-7 K a1 =1.4×10-2
K 5.8×10-10 3.0×10-8 1.8×10-5
a
K a2 =4.7×10-11 K a2 =6.0×10-8
(1)常温下,浓度相同的①Na CO ;②Na[B(OH) ];③CH COONa三种溶液的pH由大到小的顺序为
2 3 4 3
(填编号)。
(2)从粒子的电荷角度,叙述碳酸溶液的K >K 的原因: 。
a1 a2
共8页 第7页(3)下列离子方程式中正确的是 。
a.少量CO 通入次氯酸钠溶液中:CO +H O+ClO-=HCO -+HClO
2 2 2 3
b.少量SO 通入次氯酸钙溶液中:Ca2++2ClO-+SO +H O=CaSO ↓+2HClO
2 2 2 3
c.少量的氯水滴加到碳酸氢钠溶液中:2HCO —+Cl =Cl—+ClO—+2CO ↑+H O
3 2 2 2
d.少量SO 通入碳酸钠溶液中:SO +CO 2-+H O=HCO -+HSO -
2 2 3 2 3 3
(4)常温下,向amol·L-1CH COONa溶液中滴加等体积的bmol·L-1盐酸使溶液呈中性(不考虑盐酸和醋
3
酸的挥发;溶液体积变化忽略不计),CH COOH的电离常数K = (用含a和b的代数式表示)。
3 a
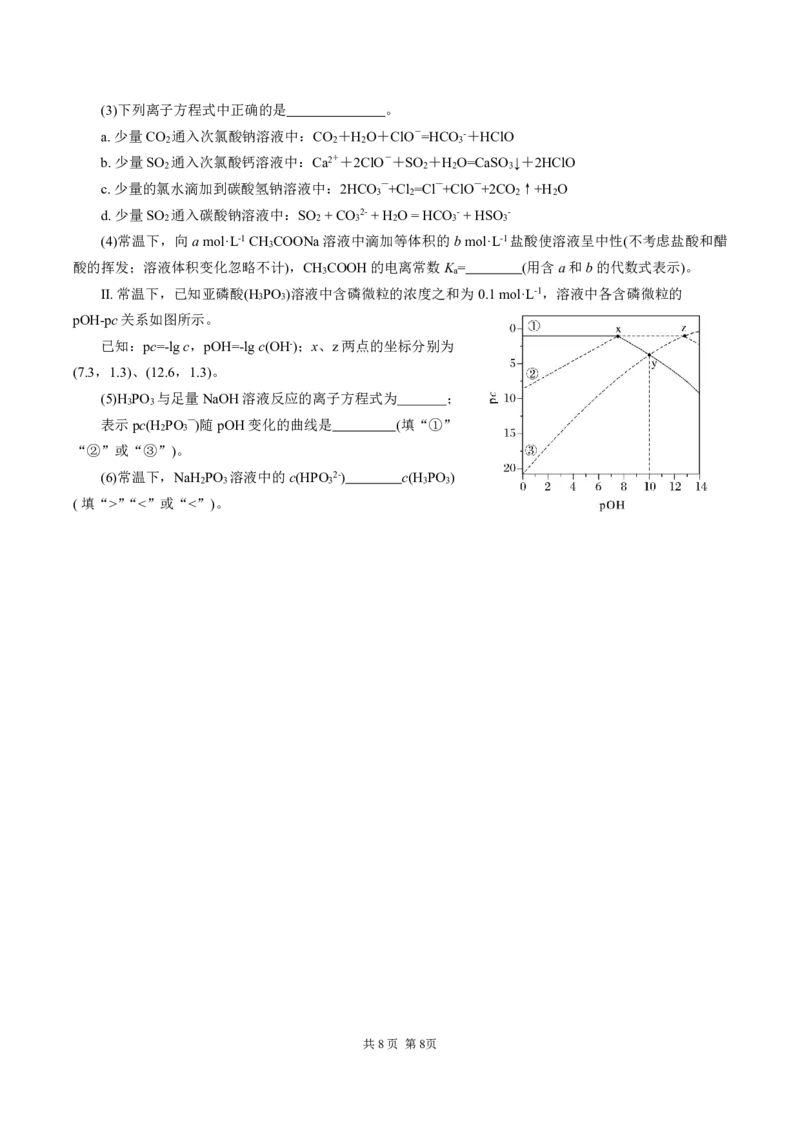
Ⅱ.常温下,已知亚磷酸(H PO )溶液中含磷微粒的浓度之和为0.1mol·L-1,溶液中各含磷微粒的
3 3
pOH-pc关系如图所示。
已知:pc=-lgc,pOH=-lgc(OH-);x、z两点的坐标分别为
(7.3,1.3)、(12.6,1.3)。
(5)H PO 与足量NaOH溶液反应的离子方程式为 ;
3 3
表示pc(H PO —)随pOH变化的曲线是 (填“①”
2 3
“②”或“③”)。
(6)常温下,NaH PO 溶液中的c(HPO 2-) c(H PO )
2 3 3 3 3
(填“>”“<”或“<”)。
共8页 第8页