文档内容
宁德市 2024-2025 学年第一学期期末高二质量检测
化 学 试 题
(考试时间:75 分钟 试卷总分:100 分)
注意:
1.本学科试卷分试题卷和答题卡两部分。试题卷分第Ⅰ卷(选择题)和第Ⅱ卷(非
选择题)(共 8 页 14 题),全部答案必须按要求填在答题卡的相应答题栏内,否
则不能得分。
2.相对原子质量:H 1 N 14 O 16 S 32 Fe 56 K 39 Cu 64
第 I 卷 选择题(共 40 分)
本题包括 10 小题,每小题 4 分,共 40 分。每小题只有一个选项符合题意。
1.下列叙述错误的是
A.生铁(铁碳合金)制作的铁锅不易生锈
B.医用药品常在低温、干燥的环境下密封保存
C.氢氧燃料电池放电时将化学能转化为电能
D.人体血液中 HCO-NaHCO 等体系起到稳定血液 pH 的作用
2 3 3
2.下列溶液中,一定呈中性的是
A.1g NHCl 溶于 100 mL 水所得到的溶液
4
B.c(H+)、c(OH-) 均为 2.0×10-7 mol·L-1 的溶液
C.等物质的量的强酸与强碱反应所得到的溶液
D.将 pH=5 的盐酸稀释 100 倍所得到的溶液
3.氢气和氧气的混合气体在催化剂存在的条件下,可以发生爆炸式反应生成液态水,主
要反应机理如下。下列说法错误的是
①H → 2H•
2
②H• + O → •OH + O•
2
③O• + H → •OH + H•
2
④•OH + H → H O + H•
2 2
A.O•为反应的中间体
B.H• + O → •OH + O•称为基元反应
2
C.自由基(•OH)的反应活性很强,寿命极短
D.使用催化剂能降低反应的活化能和焓变
高二化学试卷 第 8 页,共 8 页4.下列各组粒子在溶液中能大量共存的是
A.无色溶液:Na+ 、Al3+、Cl-、NH
3
·H
2
O
B.pH=0 的溶液:Fe2+、NH
4+
、NO
3
-、HCOOH
C.在透明溶液中:Na+ 、K+ 、MnO 4 -、NO 3-
D.常温下水电离的 c(H+)=1×10-12 mol·L-1 的溶液:K+ 、NH
4+
、SO
3
2-、Cl-
5.设 N 为阿伏加德罗常数的值,下列说法正确的是
A
A.1 L 1 mol·L-1 NaCO 溶液中,含 CO2-的数目为 N
2 3 3 A
B.锌表面镀铜时,阴极质量增重 32 g,则外电路转移的电子数为 N
A
C.常温下,pH = 2 的 H
2
SO
4
溶液中含有 H+ 的数目为 0.02N
A
D.2SO (g) + O(g) 2SO (g) ΔH=-a kJ·mol-1,若充入 SO 数目为 2N ,则放
2 2 3 2 A
出热量为 a kJ
6.在一定温度下,将气体 H 和气体 I 各 0.16mol 充入 10L 恒容密闭容器中,发生反应
2 2
H(g) + I (g) 2HI(g) ΔH < 0,一段时间后达到平衡。反应过程中测定的数据如下:
2 2
t/min 2 4 7 9
n(I)/mol 0.12 0.11 0.10 0.10
2
下列说法正确的是
A.前 4min 内反应的平均速率υ(HI) = 1.25×10-3mol·L-1·min-1
B.其他条件不变,增大 H 浓度,活化分子百分数增大,反应速率加快
2
C.充入少量 He 使体系压强增大,υ 、υ 均不变
正 逆
D.其他条件不变,增大压强,平衡常数增大
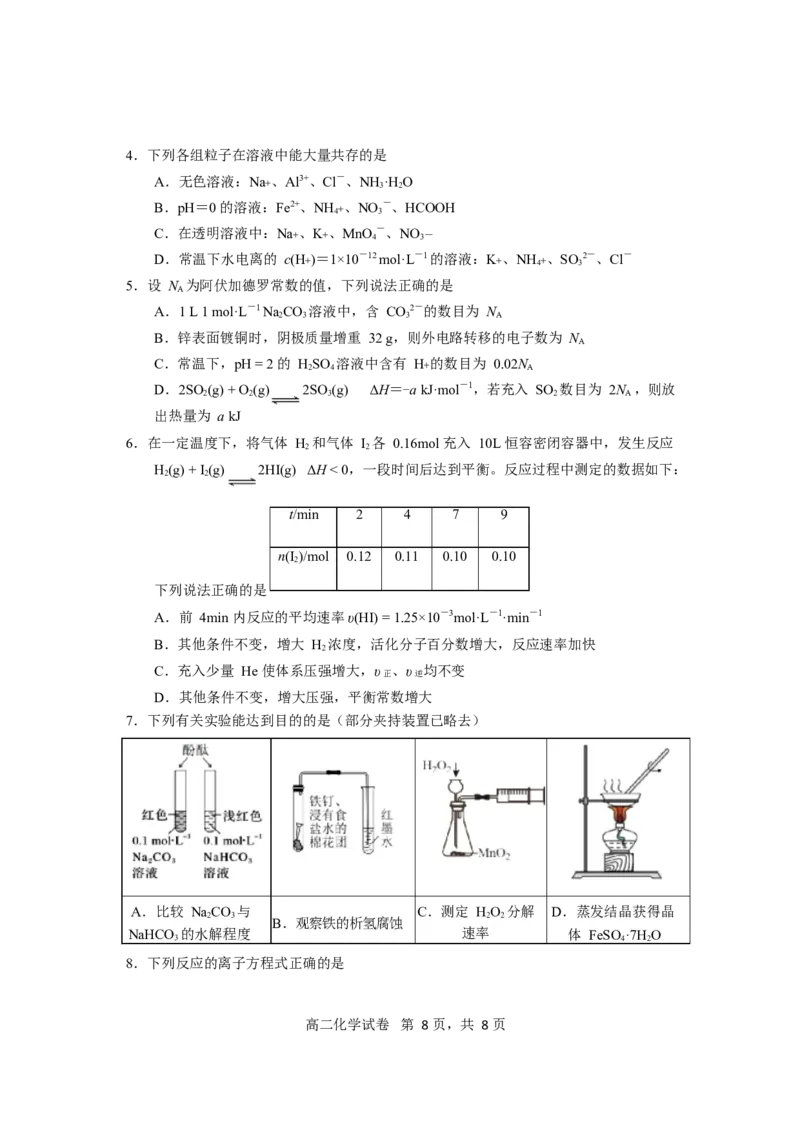
7.下列有关实验能达到目的的是(部分夹持装置已略去)
A.比较 NaCO 与 C.测定 HO 分解 D.蒸发结晶获得晶
2 3 2 2
B.观察铁的析氢腐蚀
NaHCO 的水解程度 速率 体 FeSO ·7H O
3 4 2
8.下列反应的离子方程式正确的是
高二化学试卷 第 8 页,共 8 页A.向 AgCl 悬浊液中滴加 NaI 溶液:I-(aq) + AgCl (s) AgI (s) + Cl-(aq)
B.同浓度同体积 NH 4 HSO 4 溶液与 NaOH 溶液混合: NH 4+ + OH-= NH 3 ·H 2 O
C.用惰性电极电解饱和 MgCl 溶液:2Cl-+ 2H O Cl↑ + H ↑ + 2OH-
2 2 2 2
D.铅蓄电池充电时的阳极反应:Pb2 + + 2H 2 O - 2e-= PbO 2 + 4H+
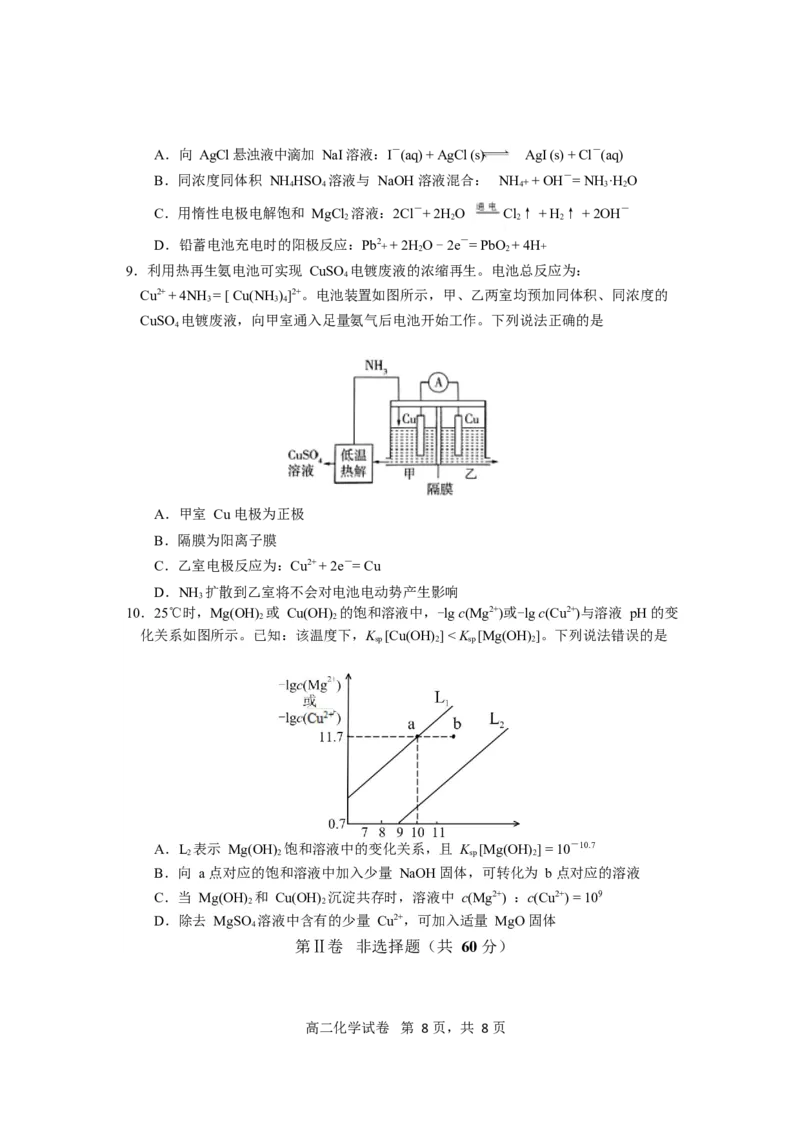
9.利用热再生氨电池可实现 CuSO 电镀废液的浓缩再生。电池总反应为:
4
Cu2+ + 4NH = [ Cu(NH )]2+。电池装置如图所示,甲、乙两室均预加同体积、同浓度的
3 3 4
CuSO 电镀废液,向甲室通入足量氨气后电池开始工作。下列说法正确的是
4
A.甲室 Cu 电极为正极
B.隔膜为阳离子膜
C.乙室电极反应为:Cu2+ + 2e-= Cu
D.NH 扩散到乙室将不会对电池电动势产生影响
3
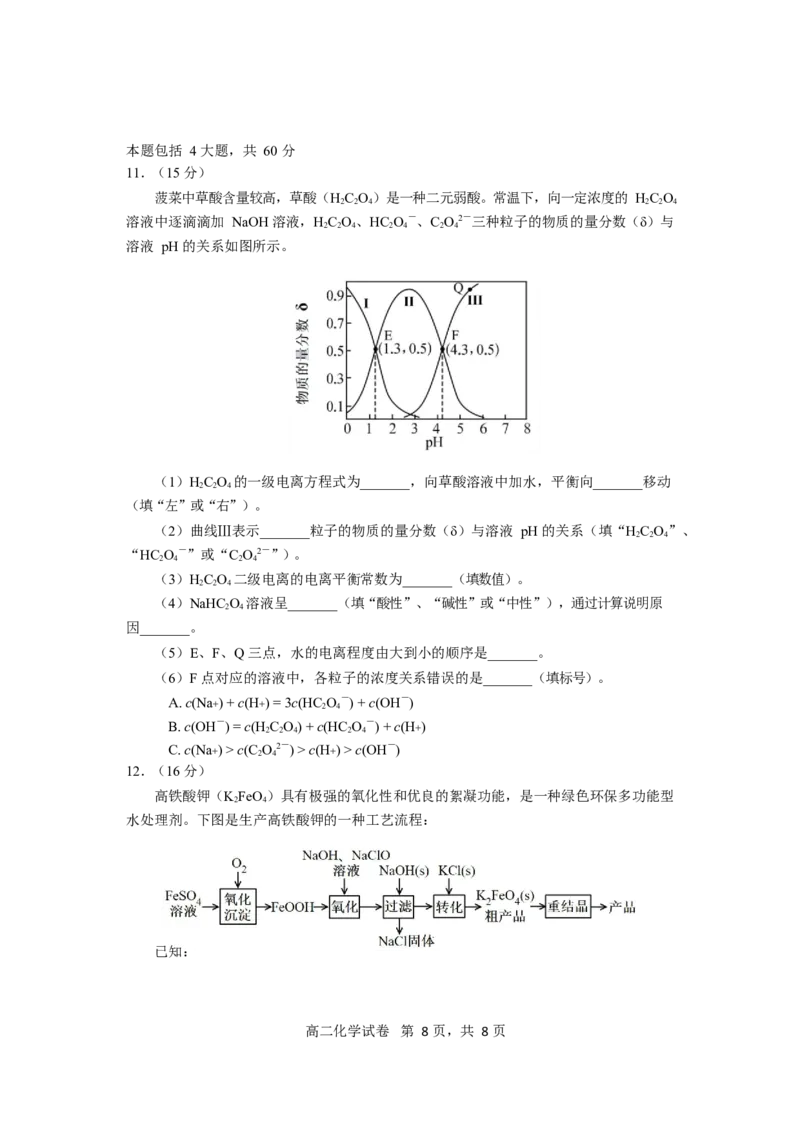
10.25℃时,Mg(OH) 或 Cu(OH) 的饱和溶液中,-lg c(Mg2+)或-lg c(Cu2+)与溶液 pH 的变
2 2
化关系如图所示。已知:该温度下,K [Cu(OH) ] < K [Mg(OH) ]。下列说法错误的是
sp 2 sp 2
A.L 表示 Mg(OH) 饱和溶液中的变化关系,且 K [Mg(OH) ] = 10-10.7
2 2 sp 2
B.向 a 点对应的饱和溶液中加入少量 NaOH 固体,可转化为 b 点对应的溶液
C.当 Mg(OH) 和 Cu(OH) 沉淀共存时,溶液中 c(Mg2+) :c(Cu2+) = 109
2 2
D.除去 MgSO 溶液中含有的少量 Cu2+,可加入适量 MgO 固体
4
第Ⅱ卷 非选择题(共 60 分)
高二化学试卷 第 8 页,共 8 页本题包括 4 大题,共 60 分
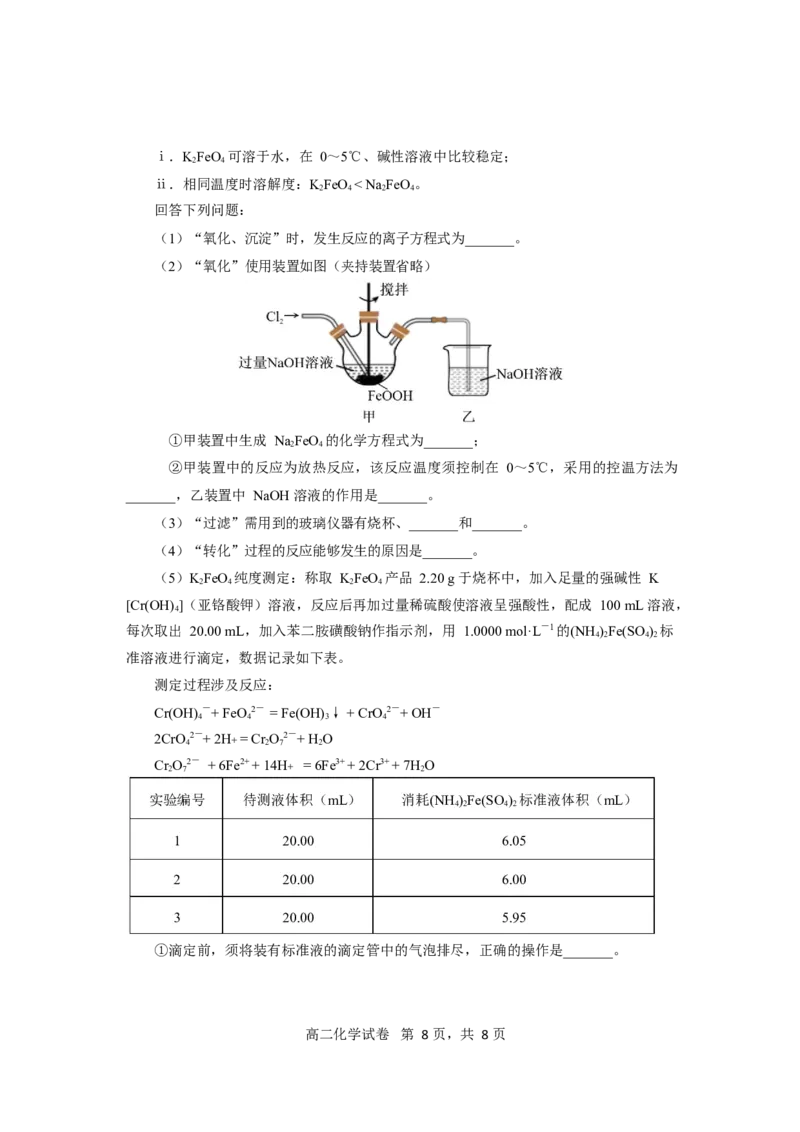
11.(15 分)
菠菜中草酸含量较高,草酸(HC O)是一种二元弱酸。常温下,向一定浓度的 HC O
2 2 4 2 2 4
溶液中逐滴滴加 NaOH 溶液,HC O、HC O-、C O2-三种粒子的物质的量分数(δ)与
2 2 4 2 4 2 4
溶液 pH 的关系如图所示。
(1)HC O 的一级电离方程式为_______,向草酸溶液中加水,平衡向_______移动
2 2 4
(填“左”或“右”)。
(2)曲线Ⅲ表示_______粒子的物质的量分数(δ)与溶液 pH 的关系(填“HC O”、
2 2 4
“HC O-”或“C O2-”)。
2 4 2 4
(3)HC O 二级电离的电离平衡常数为_______(填数值)。
2 2 4
(4)NaHC O 溶液呈_______(填“酸性”、“碱性”或“中性”),通过计算说明原
2 4
因_______。
(5)E、F、Q 三点,水的电离程度由大到小的顺序是_______。
(6)F 点对应的溶液中,各粒子的浓度关系错误的是_______(填标号)。
A. c(Na+) + c(H+) = 3c(HC
2
O
4
-) + c(OH-)
B. c(OH-) = c(H
2
C
2
O
4
) + c(HC
2
O
4
-) + c(H+)
C. c(Na+) > c(C
2
O
4
2-) > c(H+) > c(OH-)
12.(16 分)
高铁酸钾(KFeO)具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型
2 4
水处理剂。下图是生产高铁酸钾的一种工艺流程:
已知:
高二化学试卷 第 8 页,共 8 页ⅰ.KFeO 可溶于水,在 0~5℃、碱性溶液中比较稳定;
2 4
ⅱ.相同温度时溶解度:KFeO < Na FeO。
2 4 2 4
回答下列问题:
(1)“氧化、沉淀”时,发生反应的离子方程式为_______。
(2)“氧化”使用装置如图(夹持装置省略)
①甲装置中生成 NaFeO 的化学方程式为_______;
2 4
②甲装置中的反应为放热反应,该反应温度须控制在 0~5℃,采用的控温方法为
_______,乙装置中 NaOH 溶液的作用是_______。
(3)“过滤”需用到的玻璃仪器有烧杯、_______和_______。
(4)“转化”过程的反应能够发生的原因是_______。
(5)KFeO 纯度测定:称取 KFeO 产品 2.20 g 于烧杯中,加入足量的强碱性 K
2 4 2 4
[Cr(OH) ](亚铬酸钾)溶液,反应后再加过量稀硫酸使溶液呈强酸性,配成 100 mL 溶液,
4
每次取出 20.00 mL,加入苯二胺磺酸钠作指示剂,用 1.0000 mol·L-1 的(NH )Fe(SO ) 标
4 2 4 2
准溶液进行滴定,数据记录如下表。
测定过程涉及反应:
Cr(OH) -+ FeO 2- = Fe(OH) ↓ + CrO 2-+ OH-
4 4 3 4
2CrO
4
2-+ 2H+ = Cr
2
O
7
2-+ H
2
O
Cr
2
O
7
2- + 6Fe2+ + 14H+ = 6Fe3+ + 2Cr3+ + 7H
2
O
实验编号 待测液体积(mL) 消耗(NH )Fe(SO ) 标准液体积(mL)
4 2 4 2
1 20.00 6.05
2 20.00 6.00
3 20.00 5.95
①滴定前,须将装有标准液的滴定管中的气泡排尽,正确的操作是_______。
高二化学试卷 第 8 页,共 8 页A. B. C. D.
②该 KFeO 产品的纯度为_______。
2 4
13.(14 分)
用旧钴酸锂正极材料(主要成分为 LiCoO ,含少量 Fe O、Al O 等杂质),采用以下
2 2 3 2 3
工艺可制得 Co O 和 LiCO。
3 4 2 3
已知:
ⅰ.钴酸锂(LiCoO )难溶于水和 5%的 NaOH 溶液;
2
ⅱ.氧化性:Co3+ > H O > Fe3+;
2 2
ⅲ.室温时,K (Li CO) = 8.1×10-4;
sp 2 3
ⅳ.常温下,几种金属离子形成氢氧化物沉淀时的 pH 如下表:
Fe3+ Fe2+ Co3+ Co2+
开始沉淀 pH 1.9 6.8 6.8 6.6
沉淀完全 pH 3.2 8.3 9.2 7.6
回答下列问题:
(1)“80℃加热 2h”的目的是_______。
(2)“滤液”中的溶质主要有 NaOH 、_______(填化学式)。
(3)“酸浸、还原”后溶液中含有 H+ 、Fe3+、Co2+等阳离子,生成 Co2+的离子方程式
为_______。
(4)“除铁”时调节溶液 pH 范围为_______,检验“除铁”已完成的操作是_______。
(5)“沉淀 2”在“850℃煅烧”时的化学方程式为_______。
(6)若“沉锂”前 c(Li+)=2.0mol·L-1,向该溶液中加入饱和 Na
2
CO
3
溶液后
c(CO
3
2-)=0.1mol·L-1,则 Li+ 的沉淀率为_______。
[忽略溶液体积变化; ]
14.(15 分)
高二化学试卷 第 8 页,共 8 页二氧化碳是工业废气中的常见物质,有关二氧化碳的综合开发利用成为研究热点。
方法Ⅰ:捕碳技术
(1)捕碳技术(主要指捕获 CO)在降低温室气体排放中具有重要的作用。下列物
2
质中可作为捕碳剂的是_______。
A.KCO B.CaO C. NaSO D.NH Cl
2 3 2 4 4
方法Ⅱ:CO 加氢制甲醇
2
利用 CO 加氢合成甲醇的主要反应如下:
2
主反应 CO(g) + 3H (g) CHOH(g) + H O(g) ΔH= - 48.97 kJ·mol-1
2 2 3 2 1
副反应 CO(g) + H(g) CO(g) + H O(g) ΔH= + 41.17 kJ·mol-1
2 2 2 2
(2)根据上述反应,CO(g) +2H (g) CHOH(g) ΔH =_______。
2 3
(3)恒温恒容时,下列能说明 CO(g) + 3H (g) CHOH(g) + H O(g) 到达平衡状
2 2 3 2
态的是 _______(填标号)。
A.混合气体的密度不再改变
B.υ (CO) = 3υ(H )
2 2
C.每断裂 2 mol C=O 键,同时断裂 3mol H-O 键
D.CHOH(g)的质量不再改变
3
(4)向刚性容器中充入物质的量之比为 1 :3 的 CO 和 H,发生上述主、副反应。
2 2
①有利于提高甲醇平衡产率的条件是_______(填标号)。
A.高温高压 B.低温高压 C.高温低压 D.低温低压
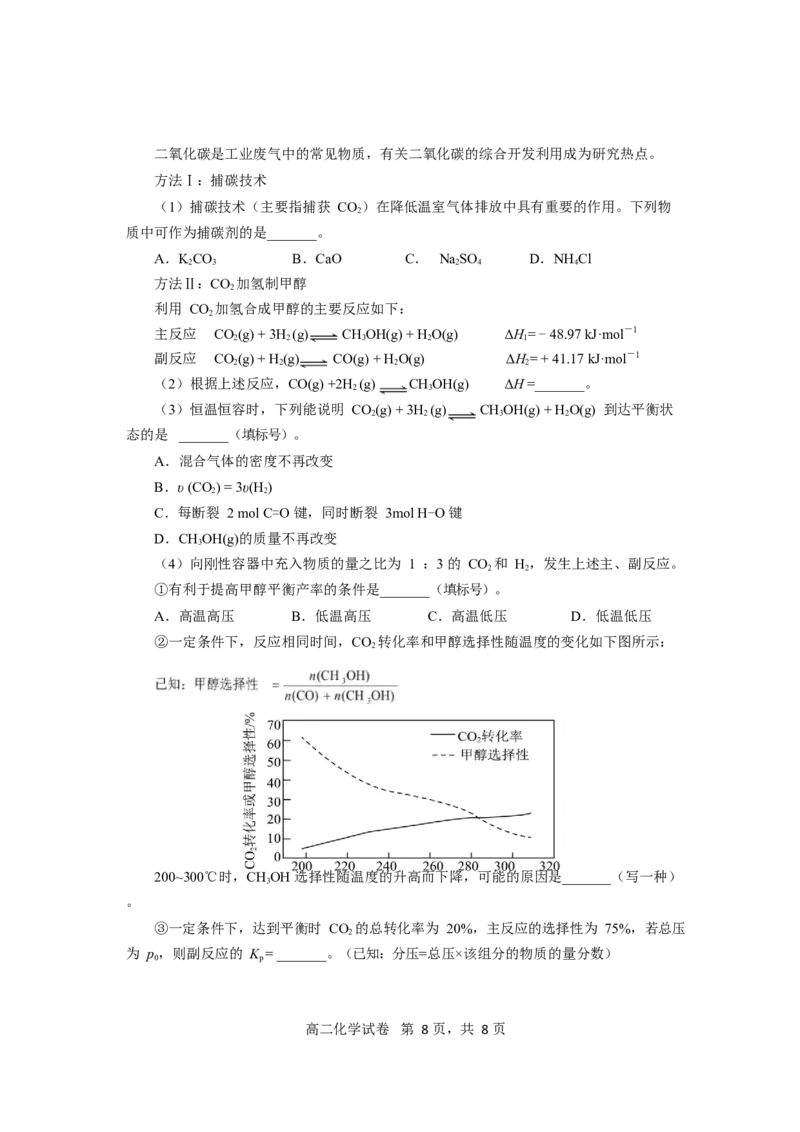
②一定条件下,反应相同时间,CO 转化率和甲醇选择性随温度的变化如下图所示:
2
200~300℃时,CHOH 选择性随温度的升高而下降,可能的原因是_______(写一种)
3
。
③一定条件下,达到平衡时 CO 的总转化率为 20%,主反应的选择性为 75%,若总压
2
为 p,则副反应的 K = _______。(已知:分压=总压×该组分的物质的量分数)
0 p
高二化学试卷 第 8 页,共 8 页方法Ⅲ:CO 电解制甲醇
2
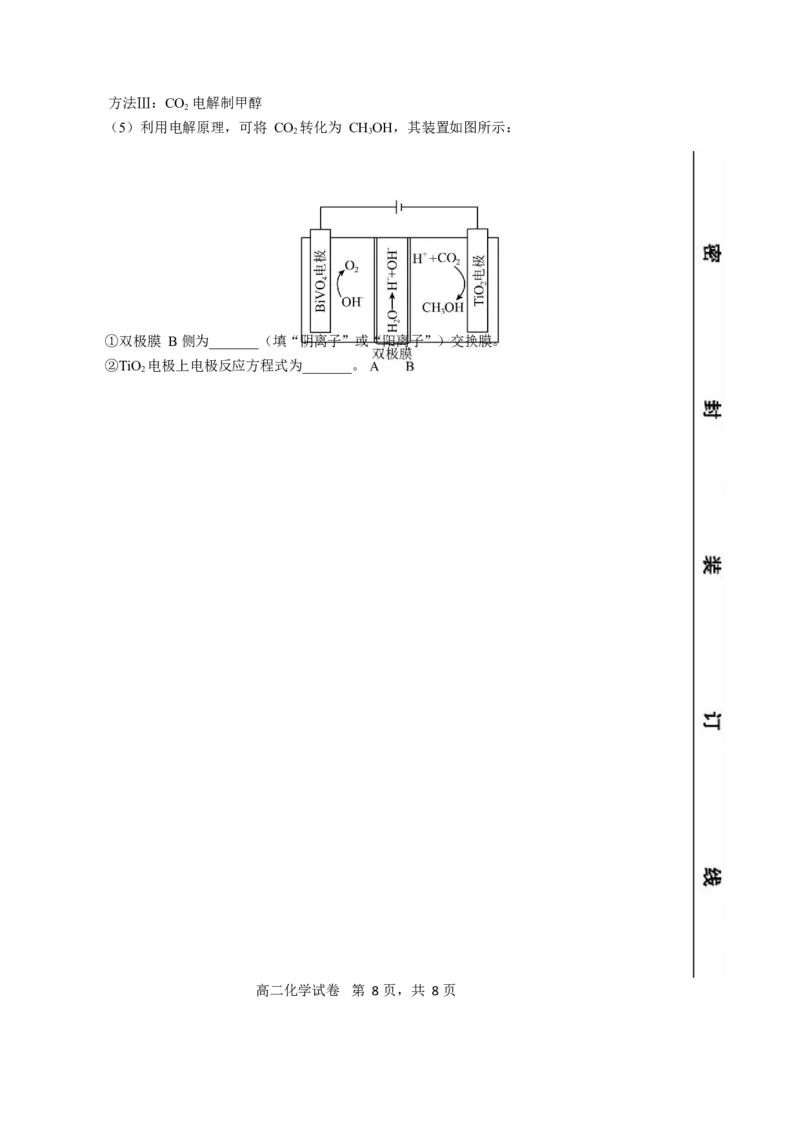
(5)利用电解原理,可将 CO 转化为 CHOH,其装置如图所示:
2 3
①双极膜 B 侧为_______(填“阴离子”或“阳离子”)交换膜。
②TiO 电极上电极反应方程式为_______。
2
高二化学试卷 第 8 页,共 8 页宁德市 2024-2025 学年第一学期期末高二质量检测
化学参考答案
本题包括 10 小题,每小题 4 分,共 40 分。
1−5 ABDCB 6−10 CAACB
本题包括 4 大题,共 60 分。
11.(15 分)
(1) H
2
C
2
O
4
H+ +HC
2
O
4
-(2 分)、右(2 分)
(2) C O2-(2 分)
2 4
(3) 10-4.3(2 分)
(4) 酸性(1 分); =1.0×10-12.7<K =10-4.3,HC O 的水解程度小于电离程度,
a2 2
溶液呈酸性(2 分);
(5) Q>F>E(2 分)
(6) B(2 分)
12.(16 分)
(1) 4Fe2+ + O
2
+ 6H
2
O = 4FeOOH↓ + 8H+ (2 分)
(2)①2FeOOH + 3NaClO + 4NaOH = 2Na FeO + 3NaCl + 3H O
2 4 2
(或 3Cl + 2FeOOH + 10NaOH = 2Na FeO + 6NaCl + 6H O)(2 分)
2 2 4 2
②冰水浴(2 分) 吸收多余的 Cl,防止污染环境(2 分)
2
(3) 玻璃棒 漏斗(各 1 分,共 2 分)
(4) 相同温度下,KFeO 的溶解度小于 NaFeO(2 分)
2 4 2 4
(5)①B(2 分) ②90%或 0.9(2 分)
13.(14 分)
(1)加快反应速率,使反应更充分(2 分)
高二化学参考答案 第 2 页,共 2 页(2)Na[Al(OH)](2 分)
4
(3)2LiCoO
2
+ H
2
O
2
+ 6H+ = 2Co2+ +2Li+ + 4H
2
O + O
2
↑(2 分)
(4)3.2≤pH<6.6(2 分) ;取适量“除铁”后的溶液于试管中,滴加少量 KSCN 溶液,若溶液未出现
血红色,则“除铁”完全。(2 分)
(5) (2 分)
(6)95.5%或 0.955(2 分)
14. (15 分)
(1) AB (2 分)
(2)-90.14 kJ·mol-1(2 分)
(3)CD(2 分)
(4)① B(2 分)
②ΔH < 0,ΔH>0,升温主反应逆向移动,副反应正向移动(或“升温对副反应速率的影响更大”或“温度
1 2
升高,催 化剂活性降低”)(2 分)
③5x10-3 (或“ ”,或列式正确未化简均给分) (2 分)
(5)①阳离子 (1 分) ②CO
2
+ 6H+ + 6e-= CH
3
OH + H
2
O(2 分)
高二化学参考答案 第 2 页,共 2 页