文档内容
2025-2026 学年度上学期高二 10 月月考
高二化学试卷
考试时间:2025年10月14日下午14:30-17:05 试卷满分:100分
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并认真
核准准考证号条形码上的以上信息,将条形码粘贴在答题卡上的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非
答题区域均无效。
3.选择题用 2B 铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡
上作答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
1. 化学与生活密切相关。下列生活生产场景中,相关措施不正确的是
选项 A B C D
场景 铁器生锈 食物的腐败 塑料的老化 氨的合成
措施 氯化铵溶液处理 置于冰箱中降温 添加增塑剂 使用铁触媒
2. 下列说法中正确的是
A.配制FeCl 溶液,将一定量的FeCl 固体溶于蒸馏水中,搅拌即可
3 3
B.Na CO 溶液水解呈碱性,热的Na CO 溶液去油污能力更强
2 3 2 3
C.草木灰可以和铵态氮肥一起使用,效果更好
D.所有的吸热反应一定都不能自发进行
3. 在一定条件下,可逆反应2SO (g)+O (g) 2SO (g) ΔH=-akJ/mol达到化学平衡状态,下
2 2 3
列说法错误的是
A.ν (SO )=ν (SO ) B.SO 、O 、SO 的浓度都不再发生变化
正 2 逆 3 2 2 3
C.反应放出的热量小于akJ D.混合气体的平均摩尔质量不变
高二化学试卷(共 8 页)第 1 页4. 亚磷酸(H PO )是一种二元弱酸,常温下电离常数K =1.0×10−2,K =2.6×10−7。下列说法
3 3 a1 a2
正确的是
A.对亚磷酸溶液升温,溶液的pH变小
B.H PO 与足量的NaOH溶液反应生成Na PO
3 3 3 3
c(H PO-)
C.向亚磷酸溶液中加入少量NaOH固体,则 2 3 变小
c(H PO )
3 3
D.对0.01mol/L的H PO 溶液加水稀释,溶液中各离子浓度均减小
3 3
5. 下列说法正确的是
A.常温常压下H (g)和O (g)混合无明显现象,则反应2H (g)+O (g)=2H O(l)在任何温度都
2 2 2 2 2
不自发
B.CO(g)+H (g) C(s)+H O(g) ΔH<0,则正反应的活化能小于逆反应的活化能
2 2
C.N (g)+3H (g) 2NH (g)反应平衡后增大压强,平衡正向移动,平衡常数增大
2 2 3
1
D.已知Na(s)+ Cl (g)=NaCl(s) ΔH <0,Na+(g)+Cl−(g)=NaCl(s) ΔH <0,则
2 1 2
2
1
Na(s)+ Cl (g)=Na+(g)+Cl−(g) ΔH<0
2
2
6. 下列有关反应的离子方程式错误的是
A.明矾净水的原理:Al3++3H O Al(OH) (胶体)+3H+
2 3
B.自然界中方铅矿(PbS)转化为铜蓝(CuS):PbS+Cu2+=CuS+Pb2+
C.龋齿的形成:Ca (PO ) OH+4H+=5Ca2++3HPO2+H O
5 4 3 4 2
D.TiCl 制备TiO :Ti4++4Cl-+(x+2)H O=TiO ·xH O↓+4HCl
4 2 2 2 2
7. 下列说法错误的是
A.2NO N O ,其他条件不变,缩小反应容器体积,气体颜色变浅
2 2 4
B.C(s)+H O(g) H (g)+CO(g),碳的质量不再改变说明反应已达平衡
2 2
C.若压强不再随时间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、C可能都是
气体
D.1molN 和3molH 反应达到平衡时H 转化率为10%,放出的热量为Q ;在相同温度和
2 2 2 1
压强下,当2molNH 分解为N 和H 的转化率为10%时,吸收的热量为Q ,则Q =Q
3 2 2 2 2 1
高二化学试卷(共 8 页)第 2 页8. 下列液体均处于25℃,有关难溶电解质的叙述错误的是
A.AgCl溶液中的c(Ag+)·c(Cl−)是一个常数
B.BaSO 在稀硫酸中的溶解度比在纯水中的溶解度小
4
C.向Mg(OH) 的悬浊液中加入少量的NH Cl固体,c(Mg2+)增大
2 4
D.向浓度均为0.1mol/L的MgCl 、CuCl 混合溶液中逐滴加入少量氨水,先生成Cu(OH)
2 2 2
沉淀,说明K [Cu(OH) ]④>②>①
C.将溶液①、④等体积混合,所得溶液中:c(CH COO-)>c(Na+),c(H+)>c(OH-)
3
D.将aL溶液②与bL溶液④混合,若所得溶液的pH=5,则a:b=101:99
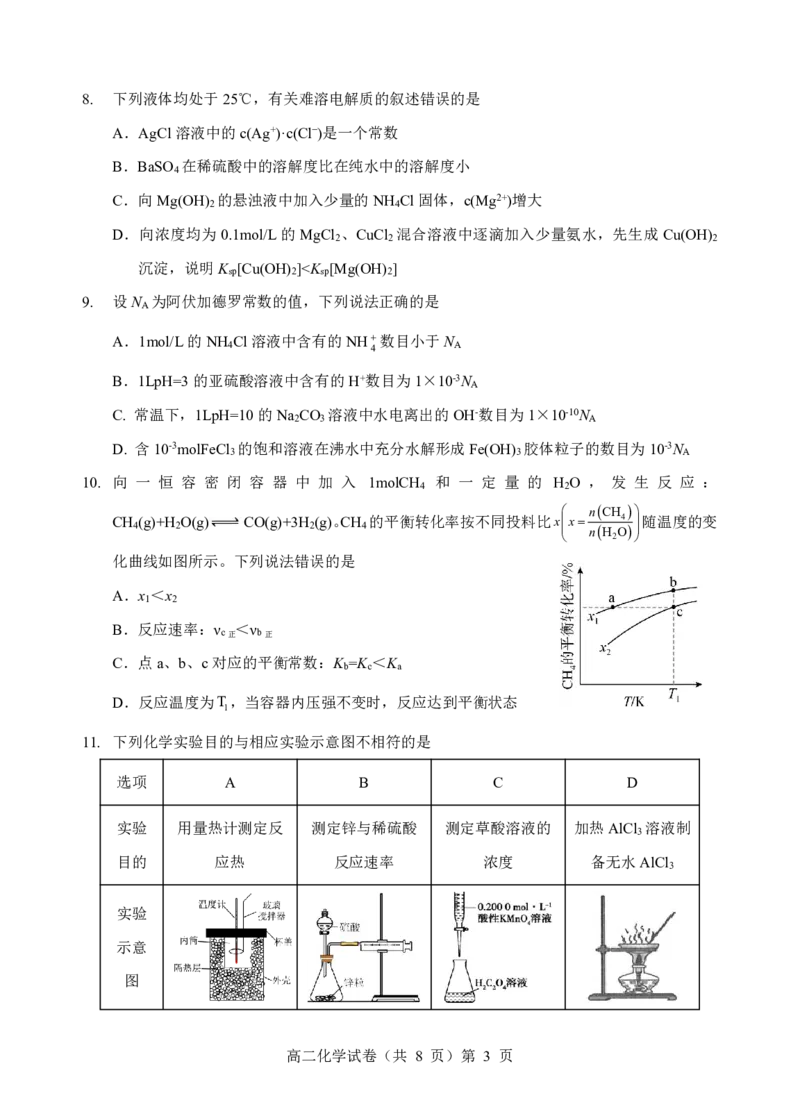
13. 密闭容器中,X和Y在有、无物质M的条件下,发生两个竞争反应:①X(g)+Y(g) Z(g),
②X(g)+Y(g) 2W(g),反应过程如图所示。下列叙述错误的是
A.恒温、有物质 M 的条件下,反应①的活化能大于反应②
B.升高温度,反应①平衡常数会增大而反应②平衡常数会减小
C.恒容条件下,分离出 W,反应①和反应②的正反应速率均减小
D.恒温条件下平衡后增大压强,再次平衡后 W的物质的量不变
14. 室温下,下列实验过程和现象能验证相应实验结论的是
选项 实验过程和现象 实验结论
A 向NaHA溶液中滴加紫色石蕊试液,溶液变蓝 K >K (H A)·K (H A)
w a1 2 a2 2
向 2mL 0.1 mol/LAgNO 溶液中滴加 2 滴 0.1
3
B mol/LNaCl溶液,有白色沉淀生成,然后滴加4 K (AgCl)>K (AgI)
sp sp
滴0.1mol/LKI溶液,有黄色沉淀生成
将装有 NO 和 N O 混合气体的烧瓶置于热水
2 2 4
C 2NO N O 的反应热ΔH>0
2 2 4
中,红棕色变深
将大小、形状相同的钠块和钙块放入相同体积的
D 金属活动性:Na>Ca
蒸馏水中,钙与水反应不如钠剧烈
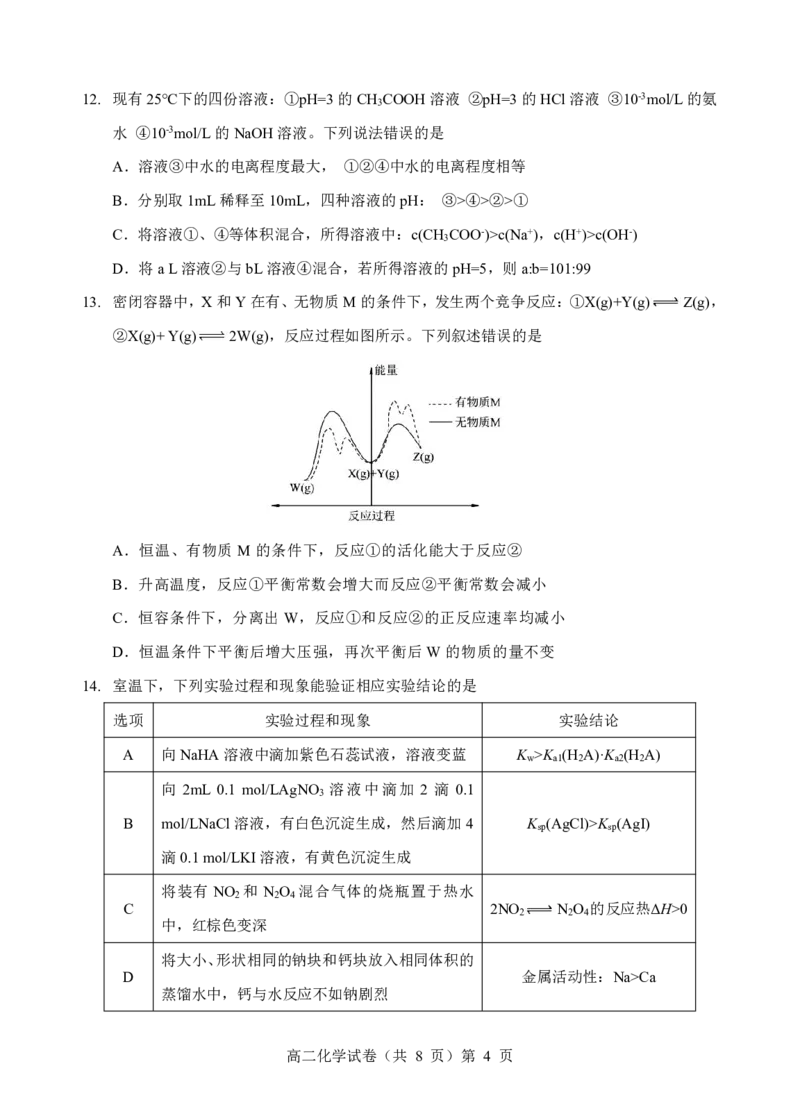
高二化学试卷(共 8 页)第 4 页15. 常温下,用浓度为 0.0200 mol/L 的 NaOH 标准溶液滴定浓度均为 0.0200 mol/L 的 HCl 和
V
标准溶液
CH COOH的混合溶液,滴定过程中溶液的pH随 ( )的变化曲线如图所示。
3
V
待测溶液
下列说法错误的是
A.K (CH COOH)数量级为10-5
a 3
B.点a∶c(Na+)=c(Cl-)=c(CH COO-)+c(CH COOH)
3 3
C.点b∶c(CH COO-)<c(CH COOH)
3 3
D.水的电离程度:a<b<c
二、非选择题:本题共4小题,共55分。
16. (14分)
下表是常温(25℃)时某些弱酸的电离平衡常数和盐的溶度积常数。回答下列问题:
化学式 HCN CH COOH H CO AgCl Ag CrO
3 2 3 2 4
K =4.5×10-7
K 或K K =6.2×10-10 K=1.75×10-5 a1 K =1.8×10-10 K =2.0×10-12
a sp a a sp sp
K =4.7×10-11
a2
(1)常温下,0.1 mol/L CH COOH 溶液加水稀释过程中,下列表达式的数据变大的是
3
_____________(填字母)。
c(H+) c(OH-) c(H+)·c(CH COO-)
a.c(H+) b. c. d. 3
c(CH COOH) c(H+) c(CH COOH)
3 3
(2)相同物质的量浓度的CH COONa和NaCN的混合溶液中,各离子浓度由大到小排序为
3
_____________。
(3)向NaCN溶液中通入少量CO ,所发生反应的化学方程式为_____________。
2
(4)①常温下向0.1mol/LCH COOH溶液中滴加等浓度的NaOH溶液。当溶液中c(CH COOH)∶
3 3
c(CH COO-)=4∶7时,此时溶液的pH=_____________。当pH=7时,所加NaOH溶液的体积与
3
CH COOH溶液体积的关系为 V(NaOH)_____________V(CH COOH)(填“大于”、“小于”或“等
3 3
于”)。
②用0.1mol/LCH COOH溶液滴定未知浓度的NaOH溶液时,下列操作会使测定的NaOH溶
3
液浓度偏大的是_____________(填字母)。
a.量取NaOH溶液时滴定管未润洗
b.盛装NaOH溶液的锥形瓶洗涤后未干燥
c.酸式滴定管滴定前尖嘴处有气泡,滴定后消失
d.酸式滴定管滴定前读数时仰视刻度线,滴定终点读数时俯视刻度线
(5)向浓度均为1.0×10-3mol/L的KCl和K CrO 的混合溶液中滴加1.0×10-3mol/L的AgNO
2 4 3
溶液,先生成_____________沉淀(填化学式)。
高二化学试卷(共 8 页)第 5 页17. (14分)
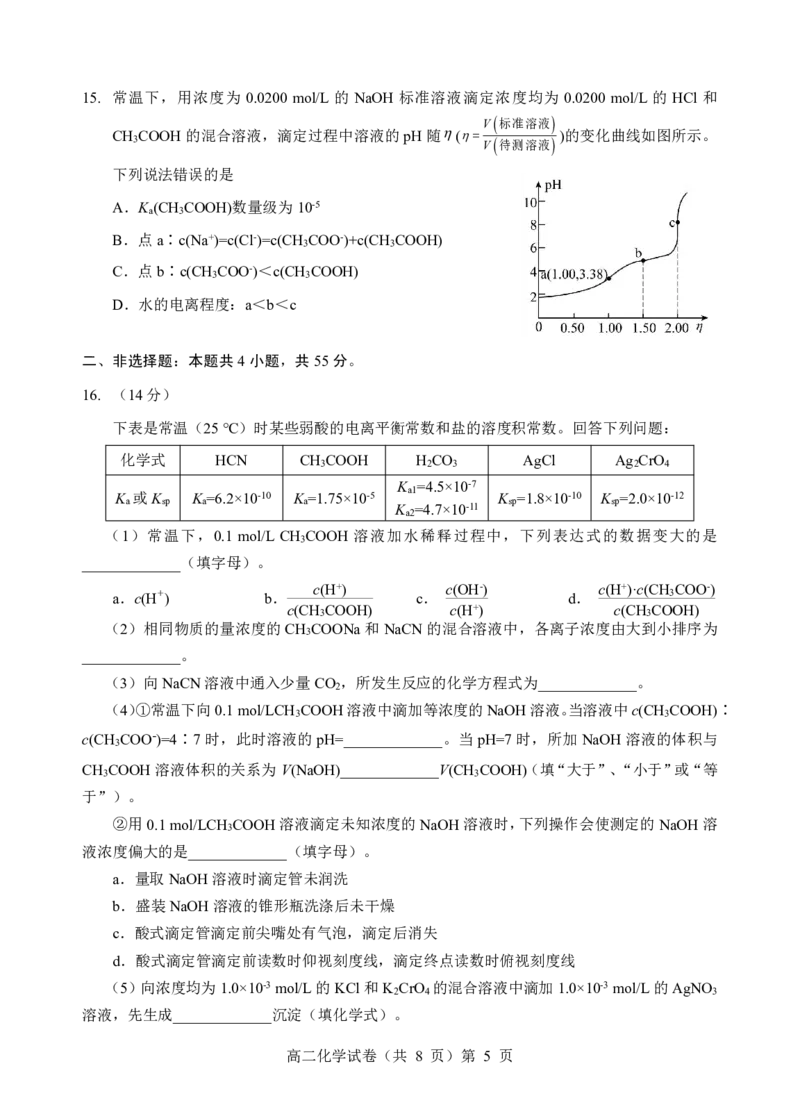
铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu S,含少量Fe O 、
2 2 3
SiO 等杂质)为原料制备不溶于水的碱式碳酸铜的流程如图:
2
离子 Fe2+ Fe3+ Cu2+ Mn2+
开始沉淀时pH 7.5 2.7 5.5 8.3
完全沉淀时pH 9.0 3.8 6.7 9.8
常温下,K [Fe(OH) ]=2.8×10-39。
sp 3
(1)加快“浸取”速率可采取的措施有_____________(任写一种)。
(2)“过滤Ⅰ”所得滤液中主要含有的金属阳离子有_____________(填离子符号)。
(3)常温下“除铁”时加入的含铜化合物A可用_____________(填化学式),调节pH范
围为_____________,若加入A后溶液的pH调为4,则溶液中c(Fe3+)=_____________mol/L。
(4)写出“沉锰”过程中生成MnCO 的离子方程式:_____________。
3
(5)“过滤Ⅱ”得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作
是_____________。
18. (12分)
食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示) 。HAc的应用与其电离平衡
密切相关。25℃时,HAc的 K =1.75×10−5=10−4.76。
a
(1)某小组研究25℃下HAc电离平衡的影响因素。
提出假设:稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。
设计方案并完成实验:用浓度均为 0.1mol/L的 HAc和NaAc 溶液,按下表配制总体积相同
的系列溶液;测定pH,记录数据。
序号 V(HAc)/mL V(NaAc)/mL V(H O)/mL n(NaAc):n(HAc) pH
2
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
…
Ⅶ 4.00 a b 3:4 4.53
Ⅷ 4.00 4.00 32.00 1:1 4.65
高二化学试卷(共 8 页)第 6 页①根据表中信息,补充数据:a=_____________,b=_____________。
②由实验Ⅰ和Ⅱ可知,稀释HAc溶液,HAc电离平衡__________(填“正”或“逆”)向移动。
③由实验Ⅱ~VIII可知,增大Ac-浓度,HAc电离平衡__________(填“正”或“逆”)向移动。
实验结论:假设成立。
n(NaAc)
(2)小组分析上表数据发现:随着 的增加,c(H+)的值逐渐接近HAc的K 。
a
n(HAc)
n(NaAc)
查阅资料获悉:一定条件下,按 =1 配制的溶液中,c(H+)的值等于HAc的K 。
a
n(HAc)
对比数据发现,实验VIII中pH=4.65与资料数据K =10−4.76存在一定差异;推测可能由物质
a
浓度准确程度不够引起,故先准确测定HAc溶液的浓度再验证。
①移取20.00mLHAc溶液,加入 2 滴_____________溶液,用 0.1000mol/LNaOH 溶液滴定
至终点的现象为_____________,消耗体积为 22.06mL,则该HAc溶液的浓度为__________mol/L。
②用上述HAc溶液和0.1000mol/LNaOH溶液,配制等物质的量的HAc与NaAc混合溶液,
测定pH,结果与资料数据相符。
(3)小组进一步提出:如果只有浓度均约为 0.1mol/L的HAc和NaOH溶液,如何准确测定
HAc的K ? 小组同学设计方案并进行实验。请完成下表中ⅱ的内容。
a
ⅰ 移取 20.00mLHAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液V mL
1
ⅱ ______________,测得溶液的pH为4.76
实验总结:得到的结果与资料数据相符,方案可行。
19. (15分)
实现碳中和方法之一是二氧化碳捕捉再利用,研究CO 转化为CH 、CH OH、C H OH等的
2 4 3 2 5
重整技术是科学家研究的热点课题,回答下列问题。
反应ⅰ:CO (g)+4H (g) CH (g)+2H O(g) ΔH
2 2 4 2 1
反应ⅱ:CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-49kJ/mol
2 2 3 2 2
(1)最新研究成果表明,在常温常压下利用水自由基阳离子((H O)•)可以实现甲烷到甲
2 2
醇的直接转化。已知断裂 1 mol化学键所吸收的能量数据如表,则 CH (g)+H O(g)
4 2
CH OH(g)+H (g) ΔH=_____________kJ/mol。
3 2
高二化学试卷(共 8 页)第 7 页化学键 H—H O—H C—H C=O
能量/kJ 436 463 413 803
(2)在一定温度下,向1L密闭容器中充入2molCO (g)和2molH (g),仅发生反应ⅱ。
2 2
①反应ⅱ能在_____________(填“高温”、“低温”或“任何温度”)下自发进行。
②下列情况表明反应ⅱ已达到平衡状态的是_____________(填字母)。
a.CO 的转化率保持不变 b.混合气体的密度保持不变
2
c.CO 的体积分数保持不变 d.CH OH与H O的物质的量之比不再改变
2 3 2
③平衡时CO 的转化率为25%,则该温度下反应ⅱ的平衡常数K=_____________。
2
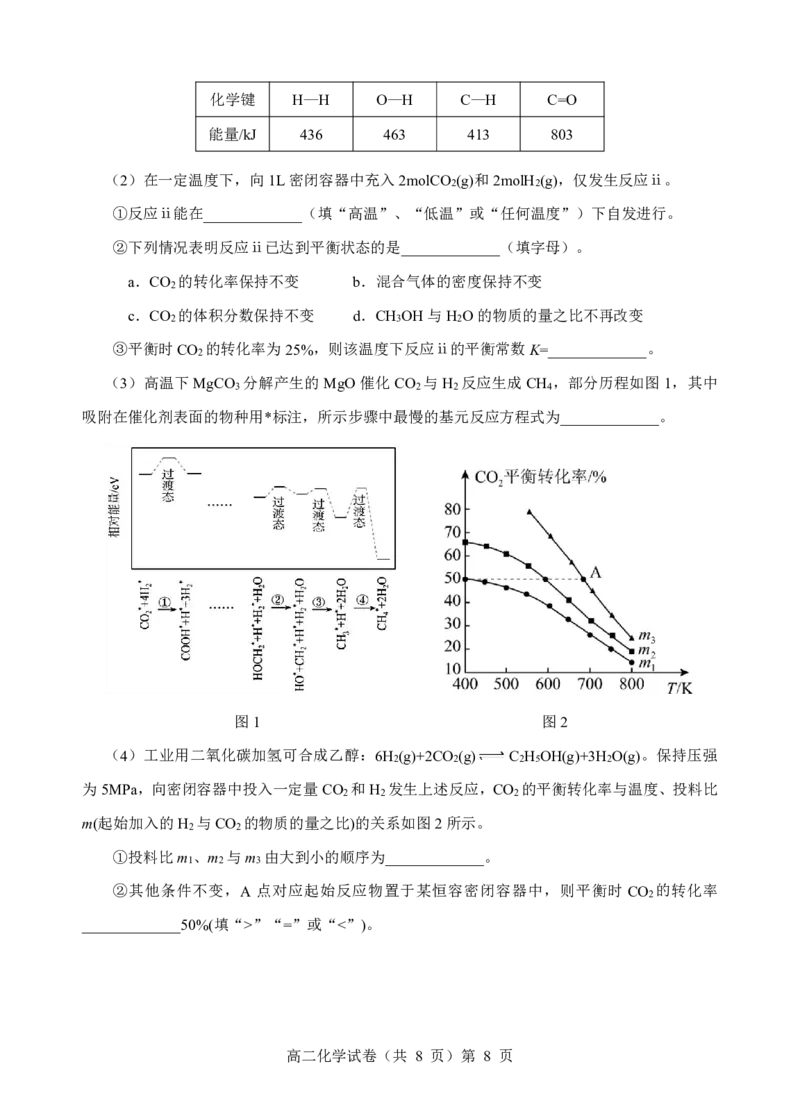
(3)高温下MgCO 分解产生的MgO 催化CO 与H 反应生成CH ,部分历程如图1,其中
3 2 2 4
吸附在催化剂表面的物种用*标注,所示步骤中最慢的基元反应方程式为_____________。
图1 图2
(4)工业用二氧化碳加氢可合成乙醇:6H (g)+2CO (g) C H OH(g)+3H O(g)。保持压强
2 2 2 5 2
为5MPa,向密闭容器中投入一定量CO 和H 发生上述反应,CO 的平衡转化率与温度、投料比
2 2 2
m(起始加入的H 与CO 的物质的量之比)的关系如图2所示。
2 2
①投料比m 、m 与m 由大到小的顺序为_____________。
1 2 3
②其他条件不变,A 点对应起始反应物置于某恒容密闭容器中,则平衡时 CO 的转化率
2
_____________50%(填“>”“=”或“<”)。
高二化学试卷(共 8 页)第 8 页