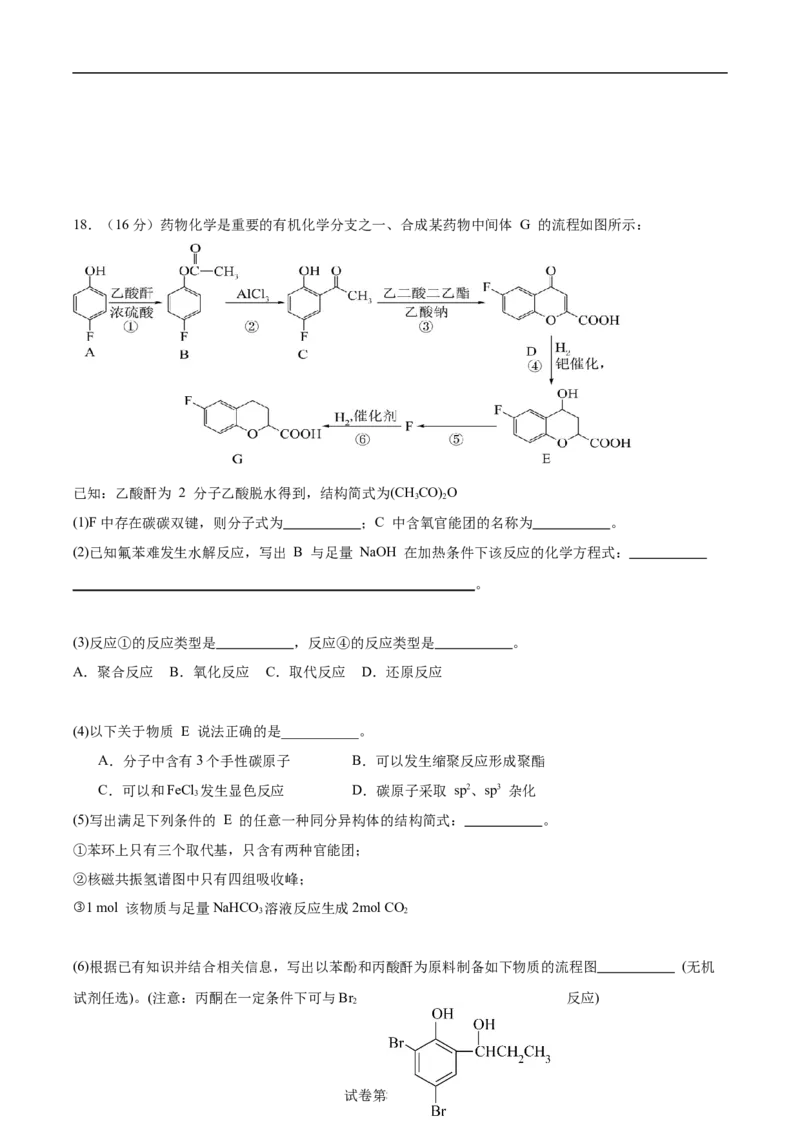
文档内容
2024 年下学期高三第二次月考化学试卷
考试时间:75分钟 总分:100分
命题人:阳恩富 审题人:周向飞
注意事项:
1.在答题卡上填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
3.可能用到的相对原子质量:Fe- 56 Cl-35.5
第I卷(选择题)
一、单选题{每小题只有一个选项符合题意,每题3分,共计42分}
1.中华文化源远流长,化学与文化传承密不可分。下列说法正确的是( )
A.清朱耷芦雁轴纸本的主要成分是淀粉,淀粉为高分子化合物
B.四千余年前用谷物酿造出酒和醋,酿造过程中只发生水解反应
C.《本草纲目》“烧酒”条目写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,
味极浓烈,盖酒露也。”叙述了“蒸馏”技术在古代酿酒工艺中的应用
D.广汉三星堆出土的青铜面具呈红棕色斑迹,是由于铜发生了吸氧腐蚀
2.下列化学用语表示正确的是( )
A.NH 分子的VSEPR模型: B.中子数为18的氯原子:
3
C.HCl的形成过程: D.碳的基态原子轨道表示式:
3.下列关于仪器使用的说法正确的是( )
A.a和f可用于蒸发结晶 B.c和d均有“0”刻度
C.b、e和g常用于物质分离 D.d、f、g使用前需检漏
4.化学与生活密切相关,下列说法正确的是( )
A.日常生活中所用的花生油、牛油、石蜡油分子中均含有酯基
B.用激光笔照射淀粉溶液、鸡蛋白溶液均能观察到丁达尔效应
C.泡沫灭火器中所用硫酸铝、碳酸氢钠溶于水后,溶液均显酸性
试卷第1页,共3页
学科网(北京)股份有限公司D.计算机芯片、硅太阳能电池、光导纤维的主要材料均为高纯硅
5.有机物Q ( )是一种重要的药物合成中间体,下列有关有机物Q的说法错误的是( )
A.分子式为 B.一定存在能使 显色的同分异构体
C.可发生加成反应、取代反应和还原反应 D.分子中所有的碳原子可能处于同一平面上
6.设 为阿伏伽德罗常数的值。已知 说法错误的是( )
A.0.1 mol 中1含有的σ键为0.4 B.标准状况下1.12 L CO含有质子数为0.7
C.每生成1 mol 转移电子数为6 D.1 L 的 溶液中,阳离子数目大于0.1
7.下列离子方程式书写正确的是( )
A.向漂白粉溶液中通入过量 的离子方程式为:
B.向明矾 溶液中滴加氢氧化钡溶液至沉淀物质的量最大时的离子方程式为:
C.向石灰乳中通入过量 的离子方程式为:
D.银和稀硝酸反应的离子方程式为:
8.部分含铁微粒所带的电荷数与其中铁元素化合价的关系如
图所示,由该图可预测含铁微粒间相互转化时所需试剂。下列
推断不合理的是( )
A.若M不溶于水,M一定为FeO
B.若R为单质,则常温下浓硫酸可使R钝化
C.若Q为金属阳离子,则可用 溶液检验
D. 与氧化剂在碱性条件下反应可生成
9.铝土矿的主要成分为氧化铝、氧化铁和二氧化硅,工业上经过下列工艺可以冶炼金属铝:
试卷第2页,共3页提示:③发生的反应是: 。下列说法中错误的是( )
A.①②中除加试剂外,还需要进行过滤操作 B.a、b中铝元素的化合价相同
C.④进行的操作是加热,而且d是氧化铝 D.⑤可采用活泼金属置换的方法
10.探究钠及其化合物的性质,下列方案设计、现象和结论都正确的是( )
实验方案 现象 结论
分别测定 和 两者都大于7,且
A 的水解能力强于
溶液的pH 溶液的pH大
B 对某未知溶液进行焰色试验 火焰呈黄色 该溶液中含有钠盐
用形状和质量相同的钠,分
钠与乙醇反应比与苯 乙醇中羟基的活性强于苯酚中羟基的活
C 别和等物质的量的苯酚和乙
酚反应剧烈 性
醇反应
向饱和 溶液中滴加 溶液变浑浊同时产生 发生的反应:
D
一定量的浓 溶液 气泡
11.化学是以实验为基础的学科,在科学实验中发现问题、分析问题、解决问题,体验实验的乐趣和科学
探究的精神是学习化学的关键,下列实验操作和实验现象以及实验目的或结论有错误的是( )
实验操作和实验现象 实验目的或结论
取少量待测液于试管中,先加入过量稀硝酸,无现象,再加入氯
A 该待测液中含有 或
化钡溶液,有白色沉淀生成
向5mL 0.2mol/L 溶液中滴加5滴0.1mol/L NaOH溶液,生 不能验证 和
B
成白色沉淀,再滴加5滴0.1mol/L 溶液,观察实验现象 的相对大小
C 向 溶液中,加入过量锌粉,溶液由深蓝色变为无色 金属性:Zn>Cu
向试管中依次加入苯、液溴、稀 溶液,将生成的气体先通入
D 苯与液溴发生取代反应
,再通入硝酸银溶液,产生白色沉淀
12.向体积均为10mL且物质的量浓度相同的两份NaOH溶液中分别通入一定
试卷第3页,共3页
学科网(北京)股份有限公司量的CO 得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1 mol·L-1盐酸。此时反应生成CO 体积(标准状
2 2
况)与所加盐酸体积间的关系如图所示。则下列叙述中正确的是( )
A.乙溶液中含有的溶质是NaCO、NaHCO
2 3 3
B.当0Cu,说明金属性:
Zn>Cu,C正确;
D.苯与液溴才可以发生取代反应, 溶液中含有水,使苯与 无法发生取代反应,
D错误;
故选D。
12.C【周考三13题、一轮复习书p44例2】
【分析】在氢氧化钠溶液中通入一定量的二氧化碳后,溶液中溶质的组成可能是NaOH和
NaCO、NaCO、NaCO 和NaHCO 、NaHCO 四种情况,没有产生二氧化碳时的反应可
2 3 2 3 2 3 3 3
能为:OH﹣+H+=HO和CO +H+=HCO ,产生二氧化碳的反应为:HCO +H+=
2
HO+CO↑;根据加入50mL盐酸时溶质为氯化钠及原子守恒计算出氢氧化钠的物质的量浓
2 2
度;根据图象可知,甲溶液中溶质只能为NaCO 和NaHCO ,乙溶液的溶质为NaOH和
2 3 3
NaCO;根据HCO +H+=HO+CO↑计算出乙溶液中产生二氧化碳的最大值。
2 3 2 2
【详解】A.氢氧化钠溶液中通入二氧化碳,溶质不可能为NaOH、NaHCO ,根据图象可
3
知,乙溶液中的溶质为NaOH和NaCO,故A错误;
2 3
B.在氢氧化钠溶液中通入一定量的二氧化碳后,溶液中溶质的组成可能是:NaOH和
NaCO、NaCO、NaCO 和NaHCO 、NaHCO 四种情况,由图中HCl的用量与产生二氧
2 3 2 3 2 3 3 3
化碳气体体积的关系可知甲溶液的溶质应该为:NaCO 和NaHCO ,所以当0<V(HCl)<
2 3 3
10mL时,甲溶液中没有产生二氧化碳的离子方程式为:CO +H+=HCO ,故B错误;
C.根据图象可知,当V(HCl)=50mL时,得到的产物为NaCl,由原子守恒可知:
n(NaOH)=n(NaCl)=n(HCl)=0.1 mol·L-1×0.05L=0.005mol,则原氢氧化钠溶液的浓度为:
答案第5页,共2页
学科网(北京)股份有限公司c(NaOH)= =0.5 mol·L-1,故C正确;
D.乙溶液中滴加盐酸,产生二氧化碳的阶段为:HCO +H+=HO+CO↑,根据消耗了
2 2
10mL盐酸可知,生成二氧化碳的物质的量为:0.1mol/L×0.01L=0.001mol,标况下
0.001mol二氧化碳的物质的量为:22.4L/mol×0.001mol=22.4mL,故D错误;
故答案为C。
13.C【一轮书p52对点演练1,周考二15题,一轮书p67第4题,p54 例2整合】
【分析】向含锌废液(主要成分为ZnSO,含少量的Fe2+、Mn2+)中加入NaSO 溶液,生成
4 2 2 8
MnO 沉淀且将Fe2+氧化为Fe3+,过滤后向滤液中加入试剂X调节pH使Fe3+转化为Fe(OH)
2 3
沉淀,为了不引入新杂质,试剂X可以为ZnO、ZnCO 、Zn(OH) 等,最后过滤后再加入
3 2
NH HCO 沉锌生成碱式碳酸锌ZnCO ·2Zn(OH) 。
4 3 3 2
【详解】A.NaSO 中硫元素的化合价为+6价,NaSO 表现氧化性来源于其中的过氧键,
2 2 8 2 2 8
故A错误;
B.氧化除锰步骤中氧化剂和还原剂的物质的量之比为1:1,故B错误;
C.沉锌时发生反应的离子方程式主要是:
,故C正确;
D.pH值过大时锌会转为Zn(OH) 沉淀,氨水过量时,Zn2+ 可以与氨水反应生成
2
[ Zn(NH) ]2+会降低的产率ZnCO ·2Zn(OH) ,故D错误;
3 4 3 2
故答案选C。
14.C【周考一第14题】
【分析】由图象可知,OA段气体一直在增加,因稀硝酸的氧化性强于稀硫酸,则OA段发
生反应为:Fe+ +4H+=Fe3++NO↑+2HO。AB段气体没有增加,是因为Fe3+的氧化性强
2
于H+,发生反应:Fe+2Fe3+=3Fe2+,BC段气体增加,是因为发生反应为:Fe+2H+=Fe2+
+H ↑。最终消耗22.4gFe,最终溶液中溶质为FeSO ,根据Fe元素守恒可以计算
2 4
n(FeSO ),进而计算硫酸的物质的量浓度。
4
【详解】A.经分析,OA段发生反应为:Fe+ +4H+=Fe3++NO↑+2HO,产生的是NO,
2
AB段气体没有增加,是因为发生反应:Fe+2Fe3+=3Fe2+,BC段气体增加,是因为发生反应
答案第6页,共2页为:Fe+2H+=Fe2++H ↑,产生的是H,故A正确;
2 2
B. OA段发生反应为:Fe+ +4H+=Fe3++NO↑+2HO,则 A点时溶液中的 都被还
2
原了,只剩SO ,阳离子有Fe3+和H+,则溶液的成分是Fe (SO ) 和HSO ,故B正确;
2 4 3 2 4
C.经分析最终溶液中的成分是FeSO ,最终消耗22.4gFe,根据铁离子和硫酸根离子的数
4
量关系,则可求出SO 的物质的量是0.4mol,OA段发生反应:Fe+ +4H+=Fe3+
+NO↑+2HO,根据消耗铁11.2g,根据反应的离子方程式,可求出NO 的物质的量是
2
0.2mol,则原混合酸中NO 和SO 物质的量之比为1:2,故C错误;
D.经上述分析,溶液中的SO 的物质的量是0.4mol,则原混合酸中的HSO 的物质的量
2 4
为0.4mol,原溶混合酸体积是200mL,则原混合酸中HSO 的物质的量浓度为2mol·L-1,
2 4
故D正确;
答案BC。
15.(1)除去铁屑表面油污
(2)O
2
(3) 冷凝回流SOCl ,提高SOCl
2 2
的利用率
(4) 95.0% K Fe(CN) 制备时SO (或+4价S)还原FeCl
3 6 2 3
【详解】(1)铁屑表面的油污可溶于碱液,则用NaOH溶液洗涤废铁屑的目的是除去铁屑
表面油污,故答案为:除去铁屑表面油污;
(2)由于生成的铁离子是过氧化氢分解的催化剂,则滴加10%双氧水时,滴加速率过快会
产生气泡,该气体为O,故答案为:O;
2 2
(3)锥形瓶中氯化铁晶体与SOCl 反应生成无水FeCl 、二氧化硫和氯化氢,其总反应的
2 3
答案第7页,共2页
学科网(北京)股份有限公司化学方程式为加热 ;仪器A是球形冷凝管,
其作用是冷凝回流SOCl ,提高SOCl 的利用率,故答案为:
2 2
;冷凝回流SOCl ,提高SOCl 的利用率;
2 2
(4)①反应的关系式为 ,所制产品的纯度为
,故答案为:95.0%;
②K Fe(CN) 与亚铁离子反应生成铁氰化亚铁钾沉淀,则所检验FeCl 的试剂为KFe(CN) 溶
3 6 2 3 6
液;产生FeCl 的原因可能是制备时SO (或+4价S)还原FeCl ,故答案为:KFe(CN) ;制
2 2 3 3 4
备时SO (或+4价S)还原FeCl 。
2 3
16.(1)b
(2) +6 2U O+O +6NaOH=3NaUO+3H O
3 8 2 2 2 7 2
(3) 2Ce(OH) +8H++2Cl﹣=2Ce3++Cl↑+8H O 4×10﹣7
4 2 2
(4)RaSO
4
【分析】独居石的主要成分为CePO,含有Th(PO )、UO 和少量镭杂质,加入55~60%
4 3 4 4 3 8
的NaOH进行热分解,UO 发生反应:2UO+O +6NaOH=3NaUO+3H O,转化为
3 8 3 8 2 2 2 7 2
NaUO,CePO 中的Ce被氧化为Ce(OH) ,将热分解后的物质加水稀释后过滤,得到的滤
2 2 7 4 4
液中含有Na+、 ,滤液浓缩结晶后,得到的晶体化学式为:NaPO •12H O,滤液可用
3 4 2
于热分解阶段循环利用,避免产生大量的高碱度废水,过滤得到的固体产物中加入盐酸和
凝聚剂,Ce(OH) 具有氧化性,与盐酸发生反应:2Ce(OH) +8H++2Cl﹣=2Ce3+
4 4
+Cl↑+8H O,废气为Cl,调节pH,使铀和Th进入沉淀,向滤液中加入硫酸铵和氯化钡,
2 2 2
使BaSO 和RaSO 形成共沉淀,得到含有Ce3+的溶液,经过一系列操作,得到
4 4
CeCl •nH O,据此分析作答。
3 2
【详解】(1)a.降低压强,分解速率降低,故a错误;
b.降低温度,分解速率降低,故b正确;
答案第8页,共2页c.反应时间越长,分解速率逐渐变慢,故c错误;
d.提高搅拌速度,分解速率加快,故d错误;
故答案为b;
(2)NaUO 中Na为+1价,O为﹣2价,根据化合价代数和为0,则铀元素的化合价为+6
2 2 7
价,热分解阶段UO 生成NaUO 的化学反应方程式为:2UO+O +6NaOH=
3 8 2 2 7 3 8 2
3NaUO+3H O
2 2 7 2
(3)①根据后续流程可知,生成+3价Ce,则盐酸溶解Ce(OH) 发生氧化还原反应,其离
4
子方程式为:2Ce(OH) +8H++2Cl﹣=2Ce3++Cl↑+8H O;
4 2 2
②当溶液pH=4.5时,c(H+)=1×10﹣4.5mol/L,c(OH﹣)=1×10﹣9.5mol/L,c(Th4+)×c4(OH﹣)=
4.0×10﹣45,则c(Th4+)=4×10﹣7 mol/L,此时完全转化为氢氧化钍沉淀;
(4)以BaSO 为载体形成共沉淀,目的是去除杂质RaSO,RaSO 的溶解度更小。
4 4 4
17.(1)
(2)
(3) 小于 向左
(4)
(5)
【详解】(1)
由盖斯定律可知, 得到
故答案为: ;
(2) 使用催化剂,可加快反应速率,故选;
降低反应温度,反应速率减小,故不选;
增大体系压强,反应速率加快,故选;
答案第9页,共2页
学科网(北京)股份有限公司不断将 从反应混合物中分离出来,平衡虽正向移动,但浓度减小、反应速率减
小,故不选;
故答案为: ;
(3) 相同温度下,同一容器中,增大压强,平衡向正反应方向移动,则 的转化率增
大,根据图象知, 小于 ,故答案为:小于;
该温度下,平衡时 参加反应
,则 、
、 ,化学平衡常数 ,
故答案为: ;
向容器中通入 、H 、 各 ,
2
则平衡向左移动,故答案为:向左;
(4)该原电池中,负极上失电子被氧化,二氧化硫到硫酸,硫的化合价升高,所以负极上
投放的气体是二氧化硫,二氧化硫失电子和水反应生成硫酸根离子和氢离子,所以负极上
的电极反应式为: ,故答案为:
;
(5)若混合前 溶液的浓度为 ,等体积混合后浓度为 ,生
成沉淀所需 溶液的最小浓度为 ;电解池中阳极
和电源正极相连,失去电子,发生氧化反应,电解 溶液可制得硫酸,硫的化合价
答案第10页,共2页升高,所以阳极是 溶液失去电子被氧化生成 ,阳极电极反应式为
,阴极上得到电子生成氢气,电解反应为
,故答案为:
。
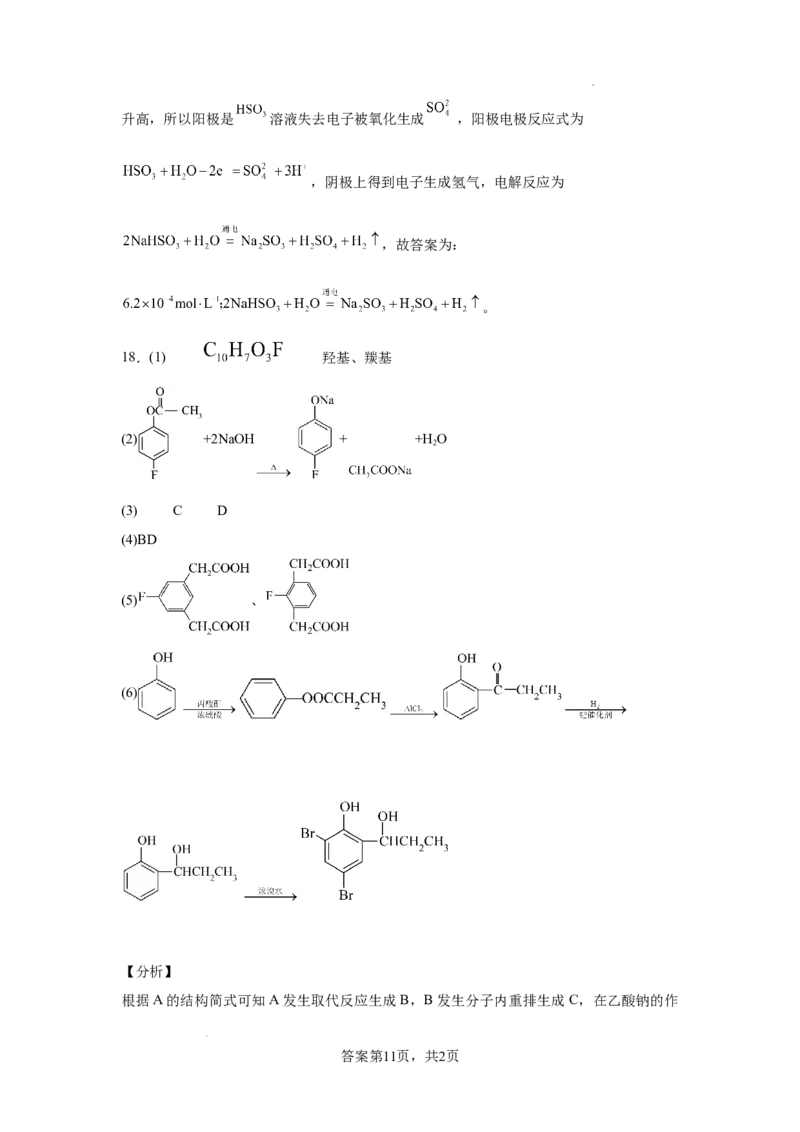
18.(1) 羟基、羰基
(2) +2NaOH + +H O
2
(3) C D
(4)BD
(5) 、
(6)
【分析】
根据A的结构简式可知A发生取代反应生成B,B发生分子内重排生成C,在乙酸钠的作
答案第11页,共2页
学科网(北京)股份有限公司用下C和乙二酸二乙酯反应生成E,E和氢气发生加成反应生成E,比较E和G的结构简
式可知F为 ,E发生消去反应得F,F再与氢气加成得G,据此解答。
【详解】(1)
F为 ,其分子式为:; ;由C的结构简式可知其含氧
官能团为羟基、羰基;
(2)
与足量 NaOH在加热条件下所含酯基发生水解反应生成 和 ,
反应方程式为: +2NaOH + +H O;
2
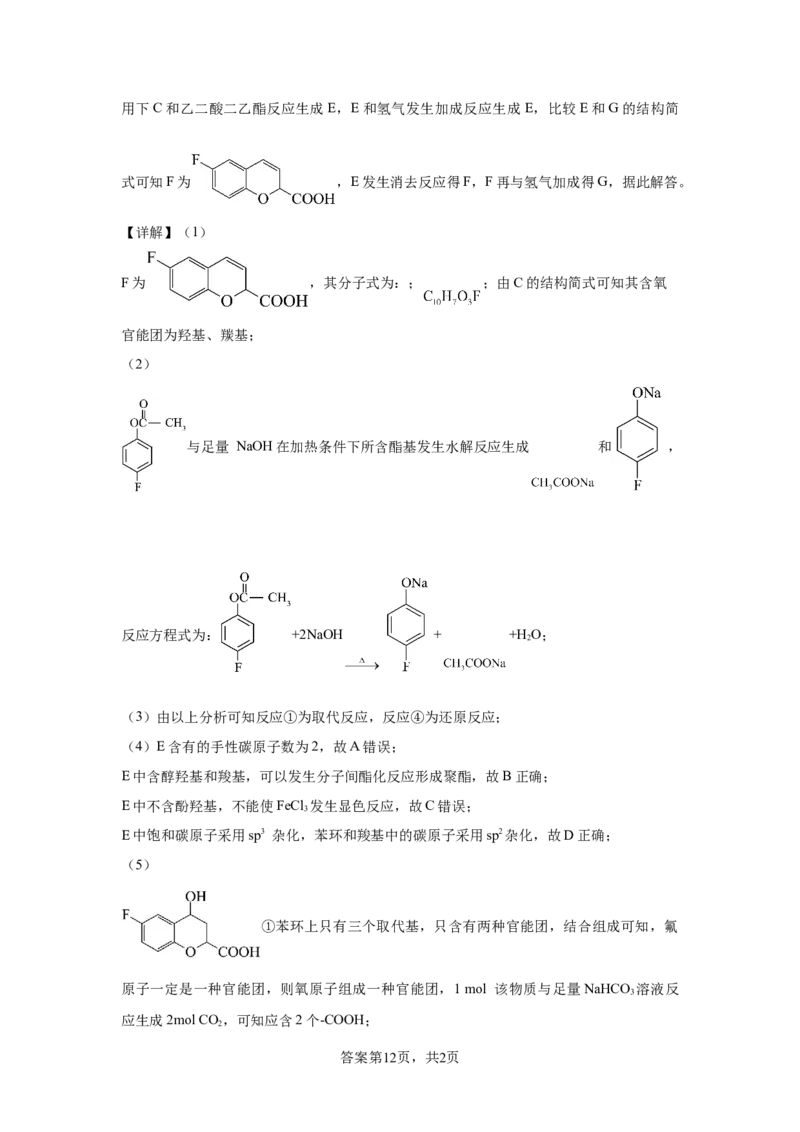
(3)由以上分析可知反应①为取代反应,反应④为还原反应;
(4)E含有的手性碳原子数为2,故A错误;
E中含醇羟基和羧基,可以发生分子间酯化反应形成聚酯,故B正确;
E中不含酚羟基,不能使FeCl 发生显色反应,故C错误;
3
E中饱和碳原子采用sp3 杂化,苯环和羧基中的碳原子采用sp2杂化,故D正确;
(5)
①苯环上只有三个取代基,只含有两种官能团,结合组成可知,氟
原子一定是一种官能团,则氧原子组成一种官能团,1 mol 该物质与足量NaHCO 溶液反
3
应生成2mol CO,可知应含2个-COOH;
2
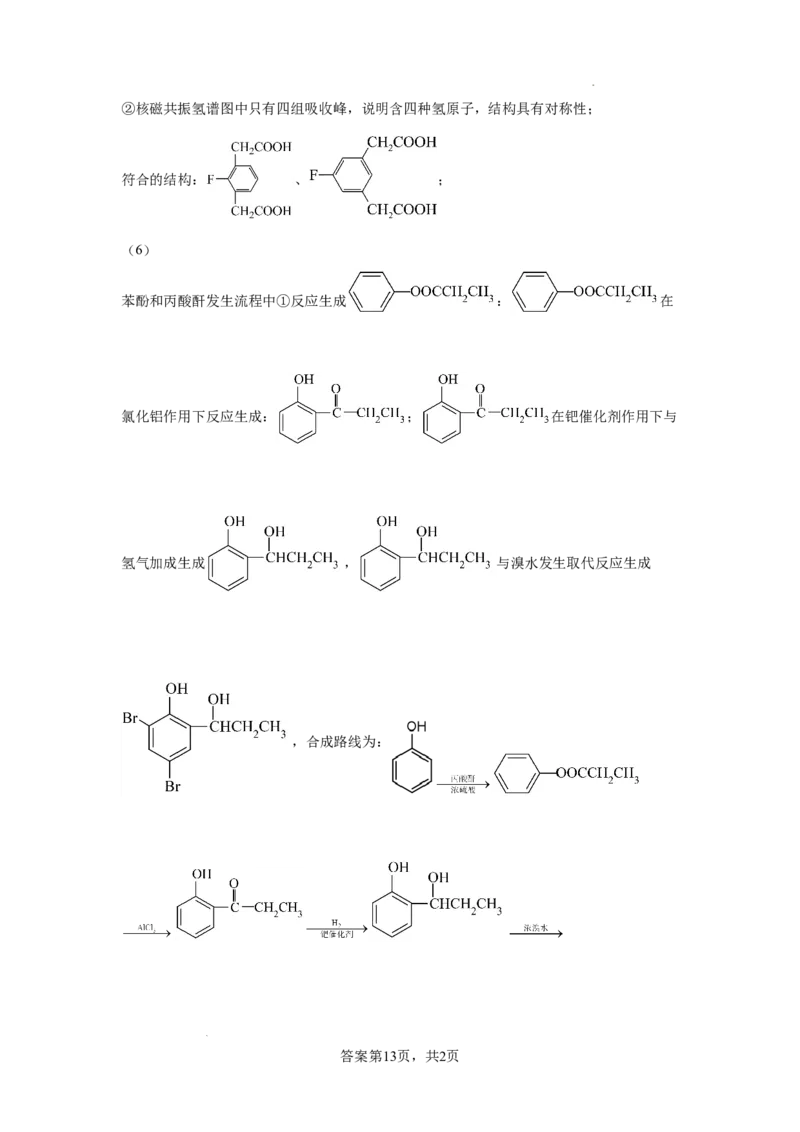
答案第12页,共2页②核磁共振氢谱图中只有四组吸收峰,说明含四种氢原子,结构具有对称性;
符合的结构: 、 ;
(6)
苯酚和丙酸酐发生流程中①反应生成 : 在
氯化铝作用下反应生成: ; 在钯催化剂作用下与
氢气加成生成 , 与溴水发生取代反应生成
,合成路线为:
答案第13页,共2页
学科网(北京)股份有限公司。
答案第14页,共2页