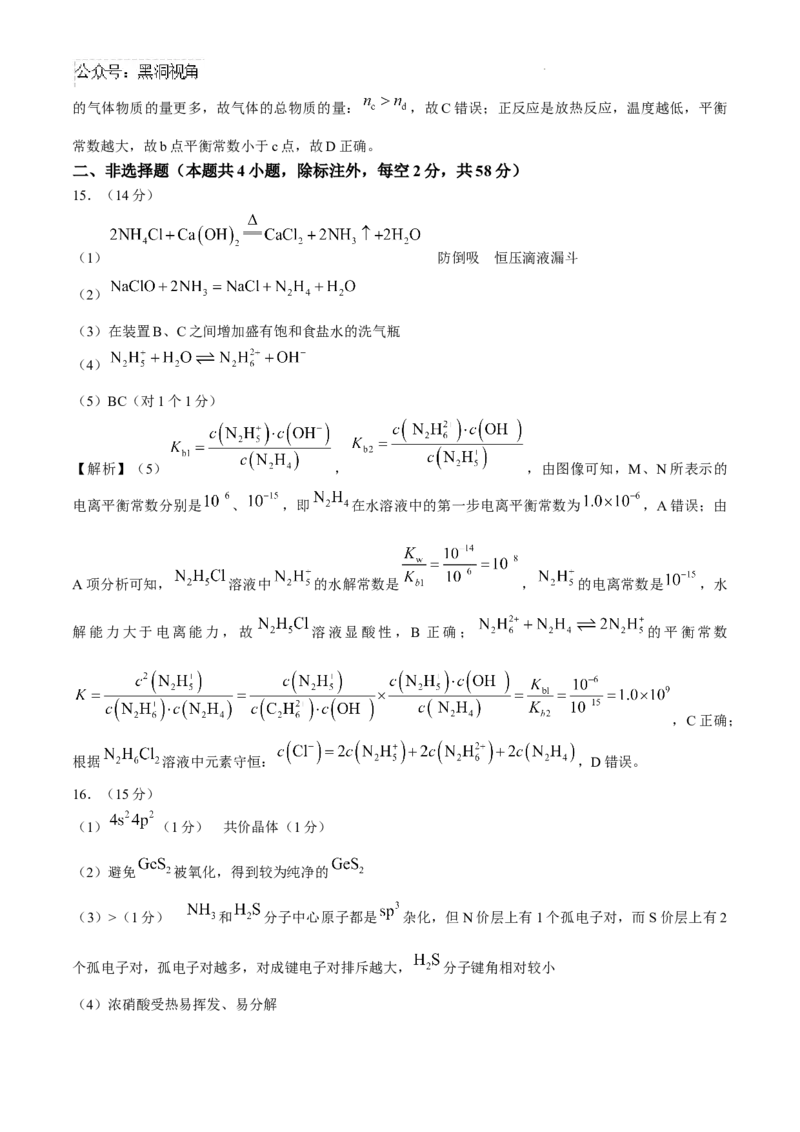文档内容
长沙市一中 2025 届高三月考试卷(一)
化学
时量:75分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Ca-40
V-51 Ge-73 Br-80
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一项符合题目要求)
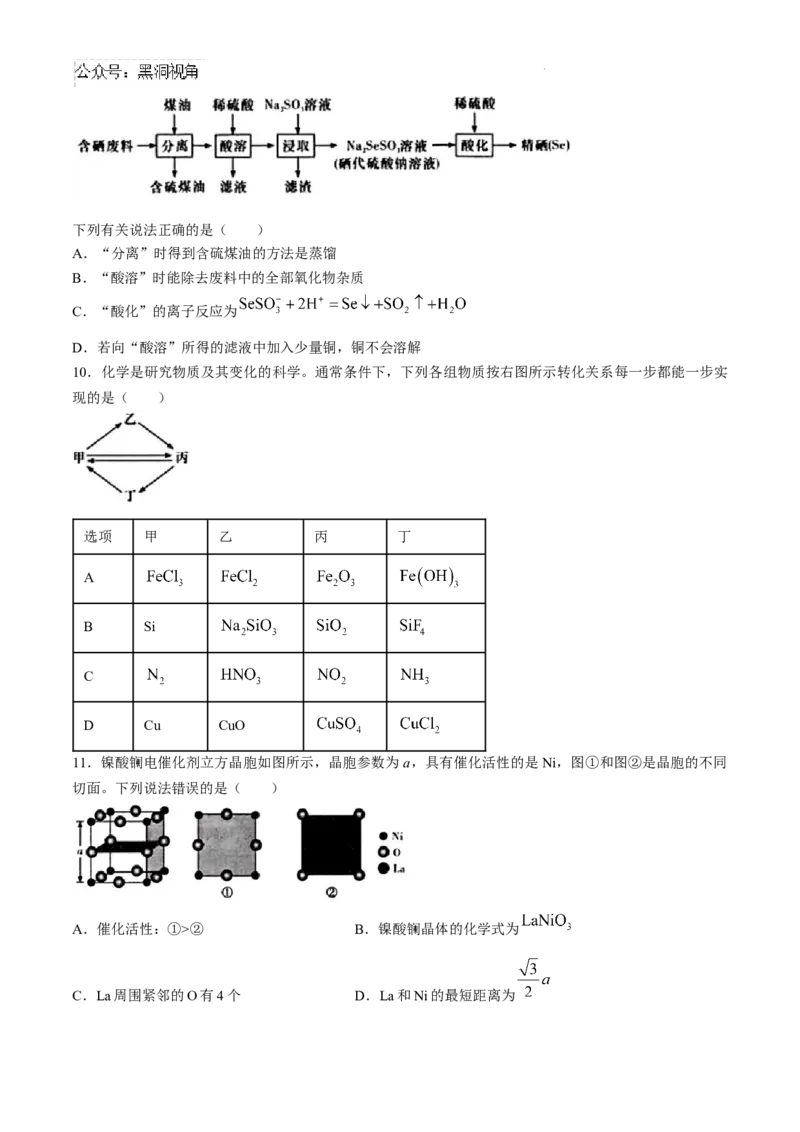
1.化学与生活密切相关,下列说法不正确的是( )
A.维生素C能帮助人体将食物中的 转化为
B.五氧化二磷可用作食品干燥剂
C.碳酸钠俗名为苏打,可用于纺织、造纸、制皂、制玻璃
D.将氯气通入冷的石灰乳中,可以制得漂白粉
2.下列化学用语表示不正确的是( )
A.乙醚的结构简式: B.HClO的电子式:
C.明矾的化学式: D. 的VSEPR模型:
3.室温下,下列各组离子一定能在指定溶液中共存的是( )
A.0.1 mol⋅L 溶液: 、 、 、
B.0.1 mol⋅L 溶液中: 、 、
C.0.2 mol⋅L 溶液: 、 、 、
D.0.2 mol⋅L 氨水中: 、 、 、
4.下列与实验相关的说法不正确的是( )
A.可用金属钠丝干燥甲苯,蒸馏得无水甲苯
B.制二氧化氮时,用水吸收尾气
C.配制溶液定容时,俯视容量瓶刻度线会使浓度偏高
D.中学实验室中可以将未用完的钠、钾、白磷放回原试剂瓶
5.设 为阿伏加德罗常数的值。下列说法正确的是( )
A.11 g的 中含有的中子数为
学科网(北京)股份有限公司B.1 L 的 溶液中 的数目为
C.将0.1 mol 通入足量 溶液中,转移电子的数目为
D.标准状况下,4.48 L甲烷与足量 完全反应生成 的分子数目为
6.下列离子方程式或电极反应式不正确的是( )
A.用铁氰化钾溶液检验亚铁离子:
B.氯化铜溶液(蓝色)加热,溶液变黄绿色:
C.电解苛性钠溶液制高铁酸盐的阳极反应式:
D.泡沫灭火器的原理:
7.短周期元素X、Y、Z、W的原子序数依次增大。X的原子核外有1个电子,Y是地壳中含量最多的元
素,Z位于元素周期表第ⅢA族,W单质可广泛用于生产芯片。下列说法正确的是( )
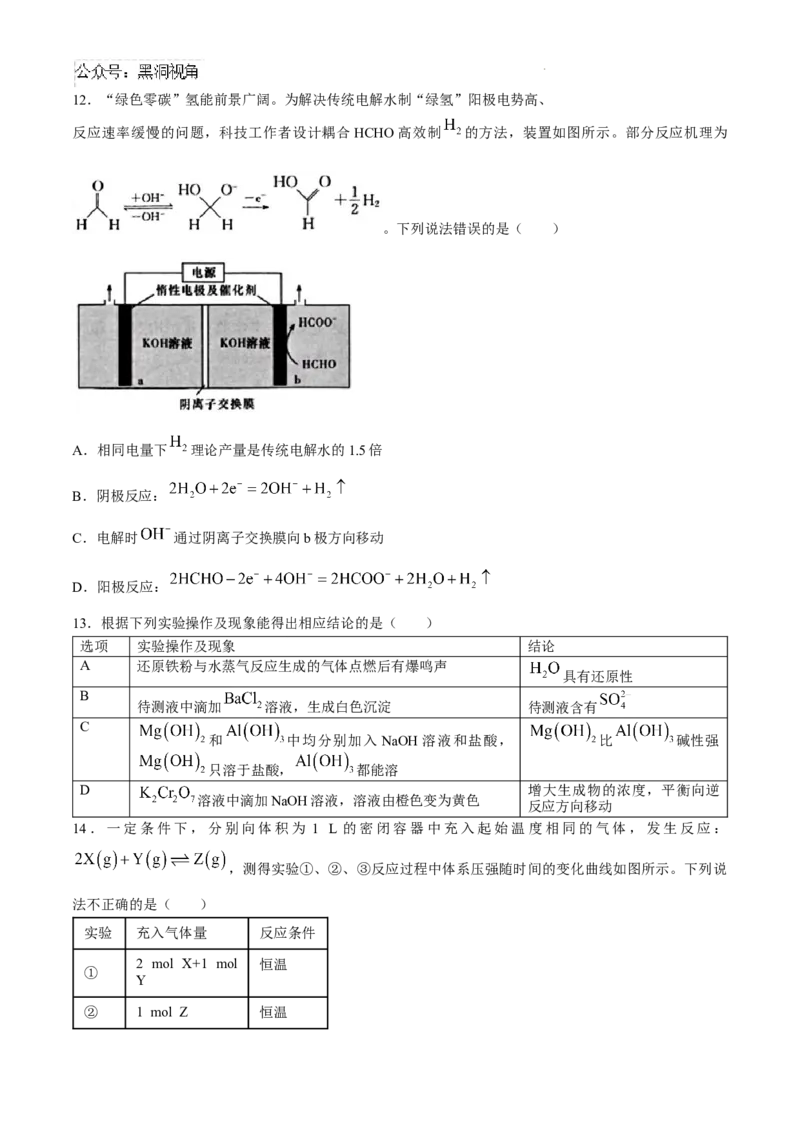
A.原子半径:Y② B.镍酸镧晶体的化学式为
C.La周围紧邻的O有4个 D.La和Ni的最短距离为
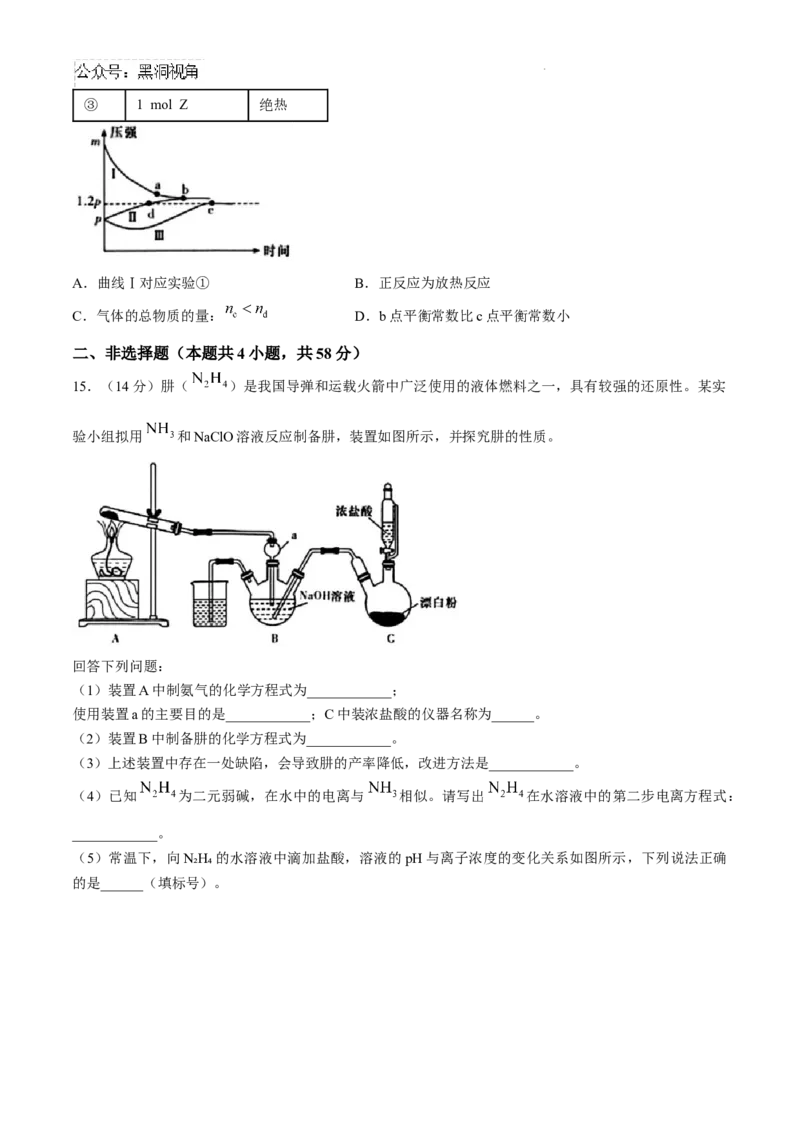
学科网(北京)股份有限公司12.“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、
反应速率缓慢的问题,科技工作者设计耦合HCHO高效制 的方法,装置如图所示。部分反应机理为
。下列说法错误的是( )
A.相同电量下 理论产量是传统电解水的1.5倍
B.阴极反应:
C.电解时 通过阴离子交换膜向b极方向移动
D.阳极反应:
13.根据下列实验操作及现象能得出相应结论的是( )
选项 实验操作及现象 结论
A 还原铁粉与水蒸气反应生成的气体点燃后有爆鸣声
具有还原性
B
待测液中滴加 溶液,生成白色沉淀 待测液含有
C
和 中均分别加入 NaOH溶液和盐酸, 比 碱性强
只溶于盐酸, 都能溶
D 增大生成物的浓度,平衡向逆
溶液中滴加NaOH溶液,溶液由橙色变为黄色
反应方向移动
14.一定条件下,分别向体积为 1 L 的密闭容器中充入起始温度相同的气体,发生反应:
,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说
法不正确的是( )
实验 充入气体量 反应条件
2 mol X+1 mol 恒温
①
Y
② 1 mol Z 恒温
学科网(北京)股份有限公司③ 1 mol Z 绝热
A.曲线Ⅰ对应实验① B.正反应为放热反应
C.气体的总物质的量: D.b点平衡常数比c点平衡常数小
二、非选择题(本题共4小题,共58分)
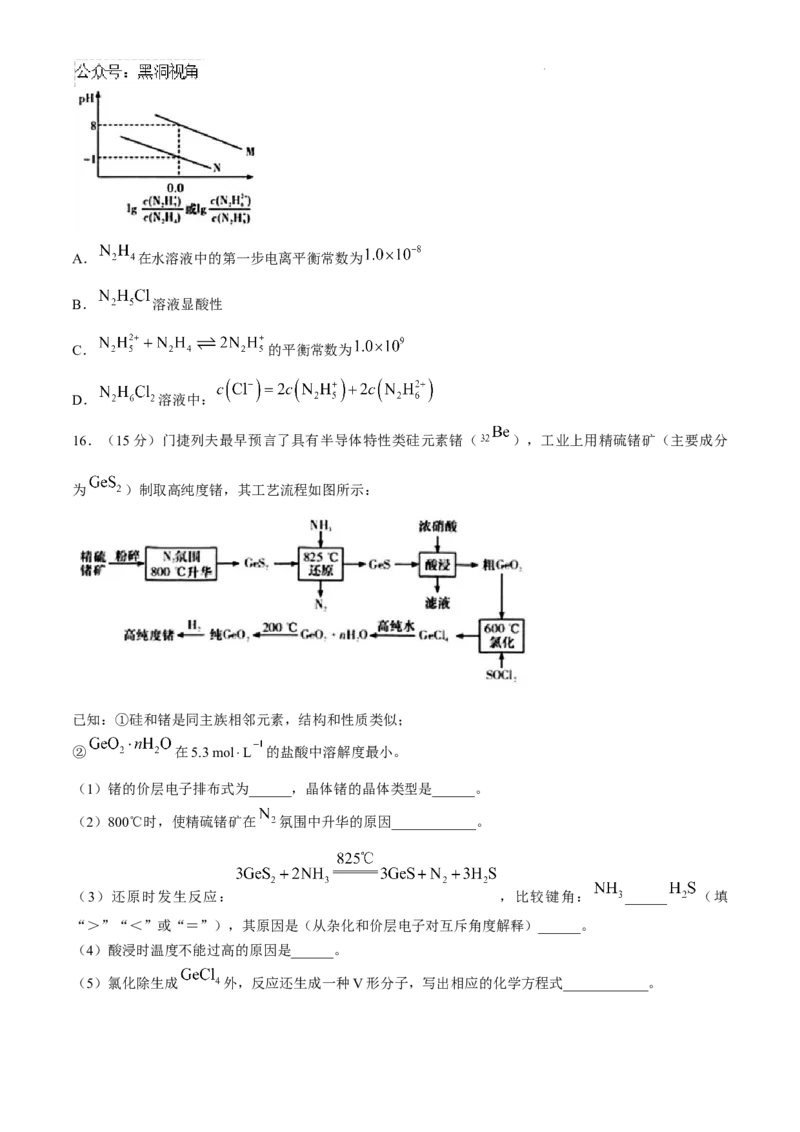
15.(14分)肼( )是我国导弹和运载火箭中广泛使用的液体燃料之一,具有较强的还原性。某实
验小组拟用 和NaClO溶液反应制备肼,装置如图所示,并探究肼的性质。
回答下列问题:
(1)装置A中制氨气的化学方程式为____________;
使用装置a的主要目的是____________;C中装浓盐酸的仪器名称为______。
(2)装置B中制备肼的化学方程式为____________。
(3)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是____________。
(4)已知 为二元弱碱,在水中的电离与 相似。请写出 在水溶液中的第二步电离方程式:
____________。
(5)常温下,向N₂H₄的水溶液中滴加盐酸,溶液的pH与离子浓度的变化关系如图所示,下列说法正确
的是______(填标号)。
学科网(北京)股份有限公司A. 在水溶液中的第一步电离平衡常数为
B. 溶液显酸性
C. 的平衡常数为
D. 溶液中:
16.(15分)门捷列夫最早预言了具有半导体特性类硅元素锗( ),工业上用精硫锗矿(主要成分
为 )制取高纯度锗,其工艺流程如图所示:
已知:①硅和锗是同主族相邻元素,结构和性质类似;
② 在5.3 mol⋅L 的盐酸中溶解度最小。
(1)锗的价层电子排布式为______,晶体锗的晶体类型是______。
(2)800℃时,使精硫锗矿在 氛围中升华的原因____________。
(3)还原时发生反应: ,比较键角: ______ (填
“>”“<”或“=”),其原因是(从杂化和价层电子对互斥角度解释)______。
(4)酸浸时温度不能过高的原因是______。
(5)氯化除生成 外,反应还生成一种V形分子,写出相应的化学方程式____________。
学科网(北京)股份有限公司(6) 水解得到 ,该步骤高纯水不能过量,原因是____________。
(7) 是一种难溶电解质,常温下的溶解度为m g/(100 g ),计算其溶度积约为______(用
含m的式子表示)。
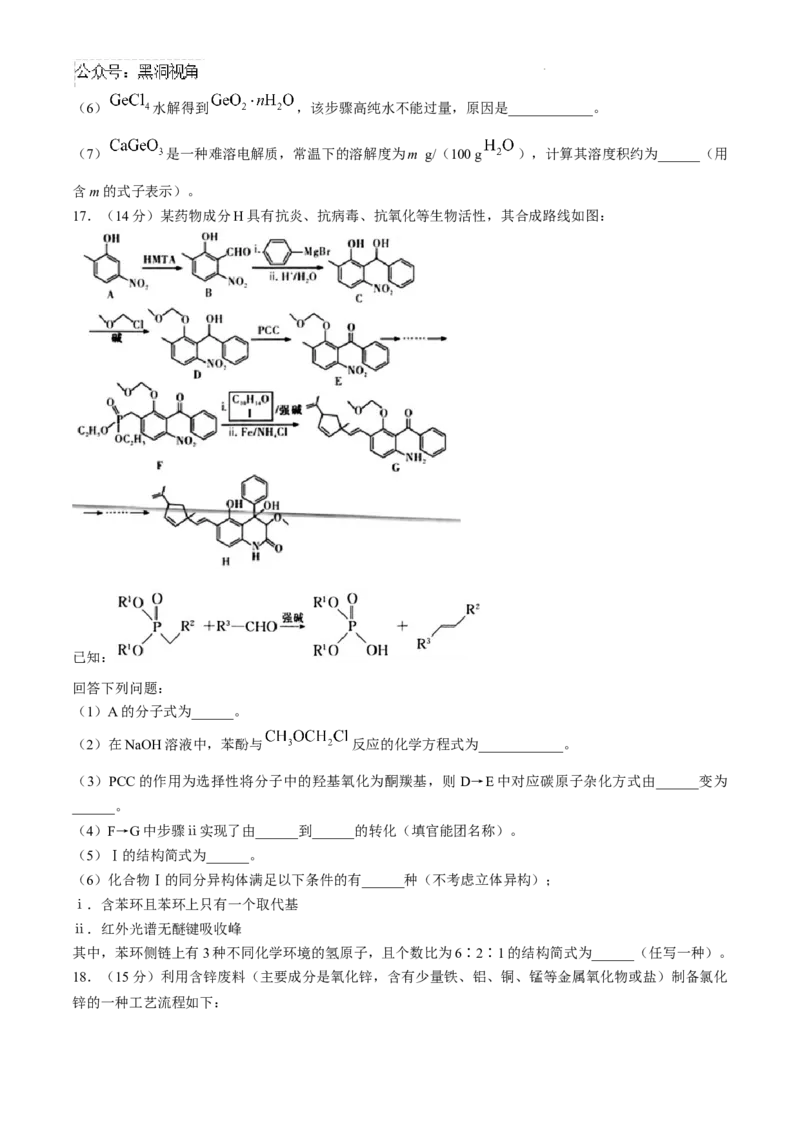
17.(14分)某药物成分H具有抗炎、抗病毒、抗氧化等生物活性,其合成路线如图:
已知:
回答下列问题:
(1)A的分子式为______。
(2)在NaOH溶液中,苯酚与 反应的化学方程式为____________。
(3)PCC的作用为选择性将分子中的羟基氧化为酮羰基,则 D→E中对应碳原子杂化方式由______变为
______。
(4)F→G中步骤ⅱ实现了由______到______的转化(填官能团名称)。
(5)Ⅰ的结构简式为______。
(6)化合物Ⅰ的同分异构体满足以下条件的有______种(不考虑立体异构);
ⅰ.含苯环且苯环上只有一个取代基
ⅱ.红外光谱无醚键吸收峰
其中,苯环侧链上有3种不同化学环境的氢原子,且个数比为6∶2∶1的结构简式为______(任写一种)。
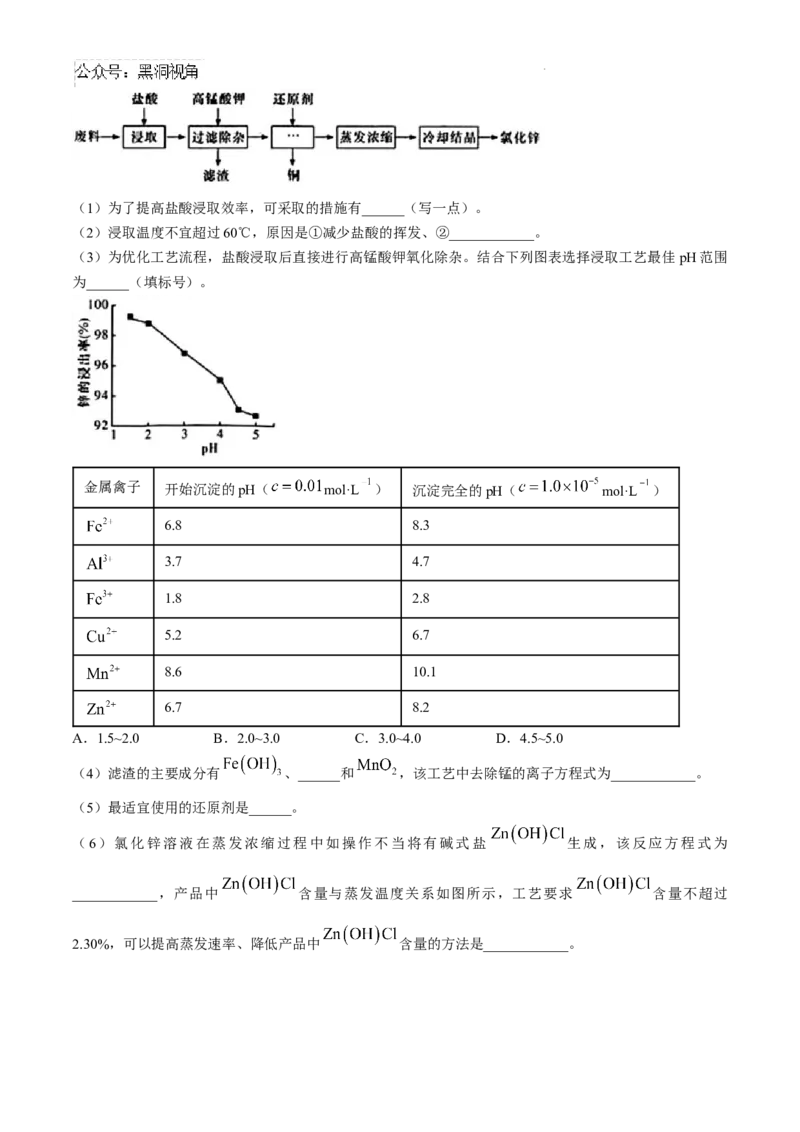
18.(15分)利用含锌废料(主要成分是氧化锌,含有少量铁、铝、铜、锰等金属氧化物或盐)制备氯化
锌的一种工艺流程如下:
学科网(北京)股份有限公司(1)为了提高盐酸浸取效率,可采取的措施有______(写一点)。
(2)浸取温度不宜超过60℃,原因是①减少盐酸的挥发、②____________。
(3)为优化工艺流程,盐酸浸取后直接进行高锰酸钾氧化除杂。结合下列图表选择浸取工艺最佳 pH范围
为______(填标号)。
金属禽子 开始沉淀的pH( mol·L ) 沉淀完全的pH( mol·L )
6.8 8.3
3.7 4.7
1.8 2.8
5.2 6.7
8.6 10.1
6.7 8.2
A.1.5~2.0 B.2.0~3.0 C.3.0~4.0 D.4.5~5.0
(4)滤渣的主要成分有 、______和 ,该工艺中去除锰的离子方程式为____________。
(5)最适宜使用的还原剂是______。
(6)氯化锌溶液在蒸发浓缩过程中如操作不当将有碱式盐 生成,该反应方程式为
____________,产品中 含量与蒸发温度关系如图所示,工艺要求 含量不超过
2.30%,可以提高蒸发速率、降低产品中 含量的方法是____________。
学科网(北京)股份有限公司长沙市一中 2025 届高三月考试卷(一)
化学参考答案
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一项符合题目要求)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 B A A B C C D D C D C A C C
1.B【解析】B. 吸水后的产物有毒,不能用作食品干燥剂。
2.A【解析】A.乙醚的结构简式为 。
4.B【解析】B.用水吸收会产生NO。
6.C【解析】C.电解苛性钠溶液制高铁酸盐的阳极反应: 。
11.C【解析】具有催化活性的是Ni,图②中没有Ni原子,则催化活性:①>②,故A正确;镍酸镧电催
化剂立方晶胞中含有1个Ni, 个O, 个La,镍酸镧晶体的化学式为 ,故B正
确;由晶胞结构可知,La在晶胞的体心,O在晶胞的棱心,则La周围紧邻的O有12个,故C错误;由晶
胞结构可知,La和Ni的最短距离为体对角线的一半,为 ,故D正确。
14.C【解析】恒温恒容条件下,气体的压强之比等于气体物质的量之比,故起始时实验②与实验③的压
强相等,实验①的压强是实验②与实验③的3倍,则曲线Ⅰ对应实验①,且 ,故A正确;实验①
与实验②的温度相等,根据等效平衡可知,实验①与实验②最终会达到相同的平衡状态,故曲线Ⅱ对应实
验②,则曲线Ⅲ对应实验③,实验②与实验③充入的Z一样多,实验③比实验②达到平衡所用的时间长,
则Z的分解反应是吸热反应,随反应的进行,实验③温度降低,反应速率减慢,故正反应是放热反应,故
B正确;根据 ,c、d两点的压强相同,V相同,由于反应吸热,c点的温度比d点低,则c点
学科网(北京)股份有限公司的气体物质的量更多,故气体的总物质的量: ,故C错误;正反应是放热反应,温度越低,平衡
常数越大,故b点平衡常数小于c点,故D正确。
二、非选择题(本题共4小题,除标注外,每空2分,共58分)
15.(14分)
(1) 防倒吸 恒压滴液漏斗
(2)
(3)在装置B、C之间增加盛有饱和食盐水的洗气瓶
(4)
(5)BC(对1个1分)
【解析】(5) , ,由图像可知,M、N所表示的
电离平衡常数分别是 、 ,即 在水溶液中的第一步电离平衡常数为 ,A错误;由
A项分析可知, 溶液中 的水解常数是 , 的电离常数是 ,水
解能力大于电离能力,故 溶液显酸性,B 正确; 的平衡常数
,C正确;
根据 溶液中元素守恒: ,D错误。
16.(15分)
(1) (1分) 共价晶体(1分)
(2)避免 被氧化,得到较为纯净的
(3)>(1分) 和 分子中心原子都是 杂化,但N价层上有1个孤电子对,而S价层上有2
个孤电子对,孤电子对越多,对成键电子对排斥越大, 分子键角相对较小
(4)浓硝酸受热易挥发、易分解
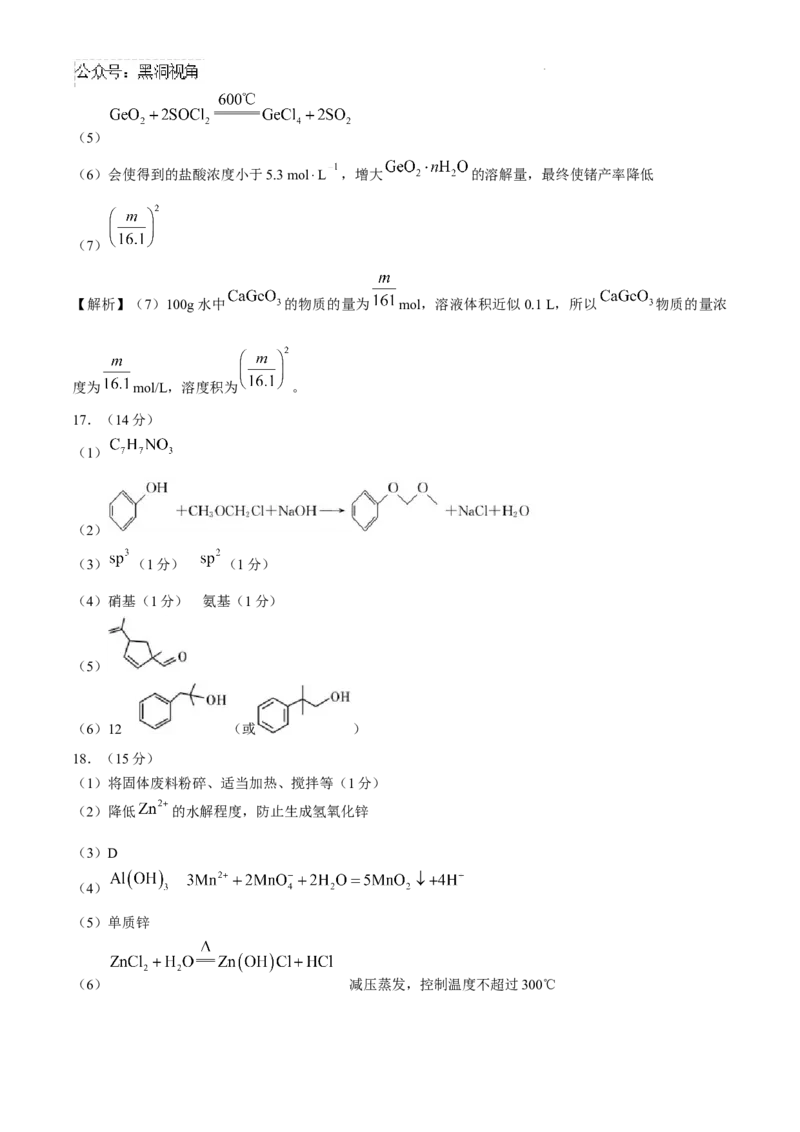
学科网(北京)股份有限公司(5)
(6)会使得到的盐酸浓度小于5.3 mol⋅L ,增大 的溶解量,最终使锗产率降低
(7)
【解析】(7)100g水中 的物质的量为 mol,溶液体积近似0.1 L,所以 物质的量浓
度为 mol/L,溶度积为 。
17.(14分)
(1)
(2)
(3) (1分) (1分)
(4)硝基(1分) 氨基(1分)
(5)
(6)12 (或 )
18.(15分)
(1)将固体废料粉碎、适当加热、搅拌等(1分)
(2)降低 的水解程度,防止生成氢氧化锌
(3)D
(4)
(5)单质锌
(6) 减压蒸发,控制温度不超过300℃
学科网(北京)股份有限公司