文档内容
郑州外国语学校 2025-2026 学年高二上期月考 1 试卷化学
(75分钟 100分)
可能用到的相对原子质量: 、 、 、 、 、
一、选择题(每小题只有一个正确选项,每小题3分,共48分)
1.下列生产活动体现了我国古代劳动人民的智慧。其中目的是减慢化学反应速率的是
A.地窖存粮 B.加酒曲酿酒
C.高温烧陶 D.风箱鼓风煮饭
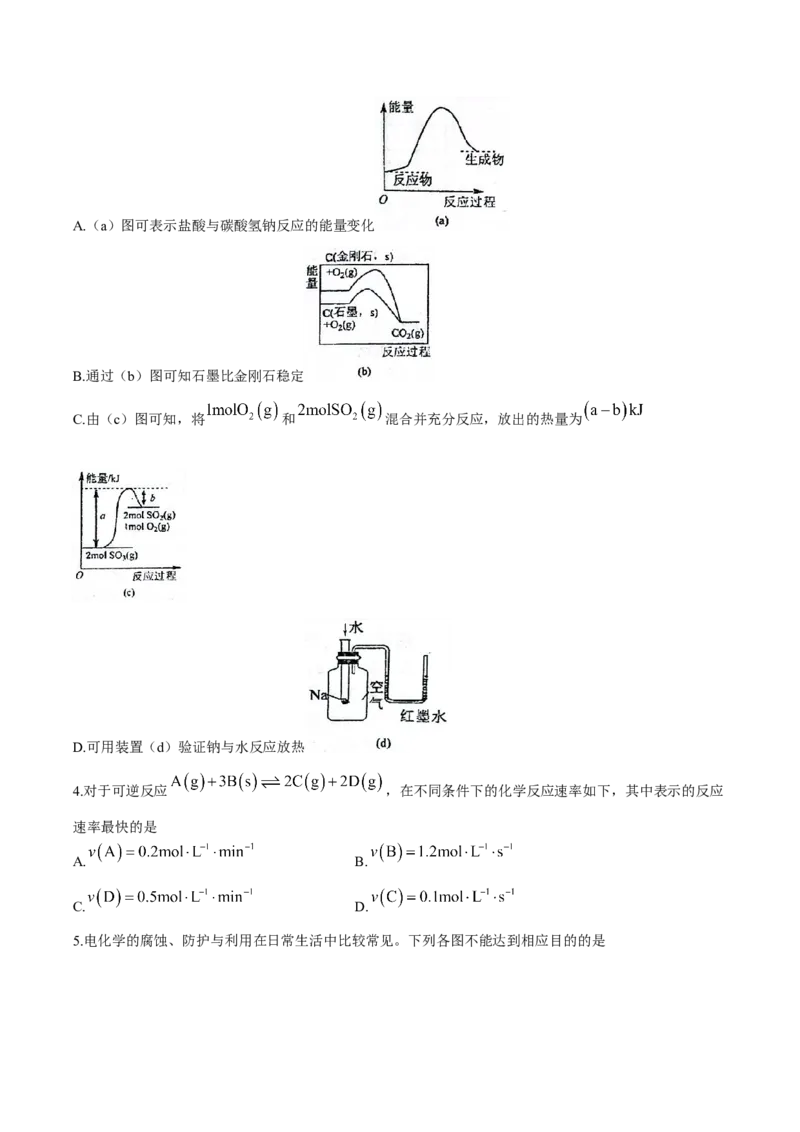
2. 可活化 放出 ,其反应历程如图所示:
下列关于该活化历程的说法正确的是
A.恒容条件下,充入稀有气体使体系压强增大,可加快化学反应速率
B.该反应的决速步是中间体2→中间体3
C. 是该反应的催化剂,可增大单位体积内活化分子百分数
D.该反应的热化学方程式为:
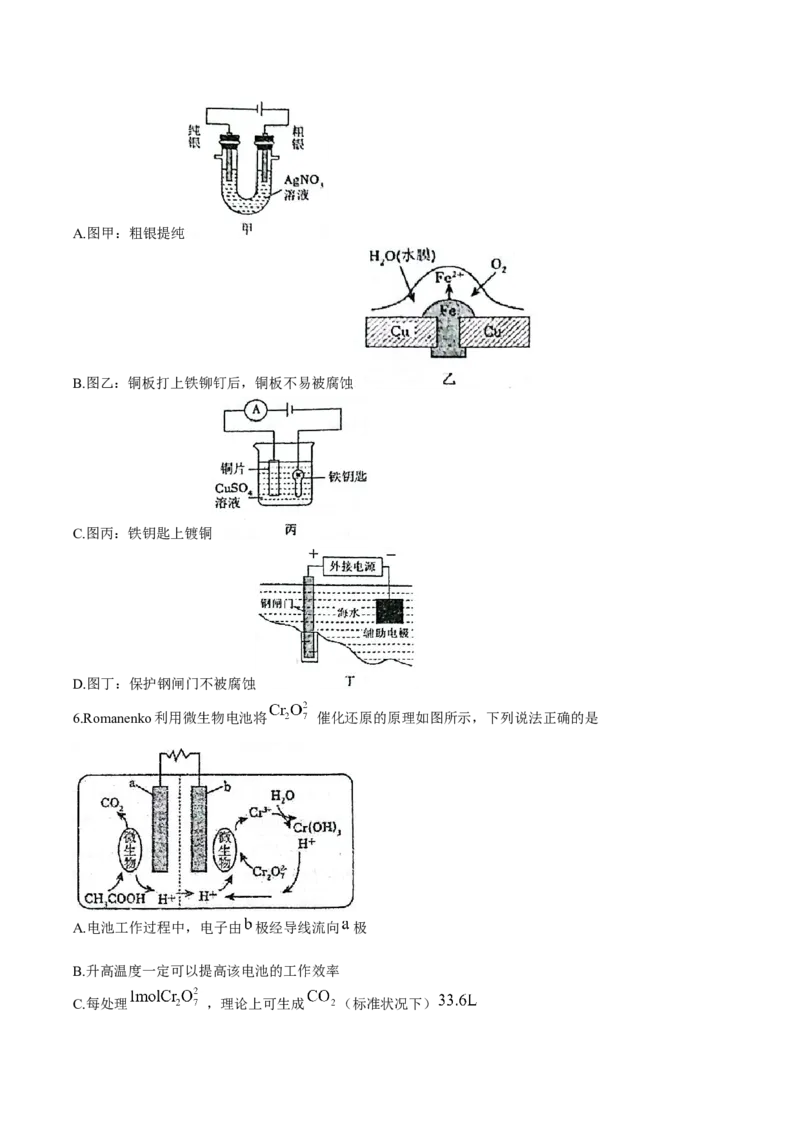
3.下列图示与对应的叙述不相符的是A.(a)图可表示盐酸与碳酸氢钠反应的能量变化
B.通过(b)图可知石墨比金刚石稳定
C.由(c)图可知,将 和 混合并充分反应,放出的热量为
D.可用装置(d)验证钠与水反应放热
4.对于可逆反应 ,在不同条件下的化学反应速率如下,其中表示的反应
速率最快的是
A. B.
C. D.
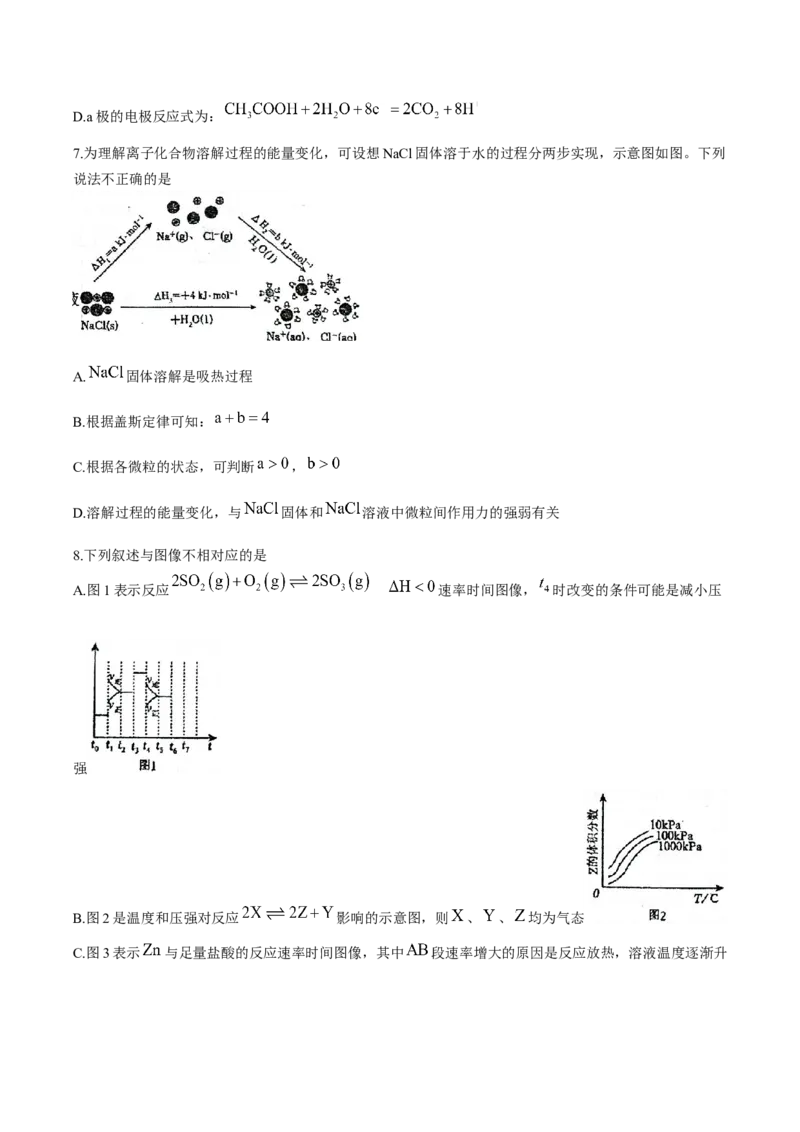
5.电化学的腐蚀、防护与利用在日常生活中比较常见。下列各图不能达到相应目的的是A.图甲:粗银提纯
B.图乙:铜板打上铁铆钉后,铜板不易被腐蚀
C.图丙:铁钥匙上镀铜
D.图丁:保护钢闸门不被腐蚀
6.Romanenko利用微生物电池将 催化还原的原理如图所示,下列说法正确的是
A.电池工作过程中,电子由 极经导线流向 极
B.升高温度一定可以提高该电池的工作效率
C.每处理 ,理论上可生成 (标准状况下)D.a极的电极反应式为:
7.为理解离子化合物溶解过程的能量变化,可设想NaCl固体溶于水的过程分两步实现,示意图如图。下列
说法不正确的是
A. 固体溶解是吸热过程
B.根据盖斯定律可知:
C.根据各微粒的状态,可判断 ,
D.溶解过程的能量变化,与 固体和 溶液中微粒间作用力的强弱有关
8.下列叙述与图像不相对应的是
A.图1表示反应 速率时间图像, 时改变的条件可能是减小压
强
B.图2是温度和压强对反应 影响的示意图,则 、 、 均为气态
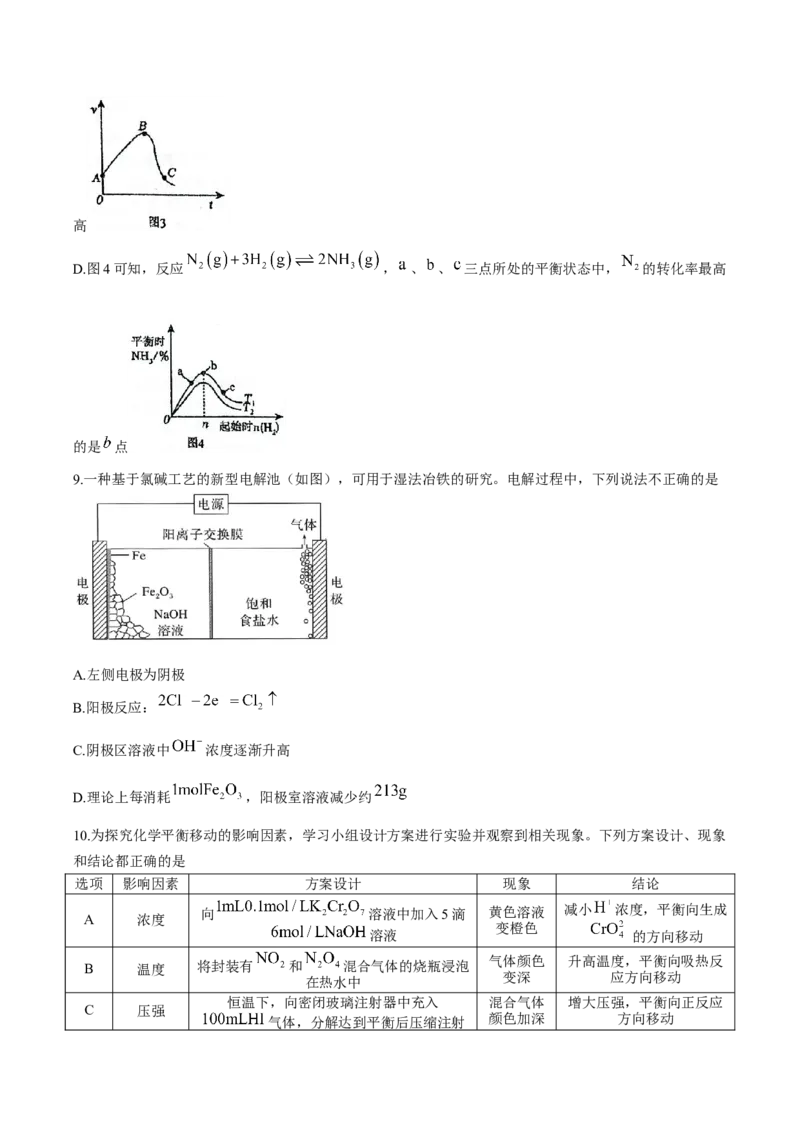
C.图3表示 与足量盐酸的反应速率时间图像,其中 段速率增大的原因是反应放热,溶液温度逐渐升高
D.图4可知,反应 , 、 、 三点所处的平衡状态中, 的转化率最高
的是 点
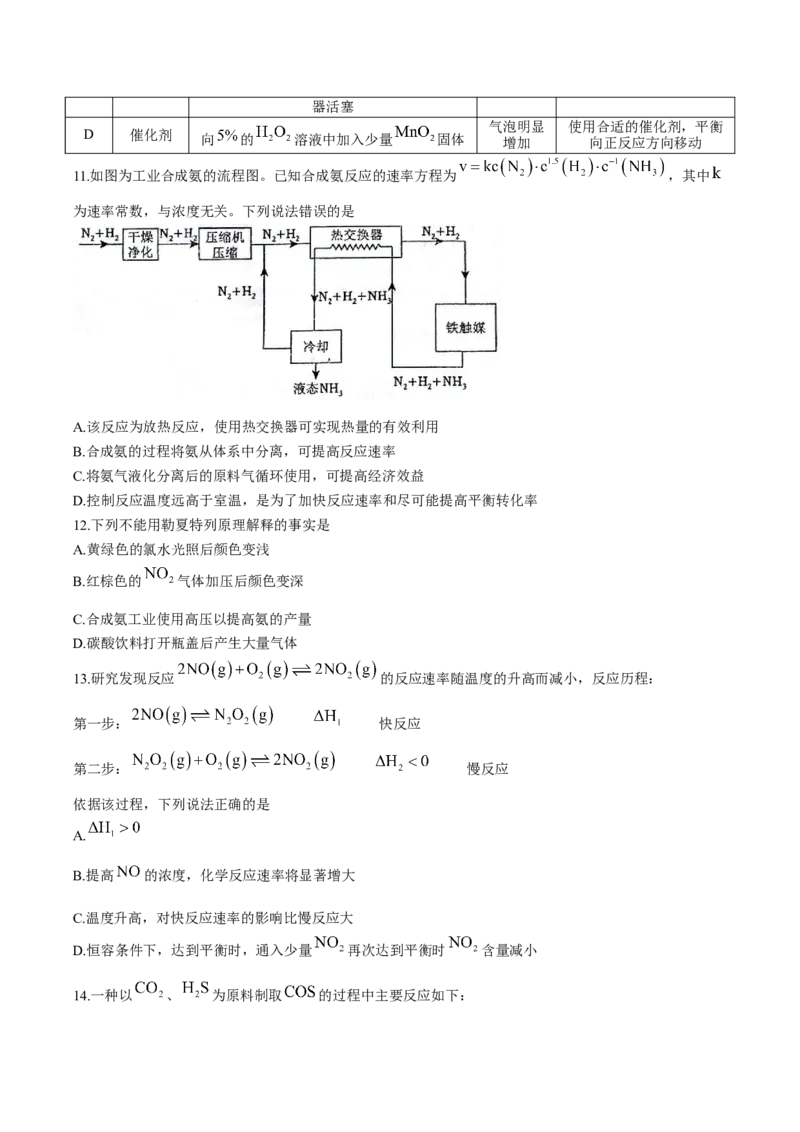
9.一种基于氯碱工艺的新型电解池(如图),可用于湿法冶铁的研究。电解过程中,下列说法不正确的是
A.左侧电极为阴极
B.阳极反应:
C.阴极区溶液中 浓度逐渐升高
D.理论上每消耗 ,阳极室溶液减少约
10.为探究化学平衡移动的影响因素,学习小组设计方案进行实验并观察到相关现象。下列方案设计、现象
和结论都正确的是
选项 影响因素 方案设计 现象 结论
向 溶液中加入5滴 黄色溶液 减小 浓度,平衡向生成
A 浓度
变橙色
溶液 的方向移动
气体颜色 升高温度,平衡向吸热反
B 温度 将封装有 和 混合气体的烧瓶浸泡
变深 应方向移动
在热水中
恒温下,向密闭玻璃注射器中充入 混合气体 增大压强,平衡向正反应
C 压强
气体,分解达到平衡后压缩注射 颜色加深 方向移动器活塞
气泡明显 使用合适的催化剂,平衡
D 催化剂
向 的 溶液中加入少量 固体 增加 向正反应方向移动
11.如图为工业合成氨的流程图。已知合成氨反应的速率方程为 ,其中
为速率常数,与浓度无关。下列说法错误的是
A.该反应为放热反应,使用热交换器可实现热量的有效利用
B.合成氨的过程将氨从体系中分离,可提高反应速率
C.将氨气液化分离后的原料气循环使用,可提高经济效益
D.控制反应温度远高于室温,是为了加快反应速率和尽可能提高平衡转化率
12.下列不能用勒夏特列原理解释的事实是
A.黄绿色的氯水光照后颜色变浅
B.红棕色的 气体加压后颜色变深
C.合成氨工业使用高压以提高氨的产量
D.碳酸饮料打开瓶盖后产生大量气体
13.研究发现反应 的反应速率随温度的升高而减小,反应历程:
第一步: 快反应
第二步: 慢反应
依据该过程,下列说法正确的是
A.
B.提高 的浓度,化学反应速率将显著增大
C.温度升高,对快反应速率的影响比慢反应大
D.恒容条件下,达到平衡时,通入少量 再次达到平衡时 含量减小
14.一种以 、 为原料制取 的过程中主要反应如下:反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
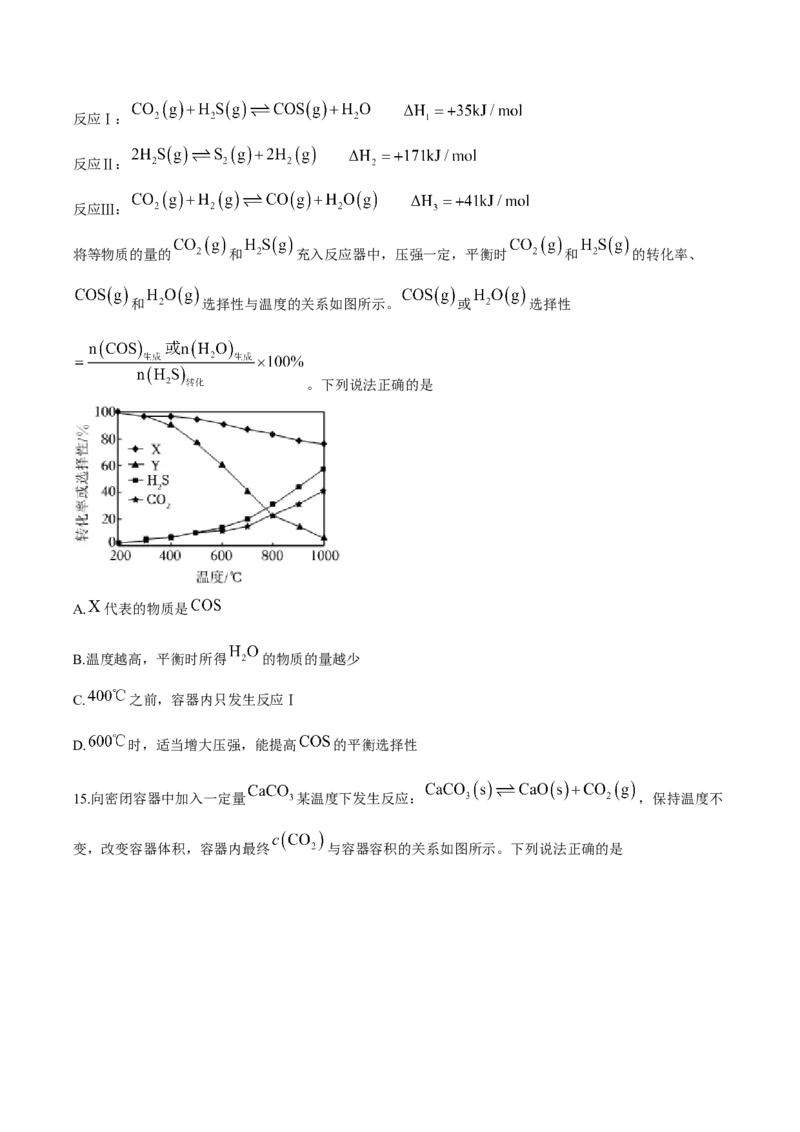
将等物质的量的 和 充入反应器中,压强一定,平衡时 和 的转化率、
和 选择性与温度的关系如图所示。 或 选择性
。下列说法正确的是
A. 代表的物质是
B.温度越高,平衡时所得 的物质的量越少
C. 之前,容器内只发生反应Ⅰ
D. 时,适当增大压强,能提高 的平衡选择性
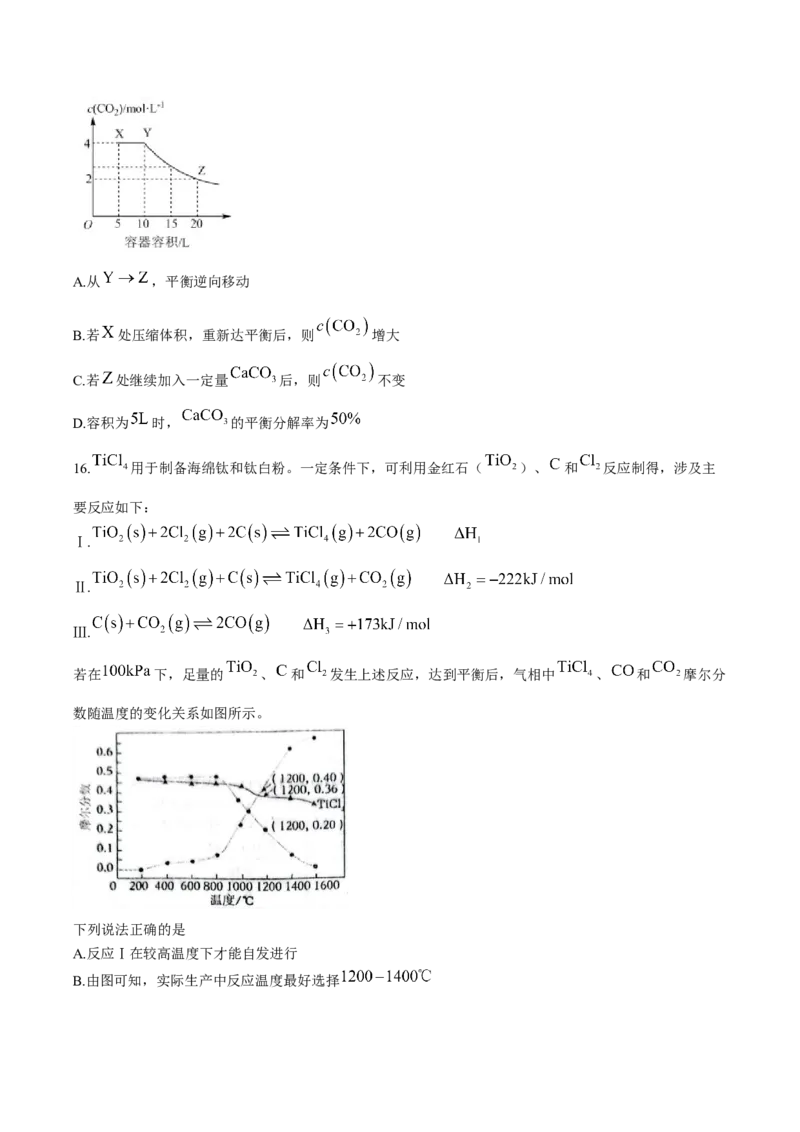
15.向密闭容器中加入一定量 某温度下发生反应: ,保持温度不
变,改变容器体积,容器内最终 与容器容积的关系如图所示。下列说法正确的是A.从 ,平衡逆向移动
B.若 处压缩体积,重新达平衡后,则 增大
C.若 处继续加入一定量 后,则 不变
D.容积为 时, 的平衡分解率为
16. 用于制备海绵钛和钛白粉。一定条件下,可利用金红石( )、 和 反应制得,涉及主
要反应如下:
Ⅰ.
Ⅱ.
Ⅲ.
若在 下,足量的 、 和 发生上述反应,达到平衡后,气相中 、 和 摩尔分
数随温度的变化关系如图所示。
下列说法正确的是
A.反应Ⅰ在较高温度下才能自发进行
B.由图可知,实际生产中反应温度最好选择C. 时,若向平衡体系中再通入少量 , 的平衡转化率不变
D. 时,反应I的平衡常数
二、填空题(共52分)
17.“水是生命之源”。回答下列问题:
(1)某些共价化合物(如 、 、 等)在液态时会发生微弱的电离,如:
,则液态 电离的方程式是__________________________________。
(2) 时,0.100 mol/L的NaOH溶液中由水电离出的 _____,向其中加入0.100 mol/L的盐
酸直至过量,水的电离程度变化情况为________________________________________。
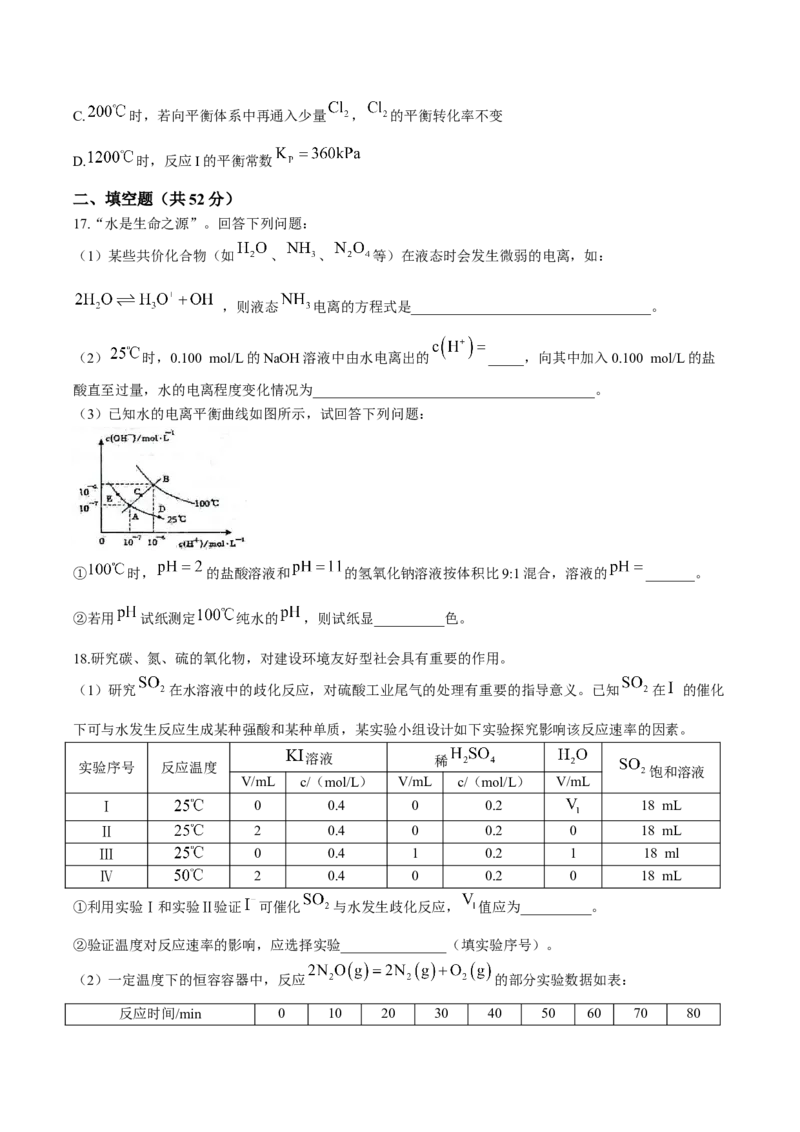
(3)已知水的电离平衡曲线如图所示,试回答下列问题:
① 时, 的盐酸溶液和 的氢氧化钠溶液按体积比9:1混合,溶液的 _______。
②若用 试纸测定 纯水的 ,则试纸显__________色。
18.研究碳、氮、硫的氧化物,对建设环境友好型社会具有重要的作用。
(1)研究 在水溶液中的歧化反应,对硫酸工业尾气的处理有重要的指导意义。已知 在 的催化
下可与水发生反应生成某种强酸和某种单质,某实验小组设计如下实验探究影响该反应速率的因素。
溶液 稀
实验序号 反应温度
饱和溶液
V/mL c/(mol/L) V/mL c/(mol/L) V/mL
Ⅰ 0 0.4 0 0.2 18 mL
Ⅱ 2 0.4 0 0.2 0 18 mL
Ⅲ 0 0.4 1 0.2 1 18 ml
Ⅳ 2 0.4 0 0.2 0 18 mL
①利用实验Ⅰ和实验Ⅱ验证 可催化 与水发生歧化反应, 值应为__________。
②验证温度对反应速率的影响,应选择实验_______________(填实验序号)。
(2)一定温度下的恒容容器中,反应 的部分实验数据如表:
反应时间/min 0 10 20 30 40 50 60 70 800.10 0.09 0.08 0.07 0.06 0.05 a 0.03 0.02
①根据表格中的数据推测 _____。
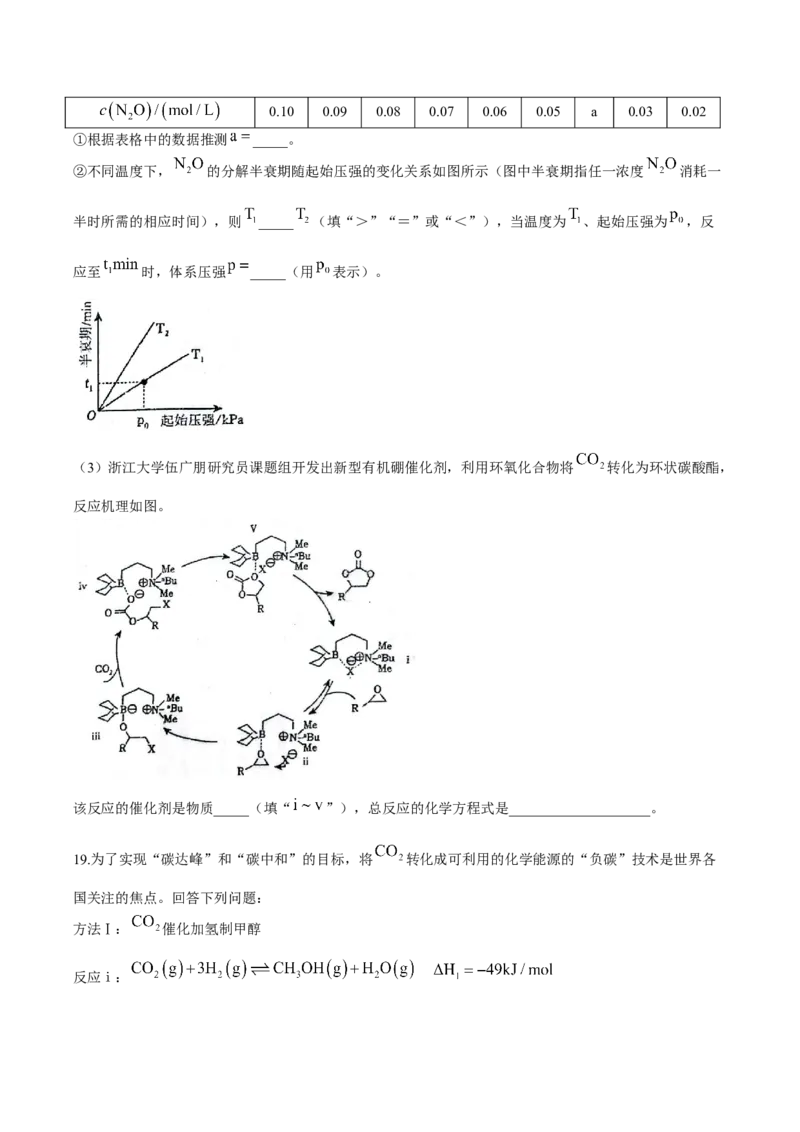
②不同温度下, 的分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一
半时所需的相应时间),则 _____ (填“>”“=”或“<”),当温度为 、起始压强为 ,反
应至 时,体系压强 _____(用 表示)。
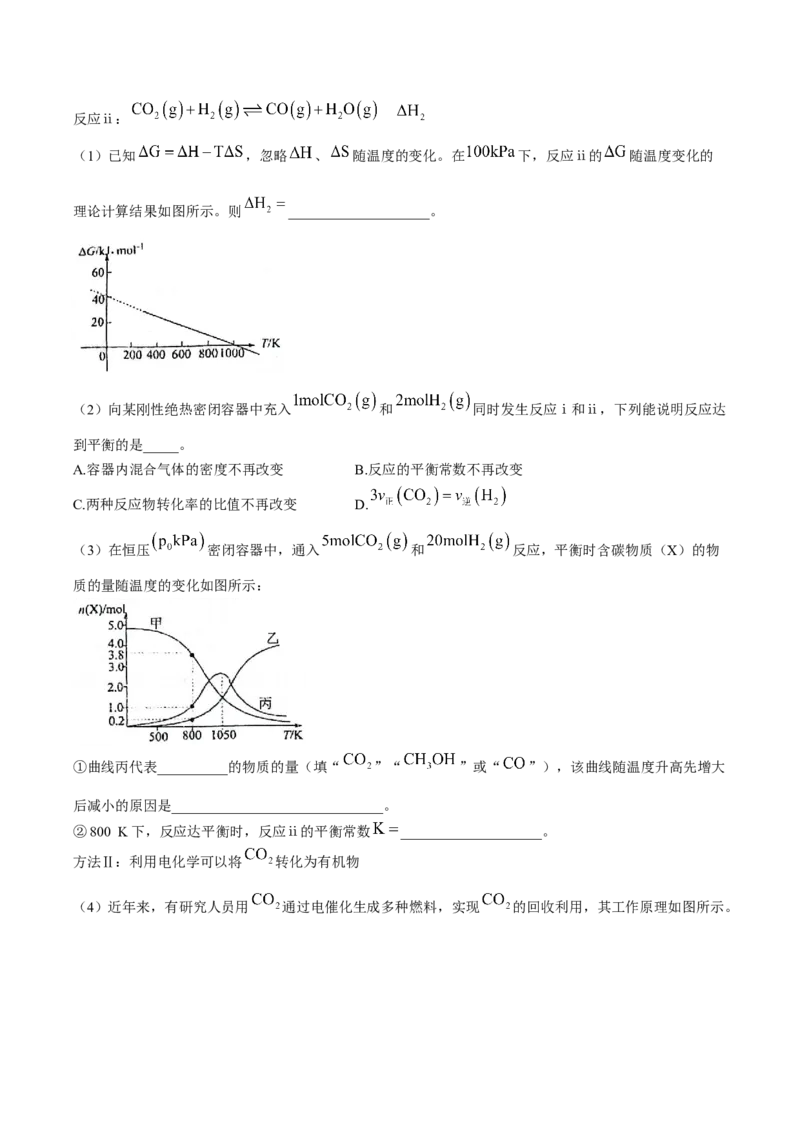
(3)浙江大学伍广朋研究员课题组开发出新型有机硼催化剂,利用环氧化合物将 转化为环状碳酸酯,
反应机理如图。
该反应的催化剂是物质_____(填“ ”),总反应的化学方程式是____________________。
19.为了实现“碳达峰”和“碳中和”的目标,将 转化成可利用的化学能源的“负碳”技术是世界各
国关注的焦点。回答下列问题:
方法Ⅰ: 催化加氢制甲醇
反应ⅰ:反应ⅱ:
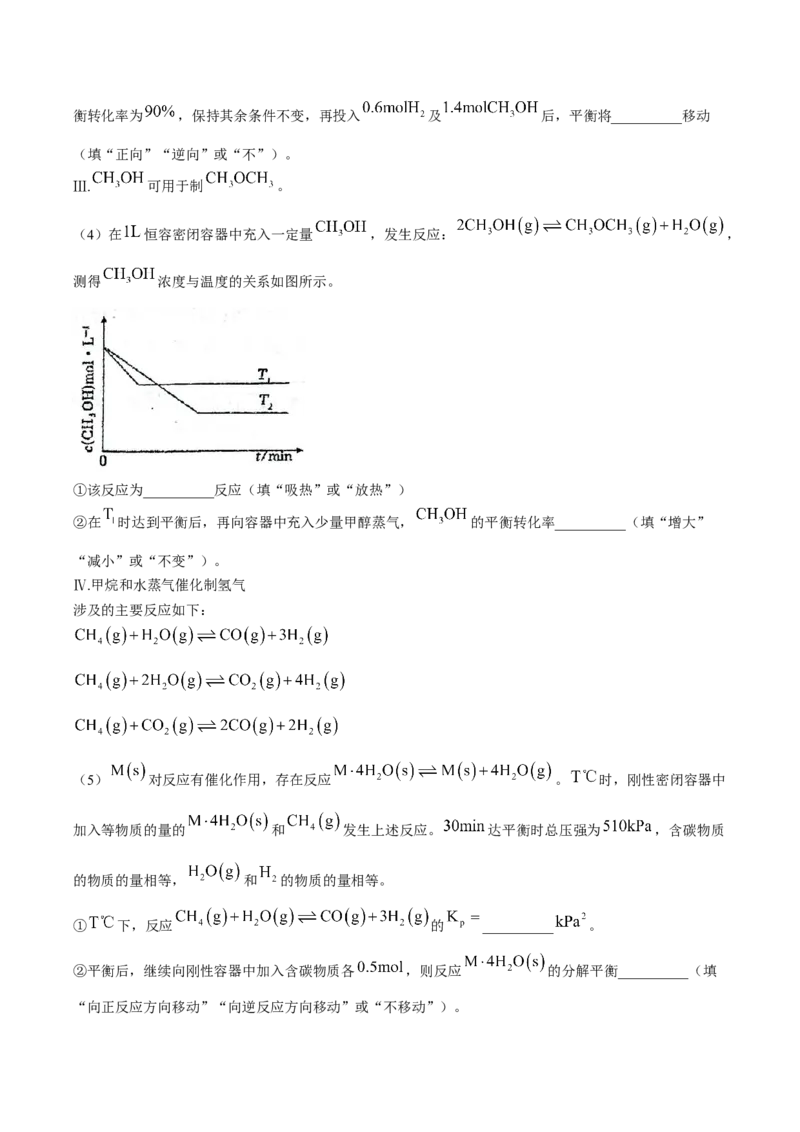
(1)已知 ,忽略 、 随温度的变化。在 下,反应ⅱ的 随温度变化的
理论计算结果如图所示。则 ____________________。
(2)向某刚性绝热密闭容器中充入 和 同时发生反应ⅰ和ⅱ,下列能说明反应达
到平衡的是_____。
A.容器内混合气体的密度不再改变 B.反应的平衡常数不再改变
C.两种反应物转化率的比值不再改变 D.
(3)在恒压 密闭容器中,通入 和 反应,平衡时含碳物质(X)的物
质的量随温度的变化如图所示:
①曲线丙代表__________的物质的量(填“ ”“ ”或“ ”),该曲线随温度升高先增大
后减小的原因是______________________________。
②800 K下,反应达平衡时,反应ⅱ的平衡常数 ____________________。
方法Ⅱ:利用电化学可以将 转化为有机物
(4)近年来,有研究人员用 通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示。①请写出 电极上产生 的电极反应式____________________。
②如果 电极上恰好只生成 和 ,则 电极上产生 的物质的量为
__________ 。
20.“一碳化学”是研究以含有一个碳原子的物质( 、 、 、 等)为原料合成化工产
品或液体燃料等。回答下列问题:
Ⅰ. 催化加氢法制乙烯:
已知: 、 的燃烧热分别为 、 ;
(1)该反应 __________ 。
Ⅱ.利用合成气合成甲醇:
(2)某温度、催化剂作用下,该反应的速率方程为 ( 为速率常数,与温度、催化
剂有关,与浓度无关)。测得速率与 、 的浓度关系如下表所示:
实
C(CO)/mol/L 速率
验
① 0.10 0.10
② 0.20 0.10
③ 0.20 0.20
④ 0.40
计算 __________。
(3)在一定温度下体积为 的恒容密闭容器中,投入 和 ,经过 达平衡, 平衡转化率为 ,保持其余条件不变,再投入 及 后,平衡将__________移动
(填“正向”“逆向”或“不”)。
Ⅲ. 可用于制 。
(4)在 恒容密闭容器中充入一定量 ,发生反应: ,
测得 浓度与温度的关系如图所示。
①该反应为__________反应(填“吸热”或“放热”)
②在 时达到平衡后,再向容器中充入少量甲醇蒸气, 的平衡转化率__________(填“增大”
“减小”或“不变”)。
Ⅳ.甲烷和水蒸气催化制氢气
涉及的主要反应如下:
(5) 对反应有催化作用,存在反应 。 时,刚性密闭容器中
加入等物质的量的 和 发生上述反应。 达平衡时总压强为 ,含碳物质
的物质的量相等, 和 的物质的量相等。
① 下,反应 的 __________ 。
②平衡后,继续向刚性容器中加入含碳物质各 ,则反应 的分解平衡__________(填
“向正反应方向移动”“向逆反应方向移动”或“不移动”)。一、选择题(共16小题,每小题3分,共48分)
1~5:ABCDD 6~10:CCDDB 11~15:DBCDD 16:C
二、填空题(每空2分,共52分)
17.(10分)
(1)
(2) ;先增大后减小
(3)①9;②黄色
18.(14分)
(1)①2 ②Ⅱ、Ⅳ
(2)①0.04 ②>;
(3)i;
19.(14分)
(1)①+40 kJ/mol (2)BC
(3)① ;其他条件不变时,温度小于 ,反应Ⅰ为主反应,温度升高,平衡逆向移动,
的物质的量增大,温度大于 ,反应Ⅱ为主反应,温度升高,平衡正向移动, 的物质的量减小
②
(4)① ②0.9
20.(14分)
(1)-127.0 (2)0.30 (3)正向
(4)①放热 ②不变