文档内容
连城一中 2025-2026 学年上期月考 1
高二化学试卷
考试时间:75 分钟满分: 100 分
注意事项:
1、答案请填图到答题卡上,做在试卷上的答案无效。
2、可能用到的相对原子质量:
H-1 Li-7 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Cu-64 Ag-108
一、单项选择题(本题共 14 小题,每小题 3 分,共 42 分。)
1.下列关于化学反应能量变化的说法正确的是( )
A.化学反应不一定伴随着能量变化
B.伴有能量变化的物质变化都是化学变化
C.化学反应中化学能可转化为热能、电能等能量
D.有颜色变化的物质变化一定是化学变化且伴随能量变化
2.下列选项中,前者是吸热反应,后者是放热反应的是( )
A.灼热的炭与二氧化碳反应,氢气在氯气中燃烧
B.镁条在二氧化碳中燃烧,碳酸氢钠受热分解
C.Ba(OH) ·8H O 与 NH Cl 反应,氢氧化钠溶于水
2 2 4
D.酸碱中和反应,在高温下焦炭与水蒸气反应
3.下列叙述正确的是( )
A.需要加热的反应说明它是吸热反应
B.已知 C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ/mol,
2
若将含 0.6 mol H SO 的浓硫酸与含 1 mol NaOH 的稀溶液混合,放出的热量等于 57.3
2 4
kJ
D.已知 2C(s)+2O (g)===2CO (g) ΔH ;2C(s)+O (g)===2CO(g) ΔH ,则
2 2 1 2 2
ΔH <ΔH
1 2
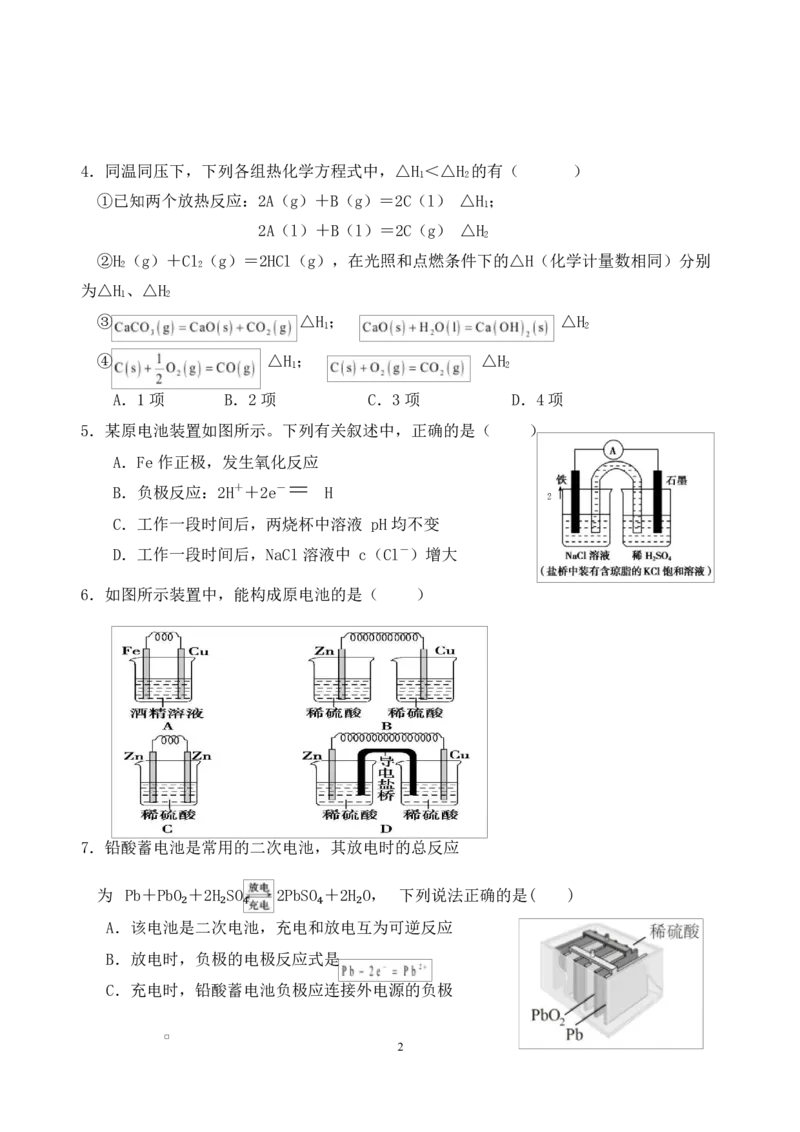
14.同温同压下,下列各组热化学方程式中,△H <△H 的有( )
1 2
①已知两个放热反应:2A(g)+B(g)=2C(l) △H ;
1
2A(l)+B(l)=2C(g) △H
2
②H (g)+Cl (g)=2HCl(g),在光照和点燃条件下的△H(化学计量数相同)分别
2 2
为△H 、△H
1 2
③ △H ; △H
1 2
④ △H ; △H
1 2
A.1 项 B.2 项 C.3 项 D.4 项
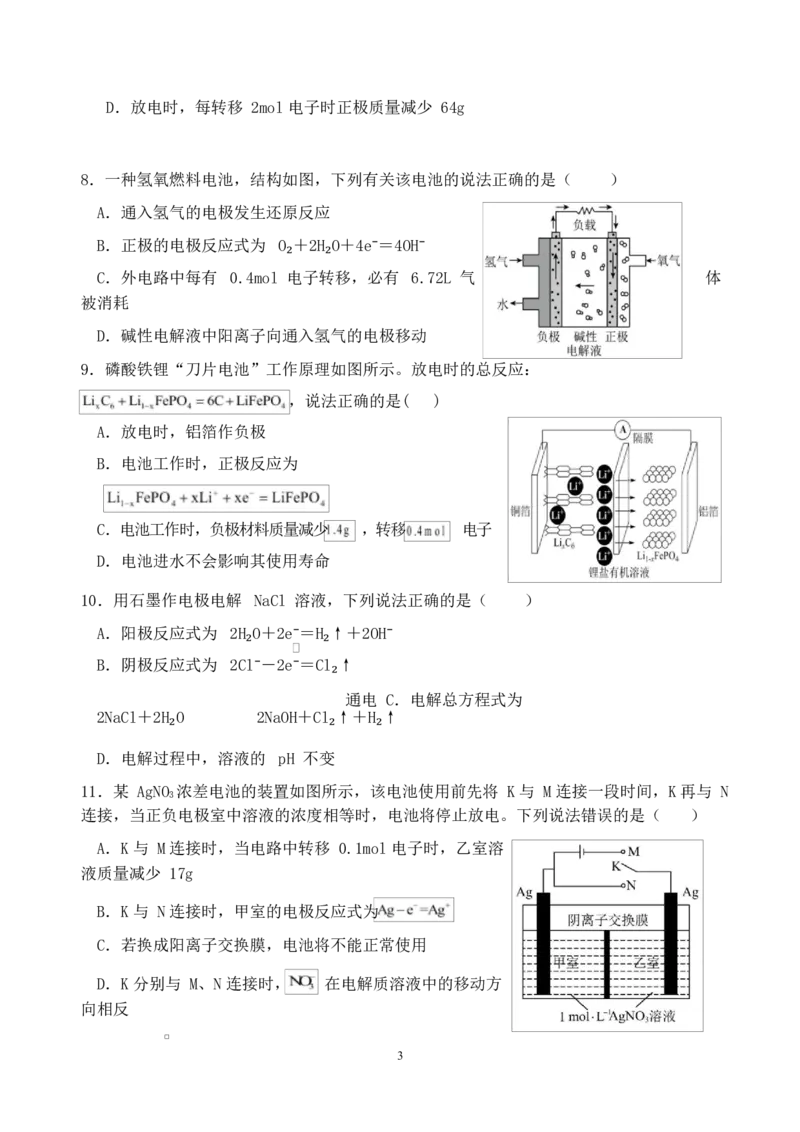
5.某原电池装置如图所示。下列有关叙述中,正确的是( )
A.Fe 作正极,发生氧化反应
=
B.负极反应:2H++2e- H ↑
2
C.工作一段时间后,两烧杯中溶液 pH 均不变
D.工作一段时间后,NaCl 溶液中 c(Cl-)增大
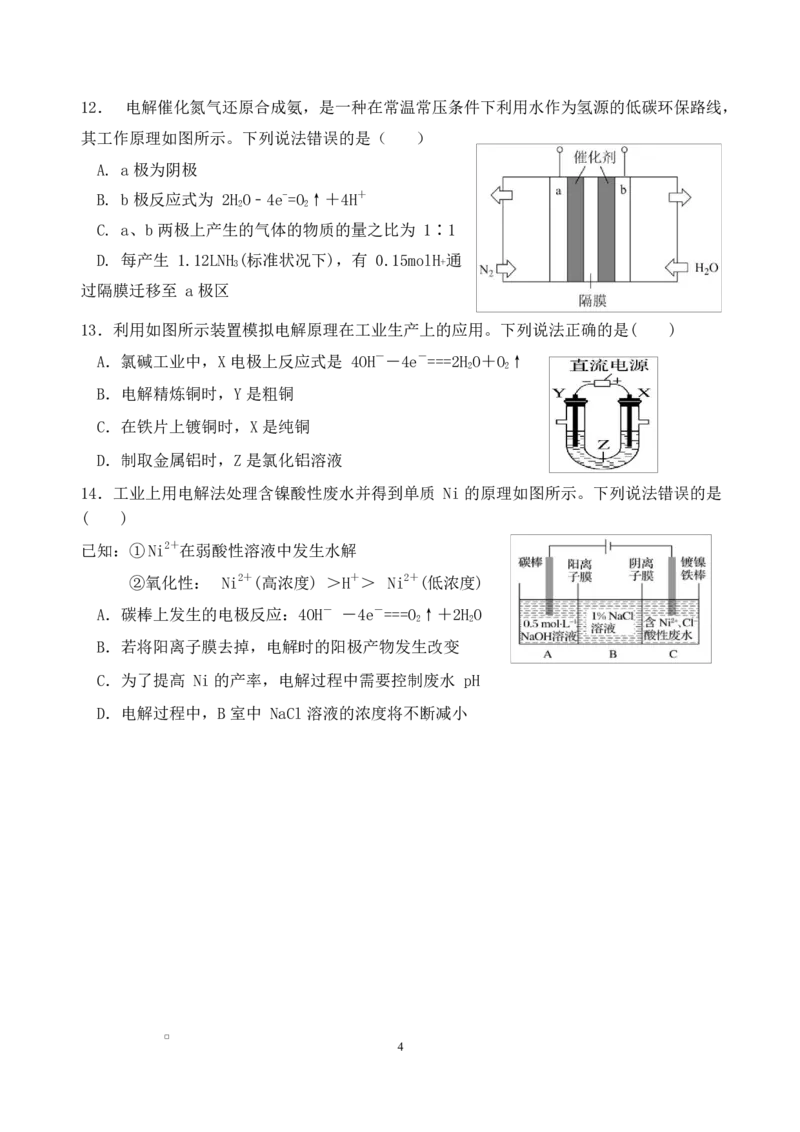
6.如图所示装置中,能构成原电池的是( )
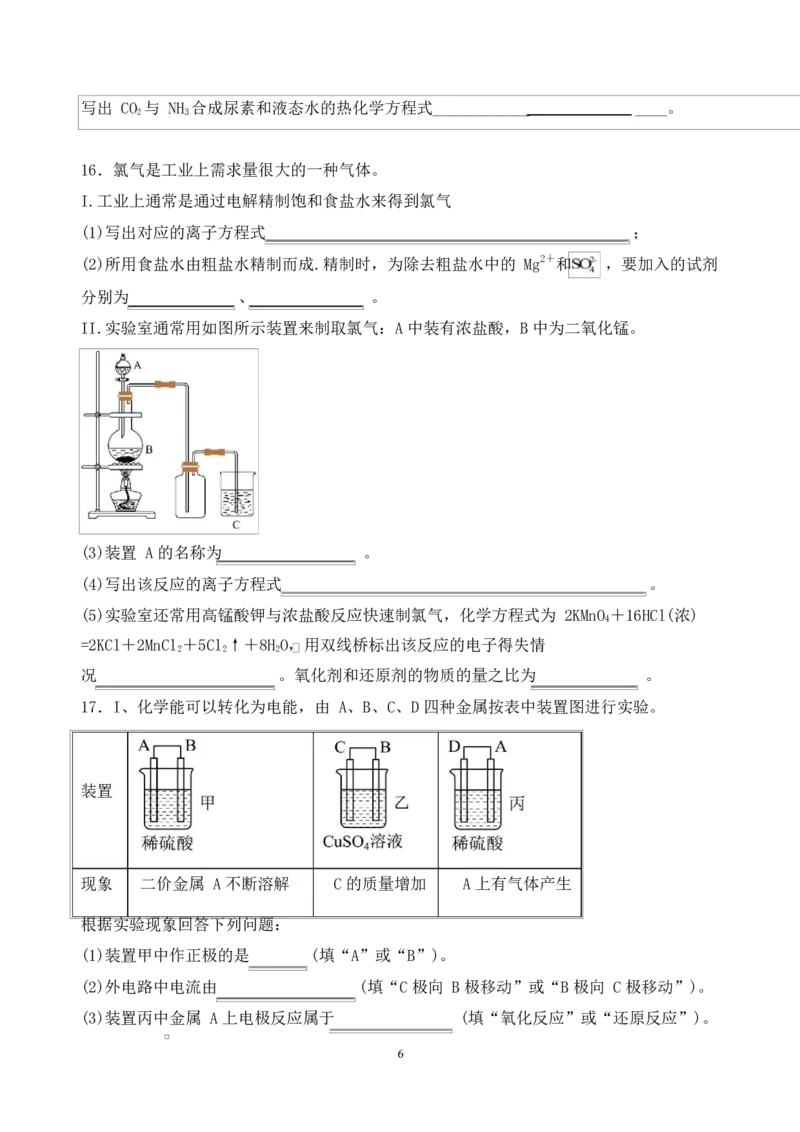
7.铅酸蓄电池是常用的二次电池,其放电时的总反应
为 Pb+PbO +2H SO 2PbSO +2H O, 下列说法正确的是( )
A.该电池是二次电池,充电和放电互为可逆反应
₂ ₂ ₄ ₄ ₂
B.放电时,负极的电极反应式是
C.充电时,铅酸蓄电池负极应连接外电源的负极
2D.放电时,每转移 2mol 电子时正极质量减少 64g
8.一种氢氧燃料电池,结构如图,下列有关该电池的说法正确的是( )
A.通入氢气的电极发生还原反应
B.正极的电极反应式为 O +2H O+4e =4OH
C.外电路中每有 0.4mol 电子转移,必有 6.72L 气 体
₂ ₂ ⁻ ⁻
被消耗
D.碱性电解液中阳离子向通入氢气的电极移动
9.磷酸铁锂“刀片电池”工作原理如图所示。放电时的总反应:
,说法正确的是( )
A.放电时,铝箔作负极
B.电池工作时,正极反应为
C.电池工作时,负极材料质量减少 ,转移 电子
D.电池进水不会影响其使用寿命
10.用石墨作电极电解 NaCl 溶液,下列说法正确的是( )
A.阳极反应式为 2H O+2e =H ↑+2OH
B.阴极反应式为 2Cl -2e =Cl ↑
₂ ⁻ ₂ ⁻
⁻ ⁻ ₂ 通电 C.电解总方程式为
2NaCl+2H O 2NaOH+Cl ↑+H ↑
D.电解过₂程中,溶液的 pH 不变₂ ₂
11.某 AgNO 浓差电池的装置如图所示,该电池使用前先将 K 与 M 连接一段时间,K 再与 N
3
连接,当正负电极室中溶液的浓度相等时,电池将停止放电。下列说法错误的是( )
A.K 与 M 连接时,当电路中转移 0.1mol 电子时,乙室溶
液质量减少 17g
B.K 与 N 连接时,甲室的电极反应式为
C.若换成阳离子交换膜,电池将不能正常使用
D.K 分别与 M、N 连接时, 在电解质溶液中的移动方
向相反
312. 电解催化氮气还原合成氨,是一种在常温常压条件下利用水作为氢源的低碳环保路线,
其工作原理如图所示。下列说法错误的是( )
A. a 极为阴极
B. b 极反应式为 2H O﹣4e-=O ↑+4H+
2 2
C. a、b 两极上产生的气体的物质的量之比为 1∶1
D. 每产生 1.12LNH
3
(标准状况下),有 0.15molH
+
通
过隔膜迁移至 a 极区
13.利用如图所示装置模拟电解原理在工业生产上的应用。下列说法正确的是( )
A.氯碱工业中,X 电极上反应式是 4OH--4e-===2H O+O ↑
2 2
B.电解精炼铜时,Y 是粗铜
C.在铁片上镀铜时,X 是纯铜
D.制取金属铝时,Z 是氯化铝溶液
14.工业上用电解法处理含镍酸性废水并得到单质 Ni 的原理如图所示。下列说法错误的是
( )
已知:①Ni2+在弱酸性溶液中发生水解
②氧化性: Ni2+(高浓度) >H+> Ni2+(低浓度)
A.碳棒上发生的电极反应:4OH- -4e-===O ↑+2H O
2 2
B.若将阳离子膜去掉,电解时的阳极产物发生改变
C.为了提高 Ni 的产率,电解过程中需要控制废水 pH
D.电解过程中,B 室中 NaCl 溶液的浓度将不断减小
4二、非选择题(本题共 4 大题,共 58 分)
15.(1)合成氨反应常使用铁触媒提高反应速率。如图为有、
无铁触媒时,反应的能量变化示意图。写出该反应的热化学
方程式 。
(2)碳及其化合物间的转化广泛存在于自然界及人类的生产和
生活中。已知 25℃,100kPa 时:
I.1mol 葡萄糖[C H O (s)]完全燃烧生成 CO (g)和 H O(l),放出 2804kJ 热量。
6 12 6 2 2
Ⅱ.CO(g)+ O (g)=CO (g) ΔH=-283kJ·mol-1。回答问题:
2 2
①25℃时,CO (g)与 H O(l)经光合作用生成葡萄糖[C H O (s)]和 O (g)的热化学方程式
2 2 6 12 6 2
为 。
②25℃,100kPa 时,气态分子断开 1mol 化学键的焓变称为键焓。
已知 O=O、C≡O 键的键焓分别为 495kJ·mol-1、799kJ·mol-1,CO (g)分子中碳氧键的键焓
2
为 kJ·mol-1。
(3)已知 CO 经催化加氢可合成低碳烯烃:2CO (g)+6H (g)= CH =CH (g)+4H O(g)ΔH
2 2 2 2 2 2
几种物质的能量(kJ·mol-1)如表所示(在 25 ℃、101 kPa 条件下,规定单质的能量为 0,
测得其他物质生成时的反应热为其具有的能量):
CO (g H (g CH =CH (g H O(g
2 2 2 2 2
物质
) ) ) )
能量
-394 0 52 -242
/(kJ·mol-1)
则该反应的ΔH= kJ·mol-1。
(4)卫星发射时可用肼(N H )作燃料,8gN H (l)在 O (g)中燃烧,生成 N (g)和 H O(l),放出
2 4 2 4 2 2 2
155.5 kJ 热量,写出反应的热化学方程式 。
(5) 以 CO 与 NH 为原料可合成化肥尿素[化学式为 CO(NH ) ]。已知:
2 3 2 2
①2NH (g)+CO (g)=NH CO NH (s) △H=-159.5 kJ/mol
3 2 2 2 4
②NH CO NH (s)= CO(NH ) (s) +H O(g) △H=+116.5 kJ/mol
2 2 4 2 2 2
③H O(l)=H O(g) △H=+44 kJ/mol
2 2
5写出 CO 与 NH 合成尿素和液态水的热化学方程式____________ ____。
2 3
16.氯气是工业上需求量很大的一种气体。
I.工业上通常是通过电解精制饱和食盐水来得到氯气
(1)写出对应的离子方程式 ;
(2)所用食盐水由粗盐水精制而成.精制时,为除去粗盐水中的 Mg2+和 ,要加入的试剂
分别为 、 。
II.实验室通常用如图所示装置来制取氯气:A 中装有浓盐酸,B 中为二氧化锰。
(3)装置 A 的名称为 。
(4)写出该反应的离子方程式 。
(5)实验室还常用高锰酸钾与浓盐酸反应快速制氯气,化学方程式为 2KMnO +16HCl(浓)
4
=2KCl+2MnCl +5Cl ↑+8H O,用双线桥标出该反应的电子得失情
2 2 2
况 。氧化剂和还原剂的物质的量之比为 。
17.I、化学能可以转化为电能,由 A、B、C、D 四种金属按表中装置图进行实验。
装置
现象 二价金属 A 不断溶解 C 的质量增加 A 上有气体产生
根据实验现象回答下列问题:
(1)装置甲中作正极的是 (填“A”或“B”)。
(2)外电路中电流由 (填“C 极向 B 极移动”或“B 极向 C 极移动”)。
(3)装置丙中金属 A 上电极反应属于 (填“氧化反应”或“还原反应”)。
6(4)四种金属活动性由强到弱的顺序是 。
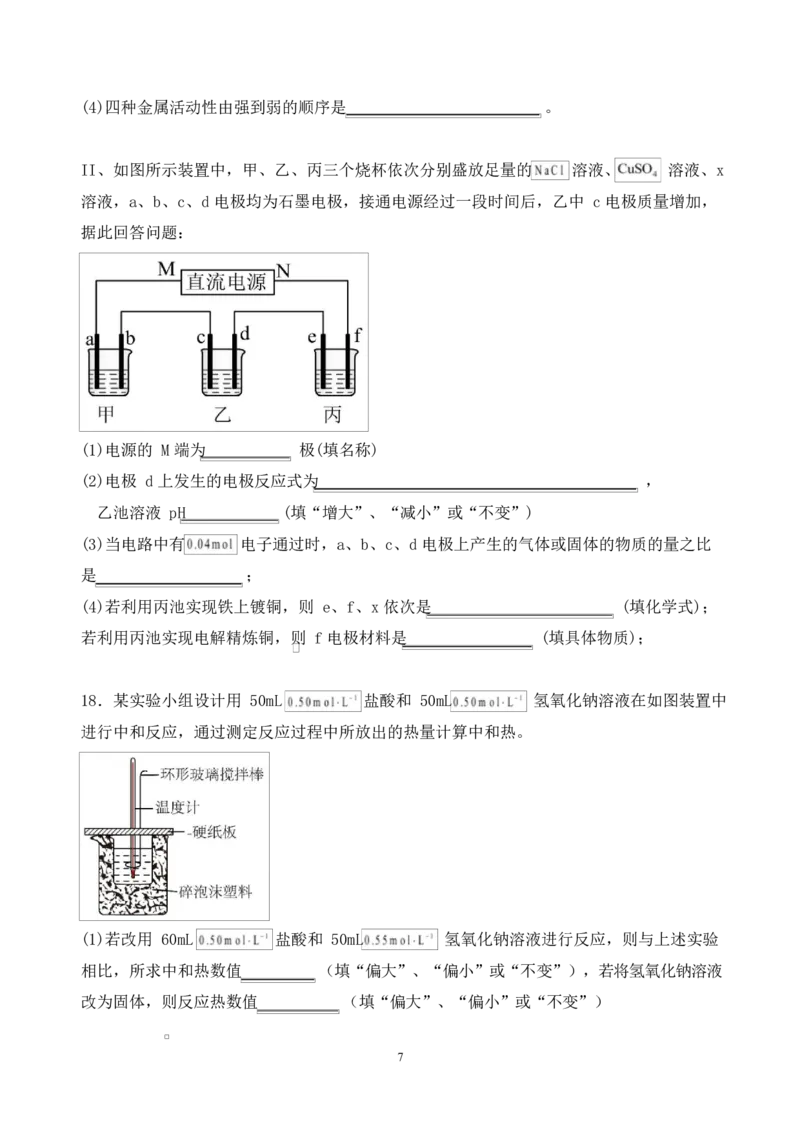
II、如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的 溶液、 溶液、x
溶液,a、b、c、d 电极均为石墨电极,接通电源经过一段时间后,乙中 c 电极质量增加,
据此回答问题:
(1)电源的 M 端为 极(填名称)
(2)电极 d 上发生的电极反应式为 ,
乙池溶液 pH (填“增大”、“减小”或“不变”)
(3)当电路中有 电子通过时,a、b、c、d 电极上产生的气体或固体的物质的量之比
是 ;
(4)若利用丙池实现铁上镀铜,则 e、f、x 依次是 (填化学式);
若利用丙池实现电解精炼铜,则 f 电极材料是 (填具体物质);
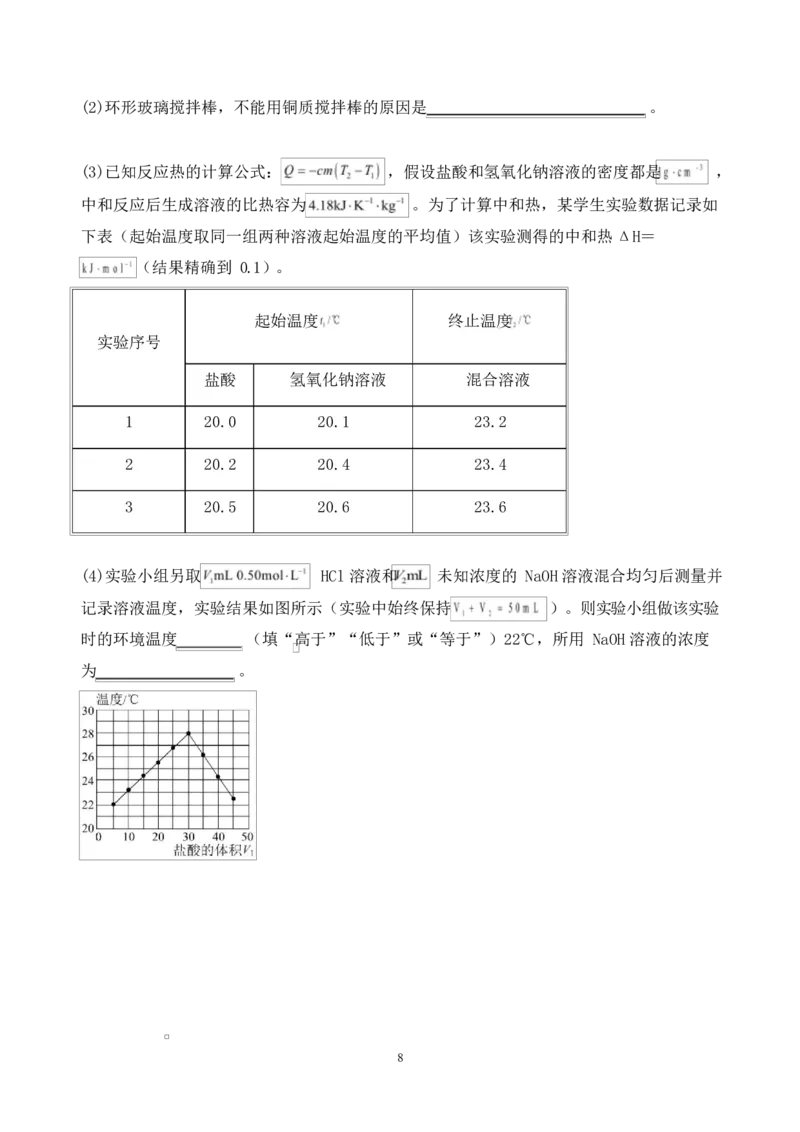
18.某实验小组设计用 50mL 盐酸和 50mL 氢氧化钠溶液在如图装置中
进行中和反应,通过测定反应过程中所放出的热量计算中和热。
(1)若改用 60mL 盐酸和 50mL 氢氧化钠溶液进行反应,则与上述实验
相比,所求中和热数值 (填“偏大”、“偏小”或“不变”),若将氢氧化钠溶液
改为固体,则反应热数值 (填“偏大”、“偏小”或“不变”)
7(2)环形玻璃搅拌棒,不能用铜质搅拌棒的原因是 。
(3)已知反应热的计算公式: ,假设盐酸和氢氧化钠溶液的密度都是 ,
中和反应后生成溶液的比热容为 。为了计算中和热,某学生实验数据记录如
下表(起始温度取同一组两种溶液起始温度的平均值)该实验测得的中和热ΔH=
(结果精确到 0.1)。
起始温度 终止温度
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.5 20.6 23.6
(4)实验小组另取 HCl 溶液和 未知浓度的 NaOH 溶液混合均匀后测量并
记录溶液温度,实验结果如图所示(实验中始终保持 )。则实验小组做该实验
时的环境温度 (填“高于”“低于”或“等于”)22℃,所用 NaOH 溶液的浓度
为 。
82025-2026 学年上期月考 1 高二化学参考答案
一、选择题:(共14 小题,每小题3 分,共42 分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C A D A D D C B B C B C C D
二、非选择题(共 29 格,每空格 2 分,共 58 分)
15. (1)N(g)+3H(g) 2NH(g) ΔH=-(a-b)kJ·mol-1
2 2 3
(2)6CO
2
(g)+6H
2
O⇌(l)=C
6
H
12
O
6
(s)+6O
2
(g) ΔH=+2804 kJ/mol 664.75
(3) -128
(4) NH(l)+O (g)=N(g)+2HO(l) △H=-622kJ/mol
2 4 2 2 2
(5) 2NH(g)+CO(g)= CO(NH)(s) +HO(l) △H=-87kJ/mol
3 2 2 2 2
16.(1) 2Cl-+2HO H↑+Cl↑+2OH-
2 2 2
(2) NaOH BaCl
2
(3) 分液漏斗
(4) MnO
2
+4H++2Cl- Mn2++Cl
2
↑+2H
2
O
(5) 1:5
17.I、(1)B (2)C 极向 B 极移动 (3)还原反应 (4)D>A>B>C
II 、(1)负极 (2) 降低
(3) 2:2:2:1
(4) Fe、Cu、CuSO 粗铜
4
18.(1) 不变偏大
(2) 防止热量散失
(3) -51.8
9(4) 低于 0.75mol·L-1
10